用于治疗自身免疫性和炎症性疾病的方法和组合物与流程
用于治疗自身免疫性和炎症性疾病的方法和组合物本申请根据美国法典35U.S.C第119条第(e)项要求2011年8月10日提交的美国临时专利申请第61/522,009号的优先权。前述申请通过引用的方式并入本文。技术领域本发明总体涉及自身免疫性和炎症性疾病领域。具体地,本发明提供用于治疗在其病理学上有自身免疫性和/或炎症性成分的疾病的新的组合物和方法。
背景技术:
当机体不能将其自身的组成部分识别为“自体”,从而导致针对其自身细胞和组织的免疫反应时,自身免疫性疾病发生。换句话说,身体实际上攻击其自身细胞。免疫系统错将身体的某些部分作为病原体并攻击它。目前对于自身免疫性疾病的治疗通常包括用非疾病修饰性抗炎药的免疫抑制和/或对症治疗,目的是减少异常免疫响应的损害。然而,本领域中存在对用于抑制和/或延迟与自身免疫性病症相关的病理学发作的方法和组合物的需求。
技术实现要素:
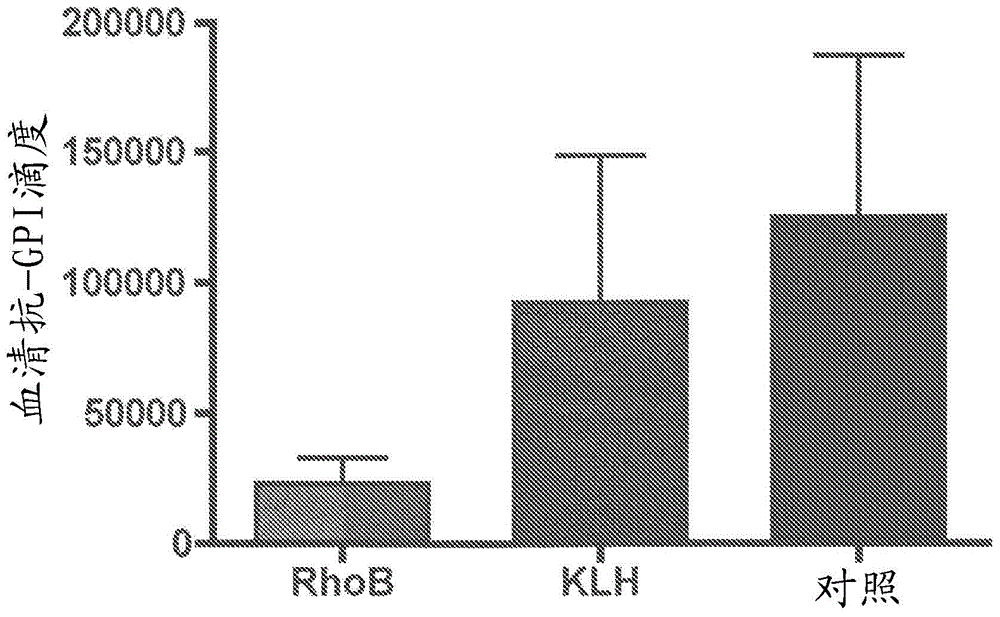
根据本发明的一个方面,提供用于在有需要的患者中抑制、治疗和/或预防自身免疫性和/或炎症性疾病和/或在其病理学上有自身免疫性和/或炎症性成分的疾病的发作的方法。该方法包括施用至少一种RhoB抑制剂。在具体的实施方案中,所述RhoB抑制剂为对RhoB或其肽片段免疫上特异的抗体或抗体片段。在具体实施方案中,所述RhoB抑制剂为所述抗体、抗体片段、肽片段或所述抗体的CDR区和由所述CDR识别的表位的化学或生物模拟物的结构相关的或衍生的小分子。在具体实施方案中,所述RhoB抑制剂为RhoB肽。在具体实施方案中,所述方法包括施用包含至少一种RhoB肽和/或对RhoB或其肽片段免疫上特异的抗体或抗体片段以及至少一种药学上可接受的载体的组合物。在具体实施方案中,所述方法还包括与至少一种RhoB抑制剂(例如,对RhoB或其肽片段免疫上特异的抗体或抗体片段)同时和/或依次施用至少一种抗炎剂和/或免疫抑制剂。还提供了用于抑制、治疗和/或预防炎症性或自身免疫性疾病的组合物。所述组合物包含至少一种RhoB抑制剂和至少一种药学上可接受的载体。在具体实施方案中,所述RhoB抑制剂为对RhoB或其肽片段免疫上特异的抗体或抗体片段。在具体实施方案中,所述RhoB抑制剂为RhoB肽。在另一个实施方案中,所述组合物进一步包含至少一种抗炎化合物和/或至少一种免疫抑制剂。本发明还提供抗-RhoB抗体、RhoB肽(例如,用于抗体的生成)或所述抗体、抗体片段、肽片段或所述抗体的CDR区和由所述CDR识别的表位的化学或生物模拟物的结构相关的或衍生的小分子,以及包含它们的组合物。根据本发明的一个方面,提供了用于在有需要的患者中抑制、治疗和/或预防与血清中免疫球蛋白的增高的水平相关的病况或病症(例如,高丙种球蛋白血症或意义不明的单克隆丙种球蛋白病)的方法。所述方法包括施用至少一种如本文所述的RhoB抑制剂。附图说明图1是用抗-RhoB肽血清、抗-KLH血清或单独的载体治疗的K/BxN小鼠的平均踝关节厚度随时间的曲线图。图2A是来自用抗-RhoB肽血清、抗K-LH血清或单独的载体治疗的K/BxN小鼠的血清抗-葡糖-6-磷酸异构酶(GPI)Ig的滴度的曲线图。图2B为用抗-RhoB肽血清、抗-KLH血清或仅用载体治疗的K/BxN小鼠的每105个细胞中抗-GPI分泌细胞的数量的曲线图。图3提供了人RhoB的氨基酸序列(SEQIDNO:3)。下划线的序列为肽1(SEQIDNO:1)。图4提供了在存在或不存在对照抗体或来自杂交瘤或其亚克隆的抗-RhoB抗体的情况下,使用或不使用脂多糖(LPS)刺激的IgM分泌的曲线图。图5提供了RhoA(SEQIDNO:4)和RhoB(SEQIDNO:3)的序列对比。下划线序列和加框序列表示RhoB抗体的抗原。图6A提供了在关节炎发作前用抗-RhoB单克隆抗体9G5或7F7或对照Ig治疗的K/BxN小鼠(21天龄)的后踝关节厚度±SEM的曲线图。图6B和6C分别提供了所述小鼠中抗-GPI自身抗体滴度和抗-GPI抗体分泌细胞(ASCs)数量的曲线图。图7A提供了在4周龄、在关节炎发作后用抗-RhoB单克隆抗体9G5或对照Ig治疗的K/BxN小鼠经过长时间过程的后踝关节厚度±SEM的曲线图。图7B提供了提供了在4周龄、在关节炎发作后用抗-RhoB单克隆抗体9G5或7F7或对照Ig治疗的K/BxN小鼠经过较短时间过程的后踝关节厚度±SEM的曲线图。图8A提供了关节炎RhoB基因敲除小鼠(RhoBKOKRN.g7)的后踝关节厚度±SEM的曲线图。图8B提供了在0天接受了来自KRNB6.g7或RhoBKOKRNB6.g7小鼠的血清转移的幼稚(naive)C57BL/6小鼠的后踝关节厚度±SEM的曲线图。图8C提供了在0天从关节炎K/BxN小鼠接受血清转移的幼稚野生型或RhoBKOC57BL/6小鼠的后踝关节厚度±SEM的曲线图。图9A提供了7F7的轻链的核苷酸(SEQIDNO:9)和氨基酸(SEQIDNO:10)序列。图9B提供了7F7的重链的核苷酸(SEQIDNO:11)和氨基酸(SEQIDNO:12)序列。垂直线表示结构域间的边界。粗体——可变区(V);下划线——接合区(J);斜体——多样性区(D);FWR——框架区;CDR——互补决定区。图10A提供了9G5的轻链的核苷酸(SEQIDNO:13)和氨基酸(SEQIDNO:14)序列。图10B提供了9G5的重链的核苷酸(SEQIDNO:15)和氨基酸(SEQIDNO:16)序列。垂直线表示结构域间的边界。粗体——可变区(V);下划线——接合区(J);斜体——多样性区(D);FWR——框架区;CDR——互补决定区。具体实施方式产生针对RhoB的单克隆抗体的稳定杂交瘤已经难以生成和维持。当试图获得杂交瘤时,已观察到最相关的杂交瘤要么死亡要么停止分泌所述抗-RhoB抗体。这种观察引起针对RhoB的抗体可能抑制B细胞中抗体产生的假想。本文中,示出了针对RhoB的抗体可抑制来自受激的小鼠B细胞的免疫球蛋白的分泌。进一步地,本文示出了针对RhoB的抗体在自身抗体驱使的类风湿关节炎(RA)的动物模型中延迟关节炎的发作并减轻关节炎的病程。作为自身抗体产生结果的疾病或疾病症状将受益于阻止或减少抗体产生的疗法。施用所述抗-RhoB抗体可与其它基于抗体的疗法(其是可耐受的尽管它们对于疾病治疗是非靶向的)相似。实例包括但不限于抗-TNF(英夫利昔(infliximab)、阿达木单抗、依那西普)、抗-CD20(利妥昔单抗)和抗-BLyS(贝利木单抗(belimumab))的抗体疗法。这些疗法通常减弱(blunt)炎症或消除B细胞或B细胞功能。对于不良耐受这些疗法的患者,所述抗-RhoB抗体提供另一种治疗选择。RhoB抗体的施用将可能有低的或没有毒性或副作用。明显地,遗传上缺乏RhoB的小鼠是正常的并缺乏明显的免疫缺陷,包括对抗原刺激或IgG记忆形成的B细胞响应的缺陷。当RhoB缺陷小鼠产生正常的IgG抗体响应时,它们表现出适度减弱的IgM二次响应。因此,所述抗-RhoB技术似乎在自身免疫抗体的产生中阻碍(retard)异常的B细胞功能,但它不破坏正常抗原刺激后正常的B细胞功能。明显地,RhoB为具有较短半衰期的应激响应蛋白,因此它可能快速耗尽并通过特异的抗体阻断而功能受损。RhoB为细胞内蛋白。在不受理论束缚的情况下,所述抗-RhoB抗体可通过Fc受体进入细胞。同样地,这将导致毒性或副作用减小,因为仅表达所述Fc受体的细胞可对抗-RhoB抗体疗法敏感。类似地,毒性也应低于目前在临床使用的非靶向性免疫调节剂比如地塞米松、强的松或萨力多胺(thalidomide)。虽然本发明公开了抗-RhoB抗体疗法,然而RhoB(例如,RhoB活性和/或表达)的其它抑制剂可代替或者与所述抗-RhoB抗体结合使用。例如,可使用抑制RhoB表达的核酸分子,比如siRNA和反义分子。已显示,微小RNA-21(microRNA-21)减少RhoB表达(Sabateletal.PLoSOne(2011)6:e16979)。此外,本文鉴定的RhoB肽序列或基于所述肽序列的结构相关的小分子或与RhoB上的相应表位相互作用的CDR也可充当RhoB活性的抑制剂,特别当结合到适当的递送系统时。抗体介导的RhoB的破坏阻碍、抑制和/或减弱牵涉B细胞的炎症性细胞响应。如上文所提及的,针对RhoB的抗体可用于缓解作为自身抗体产生和/或分泌的结果的疾病或疾病症状。然而,特异的RhoB靶向疗法(例如,通过细胞内递送系统的大分子(例如,IgG分子的可变区)递送)可被设计为捕捉(arrest)或重新定向由B细胞识别的细胞内炎症信号。以这种方式,所述抗RhoB疗法将在有助于慢性炎症的细胞类型中起作用,比如被认为有助于心血管疾病(CVD)、癌症、糖尿病或由炎症组织环境直接或间接支持的其它重大疾病的发展的间充质细胞(内皮细胞、肌成纤维细胞、平滑肌细胞、单核/巨噬细胞)。在CVD中,临床前试验已显示,RhoB由他汀类药物进行调节,并且存在他汀类药物的“非胆固醇降低”效应可归因于抗炎作用的临床证据。因此,抗RhoB疗法可用于限制动脉粥样硬化或者与他汀类药物或其它抗炎疗法结合作为新的治疗选择。在其它的炎症组织设置中,抗RhoB也可抑制成纤维细胞的炎症响应。同样地,抗RhoB疗法可减弱促进组织瘢痕形成(比如在皮肤、肝脏或心脏中)的纤维化响应。关于糖尿病,已显示,自身抗体是引起疾病的T细胞的活化所必需的(Harbersetal.(2007)J.Clin.Invest.,117:1361–1369)。因此,防止自身抗体活化T细胞的方法的发展(例如,通过减少或抑制自身抗体)将预防或治疗自身免疫性疾病。明显地,已证明对CD20特异的抗体可通过耗尽B细胞亚群而减少糖尿病的发作(Huetal.(2007)J.Clin.Invest.,117:3857–3867)。除了糖尿病之外,已证明抗体介导的其它自身免疫疾病的治疗。例如,已显示针对鞘氨醇-1-磷酸受体的抗体在小鼠模型中减少结肠炎(Liaoetal.(2009)FASEBJ.,23:1786-96)。如上文所述,本发明提供了用于抑制、治疗和/或预防自身免疫疾病和/或炎症性疾病的组合物和方法。在具体实施方案中,要被本发明的方法治疗的所述自身免疫性疾病或炎症性疾病为其中疾病的病理生理学和/或症状中牵涉B细胞的那些。此类自身免疫性疾病和炎症性疾病也可被称为B细胞介导的自身免疫性疾病或炎症性疾病。已显示B细胞在各种自身免疫性或炎症性疾病的病理生理学中起作用(参见例如Browning,J.L.(2006)Nat.Rev.DrugDiscov.,5:564-576)。如本文使用的,术语“自身免疫性疾病”指的是自身免疫响应(针对自身(auto-)或自体(self-)抗原的免疫响应)在受试者中的存在。自身免疫性疾病包括由自体耐受性故障导致(breakdown)的疾病,这样适应的免疫系统响应自体抗原并介导细胞和组织损伤。在具体实施方案中,自身免疫性疾病的特征为,是(至少部分地)体液免疫响应的结果。自身免疫性疾病的实例包括(但不限于)急性播散性脑脊髓炎(ADEM)、急性坏死性出血性脑白质炎、阿狄森氏病(Addison’sdisease)、血中丙球蛋白缺乏、变应性气喘、变应性鼻炎、斑秃、淀粉样变性、强直性脊柱炎、抗体介导的移植排斥、抗GBM/抗TBM肾炎、抗磷脂综合征(APS)、自身免疫血管性水肿、自身免疫性再生障碍性贫血、自身免疫家族性自主神经异常、自身免疫性肝炎、自身免疫性高脂血、自身免疫性免疫缺陷、自身免疫性内耳疾病(AIED)、自身免疫性心肌炎、自身免疫性胰腺炎、自身免疫性视网膜病、自身免疫性血小板减少性紫癜(ATP)、自身免疫性甲状腺疾病、自身免疫性荨麻疹、轴突&神经元神经病、巴娄病(Balodisease)、白塞氏病(Behcet’sdisease)、大疱性类天疱疮、心肌症、卡斯特雷曼氏病(Castlemandisease)、乳糜泻、查加斯病(Chagasdisease)、慢性疲劳综合症、慢性炎症性脱髓鞘多神经病(CIDP)、慢性复发性多灶性骨髓炎(CRMO)、Churg-Strauss综合症、瘢痕性类天疱疮/良性粘膜类天疱疮、克罗恩氏病(Crohn’sdisease)、Cogans综合症、冷凝集素疾病、先天性心脏传导阻滞、柯萨奇病毒性心肌炎、CREST疾病、原发性混合型冷球蛋白血症、脱髓鞘性神经病、疱疹样皮炎、皮肌炎、德维克病(视神经脊髓炎)、盘状狼疮、德雷斯勒氏综合征、子宫内膜异位症、嗜酸细胞性筋膜炎、结节性红斑、实验性变应性脑脊髓炎、Evans综合征、纤维肌痛、纤维性肺泡炎、巨细胞动脉炎(颞动脉炎)、肾小球肾炎、古德帕斯丘综合症(goodpasture’ssyndrome)、肉芽肿性多血管炎(GPA)、格雷夫斯氏病(Graves’Disease)、格林-巴利综合征、桥本氏脑炎、桥本氏甲状腺炎、溶血性贫血、亨-舍二氏紫癜(Henoch-Schonleinpurpura)、妊娠疱疹、低丙球蛋白血症、高丙种球蛋白血症、特发性血小板减少性紫癜(ITP)、IgA肾病、IgG4相关硬化性疾病、免疫调节脂蛋白、包涵体肌炎、炎症性肠病、胰岛素依赖型糖尿病(I型)、间质性膀胱炎、幼年型关节炎、幼年型糖尿病、川崎综合征、兰伯特-伊顿综合征、白细胞破碎性血管炎、扁平苔癣、硬化性苔癣、木质结膜炎、线状IgA病(LAD)、红斑狼疮(SLE)、莱姆病(lymedisease)、梅尼埃氏病(Meniere’sdisease)、显微镜下多发性血管炎(microscopicpolyangiitis)、混合性结缔组织病(MCTD)、意义不明的单克隆丙种球蛋白病(MGUS)、蚕蚀性角膜溃疡、穆哈-赫伯曼疾病(Mucha-Habermanndisease)、多发性硬化症、重症肌无力、肌炎、发作性嗜睡病(narcolepsy)、视神经脊髓炎(德维克氏病)、中性粒细胞减少、眼瘢痕性类天疱疮、视神经炎、回文风湿、PANDAS(链球菌感染相关的儿童自身免疫性神经精神障碍)、副肿瘤性小脑变性、阵发性睡眠性血红蛋白尿症(PNH)、帕里龙贝格综合征(ParryRombergsyndrome)、帕森-特纳综合征(Parsonnage-Turnersyndrome)、睫状体平坦部炎(周边葡萄膜炎)、天疱疮、周围神经病变、静脉周围性脑脊髓炎、恶性贫血、POEMS综合征、结节性多动脉炎、I型、II型及III型自身免疫性多腺体综合征、多肌痛风湿病、多发性肌炎、心肌梗塞后综合征、心包切开术后综合征(postpericardiotomysyndrome)、黄体酮皮炎、原发性胆汁性肝硬化、原发性硬化性胆管炎、牛皮癣、牛皮癣性关节炎、特发性肺纤维化、坏疽性脓皮病、纯红细胞再生障碍、雷诺氏现象(Raynaudsphenomenon)、反射性交感神经营养不良症、莱特尔氏综合征(Reiter’ssyndrome)、复发性多软骨炎、多动腿综合征、腹膜后纤维化、风湿热、类风湿性关节炎、肉状瘤病、施密特综合征(Schmidtsyndrome)、巩膜炎、硬皮病、肖格伦综合征(Sjogren'ssyndrome)、精液和睾丸自身免疫、僵人综合征(stiffpersonsyndrome)、亚急性细菌性心内膜炎(SBE)、Susac综合征、交感性眼炎、高安氏动脉炎(Takayasu’sarteritis)、颞动脉炎/巨细胞动脉炎、血小板减少性紫癜(TTP)、托洛萨-亨特综合征(Tolosa-Huntsyndrome)、横贯性脊髓炎、溃疡性结肠炎、未分化结缔组织病(UCTD)、葡萄膜炎、血管炎、水疱性皮肤病、白癜风,华氏巨球蛋白血症(Waldenstrom'smacroglobulinemia)(WM)和韦格纳肉芽肿病(肉芽肿与血管炎(GPA))。在具体实施方案中,所述自身免疫性疾病选自由类风湿性关节炎、I型糖尿病、全身性红斑狼疮(狼疮或SLE)、重症肌无力、多发性硬化、硬皮病、阿狄森氏病、大疱性类天疱疮、寻常天疱疮、格林-巴利综合征(Guillain-Barrésyndrome)、肖格伦综合征、皮肌炎、血栓性血小板减少性紫癜、高丙种球蛋白血症、意义不明的单克隆丙种球蛋白病(MGUS)、华氏巨球蛋白血症(WM)、慢性炎症性脱髓鞘多神经根神经病(CIDP)、桥本氏脑病(HE)、桥本氏甲状腺炎、格雷夫斯氏病、韦格纳肉芽肿病和抗体介导的移植排斥(例如,对于组织移植比如肾移植)组成的组。在具体实施方案中,所述自身免疫性疾病为I型糖尿病、狼疮或类风湿性关节炎。如本文使用的,“炎症性疾病”指的是由炎症引起或起因于炎症或导致炎症的疾病。术语“炎症性疾病”也指失调的炎症反应,其由巨噬细胞、粒细胞和/或T淋巴细胞引起过度的响应导致异常的组织损伤和细胞死亡。在具体实施方案中,所述炎症性疾病包括抗体介导的炎症过程。“炎症性疾病”可为急性或慢性炎症病况并可起因于感染性或非感染性病因。炎症性疾病包括(但不限于)动脉粥样硬化、动脉硬化、自身免疫性病症、多发性硬化、全身性红斑狼疮、风湿性多肌痛(PMR)、痛风性、退行性关节炎、肌腱炎、黏液囊炎、牛皮癣、囊胞性纤维症、骨关节炎、类风湿性关节炎、炎症性关节炎、肖格伦综合征、巨细胞动脉炎、进行性全身性硬化症(硬皮病)、强直性脊柱炎、多肌炎、皮肌炎、天疱疮、类天疱疮、糖尿病(例如,I型)、重症肌无力、桥本氏甲状腺炎、格雷夫斯氏病、古德帕斯丘病、混合性结缔组织病、硬化性胆管炎、炎症性肠病、克罗恩氏病、溃疡性结肠炎、恶性贫血、炎症性皮肤病、普通性间质性肺炎(UIP)、石棉肺、矽肺、支气管扩张、铍中毒、滑石肺、尘肺病、肉状瘤病、脱屑性间质性肺炎、淋巴样间质性肺炎、巨细胞间质性肺炎、细胞间质性肺炎、外部变应性牙槽炎、韦格纳肉芽肿病和脉管炎的有关形式(颞动脉炎和结节性多动脉炎)、炎症性皮肤病、肝炎、迟发型过敏反应(例如,毒漆藤皮炎)、肺炎、呼吸道炎症、成人窘迫综合征(ARDS)、脑炎、速发型过敏反应、哮喘、枯草热、敏感症、急性过敏反应、风湿热、血管球性肾炎、肾盂肾炎、蜂窝组织炎、膀胱炎、慢性胆囊炎、局部缺血(缺血性损伤)、同种异体移植物排斥、宿主抗移植物排斥、阑尾炎、动脉炎、眼睑炎、细支气管炎、支气管炎、子宫颈炎、胆道炎、绒毛膜羊膜炎、结膜炎、泪腺炎、皮肌炎、心内膜炎、子宫内膜炎、肠炎、小肠结肠炎、上踝炎、附睾炎、筋膜炎、纤维组织炎、胃炎、肠胃炎、齿龈炎、回肠炎、虹膜炎、喉炎、脊髓炎、心肌炎、肾炎、脐炎、卵巢炎、睾丸炎、骨炎、耳炎、胰腺炎、腮腺炎、心包炎、咽炎、胸膜炎、静脉炎、肺炎、直肠炎、前列腺炎、鼻炎、输卵管炎、鼻窦炎、口腔炎、滑膜炎、睾丸炎、扁桃腺炎、尿道炎、膀胱炎、葡萄膜炎、阴道炎、血管炎、外阴炎、和外阴阴道炎、脉管炎、慢性支气管炎、骨髓炎、视神经炎、颞动脉炎、横贯性脊髓炎、坏死性筋膜炎、和坏死性小肠结肠炎。在具体实施方案中,所述炎症性疾病选自由动脉粥样硬化、动脉硬化、自身免疫病症、多发性硬化、全身性红斑狼疮、类风湿性关节炎、炎症性关节炎和心肌炎组成的组。本发明还包含用于抑制、治疗和/或预防与血清中的某一免疫球蛋白的增高的水平相关的病况或病症(比如高丙种球蛋白血症或意义不明的单克隆丙种球蛋白病)的组合物和方法。在本发明的另一个实施方案中,向受试者施用RhoB抑制剂(例如抗-RhoB抗体)以治疗癌症通过抗体分泌持续。在具体实施方案中,所述癌症为血液肿瘤比如多发性骨髓瘤。在另一个实施方案中,所述癌症为实体瘤。在不受理论约束的情况下,所述抗体分泌可有助于支持炎症过程。临床前研究显示,RhoB支持对于恶性进展至关重要的肿瘤血管发生和淋巴管生成,已证明其依赖于抗体在炎症性肿瘤微环境的沉积。因此,抗-RhoB可用于在预防复发和延长缓解期的治疗后限制原发性肿瘤的进展。抗-RhoB疗法还可向受试者施用以治疗与某些类型的癌症相关的抗体介导的副肿瘤综合征。实例包括(但不限于)僵人综合征、斜视眼阵挛-肌阵挛(例如,在乳腺癌中)、外周性脑脊髓炎和视网膜病(例如,在肺癌中)。本发明的方法还包含施用至少一种其它的用于治疗自身免疫和/或炎症性疾病的剂。在不受理论束缚的情况下,抗-RhoB抗体的施用减弱了自身免疫抗体的产生。同样地,本技术不取代用于治疗自身免疫性疾病的疾病特异性方法。在具体实施方案中,所述方法包括施用至少一种免疫抑制剂。如本文使用的术语“免疫抑制剂(immunosuppressant)”和“免疫抑制剂(immunosuppressiveagent)”包括抑制免疫响应或与其相关的症状的化合物或组合物。免疫抑制剂包括(但不限于)嘌呤类似物(例如,咪唑硫嘌呤)、甲氨蝶呤、环孢霉素(例如,环孢霉素A)、环磷酰胺、来氟米特、麦考酚酯(霉酚酸酯)、类固醇(例如,糖皮质激素、皮质类固醇)、甲泼尼松、强的松、非甾族抗炎药(NSAID)、氯喹、羟基氯喹、瘤可宁、CD20拮抗剂(例如,利妥昔单抗、欧克利单抗(ocrelizumab)、维特珠单抗(veltuzumab)或奥法木单抗(ofatumumab))、阿巴西普(abatacept)、TNF拮抗剂(例如,英夫利昔、阿达木单抗、依那西普)、大环内酯类(例如,吡美莫司、他克莫司(FK506)和雷帕霉素)、脱氢表雄酮、来那度胺(lenalidomide)、CD40拮抗剂(例如,抗CD40L抗体)、阿贝莫司钠(abetimussodium)、BLys拮抗剂(例如,抗BLys(例如,贝利木单抗)、更生霉素、布西拉明(bucillamine)、青霉胺、来氟米特、巯嘌呤、嘧啶类似物(例如,胞嘧啶阿拉伯糖苷)、咪唑立宾、烷化剂(例如,氮芥、苯基丙氨酸、白消安(buslfan)和环磷酰胺)、叶酸拮抗剂(例如,氨蝶呤和甲氨蝶呤)、抗生素(例如,雷帕霉素、放线菌素D、丝裂霉素C、嘌呤霉素和氯霉素)、人IgG、抗淋巴细胞球蛋白(ALG)、抗体(例如,抗CD3(OKT3)、抗CD4(OKT4)、抗CD5、抗CD7、抗IL-2受体(例如,达利珠单抗(daclizumab)和巴利昔单抗(basiliximab))、抗α/βTCR、抗ICAM-1、莫罗莫那-CD3、抗IL-12、阿仑单抗(alemtuzumab)和针对抗霉素的抗体)、1-甲基色氨酸和它们的衍生物和类似物。在具体实施方案中,所述免疫抑制剂选自由甲氨蝶呤、羟基氯喹、CD20拮抗剂(例如,利妥昔单抗、欧克利单抗、维特珠单抗或奥法木单抗)、阿巴西普、TNF拮抗剂(例如,英夫利昔、阿达木单抗、依那西普)、雷帕霉素和BLys拮抗剂(例如,抗BLys(例如,贝利木单抗)组成的组。在具体实施方案中,所述免疫抑制剂为CD20拮抗剂、TNF拮抗剂或BLys拮抗剂。在具体实施方案中,本发明的方法包括施用至少一种抗炎剂。如本文使用的,“抗炎剂”指的是用于治疗炎症性疾病或与其相关的症状的化合物。抗炎剂包括(但不限于)非甾族抗炎药(NSAIDs;例如,阿司匹林、布洛芬、萘普生、水杨酸甲酯、二氟尼柳、消炎痛、苏灵大、双氯芬酸、酮洛芬、酮咯酸、卡洛芬、非诺洛芬、甲灭酸、吡罗昔康、美洛昔康、甲氨蝶呤、塞来昔布、伐地考昔、帕瑞考昔、依托考昔和尼美舒利)、皮质类固醇(例如,强的松、倍他米松、布地奈德、可的松、地塞米松、氢化可的松、甲基强的松龙、氢化泼尼松、曲安舒松(tramcinolone)和氟替卡松)、雷帕霉素(参见,例如,Migitaetal.,Clin.Exp.Immunol.(1997)108:199-203;Migitaetal.,Clin.Exp.Immunol.(1996)104:86-91;Foroncewiczetal.,Transpl.Int.(2005)18:366-368)、高密度脂蛋白(HDL)和HDL-胆固醇升高化合物(参见,例如,Birjmohunetal.(2007)Arterioscler.Thromb.Vasc.Biol.,27:1153-1158;Nielandetal.(2007)J.LipidRes.,48:1832-1845;Bloedonetal.(2008)J.LipidRes.,Samahaetal.(2006)Arterioscler.Thromb.Vasc.Biol.,26:1413-1414,whichdisclosestheuseofrosiglitazoneasananti-inflammatory,Duffyetal.(2005)Curr.Opin.Cardiol.,20:301-306)、rho激酶抑制剂(参见,例如,Hu,E.(2006)Rec.PatentsCardiovasc.DrugDiscov.,1:249-263)、抗疟剂(例如,羟基氯喹和氯喹)、对乙酰氨基酚、糖皮质激素、类固醇、β-激动剂、反副交感神经生理作用的剂、甲基黄嘌呤、金注射剂(例如,金硫丁二钠)、柳氮磺胺吡啶、青霉胺、抗血管生成剂、氨苯砜、补骨脂素、抗病毒剂、他汀类药物(参见,例如,Paraskevasetal.(2007)Curr.Pharm.Des.,13:3622-36;Paraskevas,K.I.(2008)Clin.Rheumatol.27:281-287)和抗生素(例如,四环素)。在具体实施方案中,所述抗炎剂为他汀类药物或高密度脂蛋白(HDL)和HDL-胆固醇升高化合物。根据本发明的另一个方面,提供了RhoB肽。在具体实施方案中,所述RhoB肽包含至少10个SEQIDNO:3的连续氨基酸。在具体实施方案中,所述RhoB肽包含RhoB的C末端的一半(98个氨基酸)。在具体实施方案中,所述RhoB肽选自由VANKKDLRSDEHVRTELARMKQEPVRTDDGRAMAVRIQAYDYLECSAKTKEGVREVFETATRAALQKRYGSQNGCINCCKVL(SEQIDNO:5),KDLRSDEHVRTELARMKQEPVRTDDGRAMAVRIQAYDYLECSAKTKEGVREVFETATRAAL(SEQIDNO:6),SDEHVRTELARMKQEPVRTDDGRAMAVRIQAYDYLECSAKTKEGVREVFETATRAALQKRYGSQNGCINCCKVL(SEQIDNO:7),DDGRAMAVRIQAY(SEQIDNO:2),RTDDGRAMAVRIQAYDYLE(SEQIDNO:1)和AVRIQAYDYLE(SEQIDNO:8)组成的组(参见,例如,图5)。所述RhoB肽可在肽的N端和/或C端比上述确定的序列长或短0、1、2、3、4、5、6、7、8、9、10或更多氨基酸,尤其是1、2、3、4或5个氨基酸。在另一个实施方案中,本发明的所述肽与SEQIDNO:3(或SEQIDNOs:1,2,5-8)具有至少90%、95%、97%、99%或100%的同源性或同一性。本发明的所述肽可以根据已知方法的各种方法制备。本发明的所述肽可通过化学肽合成(例如,固相合成)制备。编码所述肽的核酸分子的可用性使得使用本领域已知的体外表达方法和无细胞表达系统生产蛋白成为可能。体外转录和翻译系统可商购获得,例如,购自PromegaBiotech(Madison,WI)或Gibco-BRL(Gaithersburg,MD)。所述肽也可通过在合适的原核或真核系统中表达而生产。例如,编码所述肽的DNA分子的部分或全部可插入适合于在细菌细胞比如E.coli中表达的质粒载体。此类载体包括以允许所述DNA在宿主细胞中表达的方式定位的、对于所述DNA在宿主细胞中表达所必需的调控元件。对于表达所必需的此类调控元件包括启动子序列、转录起始序列和任选地增强子序列。在重组的原核或真核系统中通过基因表达产生的所述肽可根据本领域中已知的方法进行纯化。由上述方法所制备的本发明的所述肽可根据标准步骤进行分析。例如,此类蛋白可根据已知方法进行氨基酸序列分析。本发明的所述肽可偶联到载体蛋白(例如,大分子载体)。例如,所述肽可用于体内免疫目的。尽管动物可用游离肽进行免疫,然而抗肽抗体滴度仍可通过将所述肽偶联到载体而提高。载体的实例包括(但不限于)KLH(钥孔血蓝蛋白)、GST(谷胱甘肽-S-转移酶)、BSA(牛血清白蛋白)、cBSA(阳离子化的牛血清白蛋白)、OVA(卵清蛋白)、LPH(美洲鲎血蓝蛋白)和TT(破伤风类毒素)。本发明还包括对RhoB(例如,SEQIDNO:3)免疫上特异的抗体或抗体片段。本发明还包括对如上文所述的氨基酸序列免疫上特异的抗体或抗体片段。在具体实施方案中,所述肽与SEQIDNO:1、2、5、6、7或8具有至少90%、95%、97%、99%或100%的同源性或同一性。所述肽可在肽的N端和/或C端比上文经鉴定的序列长或短0、1、2、3、4、5、6、7、8、9、10或更多个氨基酸,尤其是1、2、3、4或5个氨基酸。在另一个实施方案中,本发明的所述肽与SEQIDNO:3具有至少90%、95%、97%、99%或100%的同源性或同一性。本发明的抗体分子可使用本领域中已知的各种方法制备。多克隆和单克隆抗体可如CurrentProtocolsinMolecularBiology,Ausubeletal.eds中描述的制备。抗体可通过化学交联、混合杂交瘤技术制备以及通过在宿主细胞比如细菌或酵母细胞中表达的重组抗体片段的表达制备。在具体实施方案中,所述抗体或抗体片段为对SEQIDNO:1或SEQIDNO:8免疫上特异的。在具体实施方案中,所述抗体为单克隆抗体、一对抗体或一组抗体。在具体实施方案中,所述抗体为包含SEQIDNO:10和12的单克隆抗体。在具体实施方案中,所述抗体为包含SEQIDNO:14和16的单克隆抗体。所述抗体可为天然存在的抗体或者可为合成或修饰的抗体(例如,重组产生的抗体;嵌合抗体;双特异抗体;人源化抗体;骆驼科动物抗体;等)。所述抗体可包含至少一种纯化标签。在具体实施方案中,框架抗体为抗体片段。抗体框架包括(但不限于)免疫球蛋白框架,包括(但不限于):单结构域(Dab;例如,单个可变轻链或重链结构域)、Fab、Fab'、F(ab')2和F(v);和这些免疫球蛋白片段的融合(例如,通过接头(linker)),包括(但不限于):scFv、scFv2、scFv-Fc、微型抗体、双链抗体、三链抗体和四链抗体。所述抗体还可为包含至少一种抗体或抗体片段的蛋白质(例如,融合蛋白)。在本发明的具体实施方案中,所述抗体包含Fc区。本发明的抗体或抗体片段可包含来自抗RhoB单克隆抗体7F7和9G5的至少一个结构域。例如,所述抗体或抗体片段可包含抗RhoB单克隆抗体7F7和9G5的至少一个、两个、三个、四个、五个或全部六个CDR结构域(见图9和10)。在具体实施方案中,所述抗体或抗体片段包含CDR3结构域的至少一个或两个。在具体实施方案中,所述抗体或抗体片段的结构域与存在于抗RhoB单克隆抗体7F7或9G5中的结构域具有至少90%、95%、97%、99%或100%的同源性或同一性。所述结构域可在结构域的N端和/或C端比图9和10中描述的结构域长或短大约1、2、3、4或5个氨基酸,尤其是1或2个氨基酸。所述抗体也可为模拟免疫球蛋白的合成蛋白。实例包括(但不限于)分子(Affibody,Bromma,Sweden)、darpins(设计的锚蛋白重复蛋白;Kaweetal.(2006)J.Biol.Chem.,281:40252-40263)和五价体(peptabodies)(Terskikhetal.(1997)PNAS94:1663–1668)。本发明的抗体可进一步被修饰。例如,所述抗体可被人源化。在具体实施方案中,所述杂合抗体(或其一部分)被插入抗体或抗体片段构建体的主链。例如,本发明所述抗体的可变轻链和/或可变重链可插入另一个抗体构建体。重组产生抗体的方法是本领域中已知的。事实上,用于某抗体和抗体片段构建体的商业载体是可获得的。本发明的抗体也可与其它组分偶联/连接。例如,所述抗体可可操作地连接(例如,共价连接,任选地通过接头)至少一种可检测剂、显像剂、造影剂、免疫抑制剂或抗炎剂。本发明的抗体还可包含至少一种纯化标签(例如,His标签)。包含所述RhoB抑制剂或抗体的组合物也被本发明所包括。在具体实施方案中,所述组合物包含至少一种本发明的抗体或抗体片段和至少一种药学上可接受的载体。本发明的抗体分子可使用本领域中已知的各种方法制备。抗体可通过化学交联、混合杂交瘤技术制备以及通过在宿主细胞比如哺乳动物细胞、细菌或酵母细胞中表达的重组抗体或抗体片段的表达而制备。在本发明的一个实施方案中,所述抗体分子通过重组抗体或抗体片段在宿主细胞中的表达而产生。编码所述抗体的核酸分子可插入表达载体并引入宿主细胞。然后将所产生的抗体分子从所述表达系统中分离并纯化。所述抗体任选地包含纯化标签,所述抗体可通过其进行纯化。本发明的抗体分子的纯度可使用本领域技术人员已知的标准方法(包括但不限于ELISA、免疫组化、离子交换色谱法、亲和色谱法、固定金属亲和色谱法(IMAC)、排阻色谱、聚丙烯酰胺凝胶电泳(PAGE)、蛋白免疫印迹、表面等离子体共振和质谱分析)进行评估。本发明还包括分泌单克隆RhoB抗体的杂交瘤。目前,RhoB杂交瘤为(平均)缓慢生长的并且与其它杂交瘤相比产生更低量的抗体。可采取几种方法来规避这种可能的限制。例如,可从所述杂交瘤克隆所述抗-RhoB抗体的核苷酸序列,然后通过分子生物学方法产生抗-RhoB抗体。在另一个实施方案中,可开发RhoB非依赖性分泌杂交瘤或者可改进杂交瘤培养条件以使抗体产量达到最大。本发明还包括用于鉴定作为RhoB抑制剂的小分子或其它分子实体比如小核酸、肽、碳水化物等的方法。在具体实施方案中,本发明的RhoB抗体或其片段(尤其是CDR区)或相应的表位可用于设计具有相似生物活性的RhoB抑制剂。定义化合物或药物组合物的“治疗有效量”指的是对于预防、抑制、治疗或减轻具体病症或疾病的症状有效的量。本文中炎症性病症的治疗可指医治、缓解和/或预防所述炎症性病症、其症状或对其的易感性。“药学上可接受的”表示由联邦或州政府的管理机构批准或者在美国药典或其它通常公认的药典上列出的用于动物,尤其是人类的。例如,“载体(carrier)”指的是稀释剂、佐剂、赋形剂、辅助剂或用其施用本发明的活性剂的媒介物。药学上可接受的载体可为无菌液体,比如水和油,包括石油、动物、植物或合成来源的那些,比如花生油、大豆油、矿物油、芝麻油等。水或盐水溶液和葡萄糖水溶液和甘油溶液优选用作载体,特别是用于可注射溶液。例如,合适的药学载体由E.W.Martin在“Remington'sPharmaceuticalSciences”中进行了描述。“抗体”或“抗体分子”为结合于特定抗原的任意免疫球蛋白,包括抗体和其片段。如本文使用的,抗体或抗体分子覆盖(contemplates)完整的免疫球蛋白分子、免疫球蛋白分子的免疫活性部分和免疫球蛋白分子的免疫活性部分的融合。如本文使用的,术语“免疫上特异的”指的是蛋白/多肽,尤其是抗体,其在含有混合种群的抗原性生物分子的样品中结合感兴趣的蛋白或化合物的一个或多个表位但是基本上不识别和结合其它分子。如本文使用的,术语“预防”指的是处于发病风险的受试者的预防性治疗,导致所述受试者将发展所述病况的可能性减小。如本文使用的术语“治疗”指的是赋予患有疾病的患者益处的任何类型的治疗,包括所述患者病况(例如,一个或多个症状)的改善,病况进展的延迟等。如本文使用的,术语“宿主”、“受试者”和“患者”指的是任何动物,包括人类。术语“小干扰RNA(siRNA)”指的是短的(通常不到30个核苷酸长,特别是12-30个或20-25个核苷酸长)双链RNA分子。通常,所述siRNA调节siRNA所靶向的基因的表达。鉴定和合成siRNA分子的方法为本领域中已知的(参见,例如,Ausubeletal.(2006)CurrentProtocolsinMolecularBiology,JohnWileyandSons,Inc)。如本文使用的,术语siRNA可包括短发卡RNA分子(shRNA)。通常,shRNA分子由通过小环序列分割的短互补序列组成,其中所述序列的一个与所述基因靶标互补。shRNA分子通常由内切酶在细胞中加工成siRNA。对于siRNA分子的示例性修饰在美国专利申请公开号20050032733中有提供。用于siRNA分子表达的表达载体优选使用强启动子,其可为组成型或者调节型的。此类启动子在本领域中是众所周知的,并且包括但不限于RNA聚合酶II启动子、T7RNA聚合酶启动子和RNA聚合酶III启动子U6和H1(参见,例如,Myslinskietal.(2001)Nucl.AcidsRes.,29:250209)。“反义核酸分子”或“反义寡核苷酸”包括靶向(互补的)所选序列(例如,翻译起始位点和/或剪接位点)以抑制感兴趣的蛋白表达的核酸分子(例如,单链分子)。此类反义分子通常长度在约15到约50个核苷酸之间,尤其是在约15到约30个核苷酸之间,并常常跨越mRNA分子的翻译起始位点。也可产生反义构建体,其包含相反方向的所述靶核酸分子的全部序列。靶向任何已知的核苷酸序列的反义寡核苷酸可根据标准方法通过寡核苷酸合成而制备。用于治疗自身免疫性和炎症性疾病的疗法和组合物如上文所述,本发明包括包含至少一种抗-RhoB抗体(包括其片段)和至少一种药学上可接受的载体的组合物。所述组合物可进一步包括至少一种其它抗炎剂和/或至少一种免疫抑制剂。作为选择,至少一种其它抗炎剂和/或至少一种免疫抑制剂可与至少一种药学上可接受的载体一起包含在单独的组合物中。包含至少一种抗-RhoB抗体的组合物和包含至少一种其它抗炎剂和/或至少一种免疫抑制剂的组合物可包含在试剂盒中。此类组合物可以治疗有效量向需要其的患者施用以治疗炎症性或自身免疫疾病。在具体实施方案中,所述患者在施用本发明的组合物后至少监控一次所述炎症性或自身免疫疾病以监控所述炎症性或自身免疫性疾病的治疗(例如,就类风湿性关节炎、关节(例如,手关节)痛和/或僵硬;类风湿结节的存在;和/或类风湿因子或类风湿因子抗体在血液中的存在)。本发明的组合物可通过任何合适的途径施用,例如,通过注射(例如,对于局部或全身施用)、静脉内、口服、肺部、鼻或其它施用模式。通常,所述组合物的药学上可接受的载体选自稀释剂、防腐剂、增溶剂、乳化剂、佐剂和/或载体的组。所述组合物可包括各种缓冲液内容(例如,Tris-HCl、醋酸、磷酸)、pH和离子强度的稀释剂;和添加剂比如去污剂和增溶剂(例如,吐温80、聚山梨醇酯80)、抗氧化剂(例如,抗坏血酸、焦亚硫酸钠)、防腐剂(例如,Thimersol、苯甲醇)和填充物质(例如,乳糖、甘露醇)。所述组合物还可掺入聚合化合物比如聚乳酸、聚乙醇酸等的微粒制剂,或者掺入脂质体或纳米粒子。此类组合物可影响本发明药物组合物的组分的物理状态、稳定性、体内释放速率和体内清除速率。参见,例如,Remington’sPharmaceuticalSciences,18thEd.(1990,MackPublishingCo.,Easton,PA18042)pages1435-1712,其通过引用并入本文。本发明的药物组合物可例如以液态制备,或可为干燥粉末形态(例如,冻干的)。在另一个实施方案中,本发明的药物组合物可在控释系统中递送,比如使用静脉内灌输、可移植的渗透泵、透皮贴剂、脂质体或其它施用模式。在具体实施方案中,可使用泵(见Langer,supra;Sefton,CRCCrit.Ref.Biomed.Eng.(1987)14:201;Buchwaldetal.,Surgery(1980)88:507;Saudeketal.,N.Engl.J.Med.(1989)321:574)。在另一个实施方案中,可使用聚合材料(见MedicalApplicationsofControlledRelease,LangerandWise(eds.),CRCPress:BocaRaton,Florida(1974);ControlledDrugBioavailability,DrugProductDesignandPerformance,SmolenandBall(eds.),Wiley:NewYork(1984);RangerandPeppas,J.Macromol.Sci.Rev.Macromol.Chem.(1983)23:61;还见Levyetal.,Science(1985)228:190;Duringetal.,Ann.Neurol.(1989)25:351;Howardetal.,J.Neurosurg.(1989)71:105)。在另外一个实施方案中,控释系统可放置在动物的靶组织附近,从而仅需要全身剂量的一部分(参见,例如,Goodson,inMedicalApplicationsofControlledRelease,supra,(1984)vol.2,pp.115-138)。特别是,控释系统可在接近不适当炎症的位点引入动物。其它控释系统在综述中由Langer进行了讨论(Science(1990)249:1527-1533)。本发明的方法可还包括施用至少一种其它治疗方法用于治疗所述自身免疫疾病或炎症性疾病。例如,在自身免疫疾病的治疗中,所述抗-RhoB抗体可与受试者的淋巴结辐射或与血浆除去法共同施用。在另一个实施方案中,本发明包括包含至少一种RhoB序列肽(包括其序列)和至少一种药学上可接受的载体的组合物。所述组合物可进一步包含其他剂(例如,至少一种其它抗炎剂和/或至少一种免疫抑制剂)或与其它组合物一起被包括在试剂盒中,如上文对于所述抗-RhoB抗体所描述的。所述组合物可如上文对于所述抗-RhoB抗体所描述的被递送至受试者(例如,治疗方法)。提供以下实施例以说明本发明的各种实施方案。这些实施例并非意图以任何方式限制本发明。实施例1用RhoB-肽-KLH或KLH(钥孔血蓝蛋白)免疫RhoB基因敲除小鼠。具体地址,在第0天,用完全弗氏佐剂(CFA)中的RhoB-肽-KLH或KLH注射RhoB基因敲除小鼠。在第14天,用不完全弗氏佐剂(IFA)中的RhoB-肽-KLH或KLH给予加强注射。最后,在第29天用磷酸盐缓冲液(PBS)中的RhoB-肽-KLH或KLH进行第二次加强注射。在第10天和第24天获得出血并在第32天收集血清。K/BxNTCR转基因鼠表达由II类MHC分子Ag7呈递的、对源自葡糖-6-磷酸异构酶(GPI)的自体肽反应的TCR(Korganowetal.(1999)Immunity,10:451–461;Kouskoffetal.(1996)Cell,87:811–822;Matsumotoetal.(1999)Science,286:1732–1735)。K/BxN小鼠在4到5周龄自发地发展非常凶猛的关节炎。所述K/BxN小鼠的关节炎模拟人类关节炎,因为它是慢性的、进行性的、对称的,并且表现出人类关节炎相同的组织学特征。K/BxN小鼠所经历的关节炎是关节特异的并且通过卡尺测量踝关节厚度而允许关节炎的评分(Korganowetal.(1999)Immunity,10:451–461;Jietal.(2001)J.Exp.Med.,194:321–330)。K/BxN小鼠(每组5只小鼠)用1)生理盐水,2)抗KLH血清,或者3)抗RhoB-肽血清进行治疗。具体地,血清(200μl)腹膜内施用给21天龄的小鼠。平均踝关节厚度作为关节炎的指示(indicator)随时间进行测量。如图1所见,RhoB抗血清抑制关节炎。K/BxN小鼠产生针对GPI的关节炎基因抗体,其因为优先帮助表达GPI特异的免疫球蛋白的B细胞接收显示转基因编码的TCR的GPI反应性T细胞而以高滴度发展。如上,K/BxN小鼠(每组5只小鼠)用总数为200μl(100μl血清与100μl生理盐水混合)(腹膜内)的1)生理盐水,2)抗-KLH血清,或者3)抗-RhoB-肽血清治疗。如图2A和2B所见,施用RhoB抗血清的K/BxN小鼠的血清与施用KLH抗血清或单独施用载体的K/BxN小鼠相比血清抗GPIIg水平降低(如通过酶联免疫吸附测定(ELISA)所测定的),并且与施用KLH抗血清或单独施用载体的K/BxN小鼠相比抗-GPI抗体分泌细胞数目减少(如通过酶联免疫斑点(ELISPOT)所测定的)。除了上述之外,还在K/BxN小鼠中测定了RhoB抗血清是否影响其它细胞因子。与施用KLH抗血清或单独施用载体的K/BxN小鼠相比,向K/BxN小鼠施用RhoB抗血清并不显著调节IFNγ、TNFα、IL-6、IL-10、MCP-1、MIP-1α、MIP-1β或RANTES的水平。从所述小鼠分离脾细胞并将B细胞与永生化的骨髓瘤细胞(Sp2/0)融合以产生杂交瘤。测试48个样品。7个对肽1(RTDDGRAMAVRIQAYDYLE;SEQIDNO:1;人RhoB(GenBankAccessionNo.CAA29968)的140-158位氨基酸)产生强阳性,5个对肽1和肽2(DDGRAMAVRIQAY;SEQIDNO:2;人RhoB(GenBankAccessionNo.CAA29968)的142-154位氨基酸)产生阳性。图3提供了人RhoB的氨基酸序列。肽1为下划线的。将接种包含该序列的肽抗原的小鼠分为两组抗体。这两组抗体通过稍有不同但是重叠的表位进行定义:一组抗体的结合可受Y156磷酸化的影响,但另一组抗体将不可能(见上文区别肽1和肽2的结果,其缺乏156位的酪氨酸)。两组抗体均特异地识别全长RhoB蛋白,但是在组织培养或动物中仅一组阻断由B细胞的抗体分泌。图4提供了ELISA实验结果,其中证明抗-RhoB杂交瘤上清(黑色)抑制由LPS-处理的小鼠B细胞的抗体分泌:比较基线(未活化的;菱形)、活化的红线(方形)和抑制的线(三角形)。X线为不抑制活化的非特异对照(IDO抗体)。其他线表示由自原始杂交瘤分离的抗-RhoB杂交瘤亚克隆获得的上清,显示中等抑制水平。碘化丙啶(PI)染色证明,B细胞响应LPS而增殖。使用IL6微珠阵列(beadarray)的分析显示,抗-RhoB杂交瘤不分泌IL6。实施例2K/BxN小鼠在关节炎发作前用500μg的抗-RhoB单克隆抗体9G5或7F7或对照Ig治疗(21天龄)。图6A显示抗-RhoB单克隆抗体9G5和7F7均抑制关节炎,如通过后踝关节厚度所显示的。图6B和图6C显示,抗-RhoB单克隆抗体也抑制自身抗体产生,如通过ELISA测量抗-GPI自身抗体滴度(图6B)和通过ELISpot测定测量抗-GPI抗体分泌细胞(ASCs)(图6C)。K/BxN小鼠还在关节炎发作后用500μg的抗-RhoB单克隆抗体9G5或7F7或对照Ig治疗(4周龄)。如图7可见的,抗-RhoB单克隆抗体9G5和7F7抑制关节炎的进展,如通过后踝关节厚度所测定的。除了上述之外,还在K/BxN小鼠中测定了抗-RhoB单克隆抗体是否影响其它细胞因子。K/BxN小鼠在21天龄用500μg的7F7或对照Ig治疗。在6周龄时收集来自关节引流淋巴结的细胞并在具有离子霉素(500ng/ml)的PMA(50ng/ml)中培养过夜。通过流式微珠阵列测量培养上清中的细胞因子。与施用对照Ig的K/BxN小鼠相比,向K/BxN小鼠施用抗RhoB单克隆抗体7F7并不显著调节炎症性细胞因子IFNγ、TNFα、IL-17、IL-10、MCP-1、MIP-1α、MIP-1β和RANTES或B细胞相关细胞因子IL-4,IL-5,IL-6,IL-9,IL-10和IL-13的水平。关节炎RhoB基因敲除(KO)(RhoBKOKRN.g7)小鼠通过交叉在KRN.g7背景之上而产生。KRNB6.g7小鼠为表达对于KRNT细胞活化必要的KRNTCRtg和IAg7MHCII类分子,但是缺乏其余的NOD相关基因的C57BL/6小鼠(Kouskoffetal.(1996)Cell87:811-822)。图8A显示,与KRN.g7小鼠相比,RhoBKO小鼠关节炎减轻,如通过后踝关节厚度所测定的。图8B显示,当转移到幼稚接受者(recipients)时,来自RhoBKOKRN.g7小鼠的血清也不能诱导关节炎。具体地,在第0天,将来自KRNB6.g7或RhoBKOKRNB6.g7小鼠的血清过继转移至幼稚C57BL/6小鼠。但是,图8C显示,当关节炎基因K/BxN血清被过继转移时,可在RhoBKO小鼠中诱导关节炎。来自关节炎基因K/BxN小鼠的血清在第0天被过继转移至幼稚野生型或RhoBKOC57BL/6小鼠。明显地,在所述RhoBKO小鼠所观察的关节炎更为严重并且持续时间更长。在不受理论束缚的情况下,在RhoBKO小鼠中所观察的关节炎严重性增加可能是由于所述小鼠不能清除自身抗体。的确,与KRN.g7小鼠相比,抗-GPI自身抗体滴度在RhoBKOKRN.g7小鼠中适度增加,但是抗-GPI抗体分泌细胞(ASCs)的数目在两种小鼠之间是相似的。此外,还在RhoBKO小鼠中测定了细胞因子是否受影响。在6周龄时收集来自关节引流淋巴结的细胞并在具有离子霉素(500ng/ml)的PMA(50ng/ml)中培养过夜。通过流式微珠阵列测量培养上清中的细胞因子。当与KRN.g7小鼠相比时,RhoBKOKRN.g7小鼠不显著调节炎症性细胞因子IFNγ、TNFα、IL-17、IL-10和MCP-1(尽管在RhoBKOKRN.g7小鼠中RANTES、MIP-1α和MIP-1β趋于小幅下降)或者B细胞相关的细胞因子IL-4、IL-5、IL-6、IL-9、IL-10和IL-13的水平。在不受理论束缚的情况下,RhoBKO小鼠的与施用抗-RhoB抗体的小鼠相比的小鼠表型的相似性是抗-RhoB抗体通过其与RhoB的相互作用发挥其活性的进一步的证据。RhoBKOC57BL/6小鼠也拥有正常的淋巴群。具体地,通过流式细胞术测量野生型和RhoBKOC57BL/6小鼠的骨髓、胸腺、脾脏、淋巴结和腹腔中的淋巴群的百分比。还通过ELISA测量野生型和RhoBKOC57BL/6小鼠的血清Ig水平。明显地,在野生型和RhoBKOC57BL/6小鼠之间没有观察到淋巴群或血清Ig水平(IgM、IgG1、IgG2b、IgG2c和IgG3)的显著差别。RhoB-/-、RhoB+/-、或RhoB+/+C57BL/6小鼠也在第0天用100μg明矾中的NP-KLH进行免疫。在第0、5、14和21天采取血清样品并通过ELISA分析抗NPIgM或IgG。RhoBKO小鼠表现出对免疫的正常响应。为了更充分地描述本发明所属领域的状态,在前面的说明书中引用了一些出版物和专利文献。这些引文的每个的公开内容均通过引用的方式并入本文。虽然上文已描述并具体例举了本发明的某些优选的实施方案,但是并不意味着本发明局限于这些实施方案。可在不脱离本发明的如以下权利要求中所述的范围和精神的情况下对其做出各种修改。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1