一种具有多药协同作用的抗肿瘤高分子键合药及其制备方法与流程
本发明涉及一种抗肿瘤药物,特别涉及一种具有多药协同作用的抗肿瘤高分子键合药及其制备方法;属于生物医药高分子材料领域。
背景技术:
肿瘤是一个全球性的公共健康问题。近三十年来,世界癌症发病率以每年3-5%的速度增加,二十一世纪,肿瘤已成为导致人类死亡的第一诱因。化疗作为肿瘤三大治疗手段之一,是目前肿瘤治疗的重要手段。尽管化疗在治疗肿瘤方面已经取得了长足的进步,然而在临床应用中仍存在一些障碍。如传统的肿瘤化疗采取的是单一化疗药物,其主要缺陷是单一药物的治疗往往会激活和强化肿瘤细胞其他方面的存活路径,从而导致耐药性的出现并最终导致化疗失败。同时为了达到治疗效果,需要更高的药物剂量,导致难以接受的药物毒副作用。为了解决这一难题,近年来,利用多个药物的协同作用使用联合给药的方法成为抗肿瘤药物药剂学领域的一个研究热点。
目前,临床使用的抗肿瘤药物以紫杉醇、阿霉素、喜树碱、顺铂为主。这类抗肿瘤药物因其抗癌机理的不同而作用于肿瘤细胞的不同周期。如紫杉醇作用于微管/微管蛋白系统,可影响微管蛋白的装配和解聚,从而导致微管束的排列异常,形成星状体,使纺锤体失去正常功能,导致细胞死亡,作用于细胞周期的G2和M期;阿霉素通过嵌入癌细胞的DNA碱基片段中,阻碍DNA的转录和复制,从而抑制肿瘤细胞生长,属周期非特异性药物;喜树碱能稳定拓扑异构酶I和DNA的共价化合物,形成了三元可解离复合物,通过复制冲突模型造成DNA损伤,最终导致细胞死亡,作用于细胞周期的S期。联合用药是基于不同的化疗药物对应于肿瘤细胞的不同信号通路,在肿瘤细胞的不同生长周期产生抑制作用,从而实现治疗目的。
然而小分子药物的联合存在不同药物的代谢性质、组织和器官分布、穿透各 级膜的能力的不同的问题,很难控制到达最终靶点的多种药物仍保持注射时的最初浓度。其次,小分子药物的联合,往往会带来更大的副作用和毒性。因此,使用聚合物前药或纳米药物载体成为联合用药的最佳策略。众所周知,纳米药物载体具有可通过合适的尺寸和结构设计来改变药物的药代动力学和体内分布以及通过EPR效应实现被动靶向的优点。作为载体给药系统的一员,从两亲性嵌段共聚物发展而来的聚合物胶束深受青睐。当投入到水性介质中时,在体系自由能降低的驱动下,胶束的疏水段自发聚集在一起形成微粒的内核。它既可以作为很多难溶性药物的微储库,又能避免药物在生物体内环境中失活。自组装形成的载药胶束是热力学、动力学稳定的体系,具有稳定、长效、安全等许多优良的性质,使得聚合物胶束成为难溶性药物理想的输送系统,且在药物释放、基因载体和诊断制剂等很多方面得到广泛地应用。
聚合物修饰剂的选择是药物分子修饰的关键,现有研究表明脂肪族聚酯如聚乳酸(PLA),聚乳酸-羟基乙酸共聚物(PLGA)和聚ε-己内酯(PCL)属于生物可降解聚合物。它们的分子量在相当宽的范围可以随意控制,所以在聚合物药物载体的研究中得到了广泛的应用。特别是在与水溶性聚合物形成嵌段共聚物后,不仅具有生物可降解性,而且大大地改善了材料与人体的生物相容性,作为药物载体材料时,延长了药物在体内的循环时间,提高了药效,降低了免疫响应性,已经成为生物医药高分子材料领域的研究热点。
技术实现要素:
针对传统的肿瘤化疗采取的是单一化疗药,或一些联合给药的药物载体大多都是不可降解的高分子聚合物,且其键合方式都是物理包裹,导致人体对药物的生物利用度低,抗癌活性差等缺陷;本发明的目的是在于提供一种以可生物降解高分子为载体,同时负载多种抗肿瘤药物构成的高分子键合药,该高分子键合药通过多药协同作用提高抗癌活性,同时降低化疗的毒副作用,且该高分子键合药生物相容性好,载药量高且可控,可以应用于临床研究。
本发明的另一个目的是在于提供一种经济、高效和无毒的制备上述可生物降解的具有多药协同作用的抗肿瘤药高分子键合药的方法。
为了实现上述技术目的,本发明提供了一种具有多药协同作用的抗肿瘤高分 子键合药,具有式1结构:
其中,
A为含有羟基的抗肿瘤药物基团;
B为含有氨基的抗肿瘤药物基团;
n为45~454,x为1~20,y为1~20;
R1和R2独立地选自C1~C4的亚烷基。
优选的方案,A为紫杉醇基团、多西紫杉醇基团、喜树碱基团、丝裂霉素C基团中的至少一种。
优选的方案,B为阿霉素基团、表阿霉素基团、吡喃阿霉素基团中的至少一种。
本发明还提供了一种制备所述的具有多药协同作用的抗肿瘤高分子键合药的方法,该方法包括以下步骤:
1)以聚乙二醇单甲醚引发含降冰片烯基团的丙交酯进行开环聚合,聚合产物再引发α溴代己内酯进行开环聚合,得到聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物;
2)所述聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物与含巯基的醇类化合物进行巯基-溴点击反应,得到含羟基侧基的聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物;所述含羟基侧基的聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物与对硝基苯基氯甲酸酯进行缩合反应,得到含对硝基苯基甲酸 酯侧基的聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物;所述含对硝基苯基甲酸酯侧基的聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物与含巯基的酸类化合物进行巯基-烯光点击反应,得到式2载体聚合物;
3)含羟基的抗肿瘤药物和含氨基的抗肿瘤药物与式2载体聚合物分别进行酯化反应和酰胺化反应,即得;
其中,
n为45~454;
x为1~20;
y为1~20;
R1和R2各自独立地选自C1~C4的亚烷基。
优选的方案,含有氨基的抗肿瘤药物为阿霉素、表阿霉素、吡喃阿霉素中的至少一种。
优选的方案,含有羟基的抗肿瘤药物为紫杉醇、多西紫杉醇、喜树碱、丝裂霉素C中的至少一种。
本发明的聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯聚合物的制备方法:
将丙交酯和N-溴代丁二酰亚胺(NBS),以四氯化碳或苯为溶液,以过氧化二苯甲酰(BPO)做催化剂,在60~90℃下发生取代反应,得到溴代丙交酯;得到的溴代丙交酯以二氯甲烷溶剂中,在三乙胺的作用下,0~5℃下发生消去反应得到 双键丙交酯;得到的双键丙交酯和新蒸环戊二烯在四氯化碳或苯溶液中,氩气保护,60~90℃下,通过Diels-Alder反应后,得到含降冰片烯侧基的丙交酯;
将环己酮和N-溴代丁二酰亚胺(NBS)以无水乙醚为溶剂,醋酸铵(NH4AcO)做催化剂,室温下反应得到溴代环己酮;溴代环己酮通过Baeyer-Villiger氧化反应与间氯过氧苯甲酸(m-CPBA)生成了α位溴代己内酯;
以聚乙二醇单甲醚为大分子引发剂,TBD或DBU为催化剂,二氯甲烷为溶剂,-20~40℃下引发含降冰片烯侧基的丙交酯进行开环聚合得到聚乙二醇单甲醚-b-聚丙交酯聚合物,再以聚乙二醇单甲醚-b-聚丙交酯聚合物为大分子引发剂,同样的聚合条件将α溴代己内酯引发聚合,得到聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯聚合物。
本发明的聚合物官能化的制备方法:将聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯聚合物采用巯基-溴点击化学反应和巯基-烯光点击化学反应,反应点击效率高,无副产物。
本发明的含羟基的抗肿瘤药物与高分子载体进行DIC缩合反应,其副产物易除去,避免了传统DCC缩合后剧毒物质DCU的产生。含氨基的抗肿瘤药物与对硝基苯基甲酸酯活化的高分子载体键合,其键合效率高,生成的酰胺键稳定。
本发明的具有多药协同作用的抗肿瘤高分子键合药的合成路线如下:
以抗肿瘤药物紫杉醇(paclitaxel)和阿霉素(doxorubicin)为例:
相对现有技术,本发明的技术方案带来的有益效果:
1)与现有的高分子抗肿瘤高分子键合药相比,本发明的抗肿瘤高分子键合药最大的优势在于通过将抗肿瘤药物阿霉素和紫杉醇等同时键合到高分子载体上,不同的抗肿瘤药物对应于肿瘤细胞的不同信号通路,在肿瘤细胞的不同生长周期产生抑制作用,提高治疗效果。如阿霉素通过嵌入癌细胞的DNA碱基片段 中,阻碍DNA的转录和复制,从而抑制肿瘤细胞生长;而紫杉醇作用于微管/微管蛋白系统,可影响微管蛋白的装配和解聚,从而导致微管束的排列异常,形成星状体,使纺锤体失去正常功能,导致细胞死亡。
2)本发明的高分子抗肿瘤高分子键合药另一优势在于可降低化疗药物的毒副作用,因为药物联合作用导致每种药物的给药剂量减少,同时抗癌活性不受影响,提高了药物的利用度,可以降低化疗成本。
3)本发明的高分子抗肿瘤高分子键合药在端基引入分子量较小的聚乙二醇单甲醚,聚乙二醇单甲醚不但具有较好的生物相容性及生物可降解性,并且在水相中易于自组装形成纳米胶束粒子,延长了药物在体内的循环时间,提高了药效,降低了免疫响应性。
4)本发明的高分子抗肿瘤高分子键合药的制备方法操作简单、反应条件温和、副反应少、产率高和安全无毒,且易于调控高分子键合药的载药量,满足工业生产要求。
附图说明
【图1】为聚乙二醇单甲醚-b-聚丙交酯两嵌段共聚物的核磁氢谱图;
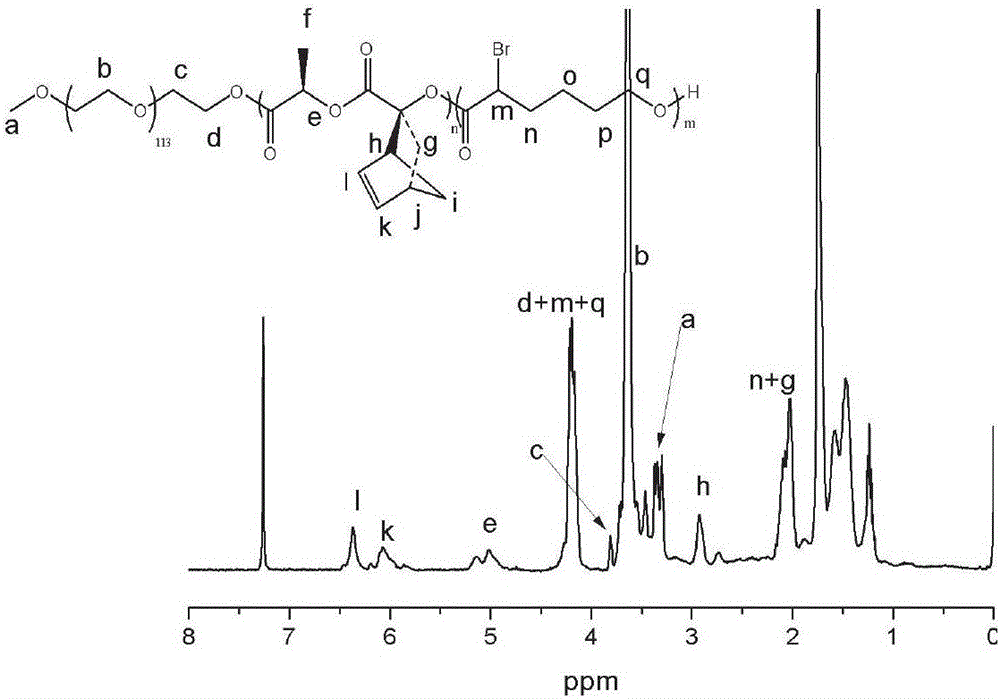
【图2】为聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物的核磁氢谱图;【图3】为实施例1的步骤1中各聚合物的分子量分布图:A为聚乙二醇单甲醚的分子量分布图,B为聚乙二醇单甲醚-b-聚丙交酯共聚物的分子量分布图,C为聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物的分子量分布图;
【图4】为聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物与巯基乙醇反生巯基-溴点击反应得到的含羟基侧基的聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物核磁氢谱图;
【图5】为含对硝基苯基甲酸酯侧基的聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物的核磁氢谱图;
【图6】为含对硝基苯基甲酸酯侧基的聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物与巯基丙酸反生巯基-烯光点击反应得到的载体聚合物的核磁氢谱图;
【图7】为含紫杉醇的抗肿瘤高分子键合药的核磁氢谱图;
【图8】为含紫杉醇和阿霉素高分子键合药的核磁氢谱图;
【图9】为实施例1中步骤2~4中各聚合物的分子量分布图:A为聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物与巯基乙醇反生巯基-溴点击反应得到的含羟基侧基的聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物的分子量分布图,B为含对硝基苯基甲酸酯侧基的聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物的分子量分布图,C为含对硝基苯基甲酸酯侧基的聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物与巯基丙酸反生巯基-烯光点击反应得到的含羧基侧基的聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物分子量分布图。
具体实施方式
以下实施例旨在是对本发明内容进一步说明,而不是限制本发明权利要求的保护范围。
实施例1
1、聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物的制备:
首先,在己真空烤过3次的安培瓶中,于氮气保护下加入0.80g的降冰片烯侧基的丙交酯和1.00g聚乙二醇单甲醚(mPEG),之后加入1mL的精制的DCM使其完全溶解,注射由精制DCM配制好的含引发剂TBD溶液1mL,常温反应48h后,用无水乙醚沉降3次,离心后真空干燥,得到聚乙二醇单甲醚-b-聚丙交酯两嵌段聚合物,结构表征如图1所示,分子量分布为图3。然后,再以其为大分子引发剂,同样聚合条件下引发α溴代己内酯聚合,得到聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物,其结构表征如图2,分子量分布见图3,说明该聚合物已成功合成。
2、含羟基侧基的聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物的制备:
称取上述聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物0.5g(0.06mmol),2-巯基乙醇0.054g(0.73mmol),溶于10mL的乙腈,加入0.05mL三乙胺做催化剂,在氩气保护下反应2h。反应结束后用水透析24h,除去季铵盐,再用无水乙醚沉降,离心后真空干燥,得到纯的含羟基侧基的聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物。其结构表征见核磁氢谱图(图4),分子量分 布见图9A,说明该聚合物已成功合成。
3、含对硝基苯基甲酸酯侧基的聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯共聚物的制备:
称取含羟基侧基的聚乙二醇单甲醚-b-聚丙交酯-b-聚α溴代己内酯聚合物0.4g(0.049mmol),溶于10mL二氯甲烷,在氩气保护下缓慢滴加0.21g对硝基苯基氯甲酸酯和0.05mL三乙胺,0℃反应24小时,反应结束后用无水乙醚沉降3次,离心后真空干燥。其结构表征见核磁氢谱图6,分子量分布见图9B。
4、载体聚合物的制备:
在氮气的保护下,将0.3g(0.45mmol)上述聚合物溶解在10mL精制的四氢呋喃(THF)中,加入0.030g(0.029mmol)3-巯基丙酸,3mg安息香二甲醚(DMPA)光引发剂,在紫外灯光照下反应0.5h。反应结束后,用无水乙醚沉降3次,离心后真空干燥,得到载体聚合物。其结构表征见核磁氢谱图6,分子量分布见图9C,说明该聚合物已成功合成。
5、含紫杉醇的高分子键合药的制备
称取载体聚合物0.1g(0.008mmol),紫杉醇0.029g(0.03mmol),N,N-二异丙基碳二亚胺(DIC)0.004g(0.03mmol)。将紫杉醇溶于10mL三氯甲烷,加入催化量的DMAP,在氮气保护下缓慢滴加溶于2mL三氯甲烷的聚合物和DIC,冰浴搅拌1h后,在45℃下反应24h。反应结束后用甲醇透析24h,除掉脲盐,然后用无水乙醚沉降3次,离心,真空干燥。其结构表征见核磁氢谱图7。
6、含紫杉醇和阿霉素的高分子键合药的制备:
称取上述紫杉醇前药0.5g,盐酸盐阿霉素0.025g,将盐酸盐阿霉素溶于干燥的DMF,加入0.01mL三乙胺,抽真空充氮气三次,反应2小时脱掉盐酸盐,再加入紫杉醇前药,避光,室温反应48h。反应结束后,用DMF透析48h,乙腈透析掉DMF,无水乙醚沉降,离心,真空干燥。其结构表征见核磁氢谱图8。
- 还没有人留言评论。精彩留言会获得点赞!