超临界抗溶剂法制备柚皮素/羟丙基‑β‑环糊精微胶囊的方法与流程
本发明涉及柚皮素/环糊精微胶囊的制备,具体涉及一种应用超临界抗溶剂法制备柚皮素/羟丙基-β-环糊精微胶囊的方法。
背景技术:
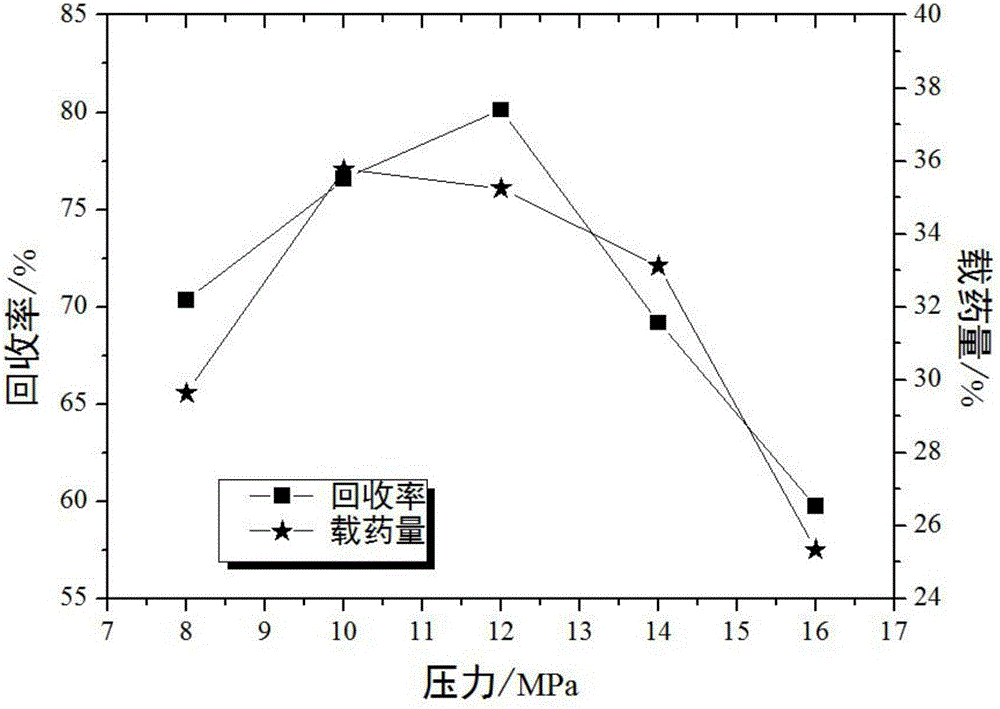
:柚皮素是一类天然黄酮类化合物,是柚皮苷的苷元,是从芸香科植物油中提取的一种单体,广泛存在于柠檬、积壳、葡萄汁、胡芦巴、胡柚皮、华中冬青等中。国外对柚皮素的生物活性研究较多。资料显示柚皮素具备抗癌、抗氧化、抗溃疡、抗动脉粥硬化、抗炎、降脂等生物活性。虽然柚皮素具有广泛的生物活性,但柚皮素水溶性差,在胃肠道中溶解度低,溶出速度慢,生物利用度低,极大程度限制了其在临床上的应用。因此提高柚皮素的溶解速率,改善柚皮素在人体内的吸收,对于提高柚皮素药物的生物利用度有着重要意义。HP-β-CD是目前研究最深入,应用最广泛的环糊精衍生物之一。在食品、医药、化妆品行业都有应用。其中,在医药工业中,由于HP-β-CD表面活性和溶血活性低且对肌肉没有刺激性,所以它是一种理想的注射剂增溶剂和药物赋形剂。可以提高难溶性药物的水溶性、稳定性、生物利用度,使药物的疗效提高,服用量减少。HP-β-CD可达到调整或控制药物的释放速度,降低药物毒副作用。超临界抗溶剂法(SupercriticalAnti-solvent,SAS)是指溶剂可以与超临界流体很好的互溶,但溶质在超临界流体中的溶解度较低,当超临界流体与溶液相互接触时,流体扩散到溶液中,导致溶液迅速膨胀,溶质在溶液中的溶解度迅速下降,瞬间形成较高的过饱和度,促使溶质沉析。SAS是一种环保且新颖的制备超细微粒的方法,在制药、医疗、生物工程和化工等多个行业有着广泛的使用前途。与传统的药物超微粉化技术方法相比,超临界抗溶剂法具有不易失活、绿色环保、粒度分布窄、尺寸小等优点;SAS技术操作温度比较低,对药物的化学结构破坏小,特别适合于制备热敏性或者具有生物活性的药物;SAS技术制备药物微粒所使用的溶剂分离简单,大大减少了有机溶剂在药物中的残留。技术实现要素:本发明的目的是提供一种应用超临界抗溶剂法制备柚皮素/羟丙基-β-环糊精微胶囊的方法,以提高柚皮素在水中的溶解度,进而提高其生物利用度。上述目的是通过如下技术方案实现的:应用超临界抗溶剂法制备柚皮素/环糊精微胶囊的方法,包括如下步骤:步骤S1,将柚皮素和羟丙基-β-环糊精溶解于有机溶剂中,得到样品溶液;步骤S2,将CO2通入结晶釜中,调节结晶釜内的温度和压力;步骤S3,继续以一定流速通入CO2,维持结晶釜内的温度和压力不变,同时将步骤S1制备的样品溶液通入结晶釜中;步骤S4,样品溶液通入完毕后,持续通入CO2,维持结晶釜内的温度和压力不变,一段时间后卸压;当结晶釜内压力降至大气压后,打开结晶釜收集柚皮素/羟丙基-β-环糊精微胶囊;其中,步骤S1和步骤S2不存在先后顺序。优选地,所述有机溶剂为丙酮和乙醇的混合溶剂,二者按照体积比1:2混合;柚皮素与羟丙基-β-环糊精的质量比为1:4。优选地,样品溶液中柚皮素质量浓度为11-19g/L。优选地,步骤S2调节结晶釜内的温度至38-46℃,压力至8-14MPa。优选地,步骤S3中样品溶液通入结晶釜的体积流量为0.9-1.5mL/min。优选地,步骤S3中CO2的流速为3-6L/min。优选地,步骤S4中所述一段时间为20-40min。优选地,样品溶液中柚皮素质量浓度为13mg/mL;结晶釜内温度为42℃,压力为10MPa;样品溶液的体积流量为1.5mL/min;CO2的流速为4.5L/min;30min后卸压。优选地,样品溶液中柚皮素质量浓度为13mg/mL;结晶釜内温度为46℃,压力为12MPa;样品溶液的体积流量为1.5mL/min;CO2的流速为4.5L/min;30min后卸压。优选地,所述有机溶剂为乙醇;样品溶液中柚皮素质量浓度为13mg/mL,样品溶液中柚皮素与羟丙基-β-环糊精的质量比为1:4;结晶釜内温度为46℃,压力为12MPa;样品溶液的体积流量为1.5mL/min;CO2的流速为4.5L/min;30min后卸压。本发明的有益效果:本发明提供的方法利用超临界抗溶剂法将柚皮素包合于HP-β-CD中,极大地提高了柚皮素在水溶液中的溶解性能,溶出度显著提高,有利于提高柚皮素的生物利用度。附图说明图1为实验流程图;图2为结晶釜压力对柚皮素/HP-β-CD微胶囊载药量和回收率的影响关系曲线图;图3为结晶釜温度对柚皮素/HP-β-CD微胶囊载药量和回收率的影响关系曲线图;图4为样品溶液质量浓度对柚皮素/HP-β-CD微胶囊载药量和回收率的影响关系曲线图;图5为样品溶液体积流量对柚皮素/HP-β-CD微胶囊载药量和回收率的影响关系曲线图;图6为柚皮素/HP-β-CD微胶囊的DSC分析图;图7为柚皮素原料药和柚皮素/HP-β-CD微胶囊的体外溶出曲线;图中:1-CO2储罐;2-CO2泵;3-冷却装置;4-溶液储罐;5-高效液相泵;6-结晶釜;7-溶剂回收釜;8-流量计。具体实施方式下面结合附图和实施例具体介绍本发明的技术方案。实施例1:单因素法确定各关键参数的优选取值范围实验仪器和材料实验中所用到的主要仪器如表1所示,主要原辅料及试剂如表2所示。表1主要仪器设备名称型号生产厂家超临界微粒制备系统Helix美国AppliedSeparations公司Series1500高压输液泵Helix美国AppliedSeparations公司空气压缩泵TYW-2苏州市同一机电有限公司低温恒温槽SDC-6南京新辰生物科技有限公司紫外可见分光光度计UV-1800日本岛津公司智能溶出实验仪ZRS-8L天津天大天发科技有限公司分析天平BS124S北京赛多利斯仪器系统有限公司表2主要原辅料及试剂试剂名称规格生产厂家柚皮素98%陕西慧科植物发展有限公司丙酮分析纯南京化学试剂有限公司乙醇分析纯南京化学试剂有限公司HP-β-CD≥98%上海源叶智源生物科技有限公司CO2质量分数>99%南京上元工业气体厂蒸馏水-中国药科大学自制磷酸盐缓冲液pH6.8实验室配置实验装置及操作流程实验流程如图1所示,操作流程具体如下:(1)首先要对整个系统进行气密性检查,确保没有泄露。打开冷却装置和结晶釜壁上的加热器,待温度达到设定值后,打开二氧化碳进口阀门,二氧化碳通过冷却装置降温,由结晶釜顶进入到结晶釜内部。同时经过二氧化碳泵压缩,结晶釜内压力慢慢上升。(2)待结晶釜内的压力达到设定值并且稳定后,打开结晶釜底部二氧化碳的出口阀门,同时通过阀门控制二氧化碳的流速,使二氧化碳的流量稳定在设定值。(3)将配置好的溶液放入溶液储罐,然后溶液通过高效液相泵从结晶釜顶部通过喷嘴喷入结晶釜内部,含有溶剂的二氧化碳经过阀门降压进入到溶剂回收釜中,可以在溶剂回收釜中实现有机溶剂的回收,二氧化碳则经过流量计排放到大气中。(4)通过上述步骤把溶液全部进样完毕后,继续通入二氧化碳20-40分钟,排除残留溶剂。最后关闭二氧化碳钢瓶,排空结晶釜内的二氧化碳气体,打开结晶釜,取出产物。溶剂种类的选择考察柚皮素和HP-β-CD在不同溶剂中的溶解度大小,HP-β-CD易溶于水、甲醇、乙醇等溶剂,柚皮素在丙酮、乙醇、二氯甲烷中有较好的溶解度。通过初步筛选,尝试采用丙酮和乙醇混溶剂作为溶剂体系制备柚皮素/HP-β-CD微胶囊。溶剂的选择和实验结果如表3所示,在压力12MPa、温度38℃、样品溶液柚皮素质量浓度15g·L-1、柚皮素与HP-β-CD的质量比为1:4、样品溶液体积流量1.1mL·min-1、CO2排出体积流量4.5L·min-1的条件下进行实验。对结晶釜内所获得的产品的的载药量、回收率及形貌特征进行考察。由表3可知,丙酮与乙醇比为1:2时载药量和回收率均较高,综合考虑,选取丙酮和乙醇按体积比1:2混合为溶剂。回收率(%)和载药量(%)计算公式如下:回收率(%)=(微胶囊的总质量/总投料量)×100%;载药量(%)=(微胶囊中柚皮素的质量/微胶囊的总质量)×100%。表3溶剂种类对载药量、回收率及产品形貌的影响单因素实验:柚皮素与HP-β-CD质量比要满足SAS条件的要求,控制好SAS过程中各类参数如结晶压力,温度,溶剂的选择,溶液体积流量,药物载体比例等因素很重要。经过多次预实验发现,柚皮素与HP-β-CD质量比1:1、1:2、1:3、1:5、1:6时存在回收率低、产品易团聚等缺点,而当质量比1:4时载药量、回收率效果都比较好。最终确定柚皮素与HP-β-CD的质量比为1:4。单因素实验:结晶压力的影响以丙酮和乙醇体积比1:2混溶剂为溶剂系统,柚皮素与HP-β-CD的质量比为1:4,在结晶温度40℃、溶液体积流量1.1mL·min-1、柚皮素质量浓度15g·L-1、CO2排出体积流量4.5L·min-1的条件下,采用超临界CO2抗溶剂法制备柚皮素/HP-β-CD微胶囊。考察结晶压力分别为8、10、12、14、16MPa对柚皮素产物载药量和回收率的影响。结果如图2所示,载药量分别为29.63%、35.77%、35.24%、33.12%、25.33%,回收率分别为70.35%、76.57%、80.12%、69.18%、59.72%。随着结晶压力的增大,柚皮素/HP-β-CD微胶囊的载药量和回收率都呈现出先增大后减小趋势,如图2所示,回收率从70.35%先升至80.12%,后降至59.72%;载药量从29.63%先升至35.77%,后降至25.33%。确定结晶压力的优选范围为8-14MPa,并选择10、12、14MPa三个水平进行正交优化。单因素实验:结晶温度的影响以丙酮和乙醇体积比1:2混溶剂为溶剂系统,柚皮素与HP-β-CD的质量比为1:4,在结晶压力12MPa、溶液体积流量1.1mL·min-1、柚皮素质量浓度15g·L-1、CO2排出体积流量4.5L·min-1的条件下,采用超临界CO2抗溶剂法制备柚皮素/HP-β-CD微胶囊。考察结晶温度分别为38、40、42、44、46℃对柚皮素产物载药量和回收率的影响。结果如图3所示,载药量分别为28.81%、35.77%、33.47%、30.12%、29.03%,回收率分别为47.12%、76.57%、78.36%、73.18%、59.36%。随着结晶温度的升高,柚皮素/HP-β-CD微胶囊的回收率和载药量都呈现先增大后减小的趋势。如图3所示,回收率从47.12%先升至78.36%,后降至59.36%;载药量从28.81%先升至35.77%,后降至29.03%。确定结晶温度的优选范围为38-46℃,并选择40、42、44℃三个水平进行正交优化。单因素实验:柚皮素质量浓度的影响以丙酮和乙醇体积比1:2混溶剂为溶剂系统,柚皮素与HP-β-CD的质量比为1:4,在结晶压力12MPa、溶液体积流量1.1mL·min-1、结晶温度40℃、CO2排出体积流量4.5L·min-1的条件下,采用超临界CO2抗溶剂法制备柚皮素/HP-β-CD微胶囊。考察柚皮素质量浓度分别为11、13、15、27、19g·L-1对柚皮素产物载药量和回收率的影响。结果如图4所示。载药量分别为24.85%、29.41%、35.77%、34.53%、30.64%,回收率分别为43.41%、69.84%、76.57%、82.77%、71.56%。随着柚皮素质量浓度的增大,柚皮素/HP-β-CD微胶囊的载药量和回收率都先增大后减小。如图4所示,回收率从43.41%先升至82.77%,后降至71.56%;载药量从24.85%先升至35.77%,后降至30.64%。柚皮素质量浓度的优选范围为11-19g/L,并选择13、15、17g/L三个水平进行正交优化。单因素实验:溶液体积流量的影响以丙酮和乙醇体积比1:2混溶剂为溶剂系统,柚皮素与HP-β-CD的质量比为1:4,在结晶压力12MPa、柚皮素质量浓度15g·L-1、结晶温度40℃、CO2排出体积流量4.5L·min-1的条件下,采用超临界CO2抗溶剂法制备柚皮素/HP-β-CD微胶囊。考察溶液体积流量分别为0.7、0.9、1.1、1.3、1.5mL·min-1对柚皮素产物载药量和回收率的影响。结果如图5所示。载药量分别为21.13%、27.85%、35.77%、33.09%、26.67%,回收率分别为57.37%、66.06%、76.57%、78.69%、62.11%。随着溶液体积流量的增大,柚皮素/HP-β-CD微胶囊的载药量和回收率都先增大后减小。如图4所示,回收率从57.37%先升至78.69%,后降至62.11%;载药量从21.13%先升至35.77%,后降至26.67%。确定溶液体积流量的优选范围为0.9-1.5mL/min,并选择1.1、1.3、1.5mL/min三个水平进行正交优化。实施例2:正交优化最佳试验参数正交实验设计和结果以回收率为指标,设计正交实验考察结晶压力(A)、结晶温度(B)、溶液浓度(C)、溶液体积流量(D),表4为因素水平设计表,表5为正交实验设计与结果。表4因素水平表表5正交设计与结果试验号A/MPaB/℃C/g·L-1D/mL·min-1回收率/%1111175.432122268.163133365.584212384.765223183.246231278.237313272.388321358.259332179.34K169.72377.52370.63779.337K282.07769.88377.42072.923K369.99074.38373.73369.530R12.3547.6406.7839.807正交实验结果分析表5分析可知,各因素对柚皮素/HP-β-CD微胶囊回收率影响从小到大依次为A<D<B<C,结晶压力<溶液体积流量<结晶温度<溶液浓度。因此优选工艺组合为A1B2C1D3,即结晶压力10MPa,结晶温度42℃,溶液中柚皮素浓度13mg/mL,溶液体积流量1.5mL·min-1。优选工艺验证对优选工艺组合A1B2C1D3进行验证,即在结晶压力10MPa,结晶温度42℃,柚皮素质量浓度13g·L-1,溶液体积流量1.5mL·min-1的工艺条件下进行验证。三批验证试验的结果如表6,载药量和回收率平均值分别为37.11%和82.87%,RSD值分别为0.426%和0.461%(n=3),小于2%。表明SAS法制备柚皮素/HP-β-CD微胶囊的优选工艺稳定可行。表6工艺验证试验实施例3:柚皮素/HP-β-CD微胶囊的表征分析DSC分析柚皮素/HP-β-CD微胶囊的DSC分析如图6所示,由C可知柚皮素熔点在251.7℃。由A、B可知柚皮素在251.7℃左右的熔点峰消失,证明柚皮素成功包合在HP-β-CD中。溶解度实验取过量的柚皮素原料药及最优工艺下制备出的柚皮素/HP-β-CD微胶囊样品各3份,置于20mL具塞锥形瓶中,加入纯化水20mL。于37℃下恒温振荡48h,取上清液,用0.45μm的微孔滤膜过滤,将续滤液经适当稀释后于288nm波长处测定其吸光度值,将吸光度值代入标准曲线方程,计算得出纯化水中柚皮素的浓度,即相应样品在纯化水中的溶解度。表7溶解度测定物系温度(℃)压力(MPa)溶解度(μg/mL)原料药--8.13包合物4210314.74体外溶出度实验分别量取一定量的柚皮素原料药和最优工艺下制备出的柚皮素/HP-β-CD微胶囊,测定其溶出度,比较其溶解性能,结果如图7所示,分析得知柚皮素/HP-β-CD微胶囊的溶出性能在任意时刻都明显高于柚皮素原料药,证明药物释放速率得到明显改善。结果讨论(1)实验证明通过SAS法能够成功制备柚皮素/HP-β-CD微胶囊,通过将柚皮素包合于HP-β-CD中的方法使柚皮素在纯化水中的溶解度由8.13μg/ml提高到314.74μg/ml,极大的提高了柚皮素的溶解性能,为减小药物服用剂量提供新的方法;(2)通过观察DSC图谱,证明柚皮素被成功包合在HP-β-CD中;(3)体外释放结果表明,相对于原料药,柚皮素/HP-β-CD微胶囊的溶出性能有了明显提高,具体表现为,经过4h的溶出度检测,柚皮素/HP-β-CD微胶囊溶出度可达到近80%,而原料药溶出度不足20%。柚皮素/HP-β-CD微胶囊溶出性能有了极大的提高。实施例4应用超临界抗溶剂法制备柚皮素/环糊精微胶囊的方法,包括如下步骤:步骤S1,将柚皮素和羟丙基-β-环糊精溶解于有机溶剂中,得到样品溶液;步骤S2,将CO2通入结晶釜中,调节结晶釜内的温度和压力;步骤S3,继续以一定流速通入CO2,维持结晶釜内的温度和压力不变,同时将步骤S1制备的样品溶液通入结晶釜中;步骤S4,样品溶液通入完毕后,持续通入CO2,维持结晶釜内的温度和压力不变,一段时间后卸压;当结晶釜内压力降至大气压后,打开结晶釜收集柚皮素/羟丙基-β-环糊精微胶囊;其中,步骤S1和步骤S2不存在先后顺序,所述有机溶剂为丙酮和乙醇的混合溶剂,二者按照体积比1:2混合;柚皮素与羟丙基-β-环糊精的质量比为1:4。样品溶液中柚皮素质量浓度为13mg/mL;结晶釜内温度为46℃,压力为12MPa;样品溶液的体积流量为1.5mL/min;CO2流速为4.5L/min;30min后卸压。该实施例制备的柚皮素/羟丙基-β-环糊精微胶囊的回收率为81.75%,载药量为48.55%,溶出度结果与上述优选工艺制备的柚皮素/羟丙基-β-微胶囊基本一致,四小时累计溶出度为85%。该实施例中,回收率比上述正交优化的最优方案略低,但载药量明显提高,不同于单因素实验中压力和温度变化对载药量的影响趋势。该实施例中,有机溶剂也可使用乙醇。对比实施例常规溶剂沉淀法制备柚皮素/羟丙基-β-环糊精微胶囊:称取HP-β-CD溶于水中,加热溶解制成HP-β-CD饱和水溶液,备用。称取柚皮素原料药,加入适量体积分数70%乙醇,置恒温磁力搅拌中,加入HP-β-CD饱和水溶液,磁力加热搅拌一定时间,静置,放入冰箱中冷藏24h,真空抽滤,用无水乙醇洗涤滤饼,干燥即得载药量为30.65%的柚皮素/羟丙基-β-环糊精微胶囊。分别测定实施例2优选工艺、实施例4和对比实施例制备的柚皮素/羟丙基-β-环糊精微胶囊的溶出性能对于高温(40℃)和光照(4500LX)的稳定性。高温和光照处理方法为:精密称取200mg的柚皮素/羟丙基-β-环糊精微胶囊,开口置于称量瓶中,称量瓶置于光照箱中,保持温度为40℃和光照强度4500LX放置10天,10天后取样测定溶出度,计算10天后4小时累计溶出度(溶出介质为纯水)比高温光照处理前溶出度的降低百分比。结果:实施例2优选工艺降低百分比为4.5%,实施例4降低百分比小于2%,对比实施例降低百分比为37.8%。上述实施例用于说明本发明的实质性内容,但并不以此限定本发明保护范围。任何对本发明技术方案的简单修改或者等同替换都不脱离本发明保护范围。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1