手工缝制带瓣外管道及其U形单元使用的模具的制作方法
本实用新型涉及技术领域,特别是涉及手工缝制带瓣外管道。
背景技术:
膨体聚四氟乙烯(ePTFE)是一种采用特殊工艺制成的多孔的理化性质极其稳定的医用高分子材料,具有极端惰性的表面和高度的化学稳定性【1】,0.1mm的ePTFE薄片非常纤薄,柔软度和活动度好,这些都为0.1mm ePTFE薄片成为新型的人造瓣膜材料提供可能。
1993年,Yamagishi【2】首次应用0.1mm聚四氟乙烯(PTFE)薄片制成肺动脉单瓣,应用于法洛四联症的右室流出道,取得了很好的抗返流效果,随后Turrentine MW【3】和Brown JW【4】相继报道0.1mmPTFE单瓣活动度好,随访未发现血栓和钙化。2008年,Nunn GR【5】介绍了PTFE双瓣抗返流的耐久性较单瓣更好,同样在随访中未见到瓣叶的钙化和增厚。近年来,日本学者应用0.1mmPTFE制作成三瓣缝合于Dacron或者Gore-tex人造血管形成新型的带瓣管道,用于重建右室流出道,取得了良好的效果。Ando M【6】于2009年报道了139例患者应用该带瓣管道后,10年随访外管道免于置换率为88.0%±6.8%,70%患者仍维持轻度或轻度以下的肺动脉返流。2011年MiyazakiT【7】带来了更为振奋人心的结果,经过多中心794例的大样本分析,其中包括PTFE瓣膜的外管道和带PTFE单瓣、双瓣补片的应用,10年再手术率非常低,外管道仅为4.6%,补片为7.7%。
根据右心系统的血流动力学特点,带瓣外管道的内置瓣膜多为生物瓣膜。来源主要有同种异体主动脉瓣或者肺动脉瓣,牛颈静脉瓣,牛心包或者猪心包的制备等。Homograft和Contegra是目前临床上最为常用的带瓣外管道,用于心脏外科手术中右心室流出道的重建。尽管带瓣外管道在临床上取得了确切的抗返流的效果,但是钙化【8】、纤维化、感染性心内膜炎【9,10】所导致的高衰败率是其无法回避的缺陷【11】。2005年,Brown JW【12】报道了117应用homograft,5年和15年的衰败率为40%,57%,而在婴儿期衰败率更高,分别为75%,84%。Oosterhof T等【13】于2006年报道158例采用homograft治疗法洛四联症患者,术后10年管道衰败率高达53%。报道了38例5岁以内的患儿接受contegra重建右室流出道,随访18个月,13.2%因为梗阻而再次手术更换了外管道。
Karamlou T【15】报道了北美17家心脏中心241例接受带瓣外管道手术并存活的患者,随访后发现因带瓣外管道病变再干预率为1年25%,3年58%。2011年Lee C【16】10年随访了181例生物瓣置换肺动脉瓣的患者,80%出现了明显的衰败,需要再次手术。
O'Keefe KL【17】指出免疫介导的炎性反应是导致生物瓣膜衰败的主要原因。2000年Grabenwoger M【18】就发现在衰败的生物瓣膜中存在大量的炎性细胞浸润,而应用自身心包制作的瓣膜没有这种现象,推测免疫反应可能是瓣膜衰败的根本原因之一。PompilioG【19】通过6年随访主动脉瓣homograft的移植后情况,发现31.5%出现瓣膜功能不全,21%需要再手术,73.6%的患者中存在HLA抗体;Wojtalik【20】发现应用contegra后B细胞量,T细胞介导的CD69和CD71明显上升。Park CS【21】在应用猪心包瓣膜的患者中检测到了a-半乳糖基(a-Gal)特异性抗体,而a-Gal抗原存在于猪心包瓣膜中,并且在衰败的瓣膜中发现了单核细胞和巨噬细胞的浸润。此后,大量的动物实验均证实了这种观点。
因此,多数学者尝试去除或者改变生物瓣膜中的抗原,降低免疫反应【22】。目前主要的方法有姨蛋白酶法、去拒剂法、酶联合去拒剂法等,但是其效果仍不确切。Cicha I【23】报道应用去细胞化瓣膜早期就出现了瓣膜的炎性反应和纤维化,引起了严重的梗阻性病变。究其原因,Cissell DD【24】认为主要有两个,一是上述方法并不能去除所有的抗原,残留的抗原仍可引起免疫反应,另一方面去细胞化也可以破坏瓣膜结构,反而加速了瓣膜的衰败。虽然近年来应用人骨髓或者脐带血来培养内皮细胞并种植在去细胞化的瓣膜上试图解决上述问题【25】,但仅仅停留于动物实验阶段,仍面临诸多不确定性。
因此,生物瓣膜的“天生缺陷”导致了带瓣外管道衰败的必然性,限制了其应用的前景【26】,特别是在小儿心脏病中的应用,因为生物瓣膜的衰败与年龄密切相关【27】。Siddiqui RF【26】发现在儿童和青少年患者中,生物瓣膜在早期就可以出现衰败,相比于大年龄组和老年组衰败率最高。Chen PC【27】分析了波士顿儿童医院227例法洛四联症患者,在接受生物瓣膜置换术后2~10年后,瓣膜的衰败率为25%,而低年龄是瓣膜衰败的独立的危险因素,这与带瓣外管道衰败因素是一致的。目前尚不清楚其原因,儿童的免疫反应的高敏感性被认为是可能的因素之一【20】。而且对于儿童而言,带瓣外管道的高衰败率就意味着需要反复多次手术,大大增加了患儿的痛苦,也增加了整个家庭的经济负担。
技术实现要素:
为了克服上述现有技术的不足,本实用新型提供了0.1mmPTFE手工缝制带瓣外管道,其是一种新型的带瓣外管道,重建右心室流出道,用于治疗小儿复杂先天性心脏畸形和术后肺动脉返流等并发症。通过体外流体学测试,动物实验和临床应用,0.1mmPTFE手工缝制带瓣外管道体现出了稳定性高,持久性强,抗返流效果好的特点。不仅解决了国内带瓣外管道缺乏的困境,而且提供了一种性能更优越,衰败率低的带瓣外管道。
本实用新型所采用的技术方案是:手工缝制带瓣外管道,包括外管体和PTFE瓣;
PTFE瓣由三个U形单元组成,每一个U形单元包括膜瓣部分和连接部分,每一个U形单元边缘缝制在外管体的内壁上;
每一个U形单元的膜瓣部分朝向外管体的中心轴方向延伸,并且若干个膜瓣部分的边缘部分相互自由搭接;
在整个PTFE瓣的从左往右5-0prolene线处以及从右往左的5-0prolene线处,设有“U”形单元与外管体等分点缝合预固定线。
进一步地,PTFE瓣的三个个U形单元相互连接成为一个整体,直接缝制在外管道内面而成。
进一步地,PTFE瓣的每一个连接部分呈U型结构。
进一步地,PTFE瓣设有三个U形片单元,其交界与外管道内面的三等分线缝合。
制作带瓣外管道的瓣膜制作模具,包括由硬质卡板本体,以及与不同外管道尺寸大小相对应的连续U形单元镂槽,硬质卡板本体上,位于每一组所述U形单元镂槽左、右两端位置处还分别设有一个定位孔。
进一步地,硬质卡板本体由透明材料制成。
与现有技术相比,本实用新型的有益效果是:0.1mmPTFE手工缝制带瓣外管道是一种新型的带瓣外管道,重建右心室流出道,用于治疗小儿复杂先天性心脏畸形和术后肺动脉返流等并发症。通过体外流体学测试,动物实验和临床应用,0.1mmPTFE手工缝制带瓣外管道体现出了稳定性高,持久性强,抗返流效果好的特点。不仅解决了国内带瓣外管道缺乏的困境,而且提供了一种性能更优越,衰败率低的带瓣外管道。
附图说明
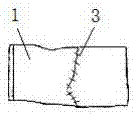
图1为0.1mmPTFE手工缝制带瓣外管道的一个实施例的主视图;
图2为图1的实施例的左视图;
图3为图1的实施例的缝制步骤结构示意图;
图4为制作带瓣外管道的瓣膜制作模具的一个实施例的结构示意图;
其中:1-外管体,2-PTFE瓣,21-“U”形单元,211-膜瓣部分,212-连接部份;3-斜线,4-PTFE瓣的从左往右5-0prolene线处,5-PTFE瓣的从右往左5-0prolene线处,6-等分点缝合预固定线,7-三等分线,8-硬质卡板本体,9-U形单元镂槽,10-定位孔。
具体实施方式
为了加深对本实用新型的理解,下面结合附图和实施例对本实用新型进一步说明,该实施例仅用于解释本实用新型,并不对本实用新型的保护范围构成限定。
如图1所示,0.1mmPTFE手工缝制带瓣外管道,包括外管体1和PTFE瓣2;PTFE瓣由三个连续相连的U形单元21组成,每一个U形单元21包括膜瓣部分211和连接部分212,每一个“U”形单元21边缘缝制在外管体1的内壁上;如图3的工序步骤F和步骤G状态所示,每一个U形单元21的膜瓣部分211朝向外管体1的中心轴方向延伸,并且若干个膜瓣部分211的边缘部分相互自由搭接;在整个PTFE瓣2的从左往右5-0prolene线处4以及从右往左的5-0prolene线处5,设有“U”形单元21与外管体1等分点缝合预固定线6。
如图3所述,为缝制0.1mmPTFE带瓣外管道的工艺步骤图,依次包括外管体材料准备工艺A,翻转外管体工艺步骤B,外管体三等分线工艺步骤C,PTFE瓣材料准备以及采用瓣膜制作模具根据所需要外管道尺寸描画出相应的U形单元,裁剪形成所需U形单元工艺步骤D,U形单元连接部分与外管体内表面三等分线间断缝合固定工艺步骤E,将U形单元缝制在外管体的内表面形成PTFE瓣工艺F以及最后回复外管体后的外观工艺G。其中工艺D所示,通过瓣膜制作模具描绘从而裁剪而成的PTFE瓣,由三个U形单元21相互连接成为一个整体,便于固定于外管体内面,直接将U形单元边缘连续缝合于外管体内面形成PTFE瓣膜。从该工序状态图所示,PTFE瓣2的每一个连接部分212呈U型结构。
在上述实施例中,PTFE瓣2设有三个U形单元21。
如图4所示,采用瓣膜制作模具可以根据不同外管道尺寸大小来裁剪相对应的U形单元,瓣膜制作模具包括由硬质卡板本体8,以及与不同外管道尺寸大小相对应的连续U形单元镂槽,9,硬质卡板本体8上,位于每一组U形单元样槽9左、右两端位置处还分别设有一个定位孔10。使用瓣膜制作模具压在PTFE瓣膜材料表面,定位孔10处固定,根据所需要的外管道大小选择相对应的U形镂槽9并描绘,然后直接剪裁即可,瓣膜制作模具的使用,不仅方便,节省制作时间,而且更加规范了U型单元的形状,使得其在不同外管道制作过程中尺寸更加精确,保证带瓣外管道瓣膜的抗返流性。
在上述实施例中,硬质卡板本体8上设有不同外管道尺寸大小相对应的连续U形单元镂槽9,可以节省样板的制作,使用方便。硬质卡板本体8由透明材料制成,具有更好的使用效果,保证操作人员在剪裁时可以充分观察材料的平整度。
本实用新型的手工缝制带瓣外管道在进行缝制时,外管道内面翻至管道外后,分别标记外管道周径三等分线,5-0prolene线将U形单元的连接部分与对应的等分线先行缝合固定,这样有利于各个瓣叶大小的一致性,保持瓣缘在同一水平,不易造成瓣叶的扭曲。该结构的设计以及该缝制方法的使用统一了缝制步骤,采用最合适的制作尺寸,应用模板化规范并大大简化了制作流程。新型带瓣外管道的耐久性可以避免多次手术更换失功的外管道,新型支架带瓣外管道可以避免开胸手术,减轻手术创伤,大大减轻患儿家庭的经济负担,具有很高的经济效益。
本实用新型的实施例公布的是较佳的实施例,但并不局限于此,本领域的普通技术人员,极易根据上述实施例,领会本实用新型的精神,并做出不同的引申和变化,但只要不脱离本实用新型的精神,都在本实用新型的保护范围内。
参考文献
1.Ito T,MaekawaA,YamanaK,et al.Use of an Expanded Polytetrafluoroethylene Patch as an Artificial Leaflet in Mitral Valve Plasty:An Early Experience.The Annals of Thoracic Surgery.2010;89(5):1620-1624.
2.Yamagishi M,Kurosawa H.Outflow reconstruction of tetralogy ofFallot using a Gore-Tex valve.Ann Thorac Surg.1993;56:1414-7.
3.TurrentineMW,Rodefeld MD,Brown JW.PolytetrafluoroethyleneMonocusp Valve Reconstruction of the Right Ventricular Outflow Tract.Ann ThoracSurg.2002;73(3):871-9.
4.Brown JW,Ruzmetov M,Vijay P,et al.Right ventricular outflow tract reconstruction with apolytetrafluoroethylenemonocusp valve:A twelve-yearexperience.J ThoracCardiovasc Surg.2007;133:1336-43.
5.NunnGR,MBBS,BennettsJ,et al.Durability of hand-sewn valves in the right ventricularoutlet.J ThoracCardiovasc Surg.2008;136:290-7.
6.Ando M,TakahashiY.Ten-year experience with handmade trileafletpolytetrafluoroethylenevalved conduit used for pulmonary reconstruction.J ThoracCardiovasc Surg.2009;137:124-31.
7.Miyazaki T,YamagishiM,Maeda Y,et al.Expanded polytetrafluoroethylene conduits and patches with bulgingsinuses and fan-shaped valves in right ventricular outflow tractreconstruction:Multicenter study in Japan.J ThoracCardiovasc Surg.2011;142:1122-9.
8.IyerA,Malik P,Malik R,et al.Early Postoperative BioprostheticValveCalcification.Heart,Lung and Circulation.2013;22:873–874.
9.Cheung G,VejlstrupN,IhlemannN,et al.Infective endocarditis following percutaneous pulmonary valvereplacement:Diagnostic challenges and application ofintra-cardiac echocardiography.International Journal of Cardiology.2013;169:425–429.
10.Malekzadeh-MilaniS,LadouceurM,IserinL,et al.Incidence and outcomes of right-sided endocarditis in patients with congenital heart disease after surgical or transcatheter pulmonary valve implantation.The Journal of Thoracic and Cardiovascular Surgery.2014;148(5):2253-2259.
11.Nair V,Law KB,Li AY,et al.Characterizing the inflammatory reaction in explanted Medtronic Freestylestentless porcine aortic bioprosthesis over a 6-year period.Cardiovascular Pathology.2012;21:158–168.
12.Brown JW,Ruzmetov M,Rodefeld MD,et al.Right Ventricular Outflow Tract ReconstructionWith an Allograft Conduit in Non-Ross Patients:Risk Factors for Allograft Dysfunction and Failu re.AnnThorac Surg.2005;80:655–64.
13.Oosterhof T,Meijboom FJ,Vliegen HW,et al.Long-term follow-up of homograftfunction after pulmonary valve replacement in patients with tetralogy ofFallot.Eur Heart J.2006;27(12):1478-1484.
14.V,Berdat P,Pavlovic M,et al.Adverse Mid-Term Outcome Following RVOTReconstruction Using the ContegraValvedBovineJugular Vein.Ann Thorac Surg.2005;79:625–31.
15.Karamlou T,Blackstone EH,Hawkins JA,et al.Can pulmonary conduit dysfunction and failure bereduced in infants and children less than age 2years at initial implantation?.J ThoracCardiovascSurg.2006;132:829-38.
16.Lee C,Park CS,Lee CH,et al.Durability of bioprosthetic valves in the pulmonary position:Long-term follow-up of 181 implants in patients with congenitalheart disease.J ThoracCardiovasc Surg.2011;142:351-8.
17.O'Keefe KL,CohleSD,McNamara JE,et al.Early Catastrophic Stentless Valve Failure Secondary to Possible Immune Reaction.The Annals of Thoracic Surgery.2011;91(4):1269-1272.
18.Grabenwoger M,Fitzal F,Gross C,et al.Different modes ofdegeneration in autologous and heterologous heart valve prostheses.J Heart Valve Dis.2000;9:104-9[discussion 110-1].
19.Pompilio G,Polvani G,Piccolo G,et al.Six-year monitoring of the donor-specific immune response to cryopreserved aortic allograft valves:implications with valve dysfunction.Ann Thorac Surg.2004 Aug;78(2):557-63.
20.Wojtalik M,Mrowczynski W,Zeromski J,etal.Doescontegraxenograft implantation evoke cellular immunityin children?Interactive CardiovascThorac Surg.2003;2:273–8.
21.Park CS,Park SS,Choi SY,et al.Anti alpha-gal immune responsefollowingporcinebioprosthesis implantation in children.J HeartValve Dis.2010;19:124-30.
22.Lisy M,Pennecke J,Brockbank K,et al.The performance of ice-free cryopreserved heart valve allografts in an orthotopicpulmonary sheep model.Biomaterials.2010;31:5306-5311.
23.Cicha I,Rüffer A,Cesnjevar R,et al.Early obstruction of decellularizedxenogenic valves in pediatric patients:involvement of inflammatory and fibroproliferative processes.Cardiovascular Pathology.2011;20:222-231.
24.Cissell DD,Hu JC,Griffiths LG,et al.Antigen removal for the production of biomechanically functional,xenogeneic tissue grafts.Journal ofBiomechanics.2014;47:1987-1996.
25.Apte SS,Paul A,Prakash S,et al.Current developments in the tissue engineering of autologous heart valves:moving towards clinical use.Future Cardiol.2011;7(1):77-97.
26.Siddiqui RF,Abraham JR,Butany J.Bioprosthetic heart valves:modesof failure.Histopathology.2009;55:135-44.
27.Chen PC,Sager MS,Zurakowski D,et al.You nger age and valve oversizing are predictors of structural valve deterioration after pulmonary valve replacement in patients with tetralogy of Fallot.The Journal of Thoracic and Cardiovascular Surgery.2012;143(2):352-360.
- 还没有人留言评论。精彩留言会获得点赞!