一种能提供药物脉冲后缓慢控释的纳米纤维及制备方法与流程
技术领域
本发明属于材料学领域,涉及一种药物缓控释纳米材料,具体来说是一种能提供药物脉冲后缓慢控释的纳米纤维及制备方法。
背景技术:
高压静电纺丝技术(电纺)是一种自上而下(top-down)的纳米制造技术,通过外加电场力克服喷头尖端液滴的液体表面张力和粘弹力而形成射流,在静电斥力、库仑力和表面张力共同作用下,液体射流被高频弯曲、拉延、分裂,在几十毫秒内被牵伸千万倍,经溶剂挥发或熔体冷却在接收端得到纳米级纤维。该技术工艺过程简单、操控方便、选择材料范围广泛、可控性强,被认为是最有可能实现连续纳米纤维工业化生产的一种方法,应用该技术制备功能纳米纤维具有良好的前景。
电纺聚合物功能纳米纤维一般以成纤聚合物为基材,通过加入活性成分而赋予纳米纤维功能,并充分利用电纺纳米纤维膜的独特性能而充分发挥活性成分的效用。这些独特的性能包括纤维直径小、纤维表面积巨大、纤维呈三维网状多孔结构、孔隙率高、纤维具有纳米尺度范围的直径却同时具有宏观范围的长度等。在生物医药领域,一般将药物加入聚合物溶液,形成共溶溶液作为纺丝液,通过普通电纺过程的快速干燥和成型,获得药物均匀分布在整个纳米纤维的载药纳米纤维。绝大部分载药纳米纤维都是该类药物均匀分布的、结构单一的纳米纤维,通过聚合物基材的理化性能和纳米纤维膜的特点而获得所需要的药物缓控释性能。
随着电纺技术的发展,人们逐渐认识到在所有的“top-down”纳米制造技术中,电纺技术最优势特点是可以通过宏观层次纺丝头结构的设计,单步有效地制备具有相应微观结构特征的纳米纤维,如通过内外两层套管结构的纺丝头制备并列结构纳米纤维(DG Yu,LM Zhu,C Branford-White,JH Yang,X Wang, Y Li, W Qian. Solid dispersions in the form of electrospun core-sheath nanofibers. International Journal of Nanomedicine, 2011, 6: 3271-3280.)、通过并排两根毛细管为纺丝头制备并列结构纳米纤维(Jalani G, Jung CW, Lee JS, Lim DW.Fabrication and characterization of anisotropic nanofiber scaffolds for advanced drug delivery systems. International journal of nanomedicine,2014, 9(Suppl 1), 33.)。目前虽有少量通过并列电纺和并列电纺调控药物在纳米纤维中的分布,以获得所需药物控释性能的电纺并列纳米纤维和乔纳斯纳米纤维,但是还没有发现应用并列纳米纤维的结构特点和成分调控以获得药物以脉冲后缓慢控释的相关应用报道。
技术实现要素:
本发明提供了一种能提供药物脉冲后缓慢控释的纳米纤维及制备方法,所述的这种能提供药物脉冲后缓慢控释的纳米纤维及制备方法要解决现有技术中的纳米纤维控制缓释药物的效果不佳的技术问题。
本发明提供了一种能提供药物脉冲后缓慢控释的纳米纤维,包括一个主纤维束,所述的主纤维束的外侧设置有一个并列纤维束,所述的主纤维束和所述的并列纤维束在长度方向上延伸,在径向截面上,所述的并列纤维束覆盖所述的主纤维束的外周40~70%,所述的主纤维束由药物和不溶于水的聚合物药用辅料构成,在主纤维束中,所述的药物和不溶于水的聚合物药用辅料的质量比为1:6~9;所述的并列纤维束由药物和易溶于水的药用辅料组成,在所述的并列纤维束中,所述的药物和易溶于水的药用辅料的质量比为1:10~15。
进一步的,所述的药物为小分子化学合成药物或者中药活性成分。
进一步的,所述的药物为布洛芬。
进一步的,所述的易溶于水的药用辅料为聚乙烯吡咯烷酮K60;所述的不溶于水的聚合物药用辅料为乙基纤维素。
本发明还提供了上述的一种能提供药物脉冲后缓慢控释的纳米纤维的制备方法,其特征在于包括如下步骤:
1)采用第一有机溶剂,将药物和不溶于水的聚合物药用辅料调配成共溶溶液,作为主纤维束一边的工作流体;
2)采用第二有机溶剂,将药物和易溶于水的药用辅料调配成共溶溶液,作为并列纤维束一边的工作流体;
3)将主纤维束一边的工作流体装入一个第一注射器中,所述的第一注射器安装在一个第一注射泵中;
4)将并列纤维束一边的工作流体装入一个第二注射器中,所述的第二注射器安装在一个第二注射泵中;
5)所述的第一注射器和所述的第二注射器分别和一个并列纺丝头的两个入口连接;
6)采用一个高压发生器,所述的高压发生器和所述的并列纺丝头连接;
7)通过两台注射泵分别控制两种溶液注入并列纺丝头的速率,开启高压发生器,在高压静电的作用下,以并列纺丝头出口为模板,通过接地纤维接收平板收集纳米纤维;制备出能提供药物脉冲后缓慢控释的纳米纤维。
进一步的,所述的第一有机溶剂和所述的第二有机溶剂均为无水乙醇。
本发明的这种提供药物以脉冲后缓慢控释模式释放的并列电纺纳米纤维具有并列结构特征,通过纳米纤维的双边采用不同溶解性能的聚合物基材,在结构的支撑下,能够调控所载的药物通过脉冲后缓慢控释的方式释放。纤维的一边药用辅料是易溶于水的,在接触到溶出液后,能够快速脉冲释放出其中所含的部分药物;纤维另外一边的聚合物是不溶于水的,将所装载的另一部分药物通过扩散机制缓慢释放,从而实现药物的两相控释模式。
本发明和已有技术相比,其技术进步是显著的。本发明的并列电纺纳米纤维通过并列电纺工艺制备,药物在初期脉冲快速释放后,药物随即开始第二相的持续缓慢释放。通过将纳米纤维膜剪切成薄片,可以直接开发出药物的经口给药系统,提供安全有效的药物控释方式。而且,本发明的制备工艺简单,单步有效、制备的纳米纤维并列结构清晰、而且纳米直径小、线性好、直径分布均匀、纤维表面光滑。本发明的并列结构纳米纤维的思路能够为众多药物的脉冲后缓慢控释模式提供实施方法。
附图说明
图1为本发明的药物脉冲后缓慢控释纳米纤维的并列电纺制备过程泰勒锥拍摄图。
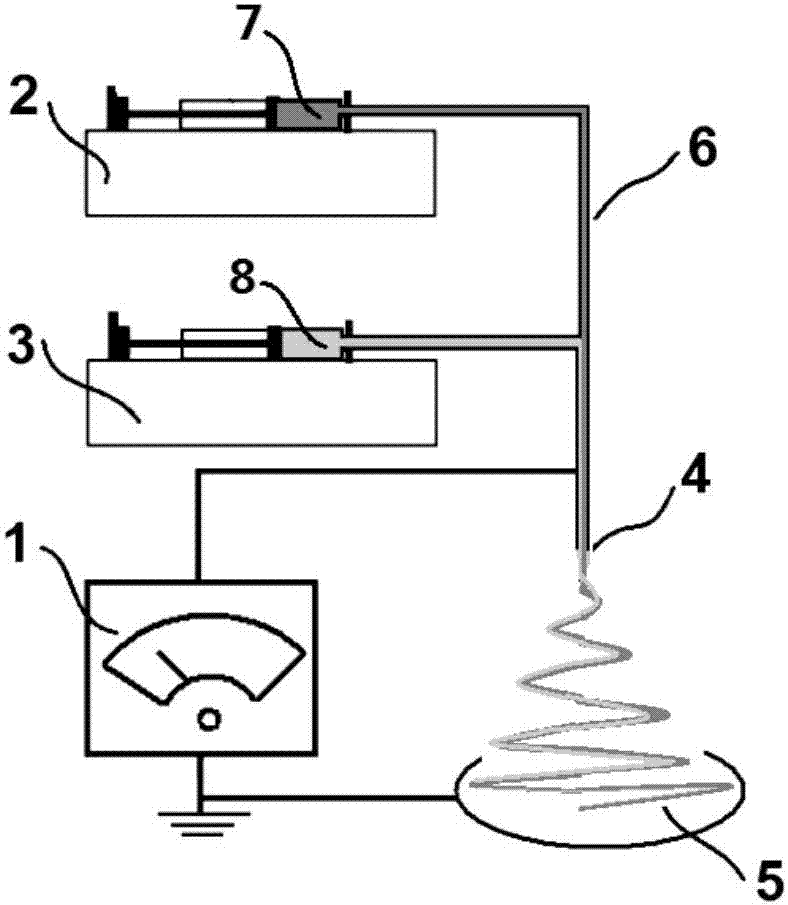
图2 为本发明所采用的并列电纺装置示意图。
图3为本发明的药物脉冲后缓慢控释纳米纤维的扫描电子显微镜图。
图4为本发明的药物脉冲后缓慢控释纳米纤维的透射电子显微镜图。
图5为本发明的药物脉冲后缓慢控释纳米纤维的内部结构示意图。
图6为本发明的药物脉冲后缓慢控释纳米纤维的药物体外两相控释图。
具体实施方式
以下结合附图和实施例对本发明进行详细说明。这些实施例仅用于解释本发明而不是用于限制本发明。凡采用与本发明相同或相似的方法,或做出的等价修改,均应落入本发明保护范围。
实施例1:电纺工艺实施和并列纳米纤维的制备
将2克药物对乙酰基氨基酚和7克聚乙烯吡咯烷酮K60共溶于100 ml 的无水乙醇中,配制并列纤维束一边工作流体。
将4克药物对乙酰基氨基酚和20克成纤聚合物乙基纤维素共溶于100 ml 无水乙醇,配制成主纤维束一边的工作流体。
将上述两种工作流体分别装入相应的注射器7、8中,安装到各自注射泵2、3上,并连接到并列纺丝头4的两个入口中,接通高压纺丝头4和高压发生器1。
通过两台注射泵2、3分别控制并列溶液注入并列纺丝头4的速率,并列流速均为1.0 mL/h,纤维接收板5离并列喷丝口距离为15 cm , 环境温度为 (22±1) ℃,环境湿度为58±5%。在上述工况下,开启高压发生器1,电压15 kV,对电纺过程进行原位放大拍摄,结果如图1所示,从并列纺丝头4出来两股流体形成一个复合并列泰勒锥体,锥体的顶端发出一个直线射流,开始高压静电纺丝的不稳定拉伸过程。
本发明采用的一种并列电纺装置如图2所示,包括高压发生器1;第一注射泵2、第二注射泵3、并列纺丝头4、纤维接收板5、硅胶软管6、第一注射器7、第二注射器8组成,所述的第一注射器7安装在第一注射泵2中,所述第一注射器7通过所述的硅胶软管6和所述的并列纺丝头4的一个入口连接,所述的第二注射器8安装在第二注射泵3中,所述第二注射器8和所述的并列纺丝头4的另外一个入口连接,所述的高压发生器1和所述的并列纺丝头4连接,所述的并列纺丝头4下端设置有一个纤维接收板5。
上述的高压发生器1;第一注射泵2、第二注射泵3、并列纺丝头4、纤维接收板5、硅胶软管6、第一注射器7、第二注射器8都可以通过市场购买获得。
实施例2:药物脉冲后缓慢控释纳米纤维的结构和形貌表征
采用场发射扫描电镜(FESEM)对实施例1所制备纤维进行表面喷金后观察,结果如图3所示。所制备的纤维呈现良好的线性状态、没有串珠结构发生、纤维表面光滑、纤维堆积均匀。直径为 720 ± 150 nm,分布比较均匀,直径分布比较集中。
采用高分辨透射电子显微镜(TEM)对所制备纤维内部结构进行观察,结果如图4所示,纳米纤维的双边并列结构特征清晰。纤维的内部结构如图5所示,药物33均匀地分布在乔纳斯纳米纤维的两边。其中由乙基纤维素和药物33组成的一边11能提供缓释效果,而由聚乙烯吡咯烷酮和药物33组成的另一边22能提供脉冲快释效果。
实施例3:药物脉冲后缓慢控释纳米纤维的药物控释功能分析
按中国药典2015版附录ⅩD释放度测定第二法浆法,采用RCZ-8A智能溶出实验仪进行对上述所得的载药纳米纤维进行体外溶出试验。控制转速50rpm,温度为37±0.1℃,溶出介质为900 mLpH7.0磷酸盐缓冲溶液,考察纳米纤维的药物体外控释性能。按预定时间取样5mL,0.22 µm微孔滤膜过滤,得到溶出液样品,并立刻补充同体积等温新鲜介质。对样品适当稀释后,在 λ= 258 nm处,采用紫外可见分光光度计进行紫外测定,计算药物对乙酰基氨基酚的溶出量和累积溶出百分比,重复6次。结果如图4所示,从图中可以看出,药物呈现明显的两相控释效果。由于一边的聚乙烯吡咯烷酮的聚合物基材易溶于水,在纳米纤维接触溶出液后,马上脉冲释放出所载的全部药物。在随后的进程中,PVP一边消失,由于另一边聚合物乙基纤维素不溶于水,所以能够控制药物通过扩散机制缓慢释放。这种药物脉冲后缓慢控释的模式一方面能够通过药物初期的快速释放获得快速的治疗效果, 另一方面,通过药物随后的持续缓慢释放,避免病人的频繁给药所带来的不便,提高病人的耐受性,增加病人的用药方便性。
实施例4:中药活性成分白姜黄素的脉冲后持续缓慢释放的并列电纺纳米纤维
按照实施例子1的纺丝液调配方法和实施工艺条件,制备姜黄素的脉冲后缓慢释放纳米纤维,按照实施例3进行药物体外溶出实验,检测纤维对药物的控释性能,结果表明,药物姜黄素的体外释放具有明显的脉冲后持续缓慢控释特点。
- 还没有人留言评论。精彩留言会获得点赞!