一种亲水空心硅球及其制备方法和应用与流程
本发明涉及药物缓释系统的构建,具体涉及一种亲水空心硅球及其制备方法和其作为药物缓释载体方面的应用。
背景技术:
国内外目前研究较多的药物缓释载体是高分子药物缓释载体。其分为合成高分子(聚乳酸、聚己内酯、聚丙烯酸酯等)和天然高分子(明胶、纤维素、壳聚糖等)。合成高分子载体常常生物相容性不好,有时还含有痕量引发剂等毒性杂质,在应用上受到一定的限制。例如在聚乳酸的一般生产方法中使用了有机锡催化剂,会产生细胞毒性。现有的天然高分子载体也存在自身的缺陷。明胶作为药物持续释放的有效载体其主要适用于亲水性药物,很多时候为了满足溶胶凝胶转换的敏感性,需要对分子的结构进行复杂的设计。壳聚糖作为天然高分子缓释载体在医药领域的应用越来越受到关注,它无毒、生物相容性好、可生物降解但其血液相容性较差,作为生物材料在体内使用时容易引起血栓,限制了其在生物医学工程特别是与血液相关领域的应用。壳聚糖载药微球是目前报道较多的药物缓释载体,但其作为靶向载体在临床上应用的报道较少,这主要是传统方法制备出来的壳聚糖载药微球本身存在的一些缺陷限制了其应用,主要表现在:制备的微球粒径大部分分散性较差;微球载药稳定性差,药物缓控释效果不理想;载药微球存在被动靶向等缺陷。综上所述,药物载体缓释系统的靶向性缓释性能及生物兼容性是药物缓释技术的关键,目前文献报道的药物缓释系统存在靶向性较差、构建方法复杂、缓释效率低等问题。
近几年,经深入研究,人们发现纳米给药系统及其使用材料的不同性质,使其在癌症治疗方面能够实现靶向给药,缓释给药,同时在降低毒副作用方面有着巨大的潜力。随着纳米技术的发展,人们可以在药物传递系统中引入特异的结构从而实现独特的治疗功能。二氧化硅纳米颗粒,尤其是空心结构的二氧化硅纳米粒子,具有易修饰功能化、生物相容性好、孔隙体积较大、密度较小,稳定性好等优点。在生物学和医学方面已经成为研究的热点之一。研究证明,空心二氧化硅纳米粒子是各种治疗药物的安全有效且有前途的载体。但是它通常需要额外的结构修饰以实现特有的功能,从而控制生物活性药物在体内的传递,而这些额外的修饰却又可能导致额外的细胞毒性,因此需要寻找合适的功能基团。
技术实现要素:
为了解决上述问题,本发明的目的是提供一种亲水空心硅球及其制备方法和其作为药物缓释载体方面的应用,所述的亲水空心硅球能够使药物缓慢释放,降低其毒副作用,且制备简单、生物兼容性良好。
为了实现上述目的,本发明所采用的技术方案是:
一种亲水空心硅球,是以乙烯基三乙氧基硅烷通过催化反应形成的硅-氧结构的双键硅球为核心,对其表面修饰谷胱甘肽,再用氢氟酸刻蚀球心,制备而成。
一种亲水空心硅球的制备方法,是以乙烯基三乙氧基硅烷为载体材料,水为溶剂,氨水作为催化剂,采用硅烷水解的方法制得硅-氧结构的双键硅球;再在引发剂作用下,在双键硅球表面修饰谷胱甘肽,最后用氢氟酸刻蚀球心,制得亲水空心硅球。
具体的,所述的亲水空心硅球的制备方法,包括以下步骤:
(1)采用硅烷水解法制备纳米双键硅球:精确量取2-4ml乙烯基三乙氧基硅烷加入30-70ml纯净水中,机械搅拌,直至乙烯基三乙氧基硅烷完全溶解;再取1ml3-7%(v/v)氨水,边搅拌边滴加,1.5h以内滴加完,滴加完后再继续搅拌1-2h,离心,收集沉淀,用无水乙醇和水依次洗涤后,减压真空干燥,得到双键硅球;
(2)谷胱甘肽修饰的双键硅球的制备:称取制备的双键硅球80-120mg,分散于40-60ml乙腈中;称取谷胱甘肽80-120mg溶于10-15ml蒸馏水中;合并以上两个溶液,超声分散混合均匀,再加入8-12mg2,2-偶氮二异丁腈,在氮气保护下,60-80℃恒温搅拌12-24h,离心,收集沉淀,用无水乙醇和水依次洗涤后,减压真空干燥,得到谷胱甘肽修饰的双键硅球;
(3)亲水空心硅球的制备:称取谷胱甘肽修饰的双键硅球200-400mg加入10-20ml无水乙醇中,超声振荡分散均匀,再加入20-30ml1%(v/v)氢氟酸,超声振荡,使谷胱甘肽修饰的双键硅球均匀分散在氢氟酸中,磁力搅拌2-10h,离心,收集沉淀,用蒸馏水洗涤至中性后,用无水乙醇洗涤,减压真空干燥,得到亲水空心硅球。
步骤(1)中机械搅拌的转速为300-400r/min。
所述的减压真空干燥的温度为40-60℃,时间为10-20h。
一种亲水空心硅球在药物缓控释放中的应用。
所述的亲水空心硅球作为药物缓释载体。
本发明的有益效果:
1、本发明以乙烯基三乙氧基硅烷通过催化反应形成的硅-氧结构的双键硅球为核心,对其表面修饰谷胱甘肽,再用氢氟酸刻蚀球心,得到亲水空心硅球,成功构建了一种以化疗药物为目标分子,空心硅球为基质,制备操作简单易行的药物缓释系统。
2、本发明亲水空心硅球的制备包括三步,第一步乙烯基硅烷水解后形成硅-氧结构为核心,外表为双键呈疏水性,疏水性硅球在水溶液中以团聚且生物兼容兼容性较低,因此为了改善其疏水性与生物兼容性,选择亲水的生物分子谷胱甘肽为功能分子,以谷胱甘肽的巯基与硅球表面的双键点击化学反应,从而使硅球表面形成一层亲水膜层,有效改善了硅球的分散性,使上载药物能够缓慢释放,进而降低其毒副作用,且生物兼容性良好。
3、硅球制备过程中氨水的滴加速度不同,制得的硅球粒径也不同,经氢氟酸刻蚀的时间不同,硅球的内部空隙体积也不同,都会影响载体对药物分子的上载量。本发明通过控制氨水的滴加速度,得到合适粒径的硅球,并通过优化氢腐蚀的刻蚀时间,进一步提高了亲水空心硅球的药物上载量。
4、药物包封及体外模拟释放实验结果显示,本发明制备空心硅球与对照组的实心硅球相比,对喜树碱的药物上载及体外释放,存在显著性差异,充分证明本发明所制备的亲水空心硅球载体对药物具有较高的负载能力和缓控释放作用。
5、本发明的亲水空心硅球设计简单,不需要高温高压等反应条件,且硅球粒径分布均匀,为亲水空心硅球的工业化生产提供了可行性,为药物缓释载体的研究提供了新的途径,具有良好的社会和经济效益。
附图说明
图1为不同处理后双键硅球的透射电镜图。其中,(a)为谷胱甘肽修饰的双键硅球,(b)为氢氟酸刻蚀后的亲水空心硅球。
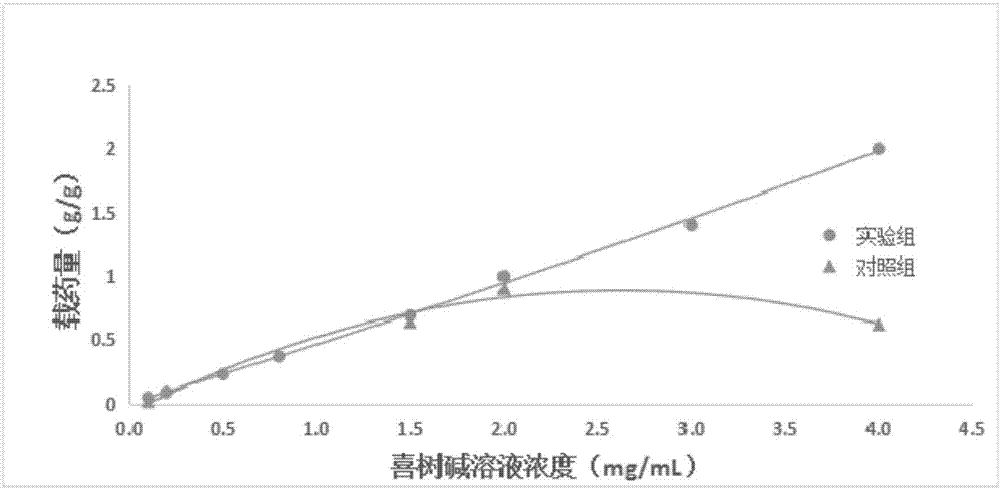
图2为亲水空心硅球的载药量曲线图。
图3为磷酸盐缓冲液中喜树碱体外模拟释放曲线图。
具体实施方式
以下结合实施例对本发明的具体实施方式作进一步详细说明。
实施例1
一种亲水空心硅球的制备方法,包括以下步骤:
(1)采用硅烷水解法制备纳米双键硅球:精确量取2.0ml乙烯基三乙氧基硅烷加入30ml纯净水中,以300r/min的转速机械搅拌,直至乙烯基三乙氧基硅烷完全溶解,溶液变澄清;再取1ml5%(v/v)氨水,边搅拌边滴加至澄清的乙烯基三乙氧基硅烷溶液中,1.5h以内滴加完,滴加完后再继续搅拌1h,离心,收集沉淀,用无水乙醇和水依次洗涤后,40℃减压真空干燥12h,得到双键硅球;
(2)谷胱甘肽修饰的双键硅球的制备:称取制备的双键硅球80mg,分散于40ml乙腈中,得到双键硅球的乙腈溶液;称取谷胱甘肽80mg溶于10ml蒸馏水中,得到谷胱甘肽溶液;合并双键硅球的乙腈溶液和谷胱甘肽溶液,超声分散混合均匀,再加入8mg2,2-偶氮二异丁腈,在氮气保护下,60℃恒温搅拌12h,离心,收集沉淀,用无水乙醇和水依次洗涤后,40℃减压真空干燥12h,得到谷胱甘肽修饰的双键硅球;对谷胱甘肽修饰的双键硅球进行电镜表征,如图1(a)所示,可以看出谷胱甘肽修饰的双键硅球具有良好分散性,平均粒径在300nm左右。
(3)亲水空心硅球的制备:称取谷胱甘肽修饰的双键硅球200mg加入10ml无水乙醇中,超声振荡分散均匀,再加入20ml1%(v/v)氢氟酸,超声振荡,使谷胱甘肽修饰的双键硅球均匀分散在氢氟酸中,磁力搅拌2h,离心,收集沉淀,用蒸馏水洗涤至中性后,用无水乙醇洗涤,40℃减压真空干燥12h,得到亲水空心硅球。对氢氟酸刻蚀后的亲水空心硅球进行电镜表征,如图1(b)所示,可以看出刻蚀过的亲水空心硅球的中间有凹陷、边缘有卷曲且稍颜色变浅,表明硅球球心是中空的。
实施例2
一种亲水空心硅球的制备方法,包括以下步骤:
(1)采用硅烷水解法制备纳米双键硅球:精确量取3.0ml乙烯基三乙氧基硅烷加入50ml纯净水中,以350r/min的转速机械搅拌,直至乙烯基三乙氧基硅烷完全溶解,溶液变澄清;再取1ml5%(v/v)氨水,边搅拌边滴加至澄清的乙烯基三乙氧基硅烷溶液中,1.5h以内滴加完,滴加完后再继续搅拌1.5h,离心,收集沉淀,用无水乙醇和水依次洗涤后,40℃减压真空干燥12h,得到双键硅球;
(2)谷胱甘肽修饰的双键硅球的制备:称取制备的双键硅球100mg,分散于50ml乙腈中;称取谷胱甘肽100mg溶于13ml蒸馏水中;合并以上两个溶液,超声分散混合均匀,再加入10mg2,2-偶氮二异丁腈,在氮气保护下,60℃恒温搅拌18h,离心,收集沉淀,用无水乙醇和水依次洗涤后,40℃减压真空干燥12h,得到谷胱甘肽修饰的双键硅球;
(3)亲水空心硅球的制备:称取谷胱甘肽修饰的双键硅球300mg加入15ml无水乙醇中,超声振荡分散均匀,再加入25ml1%(v/v)氢氟酸,超声振荡,使谷胱甘肽修饰的双键硅球均匀分散在氢氟酸中,磁力搅拌6h,离心,收集沉淀,用蒸馏水洗涤至中性后,用无水乙醇洗涤,40℃减压真空干燥12h,得到亲水空心硅球。
实施例3
一种亲水空心硅球的制备方法,包括以下步骤:
(1)采用硅烷水解法制备纳米双键硅球:精确量取4.0ml乙烯基三乙氧基硅烷加入70ml纯净水中,以400r/min的转速机械搅拌,直至乙烯基三乙氧基硅烷完全溶解,溶液变澄清;再取1ml5%(v/v)氨水,边搅拌边滴加至澄清的乙烯基三乙氧基硅烷溶液中,1.5h以内滴加完,滴加完后再继续搅拌2h,离心,收集沉淀,用无水乙醇和水依次洗涤后,40℃减压真空干燥12h,得到双键硅球;
(2)谷胱甘肽修饰的双键硅球的制备:称取制备的双键硅球120mg,分散于60ml乙腈中;称取谷胱甘肽120mg溶于15ml蒸馏水中;合并以上两个溶液,超声分散混合均匀,再加入12mg2,2-偶氮二异丁腈,在氮气保护下,60℃恒温搅拌24h,离心,收集沉淀,用无水乙醇和水依次洗涤后,40℃减压真空干燥12h,得到谷胱甘肽修饰的双键硅球;
(3)亲水空心硅球的制备:称取谷胱甘肽修饰的双键硅球400mg加入20ml无水乙醇中,超声振荡分散均匀,再加入30ml1%(v/v)氢氟酸,超声振荡,使谷胱甘肽修饰的双键硅球均匀分散在氢氟酸中,磁力搅拌10h,离心,收集沉淀,用蒸馏水洗涤至中性后,用无水乙醇洗涤,40℃减压真空干燥12h,得到亲水空心硅球。
应用例、亲水空心硅球的包封及缓释实验
(1)药物包封:以喜树碱作为模型药物。称取喜树碱10mg,用二甲基亚砜(dmso)在10ml的容量瓶中定容,得到1mg/ml的喜树碱溶液,然后用蒸馏水将喜树碱溶液稀释成0.1mg/ml。称取20mg的亲水空心硅球,加入10ml0.1mg/ml的喜树碱溶液,密封后搅拌10h,作为实验组。同时另取10ml0.1mg/ml的喜树碱溶液,加实心硅球20mg,平行操作,作为对照组。另取10ml0.1mg/ml的喜树碱溶液,不加亲水空心硅球,平行操作,作为空白组。搅拌结束后,离心,分别收集沉淀和上清。按照上述实验操作,分别考察喜树碱浓度为0.1、0.2、0.5、0.8、1.5、2.0、3.0、4.0mg/ml,亲水空心硅球20mg的包封效果。离心后上清溶液,用紫外分光光度法测定包封前后喜树碱在254nm波长下的吸收值,然后通过下面的公式(1)和(2)分别计算出药物的载药量和包封率:
结果如图2所示:实验组亲水空心硅球的载药量随着药物浓度的增加而增加,对喜树碱的上载量可达2g/g,包封率大于90%,对照组的载药量小于0.5g/g,包封率30%左右,实验组与对照组存在显著性差异,因此充分证明本发明所制备的亲水空心硅球载体对药物具有较高的负载能力。
(2)药物体外模拟释放:取喜树碱上载量20mg的亲水空心硅球载体,分散于80ml磷酸盐缓冲液(pbs,ph=7.4)中,恒温37.5℃下低速搅拌,每隔2h取出400μl混悬液,经0.2μm滤膜过滤,滤液中加3mlpbs缓冲液稀释。将稀释好的溶液用紫外分光光度法测定喜树碱在254nm波长下的吸收值,然后计算药物释放浓度,连续测定72h,结果如图3所示:释放时间40h时释放液中喜树碱药物的浓度为0.03mg/ml;40h后,喜树碱药物的释放率逐步提升,至72h喜树碱药物的浓度为0.07mg/ml。对照实验组,释放浓度在72h内基本稳定,无缓释效果。从整体趋势来看,亲水空心硅球载体在72h的体外模拟释放过程中具有较好的缓释效果。
综上所述,本发明构建的亲水空心硅球基质药物缓释载体制备过程简单、反应条件温和,可以应用于药物的缓控释放。
以上所述仅为本发明最佳的实施例,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!