甘油激酶作为糖代谢紊乱疾病的治疗靶标的用途的制作方法
本发明属于生物制药领域,更具体地,本发明涉及甘油激酶作为糖代谢紊乱疾病的治疗靶标的用途。
背景技术:
肝脏糖代谢(包括吸收血糖、糖原合成与分解、糖异生及输出)在维持血糖稳态中发挥重要作用。肝脏糖异生亢进是2型糖尿病肝糖输出增加导致血糖升高的一个重要病理机制,纠正亢进的肝糖生成有利于控制糖尿病发病进程及续发性疾病。所以靶向肝糖产生的抑制剂研究对控制和治疗糖代谢紊乱相关疾病,包括代谢综合症和2型糖尿病等,具有重要意义。
甘油激酶(glycerolkinase)能够催化甘油磷酸化为3-磷酸甘油。在脂肪细胞中,因为甘油激酶表达很低,所以不能有效利用脂肪分解产生的甘油,只有通过血液循环运输至肝、肾、肠等组织利用。甘油在甘油激酶作用下,转变为3-磷酸甘油,然后脱氢生成磷酸二羟丙酮,再循糖代谢途径进行氧化分解释放能量,也可在肝脏沿糖异生途径转变为葡萄糖或糖原。
现有技术中,目前没有报导甘油激酶在2型糖尿病中的作用以及通过调控akt-foxo-pepck/g6pase通路调控肝脏糖异生和血糖稳态。
技术实现要素:
本发明的目的在于提供甘油激酶作为糖代谢紊乱疾病的治疗靶标的用途。
在本发明的第一方面,提供甘油激酶或其调节剂的用途,用于制备改善或治疗糖代谢紊乱疾病的组合物。
在一个优选例中,所述的糖代谢紊乱疾病包括:高血糖,高胰岛素血症,胰岛素抵抗,糖耐量受损,糖尿病(包括1型糖尿病和2型糖尿病);低血糖。
在另一优选例中,所述的调节剂包括甘油激酶的表达下调剂和活性/功能抑制剂,甘油激酶的表达下调剂和活性/功能抑制剂用于制备改善或治疗高血糖,胰岛素抵抗,糖耐量受损(糖耐量降低),糖尿病(包括1型糖尿病和2型糖尿病)的组合物。
在另一优选例中,所述的甘油激酶的下调剂和活性/功能抑制剂还用于制备具有如下功能的制剂:
降低血糖和空腹血糖;
增强葡萄糖清除能力;
提高胰岛素敏感性;
减少糖异生;或
降低葡萄糖-6-磷酸酶或磷酸烯醇式丙酮酸羧激酶的表达。
在另一优选例中,所述的甘油激酶的下调剂包括下调甘油激酶的基因转录、多肽表达的下调剂;较佳地是特异性干扰甘油激酶的基因表达的干扰分子;更佳地,所述的干扰分子是以甘油激酶基因或其转录本为抑制或沉默靶标的shrna,反义核酸、小干扰rna、微小rna,或能表达或形成所述shrna,反义核酸、小干扰rna、微小rna的构建物;或所述的甘油激酶的抑制剂包括特异性抑制甘油激酶活性或功能的抗体、化合物等。
在另一优选例中,所述的干扰分子是shrna,其核苷酸序列包括seqidno:1所示的序列;或所述的干扰分子是包括seqidno:1所示的序列或以seqidno:1所示的序列为靶标的表达系统(包括但不限于:表达质粒、宿主细胞或病毒;所述的病毒包括腺病毒、腺相关病毒、慢病毒等)。
在另一优选例中,所述的调节剂是上调剂,所述的甘油激酶或其上调剂用于制备改善或治疗低血糖的组合物。
在另一优选例中,所述的甘油激酶或其上调剂还用于制备具有如下功能的制剂:
降低血液甘油浓度;
升高血糖;
增强糖异生;
升高葡萄糖-6-磷酸酶或磷酸烯醇式丙酮酸羧激酶的表达;
降低转录因子foxo1及其上游分子akt的磷酸化;或
升高foxo1下游的分子igfbp1的表达。
在另一优选例中,所述的甘油激酶的上调剂包括:表达甘油激酶的多核苷酸的表达系统(包括但不限于:表达载体、宿主细胞或病毒;所述的病毒包括腺病毒、腺相关病毒、慢病毒等);较佳地,所述的表达系统为表达载体;更佳地,所述的表达载体为病毒载体;或所述的甘油激酶的上调剂是促进甘油激酶表达或增强甘油激酶活性/功能的抗体、化合物。
在另一优选例中,所述的病毒载体选自下组:慢病毒、逆转录酶病毒,腺病毒,疱疹病毒,牛痘病毒或腺相关病毒。
在本发明的另一方面,提供一种用于调节血糖的物质,其是甘油激酶的下调剂,该下调剂具有seqidno:1所示核苷酸序列的shrna;或该下调剂是包括seqidno:1所示的序列或以seqidno:1所示的序列为靶标的表达系统(包括但不限于:表达载体、宿主细胞或病毒;所述的病毒包括腺病毒、腺相关病毒、慢病毒等)。
在本发明的另一方面,提供一种筛选改善或治疗糖代谢紊乱疾病的潜在物质的方法,所述方法包括:
(1)用候选物质处理表达甘油激酶的体系或含有甘油激酶的体系;和
(2)检测所述体系中甘油激酶的表达或活性/功能;
其中,若所述候选物质可提高甘油激酶的表达或增强其活性,则表明该候选物质是改善或治疗低血糖的潜在物质;若所述候选物质可降低甘油激酶的表达或抑制其活性/功能,则表明该候选物质是改善或治疗高血糖,胰岛素抵抗,糖耐量受损,糖尿病(包括1型糖尿病和2型糖尿病)的潜在物质。
在一个优选例中,所述的筛选方法中,步骤(1)包括:在测试组中,将候选物质加入到表达甘油激酶的体系或含有甘油激酶的体系中;步骤(2)包括:检测测试组的体系中甘油激酶的表达或活性/功能,并与对照组比较,其中所述的对照组是不添加所述候选物质的表达甘油激酶的体系或含有甘油激酶的体系;
如果测试组中甘油激酶的表达或活性在统计学上高于(优选显著高于,如提高20%以上,较佳的提高50%以上;更佳的提高80%以上)对照组,就表明 该候选物是改善或治疗低血糖的潜在物质;如果测试组中甘油激酶的表达或活性在统计学上低于(优选显著低于,如降低20%以上,较佳的降低50%以上;更佳的降低80%以上)对照组,就表明该候选物是改善或治疗高血糖,胰岛素抵抗,糖耐量受损,糖尿病(包括1型糖尿病和2型糖尿病)的潜在物质。
在另一优选例中,所述的筛选方法中,所述的候选物质可以是:基于影响甘油激酶的活性或功能、或调控其表达的基因或蛋白而设计的大分子(如肽、抗体、过表达载体或干扰分子)或小分子(如化合物)。
在另一优选例中,所述的筛选方法中,所述的体系选自:细胞体系(或细胞培养物体系)、亚细胞体系、溶液体系、组织体系、器官体系或动物体系。
在另一优选例中,所述的筛选方还包括:对获得的潜在物质进行进一步的细胞实验和/或动物试验,以从候选物质中进一步选择和确定对于改善或治疗糖代谢紊乱疾病有用的物质。
本发明的其它方面由于本文的公开内容,对本领域的技术人员而言是显而易见的。
附图说明
图1、在高脂饮食诱导的糖尿病小鼠模型抑制肝脏甘油激酶表达显著改善高血糖和胰岛素敏感性。
a:c57bl/6j小鼠喂饲常规饲料(chow)或60%高脂饲料(hfd)12周,检测肝脏甘油激酶(gyk)mrna和蛋白水平。
b-i:利用腺病毒介导在高脂饮食诱导的糖尿病小鼠过表达甘油激酶shrna(sh-gyk)或非特异性shrna(sh-nc),分别检测肝脏gyk的mrna和蛋白水平(b),血中葡萄糖(c)、胰岛素(d)和甘油(g)水平,检测糖耐量(e,gtt)、胰岛素耐量(f,itt)和丙酮酸耐量(h,ptt),检测肝脏糖异生酶基因g6pase和pepck表达(i)。图中数值为平均值±标准误差,n=6-10。*p<0.05;**p<0.01;***p<0.001,与chow喂饲组小鼠相比(a),与sh-nc组小鼠相比(b-i)。
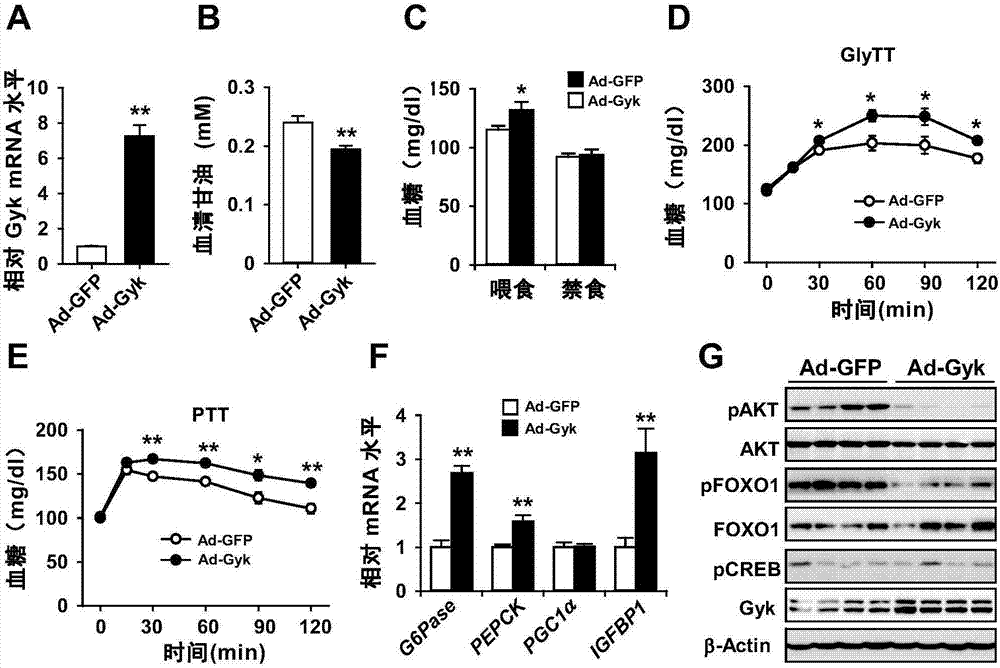
图2、甘油激酶对糖异生和血糖稳态的调控作用。
利用腺病毒介导在c57bl/6j小鼠过表达甘油激酶(ad-gyk)或对照蛋白 gfp(ad-gfp),分别检测肝脏gykmrna(a)和蛋白水平(g),血甘油水平(b),血糖水平(c),检测以甘油为前体(d,glytt)或以丙酮酸为前体(e,ptt)的糖异生,肝脏g6pase和pepckmrna表达(f),以及肝脏akt、foxo1和creb磷酸化(g)。图中数值为平均值±标准误差,n=6-9。*p<0.05;**p<0.01,与过表达gfp的对照小鼠相比。
图3、甘油激酶对糖异生和血糖稳态的调控作用。
利用腺病毒介导在c57bl/6j小鼠过表达甘油激酶shrna(sh-gyk)或非特异性shrna(sh-nc),分别检测肝脏gykmrna和蛋白水平(a),自由进食时和空腹血糖水平(b),血清胰岛素水平(c),检测糖耐量(gtt,d)、胰岛素耐量(itt,e)、丙酮酸耐量(ptt,f),以及肝脏g6pase和pepckmrna表达(g)。图中数值为平均值±标准误差,n=7-9。*p<0.05;**p<0.01,与sh-nc组小鼠相比。
图4、甘油激酶通过akt-foxo1信号通路促进肝细胞表达糖异生酶及产糖。
利用腺病毒介导在原代培养小鼠肝细胞中过表达甘油激酶(ad-gyk)或对照蛋白gfp(ad-gfp),分别检测细胞通过糖异生产生的葡萄糖量(a,n=5)、akt和foxo1磷酸化(b),以及100nm胰高血糖素刺激后糖异生酶g6pase和pepck的表达(c,n=3)。图中数值为平均值±标准误差,*p<0.05;**p<0.01,与过表达gfp的肝细胞相比。
具体实施方式
本发明人经过深入的研究,发现甘油激酶(gyk)不仅能通过催化甘油生成3-磷酸甘油而参与糖异生,还通过akt-foxo1信号通路调控糖异生酶g6pase和pepck表达而调控糖异生,在维持血糖稳态中发挥重要作用。因此,甘油激酶及其调节剂是调节血糖乃至治疗糖尿病的新靶标。
甘油激酶及其治疗用途
所述的甘油激酶的氨基酸序列可以如genbank登录号caa55365.1,gi:516124所示;或其与该序列具有保守性或同源性(如序列相同性高于80%;较佳地高于85%;更佳地高于90%;更佳地高于95%;如98%,99%)的序列。所述的甘油激酶可以分离自细胞,或者可通过基因工程方法制备。在得知了甘油激酶的序列后,本领域人员可以方便地制备获得甘油激酶。
基于本发明的阐述,甘油激酶是一个新的、与糖代谢紊乱疾病密切相关的药物靶点。针对甘油激酶的各种治疗手段可以作为防治动物(特别是人)的糖代谢紊乱疾病的新颖且有效的手段。
如本文所用,所述的“糖代谢紊乱疾病”包括但不限于:高血糖,高胰岛素血症,胰岛素抵抗,糖耐量受损,糖尿病(包括1型糖尿病和2型糖尿病);低血糖等。
并且,甘油激酶也可以用于作为药物筛选的靶点,筛选通过降低或提高甘油激酶的表达或活性而缓解或治疗糖代谢紊乱疾病的药物。
甘油激酶调节剂的治疗用途
基于本发明人的新发现,所述的甘油激酶的下调剂可用于制备改善或治疗高血糖,胰岛素抵抗,糖耐量受损(糖耐量降低),糖尿病(包括1型糖尿病和2型糖尿病)的组合物。
如本文所用,所述的“甘油激酶(表达)下调剂”及“活性或功能抑制剂”包括了核酸抑制物、拮抗剂、抑制剂、阻滞剂、阻断剂等,只要它们能够下调甘油激酶的表达水平、抑制甘油激酶的活性或功能。它们可以是化合物、化学小分子、生物分子。所述的生物分子可以是核酸水平(包括dna、rna)的,也可以是蛋白水平的。
所述的甘油激酶(表达)下调剂是指任何可降低甘油激酶的活性、降低甘油激酶的稳定性、下调甘油激酶的表达、减少甘油激酶有效作用时间的物质,这些物质均可用于本发明,作为对于下调甘油激酶有用的物质,从而可用于缓解或治疗高血糖或糖尿病。例如,所述的下调剂是:核酸抑制物、蛋白抑制剂、抗体、配体、化合物、核酸酶、核酸结合分子等,只要其能够下调甘油激酶的表达、抑制其活性或功能。所述的核酸抑制物包括但不限于:以甘油激酶基因或其转录本为抑制或沉默靶标的shrna,反义核酸、小干扰rna、 微小rna,或能表达或形成所述shrna,反义核酸、小干扰rna、微小rna的构建物。
作为本发明的优选方式,所述的甘油激酶下调剂是shrna,其核苷酸序列包括seqidno:1所示的序列;或所述的干扰分子是包括seqidno:1所示的序列或以seqidno:1所示的序列为靶标的表达系统。所述的表达系统包括但不限于:表达质粒、宿主细胞或病毒;所述的病毒包括腺病毒、腺相关病毒、慢病毒等。
基于本发明人的新发现,所述的甘油激酶的上调剂可用于制备改善或治疗低血糖的组合物。
所述的甘油激酶的上调剂是指任何可提高甘油激酶的活性、提高甘油激酶的稳定性、上调甘油激酶的表达、增加甘油激酶有效作用时间的物质,这些物质均可用于本发明,作为对于上调甘油激酶有用的物质,从而可用于提高血糖。它们可以是化合物、化学小分子、生物分子。所述的生物分子可以是核酸水平(包括dna、rna)的,也可以是蛋白水平的。
作为本发明的优选选择方式,所述的甘油激酶上调剂是表达甘油激酶的表达系统。所述的表达系统没有特别的限制,任何可表达出具有甘油激酶或其类似物、模拟物相似活性的表达系统均可应用于本发明中。例如,所述的表达系统包括但不限于:表达载体、含有表达载体的宿主细胞或病毒;所述的病毒包括腺病毒、腺相关病毒、慢病毒等。本领域技术人员了解如何表达出甘油激酶或其类似物、模拟物,并且已经有一些商业化的表达系统,均可应用于本发明中。
药物组合物
本发明还提供了一种组合物,它含有有效量(如0.000001-50wt%;较佳的0.00001-20wt%;更佳的,0.0001-10wt%)的所述的甘油激酶或其表达载体、或甘油激酶调节剂(包括上调剂或下调剂),以及药学上可接受的载体。所述的组合物可用于改善或治疗糖代谢紊乱疾病。
如本文所用,所述“有效量”是指可对人和/或动物产生功能或活性的且可被人和/或动物所接受的量。所述“药学上可接受的载体”指用于治疗剂给 药的载体,包括各种赋形剂和稀释剂。该术语指这样一些药剂载体:它们本身并不是必要的活性成分,且施用后没有过分的毒性。合适的载体是本领域普通技术人员所熟知的。在组合物中药学上可接受的载体可含有液体,如水、盐水、缓冲液。另外,这些载体中还可能存在辅助性的物质,如填充剂、润滑剂、助流剂、润湿剂或乳化剂、ph缓冲物质等。所述的载体中还可以含有细胞转染试剂。
在得知了所述甘油激酶或其调节剂的用途后,可以采用本领域熟知的多种方法来将所述的甘油激酶或其表达载体、甘油激酶调节剂或它们的药物组合物给药于哺乳动物。包括但不限于:皮下注射、肌肉注射、静脉输入、经皮给予、局部给予、植入、缓释给予等。
本发明所述的甘油激酶或其表达载体、甘油激酶调节剂的有效量可随给药的模式和待治疗的疾病的严重程度等而变化。优选的有效量的选择可以由本领域普通技术人员根据各种因素来确定(例如通过临床试验)。所述的因素包括但不限于:所述的甘油激酶或其表达载体、甘油激酶调节剂的药代动力学参数例如生物利用率、代谢、半衰期等;患者所要治疗的疾病的严重程度、患者的体重、患者的免疫状况、给药的途径等。通常,当本发明的甘油激酶或其调节剂每天以约0.00001mg-50mg/kg动物体重(较佳的0.0001mg-10mg/kg动物体重)的剂量给予,能得到令人满意的效果。例如,由治疗状况的迫切要求,可每天给予若干次分开的剂量,或将剂量按比例地减少。
药物筛选
在得知了甘油激酶与糖代谢紊乱疾病的密切相关性后,可以基于该特征来筛选调节甘油激酶的表达(及甘油激酶的调节剂)的物质。
因此,本发明提供一种筛选调节血糖的潜在物质的方法,所述的方法包括:用候选物质处理表达或含有甘油激酶的体系;和检测所述体系中甘油激酶的表达或活性/功能;若所述候选物质可降低甘油激酶的表达或活性/功能,则表明该候选物质是降低血糖的潜在物质,反之则表明该候选物质是提高血糖的潜在物质。所述的表达或含有甘油激酶的体系例如可以是细胞(或细胞培养物)体系,所述的细胞可以是内源性表达甘油激酶的细胞;或可以是表达重组甘油激酶的细胞。所述的表达或含有甘油激酶的体系还可以是亚细胞体系、 溶液体系、组织体系、器官体系或动物体系(如动物模型,优选非人哺乳动物的动物模型,如鼠、兔、羊、猴等)等。
在本发明的优选方式中,在进行筛选时,为了更易于观察到甘油激酶的表达或活性/功能的改变,还可设置对照组,所述的对照组可以是不添加所述候选物质的表达甘油激酶的体系或含有甘油激酶的体系。
作为本发明的优选方式,所述的方法还包括:对获得的潜在物质进行进一步的细胞实验和/或动物试验,以进一步选择和确定对于调节血糖真正有用的物质。
本发明对于甘油激酶的表达、活性、存在量的检测方法没有特别的限制。可以采用常规的基因定量或半定量检测技术、酶催化反应等,例如(但不限于):聚合酶链式反应技术(pcr),northern印迹法等。
另一方面,本发明还提供了采用所述筛选方法获得的可调节血糖的潜在物质。这些初步筛选出的物质可构成一个筛选库,以便于人们最终可以从中筛选出能够对于调节甘油激酶的表达和活性,进而调节血糖有用的物质。
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件如j.萨姆布鲁克等编著,分子克隆实验指南,第三版,科学出版社,2002中所述的条件,或按照制造厂商所建议的条件。
材料与方法
1、实验动物
c57bl/6j背景的雄性小鼠购自上海斯莱克实验动物有限公司。小鼠饲养于spf级动物房,12小时光照昼夜循环,除了实验特殊要求外,小鼠自由进食常规饲料和水。通过给8周龄c57bl/6j小鼠喂食60%高脂饲料(researchdiets)至少12周建立高脂诱导的糖尿病小鼠模型。所有的小鼠实验操作均遵循institutionalanimalcare以及usecommitteeoftheinstitutefornutritionalsciences有关细则。
2、腺病毒制备和纯化
甘油激酶(gyk)及gfp腺病毒表达质粒使用adeasy腺病毒表达系统(stratagene,lajolla,ca)构建。
扩增小鼠gykmrnacds区的pcr引物序列为:
正向:5′-aaggaaaaaagcggccgcgaagctgactgacttcc-3′(seqidno:3);
反向:5′-cccaagcttaatccgtgaggtggtatt-3′(seqidno:4)。
扩增gfpcdna的pcr引物序列为:
正向:5’-atggtgagcaagggcgagga-3’(seqidno:5);
反向:5’-ttacttgtacagctcgtccat-3’(seqidno:6)。
gykshrna腺病毒表达质粒(sh-gyk)使用block-ittmadenoviralrnaiexpressionsystem(invitrogen)构建。
gykshrna(sh-gyk)序列为:
5’-gctatagctggtgctgtaatcttcaagagagattacagcaccagctatagc-3’(seqidno:1)。
ncshrna(sh-nc)序列为:
5’-cctaaggttaagtcgccctcgccgaagcgagggcgacttaaccttagg-3’(seqidno:2)。
上述表达gyk、gfp、gyk-shrna或nc-shrna的腺病毒表达质粒通过酶切线性化后,分别用lipofectamine2000(invitrogen)转染hek293a腺病毒包装细胞以产生相应的腺病毒,收集上清和细胞,用0.5%np-40室温裂解细胞20min,12000rpm4℃离心10min;每100ml上清加入50mlpeg8000(20%peg8000+2.5mnacl),在冰上放置2h后,12000rpm4℃离心20min;弃上清,用1.1g/mlcscl(溶剂为20mmtri-hcl,ph8.0)重悬沉淀,7000rpm,离心5min;取上清依次进行不连续和连续cscl密度梯度离心,取病毒带用200倍体积的透析缓冲液在4℃透析三次,每次3h,分装病毒保存于-80℃,测定病毒滴度后按照需要量使用。
利用腺病毒系统在小鼠肝脏过表达gyk或其对照gfp、过表达sh-gyk或其对照nc-shrna:将上述表达gyk、gfp、sh-gyk或nc-shrna的腺病毒,通过尾静脉注射1×109pfu(plaque-formingunits,配制于200μlpbs),5天后 进行葡萄糖耐受实验(glucosetolerancetest,gtt)、丙酮酸耐受实验(pyruvatetolerancetest,ptt)或甘油耐受实验(glyceroltolerancetest,glytt)。实验后注射6%水合氯醛(0.1ml/10g)麻醉处死小鼠,收集血清和肝脏等组织样品,保存于-80℃冰箱,待之后分析。
3、葡萄糖、丙酮酸和甘油耐受实验
小鼠禁食6h后,腹腔注射2g/kg体重的葡萄糖、2g/kg体重的丙酮酸或2g/kg体重的甘油进行gtt、ptt或glytt实验。于注射前及注射后在15、30、60、90和120min用血糖仪从尾部取血测定血糖值。
4、血清生化分析
血清胰岛素浓度用millipore的胰岛素elisa测定试剂盒;血清甘油水平用普利莱的甘油(液体样品)酶法测定试剂盒检测。
5、rna抽提和荧光定量pcr
小鼠组织中的总rna使用invitrogen公司的trizol试剂抽提,步骤如下:每10mg~40mg组织在1.5mlep管中加0.4mltrizol进行研磨后补至1ml,加入0.2ml氯仿,剧烈震荡15s后将其在室温下放置5min,在4℃下以12000rpm离心10min。约取350μl水样层转移到一干净的ep管中,加入等体积异丙醇沉淀rna,室温条件下放置30min后,4℃下12000rpm离心10min。移去上层液体,用75%的乙醇溶液(depc水配制)洗涤rna沉淀一次后,用depc水溶解。
rna抽提后用takara公司的dnaseⅰ消化,以去除dna。取2μgrna用m-mlv逆转录酶通过逆转录系统将mrna逆转录得到cdna,逆转录产物通过美国appliedbiosystems公司(fostercity,ca)的sybrgreenpcrsystem进行扩增,以36b4(mrna)为内参进行mrna丰度分析。
荧光定量pcr使用的引物如表1。
表1
6、westernblot
用含cocktail蛋白酶抑制剂的ripa裂解液处理细胞或组织,离心去除细胞碎片,测蛋白质浓度。取等量的蛋白(10~20μg)与4×蛋白上样缓冲液混合上样,在恒压(80-120v)下进行sds-page电泳(凝胶厚度1.5mm,积层胶5%,分离胶10%),再用湿转法将蛋白质转移到pvdf膜上。用含5%脱脂奶粉的tbst溶液封闭pvdf膜1h,然后加入一抗,4℃结合过夜。用tbst室温洗膜3次,每次5min。加入相应的二抗于室温结合1~2h,再用tbst洗膜3次,用thermoscientific公司的supersignalwestpicochemiluminescentsubstrate检测系统显色。
7、统计学分析
实验结果均以均值±标准误的形式呈现,两组之间的差别用双尾非配对t检验进行统计分析,当p值小于0.05时认为有统计学差异(*p<0.05;**p<0.01;***p<0.001)。
实施例1、糖尿病模型小鼠肝脏甘油激酶表达升高,抑制甘油激酶表达能显著改善小鼠的高血糖和胰岛素敏感性
甘油激酶通过催化甘油生成3-磷酸甘油而参与糖异生(gluconeogenesis)。 甘油激酶主要在肝脏表达,其次是肾脏,在脂肪组织和骨骼肌有少量表达。本发明人在高脂饲料诱导的糖尿病小鼠模型中发现,肝脏甘油激酶(glycerolkinase,gyk)的表达显著高于对照饲料喂养的小鼠(图1a)。
本发明人利用腺病毒介导的rna干扰抑制糖尿病模型小鼠肝脏gyk表达(图1b)。结果发现,rna干扰gyk表达后,能显著降低小鼠在自由进食时的血糖和空腹血糖(图1c),改善高胰岛素血症(图1d)。糖耐量实验表明,小鼠的葡萄糖清除能力显著增强(图1e)。胰岛素耐量实验表明,小鼠的胰岛素敏感性显著升高(图1f)。
这些结果提示,肝脏gyk升高在高脂饮食导致的胰岛素抵抗、高血糖和糖耐量降低中发挥重要作用。
进一步研究发现,在糖尿病模型小鼠抑制肝脏gyk表达能显著升高血清甘油浓度(图1g),说明gyk表达被抑制后,其催化甘油生成3-磷酸甘油减少,从而使糖异生减少。
丙酮酸耐量实验发现,在肝脏甘油激酶表达被抑制后,以丙酮酸为前体的糖异生被抑制(图1h),肝脏糖异生关键酶葡萄糖-6-磷酸酶(g6pase)和磷酸烯醇式丙酮酸羧激酶(pepck)的表达被抑制(图1i)。
这些结果提示,gyk不但通过催化甘油生成3-磷酸甘油参与糖异生,而且还可能通过调控g6pase和pepck表达而调控其他前体物质(如丙酮酸)的糖异生,从而使血糖升高。
实施例2、甘油激酶通过调控甘油代谢以及akt-foxo1介导的糖异生基因表达而调控糖异生和血糖稳态
本实施例中,在正常小鼠中探讨gyk在肝脏糖异生及血糖稳态中的功能及机制。
1、过表达gyk的影响
本发明人利用腺病毒介导在正常小鼠肝脏过表达gyk(图2a),发现血液甘油浓度显著降低(图2b)、小鼠在自由进食时的血糖升高(图2c),以甘油作为前体的糖异生显著增强(图2d)。这些结果说明,gyk在整体水平通过调控甘油代谢而调控糖异生,证实了gyk在调控以甘油为前体的糖异生中的作用。
丙酮酸耐受实验显示,gyk过表达小鼠的糖异生能力也是增强的(图2e), 证实gyk也调控其它前体参与的糖异生。与上述结果一致,本发明人在分子水平检测到gyk过表达使小鼠肝脏糖异生关键酶g6pase和pepck表达升高(图2f)。
进一步的机制研究发现,小鼠肝脏过表达gyk使调控g6pase和pepck表达的转录因子foxo1及其上游分子akt的磷酸化都显著降低(图2g),foxo1下游的分子igfbp1(insulin-likegrowthfactorbindingprotein1)也像g6pase和pepck一样显著升高(图2f);但另一些调控糖异生的分子,如pgc1α的表达和creb的磷酸化则没有显著变化(图2f和2g)。已知akt的磷酸化能促进胞浆foxo1磷酸化继而降解,使foxo1进入细胞核减少,其对g6pase和pepck表达的促进作用减弱,从而抑制糖异生。
因此,上述结果表明,gyk除了通过影响甘油代谢调控糖异生,还通过akt-foxo1信号通路影响糖异生关键酶g6pase和pepck的表达而调控糖异生,从而维持血糖平衡。
2、干扰gyk表达的影响
本发明人进一步通过腺病毒介导的rna干扰在正常小鼠肝脏抑制gyk表达,探讨gyk在小鼠糖代谢及血糖稳态调控中的作用。
结果发现,与肝脏过表达gyk的结果相反,抑制肝脏gyk表达(图3a)能显著降低小鼠自由进食时的血糖及空腹血糖水平(图3b),降低血清胰岛素水平(图3c),小鼠的糖耐量稍有升高(图3d),但胰岛素敏感性显著升高(图3e),以丙酮酸为前体的糖异生能力显著降低(图3f),肝脏糖异生酶g6pase和pepck的表达显著降低(图3g)。
这些结果证实,肝脏gyk在生理情况下能通过调控糖异生酶基因表达而促进糖异生,在维持血糖稳态中发挥重要作用。
3、原代培养的肝细胞中过表达gyk的影响
本发明人最后通过腺病毒介导在原代培养的肝细胞中过表达gyk,发现过表达gyk能显著促进葡萄糖生成(图4a),抑制akt和foxo1磷酸化(图4b),促进胰高血糖素诱导的pepck和g6pase表达(图4c)。
这些结果在细胞水平验证了甘油激酶通过akt-foxo-pepck/g6pase通 路促进肝细胞糖异生。
实施例3、药物筛选
1、以表达甘油激酶的细胞进行药物筛选
取小鼠原代培养的肝细胞,该细胞可内源性表达甘油激酶。将该种细胞作为用于筛选改善或治疗糖代谢紊乱疾病的细胞模型。
测试组:用候选物质处理上述细胞;
对照组:未用候选物质处理上述细胞。
在处理后,测定所述细胞的甘油激酶的表达。如果与对照组相比,测试组中的甘油激酶的表达显著上升1.5倍以上,则说明该候选物质是潜在的改善或治疗低血糖的物质;如果与对照组相比,测试组中的甘油激酶的表达显著下降1.5倍以上,则说明该候选物质是潜在的改善或治疗高血糖,胰岛素抵抗,糖耐量受损,糖尿病的物质。
以前述获得的gykshrna病毒转染小鼠原代培养的肝细胞,可以使得细胞内甘油激酶表达下降,因此gykshrna病毒是一中对于改善或治疗高血糖,胰岛素抵抗,糖耐量受损,糖尿病有用的物质。
2、基于甘油激酶活性进行药物筛选
取重组表达的甘油激酶用于筛选甘油激酶调节剂。
测试组:用候选物质处理含有甘油激酶的反应溶液;
对照组:未用候选物质处理的甘油激酶反应溶液。
在处理后,根据甘油激酶催化甘油生成3-磷酸甘油,用甘油测定试剂盒(普利莱公司)测定反应前后的甘油浓度,以甘油消耗量代表甘油激酶的活性。如果与对照组相比,测试组中的甘油激酶的活性显著上升1.5倍以上,则说明该候选物质是潜在的改善或治疗低血糖的物质;如果与对照组相比,测试组中的甘油激酶的活性显著下降1.5倍以上,则说明该候选物质是潜在的改善或治疗高血糖,胰岛素抵抗,糖耐量受损,糖尿病的物质。
综上所述,本发明人在高脂饮食诱导的糖尿病小鼠模型发现肝脏gyk表达升高,抑制肝脏gyk表达能显著降低小鼠的高血糖,提高胰岛素敏感性,增强小鼠的葡萄糖清除能力。通过在正常小鼠以及离体培养肝细胞的实验, 本发明人发现,gyk不仅能通过催化甘油生成3-磷酸甘油而参与糖异生,还通过akt-foxo1信号通路调控糖异生酶g6pase和pepck表达而调控糖异生,在维持血糖稳态中发挥重要作用。因此,gyk是治疗糖尿病的新靶标。
在本发明提及的所有文献都在本申请中引用作为参考,就如同每一篇文献被单独引用作为参考那样。此外应理解,在阅读了本发明的上述讲授内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
- 还没有人留言评论。精彩留言会获得点赞!