交互式解剖标测和对解剖标测质量的估计的制作方法
本发明整体涉及解剖标测,并且更具体地涉及用于交互式解剖标测和对解剖标测质量的估计的方法和系统。
背景技术:
解剖标测可用于诊断各种类型的医疗病症,诸如心律失常。各种技术可被应用于导出解剖标测并被应用于控制标测过程。
例如,其公开内容以引用方式并入本文的美国专利8,744,566描述了用于确定和表示解剖信息的方法和系统。这些方法和系统包括基于导管电极的位置和来自电极位置的所确定的子集处的电极的电信号来生成心脏的解剖信息。
其公开内容以引用方式并入本文的美国专利8,457,371描述了用于标测结构的方法和设备。该标测设备可包括可感测电压的一个或多个电极,该电压可在感测或测量时与电极的三维位置相关。区域或体积的标测图可基于对多个点的感测来确定,而无需使用成像装置。然后可相对于标测数据对植入式医疗装置进行导航。
其公开内容以引用方式并入本文的美国专利8,900,225描述了用于执行包括使探头与患者体内的器官接触的医疗规程的方法。显示该器官的标测图并跟踪探头相对于标测图的位置。
其公开内容通过引用并入本文的美国专利申请公布2009/0099468描述了用于心脏内电生理数据的自动处理的方法、设备和计算机程序产品。该方法包括录制电描记图数据,限定包含用于确定时间位置的参考搏动的至少一个参考通道,创建时间位置的索引,实时分析至少一种电生理特征,以及提供更新的索引和分析的结果。
技术实现要素:
本文所述的本发明的实施方案提供了一种方法,该方法包括接收包括在患者的器官内的多个相应位置处获取的多个测量的解剖标测。基于该测量来计算器官的估计表面。限定器官的从器官的估计表面向内延伸并具有预定义的厚度的三维(3D)壳体。基于其位置落在3D壳体内的测量来估计解剖标测的质量。
在一些实施方案中,限定3D壳体包括在距估计表面向内预定义的距离处形成虚拟表面,从而在估计表面和虚拟表面之间限制壳体。在其他实施方案中,估计解剖标测的质量包括对其位置落在壳体的至少部分内的测量的数量进行计数。在其他实施方案中,该壳体包括多个体积像素(体素),并且基于测量落在其中的壳体的至少部分内的体素的数量来估计质量。
在实施方案中,该壳体包括包括有多个像素的表面,并且基于测量落在其中的壳体的至少部分内的像素的数量来估计质量。在另一个实施方案中,该器官包括心腔。
根据本发明的另一个实施方案另外提供了一种方法,该方法包括接收包括在患者的器官内的多个相应位置处获取的多个测量的部分解剖标测。基于测量来计算器官的估计部分表面。基于该测量来识别器官的还未由部分解剖标测进行标测的未访问区域。向用户指示未访问区域,以便帮助用户标测未访问区域并且延伸估计部分表面。
在一些实施方案中,使用导管的远侧端部来获取多个测量,并且指示未访问区域包括显示指示用户要移动远侧端部的方向的图形指示,以便标测未访问区域。在其他实施方案中,该方法包括在器官的至少部分内重叠体积像素(体素)的网格,并且识别未访问区域包括识别网格的还未由部分解剖标测进行标测的一个或多个体素。在其他实施方案中,该方法包括限定从用于获取测量的导管远侧端部向外延伸的给定体积,并且识别未访问区域包括在给定体积内识别还未由远侧端部访问的位置。
根据本发明的实施方案另外提供了包括接口和处理器的设备。该处理器被配置为从接口接收包括在患者的器官内的多个相应位置处获取的多个测量的解剖标测,基于测量来计算器官的估计表面,限定器官的从器官的估计表面向内延伸并具有预定义的厚度的三维(3D)壳体,并且基于其位置落在3D壳体内的测量来估计解剖标测的质量。
根据本发明的实施方案还提供了包括接口和处理器的设备。该处理器被配置为接收包括在患者的器官内的多个相应位置处获取的多个测量的部分解剖标测,基于测量来计算器官的估计部分表面,基于测量来识别器官的还未由部分解剖标测进行标测的未访问区域,并且在输出装置上向用户指示未访问区域,以便帮助用户标测未访问区域并且延伸估计部分表面。
以下结合附图根据本发明的实施方案的详细说明将更全面地理解本发明,在附图中:
附图说明
图1为根据本发明的实施方案的采用解剖标测的基于导管的跟踪和消融系统的示意性图解;
图2为根据本发明的实施方案的心脏的内表面的解剖标测图的示意性图解,以及朝向表面的未标测区域引导用户的可视化方案;
图3为根据本发明的实施方案的心脏的内表面的估计解剖标测图的示意性图解;并且
图4为根据本发明的实施方案的用于估计解剖标测图的质量的方案的示意性图解。
具体实施方式
概述
在一些医疗规程诸如心脏消融中,基于心脏的估计解剖标测图来将医疗探头导航到患者心脏中。可通过插入具有被设置在导管远侧端部上的感测电极的导管并且使用电极来测量心脏的内表面上的组织的多个位置处的某些信号来执行对解剖标测图的估计。基于此类测量的标测算法诸如快速解剖标测(FAM)在本领域中为已知的。该FAM方法可向医师提供附加标测能力,诸如可用于心脏消融的电生理(EP)标测。
在FAM规程期间,医师将导管的远侧端部导航到被分布在所考虑的组织上方的期望位置,以便从中收集解剖信号。原则上,该FAM可向医师提供用于表示所考虑的组织的估计解剖标测的表面。该表面将由医师在EP标测和消融规程期间使用,因此在开始EP规程之前监控解剖标测的质量为重要的。
下文所述的本发明的实施方案提供了用于交互式解剖标测的改进的技术。所公开的技术可用于向医师指示心脏表面的未标测(“未访问”)区域。在实施方案中,在接收到对解剖标测的部分测量之后,该处理器计算组织的部分表面并基于部分表面来识别组织中的一个或多个未访问区域以用于进一步的解剖标测。
在实施方案中,该处理器被配置为显示用于将医师引导到未访问区域的图形指示,以便帮助医师标测整个表面。在断定解剖标测之后,该处理器显示整个表面的估计解剖标测。
在另一个实施方案中,该处理器被配置为通过限定从估计解剖表面向内延伸的三维(3D)壳体来估计解剖标测的质量。例如,该处理器可限定平行于估计表面的虚拟表面,使得3D壳体为限制在两个表面之间的体积。在一些实施方案中,该处理器基于其位置落在预定义的体积内的标测测量的数量来估计解剖标测的质量。
所公开的技术提供正在进行的标测规程的实时可视化,并且提供关于估计解剖表面的质量的反馈,从而获取高质量标测并且缩短规程循环时间。
系统说明
图1为根据本发明的实施方案的基于导管的跟踪和消融系统20的示意性图解。系统20包括导管22(在本示例中为心脏导管)和控制台24。在本文所述的实施方案中,导管22可用于任何合适的治疗目的和/或诊断目的,诸如心脏26中的腔37的解剖标测。
控制台24包括处理器39(通常为通用计算机),该处理器39具有合适的前端和接口电路38,以用于经由导管22来接收信号并且用于控制本文所述的系统20的其他组件。控制台24还包括用户显示器35(也被称为输出装置),该显示器被配置为显示如以下图2至图4所示的用于帮助解剖标测的工具。
使用在心脏组织的相应位置处收集多个测量的远侧端部40来执行解剖标测的规程,该测量在本文中被称为标测图点。每个标测图点包括腔37的组织上的三维(3D)坐标以及对在该坐标处测量的一些生理特性的相应测量。
在一些实施方案中,处理器39被配置为基于测量或标测图点来构造(图3和图4所示的)估计解剖表面,并且在显示器35上向医师30呈现估计解剖表面。在构造估计解剖表面的过程中,处理器39可将规程诸如例如在美国专利申请公布2011/0152684中所述的快速解剖标测(FAM)规程应用于测量,该专利公开内容以引用方式并入本文。
在一些医疗规程诸如组织消融中,医师30预先创建待消融的组织的解剖标测图。为执行解剖标测,医师30将导管22插入穿过躺在手术台29上的患者28的血管系统。导管22包括通常被装配在远侧端部40处的一个或多个电极(未示出)。该电极被配置为感测心脏26的腔37的组织。医师30通过利用靠近导管近侧端部的操纵器32操纵导管22来将远侧端部40导航到腔37中,如插图23所示的。导管22的近侧端部连接至处理器39中的接口电路。
在一些实施方案中,腔37中的远侧端部的位置由磁性位置跟踪系统的位置传感器(未示出)测量。所测量的位置用作相应标测图点的坐标。
例如,该解剖测量可使用3系统的快速解剖标测(FAM)功能协同标测导管诸如导管来获取,两者均购自加利福尼亚州钻石吧市钻石肯扬路3333号的强生公司91765(Biosense Webster,Inc.,3333 Diamond Canyon Road,Diamond Bar,Calif.91765)。
在这种情况下,控制台24包括驱动电路34,该驱动电路驱动被放置在躺在手术台29上的患者28体外的已知位置处(例如,患者的躯干下方)的磁场发生器36。该位置传感器被装配到远侧端部并被配置为响应于来自场发生器36的所感测的外部磁场来生成位置信号。该位置信号指示远侧端部在位置跟踪系统的坐标系中的位置。
该位置感测方法在各种医疗应用中实现,例如在由强生公司(Biosense Webster Inc.(加利福尼亚州钻石吧市(Diamond Bar,Calif.))生产的CARTOTM系统中实现,并且详细地描述于美国专利5,391,199、6,690,963、6,484,118、6,239,724、6,618,612和6,332,089、PCT专利公布WO 96/05768,以及美国专利申请公布2002/0065455 A1、2003/0120150 A1和2004/0068178 A1中,这些专利的公开内容全部以引用方式并入本文。
在一些实施方案中,医师30可使用处理器39以用于将远侧端部40导航到目标位置并用于激活电极,以便感测和/或消融腔37处的组织。在另选的实施方案中,处理器39可仅用于帮助医师30标测未访问区域以及估计解剖标测的质量。
处理器39通常包括通用计算机,该通用计算机以软件编程执行本文所述的功能。该软件可电子形式经网络而被下载到计算机,例如作为另外一种选择或除此之外,该软件可被提供和/或存储在非临时性有形介质诸如磁性存储器、光学存储器、或电子存储器上。
通过指示未访问区域而进行的交互式解剖标测
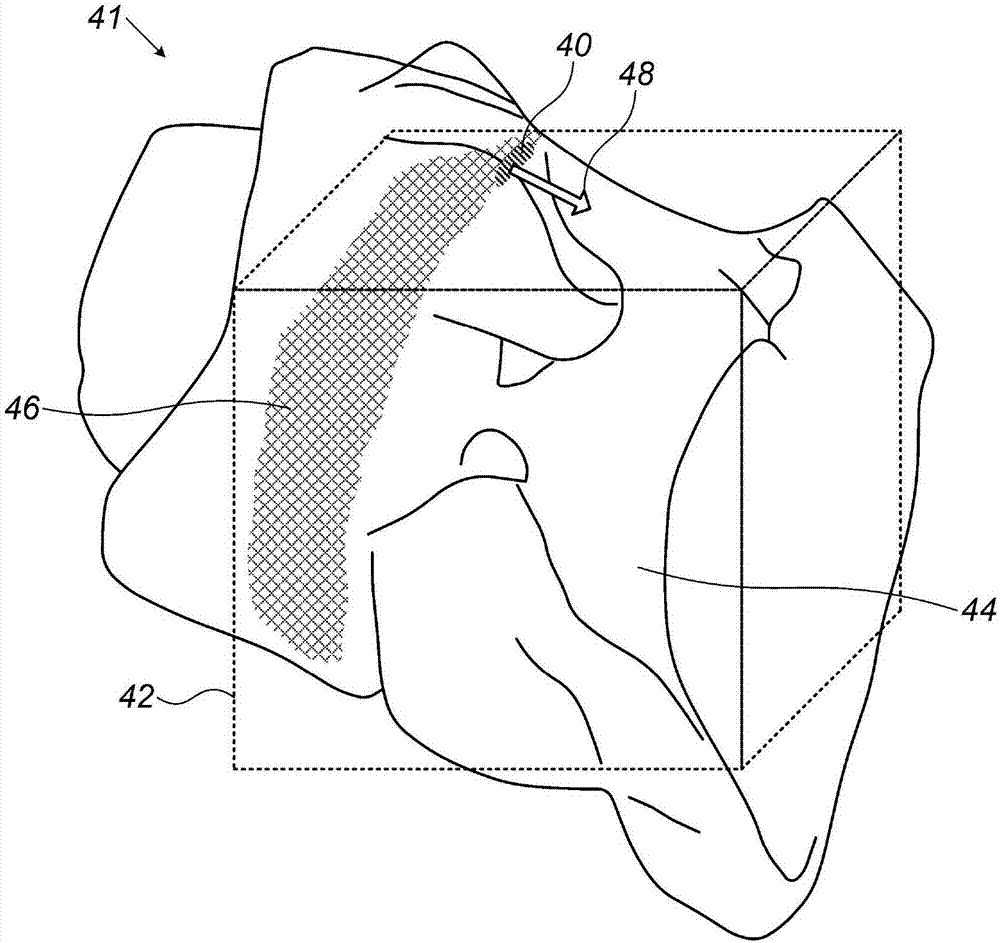
图2为根据本发明的实施方案的腔37的解剖标测图41的示意性图解,以及朝向腔37的未标测区域引导医师30的可视化方案。在一些实施方案中,处理器39接收心脏26的解剖数据,并且使用该解剖数据来显示心脏26中的腔37的估计体积42。在实施方案中,体积42可被示意性地显示为立方体形状,或使用任何其他合适的形状。
在一些实施方案中,处理器39还从远侧端部40接收部分解剖标测,该部分解剖标测包括在腔37内的多个相应位置处获取的多个测量,诸如快速解剖标测(FAM)。在实施方案中,基于这些测量,处理器39被配置为计算已在腔37中标测的估计部分表面46。
在实施方案中,使用估计体积42和已获取的测量,处理器39还被配置为识别腔37的未访问区域,诸如还未由部分解剖标测进行标测的估计表面44。在本上下文中,术语“未访问区域”是指腔37的表面的还未由估计部分表面46表示的区域。
在一些实施方案中,处理器39在解剖标测图41上显示如从位置跟踪系统接收的远侧端部40的位置,以及指示未访问区域的方向的箭头48,以便帮助医师30完成对腔37的组织的标测。
在其他实施方案中,处理器39在体积42上方重叠三维(3D)像素(也被称为体素(未示出))的网格。在该实施方案中,处理器39对体积42内的体素的部分进行采样,并且识别还未由远侧端部40访问的体素。然后,处理器39显示指示未访问体素的方向的箭头48。
在一些实施方案中,处理器39可基于在表面46和体积42处获取的测量来显示未访问区域的表面44。在其他实施方案中,处理器可仅显示表面46、远侧端部40、和箭头48,以便向医师30指示未访问区域的方向,而无需外推针对估计表面46所获取的测量。
在实施方案中,处理器39限定从远侧端部40向外延伸的给定体积(未示出)并识别给定体积内的还未由远侧端部40访问的位置。然后,处理器39显示指示给定体积内的未访问位置的方向的箭头48,以便帮助医师30完成对腔37的组织的标测。
估计解剖标测的质量
图3为根据本发明的实施方案的估计解剖标测图43的示意性图解。在一些实施方案中,为了生成解剖标测图43,处理器39接收在腔37内的多个相应位置处获取的多个解剖测量,诸如快速解剖标测(FAM)。
基于测量,处理器39计算估计表面45并在显示器35上显示解剖标测图43中的表面45。需注意,对表面45的计算基于采样测量而不是对表面45的连续标测。在一些实施方案中,对表面45的计算可涉及在其中获取的采样测量的内插,因此如标测图43中显示的表面45的至少部分可为不准确的。例如,多个测量之间的内插区域可包括可偏离由处理器39制作的估计形貌的未访问的解剖特征(例如,隆起块或凹坑)。
在一些实施方案中,医师30可限定从估计表面45向内延伸到腔37的内部体积中的3D壳体52。壳体52的形状可由处理器39使用各种方法来限定。例如,处理器39在由医师30或处理器39设定的预定义的距离(例如,7mm)处限定平行于表面45的虚拟表面50。在该实施方案中,壳体52的体积被限制在表面45和50的边界之间。在实施方案中,壳体52的体积被用于估计表面45的解剖标测质量,如以下图4所描绘的。
图4为根据本发明的实施方案的用于估计解剖标测图43的质量的方案的示意性图解。在一些实施方案中,处理器39在解剖标测图43上显示表面45和50、壳体52、以及通过使用如以上图1至图3所述的远侧端部40访问表面45处的所选择位置而获取的测量54。
在一些实施方案中,处理器39被配置为在壳体52的体积内选择一个或多个切片,诸如切片56和58。切片可由处理器39随机选择,或根据由医师30手动设定或由处理器39自动设定的预定义的参数(例如,壳体52内的特定位置)来选择。
在实施方案中,每个切片表示壳体52内的包括多个像素的子表面或子体积。为了清晰起见,在图4的示例中,每个切片包括所描绘的九个像素。在实施过程中,每个切片可包括任何合适数量的像素。
在一些实施方案中,每个切片可包括表示落在相应切片内的测量54的像素55。在实施方案中,处理器39被配置为检查落在每个切片内的像素55的一部分,以便估计由表面45表示的解剖标测的质量。在实施方案中,插图66和68分别表示切片56和58内的像素55的分布。一般来讲,高度填充的切片表示高标测质量,并且反之亦然。
在插图66中,看起来像素55表示切片56的大部分像素(例如,九个中的八个),因此切片56可获取指示标测图41的左侧上的高质量的解剖标测的高分(例如,89%(按照8/9=0.89导出))。使用相同的方法,仅两个像素55落在切片58内,并且切片58的分数为22%(通过对9个中的2个像素进行计数导出),该分数指示解剖标测图41的上部中心区域中的低质量的解剖标测。
在一些实施方案中,基于上述评分方法,处理器39被配置为显示表示用于腔37的每个区域的解剖标测的质量的量化图。在实施方案中,医师30可设定一个或多个质量阈值,使得在低于腔37的特定位置处的解剖标测的期望质量的情况下,处理器39向医师30提供警报。
在其他实施方案中,切片56和58可表示体积元素,而不是二维(2D)表面,使得像素55可表示体素(未示出)而不是2D像素。
尽管本文所述的实施方案主要论述心脏病学应用,但本文所述的方法和系统也可被用于其他应用中,诸如耳-鼻-喉(ENT)和支气管镜检中。
应当理解,上述实施方案以举例的方式被引用,并且本发明不限于上文具体示出和描述的内容。相反,本发明的范围包括上文所述的各种特征的组合和子组合,以及本领域技术人员在阅读上述说明时会想到且未在现有技术中公开的其变型和修改。以引用方式并入本专利申请的文献将视为本专利申请的整体部分,不同的是如果在这些并入的文献中定义的任何术语与在本说明书中明确或隐含地给出的定义相冲突,则应只考虑本说明书中的定义。
- 还没有人留言评论。精彩留言会获得点赞!