一种治疗光感受器损坏引起视力丧失的系统的制作方法
本发明属于医疗设备技术领域,涉及一种治疗眼睛失明的系统,具体涉及一种恢复由于光感受器损坏引起的视力丧失的受试者的视网膜的光敏感性的系统。
技术背景
视网膜病变会破坏视网膜中的感光细胞,从而使得患者无法将外界的光刺激传达到神经中枢。人口中年长者因视网膜退化而失明的比例也不断增加。视觉通常在棒状和锥状体(也称为光感受器)开始时将光信号转换为电信号,然后通过二阶和三阶视网膜神经元和视神经传递到外侧膝状核,然后到达视觉图像的视觉皮层(文献1)。对于由于光感受器损失导致视力受损的患者,根据特定损伤的性质,可通过在这些下游神经元位置之一处提供电刺激来诱导视觉。但如果损伤无法经过修复而复原,即使使用电刺激进行诱导,那么也无法使视力得到恢复。
光感受器细胞的严重损失可由先天性视网膜退行性疾病如视网膜色素变性(rp)引起(文献2),并且可导致完成失明。年龄相关性黄斑变性(amd)也是光感受器细胞变性和死亡的结果,其可能导致位于视野中心的最佳视觉区域内的严重视觉损伤。
当视锥细胞和视杆细胞损坏或死亡时,啮齿动物和人类都会逐渐失明,因为几乎没有信号传递给大脑。导致部分或全部失明的遗传性视网膜退化影响全球3000人中的一人。患有usher综合征的患者除视网膜变性外还发展为进行性耳聋。目前没有有效的治疗或治疗这些条件。
长期以来,视网膜变性方法的基础研究一直被分为两种方法:(1)保留视网膜退行性疾病患者中剩余的光感受器的治疗方法;(2)替换失去视网膜变性的光感受器的方法。患有视网膜疾病的患者通常将自己归入那些寻求减缓视力下降和那些已经在法律上失明的人(“没有光感”),由于遗传性眼病或创伤而失去光感受器的人。
对于第一种方法,用神经营养因子进行神经保护(文献3)和基于病毒载体的野生型基因递送用于隐性无效突变(文献4)已进入i/ii期临床试验的最远点(文献5)获得美国批准用于腺相关病毒(aav)介导的先天性黑蒙(lca)基因替代治疗,一种特定形式的视网膜变性。不幸的是,对于晚期视网膜变性患者,这种方法是不适用的,必须更换感光细胞。
为了替换,一种方法涉及将正常组织或细胞移植(置换)到患病视网膜。另一种方法涉及通过视网膜植入物对剩余的非视觉神经元进行电刺激以代替丢失的光感受细胞(假体置换)。但是,这两种方法都面临许多基本障碍。例如,对于成功的移植,植入的组织或细胞必须功能性地集合在宿主视网膜内。电刺激方法背负着机械和技术困难以及与缺乏植入仿生装置的长期生物相容性有关的问题。总之,对遗传性致盲疾病没有有效的视力恢复疗法。
在此公开的发明人的策略需要合适的分子“光传感器”。先前的研究报道了果蝇视紫红质的异源表达(文献6),并且最近,黑视蛋白,内在光敏视网膜神经节细胞的假定光色素(文献7)。然而,这些光敏色素通过g蛋白信号级联与膜通道偶联,并使用视黄醛顺式异构体作为其发色团。结果,需要表达多个基因来提供光敏性。另外,它们的光响应动力学相当缓慢。旨在改善时间分辨率的最近研究描述了光敏k-通道的工程化(文献8),尽管这需要引入外源“分子系链”并且使用紫外线来解除阻挡通道。该工程通道被认为可能有助于恢复退化视网膜的光敏感性,但其在视网膜中的表达和功能尚不清楚。
zhuohuapan利用与细菌视紫红质类似的微生物型视紫红质(文献9),其构象改变是由其发色团的可逆光异构化引起的组,视黄醛的全反式同种型,并且直接与通过膜的离子运动偶联(文献10)。已有研究人员从莱茵衣藻克隆了两种微生物型视蛋白,channelopinin-1和-2(chop1和chop2)(文献11)并显示直接形成光门控膜通道在全反式视黄醛存在下在非洲爪蟾卵母细胞或hek293细胞中表达时。
视网膜基因治疗对人类来说一直被认为是可能的治疗选择。例如,美国专利no.5,827,702涉及通过使细胞与外源核酸在其中外源核酸被细胞摄取用于表达的条件下接触来产生遗传工程化的眼细胞的方法。外源核酸被描述为逆转录病毒,腺病毒,腺伴随病毒或质粒。
在这种基因治疗中的努力主要集中在减缓原发性光感受器疾病的啮齿动物模型中的视网膜变性。传递给光感受器的正常基因和突变特异性核酶延长了这些细胞的寿命,否则注定其为凋亡细胞死亡(文献12)。
已有报道证实了使用重组腺相关病毒(raav)基因绿色荧光蛋白(gfp)的视网膜基因转移。然而,由视网膜色素上皮细胞(rpe)和/或感光细胞中的遗传缺陷引起的动物盲目疾病,特别是人类和其他哺乳动物的视力恢复尚未实现。jeanbennett及其同事描述了使用基因治疗挽救光感受器的快速变性光感受器模型,该模型使用rp65基因的突变和用正常基因取代或替换突变基因的替代疗法。参见例如acland,bennett及其同事的美国专利公开2004/0022766。这种治疗在视网膜变性严重疾病天然发生的狗模型中显示出一些成功--rpe65突变体狗类似于人类lca。由以上可知,目前治疗眼盲的方法主要集中在实验室阶段,方法紧局限于生物化学的方法,且通过标记的方法来追踪通道视紫红质结束的位置。
另外,美国加利福尼亚大学伯克利分校的蔡少堂和布达佩斯匈牙利国家科学院的塔马斯·罗斯卡研制出的视网膜芯片为治疗失明提供了全新的方法,尤其是近几年技术的发展,临床上已经实现了将柔性视网膜芯片植入眼睛帮助患者重获光明。2017年,香港大学眼科研究所为一名患有遗传性视网膜色素性变(rp)的香港妇人植入“人工视网膜芯片”,以帮助其找回视力。所植入的芯片质地柔韧,只有3毫米见方,不到1毫米厚。上面布有1500个电极,附带的金属电缆和线圈被分别植入头皮下和耳后,而芯片将被放入视网膜底的黄斑区域。外置的磁力控制器能透过耳后皮肤、通过电缆为芯片供电。即视网膜芯片会代替失去功能的感光细胞接收图像,发出信号刺激视神经,将图像传输到大脑,最终使患者重获光明。但目前患者只能够看到对比度较高的黑白影像,能辨认计算机屏幕上的英文字母,通过控制外置的开关旋钮,她还可以调节芯片的敏感度。不过,人工芯片的功能还远远比不上真正的视网膜,患者目力所及的最远处,只是伸出手臂时的指尖部分。视野也仅仅只有6度,即一张光碟大小的范围。人造视网膜芯片手术受制于复杂的微机电结构、生物兼容性、手术植入的复杂性、金属微电极阵列数目等使其无法得到良好的临床手术效果,同时金属微电极阵列数目的增多尽管会使像素得到提高,但同时会引起热效应,热效应达到一定程度会对眼睛造成损伤,二者之间存在不可调谐的关系,目前已有美国新闻对视网膜芯片因为微电极数目的增多导致的热效应损伤眼睛进行了负面报道。因此,视网膜芯片治疗失明目前还在进一步探索阶段。
文献1:baylord.howphotonsstartvision[j].proceedingsofthenationalacademyofsciences,1996,93(2):560-565;
文献2:sung,chetal.,1991,proc.natl.acad.sci.usa88:6481-85;humphriesp,kennap,farrargj.onthemoleculargeneticsofretinitispigmentosa[j].science,1992,256(5058):804-808;weleber,rgetal.,in:sjryan,ed,retina,mosby,st.louis(1994),pp.335-466.
文献3:lavail,mmetal.,1992,proc.natl.acad.sci.usa89:11249-53.
文献4:acland,gmetal.,2001,nat.genet.28:92-95.
文献5:hauswirth,ww,2005,retina25,s60;jacobson,s,protocol#0410-677,worldwideweburl:webconferences.com/nihoba/16_jun—2005.html.
文献6:zemelmanbv,leega,ngm,etal.selectivephotostimulationofgeneticallychargedneurons[j].neuron,2002,33(1):15-22.
文献7:melyanz,tarttelinee,bellinghamj,etal.additionofhumanmelanopsinrendersmammaliancellsphotoresponsive[j].nature,2005,433(7027):741;pandas,nayaksk,campob,etal.illuminationofthemelanopsinsignalingpathway[j].science,2005,307(5709):600-604;qiux,kumbalasirit,carlsonsm,etal.inductionofphotosensitivitybyheterologousexpressionofmelanopsin[j].nature,2005,433(7027):745.
文献8:banghartm,borgesk,isacoffe,etal.light-activatedionchannelsforremotecontrolofneuronalfiring[j].natureneuroscience,2004,7(12):1381.
文献9:oesterhelt,detal.,1973,proc.natl.acad.sci.usa70:2853-7.
文献10:oesterheltd.thestructureandmechanismofthefamilyofretinalproteinsfromhalophilicarchaea[j].currentopinioninstructuralbiology,1998,8(4):489-500.文献11:nagel,g.etal.,2002,science296:2395-8;sineshchekov,oaetal.,2002,proc.natl.acad.sci.usa99:8689-94;nagel,g.etal.,2003,proc.natl.acad.sci.usa100,13940-45.
文献12:bennett,j.,etal.1996nat.med.2,649-54;bennett,j.,etal.1998,genetherapy5,1156-64;kumar-singh,retal.,1998hum.mol.genet.7,1893-900;lewin,asetal.1998,nat.med.4,967-71;ali,retal.2000,nat.genet.25,306-10;takahashi,m.etal.,1999,jvirol.73,7812-6;lau,d.,etal.,2000,invest.ophthalmol.vis.sci.41,3622-33;andlavail,mm,etal.2000,procnatlacadsciusa97,11488-93.
技术实现要素:
为了解决上述技术问题,本发明提供了一种恢复由于光感受器损坏引起的视力丧失的受试者的视网膜的光敏感性的系统,如视网膜视细胞损坏变性或黄斑损坏变性。
本发明所采用的技术方案是:一种治疗光感受器损坏引起视力丧失的系统,其特征在于:包括飞秒激光手术装置、手术台、计算机、生物打印装置、飞秒连续/突发双模逐层成像装置、xyz精密机械手平台;
所述手术台,为治疗病人时的工作台;
所述飞秒激光手术装置,用于使用飞秒激光切除病人眼睛的坏死视细胞;
所述生物打印装置,用于打印所需的活体视细胞;
所述xyz精密机械手平台用于将活体视细胞注入眼睛;
所述飞秒激光手术装置,还用于对注入眼睛中的活体视细胞进行修复和调节,使注入的视细胞精确填充坏死区域;
所述飞秒连续/突发双模逐层成像装置,用于实时监测整个过程;所述飞秒连续/突发双模逐层成像装置和飞秒激光手术装置均与所述计算机连接,由所述计算机对整个过程进行实时动态控制与管理。
本发明使用先进的生物3d打印技术来获得所需要的感光细胞,周期短、精度高且质量有保证。率先采用先进的超快飞秒连续/突发双模逐层成像装置用来实时监控整个感光细胞和光敏蛋白的注入和转移,采用xyz精密机械手平台通过点对点的方式将打印出来的活体视细胞和光敏蛋白注入眼睛,另外使用精密飞秒激光对眼部局部组织进行实时修复与调控,本发明不仅适用于逆转由许多视网膜退行性疾病引起的视力丧失或失明,同时也适用于遗传性致盲疾病。本发明为临床上治疗眼盲疾病提供了全新的方法和系统装备。
附图说明
图1为本发明实施例的系统原理图:
其中,1为人体眼部器官;2为飞秒激光手术装置;3为手术台;4为计算机;5为超快飞秒连续/突发双模逐层成像装置;6为视网膜内部结构;9为xyz精密机械手平台;
图2为本发明实施例的激光辅助式生物打印装置示意图:
其中,701为飞秒激光光源;702为飞秒激光发射器;703为飞秒激光;704为透明玻璃板;705为吸收层;706为生物墨水层;707为培养皿;708为生物墨水;709为接收基板。
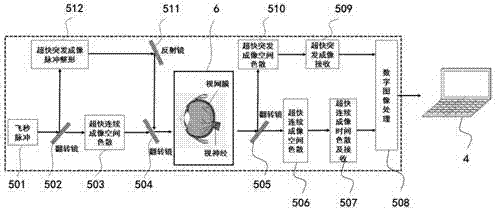
图3为本发明实施例的超快飞秒连续/突发双模逐层成像装置的原理图:
其中,501为飞秒激光脉冲;502为第一翻转镜,503为超快连续成像空间色散模块,504为第二翻转镜,505为第三翻转镜,506为超快连续成像空间色散模块,507为超快连续成像时间色散及接收模块,508为数字图像处理模块,509为超快突发成像接收模块,510为超快突发成像空间色散模块,511为反射镜,512为超快突发成像脉冲整形模块。
图4为本发明实施例的工作流程图:
其中,801为飞秒激光切除眼睛里坏死的视细胞,802为生物打印3d视细胞,803为注射视细胞,804为光敏蛋白进入眼睛,805为光导纤维照射,806为光学信号传递,807为大脑,808为恢复视觉能力。
具体实施方式
为了便于本领域普通技术人员理解和实施本发明,下面结合附图及实施例对本发明作进一步的详细描述,应当理解,此处所描述的实施示例仅用于说明和解释本发明,并不用于限定本发明。
请见图1,本发明提供的一种治疗光感受器损坏引起视力丧失的系统,包括飞秒激光手术装置2、手术台3、计算机4、生物打印装置、飞秒连续/突发双模逐层成像装置5、xyz精密机械手平台9;手术台3,为治疗病人时的工作台;飞秒激光手术装置2,用于使用飞秒激光切除病人眼睛1的坏死视细胞;生物打印装置,用于打印所需的活体视细胞;xyz精密机械手平台9用于将活体视细胞注入眼睛;飞秒激光手术装置2,还用于对注入眼睛中的活体视细胞进行修复和调节,使注入的视细胞精确填充坏死区域;飞秒连续/突发双模逐层成像装置5,用于实时监测整个过程;飞秒连续/突发双模逐层成像装置5和飞秒激光手术装置2均与计算机4连接,由计算机4对整个过程进行实时动态控制与管理。
请见图2,本实施例的生物打印装置包括飞秒激光光源701、飞秒激光发射器702、飞秒激光703、透明玻璃板704、吸收层705、生物墨水层706、培养皿707、生物墨水708、接收基板709;飞秒激光光源701为飞秒激光发射器702提供能量,二者之间通过光纤进行连接;飞秒激光发射器702发射飞秒激光703;吸收层705镀制在透明玻璃板704上,生物墨水708涂覆在吸收层705之上,形成透明玻璃板-吸收层-生物墨水层的三层结构;飞秒激光703聚焦在吸收层705上,使得照射位置的生物墨水层706有一小部分溶液气化膨胀,将该处的生物墨水708挤离表面,形成射流,然后沉积在接收基板709上的培养皿707中。
本实施例生物打印装置采用激光辅助式生物打印,其原因在于,在细胞打印时,对细胞造成损伤最大的因素,是打印时液体流动所造成的剪切力,而喷嘴结构在喷嘴口径较小时,会大大增加对细胞的损伤,所以在这种有喷嘴结构的打印方式中,细胞活性和打印精度是难以兼得的,增加喷嘴口径会降低打印分辨率,而减小喷嘴口径会降低细胞活性。对于激光辅助式而言,由于没有喷嘴结构,所以细胞活性和打印精度是能够很好处理的,因而选择激光辅助式生物打印。
本实施例的飞秒激光手术装置用于去除坏死的视细胞,同时也用来修整注入到眼睛里的视细胞,使视细胞完全填充原视细胞坏死区域。
请见图3,本实施例的飞秒连续/突发双模逐层成像装置5包括飞秒激光脉冲501、第一翻转镜502、第一连续成像空间色散模块503、第二翻转镜504、第三翻转镜505、第二连续成像空间色散模块506、超快连续成像时间色散及接收模块507、数字图像处理模块508、突发成像接收模块509、突发成像空间色散模块510、反射镜511、突发成像脉冲整形模块512;飞秒激光脉冲501经过第一翻转镜502,反射光依次经过突发成像脉冲整形模块512、反射镜511和第二翻转镜504后射入眼睛,透射光依次经过第一连续成像空间色散模块503和第二翻转镜504后射入眼睛1;脉冲光从眼睛1出射后经过第三翻转镜505,反射光依次经过突发成像空间色散模块510和突发成像接收模块509后获得突发成像,透射光依次经过第二连续成像空间色散模块506和超快连续成像时间色散及接收模块507后获得连续成像;突发成像和连续成像经过数字图像处理模块508处理,最后将结果实时显示在计算机4上;通过计算机4实时监测飞秒激光手术装置2对注入眼睛中的活体视细胞进行修复和调节的整个过程。
本实施例的超快飞秒连续/突发双模逐层成像装置采用连续成像和突发成像两种成像方式,二者相互嵌套,所使用的飞秒脉冲频谱宽度达100nm;其组成包括超短脉冲源、时间映射装置、空间映射装置、图像传感器等组成;
本实施例的超快飞秒连续/突发双模逐层成像装置,其采用的飞秒光纤激器产生中心波长为1550纳米的连续频谱。超快飞秒连续成像使用飞秒脉冲为探测光,该脉冲通过衍射光栅后,不同的频率成分被散射到空间的不同角度,落在待测物表面的不同位置,待测物体的表面信息被映射到脉冲的频谱上,将被待测物体发射回来的脉冲导入色散补偿光纤器件,由于色散效应的存在,不同的频率成分逐渐在时间上分开,这个过程等效于对脉冲进行了傅里叶变换,这个过程也成为色散傅里叶变换。通过空间和时间的双重色散,待测物体表面的信息以脉冲频谱为载体,被成功的转换到时域以便进行高速探测。这种方式可以在微米量级的空间分辨率上实现帧率1ghz以上的连续成像。超快飞秒突发成像使用飞秒脉冲为探测光。该脉冲通过时域色散将变成若干个频率不同的并在时间上依次出现子脉冲,这些脉冲依次通过待测物体,待测物体不同时刻的信息就被映射到不同的脉冲上,利用每个脉冲频率不一样的特性,将不同的脉冲映射到空间的不同位置(角度),因此不同脉冲将到达ccd的不同位置,ccd只通过一次曝光就能获得多张图像。由于子脉冲之间的间隔非常小(100fs量级),所以这种方式可以实现高达thz的帧率。利用飞秒脉冲触发待检测的超快事件,同时用该飞秒脉冲进行高速成像,保证了超快成像和超快事件发生的时间窗口对齐。所述的超快飞秒连续/突发双模逐层成像装置可以用于检测活体眼睛里坏死的视细胞及整个切除过程,同时也用于实时检测视细胞注射和友好型病毒携带光敏蛋白的注入过程。
本实施例的超快飞秒连续/突发双模逐层成像装置可以用于检测活体眼睛里坏死的视细胞及整个切除过程,同时也用于实时检测视细胞注射或光敏蛋白的注入过程;
本实施例的视细胞或光敏蛋白的注入过程还可以是注射、喷射、灌注或打印等方法;其中所述的喷射的方法可以是电喷、气喷和静电纺丝的方法,也可以是他们几种方法的结合等。
本实施例的光敏蛋白为视紫红质蛋白,其表现形式为视紫红质通道蛋白1(chr1)和视紫红质通道蛋白2(chr2),同时光敏蛋白也可以是视紫红质通道蛋白1(chr1)和视紫红质通道蛋白2(chr2)的嵌合体c1c2;另外所述的光敏蛋白也可以为抑制性的光敏蛋白如nphr、ro4等。
本实施例的xyz精密机械手平台包括一个机器人手臂或两个协作手柄,每个手臂都是基于光纤传感器的闭环控制,以便可以实现微米级别的点精度;
本实施例的视细胞或光敏蛋白的注入所采用的xyz精密机械手平台也可以使用数控系统平台,也可以使用宏微观结合的结构。喷头处使用纳米压印的方法亦可实现纳米级别的点精度。
本发明不仅适用于逆转由许多视网膜退行性疾病引起的视力丧失或失明,同时也适用于遗传性致盲疾病。本发明为临床上治疗眼盲疾病提供了全新的方法和系统装备。
本发明对整个治疗过程进行实时检测除了本发明实施例中所涉及的超快飞秒连续/突发双模逐层成像装置,还可以与空间超分辨率技术相结合等,提高本发明中所涉及的空间分辨率。
请见图4,为本发明的系统工作流程图,具体包括以下步骤:
(801)首先使用飞秒激光手术装置2进行飞秒激光切除坏死视细胞;
(802)采用图2中所示的激光辅助式生物打印装置获得所需的活体视细胞;具体方法如下:飞秒激光光源701为飞秒激光发射器702提供能量,二者之间通过光纤进行连接,飞秒激光发射器702发射飞秒激光703。生物墨水708被涂覆在镀制在透明玻璃板704上的吸收层705之上,形成透明玻璃板704-吸收层705-生物墨水层706的三层结构,然后脉冲激光703照聚焦在吸收层705上,使得照射位置的生物墨水层706,有一小部分溶液气化膨胀,将该处的生物墨水708挤离表面,形成射流,然后沉积在接收基板上的培养皿707中;
(803)使用xyz精密机械手平台9进行视细胞的注射;
(804)使用飞秒激光手术装置2对注入眼睛中的活体视细胞710进行修复和调节,使其注入的视细胞710精确填充坏死区域,同时使用超快飞秒连续/突发双模逐层成像装置5实时监测整个过程。超快飞秒连续/突发双模逐层成像装置5的原理示意图如图3所示,飞秒脉冲501经过第一翻转镜502分别进行超快连续成像空间色散503和超快突发成像脉冲整形512,接着经过第二翻转镜504和反射镜511射入眼睛,脉冲从眼睛出射经过第三翻转镜505分别进行超快突发成像空间色散510和超快连续成像空间色散506,经过超快突发成像空间色散510后由超快突发成像接收器509进行接收,获得突发成像;经过超快连续成像空间色散506后进行超快连续成像时间色散及接收,获得连续成像。从而实现突发成像和连续成像,经过数字图像处理508,最后将结果实时显示在计算机4上,通过计算机可实时监测飞秒激光手术装置2对注入眼睛中的活体视细胞710进行修复和调节的整个过程;
(806)光敏蛋白进入眼睛,使用xyz精密机械手平台9将光敏蛋白注入活体眼睛;
(807)同理,使用飞秒激光手术装置2对注入眼睛中的光敏蛋白进行修复和调节,使其精确到达预定区域,同时使用超快飞秒连续/突发双模逐层成像装置5实时监测整个过程。具体步骤同(805);
(808)使用光导纤维照射植入眼中的视细胞,从而使光学信号传递下去,并将视觉信息传递给大脑,弥补损失,并导致恢复各种视觉能力,达到恢复视力的目的。
应当理解的是,上述针对较佳实施例的描述较为详细,并不能因此而认为是对本发明专利保护范围的限制,本领域的普通技术人员在本发明的启示下,在不脱离本发明权利要求所保护的范围情况下,还可以做出替换或变形,均落入本发明的保护范围之内,本发明的请求保护范围应以所附权利要求为准。
- 还没有人留言评论。精彩留言会获得点赞!