靶向温控载多糖长循环脂质体-微泡复合物递药系统及其制备方法与流程
本发明涉及可用于药物传递的温控脂质体类物质,具体涉及一种靶向温控的长循环热敏脂质体-微泡复合物。
背景技术:
树舌多糖是从树舌的干燥子实体提取得到的有效成分,被证实具有良好抗肿瘤活性和增强机体免疫功能等作用。研究表明树舌多糖能通过调节t细胞活性,激发体内自主免疫反应,刺激ifn-γ和il-2分泌,或抑制tgf-β1、il-10和vegf生成,从而阻止肿瘤生长发展。但是目前仍存在口服用药利用度低的问题。
脂质体作为一种药物载体,近些年来备受关注。脂质体将药物包封于类似生物膜结构的双分子层中,可以提高药物的利用度、延长药物半衰期,控制药物在体内的释放。脂质体可显著降低抗癌药物的毒副作用,并提高疗效。长循环热敏脂质体是采用不同磷脂材料组成的具有不同相变温度的一类脂质体,并在脂质膜中加入表面活性剂或类脂进行修饰,通过温度控释药物,并增加循环稳定性和在体内的循环时间。
超声引导下的热消融技术,可通过射频、消融、微波等迅速升高肿瘤靶区温度到60℃以上,造成局部组织蛋白凝固,但是目前热消融技术对肝肿瘤的治疗仍存在一定局限性。由于“热沉降”,在大血管周围的组织局部温度较低,以及肿瘤热消融中消融针的位置、肿瘤组织自身对热的传导性等,使温度分布不均(41~50℃),导致出现亚高温温场,组织局部内肿瘤细胞不能被彻底杀灭,消融后仍有细胞存活,存在残余肿瘤组织。
中国专利cn104367546a公开了靶向温控的载水飞蓟宾热敏脂质体-微泡复合体递药系统的制备方法,其采用商品化的微泡,并通过化学键合偶联载药脂质体,所制备的递药系统利用亚高温温场实现局部靶向抗肿瘤药物水飞蓟宾释放,降低肿瘤残余,提高消融疗效。但对于多糖类抗肿瘤药物(特别是水溶性药物活性成分)采用该系统存在以下问题:偶联效率低、稳定性差、载药量低,导致载药系统的制备和使用效率有待提高。
技术实现要素:
本发明的目的在于提供一种靶向温控载多糖长循环脂质体-微泡复合物递药系统及其制备方法。
为达到以上目的,本发明采用的技术方案为:
一种靶向温控载多糖长循环脂质体-微泡复合物递药系统,包括微泡以及位于所述微泡周围并与该微泡偶联的若干个载多糖长循环热敏脂质体,所述微泡是以二棕榈酰磷酯酰胆碱、二硬脂酰磷脂酰乙醇胺-聚乙二醇及二硬脂酰磷脂酰乙醇胺-聚乙二醇-生物素为磷脂材料,并采用薄膜分散法制成的。
优选的,所述多糖选自树舌多糖等水溶性多糖类物质。
优选的,所述载多糖长循环热敏脂质体是以二棕榈酰磷酯酰胆碱、单棕榈酰磷脂酰胆碱、二硬脂酰磷脂酰乙醇胺-聚乙二醇及二硬脂酰磷脂酰乙醇胺-聚乙二醇-生物素为磷脂材料,并与水溶性多糖类物质(例如,树舌多糖等药物活性成分)通过复乳化溶剂挥发法制成的。
优选的,所述偶联是所述微泡及载多糖长循环热敏脂质体各自表面的生物素通过亲和素进行连接而形成的。
上述靶向温控载多糖长循环脂质体-微泡复合物递药系统的制备方法,包括以下步骤:
1)载多糖长循环热敏脂质体的制备
将二棕榈酰磷酯酰胆碱、单棕榈酰磷脂酰胆碱、二硬脂酰磷脂酰乙醇胺-聚乙二醇及二硬脂酰磷脂酰乙醇胺-聚乙二醇-生物素加入有机溶剂中,得磷脂材料溶液a;将上述多糖类物质的水溶液加入到磷脂材料溶液a中后超声乳化,得到乳化液,将乳化液加入水中后超声乳化,得到w/o/w型复乳,除去该复乳中的有机溶剂,得到脂质体混悬液,将脂质体混悬液用水稀释后依次经微孔滤膜过滤、磷酸盐缓冲液透析,得到含有载多糖长循环热敏脂质体的溶液;
2)微泡的制备
将二棕榈酰磷酯酰胆碱、二硬脂酰磷脂酰乙醇胺-聚乙二醇及二硬脂酰磷脂酰乙醇胺-聚乙二醇-生物素加入有机溶剂中,得到磷脂材料溶液b,通过蒸发除去磷脂材料溶液b中的有机溶剂,得到薄膜状物质,将薄膜状物质真空干燥后与由tris-hcl、甘油及丙二醇组成的液体介质混合,然后依次经置换空气、机械振动,得到白色浑浊状微泡分散体系,向该分散体系中加入磷酸盐缓冲液后通过离心除去未配合的磷脂材料,得到生物素化的微泡的溶液;
3)载多糖长循环热敏脂质体-微泡复合物的制备
向生物素化的微泡的溶液中加入过量亲和素后振摇混匀,然后再加入含有载多糖长循环热敏脂质体的溶液并进行孵育,使得所述微泡及载多糖长循环热敏脂质体各自表面的生物素通过亲和素进行连接,得到载多糖长循环热敏脂质体-微泡复合物。
优选的,所述步骤1)中,二棕榈酰磷酯酰胆碱:单棕榈酰磷脂酰胆碱:二硬脂酰磷脂酰乙醇胺-聚乙二醇:二硬脂酰磷脂酰乙醇胺-聚乙二醇-生物素的质量比为(30~35):(3~5):(2~5):(2~5),上述多糖类物质的水溶液是将2~10mg的多糖类物质溶于1~5ml水而制成的,多糖类物质和磷脂材料(二棕榈酰磷酯酰胆碱、单棕榈酰磷脂酰胆碱、二硬脂酰磷脂酰乙醇胺-聚乙二醇及二硬脂酰磷脂酰乙醇胺-聚乙二醇-生物素)的质量比为1:5~20。
优选的,所述步骤1)中,超声乳化的条件为:超声功率为80~150w,超声时间为2~10min,乳化温度为0~4℃;乳化液的有机相:水相的体积比为1~4:1,所述复乳的水相:有机相:水相的体积比为1:(1~4):5(有机相指有机溶剂)。
优选的,所述步骤1)中,微孔滤膜的孔径为0.2~0.8微米(滤膜过滤的目的:1.除菌,2.挤压过滤除去粒径较大的脂质体);透析的条件为:透析袋截留分子量为8000~50000da,透析液(磷酸盐缓冲液)每4~8h换液一次,透析24~36小时。
优选的,所述步骤2)中,二棕榈酰磷酯酰胆碱:二硬脂酰磷脂酰乙醇胺-聚乙二醇:二硬脂酰磷脂酰乙醇胺-聚乙二醇-生物素的质量比为(5~50):(0.5~3):(0.5~3)。
优选的,所述步骤2)中,蒸发采用旋转蒸发仪,旋蒸温度为20~40℃。
优选的,所述步骤2)中,液体介质中tris-hcl:甘油:丙二醇的体积比为(70~90):(10~30):(10~30),其中,tris-hcl选自ph7.4~8的0.1~0.3mtris-hcl。
优选的,所述步骤2)中,真空干燥的温度为20~35℃,时间为12~24h(真空干燥的目的:除去有机溶剂)。
优选的,所述步骤2)中,机械振动采用振荡器,功率为30~50w,时间为30~60s。从而保证制备的微泡可以在体外稳定存在,提高所述复合物的制备效率和稳定性。
优选的,所述步骤2)中,为了达到纯化目的,离心设置的转速为1250~3500r/min。
优选的,所述步骤3)中,孵育采用摇床,孵育条件为:转速为100~150r/min,时间为10~20min,温度为20~25℃。从而提高孵育过程中的偶联效率。
本发明的有益效果体现在:
本发明针对树舌多糖等水溶性多糖类药物成分口服用药生物利用度低,以及现有靶向温控亚高温温场局部给药系统用于该类药物成分时稳定性不足的问题,利用二棕榈酰磷酯酰胆碱、二硬脂酰磷脂酰乙醇胺-聚乙二醇及二硬脂酰磷脂酰乙醇胺-聚乙二醇-生物素为磷脂原料,并采用薄膜分散法制备的生物素化的微泡,与同样生物素化的载药长循环热敏脂质体利用亲和素进行偶联,从而提出了一种载多糖长循环热敏脂质体-微泡复合物。该复合物作为递药系统不仅能够利用微泡的靶向爆破和热敏脂质体的局部温控效应,实现药物在亚高温温场局部高效释放,从而提高药物的生物利用度,并降低热消融治疗中的肿瘤残余,而且借助微泡的稳定性,提高了复合物的偶联效率和稳定性。
进一步的,本发明采用二棕榈酰磷酯酰胆碱、单棕榈酰磷脂酰胆碱、二硬脂酰磷脂酰乙醇胺-聚乙二醇及二硬脂酰磷脂酰乙醇胺-聚乙二醇-生物素和水溶性多糖药物(例如,树舌多糖等)成分为原料,采用复乳化溶剂挥发法制备得到载多糖长循环热敏脂质体,药物成分的包封率显著提高,从而提高了递药系统的载药量,可以更好的在局部组织发挥药效。
附图说明
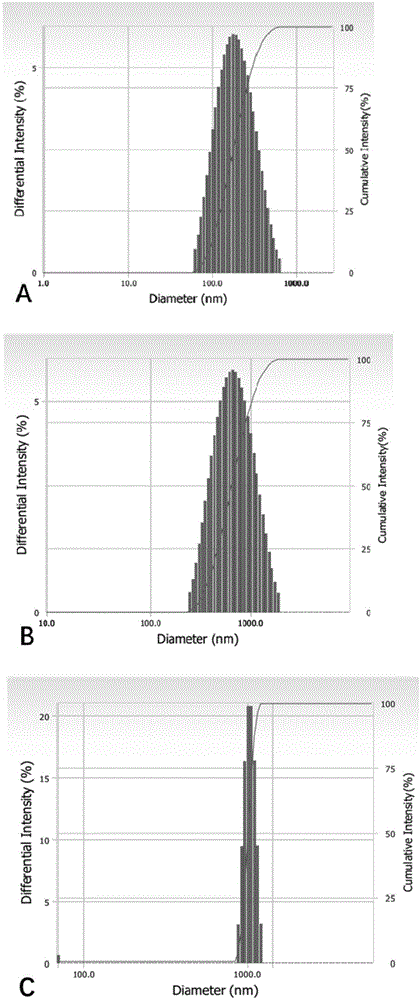
图1是实施例1中载树舌多糖热敏脂质体(a)、全氟丙烷微泡(b)及载树舌多糖热敏脂质体-全氟丙烷微泡复合物(c)的粒径分布图。
图2是实施例1中载树舌多糖热敏脂质体-全氟丙烷微泡复合物的显微视图。
具体实施方式
下面结合附图和实施例本发明做进一步详细说明。所述实施例仅用于解释本发明,而非对本发明保护范围的限制。
实施例1
1)载树舌多糖热敏脂质体的制备
称取32mg二棕榈酰磷酯酰胆碱(dppc)、5mg单棕榈酰磷脂酰胆碱(mppc)、3mg二硬脂酰磷脂酰乙醇胺-聚乙二醇(dspe-mpeg2000)及3mg二硬脂酰磷脂酰乙醇胺-聚乙二醇-生物素(dspe-mpeg2000-biotin)溶于预先加入至50ml离心管内的2ml氯仿于中,称取4mg树舌多糖溶于1ml蒸馏水中,得树舌多糖水溶液,将树舌多糖水溶液加入到溶有磷脂材料(即上述dppc、mppc、dspe-mpeg2000及dspe-mpeg2000-biotin)的氯仿中,冰浴条件下用探头超声乳化2min,形成乳白色的w1/o型初乳(即乳化液),将初乳加入到5ml蒸馏水中,冰浴条件下超声乳化3min形成w1/o/w2型复乳,超声功率均为90w;超声乳化后将复乳置于室温挥发除去有机溶剂(氯仿),得到淡黄色有乳光的脂质体混悬液,加水稀释到10ml,用0.4微米和0.2微米微孔滤膜过滤,用pbs(ph7.4)透析,每8小时换一次透析液,透析24小时,除去游离树舌多糖,得到含有载树舌多糖热敏脂质体的溶液,密封置于4℃冰箱保存。
2)全氟丙烷微泡的制备
称取36mg二棕榈酰磷酯酰胆碱(dppc)、2mg二硬脂酰磷脂酰乙醇胺-聚乙二醇(dspe-mpeg2000)及2mg二硬脂酰磷脂酰乙醇胺-聚乙二醇-生物素(dspe-mpeg2000-biotin)于50ml茄形瓶中,加入10ml氯仿溶解,用旋转蒸发仪在30℃下减压蒸发除去有机溶剂(氯仿),在瓶壁形成薄膜,用25℃真空干燥箱干燥过夜,加入0.1mtris-hcl(ph7.4):甘油:丙二醇(体积比80:10:10)的混合液3ml,用全氟丙烷置换出空气,用银汞调和振荡器机械振动45s(30w),得到白色浑浊的微泡分散体系,加入pbs(ph7.4)后在转速为1250r/min的离心机上离心除去未配合的磷脂材料,得到生物素化的微泡的溶液。
3)载树舌多糖热敏脂质体-全氟丙烷微泡复合物递药系统的制备
向6ml生物素化的微泡的溶液(预先机械振动,使微泡分散均匀,呈白色混浊状)中加入0.5mg亲和素在摇床上于室温振摇15min,加入6ml含有载树舌多糖热敏脂质体的溶液,在摇床上于室温孵育15min,偶联反应完后离心除去未反应的亲和素,离心转速为1250r/min,得到载树舌多糖热敏脂质体-全氟丙烷微泡复合物。
实施例2
1)载树舌多糖热敏脂质体的制备
称取35mg二棕榈酰磷酯酰胆碱(dppc)、5mg单棕榈酰磷脂酰胆碱(mppc)、3mg二硬脂酰磷脂酰乙醇胺-聚乙二醇(dspe-mpeg2000)及3mg二硬脂酰磷脂酰乙醇胺-聚乙二醇-生物素(dspe-mpeg2000-biotin)溶于预先加入至50ml离心管内的2ml氯仿中,称取5mg树舌多糖溶于1ml蒸馏水中,得树舌多糖水溶液,将树舌多糖水溶液加入到溶有磷脂材料(即上述dppc、mppc、dspe-mpeg2000及dspe-mpeg2000-biotin)的氯仿中,冰浴条件下用探头超声乳化3min,形成乳白色的w1/o型初乳(即乳化液),将初乳加入到5ml蒸馏水中,冰浴条件下超声乳化5min形成w1/o/w2型复乳,超声功率均为100w;超声乳化后将复乳置于室温挥发除去有机溶剂(氯仿),得到淡黄色有乳光的脂质体混悬液,加水稀释到10ml,用0.4微米和0.2微米微孔滤膜过滤,用pbs(ph7.4)透析,每8小时换一次透析液,透析24小时,除去游离树舌多糖,得到含有载树舌多糖热敏脂质体的溶液,密封置于4℃冰箱保存。
2)全氟丙烷微泡的制备
称取40mg二棕榈酰磷酯酰胆碱(dppc)、2mg二硬脂酰磷脂酰乙醇胺-聚乙二醇(dspe-mpeg2000)及2mg二硬脂酰磷脂酰乙醇胺-聚乙二醇-生物素(dspe-mpeg2000-biotin)于50ml茄形瓶中,加入10ml氯仿溶解,用旋转蒸发仪在30℃下减压蒸发除去有机溶剂(氯仿),在瓶壁形成薄膜,用25℃真空干燥箱干燥过夜,加入0.1mtris-hcl(ph7.4):甘油:丙二醇(80:10:10)的混合液4ml,用全氟丙烷置换出空气,用银汞调和振荡器机械振动50s(30w),得到白色浑浊的微泡分散体系,加入pbs(ph7.4)后在转速是3500r/min的离心机上离心除去未配合的磷脂材料,得到生物素化的微泡的溶液。
3)载树舌多糖热敏脂质体-全氟丙烷微泡复合物递药系统的制备
向6ml生物素化的微泡的溶液(预先机械振动,使微泡分散均匀,呈白色混浊状)中加入0.5mg亲和素,在摇床上室温振摇15min,加入12ml含有载树舌多糖热敏脂质体的溶液,在摇床上于室温孵育15min,偶联反应完后离心除去未反应的亲和素,离心转速为3500r/min,得到载树舌多糖热敏脂质体-全氟丙烷微泡复合物。
实施例3
1)载树舌多糖热敏脂质体的制备
称取30mg二棕榈酰磷酯酰胆碱(dppc)、5mg单棕榈酰磷脂酰胆碱(mppc)、4mg二硬脂酰磷脂酰乙醇胺-聚乙二醇(dspe-mpeg2000)及4mg二硬脂酰磷脂酰乙醇胺-聚乙二醇-生物素(dspe-mpeg2000-biotin)溶于预先加入至50ml离心管内的2ml氯仿中,称取4mg树舌多糖溶于1ml蒸馏水中,得树舌多糖水溶液,将树舌多糖水溶液加入到溶有磷脂材料(即上述dppc、mppc、dspe-mpeg2000及dspe-mpeg2000-biotin)的氯仿中,冰浴条件下用探头超声乳化3min,形成乳白色的w1/o型初乳(即乳化液),将初乳加入到5ml蒸馏水中,冰浴条件下超声乳化3min形成w1/o/w2型复乳,超声功率均为150w;超声乳化后将复乳置于室温挥发除去有机溶剂(氯仿),得到淡黄色有乳光的脂质体混悬液,加水稀释到10ml,用0.4微米和0.2微米微孔滤膜过滤,用pbs(ph7.4)透析,每8小时换一次透析液,透析24小时,除去游离树舌多糖,得到含有载树舌多糖热敏脂质体的溶液,密封置于4℃冰箱保存。
2)全氟丙烷微泡的制备
称取50mg二棕榈酰磷酯酰胆碱(dppc)、1mg二硬脂酰磷脂酰乙醇胺-聚乙二醇(dspe-mpeg2000)及1mg二硬脂酰磷脂酰乙醇胺-聚乙二醇-生物素(dspe-mpeg2000-biotin)于50ml茄形瓶中,加入10ml氯仿溶解,用旋转蒸发仪在30℃下减压蒸发除去有机溶剂(氯仿),在瓶壁形成薄膜,用25℃真空干燥箱干燥过夜,加入0.1mtris-hcl(ph7.4):甘油:丙二醇(80:10:10)的混合液5ml,用全氟丙烷置换出空气,用银汞调和振荡器机械振动55s(30w),得到白色浑浊的微泡分散体系,加入pbs(ph7.4)在转速是3000r/min的离心机上离心除去未配合的磷脂材料,得到生物素化的微泡的溶液。
3)载树舌多糖热敏脂质体-全氟丙烷微泡复合物递药系统的制备
向6ml生物素化的微泡的溶液(预先机械振动,使微泡分散均匀,呈白色混浊状)中加入0.5mg亲和素,在摇床上室温振摇15min,加入12ml含有载树舌多糖热敏脂质体的溶液,在摇床上于室温孵育15min,偶联反应完后离心除去未反应的亲和素,离心转速为3000r/min,得到载树舌多糖热敏脂质体-全氟丙烷微泡复合物。
本发明采用多种表征方法考察所制备的载树舌多糖热敏脂质体-全氟丙烷微泡复合物作为递药系统的靶向温控释放药物的性能,具体如下(实施例1):
图1显示了激光粒径仪所测载树舌多糖热敏脂质体、全氟丙烷微泡、载树舌多糖热敏脂质体-全氟丙烷微泡的粒径分布。载树舌多糖热敏脂质体的平均粒径为163.2±17.1nm,多分散系数为0.183±0.052;全氟丙烷微泡的平均粒径为630±18nm,多分散系数为0.181±0.071;载树舌多糖热敏脂质体-全氟丙烷微泡的平均粒径为1510±100nm,多分散系数为0.025。
图2显示了倒置荧光显微镜下载树舌多糖热敏脂质体-全氟丙烷微泡复合物的显微结构。其中载树舌多糖热敏脂质体用罗丹明6g染色,激发出红色荧光,从图2中可以看出脂质体围绕在全氟丙烷微泡外围。
精密称取d-葡萄糖标准品于10ml容量瓶中,加入蒸馏水稀释,摇匀,定容,得浓度为1mg/ml的葡萄糖对照品溶液。精密吸取1mg/ml葡萄糖溶液,分别置于5ml的容量瓶中,加水稀释,摇匀,定容,配成溶度为0.03mg/ml、0.06mg/ml、0.09mg/ml、0.12mg/ml、0.15mg/ml的葡萄糖溶液,分别吸取1ml于比色管,精密加入1ml5%的苯酚溶液,及3ml的浓硫酸,在涡旋仪上摇匀,置于沸水中加热15min后,在冷水浴中冷却至室温,取出。于490nm波长处测定吸光度。以吸光度a为纵坐标,葡萄糖浓度c为横坐标,绘制标准曲线,得回归方程:a=6.814c-0.0508、r=0.9973,结果表明葡萄糖标准品在0.03-0.15之间线性关系良好。
包封率测定:取制备好的载树舌多糖热敏脂质体混悬液10ml,放入低温高速离心机中(12000r/min)离心30min,吸出上清液,取1ml,用蒸馏水稀释5倍后,取1ml溶液,加入1ml5%苯酚溶液,及3ml浓硫酸,在涡旋仪上摇匀,置于沸水中加热15min后,在冷水浴中冷却至室温,取出。于490nm波长处测定吸光度,带入标准曲线,计算上清液中树舌多糖含量。计算出包封率为82.4%。
载树舌多糖热敏脂质体体外释药:取载树舌多糖热敏脂质体混悬液2份,各2ml,置于透析袋中,分别测定在37℃和42℃的体外释放速度。加入10倍体积的pbs中透析。在0,10,20,30,40,80,120,150,180,210,270,340min处取样2ml,再补充同等体积的透析液,由苯酚-硫酸法于紫外分光光度计下测定体外水相中的药物浓度,平行测定三次,以时间为横坐标,药物释放百分比为纵坐标,脂质体体外热敏释放结果表明,在42℃时,300min内累计释药量达到90%以上;在37℃条件下,基本不释药。结论:载树舌多糖热敏脂质体能够在一定亚高温温场下释放药物,具有较好的温控特性。
将所制备的载树舌多糖热敏脂质体-全氟丙烷微泡复合物经兔耳缘静脉注入兔体内,在超声诊断仪超声造影模式下,可以在肝脏肿瘤中看到很明显的显影效果,超声击碎微泡,可释放载树舌多糖热敏脂质体,并且在脂质体中引入亲水材料聚乙二醇所制备的脂质体,可延长体内的循环时间,具有长循环特点。结论:全氟丙烷微泡能够在一定场强的超声波下爆破产生空化效应,打开局部血管内皮屏障。
总之,本发明所制得的载树舌多糖热敏脂质体-全氟丙烷微泡复合物递药系统能够利用微泡的靶向爆破和热敏脂质体的局部温控效应,实现药物在亚高温温场局部组织的高效释放,其对该类递药系统在提高药物(特别是水溶性多糖抗肿瘤药物)的生物利用度,并且降低热消融肿瘤的残留中应用具有重要的指导和借鉴价值,应用前景广泛。
- 还没有人留言评论。精彩留言会获得点赞!