双功能性融合蛋白及其用途的制作方法
本发明涉及双功能性融合蛋白,其中一抗c5抗体的重链与一血管内皮生长因子(vascularendothelialgrowthfactor,vegf)捕获物融合,或一抗血管内皮生长因子(vegf)抗体fab的重链与一抗c5抗体scfv片段融合。
背景技术:
在美国及其他先进国家,老年性黄斑部病变(age-relatedmaculardegeneration,amd)为老年人(>50岁)失明与视力障碍的主要原因(1)。85%的老年性黄斑部病变(amd)为干性(非渗出)形式,其中称为隐结的细胞碎片积聚在视网膜与脉络膜之间。在晚期干性老年性黄斑部病变(amd)中,发生中央地理萎缩,导致眼中心视力丧失。湿性(渗出性或新血管性)形式的老年性黄斑部病变(amd)为更严重的病变形式,其中异常血管(脉络膜新血管形成,choroidalneovascularization,cnv)从脉络膜穿过黄斑部后的布鲁赫膜长大,导致视力迅速丧失。近年来,越来越多的证据显示补体活化在老年性黄斑部病变(amd)的发病机制中具有重要的作用(2)。在隐结中已检测到高含量的补体蛋白。遗传研究证实老年性黄斑部病变(amd)风险与补体蛋白基因(包括因子h(cfh)、cfhr1、cfhr3、c2、c3、c5、因子b、因子i)的多型态相关。特别是,cfhy402h等位基因与老年性黄斑部病变(amd)风险高度相关。在老年性黄斑部病变(amd)患者的血浆中也发现补体活化产物的含量增加。因此,目前有几种补体抑制剂正被用于治疗老年性黄斑部病变(amd)的临床试验中。
补体系统为先天免疫系统的功能性效应子,其由许多血浆蛋白以及细胞膜蛋白组成。补体的活化导致一系列蛋白酶活化级联反应,触发细胞激素的释放与活化级联反应的放大。补体活化的最终结果为细胞杀伤膜攻击复合物(membraneattackcomplex,mac)的活化、由过敏毒素c3a与c5a引起的发炎反应,以及病原体的助噬作用。通过c5裂解启动的膜攻击复合物(mac)对消除入侵的病原体以及受损、坏死,以及凋亡的细胞非常重要。
对于补体系统,必须在抵御病原体以及避免过度发炎之间达到微妙的平衡(3)。许多发炎反应、自体免疫、神经变性以及感染性疾病已经显现出与补体活性过度有关。缺血/再灌注损伤的发病机制显示,补体活化可导致多种疾病引起发炎反应诱导的损伤,这些疾病包括急性心肌梗塞、中风、出血性与败血性休克,以及冠状动脉绕道手术的并发症(4)。补体途径似乎是许多自体免疫性疾病的主要诱因,包括全身性红斑性狼疮(5)、类风湿性关节炎、干癣、以及气喘(6)。补体活化还与阿兹海默症(7)以及其他神经退行性疾病,例如杭丁顿氏症、帕金森氏症,以及老年性黄斑部病变(amd)(8)的病理相关。
补体系统可通过三种不同的途径活化:典型途径、替代途径,以及凝集素途径(9)。所有这三种途径都通过关键的c3转化酶与c5转化酶蛋白酶复合物,它们分别裂解补体成分c3与c5。典型途径是通过c1q与抗体igm或igg结合而引发的,进而导致裂解补体成分c2与c4的c1复合物活化,进而产生c2a、c2b、c4a,以及c4b。然后,c4b与c2b形成典型途径c3转化酶,促进c3裂解为c3a与c3b。然后,c3b通过与c4bc2b结合形成c5-转化酶(c3-转化酶)。凝集素途径与c3转化酶下游的典型途径相同,并通过甘露糖结合凝集素(mannose-bindinglectin,mbl)与病原体表面上的甘露糖残基的结合而被活化。然后,与甘露糖结合凝集素(mbl)相关的丝氨酸蛋白酶masp-1与masp-2可以裂解c4与c2,形成与典型途径相同的c3转化酶。与典型及凝集素途径需要抗原的特异性免疫反应不同,替代途径是非特异性免疫反应,其在低含量下持续活化。c3自发水解产生c3a与c3b。c3b可结合因子b,然后在促进因子d的作用下将因子b裂解为ba与bb。可通过结合因子p(备解素,properdin)来稳定的c3bbb复合物为将c3裂解为c3a与c3b的替代途径的c3转化酶。c3b可加入c3bbb复合物形成c3bbbc3b复合物,该复合物为替代途径的c5转化酶。来自所有三个途径的c5-转化酶可将c5切割为c5a与c5b。然后,c5b募集并组装c6、c7、c7、c8以及多个c9分子以组装膜攻击复合物(mac)。这会在膜上形成一个洞或孔,进而杀死或破坏该病原体或细胞。
几种针对补体蛋白的单株抗体已被作为治疗剂(10)。依库珠单抗(eculizumab)为一种抗c5蛋白的人源化抗体,已于2007年被核准用于治疗阵发性夜间血红蛋白尿(paroxysmalnocturnalhemoglobinuria,pnh)(该专利将于2021年3月16日在美国到期,以及将于2020年5月1日在欧洲到期)。对依库珠单抗进行了系统测试以在临床上治疗老年性黄斑部病变(amd)。尽管在试验中耐受性良好,但依库珠单抗在临床上并未显著降低ga(一种老年性黄斑部病变(amd)的晚期形式)的生长速率。可能的解释为由于使用的依库珠单抗剂量低,或者依库珠单抗需要直接进行玻璃体内注射才能达到足够的功能含量。目前正在试验一些抗c5抗体,例如培克珠单抗(pexelizumab)以及特斯多鲁单抗(tesidolumab),以治疗地理萎缩、非感染性胰腺炎、渗出性黄斑部病变、非感染性后眼色素层炎,及/或老年性黄斑部病变。抗c5a(tnx-558)、因子d(tnx-234)、因子p,以及c3b的抗体已被开发并在各种疾病模型中进行评估。另外,以临床试验评估人类c5的适体抑制剂(arc1905)以及抗c3的13个氨基酸的环肽(compastatin)治疗老年性黄斑部病变(amd)的效用。
血管内皮生长因子(vascularendothelialgrowthfactor,vegf)为促进血管生成最重要的蛋白质之一,这是从现有的血管网络发育新血管的严格调控的过程(11)。人类血管内皮生长因子(vegf)基因家族包含5个成员:vegf-a、vegf-b、vegf-c、vegf-d,以及胎盘生长因子(placentalgrowthfactor,plgf)。另外,vegf-a、vegf-b,以及胎盘生长因子(plgf)的多种同工型通过替代rna剪接产生(12)。vegf-a为该家族的原型成员,也是被研究最多的成员。vegf-a已显示出刺激内皮细胞有丝分裂、促进细胞存活及增殖、诱导细胞迁移并增加微血管通透性的作用。血管内皮生长因子(vegf)家族的所有成员通过结合细胞表面血管内皮生长因子(vegf)受体(vegfrs)来刺激细胞反应。该vegfr受体为酪氨酸激酶受体,具有由7个类免疫球蛋白(immunoglobulin,ig)结构域所组成的细胞外区域。vegfr-1(flt-1)结合vegf-a、-b,以及胎盘生长因子(plgf),并可作为血管内皮生长因子(vegf)的诱饵受体或vegfr-2的调节剂。vegfr-2(kdr/flk-1)结合所有血管内皮生长因子(vegf)同工型,且为血管内皮生长因子(vegf)诱导的血管生成信息的主要媒介。vegfr-3(flt-4)结合vegf-c与vegf-d,但不结合vegf-a,并作为淋巴管生成的主要媒介。
在发育及正常的生理过程,例如伤口愈合及月经周期,中需要血管生成,且血管生成已被证明与许多疾病的发病机制有关,包括老年性黄斑部病变(amd)、ra、糖尿病视网膜病变、肿瘤生长及转移。抑制血管生成已显示在治疗应用中是有效的。fda已核准了几种针对vegf-a的抑制剂。例如,针对vegf-a的人源化抗体(avastin)、针对vegf-a的抗体fab片段(lucentis),以及血管内皮生长因子(vegf)陷阱(eylea)。avastin被核准用于治疗转移性大肠癌(metastaticcolorectalcancer,mcrc)、非小细胞肺癌(non–smallcelllungcancer,nsclc)、神经胶质母细胞瘤(glioblastoma,gbm),以及转移性肾癌(metastatickidneycancer,mrcc)。lucentis与eylea被核准用于治疗湿性老年性黄斑部病变(amd)。许多其他抗血管内皮生长因子(vegf)分子,例如brolucizumab、varisacumab,以及conbercept目前正在临床开发阶段。
技术实现要素:
本发明的目的为通过更有效地同时抑制补体及血管内皮生长因子(vegf)途径来开发能够治疗多种补体及血管内皮生长因子(vegf)相关的疾病,例如老年性黄斑部病变(amd)等的治疗剂,进而解决上述问题,结果发现,同时以补体及血管内皮生长因子(vegf)为标靶的双功能性融合蛋白有效地表现出抗补体及抗血管内皮生长因子(vegf)的功效。
本发明提供了抑制补体信息传递途径以及血管内皮生长因子(vegf)信息传递途径的融合蛋白,其中该融合蛋白包含一补体结合域以及一血管内皮生长因子(vegf)结合域。
于一实施例,本发明提供一种双功能性融合蛋白,包含一或多个含有c5结合基序的片段以及一或多个含有血管内皮生长因子(vegf)结合基序的片段,其与一短的柔性连接子融合,进而在同时抑制补体及血管生成方面提供显著改善的功效。
于一具体实施例中,本发明提供一种双功能性融合蛋白c5v,其同时以补体及血管内皮生长因子(vegf)为标靶,并同时提供一补体c5切割阻断活性以及一抗血管生成功效,其中c5为一补体c5结合基序,例如依库珠单抗的重链;v为一血管内皮生长因子(vegf)结合基序,例如vegfr1ecdd2以及vegfr2ecdd3,或其嵌合结构域;以及在它们之间插入一个短的柔性gs连接子,以确保每个结构域的正确折迭以及最小的立体阻碍。
于另一具体实施例中,本发明提供一种双功能性融合蛋白vc5,其同时以补体及血管内皮生长因子(vegf)为标靶,并同时提供一补体c5切割阻断活性以及一抗血管生成功效,其中v为一血管内皮生长因子(vegf)结合基序,例如雷珠单抗(ranibizumab)fab的重链;c5为一补体c5结合基序,例如依库珠单抗的scfv;以及在该重链与scfv之间放置的一短的柔性gs连接子。
于另一具体实施例中,本发明提供一种用于治疗补体及血管内皮生长因子(vegf)相关疾病的双功能性融合蛋白。
因此,本发明还提供一种药物组合物,包含本发明的双功能性融合蛋白以及一药学上可接受的载体。
于一具体实施例中,该药物组合物可用于治疗补体及血管内皮生长因子(vegf)相关疾病。
此外,本发明提供一种在一有需要的受试者中治疗一补体及血管内皮生长因子(vegf)相关疾病的方法,该方法包括对该受试者施用一治疗有效量的本文公开的双功能性融合蛋白。
于一具体实施例中,本文公开的补体及血管内皮生长因子(vegf)相关疾病选自由下列所组成的群组:动脉粥状硬化、老年性黄斑部病变、急性心肌梗塞(acutemyocardialinfarction,ami)、肾小球性肾炎、气喘、血栓形成、深层静脉栓塞、多发性硬化症、阿兹海默症、自体免疫性眼色素层炎、全身性红斑性狼疮(systemiclupuserythematosus,sle)、狼疮性肾炎、溃疡性结肠炎、发炎性肠病、克罗恩病、成人呼吸窘迫症候群(adultrespiratorydistresssyndrome,ards)、多发性硬化症、糖尿病、杭丁顿氏症、帕金森氏症、类风湿关节炎、青少年期的类风湿关节炎、骨关节炎、牛皮癣性关节炎、中枢神经系统发炎性疾病、重症肌无力症、肾小球性肾炎,以及自体免疫性血小板减少症、动脉瘤、非典型溶血性尿毒症症候群、自然流产、复发性流产、外伤性脑损伤、干癣、自体免疫性溶血性贫血、遗传性血管性水肿、中风、失血性休克、败血性休克、例如冠状动脉绕道手术(coronaryarterybypassgraft,cabg)等手术带来的并发症、肺部并发症,例如慢性阻塞性肺脏疾病(chronicobstructivepulmonarydisease,copd)、缺血再灌注损伤、器官移植排斥反应、多器官衰竭以及癌症。较佳地,该补体及血管内皮生长因子(vegf)相关的疾病为老年性黄斑部病变以及癌症。更佳地,该补体及血管内皮生长因子(vegf)相关疾病为老年性黄斑部病变。
于以下的描述中阐述了本发明的一或多个实施例的细节。从以下附图以及数个具体实施例的详细描述以及从所附申请专利范围,本发明的其他特征或优点将变得显而易见。
附图说明
当结合附图阅读时,将更好地理解前述发明内容及下述本发明的实施方式。出于说明本发明的目的,图式显示了目前较佳的具体实施例。
在图式中:
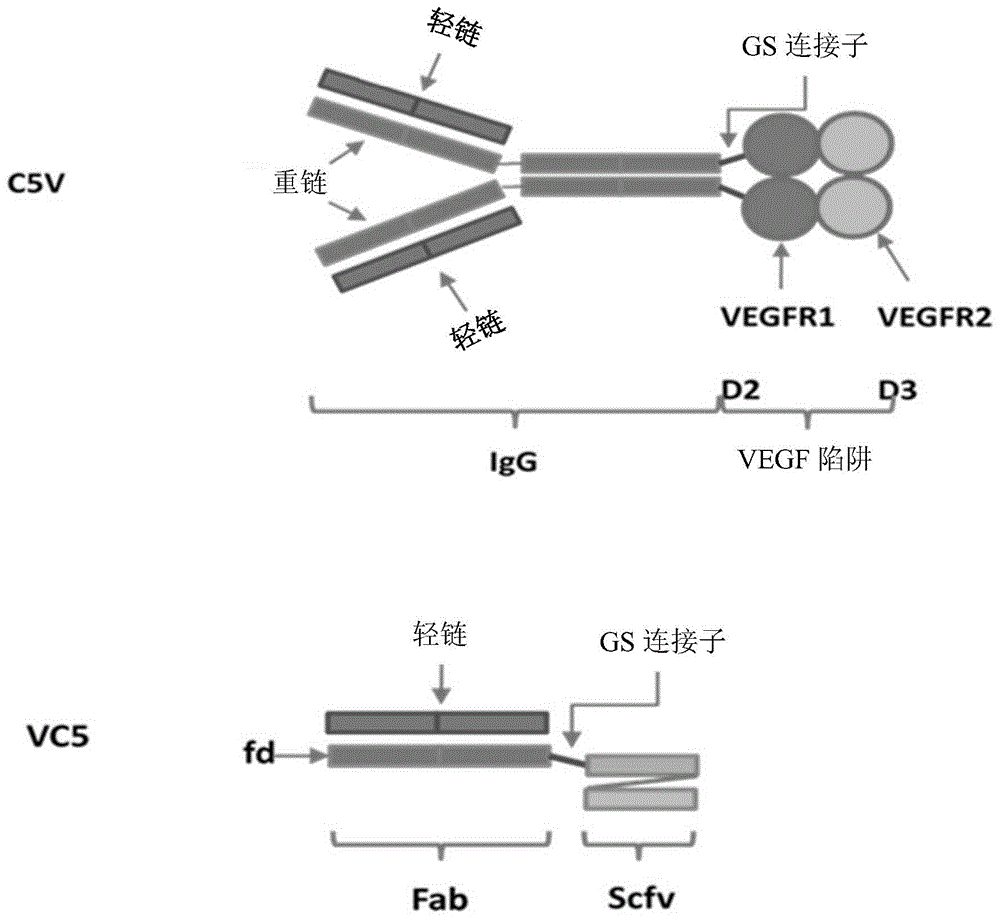
图1为同时具有补体c5切割阻断活性以及血管内皮生长因子(vegf)抑制活性的双功能性融合蛋白的示意图。该双功能性融合蛋白c5v为通过将一血管内皮生长因子(vegf)抑制基序融合于依库珠单抗的重链的c端而产生。该构筑中使用的血管内皮生长因子(vegf)结合基序包含vegfr1d2以及vegfr2d3嵌合结构域(专利将于2020年在美国到期,于2021年在欧洲到期)。该双功能性融合蛋白vc5为通过将来自lucentis的fab的重链fd链(lucentis的专利将于2020年6月在美国和2022年在欧洲到期[1])融合于依库珠单抗(scfv)的c端而产生。这二种融合蛋白均在功能实体之间包含一短的gs连接子,以确保柔韧性及折迭性。
图2a及2b分别为纯化的双功能性融合蛋白c5v与vc5的sds-page凝胶分析。在每个泳道中载入2μg蛋白质。泳道1为非还原条件;泳道2为还原条件。
图3为使用纯化的双功能性融合蛋白的补体c5的直接体外结合。洗涤后,以针对c5v的hrp偶联的山羊抗人类iggfc特异性抗体或针对vc5的hrp偶联的山羊抗人fab特异性抗体检测结合的蛋白。
图4所示为血管内皮生长因子(vegf)与纯化的双功能性融合蛋白的直接体外结合。洗涤后的结合蛋白以针对c5v的hrp偶联的山羊抗人类iggfc特异性抗体以及针对vc5的hrp偶联的山羊抗人类fab特异性抗体检测。
图5为溶液中双功能性融合蛋白对vegf-a的亲和力评估。在溶液中双功能性融合蛋白与血管内皮生长因子(vegf)培养过夜后,通过三明治elisa分析确定游离的血管内皮生长因子(vegf)的浓度。
图6为纯化的双功能性融合蛋白对替代补体途径的抑制。正常人类血清首先与各种浓度的双功能性融合蛋白一起培养,然后在5mmmg2+以及5mmegta存在下用以裂解兔红血球。通过在412nm波长处测量吸亮度来检测溶血。
图7为人类脐静脉内皮细胞(huvecs)生长抑制试验的结果。人类脐静脉内皮细胞(huvecs)维持在含有2%fbs的内皮细胞生长培养基(lonza公司)中。将96孔平底微量滴定盘涂覆胶原蛋白,然后与50μl1nm的vegf-a(r&d系统公司,美国)以及各种浓度的融合蛋白一起培养。于37oc、5%co2中培养72小时后,通过对每个孔中添加10μlmts检测试剂(promega公司,美国),然后在450/650nm波长处测量吸亮度,以分析细胞增殖。
图8所示为双功能性融合蛋白c5v对血管内皮生长因子(vegf)诱导的人类脐静脉内皮细胞(huvecs)血管形成的抑制作用。内皮网络形成的量化是通过imagej血管生成系统(5张影像/样本)进行的,表示为相较于以血管内皮生长因子(vegf)处理的倍数变化。
图9所示为双功能性融合蛋白c5v对血管内皮生长因子(vegf)诱导的内皮细胞入侵的抑制作用。
图10a与10b所示为双功能性融合蛋白c5v对小鼠的雷射诱导的脉络膜新血管形成(choroidalneovascularization,cnv)的抑制。图10a表示雷射诱导的脉络膜新血管形成(cnv)模型中的血管渗漏。图10b表示雷射诱导的脉络膜新血管形成(cnv)损伤的定量。
具体实施方式
应当理解的是,本发明不限于所描述的特定方法及实验条件,因为这样的方法及条件是可以变化的。
还应理解的是,本文中使用的术语仅出于描述特定具体实施例的目的,而无意用于限制本发明,因为本发明的范围将仅由所附申请专利范围所限制。
除非本文另有定义,否则本文使用的科学及技术术语具有本领域普通技术人员通常理解的含义。
如本文所使用,不定冠词「一」以及「一个」以及定冠词「该」目的在于包括单数及复数,除非使用它们的上下文另外明确指出。
于某些实施例,本发明涉及同时以补体c5以及血管内皮生长因子(vegf)途径为标靶的双功能性融合蛋白。由于该补体及血管内皮生长因子(vegf)途径与许多疾病有关,包括老年性黄斑部病变(amd),因此相较于补体及血管内皮生长因子(vegf),具有双特异性抑制活性的蛋白可能会提供比分别抑制补体或血管内皮生长因子(vegf)的蛋白显著更好的治疗效果。于本发明中,该双功能性融合蛋白可为双功能性融合蛋白c5v,其通过将一抗-c5抗体的重链,在其c端与一含有vegfr1胞外结构域2以及vegfr2细胞外结构域3的血管内皮生长因子(vegf)抑制基序融合而产生。于另一方面,该双功能性融合蛋白可为双功能性融合蛋白vc5,其通过将一抗血管内皮生长因子(vegf)抗体fab的fd链,在其c端与一抗-c5抗体scfv片段融合而产生。已显示该双功能性融合蛋白c5v与vc5能够以高亲和力结合补体c5蛋白以及血管内皮生长因子(vegf),还能够分别在基于细胞的测定中抑制该补体及血管内皮生长因子(vegf)途径的功能。该双功能性融合蛋白包含人类蛋白的结构域,且皆为人类来源的,并且预期为非免疫原性的,因此,有可能被进一步开发为用于治疗涉及补体及血管生成的疾病的疗法。
如本文所用,术语「融合蛋白」指通过二个或更多个结合蛋白或基序或编码不同基因的胜肽/氨基酸片段的连接而产生的蛋白,该些基因的转译导致单个或多个衍生自每个原始蛋白质的具有多功能特性的多胜肽。一融合蛋白可包括偶联至一抗体的蛋白、偶联至一不同抗体的抗体,或偶联至一fab片段的抗体。
如本文所用,术语「补体」指补体级联反应的任何小蛋白,有时在文献中称为补体系统或补体级联。补体的活化导致一系列蛋白酶活化级联反应,进而触发细胞激素的释放以及活化级联反应的放大,进而导致细胞杀伤性膜攻击复合物(mac)的活化、由过敏毒素c3a与c5a引起的发炎反应,以及病原体的助噬作用。通过c5裂解启动的膜攻击复合物(mac)对消除入侵的病原体以及受损、坏死,以及凋亡的细胞非常重要。
如本文所用,术语「fab」指抗体上与抗原结合的区域。其由轻链的可变及恒定结构域以及重链抗体的可变结构域以及第一恒定结构域所组成。
如本文所用,术语「连接子」指一氨基酸残基或片段,或包含通过胜肽键连接的二个或更多个氨基酸残基的多胜肽,该胜肽键用于连接二个胜肽、多胜肽或蛋白质。该连接子可为一fc片段,其为一野生型的免疫球蛋白fc区或任何其人类免疫球蛋白同种型、亚类或同种型的变体。
如本文所用,术语「scfv」指由重链(vh)以及轻链(vl)的可变区组成的单链片段变体,其通过一柔性胜肽连接子连接在一起,其可以功能形式容易地在大肠杆菌中表现,可进行蛋白质工程改造以改善scfv的特性,例如增加亲和力及改变特异性。
于本发明中,可使用具有阻断血管内皮生长因子(vegf)活性的任何基序、胜肽、蛋白质或片段,例如抗血管内皮生长因子(vegf)抗体、血管内皮生长因子(vegf)陷阱,或血管内皮生长因子(vegf)受体(vegfr)胞外ig结构域,例如d1-d7,特别是vegfr1胞外ig结构域2(ecd、d2)、vegfr2胞外ig结构域3(ecd、d3)。
于本发明中,可使用与补体c5结合的任何基序、胜肽、蛋白质或片段,例如依库珠单抗的重链或scfv。
由于补体及血管内皮生长因子(vegf)涉及多种疾病,例如老年性黄斑部病变(amd),以同时阻断补体c5的裂解以及血管内皮生长因子(vegf)活性,因此在本发明中产生了针对补体c5与血管内皮生长因子(vegf)的双功能性融合蛋白以对其进行治疗。
于本发明的一具体实施例中,具有依库珠单抗的重链的片段用于产生在其c端具有血管内皮生长因子(vegf)捕获物的双功能性融合蛋白c5v(seqidno:1),其中在其之间插入一短的柔性gs连接子(seqidno:3)以确保每个结构域的正确折迭以及最小的空间立体阻碍。于相关具体实施例中,该c5v融合蛋白包含与seqidno:1具有至少约45%,约50%,约55%,约60%,约65%,约70%,约75%,约80%,约85%,约90%,约95%,或约99%的同一性的氨基酸序列。
较佳地,该双功能性融合蛋白c5v的该血管内皮生长因子(vegf)捕获物包含vegfr1ecdd2以及vegfr2ecdd3。
于本发明的另一具体实施例中,将一含有雷珠单抗fab的重链的片段与一补体c5结合基序的c端融合,以构筑具有一介于其中间的短的柔性gs连接子(seqidno:3)的双功能性融合蛋白vc5(seqidno:2),以确保正确折迭及最小化立体阻碍。在相关具体实施例中,该双功能性融合蛋白vc5包括与seqidno:2具有至少约45%,约50%,约55%,约60%,约65%,约70%,约75%,约80%,约85%,约90%,约95%,或约99%同一性的氨基酸序列。
特别地,该双功能性融合蛋白vc5的该补体c5结合基序包含依库珠单抗的scfv片段。
于另一具体实施例中,于本发明中描述的所有融合蛋白由用于表现蛋白的胞外分泌的信号胜肽(seqidno:4)引导。
该双功能性融合蛋白c5v及vc5的所得序列分别示于seqidno:1以及seqidno:2。
于本发明中,上述双功能性融合蛋白c5v及/或vc5由hek293细胞瞬间表现,并通过蛋白g色层分析法从转染的细胞培养上清液中纯化。发现在一步纯化过程中获得了纯度大于90%的产物,且所有融合蛋白都被正确地形成及表现。
于本发明的一具体实施例中,该双功能性融合蛋白c5v或vc5与补体c5的结合能力通过elisa结合测定法得以验证。于某些具体实施例中,该双功能性融合蛋白c5v或vc5表现出与补体c5蛋白的强结合,分别具有ec503.57nm以及2.77nm。
于本发明的另一具体实施例中,该双功能性融合蛋白c5v或vc5与血管内皮生长因子(vegf)的结合能力通过使用elisa结合测定法来验证。于某些具体实施例中,该双功能性融合蛋白c5v或vc5表现出与vegf-a蛋白的强结合,分别为ec50为0.288nm以及1.675nm。
于本发明的另一具体实施例中,该双功能性融合蛋白c5v与溶液中的血管内皮生长因子(vegf)的结合亲和力通过竞争结合测定法确定。于本发明中,该c5v融合蛋白与vegf-a蛋白以高亲和力结合,且c5v对vegf-a蛋白的结合亲和力比eylea更高。
本领域已知且本文所述的测定(例如,实例2-7)可用于鉴定及测试本发明的双功能性融合蛋白c5v或vc5的生物学活性。于一些具体实施例中,提供用于测试双功能性融合蛋白c5v或vc5抑制补体途径及血管内皮生长因子(vegf)依赖性人类脐静脉内皮细胞(huvecs)增殖的能力的测定法。
本发明的某些实施例涉及该双功能性融合蛋白c5v或vc5对替代补体途径的抑制活性。具体而言,将该双功能性融合蛋白c5v或vc5与正常人类血清一起作用,以在mg2+及egta存在的情况下抑制兔红血球的溶解。于本发明的某些具体实施例中,c5v及vc5引起的红血球溶血的ic50分别为25.31nm以及36.65nm。
此外,可通过测量血管内皮生长因子(vegf)依赖性人类脐静脉内皮细胞(huvecs)生长来描述血管内皮生长因子(vegf)活性的特征。根据某些具体实施例,将双功能性融合蛋白c5v或vc5以及vegfa加载到预包覆胶原蛋白的孔中,然后于其中培养人类脐静脉内皮细胞(huvecs)。培养后,通过mts测定法分析该细胞的生长,c5v与vc5的ic50分别为0.195nm以及0.313nm。
因此,于一实施例,本发明提供了一种药物组合物,包含本发明的双功能性融合蛋白以及一药学上可接受的载体。
于一些具体实施例中,本发明提供一种用于抑制补体途径的药物组合物。于一些具体实施例中,本发明提供一种用于抑制血管内皮生长因子(vegf)信息传递途径的药物组合物。于一些具体实施例中,本发明提供一种用于在一受试者中抑制补体活化及血管内皮生长因子(vegf)信息传递途径的药物组合物,其包括对该受试者施用一有效量的该融合蛋白以抑制补体活化及血管内皮生长因子(vegf)信息传递途径。
于一些具体实施例中,该药物组合物可用于治疗一补体及/或血管内皮生长因子(vegf)相关疾病,包括但不限于,动脉粥状硬化、黄斑部病变(例如,老年性黄斑部病变)、急性心肌梗塞(acutemyocardialinfarction,ami)、肾小球性肾炎、气喘、血栓形成、深层静脉栓塞、多发性硬化症、阿兹海默症、自体免疫性眼色素层炎、全身性红斑性狼疮(systemiclupuserythematosus,sle)、狼疮性肾炎、溃疡性结肠炎、发炎性肠病、克罗恩病、成人呼吸窘迫症候群(adultrespiratorydistresssyndrome,ards)、多发性硬化症、糖尿病、杭丁顿氏症、帕金森氏症、类风湿关节炎、青少年期的类风湿关节炎、骨关节炎、牛皮癣性关节炎、中枢神经系统发炎性疾病、重症肌无力症、肾小球性肾炎,以及自体免疫性血小板减少症、动脉瘤、非典型溶血性尿毒症症候群、自然流产、复发性流产、外伤性脑损伤、干癣、自体免疫性溶血性贫血、遗传性血管性水肿、中风、失血性休克、败血性休克、例如冠状动脉绕道手术(coronaryarterybypassgraft,cabg)等手术带来的并发症、肺部并发症,例如慢性阻塞性肺脏疾病(chronicobstructivepulmonarydisease,copd)、缺血再灌注损伤、器官移植排斥反应、多器官衰竭以及癌症。于一些具体实施例中,可通过本文所述的融合蛋白治疗或预防的癌症包括结肠直肠癌、转移性结直肠癌、非小细胞肺癌、淋巴瘤、白血病、腺癌、胶质母细胞瘤、肾癌、转移性肾癌、胃癌、前列腺癌、视网膜母细胞瘤、卵巢癌、子宫内膜癌,以及乳癌。
于一些具体实施例中,该药物组合物可用于治疗眼病,包括但不限于湿性老年性黄斑部病变、干性黄斑部病变、糖尿病性视网膜病变、糖尿病性视网膜水肿、糖尿病性黄斑部水肿、视网膜后纤维化、视网膜中央闭塞、视网膜静脉阻塞、缺血性视网膜病变、高血压性视网膜病、眼色素层炎(例如,前、中、后或全葡萄膜炎)、白塞病(behcet'sdisease)、bietti晶体营养不良、睑缘炎、青光眼(例如,开角型青光眼)、新生血管性青光眼、角膜新生血管、脉络膜新血管形成(cnv)、视网膜下新生血管形成、角膜发炎,以及角膜移植并发症。
于各种具体实施例中,与补体及血管生成有关的疾病可为老年性黄斑部病变(amd)。
如本文所用,术语「老年性黄斑部病变(amd)」为一种严重的眼部疾病,模糊了「直向」活动,例如,阅读、缝纫,以及驾驶,所需的清晰中央视力。通常,老年性黄斑部病变(amd)影响黄斑部,其为眼睛的一部分。大多数老年性黄斑部病变(amd)为干燥形式,细胞碎片堆积在视网膜与脉络膜之间。在晚期干性老年性黄斑部病变(amd)中,发生中央地理萎缩,导致眼中心视力丧失。湿性老年性黄斑部病变(amd)为更严重的形式,异常血管(脉络膜新血管形成,cnv)从脉络膜穿过黄斑后的布鲁赫膜长大。这些血管将血液及液体泄漏到视网膜中,导致视力失真,使直线看起来呈波浪形,并造成盲点及中枢视力丧失。这些异常的血管最终会结疤,导致永久性中央视力丧失。
根据本发明的药物组合物可配制为单独包含该双功能性融合蛋白或与药学上可接受的载体一起的合适形式,并可进一步包含一赋形剂或一稀释剂。该载体可为溶剂、分散介质、等渗剂等。该载体可为液体、半固体或固体载体。于一些具体实施例中,该载体可为水、盐溶液或其他缓冲液(例如,血清白蛋白以及明胶)、碳水化合物(例如,单醣、二糖,以及其他碳水化合物,包括葡萄糖、蔗糖、海藻糖、甘露糖、甘露醇、山梨糖醇,或糊精)、凝胶、脂质、脂质体、树脂、多孔基质、黏合剂、填料、涂料、稳定剂、防腐剂、抗氧化剂(包括抗坏血酸以及甲硫氨酸)、螯合剂(例如,edta)、成盐的抗衡离子(例如,钠)、非离子界面活性剂[例如tweentm、pluronicstm,或聚乙二醇(polyethyleneglycol,peg)]或其组合。
本发明的药物组合物可通过任何方法施用于包括人类在内的哺乳动物。例如,本发明的组合物可口服或局部给药。局部给药可为但不限于静脉内、肌肉内、动脉内、髓内、硬膜内、心内、透皮、皮下、腹膜内、鼻内、肠、外用、舌下,或直肠给药。
该药物组合物可包含一种以上的用于预防或治疗补体及/或血管内皮生长因子(vegf)相关疾病的另外的有益化合物。
于一些具体实施例中,该药物组合物可包含一种以上用于治疗该待治疗疾病或病症的另外的治疗剂。例如,该附加剂可为一抗血脂异常剂、一ppar-α激动剂、一ppar-β激动剂、一ppar-γ激动剂,一抗类淀粉蛋白剂、一脂褐素的抑制剂、一视光周期调节剂、一抗氧化剂、一神经保护剂、一凋亡抑制剂、一坏死抑制剂、一c反应蛋白抑制剂、一发炎反应小体抑制剂、一抗发炎药、一免疫抑制剂、一基质金属蛋白酶的调节剂、一补体系统或组成分的抑制剂,以及一抗血管生成剂。
通过以下实例进一步说明本发明,但不应将其解释为进一步的限制。
实施例1抑制补体及血管内皮生长因子(vegf)途径的双功能性融合蛋白的表现及纯化
具有结合并抑制补体c5裂解活性的抗体或抗体片段可作为补体活化阻断剂。抗血管内皮生长因子(vegf)抗体片段或血管内皮生长因子(vegf)捕获物可作为血管内皮生长因子(vegf)抑制基序。合成cdna并用于产生双菜单现载体。补体c5裂解阻断剂可置于血管内皮生长因子(vegf)抑制基序的n端或c端的任一端,如图1所示。融合蛋白在功能实体之间包含一个gs连接子,并在n端带有一信号胜肽,以分泌出细胞。纯化的表现载体用于瞬间转染hek293细胞,作用96小时后收获细胞培养基,并通过proteing层析纯化。在还原及非还原条件下对2μg纯化的双功能性融合蛋白进行page分析(图2a及2b)。在两种情况下,第一步纯化的纯度皆大于90%。
实施例2双功能性融合蛋白与补体c5及血管内皮生长因子(vegf)的体外结合
为了在elisa中测试纯化的融合蛋白与补体c5或血管内皮生长因子(vegf)的直接结合,将c5或vegf-a预包覆的孔(100ng/孔)与0-30nm的纯化蛋白培养1小时。洗涤后,将1:2500稀释的hrp结合的抗人类fc抗体(jacksonimmunochemicals公司,美国)添加到每个孔中,再培养1小时。最终洗涤后,加入tmb试剂(thermofisher公司,美国)并测量在波长450nm处的吸亮度,并使用prism4软件通过s型曲线拟合分析数据。如图3所示,双功能性融合蛋白c5v与vc5分别以ec503.57nm以及2.77nm表现出与c5的强结合。双功能性融合蛋白c5v与vc5还表现出与vegf-a的强结合,ec50分别为0.288nm以及1.675nm(图4)。
为了更好地评估溶液中融合蛋白与血管内皮生长因子(vegf)的结合亲和力,将5pmvegf-a(r&dsystems公司)与0-100pm纯化蛋白培养过夜。第二天,使用dev00试剂盒(r&dsystems公司,美国)测定游离的血管内皮生长因子(vegf)的浓度。相应地,通过s形曲线拟合来分析数据。如图5所示,双功能性融合蛋白c5v以高亲和力与vegf-a蛋白结合,相较于eylea,c5v对vegf-a蛋白具有更高的结合亲和力。
实施例3双功能性融合蛋白c5v与vc5对替代补体途径的抑制
补体替代途径的活化仅需要mg2+,而典型与凝集素补体途径则需要ca2+以及mg2+离子。因此,当测定中包括5mm的mg2+以及5mm的egta时,可在典型途径蛋白存在下测定替代补体活性,其中egta优先螯合ca2+。溶血分析可用于评估融合蛋白对替代补体活化的抑制作用。于该实验中,在37oc培养30分钟后,首先确定了90%的1.25x107个兔红血球/ml(er,补体科技公司)裂解的正常人类血清稀释度(comptech公司,美国)。在含有5mmmgcl2以及5mmegta的gvb0缓冲液(0.1%明胶,5mmveronal,145mmnacl,0.025%nan3,ph7.3)中进行测定。通过将可裂解90%的er的正常人类血清稀释液与0-500nm的纯化融合蛋白c5v以及vc5在37oc下混合1小时,开始抑制替代补体途径。然后在血清与er培养30分钟后测定er的溶血程度。使用prism4分析数据。图6中的结果显示,对于补体替代途径,双功能性融合蛋白c5v以及vc5的ic50分别为25.31nm以及36.65nm。
实施例4血管生成阻断剂对血管内皮生长因子(vegf)依赖性人类脐静脉内皮细胞(huvecs)增殖测定的抑制
纯化的双功能性融合蛋白c5v与vc5在细胞碱基测定中用于抑制血管内皮生长因子(vegf)活性。人类脐静脉内皮细胞(humanumbilicalveinendothelial,huvec细胞,lonza公司,美国)通常用于证明可被血管内皮生长因子(vegf)阻断剂抑制的血管内皮生长因子(vegf)依赖性细胞增殖。在该实验中,人类脐静脉内皮细胞(huvecs)维持在含有2%fbs的内皮细胞生长培养基(lonza公司,美国)中。将50μl的lnmvegf-a(r&dsystems公司)以及各种浓度的c5v或vc5加到以胶原蛋白预包覆的孔中,在37oc下作用1小时,然后在每个孔中加入含有1x105个人类脐静脉内皮细胞(huvecs)/ml的培养基199(10%fbs,hyclone公司,美国)50μl。于37oc及5%co2下培养72小时后,通过对每个孔中添加10μlmts检测试剂(promega公司,美国),然后在波长450/650nm下测量吸亮度以分析细胞的生长。如图7所示,该双功能性融合蛋白c5v或vc5表现出良好的抑制血管内皮生长因子(vegf)依赖性人类脐静脉内皮细胞(huvecs)增殖的能力,ic50分别为0.195nm以及0.313nm。
实施例5双功能性融合蛋白c5v抑制血管内皮生长因子(vegf)诱导的内皮细胞管形成
为了检查c5v在血管生成中的功能,在人类脐静脉内皮细胞中进行了体外matrigel管形成分析。将人类脐静脉内皮细胞(huvecs)在无血清的基础培养基中培养2小时,然后通过accutase进行胰蛋白酶消化。将4x103个人类脐静脉内皮细胞(huvecs)接种到含有血管内皮生长因子(vegf)(1μg/ml)以及eylea(100μg/ml)或c5v蛋白(100μg/ml)的matrigel预包覆的孔中,于37℃下静置4.5小时。通过imagej血管生成系统(5张影像/样本)对内皮网络的形成进行定量。
在血管内皮生长因子(vegf)处理下,当在matrigel上培养4.5小时后,人类脐静脉内皮细胞(huvecs)显示出主要的血管管状网络。但是,双功能性融合蛋白c5v破坏了管状结构的形成(图8a及8b)。
实施例6双功能性融合蛋白c5v抑制血管内皮生长因子(vegf)诱导的内皮细胞入侵
通过transwell分析检查了该双功能性融合蛋白c5v对血管内皮生长因子(vegf)刺激的入侵作用。根据制造商的说明,通过以matrigel基底膜基质(bdbiosciences公司,圣地亚哥,加州,美国)预涂覆transwell插入物以进行入侵测定。将具有培养基199的人类脐静脉内皮细胞(huvecs)(2x105个)放在上部孔中。将配体人类血管内皮生长因子(vegf)(0.2μg/ml)与eylea(2μg/ml)或c5v(2μg/ml)分别在底部室中混合。将transwell盘在5%培养箱中培养24小时,以使来自上部孔的细胞向底部室迁移。然后将膜插入物固定并以1%结晶紫染色。通过显微镜观察黏附在膜插入物下表面的细胞,并使用imagej软件计算迁移细胞的平均数目。
如图9a及9b所示,该双功能性融合蛋白c5v显著抑制了血管内皮生长因子(vegf)诱导的人类脐静脉内皮细胞(huvecs)的入侵。
实施例7双特异性蛋白c5v在雷射诱导的脉络膜新血管形成(cnv)小鼠模型中抑制新血管的形成
血管内皮生长因子(vegf)与c5似乎与病理性新血管形成以及血管通透性密切相关,这是眼部新血管疾病的标志。较高的c5含量还与人类湿性老年性黄斑部病变(amd)以及发炎反应中的疾病严重程度相关。我们创造了一个以血管内皮生长因子(vegf)以及c5为共同标靶的创新设计。我们通过雷射诱导的脉络膜新血管形成小鼠模型测试了双特异性蛋白c5v对血管生成的影响。在雷射诱导的脉络膜新血管形成(cnv)模型中,在第1天对雄性c57bl/6小鼠的右眼玻璃体内注射载体对照,eylea(40μg)或c5v(40μg)(n=5只/组)。雷射对bruch氏膜造成的损害在雷射施用部位被发现有气泡。为了进行眼底荧光血管造影(fundusfluoresceinangiography,ffa)分析,向麻醉的动物腹膜内注射5%荧光素钠。使用microniii视网膜成像显微镜(凤凰研究实验室,圣拉蒙,加州,美国)捕获影像。在雷射后21天获取光同调断层扫描(opticalcoherencetomography,oct)图像,并以椭圆体形式测量新血管病变体积。椭圆体体积以公式v=4/3πabc计算,其中a(宽度),b(深度)以及c(长度)为椭圆体的水平面或垂直平面的半径。
如图10a所示,该双功能性融合蛋白c5v减少了雷射诱导的脉络膜新血管形成(cnv)模型中的血管渗漏(图10a)。通过光同调断层扫描(oct)量化雷射脉络膜新血管形成(cnv)病变为椭球体后,显示该双功能性融合蛋白c5v处理后病变体积显著减少(图10b)。
尽管已经通过较佳实施方式公开了本发明,但并非意图限制本发明。在不脱离本发明的精神及范围的情况下,本领域的普通技术人员可被允许进行修改及修饰。因此,本发明的保护范围应由所附申请专利范围所限定。
参考书目
1.bird,a.c.,“therapeutictargetsinage-relatedmaculardisease”,2010,j.clin.invest.,120(9):3033–3041
2.issa,p.c.,etal,“thesignificanceofthecomplementsystemforthepathogenesisofage-relatedmaculardegeneration—currentevidenceandtranslationintoclinicalapplication”,2011,graefes.arch.clin.exp.ophthalmol.,249:163–174
3.ricklin,d.,etal.,“complement-targetedtherapeutics”,2007,naturebiotechnology,25(11):1265–1275
4.markiewski,m.m.,etal,“theroleofcomplementininflammatorydiseases—frombehindthescenesintothespotlight”,2007,am.j.pathol.171:715–727
5.manderson,a.p.,etal,“theroleofcomplementinthedevelopmentofsystemiclupuserythematosus”,2004,annul.rev.immunol.22:431–456
6.guo,r.f.,etal,“roleofc5aininflammatoryresponses”,2005,annul.rev.immunol.23:821–852
7.bonifati,d.m.,etal,“roleofcomplementinneurodegenerationandneuroinflammation”,2007,mol.immunol.44:999–1010
8.gehrs,k.m.,“complement,age-relatedmaculardegenerationandavisionofthefuture”,2010,arch.ophthalmol.,128(3):249–258
9.wagner,e.,etal.,“therapeuticpotentialofcomplementmodulation”,2010,nat.rev.drugdiscovery,9(1):43–56
10.ehrnthaller,c.,etal,“newinsightsofanolddefensesystem:structure,function,andclinicalrelevanceofthecomplementsystem”,2011,mol.med.,17:317–329
11.ferrara,n.,“vascularendothelialgrowthfactor:basicscienceandclinicalprogress”,2004,endocrinereviews,25(4):581–611
12.sullivanl.a.,etal,2010,“thevegffamilyincancerandantibody-basedstrategiesfortheirinhibition”,mabs,2(2):165–175
13.derbyshirem.patentexpirydatesforbiologicals:2017update,2018,genericsandbiosimilarsinitiativejournal,7(1):29-34.
序列表
<110>三钰生物科技股份有限公司
<120>双功能性融合蛋白及其用途
<130>trb0004cn
<150>us62/744,936
<151>2018-10-12
<160>4
<170>patentinversion3.5
<210>1
<211>666
<212>prt
<213>人工序列
<220>
<223>c5v
<400>1
glnvalglnleuvalglnserglyalagluvallyslysproglyala
151015
servallysvalsercyslysalaserglytyrilepheserasntyr
202530
trpileglntrpvalargglnalaproglyglnglyleuglutrpmet
354045
glygluileleuproglyserglyserthrglutyrthrgluasnphe
505560
lysaspargvalthrmetthrargaspthrserthrserthrvaltyr
65707580
metgluleuserserleuargsergluaspthralavaltyrtyrcys
859095
alaargtyrphepheglyserserproasntrptyrpheaspvaltrp
100105110
glyglnglythrleuvalthrvalserseralaserthrlysglypro
115120125
servalpheproleualaprocysserargserthrsergluserthr
130135140
alaalaleuglycysleuvallysasptyrpheprogluprovalthr
145150155160
valsertrpasnserglyalaleuthrserglyvalhisthrphepro
165170175
alavalleuglnserserglyleutyrserleuserservalvalthr
180185190
valproserserasnpheglythrglnthrtyrthrcysasnvalasp
195200205
hislysproserasnthrlysvalasplysthrvalgluarglyscys
210215220
cysvalglucysproprocysproalaproprovalalaglyproser
225230235240
valpheleupheproprolysprolysaspthrleumetileserarg
245250255
thrprogluvalthrcysvalvalvalaspvalserglngluasppro
260265270
gluvalglnpheasntrptyrvalaspglyvalgluvalhisasnala
275280285
lysthrlysproargglugluglnpheasnserthrtyrargvalval
290295300
servalleuthrvalleuhisglnasptrpleuasnglylysglutyr
305310315320
lyscyslysvalserasnlysglyleuproserserileglulysthr
325330335
ileserlysalalysglyglnproarggluproglnvaltyrthrleu
340345350
proproserglngluglumetthrlysasnglnvalserleuthrcys
355360365
leuvallysglyphetyrproseraspilealavalglutrpgluser
370375380
asnglyglnprogluasnasntyrlysthrthrproprovalleuasp
385390395400
seraspglyserphepheleutyrserargleuthrvalasplysser
405410415
argtrpglngluglyasnvalphesercysservalmethisgluala
420425430
leuhisasnhistyrthrglnlysserleuserleuserleuglygly
435440445
glyglyserglyglyglyglyserglyglyglyglyserseraspthr
450455460
glyargprophevalglumettyrsergluileprogluileilehis
465470475480
metthrgluglyarggluleuvalileprocysargvalthrserpro
485490495
asnilethrvalthrleulyslyspheproleuaspthrleuilepro
500505510
aspglylysargileiletrpaspserarglysglypheileileser
515520525
asnalathrtyrlysgluileglyleuleuthrcysglualathrval
530535540
asnglyhisleutyrlysthrasntyrleuthrhisargglnthrasn
545550555560
thrileileaspvalvalleuserproserhisglyilegluleuser
565570575
valglyglulysleuvalleuasncysthralaargthrgluleuasn
580585590
valglyileasppheasntrpglutyrproserserlyshisglnhis
595600605
lyslysleuvalasnargaspleulysthrglnserglyserglumet
610615620
lyslyspheleuserthrleuthrileaspglyvalthrargserasp
625630635640
glnglyleutyrthrcysalaalaserserglyleumetthrlyslys
645650655
asnserthrphevalargvalhisglulys
660665
<210>2
<211>485
<212>prt
<213>人工序列
<220>
<223>vc5
<400>2
gluvalglnleuvalgluserglyglyglyleuvalglnproglygly
151015
serleuargleusercysalaalaserglytyraspphethrhistyr
202530
glymetasntrpvalargglnalaproglylysglyleuglutrpval
354045
glytrpileasnthrtyrthrglygluprothrtyralaalaaspphe
505560
lysargargphethrpheserleuaspthrserlysserthralatyr
65707580
leuglnmetasnserleuargalagluaspthralavaltyrtyrcys
859095
alalystyrprotyrtyrtyrglythrserhistrptyrpheaspval
100105110
trpglyglnglythrleuvalthrvalserseralaserthrlysgly
115120125
proservalpheproleualaproserserlysserthrserglygly
130135140
thralaalaleuglycysleuvallysasptyrpheprogluproval
145150155160
thrvalsertrpasnserglyalaleuthrserglyvalhisthrphe
165170175
proalavalleuglnserserglyleutyrserleuserservalval
180185190
thrvalproserserserleuglythrglnthrtyrilecysasnval
195200205
asnhislysproserasnthrlysvalasplyslysvalgluprolys
210215220
sercysglyglyglyglyserglyglyglyglyserglyglyglygly
225230235240
serglnvalglnleuvalglnserglyalagluvallyslysprogly
245250255
alaservallysvalsercyslysalaserglytyrilepheserasn
260265270
tyrtrpileglntrpvalargglnalaproglyglnglyleuglutrp
275280285
metglygluileleuproglyserglyserthrglutyrthrgluasn
290295300
phelysaspargvalthrmetthrargaspthrserthrserthrval
305310315320
tyrmetgluleuserserleuargsergluaspthralavaltyrtyr
325330335
cysalaargtyrphepheglyserserproasntrptyrpheaspval
340345350
trpglyglnglythrleuvalthrvalserserglyglyglyglyser
355360365
glyglyglyglyserglyglyglyglyseraspileglnmetthrgln
370375380
serproserserleuseralaservalglyaspargvalthrilethr
385390395400
cysglyalasergluasniletyrglyalaleuasntrptyrglngln
405410415
lysproglylysalaprolysleuleuiletyrglyalathrasnleu
420425430
alaaspglyvalproserargpheserglyserglyserglythrasp
435440445
phethrleuthrileserserleuglnprogluaspphealathrtyr
450455460
tyrcysglnasnvalleuasnthrproleuthrpheglyglnglythr
465470475480
lysvalgluilelys
485
<210>3
<211>15
<212>prt
<213>人工序列
<220>
<223>gslinker
<400>3
glyglyglyglyserglyglyglyglyserglyglyglyglyser
151015
<210>4
<211>20
<212>prt
<213>人工序列
<220>
<223>signalpeptide
<400>4
metgluthraspthrleuleuleutrpvalleuleuleutrpvalpro
151015
glyserthrgly
20
- 还没有人留言评论。精彩留言会获得点赞!