一种化合物在制备抑制细菌群体感应系统药物中的应用的制作方法
本发明属于医药技术领域,尤其涉及一种化合物在制备抑制细菌群体感应系统药物中的应用。
背景技术:
随着抗生素在临床上广泛使用,细菌产生的抗药性逐渐增强,不仅使抗生素对致病菌的敏感性不断降低,而且还可能改变细菌的生理和生化特性,使病菌产生原本不具备的特征,如药物渗透性障碍、生成药物灭活酶、形成生物被膜等,从而降低抗生素的作用。目前,抗生素耐药性已经成为全球严重的公共卫生问题。
近年来,细菌群体感应(quorumsensing,qs)系统已成为研究新型抗耐药菌药物的重要靶标。qs是细菌细胞内或细胞间信号传递的一种方式,通过监控某些信号分子(又称自体诱导分子)如高丝氨酸内酯(acyl-homoserinelactone,ahl)的浓度,来控制并协调整个细菌群体行为,共同对周围环境刺激做出反应,极大增强了整个细菌群体的生存能力。
病原菌的致病性由qs调控,qs系统通过介导致病基因的表达以实现其致病性。当致病菌密度达到一定程度时,致病菌自身合成、释放某种信号分子,能够启动相关基因的表达,调控致病菌的多种生物行为,诸如生物发光、产生毒素、形成生物被膜、产生抗生素等等。
因而,寻找抑制细菌群体感应系统的药物成为领域内研究人员亟待解决的问题。
技术实现要素:
有鉴于此,本发明提供了一种化合物在制备抑制细菌群体感应系统药物中的应用,用于提供抑制细菌群体感应系统的药物,使得在不抑制致病菌生长的前提下,减弱致病菌毒性。
本发明的具体技术方案如下:
2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛在制备抑制细菌群体感应系统的药物中的应用。
实验结果表明,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛能够在报告菌株对数生长期内对菌株lasb-gfp、pqsa-gfp和rhla-gfp有显著的抑制作用,且呈现量效关系,浓度越高,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对菌株lasb-gfp、pqsa-gfp和rhla-gfp的抑制作用越强;2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛能对铜绿假单胞菌弹性蛋白酶、绿脓素和鼠李糖脂的分泌产生抑制效果,且对于铜绿假单胞菌的生物膜具有抑制效果。2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛能够在不抑制铜绿假单胞菌生长的情况下,抑制铜绿假单胞菌群体感应系统pqsa、lasb和rhla三种信号通路,抑制铜绿假单胞菌群体感应系统活性,进而降低细菌致病力及毒力而又不抑制其生长,减缓细菌多重耐药性的产生。
2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛的结构式如下:
优选的,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛在制备抑制pqsa、lasb和/或rhla通路的药物中的应用。
实验结果表明2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛可抑制铜绿假单胞菌pqsa、lasb和rhla基因编码的表达。
美国国立卫生研究院发布的一份权威调查报告指出,人类微生物感染有超过80%是通过细菌生物被膜介导的。生物被膜作为一种细菌群体行为,其分化与发育与细菌群体感应密切相关。细菌群体感应系统完整的细菌可以形成发育和分化正常的、典型的能对抗杀菌剂的生物被膜,而细菌群体感应系统残缺的的细菌则不能形成典型的生物被膜,对抗生素的抵抗力显著下降,容易被冲洗掉,并且对杀菌剂敏感。铜绿假单胞菌具有很强的在组织表面形成生物被膜的能力,生物被膜的形成和扩散也是造成铜绿假单胞菌多重耐药的一个重要机制。
优选的,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛在制备降低细菌生物被膜形成的药物中的应用。
铜绿假单胞菌(p.aeruginosa)又称绿脓杆菌,是一种革兰氏阴性菌,也是一种重要的条件致病菌,常常引起呼吸道感染、肺炎、泌尿道感染等医院内感染,被认为是病人在医院期间发生感染的第三大致病菌,严重危害着人类的健康与生命。铜绿假单胞菌多表现出强耐药性,其耐药机制主要是形成生物膜、产生抗生素灭活酶、抑制药物的渗透力。铜绿假单胞菌群体感应系统包括las系统、rhl系统、pqs系统,它们所编码的信号分子可共同参与调节鼠李糖脂、溶血素、几丁质酶、氰化物等次级代谢产物的生成;另外,各子系统存在级联调节机制,las系统的主控因子,可调节其他系统基因的表达,而pqs系统也是las系统和rhl系统的连接枢纽。铜绿假单胞菌的las系统主导生物被膜生长、成熟的过程,通过抑制las系统,可以有效地抑制生物被膜的形成,而rhl系统对生物被膜的形成也起到重要的作用,rhl系统可调控鼠李糖脂的产生,起到维持生物被膜通道开放、固定结构等作用,说明生物被膜的产生与细菌群体感应密切相关,因此抑制或者破坏细菌之间的交流、不施与细菌选择性压力的药物成为阻止致病菌生物被膜产生以及抗药性形成的重要选择。铜绿假单胞菌的高内在抗药性与其群体感应系统密不可分,其群体感应系统控制着包括生物被膜、外毒素、弹性蛋白酶、溶血素、绿脓菌素等致病因子的表达,这些致病因子决定了铜绿假单胞菌对宿主的致病能力。
优选的,所述细菌为铜绿假单胞菌和/或耐药铜绿假单胞菌。
优选的,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛在制备抑制弹性蛋白酶、绿脓菌素和/或鼠李糖脂分泌的药物中的应用。
优选的,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛通过提取莲子心得到。莲子心(plumulanelumbinis),又称莲薏、苦薏、莲心,最早见于唐末的《食性本草》中,为睡莲科多年生水生植物莲成熟种子中的干燥胚芽,其主要产地分布在我国湖南、湖北、福建、江苏、浙江、江西等省。莲子心性寒,味苦,归心、肾经,具有清心安神、交通心肾和涩精止血的功效,用于治疗热入心包、神昏谵语、心肾不交、失眠遗精和血热吐血等症,是常用的具有“清热解毒”作用的中药之一。
本发明中,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛的提取包括以下步骤:
a)将莲子心采用溶剂进行回流提取,除去不溶物,得到第一提取物;
b)将第一提取物依次采用石油醚、乙酸乙酯和正丁醇萃取,取乙酸乙酯萃取液,得到乙酸乙酯萃取物;
c)将乙酸乙酯萃取物采用色谱法进行分离,得到2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛。
步骤a)中,莲子心与溶剂的质量比为1:10~15,溶剂选自水、甲醇、乙醇、丙酮或乙酸乙酯,采用过滤或离心除去不溶物,回流提取的温度为60℃~150℃,回流提取的时间为0.5h~80h。
除去不溶物之后,得到第一提取物之前,还包括:减压干燥。
步骤b)中,第一提取物依次采用石油醚、乙酸乙酯和正丁醇萃取之前,还包括:将第一提取物分散于等体积水中;
取乙酸乙酯萃取液之后,得到乙酸乙酯萃取物之前,还包括:真空减压干燥。
步骤c)中,色谱法选自正相色谱法、反相色谱法或凝胶色谱法。
需要说明的是,本发明2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛可通过购买得到。
本发明还提供了一种抑制细菌群体感应系统的药物,包括2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛和药学上可接受的辅料。
实验结果表明2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛在不抑制细菌生长的情况下,抑制了lasb-gfp、pqsa-gfp和rhla-gfp报告基因的表达,对调控铜绿假单胞菌群体感应系统发挥作用的三种主要信号通路均具有较好的抑制效果,las系统、pqs系统及rhl系统与弹性蛋白酶、绿脓素和鼠李糖脂等毒力因子的产生有关,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛具备抑制铜绿假单胞菌毒力的功效。而且,实验结果表明2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对铜绿假单胞菌的生物膜具有抑制效果。本发明抑制细菌群体感应系统的药物有利于从根源上有效解决抗生素耐药性问题。
优选的,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛和所述药学上可接受的辅料的质量比为(1~9):(1~9)。
优选的,所述药物为口服制剂。
优选的,所述口服制剂为胶囊剂、片剂或颗粒剂。
综上所述,本发明提供了2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛在制备抑制细菌群体感应系统的药物中的应用,实验结果表明,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛能够在不抑制铜绿假单胞菌生长的情况下,抑制铜绿假单胞菌群体感应系统pqsa、lasb和rhla三种信号通路,抑制铜绿假单胞菌群体感应系统活性,进而降低细菌致病力及毒力而又不抑制其生长,减缓细菌多重耐药性的产生。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍。
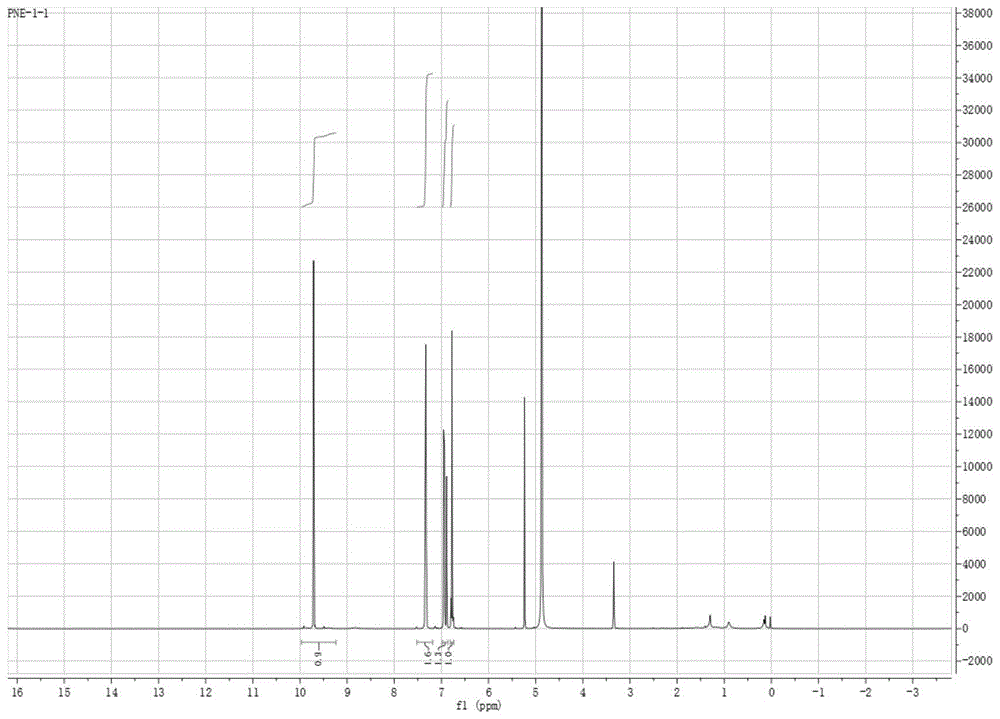
图1为本发明实施例1提取得到的目标化合物的核磁共振氢谱图(600mhz);
图2为本发明实施例1提取得到的目标化合物的核磁共振碳谱图(600mhz);
图3为本发明实施例2中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对lasb-gfp表达的抑制效果图;
图4为本发明实施例2中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对pao1-lasb-gfp菌株生长的影响图;
图5为本发明实施例3中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对pqsa-gfp表达的抑制效果图;
图6为本发明实施例3中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对pao1-pqsa-gfp菌株生长的影响图;
图7为本发明实施例4中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对rhla-gfp表达的抑制效果图;
图8为本发明实施例4中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对pao1-rhla-gfp菌株生长的影响图;
图9为本发明实施例5中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对绿脓菌素分泌的抑制作用图;
图10为本发明实施例6中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对弹性蛋白酶分泌的抑制作用图;
图11为本发明实施例7中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对鼠李糖脂分泌的抑制作用图;
图12为本发明实施例8中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对生物膜抑制影响图;
其中,图3至图8中,“c25”表示2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛组,“positive”表示化合物iberin组,“bacteria”表示只含有pao1-lasb-gfp菌株在37℃,200rpm的lb培养基中生长12~16h的培养物的细菌对照组;图9和图11中,“c25”表示2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛组,“ery”表示红霉素组,“control”表示只含有培养基的空白对照组,“dmso+control”表示dmso溶剂对照组;图10中,“c25”表示2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛组,“fur”表示呋喃酮组,“control”表示只含有培养基的空白对照组,“dmso+control”表示dmso溶剂对照组;图12中,“c25”表示2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛组,“aq”表示阿奇霉素阳性对照组,“dmso+control”表示0.2%dmso溶剂对照组。
具体实施方式
本发明提供了一种化合物在制备抑制细菌群体感应系统药物中的应用,用于提供抑制细菌群体感应系统的药物,使得在不抑制致病菌生长的前提下,减弱致病菌毒性。
下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
本发明实施例中所用原料均为市售或自制,其中pao1-lasb-gfp绿色荧光蛋白报告菌株、pao1-pqsa-gfp绿色荧光蛋白报告菌株、pao1-rhla-gfp绿色荧光蛋白报告菌株以及铜绿假单胞菌pao1均来自南洋理工大学。
实施例12-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛的提取
本实施例进行2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛的提取,包括以下步骤:
(1)将10kg莲子心置于80%(v/v)的乙醇中浸泡12h后加热回流提取3次,提取温度为(具体值)℃,每次2h,趁热减压抽滤除去不溶物,滤液减压干燥得到第一提取物。其中,莲子心与乙醇的质量比为1:12。
(2)将第一提取物依次采用等体积石油醚、乙酸乙酯和正丁醇萃取3次,取乙酸乙酯萃取液,真空减压干燥,得乙酸乙酯萃取物4.5g;
(3)将乙酸乙酯萃取物采用反复硅胶柱色谱、开放ods柱色谱、sephadexlh-20柱色谱和制备型高效液相色谱进行化学成分分离,最终分离得到目标化合物。
目标化合物为黄色无定形粉末,分子式为c14h10o5。请参阅图1和图2,分别为本发明实施例1提取得到的目标化合物的核磁共振氢谱图和核磁共振碳谱图(600mhz),目标化合物的波谱数据如下:esi-msm/z:257.2[m-h]-,281.3[m+na]+;1h-nmr(cd3od,500mhz)δ:5.20(1h,s,h-2),7.31(1h,d,j=1.6hz),7.30(1h,dd,j=1.6,6.4hz),6.91(1h,dd,j=2.5,6.0hz),9.67(1h,s,h-10),6.85(1h,d,j=1.0hz),6.73(1h,d,j=1.2hz,h-5’),6.73(1h,d,j=1.2hz,h-6’);13c-nmr(cd3od,125mhz)δ:104.8(c-2),114.8(c-4),l30.8(c-5),126.4(c-6),116.2(c-7),147.1(c-8),153.7(c-9),193.1(c-10),146.6(c-1'),115.4(c-2'),146.1(c-3'),131.1(c-4'),115.8(c-5'),119.4(c-6')。以上数据表明目标化合物为2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛。
实施例22-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对pao1-lasb通路的影响
测试化合物:将本发明化合物2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛用100%dmso配制成200mm的储备液,以异硫氰酸酯类化合物iberin(10μm)为阳性对照,以0.2%dmso为溶剂对照。
实验方法:将本发明化合物在96孔微量滴定板中与abtgc培养基混合用二倍稀释法混合最终每孔中有100μl含药的abtgc培养基。将pao1-lasb-gfp菌株在37℃,200rpm的lb培养基中生长12~16h的培养物在abtgc培养基中稀释至600nm(od600)的最终光学密度为0.02(2.5×108cfu/ml)。接着,在96孔微量滴定板的每孔中加入100μl的细菌悬浮液,以使最终每孔中本发明化合物的最终浓度为200、100、50、25、12.5、6.25、3.125、1.5625μm。并在同一个96孔板上设置iberin阳性对照组、0.2%dmso溶剂对照组以及200μl均为pao1-lasb-gfp菌株的细菌对照组。将96孔微量滴定板在37℃的tecaninfinate200pro读板仪中孵育至少16小时,其中每隔15分钟测量以下参数:od600,gfp荧光信号(激发485nm,发射535nm)。所有测试化合物和对照的抑制测定均一式三份进行。
实验结果:请参阅图3,为本发明实施例2中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对lasb-gfp表达的抑制效果图。图3表明,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对lasb-gfp报告基因的表达具有抑制作用。经过4h的培养,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛组lasb-gfp的表达水平开始增大,直到培养时间到8h,各浓度2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛组的lasb-gfp水平开始稳定;在菌株对数生长期的6-8h,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对菌株lasb-gfp的荧光有显著的抑制作用,且呈现量效关系,浓度越高,化合物对菌株lasb-gfp荧光的抑制作用越强。
请参阅图4,为本发明实施例2中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对pao1-lasb-gfp菌株生长的影响图。图4表明,除阳性对照iberin组外,各浓度2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛组pao1-lasb-gfp菌株生长情况几乎一样,而且几乎不随2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛浓度变化而变化。表明本发明2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛在不影响报告菌株pao1-lasb-gfp生长的情况下,对细菌群体感应系统的lasb通路有抑制作用。
实施例3:2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对pao1-pqsa通路的影响
测试化合物:将本发明化合物2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛用100%dmso配制成200mm的储备液,以异硫氰酸酯类化合物iberin为阳性对照,以0.2%dmso为溶剂对照。
实验方法:取过夜培养好的pao1-pqsa-gfp绿色荧光蛋白报告菌株重复实施例2实验方法步骤,检测2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对铜绿假单胞菌群体感应系统pqsa信号通路的影响。
实验结果:请参阅图5,为本发明实施例3中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对pqsa-gfp表达的抑制效果图。图5表明2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对pqsa-gfp报告基因的表达具有抑制作用,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛组pqsa-gfp的表达水平随培养时间增大呈现先增后降,然后逐渐稳定的趋势;在菌株对数生长期的4-8h,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对菌株pqsa-gfp的荧光有显著的抑制作用,且呈现量效关系,浓度越高,化合物对菌株pqsa-gfp荧光的抑制作用越强。
请参阅图6,为本发明实施例3中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对pao1-pqsa-gfp菌株生长的影响图。图6表明,各浓度2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛组pao1-pqsa-gfp菌株生长情况相近,而且与2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛的浓度无关,表明本发明2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛在不影响报告pao1-pqsa-gfp菌株生长的情况下,可以抑制细菌群体感应系统的pqsa通路。
实施例4:2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对pao1-rhla通路的影响
测试化合物:将本发明化合物2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛用100%dmso配制成200mm的储备液,以异硫氰酸酯类化合物iberin(10μm)为阳性对照,以0.2%dmso为溶剂对照。
实验方法:取过夜培养好的pao1-rhla-gfp绿色荧光蛋白报告菌株重复实施例2实验方法步骤。
实验结果:请参阅图7,为本发明实施例4中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对rhla-gfp表达的抑制效果图。图7表明2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对rhla-gfp报告基因的表达具有抑制作用,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛组rhla-gfp的表达水平随培养时间增大,呈平缓上升趋势;在菌株对数生长期的5-8h,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对菌株rhla-gfp的荧光有显著的抑制作用,且呈现量效关系,浓度越高,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对菌株rhla-gfp荧光的抑制作用越强。
请参阅图8,为本发明实施例4中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对pao1-rhla-gfp菌株生长的影响图。图8表明,各2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛组pao1-rhla-gfp菌株生长情况相近,而且不受2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛浓度变化的影响,表明本发明2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛在不影响报告菌株pao1-rhla-gfp生长的情况下,对细菌群体感应系统的rhla通路有抑制作用。
实施例5:2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对绿脓菌素的抑制作用
测试化合物:将本发明化合物2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛用100%dmso配制成200mm的储备液,以红霉素(10μm)为阳性对照,以0.2%dmso为溶剂对照。
细菌预处理:取培养好之后的铜绿假单胞菌,于100ml锥形瓶,内含已经灭菌好的50mllb培养基,向其中加入相应化合物至所需浓度,并将过夜的细菌标定在od600=0.01加入到锥形瓶中,放入37℃摇床,200r/min,培养24小时。细菌生长24小时以后,均全部混匀先测od600。
测定方法:将锥形瓶中的细菌转移至50ml离心管中,10000rpm/min,4℃离心10min。离心后取上清液40ml加入3ml氯仿提取,后将氯仿层(下层)移至新管,加入0.3倍氯仿的0.2mhcl,离心后取上层测od520。
请参阅图9,为本发明实施例5中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对绿脓菌素分泌的抑制作用图。图9表明,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛组绿脓杆菌的分泌水平比对照组及dmso组的分泌水平低,但比红霉素组的分泌水平高,表明2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对铜绿假单胞菌绿脓菌素的分泌起抑制作用。
实施例6:2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对铜绿假单胞菌弹性蛋白酶分泌的抑制作用
测试化合物:将本发明化合物2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛用100%dmso配制成200mm的储备液,以呋喃酮(10μm)为阳性对照,以0.2%dmso为溶剂对照。
测定方法:铜绿假单胞菌pao1预处理步骤同上实施例5,细菌培养24小时之后,取5ml菌液,10000rpm/min,4℃离心10min。并用0.22μm过滤器过滤一次,遵照试剂盒enzchekfiproteaseassaykite6638操作步骤,用1×reactionbuffer配置弹性蛋白(注意避光,且室温不能放很久)浓度到50μg/ml,细菌上清液和已经配好的底物各加100μl,稍稍混匀之后,立马放入酶标仪,每隔10min,连续4小时测荧光(激发波长400nm,发射波长450nm),荧光含量的高低表示弹性蛋白酶含量的多少。
请参阅图10,为本发明实施例6中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对弹性蛋白酶分泌的抑制作用图。图10表明,各实验组弹性蛋白酶水平随时间延长呈缓慢上升的趋势,但2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对弹性蛋白酶分泌的抑制效果远强于对照组和dmso组,表明2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对铜绿假单胞菌弹性蛋白酶的分泌具有一定的抑制作用。
实施例7:2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对铜绿假单胞菌鼠李糖脂的分泌抑制作用
测试化合物:将本发明化合物2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛用100%dmso配制成200mm的储备液,以红霉素(10μm)为阳性对照,以0.2%dmso为溶剂对照。
测定方法:细菌预处理步骤同上实施例5,细菌培养24小时之后,取5ml菌液,10000rpm/min,4℃离心10min。取2ml上清液于10mlep管中,加入4ml乙醚震摇混匀萃取。乙醚层取1ml于1.5mlep管中,放入通风橱中,自然挥干乙醚。之后用40μl超纯水溶解提取出来的鼠李糖脂,加入360μl已经用50%浓硫酸现配的0.9%的苔黑酚溶液,混匀之后80℃水浴锅煮30min。冷却之后取200μl于96孔板中,测od421。
请参阅图11,为本发明实施例7中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对鼠李糖脂分泌的抑制作用图。图11表明,2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛组绿脓杆菌的分泌水平比对照组及dmso组的分泌水平低,甚至略低于红霉素组的分泌水平,表明2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对铜绿假单胞菌鼠李糖脂的分泌具有较强的抑制作用,其抑制效果与阳性药红霉素相近。
实施例8:2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛的生物膜抑制实验
测试化合物:将本发明化合物2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛用100%dmso配制成200mm的储备液,以阿奇霉素(10μm)为阳性对照,以0.2%dmso为溶剂对照。
实验方法:往孔板中分别加入100μl所准备的待测样品,接种100μl铜绿假单胞菌pao1菌液。设置0.2%dmso溶剂对照组和阿奇霉素(10μm)阳性对照组。置于37摄氏度温箱中孵化。20h后,吸取孔内表层菌液,蒸馏水洗涤三次,洗去浮游细菌。干燥或者烘箱烘干后,加入220μl浓度为1%的结晶紫,室温放置30min,然后蒸馏水小心洗涤3次;加入230μl95%乙醇溶解生物膜-结晶紫复合物,酶标仪630nm波长处测定孔板吸光度值,平行测定三次。
请参阅图12,为本发明实施例8中2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对生物膜抑制影响图。实验数据表明2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛对铜绿假单胞菌的生物膜具有良好的抑制效果,表明可以通过抑制细菌的群体感应系统,从而达到抑制细菌生物膜形成,不易产生细菌耐药性的效果。
实施例9:抗铜绿假单胞菌群体感应颗粒剂
抗铜绿假单胞菌群体感应颗粒剂的制备步骤为:
(1)首先将2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛与乳糖、甘露醇及cms-na混合均匀;
(2)然后将配制好的10%淀粉浆加入上述混合物中,过16目筛制软材;
(3)在真空干燥箱中,60℃烘干,整粒,即得抗铜绿假单胞菌群体感应颗粒剂。
实施例10:抗铜绿假单胞菌群体感应胶囊剂
抗铜绿假单胞菌群体感应胶囊剂的制备步骤为:
(1)将2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛与乳糖混合10-15分钟;
(2)再加入微晶纤维素后混合10-15分钟;
(3)再加入滑石粉后混合3-5分钟;
(4)混合物装入明胶胶囊壳,即得本发明抗铜绿假单胞菌群体感应胶囊剂。
实施例11:抗铜绿假单胞菌群体感应片剂
抗铜绿假单胞菌群体感应片剂的制备步骤为:
(1)将2-(3’,4’-二羟苯基)-1,3-胡椒环-5-醛与乳糖混合10-15分钟;
(2)加入10%淀粉浆制软材,过14目筛,制粒后干燥,过12目筛整粒;
(3)然后加入交联聚维酮和硬脂酸镁,混合3-5分钟;
(4)混合均匀后压片,即得本发明抗铜绿假单胞菌群体感应片剂。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!