一种枸橼酸托法替布片剂的制备方法与流程
本发明属于药物制剂技术领域,特别涉及一种枸橼酸托法替布片剂的制备方法。
背景技术:
类风湿性关节炎(ra)是一种慢性、炎性、系统性的自身免疫性疾病,以关节和关节组织化脓性炎症为主要特征,主要表现为关节滑膜炎,终致关节的软骨、韧带、肌腱等各种组织以及多脏器损害。其基本病理改变是滑膜炎,急性期滑膜肿胀、渗出,粒细胞侵润;慢性期滑膜增生肥厚,形成血管豁,后者是造成关节破坏、关节畸形、障碍、使疾病进入不可逆阶段的病理基础。患者同时伴有发热、贫血、巩膜炎、心包炎、血管炎及淋巴肿大等关节外表现,血清中可以查到多种自身抗体,故称类风湿性关节炎。
托法替布是辉瑞公司开发的一种新型口服jak通路抑制剂。与当前多数其他ra治疗药物主要作用于细胞外靶点不同的是,托法替布以细胞内信号转导通路为靶点,作用于细胞因子网络的核心部分。托法替布对jak3的抑制强度是对jak1及jak2的5-100倍。托法替布是开发用于人类风湿性关节炎治疗的首创药物,fda于2012年11月6日批准了jak抑制剂用于治疗成人活动期及对甲氨蝶呤反应不佳的中至重度类风湿性关节炎患者。托法替布可单用,也可与甲氨蝶呤及其他特定的标准治疗药物合用。该药具体化学结构式如下所示:
国内目前已有较多关于枸橼酸托法替布片剂的制备方法的研究。例如中国专利cn104622827a公开了一种托法替布片剂及其制备方法。该专利公开的片剂选用流动性、压缩成形性好的直压乳糖和微晶纤维素作为稀释剂和干粘合剂,并采用工艺简单的粉末直压片法制备,工艺简单,省时节能,制备得到的托法替布片组合物质量可控,并确保了产品的稳定性。该文献方法的一个示例性片剂配方中包含:托法替布5份、直压乳糖40份、微晶纤维素50份、交联羧甲基纤维素钠2份、硬脂酸镁2份,该片剂采用粉末直接压片法制备。
中国专利cn105878202a公开了一种枸橼酸托法替布片,它由枸橼酸托法替布与药学上可接受的辅料组成,所述辅料包括填充剂、崩解剂、助流剂和包衣剂,所述填充剂为型号为celactose80的微晶纤维素乳糖预混物,所述枸橼酸托法替布与型号为celactose80的微晶纤维素乳糖预混物的重量比为1:5-25,在该发明使用的助流剂最为优选的是硬脂酸镁,其中一个典型配方实例中包括枸橼酸托法替布、填充剂celactose80(一种直压乳糖)、崩解剂低取代羟丙纤维素和助流剂硬脂酸镁,通过粉末直接压片法制备。本发明不仅具有较高的含量均匀度高,而且具有溶出速度快、化学性质稳定等优点。但上述两件专利公开的片剂均采用干法直压制得,片剂溶出太快,与原研药溶出差异大。
中国专利cn106389371a公开了一种枸橼酸托法替布药物组合物,其呈片剂形式,该药物组合物包括活性成分枸橼酸托法替布、稀释剂、崩解剂、粘合剂、润滑剂。还涉及该药物组合物的制备方法,其制药用途以及其质量控制方法。该专利在组方中加入硫酸钙使其先与活性成分研磨混合后再加入其它组分,制得和片剂表现出优异的溶出性能。
一方面该专利相对原研药品改变了制剂组方,加入了硫酸钙等成分,使得在湿法制粒前需先将活性成分与硫酸钙先混合压片处理,然后才能进行制粒,制备工艺复杂化;另一方面,虽然该片剂在中性介质中表现出优异的溶出性能,但在更接近枸橼酸托法替布的体内使用环境(ph为4.0-5.0)下,溶出效果并不理想,与原研药存在较大差异。
技术实现要素:
针对现有技术中存在的上述问题,本发明的目的在于提供一种枸橼酸托法替布片剂的制备方法。该制备方法工艺简单,对生产设备要求低,而且制得的制剂与原研药一致性程度高。
为了实现上述发明目的,本发明提供以下技术方案:
一种枸橼酸托法替布片剂的制备方法,其包括以下步骤:
s1称取微晶纤维素、枸橼酸托法替布、交联羧甲基纤维素钠、乳糖,分别过筛后混合,备用;
s2将s1中过筛混合后的物料送入湿法制粒机中干混合数分钟,加入纯化水进行制粒,出料;
s3对所得湿颗粒进行整粒,干燥;
s4将干燥后的颗粒二次整粒,整粒结束后加入硬脂酸镁,混合至均匀,压片,包衣后即得枸橼酸托法替布片。
优选地,所述枸橼酸托法替布片剂中的片芯的原辅料以重量比计,包括如下各组分:枸橼酸托法替布的量以托法替布计为2-10:乳糖60-130:微晶纤维素60-130:交联羧甲基纤维素钠1-10:硬脂酸镁0.5-3。
进一步优选地,所述乳糖和微晶纤维素占片剂的40%-50%,交联羧甲基纤维素钠占片剂的1.0%-3.0%,硬脂酸镁占片剂的1.0%-2.0%。
优选地,步骤s1中过筛尺寸为50-60目。
优选地,所述s2中制粒过程,搅拌速度为120-200rpm,和/或混合时间为6-15min。
优选地,步骤s2中加液时间为1-2min。
优选地,步骤s2中加入的纯化水与步骤s2中干混合后的物料质量比为1:2.5-2.8。
优选地,步骤s2中加水后继续搅拌制粒0.5-3min;进一步优选为0.5-1.5min。
优选地,步骤s3中干燥采用流化床干燥制粒机进行干燥,设定风机频率20-40hz;
优选地,步骤s3中,将所得湿颗粒用10-24目不锈钢筛在摇摆式颗粒机上进行湿颗粒整粒。
进一步优选地,所述干燥设置进风温度为40-60℃,控制物料温度<65℃,干燥至水分1.0-3.0%。
优选地,所述步骤s4中,将干燥后的颗粒用18-30目不锈钢筛在摇摆式颗粒机上进行二次整粒。
优选地,所述步骤s4中加入硬脂酸镁后使用三维混合机混合5-10min。
本发明与现有技术相比,具有如下有益效果:
本发明提供了一种枸橼酸托法替布片剂的制备方法,该方法对生产设备要求低、生产工艺操作简单;而且由该工艺制得的片剂具有优异的溶出性能、可加工性、含量均匀性及稳定性,与原研药具有较好的一致性。
附图说明
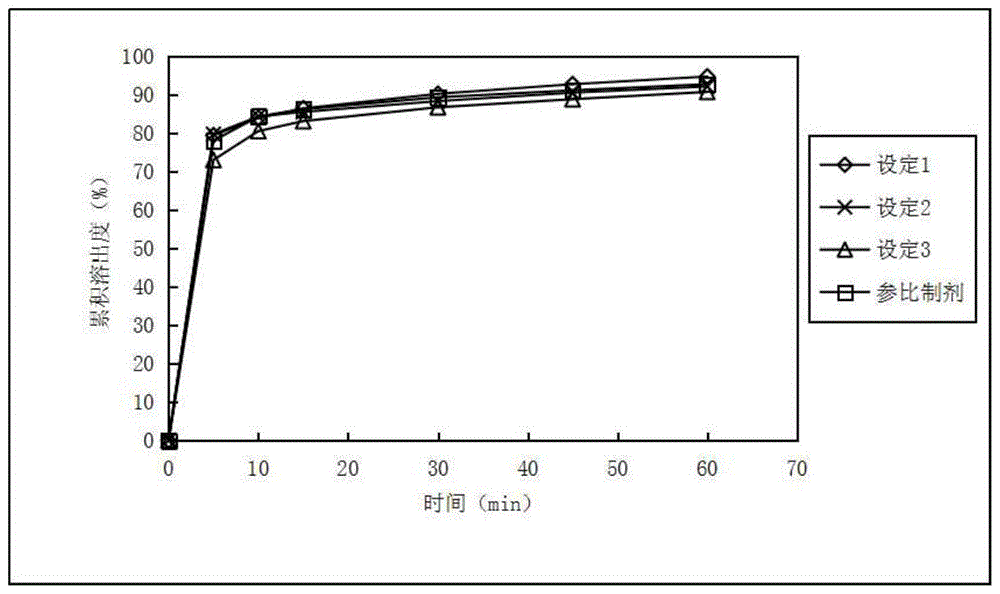
图1为实施例1提供的枸橼酸托法替布片剂的溶出曲线。
具体实施方式
以下结合附图对本发明的优选实施例进行说明,应当理解,此处所描述的优选实施例仅用于说明和解释本发明,并不用于限定本发明。
实施例1
评估制粒时间对本品溶出行为的影响,具体实施例如下述;
s1称量备料;称取80.8g枸橼酸托法替布、939.2g乳糖、930.0g微晶纤维素、30.0g交联羧甲基纤维素钠、20.0g硬脂酸镁;
s2将称取的枸橼酸托法替布、乳糖、微晶纤维素、交联羧甲基纤维素钠分别过50目筛一次,备用。将过筛后的原辅料置于卧式湿法制粒机中160rpm搅拌速度下干混合6分钟,然后加入纯化水,加水制粒时间为1min,加水后制粒0.5-3min,在此制粒过程中仅开启制粒机的搅拌桨;出料,过18目筛进行湿颗粒整粒;
s3湿颗粒置于流化床中进行干燥,流化床干燥制粒机设定风机频率25hz,干燥条件设置进风温度为50℃,干燥至水分1.0-3.0%;
s4干燥后过24目筛进行整粒,整粒后颗粒加入硬脂酸镁混合5min,压片,素片包衣后即得枸橼酸托法替布片。试验结果如下表1所示。如图1所示,为实施例1提供的枸橼酸托法替布片剂的溶出曲线(ph为4.5)。
表1制粒时间考察试验结果统计表
解读:
由上述实施例可知,湿法制粒时,制粒时间对枸橼酸托法替布片在ph4.5介质中的溶出行为有一定影响,制粒时间越长,溶出行为有减慢的趋势。从5min和10min的累积溶出度可知,设定3的前期累积溶出较设定1慢4%-5%。
本品药物在体内血药浓度达峰时间短,主要被十二指肠吸收入血,而十二指肠内的ph环境为4.0-5.0,所以本品在ph4.5介质中的前十分钟的溶出快慢可能会影响药物在体内的吸收速度。
因此,为了确保本品在ph4.5介质中的溶出与参比制剂保持一致,进而降低本品与参比制剂be不等效风险,选择湿法制粒最优时间为1.5min。
本实施例过程中发明人考察了包衣材质对片剂溶出性能的影响,结果发现,本领域常规包衣材质及常规的包衣工艺制得的片剂的溶出性能无实质差异。
实施例2
评估纯化水用量对枸橼酸托法替布片剂溶出行为的影响,具体实施例如下述;
(1)称量备料;称取80.8g枸橼酸托法替布、939.2g乳糖、930.0g微晶纤维素、30.0g交联羧甲基纤维素钠、20.0g硬脂酸镁;
(2)制备方法;
将称取的枸橼酸托法替布、乳糖、微晶纤维素、交联羧甲基纤维素钠分别过50目筛一次,备用。将过筛后的原辅料置于制粒机中低速搅拌干混合6分钟。然后加入不同量的纯化水,160rpm搅拌速度下制粒1.5分钟,过18目筛进行湿颗粒整粒,湿颗粒置于流化床中进行干燥,流化床干燥制粒机设定风机频率25hz,干燥条件设置进风温度为50℃,干燥至水分1.0-3.0%。干燥后过24目筛进行整粒,整粒后颗粒加入硬脂酸镁混合5min,压片,素片包衣后即得枸橼酸托法替布片。试验结果如下表2所示。
表2润湿剂用量考察试验结果统计表
解读:
由上述实施例可知,润湿剂纯化水与干混后物料的质量比在1:2.5-2.8时对枸橼酸托法替布片的溶出行为无实质影响。片剂的溶出行为基本一致。
实施例3
评估枸橼酸托法替布片的稳定性,具体实施例如下:
(1)称量备料;称取808g枸橼酸托法替布、9392g乳糖、9300g微晶纤维素、300g交联羧甲基纤维素钠、200g硬脂酸镁;
(2)制备方法:
将称取的枸橼酸托法替布、乳糖、微晶纤维素、交联羧甲基纤维素钠使用摇摆式颗粒机过50目筛一次,备用。设置制粒机的搅拌速度为160rpm,将过筛后的原辅料置于制粒机中干混合6分钟,然后160rpm搅拌速度下加入8kg纯化水制粒1min,纯化水加毕后继续制粒0.5分钟,过18目筛进行湿颗粒整粒,湿颗粒置于流化床中进行干燥,流化床干燥制粒机设定风机频率25hz,干燥条件设置进风温度为50℃,控制物料温度<65℃,干燥至水分1.0-3.0%。干燥后过24目筛进行整粒,整粒后颗粒加入硬脂酸镁混合5min,压片,素片包衣后即得枸橼酸托法替布片。
对制备的枸橼酸托法替布片进行含量均匀度检测,实验结果如下表3
(3)对制备的枸橼酸托法替布片进行不同条件与方式的稳定性考察,实验结果如表4-表8所示。
表4多剂量包装产品开启后稳定性考察结果
表5实施例加速试验考察结果(温度40℃±2℃,湿度75%±5%)
表6参比制剂加速试验考察结果(温度40℃±2℃,湿度75%±5%)
表7实施例长期试验考察结果(温度30℃±2℃,湿度65%±5%)
注:表4-表7中溶出度数据为ph4.5条件下,测得枸橼酸托法替布片(每次试验取6片)在15min时的溶出度数据。
解读:
由实施例3可知,采用本发明提供的方法制备生产的枸橼酸托法替布片含量均匀,在贮存期间以及使用期间均具有良好的稳定性,且溶出速度快,药品质量极其稳定可靠。
其中,各相关物质的结构如下表8所示。
表8
对比例1
处方:枸橼酸托法替布5mg(以托法替布计)、乳糖一水合物30mg、微晶纤维素70mg、低取代羟丙基纤维素10mg、羟丙甲纤维素8mg(粘合剂,用水配制成3%液体使用)、硬脂酸镁2mg。
将称取的枸橼酸托法替布、乳糖一水合物、微晶纤维素、低取代羟丙基纤维素分别过50目筛一次,备用。将过筛后的原辅料置于制粒机中低速搅拌,干混合6分钟。然后加入羟丙甲纤维素溶液制粒,制粒后过18目筛进行湿颗粒整粒,湿颗粒置于流化床中进行干燥,流化床干燥制粒机设定风机频率25hz,干燥条件设置进风温度为50℃,干燥至水分1.0-3.0%。干燥后过24目筛进行整粒,整粒后颗粒加入硬脂酸镁混合5min,压片,素片包衣后即得枸橼酸托法替布片。
采用本发明上述溶出度测试方法,测得该片剂的溶出数值如下表9所示。
表9对比例1提供的枸橼酸托法替布片的溶出数据。
由表9的数据可以看出:对比例1的样品在ph4.5醋酸盐缓冲液中各时间点的累积溶出度较参比制剂偏低且15min累积溶出度仅79.2%,低于85%,与参比制剂溶出行为不相似。
最后应说明的是:以上仅为本发明的优选实施例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!