用于诊断肺病的生物标记物及其使用方法与流程
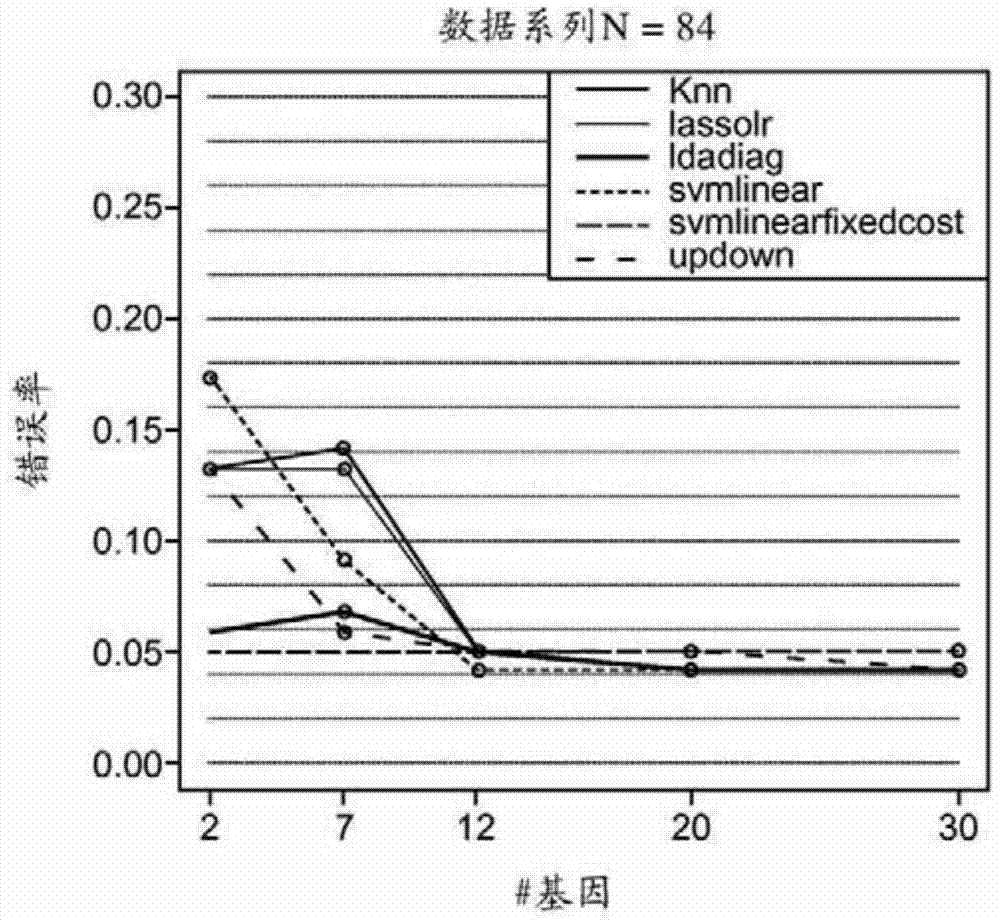
本申请要求获得美国临时专利申请号61/799,754的权益,其于2013年3月15日提出申请,本文引用该申请的全部内容作为参考。引言间质性肺病(ILD),也被称作弥漫性实质性肺病(DPLD),代表了多种病症,其可导致对正常肺组织的弥漫性重塑(diffuseremodeling)、结构损伤(architecturaldamage)和可导致肺功能进行性丧失的炎症。在ILD中,除了经常在肺实质中见到的炎症和纤维化之外,气管和脉管也会受到显著的影响。ILD最突出的形式是IPF和肺结节病。一些临床发现是ILD共有的:呼吸困难或咳嗽;胸片上双侧弥漫性间质浸润;生理和气体交换异常,包括一氧化碳扩散能力降低(DLCO)和肺泡-小动脉氧分压差(PO2difference)异常;和肺实质组织病理学异常,其特征是不同程度的炎症、纤维化和重塑。ILD的发病率估计为男性是31.5人/10万人/年,女性为26.1人/10万人/年,这些疾病的临床预后范围从轻微的疾病到呼吸衰竭和死亡。ILD的标准疗法包括皮质类固醇和免疫抑制剂,但是目前的治疗效果取决于被治疗的具体疾病实体而不同。特发性肺纤维化(IPF)是一种慢性、渐进性的下呼吸道纤维化异常。相比于其他的ILD,目前对于IPF尚无有效的疗法。纤维化增加导致肺功能减低,患者通常在生物活检确诊的3年内死于呼吸衰竭或其他并发症。虽然高分辨率计算机断层扫描(HRCT)已显著帮助间质性肺病(ILD)的诊断,但是在IPF中观察到的经典普通型间质性肺炎(UIP)模式也同时是许多其它ILD所共有的,因此全面的临床和职业史对于排除可治疗的疾病是至关重要的。当前用于诊断ILD的诊断范式昂贵、费时,并且往往导致显著比例的患者由于治疗不足或治疗过度以及由此导致的病态后果而备受煎熬。在本领域需要有诊断ILD的方法。发明概要本公开提供了用于诊断间质性肺病(ILD)的方法。本公开提供了用于区别诊断特发性肺纤维化与其它ILD的方法。还提供了可用于执行主题方法的组合物和试剂盒。本公开提供了用于评估肺组织的方法,该方法包括:a)确定在图6A-27E、33A-B、或34A-B中的任一个或在表3、5、8和9中的任一个中列出的一个或多个基因的基因产物在从患者获得的肺组织样品中的表达水平,生成表达水平值;和b)通过比较该表达水平值与参考表达水平值将该肺组织样品分类为间质性肺病(ILD)组织样品。本公开提供了诊断患者体内间质性肺病(ILD)的方法,该方法包括:a)确定在图6A-27E、33A-B、或34A-B中的任一个或在表3、5、8和9中的任一个中列出的一个或多个基因的基因产物在从疑似患有ILD的患者获得的肺组织样品中的表达水平;和b)根据该表达水平值与参考表达水平值的比较提供ILD的诊断。本公开提供了诊断患者体内间质性肺病(ILD)的方法,该方法包括:a)在从疑似患有ILD的患者获得的肺组织样品中测定在图6A-27E、33A-B、或34A-B中的任一个或在表3、5、8和9中的任一个中列出的一个或多个基因的基因产物的表达水平,生成表达水平值;b)当表达水平值与参考基因表达水平值有显著差异时,将患者鉴定为患有ILD;和c)根据所述鉴定输出指示患者患有ILD的报告,以促成临床医师的治疗决定。本公开提供了诊断患者体内间质性肺病(ILD)的方法,该方法包括:a)在从疑似患有ILD的患者获得的肺组织样品中测定在图6A-27E、33A-B、或34A-B中的任一个或在表3、5、8和9中的任一个中列出的一个或多个基因的基因产物的表达水平,生成表达水平值;和b)将该表达水平值输入到计算机中,其被编程执行比较表达水平值与参考基因表达水平值的算法,并确定该表达水平值与参考表达水平值是否有显著差异,所述输入生成该算法的运行结果;和c)生成提供该结果的报告。本公开提供了诊断患者体内特发性肺纤维化(IPF)的方法,该方法包括:a)在从疑似患有间质性肺病的患者获得的肺组织样品中确定在图9A-9D、10A-10G、19A-22C和33A-B中的任一个或在表4中列出的一个或多个基因的基因产物的表达水平,生成表达水平值;b)当该表达水平值与参考表达水平值有显著差异时,将患者鉴定为患有IPF。在相关实施方案中,ILD是特发性肺纤维化、结节病、哈曼-里奇综合征、抗合成酶综合征、矽肺、石棉肺、铍中毒、超敏感性肺炎,或非特异性间质性肺炎。在进一步相关的实施方案中,ILD与选自下组的结缔组织疾病有关:系统性硬化症、多发性肌炎、系统性红斑狼疮,或类风湿性关节炎。在进一步的实施方案中,ILD是药物诱发的,或者是由病毒感染、细菌感染或肺结核导致的。在本公开方法的一些实施方案中,该诊断可提供对ILD和无ILD的诊断。在本公开方法的一些实施方案中,该诊断可提供对ILD类型(例如IPF、超敏感性肺炎、NSIP等)的诊断。在本公开方法的一些实施方案中,该诊断可提供ILD不同类型之间的区别(例如特发性肺纤维化(IPF)与除IPF之外的ILD之间的区别)(例如,IPF对非特发性间质性肺炎;IPF对超敏感性肺炎,等)。在一些实施方案中,该方法中所用基因选自:1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些实施方案中,该方法包括生成总结所述诊断的报告。在一些实施方案中,该方法包括提供治疗ILD的建议。在一些实施方案中,该基因产物是mRNA。在相关实施方案中,该方法包括使用微阵列、基因表达系列分析、印迹(blotting)、逆转录聚合酶链式反应、测序或定量聚合酶链式反应来确定mRNA的水平。在一些实施方案中,表达水平相对于至少一个参考基因的RNA转录本的表达水平进行标准化。在一些实施方案中,该方法包括获得样品中基因的基因产物的标准化表达,并将该标准化的表达水平与至少2个不同系列生物标记物的基因表达数据进行比较,每个系列生物标记物的基因表达数据包括与一种或多种组织类型存在相关联的一个或多个参考基因表达水平,其中所述表达水平与所述至少两个系列生物标记物的基因表达数据顺次进行比较。在相关的实施方案中,顺次比较结束于通过使用一个主要分类器(classifier)对所述表达水平进行分析而将所述表达水平与最终系列生物标记物的基因表达数据进行比较,所述主要分类器从来自一个或多个系列生物标记物的基因表达数据获得。在一些实施方案中,方法涉及对在图6A-27E、图33A-B、图34A-B、表3、表5、表8和/或表9的任何一个或多种中列出的基因进行分析。本公开的方法包括修改患者疗法的方法,该方法包括:根据本公开的方法诊断患者的间质性肺病(ILD),和根据所述诊断修改患者的疗法。本公开的方法包括修改患者疗法的方法,该方法包括:根据本公开的方法诊断患者的间质性肺病(ILD),和治疗个体的ILD。例如,如果诊断表明个体患有特发性肺纤维化,则所述治疗步骤包括向个体施加有效量的吡非尼酮、强的松、硫唑嘌呤、或N-乙酰半胱氨酸。本公开提供了包含多个核酸的阵列,其每一个可以和如下的基因杂交,其在从被测试间质性肺病的个体获得的组织样品中存在的细胞中差异性表达。本公开提供了用于分析肺组织样品的试剂盒,该试剂盒包括本公开的阵列和用于分析基因产物表达水平的试剂。附图简述图1描述了使用30基因标识(genesignature)的IPF对NSIP的分类错误率(classificationerrorrate)。图2描述了使用30基因标识的IPF对NSIP的分类。图3描述了使用50基因标识的IPF对正常的分类错误率。图4描述了使用50基因标识的IPF对正常的分类。图5提供了用于本公开方法的计算机化系统的一般原理图。图6A和6B提供了使用微阵列数据在IPF和NSIP之间差异表达的基因。图7提供了使用RNA-Seq在IPF和NSIP之间差异表达的基因。图8提供了使用RNA-Seq在IPF和NSIP之间差异表达的基因。图9A-27E提供了可作为合适生物标记物的差异表达基因的列表。图28A-E描述了ILD分类器的准确度。图29A-C描述了分类器比较。图30描述了IPF表达信号假设。图31描述了使用9基因标识的IPF对NSIP的分类错误率。图32描述了使用15基因标识的IPF对NSIP的分类错误率。图33A-B是可用于IPF对其余/非IPF分类的生物标记物的列表。图34A-B是可用于IPF对ILD炎症的生物标记物的列表。图35提供了ENSEMBL标识符(identifier)和相应的基因符号。定义如本文所使用的,“间质性肺病”或“ILD”(也称作弥散性实质性肺病(DPLD))是指一组可影响间质组织(肺泡周围的组织和空间)的肺病。ILD可以根据怀疑的或已知的原因进行分类,或者可以是特发性的。例如,ILD可分类为由吸入物质(无机或有机)引起的,药物诱导的(例如,抗生素、化疗药物、抗心律失常药、他汀类药物)、与结缔组织疾病(例如,全身性硬化症、多发性肌炎、皮肌炎、系统性红斑狼疮、类风湿关节炎)相关的、与肺部感染(例如,非典型肺炎、肺囊虫肺炎(PCP)、肺结核、沙眼衣原体、呼吸道合胞病毒)相关的、与恶性肿瘤(例如,淋巴管癌)相关的,或者可以是特发性的(例如,结节病、特发性肺纤维化、哈曼-里奇综合征、抗合成酶综合征)。如本文所使用的,“ILD炎症”是指以潜在炎症为特征的炎性ILD亚型的分析分组(analyticalgrouping)。这些亚型可以共同用作相对于IPF和/或任何其它非炎性肺部疾病亚型的比较者。“ILD炎症”可以包括HP、NSIP、结节病、和/或机化性(organizing)肺炎。“特发性间质性肺炎”或“IIP”(也被称为非感染性肺炎)是指一类ILD,其包括,例如,脱屑性间质性肺炎、非特异性间质性肺炎、淋巴样间质性肺炎、隐源性机化性肺炎和特发性肺纤维化。如本文所使用的,“特发性肺纤维化”或“IPF”是指一种慢性渐进形式的肺病,其特征在于所述肺部支撑框架(间质)的纤维化。根据定义,该术语在肺纤维化的病因未知的时(“特发性”)使用。在显微镜下,来自患有IPF的患者的肺组织显示特征性的一组组织学/病理学特征,其被称为普通型间质性肺炎(UIP),这是IPF的病理对应。“非特异性间质性肺炎”或“NSIP”是特发性间质性肺炎的一种形式,其一般的特征是连续或片状的由慢性炎性细胞与胶原沉积限定的细胞模式(cellularpattern),和由弥散片状纤维化限定的纤维化模式。与UIP不同,没有作为普通型间质性肺炎特征的蜂窝状外观和成纤维细胞灶。“超敏感性肺炎”或“HP”也被称为外源性过敏性肺泡炎(EAA),是指肺部由于对吸入抗原(例如,有机灰尘)的过大免疫反应和过敏造成的肺泡炎症。“肺结节病”或“PS”是指涉及能够形成结节的慢性炎症细胞的异常集合(肉芽肿)的综合征。HP的炎症过程一般涉及肺泡、小支气管和小血管。在HP的急性和亚急性病例中,体检通常会显示干性罗音。术语“微阵列”是指可杂交阵列元件,优选地多核苷酸探针,在基片上的有序排列。在以单数或复数使用时,术语“多核苷酸”一般是指任何多聚核糖核苷酸或多聚脱氧核糖核苷酸,其可以是未修饰的RNA或DNA或经过修饰的RNA或DNA。因此,例如,如本文所定义的多核苷酸包括,但不仅限于,单链和双链DNA,包含单链和双链区的DNA,单链和双链RNA,和包含单和双链区的RNA,包含DNA和RNA的杂合分子,其可以是单链或更典型地双链的,或者包含单链和双链区域的杂合分子。此外,如本文所使用的,术语“多核苷酸”是指包含RNA或DNA或RNA和DNA两者的三链区。这样的区域中的链可以来自相同的分子或来自不同分子。该区域可以包括一个或多个分子的全部,但更典型地仅涉及一些分子的一个区域。具有三螺旋区的分子常常是寡核苷酸。术语“多核苷酸”也可包括含有一个或多个修饰碱基(例如,用于提供可检测信号,例如荧光团)的DNA(例如,cDNA)和RNA。因此,出于稳定性或其它原因具有经过修饰的骨架的DNA或RNA是本文所预期术语的“多核苷酸”。而且,包含稀有碱基(例如肌苷,或经修饰的碱基,如氚化碱基)的DNA或RNA也包括在如本文所定义的术语“多核苷酸”中。一般来说,术语“多核苷酸”包括未修饰多核苷酸的所有化学、酶学和/或代谢修饰形式,以及病毒和细胞(包括简单和复杂细胞)的DNA和RNA特性的化学形式。术语“寡核苷酸”是指相对短的多核苷酸(例如,100,50,20或更少的核苷酸),包括但不仅限于,单链脱氧核糖核苷酸、单链或双链核糖核苷酸、RNA:DNA杂交体和双链DNA。寡核苷酸,例如单链DNA探针寡核苷酸,通常是通过化学方法合成的,例如使用商业上可得的自动化寡核苷酸合成仪。然而,寡核苷酸可通过多种其它方法制备,包括体外重组DNA介导的技术和通过在细胞和生物体中表达DNA。如本文所使用的,术语“基因产物”或“表达产物”可互换使用,是指基因的RNA转录产物(RNA转录本),包括mRNA,以及这些RNA转录本的多肽翻译产物。基因产物可以是,例如,多核苷酸的基因表达产物(例如,未剪接的RNA、mRNA、剪接变体mRNA、microRNA、片段化的RNA,等等)或蛋白表达产物(例如,成熟多肽、翻译后修饰的多肽、剪接变体多肽,等等)。当用于基因表达产物时,术语“标准化的表达水平”是指基因产物相对于一个或多个参考(或对照)基因表达产物进行标准化的水平。当用于基因表达产物时,“参考表达水平值”是指用于一个或多个参考(或对照)基因表达产物的表达水平值。当用于基因表达产物时,“参考标准化表达水平值”是指用于一个或多个参考(或对照)基因表达产物的标准化表达水平值。杂交反应的“严格度”是本领域普通技术人员容易确定的,通常是根据探针长度、洗涤温度和盐浓度的经验性计算。一般地,较长的探针要求较高的温度以便正确退火,而较短的探针需要较低的温度。杂交通常取决于当互补链所在的环境温度低于其熔解温度时,变性的DNA重新退火的能力。探针和可杂交序列之间的期望同源性程度越高,可使用的相对温度越高。结果,相对温度越高,趋向于使反应条件越严格,而温度越低则严格度越小。关于杂交反应严格度的更多细节和解释,参见Ausubel等,CurrentProtocolsinMolecularBiology,(WileyInterscience,1995)。如本文定义的,“严格条件”或“高严格条件”通常为:(1)采用低离子强度溶液和高温用于洗涤,例如0.015M氯化钠/0.0015M柠檬酸钠/0.1%十二烷基硫酸钠,在50℃;(2)在杂交过程中采用变性剂,例如甲酰胺,例如,50%(v/v)甲酰胺与0.1%牛血清白蛋白/0.1%Ficoll/0.1%聚乙烯吡咯烷酮/50mM磷酸钠缓冲液(pH6.5)和750mM氯化钠,75mM柠檬酸钠,在42℃;(3)采用50%甲酰胺,5xSSC(0.75M氯化钠,0.075M柠檬酸钠),50mM磷酸钠(pH6.8),0.1%焦磷酸钠,5xDenhardt氏溶液,声处理的鲑鱼精DNA(50μg/ml),0.1%SDS和10%硫酸右旋糖酐,在42℃,及在42℃用0.2xSSC(氯化钠/柠檬酸钠)洗涤和在55℃用50%甲酰胺洗涤,随后进行高严格性洗涤,包括含有EDTA的0.1xSSC,在55℃。“中等严格条件”可以如Sambrook等,MolecularCloning:ALaboratoryManual(ColdSpringHarborPress,1989)所述鉴定,并且包括使用如上所述的严格性较小的洗涤溶液和杂交条件(例如温度、离子强度和%SDS)。中等严格条件的一个实例是,在包含20%甲酰胺,5xSSC(150mMNaCl,15mM柠檬酸三钠)、50mM磷酸钠(pH7.6)、5xDenhardt氏溶液、10%硫酸右旋糖酐和20mg/ml变性剪切的鲑鱼精DNA的溶液中在37℃过夜温育,接着用1×SSC在大约37-50℃对滤器进行洗涤。技术人员会认识到如何根据需要调整温度、离子强度等以适应如下因素,例如探针长度等。如本文所使用的,“灵敏度”是指真实具有目标病症的真实阳性者在测试总数中的比例(也就是,具有阳性测试结果的患有目标病症的患者的比例)。如本文所使用的,“特异性”是指实际上不具有目标病症的真实阴性者在所有测试患者中的比例(也就是,具有阴性测试结果的不患有目标病症的患者的比例)。在本发明的上下文中,指称任何特殊基因系列中列举的“至少一个”、“至少两个”、“至少五个”等的意思是,所列基因的任何一个或任何多个或所有的组合。术语“剪接”和“RNA剪接”可互换使用,是指去除内含子并连接外显子以产生具有连续编码序列并移动到真核细胞细胞质中的成熟mRNA的RNA加工。术语“外显子”是指中断基因的任何节段,其在成熟的RNA产物中存在(B.Lewin,GenesIV(CellPress,1990))。在理论上,术语“内含子”是指被转录但通过其任一侧的外显子的剪接而被从转录本中除去的任何DNA节段。在操作上,外显子序列出现在如Ref.SEQID编号所定义的基因的mRNA序列中。在操作上,内含子序列是基因的基因组DNA中的居间序列,被外显子序列包围,通常在其5'和3'边界处具有GT和AG剪接共有序列。“基于计算机的系统”是指用于分析信息的由硬件、软件和数据存储介质构成的系统。患者的基于计算机的系统的最少硬件包括中央处理单元(CPU),和用于数据输入、数据输出(例如显示)和数据存储的硬件。普通技术人员可以很容易意识到,任何目前可得的基于计算机的系统和/或其组件均适用于和本发明的方法结合使用。数据存储介质可以包括任何制成品(manufacture),包括记录上述的信息,或者可以访问这种制成品的记忆存储装置。为了“记录”数据,计算机可读介质上的程序或其它信息是指用于存储信息的处理,其使用本领域已知的任何这类方法。可以根据访问存储信息的方法选择任何方便的数据存储结构。有大量数据处理器程序和格式可用于存储,例如Word处理文本文件、数据库格式,等。“处理器”或“计算机装置”是指任何可执行其所需功能的硬件和/或软件的组合。例如,合适的处理器可以是可编程的数字微处理器,例如可以作为电子控制器、大型机、服务器或个人计算机(台式或便携式)的形式提供。当处理器可以编程时,合适的程序可以在远程位置与处理器通讯,或者先前被保存在计算机程序产品中(例如,便携式或固定计算机可读存储介质,无论是基于磁、光还是固态装置)。例如,磁介质或光盘可以携带程序,并且可以通过合适的读取器阅读,与相应工作站的每个处理器进行通讯。在进一步描述本发明之前,应当理解,本发明并不仅限于所述的特殊实施方案,其本身当然是可以变化的。还应当理解,本文所用的专有名词只是出于描述特殊实施方案的目的,并不意图具有限制,因为本发明的范围只由所附权利要求限制。当提供一个数值范围时,应当理解,除非上下文另有明确说明,否则本发明包括该范围上限和下限之间的每一个中间值,直至下限单位的十分之一,以及所述范围内的任何其它所述值或中间值。这些较小范围的上限和下限可以独立地包含在较小的范围内,并且也包含在本发明之内,服从于所述范围中任何具体排除意义的界限。当所述范围包括一个或两个极限时,不包括所含极限的任一个或两个的范围也包括在本发明中。除非另有定义,否则本文使用的所有技术和科学术语具有与本发明所属领域普通技术人员所通常理解的相同的含义。虽然在实践或测试本发明时也可以使用与本文所述相似或等价的任何方法和材料,但是现在描述的是优选的方法和材料。本文引用这里所提到的所有出版物作为参考,以联系所引用的出版物公开和描述这些方法和/或材料。必须注意,如本文和附加权利要求中所使用的,除非上下文另有明确说明,否则单数形式“一”,“一个”和“该”包括复数受试者。因此,例如,指称“一种基因产物”包括多个这样的基因产物,指称“该算法”包括指称一种或多种本领域技术人员已知的算法和等价物,等等。还应当注意,权利要求书可以撰写成排除任何任选的元素。因此,本声明意图作为与权利要求元素的记载相联使用这些排除性术语如“仅”、“只”等或使用“负”限制的先行基础。应当认识到,为清楚起见,在不同实施方案的上下文中描述的本发明的某些特征,也可以组合地在单个实施方案中提供。相反,为简洁起见,在单个实施方案的上下文中描述的本发明的各种特征,也可以分别提供或者以任何合适的亚组合提供。本发明实施方案的所有组合被具体地包含在本发明中,并且在本文中公开,就如同每个组合被单独而明确地被公开一样。此外,各种实施方案及其元件的所有亚组合也被具体地包含在本发明中,就如同每个这样的组合被单独而明确地被公开一样。提供本文中讨论的公开只是由于它们的公开早于本申请的归档日期。在这里没有任何内容可以被解释为:我们承认由于它们是先前发明,所以本发明不会早于这些公开。此外,提供的公开日期可能与其真实的公开日期不同,这可能需要单独地确认。详细说明本公开提供了用于诊断间质性肺病(ILD)的方法。本公开提供了用于区别诊断特发性肺纤维化与其他ILD的方法。还提供了可用于执行主题方法的组合物和试剂盒。用于评估肺组织样品的方法本公开提供了用于评估肺组织的方法,该方法一般包括:a)确定在图6A-27E、33A-B、或34A-B中的任一个,或在表3、5、8和9中的任一个,或在实施例3中列出的基因的基因产物在从患者获得的肺组织样品中的表达水平,生成表达水平值;和b)通过比较该表达水平值(例如,标准化的表达水平值)与基于包含ILD组织的人群研究的基因表达数据,将该肺组织样品分类为ILD组织样品。用于诊断间质性肺病的方法本公开提供了用于诊断间质性肺病(ILD)的方法,该方法一般包括确定在图6A-27E、33A-B、或34A-B中的任一个,或在表3、5、8和9中的任一个,或在实施例3中列出的基因的基因产物在从患者获得的肺组织样品中的表达水平(例如,标准化的表达水平值),生成表达水平值;和通过比较该表达水平值(例如,标准化的表达水平值)与基于包含ILD组织的人群研究的基因表达数据,将该肺组织样品分类为间质性肺病(ILD)组织样品。“ILD”是指一组影响间质(肺的肺泡周围的组织和空间)的肺病。受ILD影响的肺组织包括肺泡上皮细胞,肺毛细血管内皮细胞,基底膜,血管周围和外淋巴肺组织。ILD可分为七个主要组:医源性或药物引起的;职业或环境性的;肉芽肿性疾病,包括肺结节病胶原血管疾病;独特性实体(uniqueentities),如肺泡蛋白沉积症,朗格汉斯细胞肉芽肿,和淋巴管肌瘤;特发性间质性肺炎,包括特发性肺纤维化(IPF);和遗传性疾病,如结节性硬化症,神经纤维瘤病,代谢贮积症和Hermansky-Pudlak综合症。ILD包括,但不仅限于,特发性肺纤维化;淋巴管肌瘤病;非特异性间质性肺炎;隐源性机化性肺炎;急性间质性肺炎;呼吸性细支气管炎伴间质性肺病;脱屑性间质性肺炎;淋巴细胞性间质性肺炎;和肺结节病。ILD可能伴有选自下组的结缔组织疾病:系统性硬化症、多肌炎、系统性红斑狼疮、或类风湿性关节炎。间质性肺病也可以是药物引起的,例如,抗生素、化疗剂、抗心律失常剂、他汀类药物、和类似物。ILD还可能是病毒感染、细菌感染或结核病导致的。在执行主题诊断方法时,可以测定基因表达产物(“生物标记物”)或一系列(“组”)生物标记物(例如“基因系列”)的表达水平。用于本公开方法的生物标记物的实例包括图6A-27E、33A-B、或34A-B,表3、5、8和9,和实施例3中的基因的基因产物。本方法和组合物构想了使用“生物标记物组”用于鉴定、分类、诊断或者表征生物样品。方法和组合物还可以使用多组生物标记物组,在本文中称作“分类组”,其实例可见于图6A-27E、33A-B或34A-B,和表3、4、8和9的每一个中。每组生物标记物的基因表达水平的模式(或“标识”(signature))可以被确定,然后用于评估生物样品中相同组生物标记物的标识,例如通过测量样品标识与参考标识之间的相似性。在一些实施方案中,该方法涉及测量(或获得)生物标记物组和/或分类组中两个或多个基因表达产物的水平。例如,在一些实施方案中,生物标记物组或分类组可以包含至少1,2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34,35,36,37,38,39,40,41,42,43,44,45,46,47,48,49,或50或更多个不同的生物标记物。在一些实施方案中,生物标记物组或分类组包含不超过1,2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34,35,36,37,38,39,40,41,42,43,44,45,46,47,48,49,或50个不同的生物标记物。在一些实施方案中,分类组包含至少1,2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或30个不同的生物标记物组。在其他实施方案中,分类组包含不超过1,2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或30个不同的生物标记物组。在一些实施方案中,本公开提供了鉴定、分类、或诊断ILD的方法,包括以下步骤:获得生物样品的一个或多个基因表达产物的表达水平;和当生物样品中的基因表达水平指示不存在所测定的ILD时,将该生物样品鉴定为缺少所测ILD的指示。在一些实施方案中,本发明提供了鉴定、分类、或诊断ILD的方法,包括以下步骤:获得生物样品的一个或多个基因表达产物的表达水平;和当生物样品中的基因表达水平指示所测定的ILD时,将该生物样品鉴定为受到所测ILD的影响。例如,这可以通过将在本文所述分类组中限定的基因表达水平的模式与样品的基因表达水平进行关联,以鉴定(或排除)生物样品中存在ILD。在一些实施方案中,本公开提供了使用本文所述的主题方法鉴定、分类、或诊断ILD的方法,以提供至少50%或70%的特异性和灵敏度,其中基因表达产物水平在生物样品与生物标记物组之间,或在生物样品与分类组之间进行比较;和根据基因表达谱的比较将生物样品鉴定为受到或不受所测ILD的影响。在一些实施方案中,本方法的特异性为至少50%,60%,70%,75%,80%,85%,86%,87%,88%,89%,90%,91%,92%,93%,94%,95%,96%,97%,98%,或99%。在一些实施方案中,本发明的灵敏度为至少50%,60%,70%,75%,80%,85%,86%,87%,88%,89%,90%,91%,92%,93%,94%,95%,96%,97%,98%,或99%。在一些实施方案中,本发明的特异性为至少50%且灵敏度为至少50%。在一些实施方案中,本发明的特异性为至少70%且灵敏度为至少70%。在一些实施方案中,本发明的特异性为至少50%且灵敏度为至少70%。在一些实施方案中,标称特异性(nominalspecificity)大于或等于50%。在一些实施方案中,标称特异性大于或等于70%。在一些实施方案中,标称阴性预测值(NPV)大于或等于95%。在一些实施方案中,NPV是至少90%,91%,92%,93%,94%,95%,95.5%,96%,96.5%,97%,97.5%,98%,98.5%,99%,99.5%(例如,90%,91%,92%,93%,94%,95%,95.5%,96%,96.5%,97%,97.5%,98%,98.5%,99%,99.5%,或100%),特异性(或阳性预测值(PPV))为至少30%,35%,40%,50%,60%,70%,80%,90%,95%,95.5%,96%,96.5%,97%,97.5%,98%,98.5%,99%,或99.5%(例如,30%,35%,40%,50%,60%,70%,80%,90%,95%,95.5%,96%,96.5%,97%,97.5%,98%,98.5%,99%,99.5%,或100%)。在某些情况下,NPV是至少95%且特异性为至少50%。在某些情况下,NPV是至少95%且特异性为至少70%。在一些实施方案中,在相互比较的样品亚型或系列之间,基因表达存在特异性(或一定范围)的差异。在一些实施方案中,一些相似的基因表达被合并形成一超类,然后再与另一个亚型或另一个超类或所有其他亚型的系列进行比较。在一些实施方案中,基因表达水平的差异为至少5%,10%,15%,20%,25%,30%,35%,40%,45%或50%或更多。在一些实施方案中,基因表达水平的差异为至少2,3,4,5,6,7,8,9,10倍或更高。在一些实施方案中,生物样品被鉴定为具有ILD(例如,IPF,NSIP,等),准确度为至少50%,60%,70%,75%,80%,85%,90%,95%,99%或更高。在一些实施方案中,生物样品被鉴定为具有ILD,准确度大于50%,60%,70%,75%,80%,85%,90%,95%,99%或更高。在一些实施方案中,准确度用已经训练的算法进行计算。在一些实施方案中,生物样品被鉴定为受ILD影响(例如,受所选ILD的影响),灵敏度大于50%或70%。在一些实施方案中,生物样品被鉴定为受ILD影响(例如,受所选ILD的影响),特异性大于50%或70%。在一些实施方案中,生物样品被鉴定为受ILD影响(例如,受所选ILD的影响),灵敏度大于50%并且特异性大于70%。在一些实施方案中,方法使用一组生物标记物(例如,生物标记物组、分类组、分类器),使得该方法的特异性大于50%,70%,75%,80%,85%,86%,87%,88%,89%,90%,91%,92%,93%,94%,95%,96%,97%,98%,99%,或99.5%,灵敏度大于50%,70%,75%,80%,85%,86%,87%,88%,89%,90%,91%,92%,93%,94%,95%,96%,97%,98%,99%,或99.5%。在一些实施方案中,方法使用一组生物标记物(例如,生物标记物组、分类组、分类器),使得该方法的阳性预测值为至少95%,95.5%,96%,96.5%,97%,97.5%,98%,98.5%,99%,99.5%或更高;和/或阴性预测值为至少95%,95.5%,96%,96.5%,97%,97.5%,98%,98.5%,99%,99.5%或更高。在一些实施方案中,方法使用一组生物标记物(例如,生物标记物组、分类组、分类器),使得该方法的特异性或灵敏度大于50%,70%,75%,80%,85%,86%,87%,88%,89%,90%,91%,92%,93%,94%,95%,96%,97%,98%,99%,或99.5%,阳性预测值或阴性预测值为至少95%,95.5%,96%,96.5%,97%,97.5%,98%,98.5%,99%,99.5%或更高。在一些实施方案中,方法使用一组生物标记物(例如,生物标记物组、分类组、分类器),使得该方法的阴性预测值为至少95%,95.5%,96%,96.5%,97%,97.5%,98%,98.5%,99%,99.5%或更高。在一些实施方案中,本公开提供了基因表达产物,其相应于从在图6A-27E、33A-B或34A-B和表3,4,8,和9,以及实施例3中列出的那些中选出的生物标记物。本文提供的方法和组合物可以包括相应于从图6A-27E、33A-B或34A-B和表3,4,8,和9,以及实施例3中选出的任何或全部生物标记物,及其任何亚系列和任意组合。例如该方法可以使用的基因表达产物相应于在图6A-27E、33A-B或34A-B和表3,4,8,和9,以及实施例3中提供的至少1,2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34,35,36,37,38,39,40,41,42,43,44,45,46,47,48,49,或50种或更多种生物标记物。在某些情况下,某些生物标记可以被排除或被其他生物标记物取代,例如用相对于特定组织类型或亚类型显示出相似表达水平谱的生物标志物。标记物组可以被选择以便能够充分区分受ILD影响的和不受ILD影响的,和/或区分受第一ILD影响的患者与受不同于第一ILD的第二ILD影响的患者。这种多维分类器(即算法)的训练可以在大量生物样品上进行,例如至少50,100,200,300,400,500,600,700,800,900,1000,1500,2000,2500,3000,3500,或4000个生物样品(例如,肺组织样品)。在一些实施方案中,使用许多训练/测试系列开发初步算法。整体算法错误率可以被示出为ILD对非-ILD(或第一ILD对第二ILD)样品的基因数目的函数。在一些实施方案中,可以使用其他的性能度量(performancemetric),例如是ILD对非-ILD(或第一ILD对第二ILD)的基因数目的函数的性能度量。这样的性能度量可以使用交叉验证,或本领域中已知的其它方法获得。所有结果可以使用支持向量机模型(supportvectormachinemodel)或其他分类方法获得,其中这些分类方法在样品上以交叉验证模式进行训练和测试。本公开的方法能够方便ILD的诊断,其是通过比较在图6A-27E、33A-B或34A-B中的任一个,或在表3,4,8,和9中的任一个,或者在实施例3中列出的一个或多个基因的基因产物的表达水平,确定这些表达水平是否与参考表达水平(相同基因的基因产物在具有已知指示(例如,不受影响或受影响)的组织中的表达水平)具有显著差异。在图6A-27E、33A-B或34A-B中的任一个,或在表3,4,8,和9中的任一个,或者在实施例3中,给定基因的负数logFC值表明给定基因的基因产物在第一疾病适应症(例如IPF)组织中的表达水平低于参考表达水平(例如,给定基因的基因产物在第二适应症(例如NSIP)组织中的表达水平)。参考表达水平可以是在第二疾病适应症中的基因表达水平,或者可以是在正常(非疾病)组织中的基因表达水平。因此,给定基因的负数logFC值表明,表达的降低与第一疾病适应症的存在相关联。相反,给定基因的正数logFC值表明给定基因的基因产物在第一疾病适应症(例如IPF)组织中的表达水平高于参考表达水平(例如,给定基因的基因产物在第二适应症(例如NSIP)组织中的表达水平)。参考表达水平可以是在第二疾病适应症中的基因表达水平,或者可以是在正常(非疾病)组织中的基因表达水平。因此,给定基因的负数/正数logFC值表明,表达的降低/增加与第一疾病适应症的存在相关联。在一个实施方案中,给定基因产物的表达水平可以和通过对大量个体的肺组织样品的基因表达水平进行分析的群体研究中获得的参考表达水平进行比较。包括使用参考表达水平值(例如,参考标准化表达水平值)的本公开方法包括使用代表一个或多个参考(或对照)基因的表达水平(例如标准化表达水平)的参考表达水平值。代表超过一个参考(或对照)基因的表达水平的参考表达水平值可以通过对参考表达水平值(例如,参考标准化表达水平值)采用一种算法以提供一个得分而提供,其中该得分代表诊断指示的阈值(也称作“阈值”或“截止值”)(例如,高于阈值得分的测试得分表明ILD的诊断或ILD的区别诊断(例如IPF对NISP)。在一个实施方案中,LogFC值可以使用测试基因表达水平与参考基因表达水平相比增加或降低的阈值水平,以便根据所选比较帮助ILD的诊断,例如IPF对NSIP等。这类LogFC值的非限制性实例在图6A-27E,33A-B,和34A-B,和表3,4,8,和9中提供。具有期望LogFC值的基因可以被选择作为训练分类算法中的特征。例如,可以使用大于1.2或小于-1.2的LogFC值鉴定其信号可以被各种算法使用以实现分类的基因。诊断超敏感性肺炎本公开提供了诊断ILD的方法,其中ILD是超敏感性肺炎(HP)。在一些情况下,该方法涉及在来自受试者的肺组织样品中确定在图14-16中列出的基因的基因产物的表达水平(例如,标准化基因表达水平)。例如,当图14-16中一个或多个基因的基因产物的表达水平(例如,标准化基因表达水平)与该基因产物的阈值基因表达水平有显著差异时,指示HP的诊断。在一些情况下,本发明方法涉及在受试者的肺组织样品中确定从图14-16的任一个中选出的一个或多个基因的基因产物的表达水平(例如,标准化基因表达水平),其中该一个或多个基因可以是一系列从图14-16的任一个中所提基因中选出的2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34,35,36,37,38,39,40,41,42,43,44,45,46,47,48,49,或50或更多个基因。诊断非特异性间质性肺炎本公开提供了诊断ILD的方法,其中ILD是非特异性间质性肺炎(NSIP)。在一些情况下,该方法涉及在来自受试者的肺组织样品中确定在图11A-11F,12,25,和26A-26E的任一个中列出的一个或多个基因的基因产物的表达水平(例如,标准化基因表达水平)。例如,当图11A-11F,12,25,和26A-26E的任一个中的基因的基因产物的表达水平(例如,标准化基因表达水平)与该基因产物的阈值基因表达水平有显著差异时,指示NSIP的诊断。在一些情况下,主题方法涉及在受试者的肺组织样品中确定从图11A-11F,12,25,和26A-26E的任一个中选出的一个或多个基因的基因产物的表达水平(例如,标准化基因表达水平),其中该一个或多个基因可以是一系列从图11A-11F,12,25,和26A-26E的任一个中所列出基因中选出的2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34,35,36,37,38,39,40,41,42,43,44,45,46,47,48,49,或50或更多个基因。诊断特发性肺纤维化本公开提供了诊断ILD的方法,其中ILD是IPF。在一些情况下,该方法涉及在来自受试者的肺组织样品中确定在图9A-9D,10A-10G,19A-22C,和33A-B或表4的任一个中列出的一个或多个基因的基因产物的表达水平(例如,标准化基因表达水平)。例如,当图9A-9D,10A-10G,19A-22C,和33A-B或表4的任一个中的基因的基因产物的表达水平(例如,标准化基因表达水平)与该基因产物的阈值基因表达水平有显著差异时,指示IPF的诊断。在一些情况下,主题方法涉及在受试者的肺组织样品中确定从图9A-9D,10A-10G,19A-22C,和33A-B或表4的任一个中选出的一个或多个基因的基因产物的表达水平(例如,标准化基因表达水平),其中该一个或多个基因可以是一系列从图9A-9D,10A-10G,19A-22C,和33A-B或表4的任一个中所列出基因中选出的2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34,35,36,37,38,39,40,41,42,43,44,45,46,47,48,49,或50或更多个基因。在一些情况下,主题方法涉及在受试者的肺组织样品中确定从表4中选出的一个或多个基因的基因产物的表达水平(例如,标准化基因表达水平),其中该一个或多个基因可以是一系列从表4中所列出基因中选出的2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34,35,36,37,38,39,40,41,42,43,44,45,46,47,48,49,或50或更多个基因。例如,在一些情况下,主题方法涉及在受试者的肺组织样品中确定从下列选出的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34,35,36,37,38,39,40,41,42,43,44,45,46,47,48,49,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)THY1;2)GALNT13;3)CFH;4)CRTAC1;5)CHD3;6)TSHZ2;7)ENSG00000123119;8)ISM1;9)ENSG00000236972;10)PDE7B;11)SULF1;12)FABP5;13)FABP5;14)PTGFRN;15)IGFBP5;16)CFHR1;17)MS4A15;18)FAM13C;19)STC1;20)RCAN2;21)LG12;22)CCND2;23)DCLK1;24)C22orf46;25)IGF1;26)CSF3R;27)PPP4R4;28)CEBPD;29)NMNAT2;30)EPB41L5;31)ZNF385D;32)FCN3;33)CNTN6;34)DGKA;35)CSGALNACT1;36)SYT15;37)STX11;38)ITSN1;39)TMEM100;40)EGFLAM;41)C13orf15;42)ENSG00000182010;43)ERRFI1;44)RGS16;45)SLN;46)ENSG00000146374;47)TCID8066275;48)CSCL2;49)ITLN1;和50)PDE2A。区别诊断特发性肺纤维化对非特异性间质性肺炎本公开提供了区别诊断IPF对NSIP的方法。该方法一般地涉及在来自受试者的肺组织样品中确定在图6A-8和表3和8的任一个中列出的基因的基因产物的标准化表达水平。在一些情况下,主题方法涉及在受试者的肺组织样品中确定从图6A-8,表3和8,和实施例3中列出的基因中选出的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34,35,36,37,38,39,40,41,42,43,44,45,46,47,48,49,或50或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平)。在一些情况下,主题方法涉及在受试者的肺组织样品中确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,或15个基因)的基因产物的表达水平(例如,标准化基因表达水平):CDKL2,CEACAM1,DST,EDIL3,HLA-F,KIF18A,LMOD1,MSRB3,MYH11,MYLK,PPP1R3C,PTCHD4,PTTG1,TMEM47,和TTLL7。在一些情况下,主题方法涉及在受试者的肺组织样品中确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或30个或更多基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定ASPM基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定BUB1基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定PTTG1基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定SHCBP1基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定NUSAP1基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定MKI67基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定HJURP基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定CDCA3基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定PKL1基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定PRR11基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定BRCA2基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定ORM1基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定CCNB2基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定SMC4基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定HM13基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定DMD基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定FHL1基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定ORM2基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定NDUFC2-KCTD14基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定NCAPH基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定TTLL7基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定DEPDC1B基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定CNTN4基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定PRKAA2基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定PRKCQ基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定CDC42BPA基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定PARD3B基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;28)SCTR;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定SCTR基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;29)CSF3R;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定CSF3R基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;和30)MPDZ。在一些情况下,主题方法涉及在受试者的肺组织样品中确定MPDZ基因产物的表达水平(例如,标准化基因表达水平)。在这些实施方案的一些中,该方法进一步包括确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;和29)CSF3R。在一些情况下,主题方法涉及在受试者的肺组织样品中确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):ACTA2,ACTG2,AHNAK,AHNAK2,AKT3,ANO2,AOC3,ARHGEF25,ATP1A2,CALD1,CAMK2N1,CD109,CDH13,CNKSR2,CNN1,COL21A1,COPZ2,COX7A1,CRIM1,CRYAB,CSRP1,DENND2A,DES,DGKG,DIXDC1,DMD,DNAJB4,DPYSL3,DST,DTNA,EDIL3,EOGT,EPB41L2,FGF14,FHL1,FMO2,FMO3,GARNL3,HOXA-AS2,HOXA4,HOXA6,HPSE2,LAMA4,LARP6,LHFP,LMCD1,LMOD1,LRRFIP1,MAP1B,MARK1,MCAM,MFAP4,MPDZ,MSRB3,MXRA7,MYH10,MYH11,MYL9,MYLK,MYOCD,NEXN,PALLD,PCDHB10,PCDHGC5,PDE1C,PDE5A,PDLIM3,PEAK1,PGM5,PGM5P2,PHLDB2,PKD2,PKIG,PLCB4,PLCE1,PLN,PPP1R3C,PREX2,PRKAA2,PRKAB2,PRKG1,PRUNE2,PTCHD4,PTPRB,REEP1,RERG,SBF2,SORBS1,SYNM,SYNPO2,TAGLN,TIMP2,TIMP3,TMEM47,TMOD1,TPM1,TPM2,TRPC1,TTLL7,UACA,ZC3H12B。在一些情况下,主题方法涉及在受试者的肺组织样品中确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):ABCA3,ACADSB,ACOXL,ADAR,APOL6,ARHGEF38,ARPC5L,ASPM,ATP11A,ATP2C2,ATP8A1,BUB1,C18orf8,C2,CASC5,CCL4,CCL4L1,CCNA2,CCNB1,CCNB2,CCR5,CD38,CDC45,CDK1,CDKL2,CEACAM1,CFTR,CISH,CLINT1,CNDP2,CRTAC1,CSF3R,CXCL10,CXCL11,CXCL9,CXCR6,DGKD,DLGAP5,DRAM1,DUSP16,EDEM1,EFNA1,EPSTI1,ESRP2,ETV7,EZH2,FHDC1,FOXM1,FZD5,GALNT3,GBP1,GBP5,GPR98,GRAMD1A,GUCD1,HAS3,HERC6,HIST1H2BI,HIST1H2BM,HIST1H3E,HIST1H3J,HLA-A,HLA-B,HLA-C,HLA-DOA,HLA-F,HLA-H,HMMR,IFI35,IRF1,IRF9,KCNJ15,KCNQ3,KCTD14,KIF11,KIF14,KIF18A,KIF4A,LARP4B,LGALS3BP,LNX2,MAP3K13,MAPK13,MARK2,METTL7B,MKI67,MTUS1,NPC1,NUSAP1,OAS2,ORM1,ORM2,PARP14,PARP9,PLAGL2,PRKCQ,PSMB10,PSMB8,PSMB9,PSME1,PSME2,PTTG1,PXMP4,RABGAP1L,RAD51AP1,RAPIGAP,RBM47,RCORl,RFX5,RGS16,RNF145,RNF213,SCTR,SDC4,SDR16C5,SEMA4A,SFTPD,SLC16A13,SLC22A3,SMC4,SNX30,SQSTM1,SREBF2,STAT1,STIL,TAP1,TAPBP,TCID-7896714,TCF19,TKT,TLR2,TMED6,TMEM164,TMEM41B,TOP1,TOP2A,TOX,TRAFD1,TRIM26,TYMP,UBD,UBE2S,USP44,VDR,WARS,WWC1,YARS,ZDHHC16,ZNF385B。区别诊断特发性肺纤维化对超敏感性肺炎本公开提供了区别诊断IPF与超敏感性肺炎(HP)的方法。该方法一般地涉及在来自受试者的肺组织样品中确定在图17和18,表9和实施例3的任一个中列出的基因的基因产物的标准化表达水平。在一些情况下,主题方法涉及在受试者的肺组织样品中确定从图17和18,表9和实施例3中列出的基因中选出的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34,35,36,37,38,39,40,41,42,43,44,45,46,47,48,49,或50或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平)。在一些情况下,主题方法涉及在受试者的肺组织样品中确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):ALDH3A1,DDX3Y,ENSG00000099725,ENSG00000176728,ENSG00000233864,ENSG00000235834,FCRL1,KDM5D,KRT15,LGR6,MMP1,MMP13,NLGN4Y,PAX5,PC,RASGRP2,RPS4Y1,SOX2,TXLNG2P,TXLNG2P,USP9Y;CHIA,EDN3,ENSG00000215874,ENSG00000225076,ENSG00000227597,ENSG00000229155,ENSG00000233339,ENSG00000235027,ENSG00000251521,ENSG00000254139,ENSG00000256282,GALNT13,HLA-DOA,HLA-DQB2,HMGCS2,HSD17B6,LZTS2,PRRG2,SLC17A9,和WFDC12。在一些情况下,主题方法涉及在受试者的肺组织样品中确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,或24个基因)的基因产物的表达水平(例如,标准化基因表达水平):ALDH3A1,DDX3Y,FCRL1,KDM5D,KRT15,LGR6,MMP1,MMP13,NLGN4Y,PAX5,RPS4Y1,SOX2,TXLNG2P,USP9Y,UTY,ZFY,CHIA,EDN3,GALNT13,HLA-DOA,HMGCS2,HSD17B6,PRRG2,WFDC12。在一些情况下,主题方法涉及在受试者的肺组织样品中确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,或24个基因)的基因产物的表达水平(例如,标准化基因表达水平):ACTA2,ACTG2,ARHGEF25,CACNAIC,CALDl,CNNl,COL21A1,DST,EDIL3,GPC6,HERC2P2,HSPA2,KALRN,LINC00328,LMODl,MAPIB,MEIS1,MEOX2,MYH11,MYLK,MYOCD,NBPF3,NEXN,OSMR,PAPPA,PCDHB18,PDE3A,PLXNA4,PRUNE2,PTCHD4,PTGFRN,SCRG1,SLC25A27,SLIT3,SOGA1,SORBS1,SYNPO2,TAGLN,TCID-7906969,TPM1,TPM2,VCAN,ZNF154。在一些情况下,主题方法涉及在受试者的肺组织样品中确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,或24个基因)的基因产物的表达水平(例如,标准化基因表达水平):ADAMDEC1,ANKRD22,APOBEC3C,APOBEC3F,APOBEC3G,APOBEC3H,APOL1,APOL3,APOL4,APOL6,ASCL2,BATF,BATF2,BST2,BTN2A2,BTN3A1,BTN3A2,BTN3A3,C17orf49,CAMK4,CASP1,CASP4,CCL4,CCL4L1,CCL5,CCR5,CD2,CD226,CD244,CD247,CD274,CD3D,CD3E,CD3G,CD40,CD40LG,CD5,CD6,CD72,CD74,CD8A,CD96,CIITA,CLEC6A,CMTM1,COROIA,CRTAM,CST7,CTLA4,CXCL10,CXCL11,CXCL9,CXCR3,CXCR6,DDX60,DNASE2,EBI3,EIF4E3,EPSTI1,ETV7,FAM26F,FAM78A,FASLG,FGL2,FYB,GATA3,GBP1,GBP2,GBP3,GBP4,GBP5,GBP7,GCH1,GPR171,GPR174,GPR68,GRAMD1B,GZMA,GZMB,GZMH,HCP5,HCST,HIST1H2BI,HLA-A,HLA-B,HLA-C,HLA-DMA,HLA-DMB,HLA-DOA,HLA-DPA1,HLA-DPB1,HLA-DPB2,HLA-E,HLA-F,HLA-G,HLA-H,HLA-J,HLA-L,ICOS,IDO1,IFI27,IFI27L2,IFI35,IFNG,IL12RB2,IL23A,IL26,IL27RA,IL2RB,IL2RG,IL32,IL6R,IRF1,IRF9,ITGA4,ITGAE,ITGAL,ITGB2,ITGB7,ITK,JAKMIP1,KIAA1324,KIF18A,KLRC2,KLRK1,L3MBTL4,LAP3,LAT,LCK,LCP2,LGALS2,LGR5,MIA2,NAGK,NFATC2,PAQR8,PARP12,PARP14,PARP9,PDCD1LG2,PLA2G12B,PLXNCl,PRKCQ,PSMBIO,PSMB8,PSMB9,PSME1,PSME2,PTPN22,PTPRJ,PTTG1,PYCARD,PYHIN1,RABGAP1L,RARRES3,RASGRP1,RFX5,RGS10,RNF167,RNF19B,RNF213,RTP4,RUNX3,SAMD9L,SEMA4D,SEPT1,SH2D1A,SH2D2A,SKAP1,SLA2,SLAMF8,SLC35D2,STAT1,STAT4,TAP1,TAP2,TAPBP,TARP,TCID-7896691,TCID-7896701,TCID-7896702,TCID-7896719,TCID-7896720,TCID-7917530,TCID-7948502,TCID-8117739,TCID-8163000,TDRKH,THEMIS,TLR3,TLR8,TNF,TRAFD1,TRAT1,TRAV8-3,TRDV2,TRERF1,TUBA4A,UBASH3A,UBD,UBE2L6,VAMP5,WARS,XCL1,ZAP70,ZNF683,ZNF831。区别诊断特发性肺纤维化对间质性肺病炎症本公开提供了区别诊断IPF与间质性肺病炎症(ILD炎症;例如HP,NSIP,结节病,和机化性肺炎(OP)的炎症亚型)的方法。该方法一般地涉及在来自受试者的肺组织样品中确定在图34A-B中列出的基因的基因产物的标准化表达水平。在一些情况下,主题方法涉及在受试者的肺组织样品中确定从图34A和34B中列出的基因中选出的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,30,31,32,33,34,35,36,37,38,39,40,41,42,43,44,45,46,47,48,49,或50或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平)。在一些情况下,主题方法涉及在受试者的肺组织样品中确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或30个或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):ABCA6,ACTA2,ACTG2,ADCY5,AHNAK2,ANKRD20A8P,ANO2,ARHGEF25,ATP1A2,C16orf45,CALD1,CAMK2N1,CNN1,COL21A1,CRYAB,CSRP1,CTTNBP2,DES,DGKG,DIXDC1,DMD,DST,DTNA,DZIP1,EDIL3,FAM124B,FAM13C,FHL1,GARNL3,HPSE2,HSPA2,KALRN,LAMA4,LAMC1,LDB3,LMOD1,LPP,MAPIB,MAP7D3,MARK1,MCAM,MEIS1,MPDZ,MRVI1,MSRB3,MUSTN1,MXRA7,MYH10,MYH11,MYL9,MYLK,MYOCD,MYOM1,NEXN,NFASC,NTRK3,PALLD,PBX1,PCDHB10,PCDHB13,PCDHGC5,PDE1C,PDE5A,PDLIM3,PGM5,PGM5P2,PKD2,PLA2R1,PLCB4,PLN,PPP1R3C,PREX2,PRKAA2,PRKG1,PRUNE2,PTCHD4,PWAR5,RAB9B,SBSPON,SCRG1,SNORD116-21,SORBS1,STON1-GTF2A1L,SYNM,SYNPO2,SYTL4,TAGLN,TCEAL4,TCEAL6,TCID-7919139,TIMP2,TIMP3,TMEM47,TMOD1,TPM1,TPM2,TRPC1,TTLL7,ZC3H12B,和ZNF154。在一些情况下,主题方法涉及在受试者的肺组织样品中确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或30个或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):ACSF2,ANKRD22,AP1M2,APOBEC3F,APOBEC3G,APOL1,APOL4,APOL6,ARHGEF38,ASPM,ATP2C2,ATP8A1,BATF2,BST2,BTN3A3,BUB1,C18orf8,C2,CCL4,CCL4L1,CCL5,CCR5,CD2,CD274,CD38,CD74,CD8A,CDK1,CDKL2,CEACAM1,CFTR,CKS2,CNDP2,CRTAM,CTLA4,CXCL10,CXCL11,CXCL9,CXCR6,DDX60,DRAM1,DUSP16,EFNA1,EPSTI1,ESRP2,ETV7,FAM26F,FHDC1,FPR3,FZD5,GBP1,GBP4,GBP5,GCH1,GPR98,GRAMD1A,GUCD1,GZMB,GZMH,HAS3,HCP5,HIST1H2AI,HIST1H2BH,HIST1H2BI,HIST1H3B,HIST1H3J,HLA-A,HLA-B,HLA-C,HLA-DMA,HLA-DOA,HLA-DPB1,HLA-E,HLA-F,HLA-G,HLA-H,HLA-J,HLA-L,HN1,IFI35,IFIH1,IFNG,IL32,IL6R,IRF1,IRF9,ITGAE,ITGAL,KCNJ15,KCTD14,KIF18A,LAP3,LARP4B,LCP2,LGALS3BP,MAP3K13,MOV10,MREG,NUSAP1,OAS2,PARP12,PARP14,PARP9,PFKFB3,PRKCQ,PSMB10,PSMB8,PSMB9,PSME1,PSME2,PTPRJ,PTTG1,PXMP4,RABGAP1L,RARRES3,RASGRP1,RBM47,RFX5,RGS16,RNF213,SAMD9L,SCTR,SDC4,SEMA4A,SFTPD,SLAMF8,SLC37A1,SMC4,SQRDL,SREBF2,STAT1,TAP1,TAP2,TAPBP,TCID-7896714,TCID-8107094,THEMIS,TLR2,TLR3,TMEM164,TNFAIP3,TOX,TRAFD1,TRIM59,TYMP,UBD,UBE2L6,USP44,WARS,ZNF385B。区别诊断特发性肺纤维化对除IPF之外的间质性肺病本公开提供了区别诊断IPF对除IPF之外的间质性肺病的方法。该方法一般地涉及在来自受试者的肺组织样品中确定在图33A-B中列出的基因的基因产物的标准化表达水平。除IPF之外的ILD被称为“其余(Rest)”或“其余/非-IPF”。“其余(Rest)”是指如下的ILD,如HP、NSIP和结节病。在一些情况下,主题方法涉及在受试者的肺组织样品中确定从图9A-9D,21,和33的任一个中列出的基因中选出的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或30或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平)。在一些情况下,主题方法涉及在受试者的肺组织样品中确定从图9A-9D中列出的基因中选出的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或30或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平)。在一些情况下,主题方法涉及在受试者的肺组织样品中确定从图21A-21B中列出的基因中选出的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或30或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平)。在一些情况下,主题方法涉及在受试者的肺组织样品中确定从图33A-B中列出的基因中选出的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或30或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平)。在一些情况下,主题方法涉及在受试者的肺组织样品中确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或30个或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):ABCA6,ABLIM3,ACTA2,ACTG2,ADCY5,AHNAK2,AKAP12,ANO1,ANO2,ARHGEF25,ATP1A2,ATP1B2,BAG2,BHMT2,BMX,C16orf45,C3orf55,C3orf70,CACNA1C,CACNB2,CALD1,CAMK2N1,CCDC3,CDH6,CDR1,CLIP3,CLU,CNN1,COCH,COL21A1,COPZ2,COX7A1,CRYAB,CSRP1,CTTNBP2,DACT1,DDR2,DENND2A,DES,DIXDC1,DMD,DST,DTNA,DYNC1I1,DZIP1,EBF1,EDIL3,EFHD1,F10,FAM124B,FAM13C,FBLIM1,FEZ1,FGF10,FGF14,FGF2,FGFR1,FHL1,FHL2,FLNC,GADL1,GARNL3,GAS7,GNG12,GRIA3,GRIN2A,HOXA2,HOXA6,HOXA7,HPSE2,HRC,HRH1,HSPA2,HSPB6,HSPB7,IGFBP5,ITGB4,ITIH5,KALRN,LAMA4,LAMC1,LARP6,LDB3,LGI4,LMOD1,LPP,LTBP1,MAP1B,MAP7D3,MARK1,MCAM,MEIS1,MEOX2,MPDZ,MRGPRF,MRVI1,MSRB3,MUSTN1,MXRA7,MYH11,MYL9,MYLK,MYOCD,MYOM1,NCAM1,NEXN,NFASC,NPR2,NR2F1,NR2F2,NTRK3,OSR2,PALLD,PALMD,PARVA,PBX1,PCDH7,PCDHB10,PCDHB12,PCDHB13,PCDHB14,PCDHB18,PCDHB3,PCDHB7,PCDHGC5,PDE10A,PDE1A,PDE2A,PDE3A,PDE5A,PDE7B,PDGFRB,PDLIM3,PDZRN4,PEG3,PFKM,PGM5,PGM5P2,PHYHIPL,PKD2,PLA2R1,PLCB4,PLN,PLXNA4,PODN,PPP1R3C,PRKAA2,PRKG1,PRSS23,PRUNE2,PTCHD4,PYGM,RAB9B,RASD2,RBM24,RCAN2,RERG,RGS5,RGS7BP,RYR3,S1PR3,SBSPON,SCRG1,SCUBE1,SEMA3D,SETBP1,SGCA,SLC38A11,SLIT3,SLN,SMIM10,SNED1,SNORD116-17,SNORD116-21,SNX9,SOGA1,SORBS1,SPARCL1,SSPN,SYNM,SYNPO2,SYTL2,TAGLN,TCEAL4,TCEAL6,TIMP2,TMEM252,TMEM47,TMOD1,TPM1,TPM2,TRPC1,TTLL7,WISP2,ZAK,ZC3H12B,ZCCHC24,ZEB2,ZHX3,ZNF135,ZNF154,ZNF521。在一些情况下,主题方法涉及在受试者的肺组织样品中确定如下基因系列的一个或多个基因(例如,一系列2,3,4,5,6,7,8,9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24,25,26,27,28,29,或30个或更多个基因)的基因产物的表达水平(例如,标准化基因表达水平):ACADL,ACOXL,ACSF2,AHCYL2,ANK3,AP1M2,APOL1,APOL4,APOL6,AQP4,ARAP2,ARHGEF38,ARSD,ASPM,ATP1A1,ATP2C2,ATP8A1,BATF2,BAZ1A,BMP3,BST2,BTG3,BTN3A3,BUB1,C18orf8,C2,CASP1,CASP4,CCL4,CCL4L1,CCL5,CCNA2,CCR5,CD274,CD40,CD47,CD74,CD8A,CDCA7L,CDK1,CDKL2,CEACAM1,CFTR,CKAP2,CLDN4,CLINT1,CNDP2,CNKSR1,CRTAC1,CRTAM,CSF3R,CXCL10,CXCL11,CXCL9,CXCR6,CYB5A,CYP2B6,CYP2B7P1,DAPK1,DBI,DDX60,DENND1B,DHCR24,DNASE2,DOCK8,DRAM1,DTNB,DTX3L,DUSP16,DYNLTl,EDEMl,EFNA1,EML4,ENTPD3,EPSTI1,ERAP1,ERBB3,ESRP1,ESRP2,ETV7,FAM111A,FCGR1A,FCGR1B,FDFT1,FGFR2,FHDC1,FLRT3,FNIP2,FREM2,FZD5,GALNT3,GBP1,GBP4,GBP5,GBP7,GCH1,GCNT2,GK,GNPTAB,GPR98,GRAMD1B,GRHL2,GSAP,GUCD1,GZMB,GZMH,HAS3,HCP5,HIST1H2AI,HIST1H2BI,HIST1H3B,HLA-A,HLA-B,HLA-C,HLA-DMA,HLA-DOA,HLA-DPA1,HLA-DPB1,HLA-DQA2,HLA-DRA,HLA-E,HLA-F,HLA-G,HLA-H,HLA-J,HLA-L,HMGCL,HMGCR,HMMR,HN1,HNF1B,HPS5,ICOS,IDI1,IDO1,IFI27,IFI35,IFIH1,IFIT3,IFIT5,IGSF3,IL10RB,IL32,IL6R,INADL,IRF1,IRF9,ITGAE,ITGAL,JPH1,KCNJ15,KCTD14,KIAA0247,KIAA0319L,KIAA1958,KIF18A,KLF5,L3MBTL4,LAMP3,LAP3,LARP4B,LCP2,LIMD1,LNX2,LPIN2,MAGI3,MAP3K13,MAPK13,MARK2,MB21D1,MBIP,MIA2,MICALCL,MID1IP1,MREG,MRPL14,MTMR14,MTRR,MYL1,MYO5B,N4BP1,NAV2,NEDD4L,NMI,NPC1,NUB1,NUSAP1,OAS2,OCLN,ORM1,PARP12,PARP14,PARP9,PCK2,PCLO,PDZK1IP1,PEBP4,PFKFB3,PHACTR1,PI4K2B,PLA2G12B,PLAGL2,PLCH1,PLS1,PPP1R9A,PPP2R5A,PRKCQ,PRKCZ,PRRG4,PRSS8,PSMB10,PSMB8,PSMB9,PSME1,PSME2,PTP4A1,PTPN1,PTPRJ,PTTG1,PXMP4,RAB20,RAB3IP,RABGAP1L,RANBP17,RARRES3,RBM47,RCOR1,RFC1,RFX5,RGS16,RNF19B,RNF213,S100A14,SAMD9L,SCNIA,SCTR,SDC4,SELENBPl,SEMA4A,SFTPD,SH2D4A,SHANK2,SLAMF8,SLC15A3,SLC16A13,SLC22A3,SLC37A1,SLC04C1,SMARCA5,SMC4,SQLE,SQRDL,SREBF2,ST7,STARDIO,STATl,STXll,STX19,SYT15,TAPl,TAP2,TAPBP,TAPT1,TC2N,TCID-7895602,TCID-7896651,TCID-7896695,TCID-7951593,TCID-8113717,TDRKH,THEMIS,TKT,TLR2,TLR3,TMEM164,TMEM180,TMEM41B,TMEM87A,TMPRSS2,TMPRSS3,TNFAIP3,TOX,TRAFD1,TRIM21,TRIM24,TTLL4,UBALD2,UBD,UBE2L6,USP38,USP44,USP54,WARS,WHSC1,WWC1,ZDHHC16,ZDHHC2,ZNF385B。组织样品用于主题分析和诊断方法的肺组织样品可以是活检样品(例如通过视频辅助的胸腔镜手术获得活检样本;VATS);支气管肺泡灌洗(BAL)样品;支气管活检;冷冻支气管活检;和类似物。用于分析的肺组织样品可以被提供在合适的保存液中。组织样品可以从疑似患有肺部疾病(例如ILD)的患者获得,根据该患者呈现临床症状和体征(例如,呼吸短促(通常运动加剧)、干咳),和任选地一种或多种成像测试的结果(例如,胸部X射线,计算机化断层扫描(CT)),肺功能测试(例如,肺活量测定、血氧饱和度、运动负荷试验),肺组织分析(例如,通过支气管镜、支气管肺泡灌洗、手术活检获得的样品的组织学和/或细胞学分析)。肺组织样品可以用多种方式中的任一种进行处理。例如,肺组织样品可以进行细胞裂解。肺组织样品可以被保存在RNA保护溶液(抑制RNA降解,例如,抑制RNA核酸酶消化的溶液)中,随后进行细胞裂解。组分,例如核酸和/或蛋白质可以从肺组织样品中富集或分离,并且经过富集或分离的组分可以用于主题方法。用于富集和分离组分(例如核酸和蛋白质)的方法是本领域已知的;并且可以使用任何已知的方法。分离RNA用于表达分析的方法在本领域中已有描述。确定表达产物水平的体外方法用于确定基因表达产物水平的一般方法是本领域已知的,并且可以包括但不仅限于如下的一个或多个:额外的细胞学测定,测定特定的蛋白质或酶活性,测定特定的表达产物包括蛋白质或RNA或特定的RNA剪接变体,原位杂交,整体或局部基因组表达分析,微阵列杂交测定,基因表达系列分析(SAGE),酶联免疫吸附测定,质谱,免疫组织化学,印迹,测序,RNA测序,DNA测序(例如,对从RNA获得的cDNA的测序);新一代测序,纳米孔测序,焦磷酸测序,或Nanostring(纳米链)测序。基因表达产物的水平可以相对于内标(如总mRNA)或特定基因(包括但不仅限于,甘油醛3磷酸脱氢酶或微管蛋白)的表达水平进行标准化。在某些实施方案中,可以通过全转录组鸟枪测序法("WTSS"或"RNA-seq";见例如Ryan等BioTechniques45:81-94)获得基因表达图谱,其使用高通量测序技术对cDNA测序,以获得关于样品RNA内容的信息。一般而言,从RNA制成cDNA,对cDNA进行扩增,并对扩增产物进行测序。扩增之后,可以使用任何方便的方法对cDNA进行测序。例如,片段测序可以使用Illumina的可逆终止子方法、Roche的焦磷酸测序法(454)、LifeTechnologies的连接酶测序法(SOLiD平台)或LifeTechnologies的IonTorrent平台。这些方法的实例在下列参考文献中有描述:Margulies等(Nature2005437:376-80);Ronaghi等(AnalyticalBiochemistry1996242:84-9);Shendure(Science2005309:1728);Imelfort等(BriefBioinform.200910:609-18);Fox等(MethodsMolBiol.2009;553:79-108);Appleby等(MethodsMolBiol.2009;513:19-39)和Morozova(Genomics.200892:255-64),本文引用其内容作为方法一般描述和方法特殊步骤的参考,包括所有起始产物、试剂、和每个步骤的终产物。可以显而易见,在扩增步骤期间可以在片段末端添加与所选下一代测序平台兼容的正向和反向测序引物位点。在其它实施方案中,产物可以使用纳米孔测序法(例如,在Soni等ClinChem53:1996-2001,2007中所述,或者如OxfordNanoporeTechnologies所述)进行测序。纳米孔测序是一种单分子测序技术,当DNA的单分子通过纳米孔时直接进行测序。纳米孔是一个很小的洞,直径在1纳米的量级。纳米孔浸没在导电流体中并在两端施加电位(电压),由于离子传导通过纳米孔而产生轻微的电流。电流流动的量对纳米孔的尺寸和形状敏感。当DNA分子通过纳米孔时,DNA分子上的每个核苷酸以不同的程度阻塞纳米孔,以不同的程度改变通过纳米孔的电流大小。因此,电流随着DNA分子通过纳米孔的这种变化提供了DNA序列的阅读。纳米孔测序技术在下列专利中被公开:美国专利号号5,795,782,6,015,714,6,627,067,7,238,485和7,258,838和美国专利申请公开US2006003171和US20090029477。在一些实施方案中,主题发明方法的基因表达产物是蛋白质,并使用从样品队列获得的蛋白质数据产生的分类器对特殊生物样品中的蛋白质的量进行分析。蛋白的量可以通过如下的一种或多种加以确定:酶联免疫吸附测定(ELISA)、质谱、印迹、或免疫组织化学。在一些实施方案中,基因表达产物的标记物和可选择剪接标记物可以通过微阵列分析加以确定,使用例如Affymetrix阵列、cDNA微阵列、寡核苷酸微阵列、斑点微阵列,或其它来自Biorad,Agilent,或Eppendorf公司的微阵列产品。微阵列提供特别的优势,因为它们可以含有大量基因或可选择剪接变体,并可以在一次实验中被测定。在一些情况下,微阵列装置可能包含整个人类基因组或转录组或其相当大的组分,允许对基因表达模式、基因组序列、或可选择性剪接进行全面的评估。标记物可以使用标准分子生物学和微阵列分析技术发现,如在SambrookMolecularCloningaLaboratoryManual2001和Baldi,P.和Hatfield,W.G.,DNAMicroarraysandGeneExpression2002中所述。微阵列分析一般开始于使用本领域已知的方法从生物样品(例如组织活检或细针穿刺)提取和纯化核酸。对于表达和可选择剪接分析,可能有利的是提取和/或纯化RNA,使之与DNA分离。可能更有利的是提取和/或纯化mRNA,使之与其它形式的RNA如tRNA和rRNA分离。纯化的核酸可以进一步用荧光标签、放射性核素、或化学标记如生物素、洋地黄毒苷、地高辛进行标记,例如通过逆转录、聚合酶链式反应(PCR)、连接、化学反应或其他技术。标记可以是直接的或间接的,其可能进一步需要一个偶联阶段。偶联阶段可以在杂交之前发生,例如使用氨基烯丙基-UTP和NHS-氨基活性染料(如花青染料),或者在之后发生,例如使用生物素和标记的链霉亲和素。在一个实施例中,经修饰的核苷酸(例如,以1aaUTP:4TTP的比例)被酶促添加的比例低于正常核苷酸,典型地导致每60个碱基有1个(用分光光度计测量)。然后,该aaDNA可以用例如柱子或渗滤设备纯化。氨基烯丙基基团是连接于核苷碱基的长连接子上的胺基,它可以和反应性标签(例如荧光染料)反应。被标记的样品随后与杂交溶液混合,该杂交溶液可以含有十二烷基硫酸钠(SDS)、SSC、硫酸右旋糖酐、封闭剂(例如COT1DNA,鲑鱼精DNA,牛胸腺DNA,PolyA或PolyT)、Denhardt氏溶液、甲酰胺,或其组合。杂交探针是不同长度的DNA或RNA片段,其用于检测DNA或RNA样品中与探针序列互补的核苷酸序列(DNA靶)的存在。借此探针与单链核酸(DNA或RNA)杂交,其碱基序列允许由于探针和靶之间的互补性而发生探针-靶碱基配对。被标记探针首先被变性(通过加热或在碱性条件下)变成单DNA链,然后与靶DNA杂交。为了检测探针与其靶序列的杂交,探针用分子标记物加标签(或标记);常用的标记物是32P或地高辛,其是非放射性的基于抗体的标记物。然后检测与探针具有中度到高度序列互补性(例如至少70%,80%,90%,95%,96%,97%,98%,99%,或更高互补性)的DNA序列或RNA转录本,其是通过放射自显影或其他成像技术使杂交探针可视化。具有中度或高度互补性的序列的检测取决于所用杂交条件的严格程度;高严格度,例如高杂交温度和杂交缓冲液中低盐,只允许高度相似的核酸序列之间杂交,而低严格度,例如较低的温度和高盐,允许相似性较小的序列杂交。在DNA微阵列中使用的杂交探针是指共价附着于惰性表面(例如涂层玻璃载片或基因芯片)的DNA,并且游离的cDNA靶标与之杂交。包含准备与阵列上的探针杂交的靶核酸的混合物可以通过热或化学方法变性,并加入到微阵列的端口中。孔随后密封,将微阵列在例如杂交炉中杂交,其中微阵列通过旋转或者在混合器中混合。过夜杂交后,洗去非特异性结合(例如使用SDS和SSC)。然后,微阵列被干燥并包含激光器和检测器的机器中扫描,该激光器激发染料,检测器测量染色发射。图像与模板网格重叠,并可以对特征(例如,包含若干个像素的特征)的强度进行定量。可以使用各种试剂盒扩增本发明方法的核酸和探针产生。可以在本发明中使用的试剂盒的实施例包括但不仅限于NugenWT-的OvationFFPE试剂盒,具有Nugen外显子模块和Frag/Label模块的cDNA扩增试剂盒。NuGENWT-OvationTM.FFPE系统V2是一个全转录组扩增系统,它能够对来自FFPE样品的小和降解RNA的广大档案进行全局基因表达分析。该系统包括用于扩增少至50ng总FFPERNA所需的试剂和方案。该方案可以用于qPCR、样品归档、断裂和标记。扩增的cDNA可以被断裂和标记,对于使用NuGEN'sFL-OvationTMcDNA生物素模块V2的GeneChipTM3'表达阵列分析而言不到2个小时。对于使用AffymetrixGeneChipTM外显子和基因ST阵列的分析,扩增的cDNA可以使用WT-Ovation外显子模块,然后断裂并用FL-OvationTM.cDNA生物素模块V2标记。对于Agilent阵列上分析,扩增的cDNA可以被断裂并用NuGEN'sFL-OvationTM.cDNA荧光模块进行标记。关于NugenWT-OvationFFPE试剂盒的更多信息可以在www.nugeninc.com/nugen/index.cfm/products/amplification-systems/wt-ovatio-n-ffpeA获得。在一些实施方案中,可以使用AmbionWT-表达试剂盒。AmbionWT-表达试剂盒允许直接扩增总RNA,而无需单独的核糖体RNA(rRNA)清除步骤。使用AmbionWT-表达试剂盒,可以在AffymetrixTM.GeneChipTM人、小鼠和大鼠外显子和基因1.0ST阵列上对小至50ng总RNA的样品进行分析。除了所需输入的RNA更少和AffymetrixTM方法与TaqManTM实时PCR数据的一致性更高之外,AmbionWT-表达试剂盒还显著提高了灵敏度。例如,由于增加了信噪比,使用AmbionWT-表达试剂盒在外显子水平上可以检测到大量高于背景的探针。AmbionWT-表达试剂盒可以和额外的Affymetrix标记试剂盒联合使用。在一些实施方案中,本发明方法可以使用AmpTecTrinucleotideNanomRNA扩增试剂盒(6299-A15)。ExpressArtTMTRinucleotidemRNA扩增Nano试剂盒适合于1ng-700ng的大范围输入总RNA。根据输入的总RNA量和所需的aRNA产量,它可以被使用1轮(输入>300ng总RNA)或2轮(最少输入量为1ng总RNA),aRNA产量范围>10μg。AmpTec独有的TRinucleotide引发技术导致mRNA优先扩增(独立于通用的真核生物3'-poly(A)-序列),组合以针对rRNA的选择。关于AmpTecTrinucleotideNanomRNA扩增试剂盒的更多信息可以在www.amp-tec.com/products.htm获得。这种试剂盒可以和cDNA转换试剂盒(cDNAconversionkit)和Affymetrix标记试剂盒组合使用。然后,可以对原始数据进行标准化,例如通过减去背景强度,随后除以强度使每个通道上特征的总强度或参考基因的强度相等,然后可以计算所有强度的t值。更复杂的方法包括z比值、Loess和Lowess回归和RMA(稳固多芯片分析),例如用于Affymetrix芯片。数据分析(i)样品与正常比较对来自受试者的样品(测试样品)执行的分子谱的结果可以和已知或疑似正常的生物样品进行比较。在一些实施方案中,正常样品是不包含或者预期不包含ILD或所评估病症的样品,对于所评估的一种或多种ILD的分子谱测定预期是测试阴性的。在一些实施方案中,正常样品是或者预期是没有任何ILD的,或者样品在分子谱测定中对于任何ILD均是测试阴性的。正常样品可以来自与被测试受试者不同的受试者,或者来自同一受试者。在一些情况下,正常样品是从受试者,例如被测试受试者获得的肺组织样品。正常样品与测试样品同时或者在不同时间测定。测试样品的测定结果可以和具有已知疾病状态(例如,正常、被所选ILD(例如IPF,NSIP等)影响)的样品的相同测定结果进行比较。在一些情况下,正常样品的测定结果来自数据库或参照物。在一些情况下,正常样品的测定结果是本领域技术人员已知的或者一般接受的数值或数值范围。在一些情况下,比较是定性的。在其他情况下,比较是定量的。在一些情况下,定性或定量比较可能涉及但不仅限于如下的一种或多种:比较荧光值、斑点强度、吸光度值、化学发光信号、直方图、临界阈值、统计显著性值、基因产物表达水平、基因产物表达水平的变化、可替代外显子的使用情况、可替代外显子使用情况的改变、蛋白质水平、DNA多态性、拷贝数变异、存在或不存在一种或多种DNA标记物或区域的指示,或核酸序列。(ii)结果评估在一些实施方案中,分子谱结果使用本领域已知的用于关联基因产物表达水平或可替代外显子使用与特定表型,例如特定ILD或正常状态(例如,无疾病或病症)的方法进行评估。在一些情况下,可以确定特定的统计置信水平,以提供诊断置信水平。例如,可以确定,大于90%的置信水平可用于预测ILD的存在。在其他实施方案中,可以选择更高或更低严格度的置信水平。例如,可以选择大约或者至少大约50%,60%,70%,75%,80%,85%,90%,95%,97.5%,99%,99.5%,或99.9%的置信水平作为有用的表型预测子。在某些情况下,所提供的置信水平可能与样品的质量、数据的质量、测定的质量、所用的具体方法,和/或被分析基因表达产物的数量有关。用于提供诊断的特定置信水平可以根据假阳性或假阴性的预期数目和/或成本来选择。用于选择参数以实现特定置信水平或者用于鉴定具有诊断力的标记物的方法包括,但不仅限于,受试者工作特征(ROC)曲线分析、副法线ROC、主成分分析、偏最小二乘分析、奇异值分解、最小绝对收缩率和选择操作者分析、最小角回归、和阈值梯度定向正则化方法。(iii)数据分析在一些情况下,原始的基因表达水平和可选择剪接数据可以通过应用旨在标准化和/或提高数据可靠性的算法加以改进。在本公开的一些实施方案中,数据分析要求计算机或其它设备、机器或装置,用于采用本文所述的各种算法,因为需要处理大量的单个数据点。“机器学习算法”是指一种基于计算的预测方法,本领域技术人员也称作“分类器”,用于表征基因表达谱。对应于某些表达水平的信号,其是通过例如基于微阵列的杂交测定获得的,通常要经历该算法以便对表达谱进行分类。监督学习一般涉及“训练”分类器以识别类之间的区别,然后在独立的测试系列上“测试”分类器的准确度。对于新的未知样品,分类器可用于预测样品属于哪个类别。在一些情况下,强大的多阵列平均(RMA)方法可以用于标准化原始数据。RMA方法首先为大量微阵列上的每个匹配小室(cell)计算背景校正强度。该背景校正强度被限制于正值,如Irizarry等Biostatistics2003April4(2):249-64所述。背景校正之后,获得每个经过背景矫正的匹配小室强度的以2为底的对数。然后,使用分位数标准化方法将每个微阵列上经过背景校正、对数转换的匹配强度标准化,其中对于每个输入阵列和每个探针表达值,阵列百分位探针数值被所有阵列百分位点的平均值代替,这种方法在Bolstad等Bioinformatics2003中有更完整的描述。在分位数标准化之后,将经过标准化的数据与线性模型拟合,从而获得每个微阵列上每个探针的表达测量。然后可以使用Tukey的中值抛光算法(Tukey,J.W.,ExploratoryDataAnalysis.1977)确定标准化探针系列数据的对数尺度的表达水平。进一步对数据进行过滤,以除去值得怀疑的数据。在一些实施方案中,从具有少于大约4,5,6,7或8个鸟苷+胞嘧啶核苷酸的微阵列探针产生的数据可以被认为是不可靠的,因为它们具有异常的杂交倾向或二级结构问题。类似地,从具有超过大约12,13,14,15,16,17,18,19,20,21,或22个鸟苷+胞嘧啶核苷酸的微阵列探针产生的数据可以被认为是不可靠的,因为它们具有异常的杂交倾向或二级结构问题。在一些情况下,可以通过探针系列针对一系列参考数据集的排名选择不可靠的探针系列,将其从数据分析中排除。例如,RefSeq或Ensembl(EMBL)被认为是非常高质量的参考数据集。在一些情况下,来自与RefSeq或Ensembl序列匹配的探针系列的数据可以被特别包含在微阵列分析实验中,因为它们预期具有高可靠性。类似地,来自与可靠性较低的参考数据集相匹配的探针系列的数据可以被排除不用于分析,或者根据具体情况考虑纳入。在一些情况下,Ensembl高通量cDNA(HTC)和/或mRNA参考数据集可用于分别或一起确定探针集的可靠性。在另一些情况下,探针集的可靠性可被排名。例如,与所有参考数据集如RefSeq,HTC,和mRNA完美匹配的探针和/或探针系列可以被排名为最可靠的(1)。此外,与三个参考数据集中的2个相匹配的探针和/或探针系列可以被排名为第二最可靠的(2),与三个参考数据集中的1个相匹配的探针和/或探针系列可以被排在下面(3),而与参考数据集均不匹配的探针和/或探针系列被排在最后(4)。然后,可以根据它们的排名,将探针和/或探针系列包含或排除用于分析。例如,可以选择纳入来自分类1、2、3和4的探针系列;分类1、2和3的探针系列;分类1和2的探针系列;或分类1的探针系列的数据用于进一步的分析。在另一实例中,探针系列可以通过与参考数据集实体不匹配的碱基对的数目进行排名。应当理解,本领域有多种方法用于评估给定探针和/或探针系列用于分子谱的可靠性,并且本公开方法的包括这些方法及其组合的任一种。在本发明的一些实施方案中,如果它们不表达或以不可检测的水平表达(不高于背景),则来自探针系列的数据可以被从分析中排除。如果对于任意组:正态分布从T0到无穷大的积分<显著性(Significance)(0.01),其中T0=Sqr(GroupSize)(T-P)/Sqr(Pvar);GroupSize=组中CEL文件的数目,T=探针系列中探针得分的平均值,P=GC含量背景探针平均值的均值,和Pvar=背景探针变异总和/(探针系列中探针的数目)2,则判断探针系列的表达高出背景。这允许包含如下的探针系列,其中组中探针系列的平均值大于背景探针的平均表达,该背景探针与该探针系列探针具有相似GC含量并作为该探针系列的背景的中心,并且能够导出该探针系列与该背景探针系列变异的差量(dispersion)。在本公开的一些实施方案中,显示没有或低变异的探针系列可以被排除出进一步的分析。低变异的探针系列可以通过卡方检验从分析中排除。如果转换方差位于具有(N-1)自由度的卡方分布99%置信区间的左侧,则该探针系列被认为是低变异的。(N-l)*探针系列变异/(基因探针系列变异).about.Chi-Sq(N-l),其中N是输入CEL文件的数目,(N-1)是卡方分布的自由度,“基因的探针系列变异”是基因间探针系列变异的平均值。在本发明的一些实施方案中,给定基因或转录本集群的探针系列可以被排除出进一步的分析,如果它们含有少于最小数目的能够通过前述用于GC含量、可靠性、变异等的过滤步骤的探针的话。例如,在一些实施方案中,如果给定基因或转录本集群的探针系列含有少于大约1,2,3,4,5,6,7,8,9,10,11,12,13,14,15,或少于约20个探针,则可以被排除出进一步的分析。基因表达水平或可选择剪接的数据分析方法可以进一步包括使用本文所提供的特征选择算法。在本发明的一些实施方案中,特征选择通过使用LIMMA软件包(Smyth,G.K.(2005).Limma:linearmodelsformicroarraydata.In:BioinformaticsandComputationalBiologySolutionsusingRandBioconductor,R.Gentleman,V.Carey,S.Dudoit,R.Irizarry,W.Huber(编),Springer,NewYork,pages397-420)提供。基因表达水平或可选择剪接的数据分析方法可以进一步包括使用预分类算法。例如,算法可以使用细胞特异的分子指纹,根据其组成对样品进行预分类,然后施加矫正/标准化因子。这个数据/信息随后被提供到最终的分类算法,其合并该信息以帮助最终诊断。基因表达水平或可选择剪接的数据分析方法可以进一步包括使用本文提供的分类器算法。在本发明的一些实施方案中,提供了对角线线性判别分析、k近邻算法、支持向量机(SVM)算法、线性支持向量机、随机森林算法、或基于概率模型的方法或它们的组合,用于对微阵列数据进行分类。在一些实施方案中,可区分样品(例如,第一ILD与第二ILD,正常对ILD)或区分亚型(例如IPF对NSIP)的鉴定标记物可以根据在感兴趣的类别之间表达水平的统计学显著性差异加以选择。在一些情况下,统计显著性可以通过对错误发现率(FDR)进行BenjaminHochberg或其它校正加以调整。在一些情况下,分类器算法可以补充荟萃分析(Meta-analysis)方法,例如Fishel和Kaufman等2007Bioinformatics23(13):1599-606所述。在一些情况下,分类器算法可以补充荟萃分析方法,例如重复性分析。在一些情况下,重复性分析选择在至少一个预测表达产物标记系列中出现的标记。用于向微阵列数据分析推导和应用后验概率的方法是本领域已知的,并且在例如Smyth,G.K.2004Stat.Appi.Genet.Mol.Biol.3:Article3中已有描述。在一些情况下,后验概率可用于对分类器算法提供的标记进行排名。在某些情况下,标记可以根据它们的后验概率进行排名,并且那些通过了所选阈值的可以被选择作为标记物,其差异性表达可指示或诊断样品是例如IPF或NSIP。例证性阈值包括0.7,0.75,0.8,0.85,0.9,0.925,0.95,0.975,0.98,0.985,0.99,0.995或更高的先验概率。分子谱结果的统计学评估可以提供指示如下一种或多种的定量数值:诊断准确性的可能性;ILD的可能性;特殊ILD的可能性;和特殊治疗干预成功的可能性。因此,可能没有经过遗传学或分子生物学训练的医生不需要理解原始数据。而是,数据以其最有用的形式被直接呈现给医师,以指导患者护理。分子谱的结果可以使用大量本领域已知的方法进行统计学评估,包括但不仅限于:StudentsT检验、两侧t检验、皮尔森秩和分析、隐马尔可夫模型分析、q-q图分析、主成分分析、单因素ANOVA、双因素ANOVA、LIMMA等。在本发明的一些实施方案中,单独使用或与细胞学分析组合使用分子谱的可提供分类、鉴定、或诊断,其准确度为大约85%-大约99%或大约100%。在一些情况下,分子谱处理和/或细胞学可提供ILD的分类、鉴定、诊断,其准确度为大约或者至少大约85%,86%,87%,88%,90%,91%,92%,93%,94%,95%,96%,97%,97.5%,98%,98.5%,99%,99.5%,99.75%,99.8%,99.85%,或99.9%。在一些实施方案中,分子谱处理和/或细胞学可提供特殊ILD类型(例如IPF;NSIP;HP)存在的分类、鉴定或诊断,准确度为大约或者至少大约85%,86%,87%,88%,90%,91%,92%,93%,94%,95%,96%,97%,97.5%,98%,98.5%,99%,99.5%,99.75%,99.8%,99.85%,或99.9%。在一些情况下,准确度的确定可以通过在一段时间内跟踪受试者以确定原始诊断的准确性。在其它情况下,准确度可以用确定的方式或者采用统计学方法加以建立。例如,受试者工作特征(ROC)分析可以用于确定最佳测定参数,从而实现特定水平的准确度、特异性、阳性预测值、阴性预测值,和/或错误发现率。在本发明的一些实施方案中,一些产物被确定在第一ILD和第二ILD之间(例如,在IPF和NSIP之间)或者在ILD和正常之间显示最大的表达水平差异或者最大的可选择剪接差异,可以选择这些基因表达产物和编码这些产物的核苷酸组合物用作本公开的分子谱试剂。这些基因表达产物可以是特别有用的,因为它们与本领域已知或使用的其它方法相比,可以提供更宽的动态范围,更高的信噪比,改进的诊断能力,更低的假阳性或假阴性可能性,或者更大的统计置信水平。在本发明的其它实施方案中,单独使用或与细胞学分析组合使用分子谱与使用本领域已知的标准细胞学技术相比,可以将得分为非诊断的样品数目减少大约,或者至少大约100%,99%,95%,90%,80%,75%,70%,65%,或大约60%。在一些情况下,本发明的方法与本领域所用的标准细胞学方法相比可以将得分为中间或疑似的样品的数目减少大约,或者至少大约100%,99%,98%,97%,95%,90%,85%,80%,75%,70%,65%,或大约60%。在一些情况下,分子谱测定的结果被输入到数据库中,用于被分子谱公司、个人、医疗提供者或保险提供商的代表或代理人访问。在某些情况下,测定结果包括由公司代表、代理人或顾问,例如医学专业人员进行的样品分类、鉴定、或诊断。在其他情况下,数据的计算机或算法分析被自动提供。在某些情况下,分子谱公司可能给个人、保险提供商、医疗服务提供者、研究人员或政府实体提供如下一种或多种的账单:被执行的分子谱测定、咨询服务、数据分析、报告结果,或数据库访问。在本发明的一些实施方案中,分子谱的结果作为计算机屏幕上的报告或者作为纸质记录提供。在一些情况下,报告可以包括,但不仅限于,如下的一种或多种信息:差异表达的基因数量,原始样品的适宜性,显示差异性可选择剪接的基因数量,诊断,用于诊断的统计置信度,ILD的可能性,和指示的疗法。(iv)根据分子谱结果对样品进行分类分子谱的结果可以被分类成如下的一种:ILD,特定类型ILD,非ILD,或者非诊断(不能提供关于ILD存在或者不存在的充分的信息)。在一些情况下,分子谱的结果可以被分类成IPF对NSIP类别。在本发明的一些实施方案中,结果使用经过训练的算法进行分类。本发明经过训练的算法包括如下算法,其是使用已知ILD和正常样品的参考系列开发的,包括但不仅限于具有表1和2中列出的一种或多种组织病理学的样品。在一些实施方案中,算法进一步使用表3-11和13-34中任一个的一个或多个分类组或其组合进行训练。在一些实施方案中,训练包括比较来自第一ILD的第一系列生物标记物的基因表达产物水平与来自第二ILD的第二系列生物标记物的基因表达产物水平,其中第一系列生物标记物包括至少一个不在第二系列中的生物标记物。在一些实施方案中,整个算法或者部分算法可以被训练,其是通过比较分类组内生物标记物组的表达水平与算法所用的所有其它生物标记物组(或所有其它生物标记物标识)的表达水平。适合于对样品进行分类的算法包括但不仅限于:K近邻算法,支持向量机,线性判别分析,对角线线性判别分析,updown,朴素贝叶斯算法,神经网络算法,隐马尔可夫模型算法,遗传算法,或它们的任意组合。在一些情况下,本发明经过训练的算法可以合并除基因表达或可选择剪接数据外的数据,例如但不仅限于,DNA多态性数据、测序数据、本发明细胞学家或病理学家的打分或诊断、由本公开预分类器算法提供的信息、或者关于本公开受试者医疗历史的信息。当分类生物样品用于诊断ILD时,二元分类器通常有两种可能的输出。当二元分类器与实际真值(例如,来自生物样品的数值)进行比较时,通常有4种可能的输出。如果预测的输出是p(其中"p"是阳性分类器输出,例如特定ILD)且真值也是p时,则称作真实阳性(TP);然而,如果真实值是n,那么被称作是假阳性(FP)。相反,当预测输出和真实值都是n时则发生真实阴性(其中"n"是阴性分类器输出,例如无ILD,或不存在本文所述的特殊疾病组织),当预测输出是n而真实值是p时,则是假阴性。在一个实施方案中,考虑旨在确定某人是否患有特定疾病的诊断测试。当个人测试为阳性但实际上没有患有该疾病时,在这种情况下是假阳性。另一方面,当个人测试为阴性提示是健康的但实际上患有该疾病时,则是假阴性。在一些实施方案中,假定亚型真实世界流行率的受试者工作特征(ROC)曲线可以通过以相关比例在可得样品上获得的重新抽样误差加以产生。疾病的阳性预测值(PPV)或精确率或后验概率,具有正确诊断的阳性测试结果的患者的比例。这是诊断方法最重要的测量,因为它反映了阳性测试反映被测试的潜在病症的概率。然而,其数值取决于疾病的流行率,它是可能变化的。在一个实施例中,FP(假阳性);TN(真阴性);TP(真阳性);FN(假阴性)。假阳性率(.alpha.)=FP/(FP+TN)-特异性;假阴性率(.beta.)=FN/(TP+FN)-灵敏性;功率=灵敏性=l-β;似然-比阳性=敏感性/(1-特异性);似然-比阴性=(1-灵敏性)/特异性。阴性预测值是具有正确诊断的阴性测试结果的患者的比例。PPV和NPV测量可以使用适当的疾病亚型患病率估计得出。汇集患病率的估算值可以从通过手术大致分为B对M的不确定池中计算。对于亚型特异性的估计,在一些实施方案中,患病率有时可能是无法估算的,因为没有任何可得的样本。在这些情况下,亚型疾病患病率可以用汇集的疾病患病率估计值取代。在一些实施方案中,表达产物或可选择外显子使用的水平可指示如下的一个或多个:IPF,NSIP或HP。在一些实施方案中,本发明方法的表达分析结果提供了给定诊断为正确的统计置信水平。在一些实施方案中,这种统计置信水平为至少大约,或者超过大约85%,90%,91%,92%,93%,94%,95%,96%,97%,98%,99%,99.5%,或者更高。报告主题方法包括生成报告,其提供样品(肺组织样品)是ILD样品的指示。主题诊断方法可以包括生成报告,其提供被测试个体是否患有ILD的指示。主题方法可以包括生成报告,其提供被测试个体是否患有IPF的指示(和不患有,例如除IPF之外的ILD;例如报告可以指示个体患有IPF或不患有NSIP)。在一些实施方案中,诊断ILD的主题方法涉及生成报告。这种报告可以包括如下信息,例如患者患有ILD的可能性;关于进一步评估的推荐;关于治疗药物和/或设备干预的推荐;等等。例如,本文公开的方法可以进一步包括生成或输出报告的步骤,其提供主题诊断方法的结果,该报告可以电子介质的形式提供(例如,计算机监视器上的电子显示),或者以有形介质的形式提供(例如,印刷在纸或其它有形介质上的报告)。对主题诊断方法的结果(例如,个体患有ILD的可能性;个体患有IPF的可能性)的评估可以被称作“报告”或简称为“得分”。准备报告的人或实体(“报告生成者”)还可以执行如下步骤,例如样品收集,样品处理等。可选择地,除报告生成者之外的实体可以执行如下步骤,例如样品收集,样品处理等。诊断评估报告可以提供给用户。“用户”可以是卫生专业人员(例如,临床医生,实验室技术员,医生(如心脏病专家),等等)。主题报告可以进一步包括如下的一种或多种:1)服务提供者的信息;2)患者数据;3)关于给定基因产物或系列基因产物的表达水平、得分或算法判定的数据;4)随访评估建议;5)治疗干预的建议;和6)其他特征。进一步评估根据给定基因产物或系列基因产物的表达水平,和/或根据报告(如上所述),医生或其他合格的医务人员能够确定是否需要对测验受试者(患者)进行进一步的评估。进一步的评估可以包括,例如,肺活量测定。治疗干预根据给定基因产物或系列基因产物的表达水平,和/或根据报告(如上所述),医生或其他合格的医务人员能够确定是否需要建议适当的治疗干预。治疗干预包括基于药物的治疗干预、基于设备的治疗干预,和手术干预。当报告指示个体可能患有IPF时,基于药物的治疗干预包括例如向个体施加有效量的吡非尼酮、强的松、硫唑嘌呤、或N-乙酰半胱氨酸。手术干预包括,例如,动脉搭桥手术。计算机实现的方法、系统和设备本公开的方法可以是计算机实现的,从而该方法步骤(例如,测定、比较、计算等)的全部或部分是自动的。因此,本公开提供了方法、计算机系统、设备等与计算机实现的方法联用,以方便间质性肺病的诊断(例如,IPF、NSIP、HP等的诊断),包括区别诊断。例如,方法步骤包括获得生物标记物水平的值,比较标准化生物标志物(基因)的表达水平与对照水平,计算ILD的可能性,生成报告等,可以全部或部分地通过计算机程序产品执行。获得值可被电子存储在例如数据库中,并能够进行通过编程计算机执行的算法。例如,本发明的方法可以涉及将生物标记物水平(例如,基因产物的标准化表达水平)输入计算机中,其被编程执行本文所述比较和计算步骤的算法,并生成本文所述的报告,例如通过显示或打印报告到位于计算机本地或远程的输出装置。输出的报告可以是得分(例如,数值得分(数值表示)或非数值得分(例如,非数值输出(例如,”IPF”,”无IPF证据”)),数值或数值范围的表示。因此,本发明提供了计算机程序产品,包括在其中存储了计算机程序的计算机可读存储介质。该程序在被计算机阅读时能够根据从个体的一个或多个生物样品(例如肺组织样品)的分析获得的数值执行相关计算。计算机程序产品被存储在用于执行计算的计算机程序中。本公开提供了用于执行上述程序的系统,该系统一般包括:a)中央计算环境;b)输入装置,与计算环境操作连接以接收患者数据,其中患者数据可以包括,例如,使用患者的生物样品从测定获得的生物标记物水平或其它数值,如上所述;c)输出装置,与计算环境连接以便提供信息给用户(例如,医疗人员);和d)由中央计算环境(例如,处理器)执行的算法,其中算法根据被输入设备接收的数据执行,并且其中该算法计算一个数值,该数值指示受试者患有ILD的可能性,如本文所述。计算机系统图5描述了计算机化实施方案的一般实例,其中可以执行程序以方便本公开方法的执行,其例证了处理系统100,其一般包括至少一个处理器102或处理单元或多个处理器,存储器104,至少一个输入设备106和至少一个输出设备108,其通过总线或总线组110偶联在一起。在某些实施方案中,输入设备106和输出设备108可以是相同的设备。还可以提供接口112,用于将处理系统100偶联到一个或多个外围设备,例如接口112可以是PCI卡或PC卡。可以提供至少一个存储装置114,其容纳至少一个数据库116。存储器104可以是任何存储设备形式,例如易失性或非易失性存储器,固态存储设备,磁设备等。处理器102可以包括多个不同的处理设备,例如,以处置该处理系统100内的不同功能。输入设备106接收输入数据118,并可以包括例如键盘,指针装置如笔状装置或鼠标,用于语音控制激活的音频接收设备如麦克风,数据接收器或天线例如调制解调器或无线数据适配器、数据采集卡等。输入数据118可以来自不同的来源,例如通过网络与接收数据联系的键盘装置。输出装置108产生或生成输出数据120,并且可以包括,例如,显示装置或监视器,在这种情况下输出数据120是可视的,打印机,在这种情况下输出数据120被打印,端口例如USB端口,外围部件接口,数据发送器或天线如调制解调器或无线网络适配器等。输出数据120可以是不同的并且来自于不同的输出设备,例如在监视器上可视显示并连同发送到网络。用户可以在例如监视器上或使用打印机查看数据输出或输出数据的解释。存储装置114可以是任何形式的数据或信息存储装置,例如易失性或非易失性存储器,固态存储设备,磁设备等。在使用时,处理系统100适于允许数据或信息被存储在至少一个数据库116中,和/或通过有线或无线通信装置进行检索。接口112可以允许在处理单元102和可能用作专门用途的外围组件之间进行有线和/或无线通讯。一般地,处理器102可以经由输入设备106接收作为输入数据118的指令,并能够通过利用输出装置108向用户显示经过处理的结果或其它输出。可以提供多个输入装置106和/或输出设备108。处理系统100可以是任何合适形式的终端、服务器、专用硬件或类似物。处理系统100可以是网络化通信系统的一部分。处理系统100可以连接到网络上,例如因特网或WAN。输入数据118和输出数据120可以通过网络与其他设备通讯。可以使用有线通信装置或无线通信装置实现信息和/或数据在网络上的传输。服务器可以方便数据在网络和一个或多个数据库之间的转移。服务器和一个或多个数据库提供信息源的一个实例。因此,图3所示的处理计算系统环境100可以在互联网环境中使用与一个或多个远程计算机的逻辑连接进行操作。远程计算机可以是个人计算机、服务器、路由器、网络PC、对等设备、或其它常见的网络节点,并且通常包括许多或所有上述元件。图5所示的逻辑连接包括局域网(LAN)和广域网(WAN),但也可以包括其它网络,例如个人区域网(PAN)。这样的联网环境常见于办公室、企业范围的计算机网络、内联网和因特网。例如,当在LAN联网环境中使用时,计算系统环境100通过网络接口或适配器连接到LAN。当在WAN联网环境中使用时,计算系统环境通常包括调制解调器或其他装置,用于建立跨越WAN(如因特网)的通信。调制解调器可以是内置或外置的,可以通过用户输入接口或者通过其它合适的机制连接到系统总线。在联网环境中,相对于计算系统环境100或其部分描述的程序模块可以被存储在远程存储器存储设备中。应该理解,图5示例的网络连接是实施例,可以使用其它方法在多个计算机之间建立通讯连接。图5意图提供一个关于计算环境的例证性和/或合适实例的简要的一般性描述,其中可以实现本文公开方法的实施方案。图5是合适环境的一个实例,并且不旨在提出对本发明实施方案的结构、使用范围、或功能具有任何限制。特殊的环境不应被解释为具有任何依赖性或要求与示例操作环境中例证的任何一个组件或其组合相关。例如,在某些情况下,环境的一个或多个元件可被认为是不必要的并可省略。在其他情况下,一个或多个其它元件可以被看作是必要的并且纳入。某些实施方案可以参考操作的行为(act)和符号表示进行描述,其由一个或多个计算设备,例如图5的计算系统环境100执行。因此,可以理解,这种行为和操作在指示由计算机执行时,包括由计算机处理器操作代表具有结构化形式的数据的电子信号。这种操作转换数据或者将它们保持在计算机存储系统中,其重新配置或者以其他方式改变计算机的操作,该方式是本领域技术人员可以理解的。保持数据的数据结构是存储的物理位置,其具有被该数据格式限定的特殊属性。然而,尽管实施方案在前述内容中被描述,但是并不意味着是限制性的,因为本领域技术人员会意识到,在下文中描述的行为和操作描述也可以在硬件中实现。实施方案可以用大量其他通用或专用计算设备和计算系统环境或配置来实施。可适用于实施方案的众所周知的计算系统、环境和配置的实例包括,但不仅限于,个人计算机、手持或膝上型设备、个人数字助理、多处理器系统、基于微处理器的系统、可编程消费类电子产品、网络、微型计算机、服务器计算机、网络服务器计算机、大型计算机,以及包括任何上述系统或设备的分布式计算环境。实施方案可以在计算机可执行指令的一般内容中被描述,例如由计算机执行的程序模块。一般而言,程序模块包括例程、程序、对象、组件、数据结构等,其执行特定任务或实现特定抽象数据类型。实施方案还可以在分布式计算环境中执行,其中任务由通过通信网络连接的远程处理设备执行。在分布式计算环境中,程序模块可以位于本地和远程计算机存储介质中,包括存储器存储设备。计算机程序产品本公开提供了计算机程序产品,其在可编程计算机上例如参考图5所述的那些执行时,能够执行本公开的方法。如上面讨论的,本文所描述的主题可体现为系统、设备、方法、和/或制品,其取决于所期望的配置。这些各种实现可以包括在一个或多个计算机程序中实现,其是可以在包括至少一个可编程处理器的可编程系统上执行和/或解释的,其可以是专用或通用,被偶联从存储系统、至少一个输入装置(例如,摄像机,话筒,操纵杆,键盘,和/或鼠标)、以及至少一个输出装置(例如显示监视器,打印机等)接收数据和指令并向其传送数据和指令。计算机程序(也称作程序、软件、软件应用、应用、组件或编码)包括用于可编程处理器的指令,并且可以用高级程序和/或面向受试者的编程语言,和/或汇编/机器语言实现。如本文所使用的,“机器可读介质”是指任何计算机程序产品、装置和/或设备(例如,磁盘、光盘、存储器,等等),用于提供机器指令和/或数据到一个可编程处理器,包括接收机器指令作为机器可读信号的机器可读介质。从本描述可以显见,本公开的方面可以,至少部分地,在软件、硬件、固件、或其任何组合中实现。因此,本文描述的技术并不仅限于硬件电路和/或软件的任何特定组合,或者仅限于通过计算机或其他数据处理系统执行的指令的任何特定来源。相反,这些技术可以在计算机系统或其它数据处理系统中响应一个或多个处理器例如微处理器被执行,指令的执行序列存储在存储器或其它计算机可读介质中,包括任何类型的ROM、RAM、高速缓冲存储器、网络存储器、软盘、硬盘驱动器磁盘(HDD)、固态器件(SSD)、光盘、CD-ROM、和磁光盘、EPROM、EEPROM、闪存、或任何其他类型的适用于以电子格式存储指令的介质。此外,处理器(多个处理器)可以是,或者可以包括,一个或多个可编程通用或专用微处理器、数字信号处理器(DSP)、可编程控制器、专用集成电路(ASIC)、可编程逻辑器件(PLD)、可信平台模块(TPM),或类似物,或这些设备的组合。在可选择的实施方案中,专用硬件例如逻辑电路或其它硬件电路可以和软件指令组合使用,以实现本文所述的技术。阵列和试剂盒本公开提供了用于执行主题评估方法或主题诊断方法的阵列和试剂盒。阵列主题阵列可以包括多种核酸,其每一个与从进行ILD测试的个体获得的组织样品中存在的细胞中差异表达的基因杂交。主题阵列可以包括多个成员核酸,其中每一个成员核酸与不同的基因产物杂交,其中感兴趣的基因产物是在表3-11和13-34中列出的那些。在一些情况下,两个或更多个成员核酸与相同基因产物杂交;例如,在某些情况下,2,3,4,5,6,7,8,9,10或更多个成员核酸与相同的基因产物杂交。成员核酸的长度可以是大约5个核苷酸(nt)到大约100nt,例如,5,6,7,8,9,10,11,12,13,14,15,16,1718,19,20,20-25,25-30,30-40,40-50,50-60,60-70,70-80,80-90,或90-100nt。核酸可以具有一个或多个磷酸酯骨架修饰。主题阵列可以包括大约10-大约105个独特的成员核酸,或者超过105个独特的成员核酸。例如,主题阵列可以包括大约10-大约102,大约102-大约103,大约103-大约104,大约104-大约105,或超过105个独特的成员核酸。在一些情况下,主题阵列包括多个成员核酸,其中一个或多个成员核酸与选自下面的基因的不同基因产物杂交:1)THY1;2)GALNT13;3)CFH;4)CRTAC1;5)CHD3;6)TSHZ2;7)ENSG00000123119;8)ISM1;9)ENSG00000236972;10)PDE7B;11)SULF1;12)FABP5;13)FABP5;14)PTGFRN;15)IGFBP5;16)CFHR1;17)MS4A15;18)FAM13C;19)STC1;20)RCAN2;21)LG12;22)CCND2;23)DCLK1;24)C22orf46;25)IGF1;26)CSF3R;27)PPP4R4;28)CEBPD;29)NMNAT2;30)EPB41L5;31)ZNF385D;32)FCN3;33)CNTN6;34)DGKA;35)CSGALNACT1;36)SYT15;37)STX11;38)ITSN1;39)TMEM100;40)EGFLAM;41)C13orf15;42)ENSG00000182010;43)ERRFI1;44)RGS16;45)SLN;46)ENSG00000146374;47)TCID8066275;48)CSCL2;49)ITLN1;和50)PDE2A。在一些情况下,主题阵列包括多个成员核酸,其中一个或多个成员核酸与选自下面的不同基因的基因产物杂交:1)ASPM;2)BUB1;3)PTTG1;4)SHCBP1;5)NUSAP1;6)MKI67;7)HJURP;8)CDCA3;9)PLK1;10)PRR11;11)BRCA2;12)ORM1;13)CCNB2;14)SMC4;15)HM13;16)DMD;17)FHL1;18)ORM2;19)NDUFC2-KCTD14;20)NCAPH;21)TTLL7;22)DEPDC1B;23)CNTN4;24)PRKAA2;25)PRKCQ;26)CDC42BPA;27)PARD3B;28)SCTR;29)CSF3R;和30)MPDZ。试剂盒本公开的试剂盒可以包括阵列,如上所述;和用于分析基因产物表达水平的试剂。用于分析核酸基因产物表达水平的试剂包括,例如,适于测序核酸的试剂;适于扩增核酸的试剂;和适于核酸杂交的试剂。试剂盒的其它任选组分包括:缓冲液;可检测标签;用于可检测标签显影的组分(例如,其中核酸探针包括可检测的标签);等。试剂盒的各种组分可以存在于分开的容器中,或者某些相容的成分可以根据需要预先组合在单一容器中。除了上述组分之外,主题试剂盒可以包括用于使用试剂盒组分实践主题方法的说明书。用于实践主题方法的说明书一般被记录在合适的记录介质中。例如,说明书可以印刷在基质上,例如纸或塑料等。因此,该说明书可以作为包装插页存在于试剂盒中,在试剂盒或其组分的容器物标签中(即,与包装或分装相关)等。在其他实施方案中,说明书作为电子存储数据文件存在于合适的计算机可读存储介质中,例如只读光盘存储器(CD-ROM)、数字多功能盘(DVD)、软盘等。在其它实施方案中,实际的说明书不存在于试剂盒中,但是提供了通过例如互联网从远程源获得说明书的方法。这种实施方案的实例是如下的试剂盒,其包括一个网址,其中可以查看说明书和/或从那里下载说明书。对于该说明书,这种用于获得说明书的方法被记录在合适的基质上。实施例阐述了如下的实施例,以便给本领域的普通技术人员提供完整的公开,和如何制造和使用本发明的描述,但并不意图限制本发明人考虑本发明的范围,也不意图表示下面的实验是可执行的全部或仅有的实验。我们已经努力确保所用数字(例如,量、温度等)的准确性,但是一些实验误差和偏差应该予以考虑。除非另外指出,否则份数是重量份数,分子量是重均分子量,温度为摄氏度,压力为大气压或接近大气压。可以使用标准缩写,例如,bp,碱基对;kb,千碱基;pi,皮升;s或sec,秒;min,分钟;h或hr,小时;aa,氨基酸;kb,千碱基;bp,碱基对;nt,核苷酸;i.m.,肌内注射;i.p.,腹膜内注射;s.c.,皮下注射;等。术语和缩写下面的实施例使用这里简述的术语和缩写:“ENSEMBLID”是指来自ENSEMBL基因组浏览器数据库的基因标识符号码。每个标识符以字母ENSG开始,表示“Ensembl基因”。每个ENSEMBLID号码(即,在ENSEMBL数据库中的每个的“基因”)是指由特殊人染色体上的特定的开始和结束位置限定的基因,因此限定了图35中定义的人基因组的特定基因座。例如,图35的第一ENSEMBLID是ENSG00000000938,它位于人染色体(“Chrom.”)1((“chrl”)上。ENSG00000000938的基因座开始与1号染色体上的核苷酸位置27938575并结束于核苷酸位置27961788,因此该基因座,其包括内含子序列,可以说是长度为23,213个核苷酸。数据库中的大多数基因被命名,而一些残余的尚未命名(标注为“NA”)。来自人基因组的转录本序列被分配转录本标识符号码,其开头字母ENST表示“Ensembl转录本”。每个转录本映射到人基因组的一个区域,因此是特殊区域的表达产物。因为基因组中的每个基因座可能有一个或多个不同的转录本(例如,一些基因有多个启动子位点,编码多个不同的剪接形式等),每个ENSG编号的标识符可能与多个转录本相关联(例如,重叠的转录本)。如本文所使用的,指称“ENSG”ENSEMBLID”是指从人基因组相应基因座产生的基因表达产物。例如,指称ENSG00000000938(见例如图35)包括从人1号染色体上从开始于核苷酸位置27938575并终止于核苷酸位置27961788的基因座所产生的任何基因产物。因此,指称ENSG00000000938包括表35(图35)中列出的所有与特殊ENSG号码(在这种情况下:ENST00000374005,ENST00000399173,ENST00000545953,ENST00000374004,ENST00000469062,ENST00000374003,ENST00000457296,ENST00000475472,和/或ENST00000468038)相关的转录本以及从该基因座产生的任何其它转录本(或编码多肽)。本申请书中出现的所有“ENSG”ENSEMBLID”号码可以和图35交叉参考。用于检测来自给定基因座的基因表达产物的方法是本领域普通技术人员容易理解的,并且可以使用任何方便的方法。作为非限制性实例,用于检测来自给定基因座的RNA基因表达产物的合适方法包括基于杂交的方法(例如Northern印迹分析)、逆转录酶聚合酶链式反应(RT-PCR)、定量RT-PCR(QRT-PCR)、实时RT-PCR、微阵列、RNAseq(RNA测序),等等。作为非限制性实例,用于检测来自给定基因座的蛋白质基因表达产物的合适方法包括基于抗体的方法(例如,Western印迹、免疫组织化学、免疫荧光、FACS(荧光激活细胞分选)等),蛋白质测序方法、基于质谱的方法,等等。实施例1:微阵列样品队列-IPF的生物标记物和分类样品与使用专家标签(expertlabel)的病理分类一起列出。毛细支气管炎(BRONCH,n=l)、未分类的慢性间质纤维化(CIF-NOC,n=4)、超敏感性肺炎(HP,n=4)、特发性肺纤维化(IPF,n=21)、正常肺(NML,n=4)、非特异性间质性肺炎(NSIP,n=8)、机化性肺炎(OP,n=2)、其他(OTHER,n=4)、呼吸性细支气管炎(RB,n=2)、结节病(SARC,n=2)、吸烟相关的间质纤维化(n=l)、普通人类参考RNA(n=3)。所有样品均通过视频辅助的胸腔镜手术(VATS)获得。表1提供了样品列表和每种的病理标签表1病理标签病理缩写毛细支气管炎BRONCH未分类的慢性间质性纤维化CIF-NOC未分类的慢性间质性纤维化CIF-NOC未分类的慢性间质性纤维化CIF-NOC未分类的慢性间质性纤维化CIF-NOC超敏感性肺炎HP超敏感性肺炎HP超敏感性肺炎HP超敏感性肺炎HP特发性肺纤维化IPF特发性肺纤维化IPF特发性肺纤维化IPF特发性肺纤维化IPF特发性肺纤维化IPF特发性肺纤维化IPF特发性肺纤维化IPF特发性肺纤维化IPF特发性肺纤维化IPF特发性肺纤维化IPF特发性肺纤维化IPF表1病理标签病理缩写特发性肺纤维化IPF特发性肺纤维化IPF特发性肺纤维化IPF特发性肺纤维化IPF特发性肺纤维化IPF特发性肺纤维化IPF特发性肺纤维化IPF特发性肺纤维化IPF特发性肺纤维化IPF特发性肺纤维化IPF正常肺NML正常肺NML正常肺NML正常肺NML正常肺NML正常肺NML正常肺NML正常肺NML正常肺NML正常肺NML非特异性间质性肺炎NSIP非特异性间质性肺炎NSIP非特异性间质性肺炎NSIP非特异性间质性肺炎NSIP非特异性间质性肺炎NSIP非特异性间质性肺炎NSIP非特异性间质性肺炎NSIP非特异性间质性肺炎NSIP机化性肺炎OP机化性肺炎OP其它OTHER其它OTHER其它OTHER其它OTHER呼吸性细支气管炎RB呼吸性细支气管炎RB结节病SARC表1病理标签病理缩写结节病SARC吸烟相关的间质纤维化SRIF普通人类参考RNAUHR普通人类参考RNAUHR普通人类参考RNAUHR表2提供了关于RNAseq样品队列的信息。样品使用专家标签的病理分类一起列出。未分类的慢性间质纤维化(CIF-NOC,n=3)、恶性甲状腺RNA(CONTROL,n=6)、超敏感性肺炎(HP,n=3)、正常肺(NML,n=5)、非特异性间质性肺炎(NSIP,n=7)、机化性肺炎(OP,n=1)、其他(OTHER,n=1)、呼吸细支气管炎(RB,n=1)、鳞状细胞癌(SQC,n=2)、普通型间质性肺炎(n=18)。所有样品均通过视频辅助的胸腔镜手术(VATS)获得。表2病理标签标签缩写未分类的慢性间质性纤维化CIF-NOC未分类的慢性间质性纤维化CIF-NOC未分类的慢性间质性纤维化CIF-NOC恶性甲状腺RNA对照恶性甲状腺RNA对照恶性甲状腺RNA对照恶性甲状腺RNA对照恶性甲状腺RNA对照恶性甲状腺RNA对照超敏感性肺炎HP超敏感性肺炎HP超敏感性肺炎HP正常肺NML正常肺NML正常肺NML正常肺NML正常肺NML非特异性间质性肺炎NSIP非特异性间质性肺炎NSIP非特异性间质性肺炎NSIP非特异性间质性肺炎NSIP非特异性间质性肺炎NSIP非特异性间质性肺炎NSIP非特异性间质性肺炎NSIP表2病理标签标签缩写机化性肺炎OP其它OTHER呼吸性细支气管炎RB鳞状细胞癌SQC鳞状细胞癌SQC普通间质性肺炎UIP普通间质性肺炎UIP普通间质性肺炎UIP普通间质性肺炎UIP普通间质性肺炎UIP普通间质性肺炎UIP普通间质性肺炎UIP普通间质性肺炎UIP普通间质性肺炎UIP普通间质性肺炎UIP普通间质性肺炎UIP普通间质性肺炎UIP普通间质性肺炎UIP普通间质性肺炎UIP普通间质性肺炎UIP普通间质性肺炎UIP普通间质性肺炎UIP普通间质性肺炎UIP结果如图1-4所示。图1和3使用如下的缩写:knn:指“K最近邻”,这是一种根据特征空间中最接近训练实例对样品进行分类的方法。样品通过其近邻的多数投票进行分类,将目标指定给k个最近邻中最常见的分类(k是正整数,通常较小)。如果k=1,那么该目标可以简单地指定给它最近邻所属的类别。lassolr:指“Lasso线性回归”,这是一种使用变量选择方法的分类方法,其基于Lasso线性回归方法,以线性模型进行评估(TibshiraniR.J.RegressionshrinkageandselectionviatheLASSO.JRoyStatistSocB.1996;58(1):267-288),其使残余平方和(residualsumofsquares)最小化,系数的绝对值之和小于一个常数。Ldadiag:指“DiagonalLDA”,这是一种在机器学习中用于发现可表征或分离两类或多类样品的特征线性组合的方法。在DLDA中的“diagonaF”表示训练中使用的基因之间相互独立的假设。这种假设,在通过适当的基因选择,通常可以比更一般的LDA技术提供更高的性能。Svmlinear:是指“具有线性Kernel支持向量机”,这是一种用于分类的与分析数据和识别模式的相关学习算法相关的监督学习模型(supervisedlearningmodel)。基本的SVM为每个给定的输入采用一系列输入数据和预测,其中两个可能的类构成输出,使之成为一个非概率二进制线性分类器。给定一系列训练示例,每一个被标记为属于两个类别之一,SVM训练算法将构建模型,将新的实例指定给一个分类或其他。SVM模型是一个实例代表,对空间中的点进行映射,使得不同类别的实例被分割出一个尽可能宽的明显间隙。然后,新的实例被映射到相同的空间中,并基于它们落在间隙的哪一侧来预测所属类别。SVM由核函数(kernelfunction)(在当前实现中是线性、径向或多项式的)的选择和对于误判的成本惩罚加以限定,其中对于误判的成本惩罚可以被保持恒定的“固定成本”或者在网格上变化以检查跨越成本景观(costlandscape)的性能。updown:是指“Up-Down”,其为一种对样品进行分类的方法,并不是根据标准化表达强度的真实值,而是根据在训练中使用的每个基因在一个类别中对其他通常是“up”(即,上调)还是“down”(即,下调)。这种分类方法对于实验噪音和批次影响是非常强大的,但是需要基因在所研究的两类样品之间具有大且可重复的倍数变化。Svmlinearfixedcost:是指使用单成本值(例如0.01)而不是“linearsvm”训练SVM分类器,其涉及使用多种成本值(例如-0.001、-0.01、-0.1、1、10、100)训练SVM,并在性能与复杂性之间选择最佳的权衡。这种成本参数决定误判罚分—较高的罚分导致更高的复杂性和潜在的过度拟合分类,而较低的成本罚分则导致更简单的SVM分类并且在训练系列中的性能降低,但是有可能为测试系列的推广提供更好的机会。本文提供的生物标记物是使用NugenWT扩增系统扩增的RNA进行的AffymetrixGene1.0ST微阵列分析获得的。差异性基因表达和特征选择使用Limma模型(Smyth2004)。特征选择策略可以细分为如下步骤:1)选择数据集中上面50%的最可变转录本集群ID(TCID,aka基因)(即在两组之间,例如IPF对NSIP,表达差异最高的),和步骤2)通过Limma以10%的FDR截止对这些TCID进行分析。在交叉验证期间使用弃一(leave-one-out)方法对分类性能进行评估。图2.NSIP样品在分类器上的得分较低,而IPF样品得分高。图2X-轴从左至右,前8个样品的结果对应NSIP样品,其余结果对应IPF样品。在本实施例中,只有2个样品(一个NSIP和一个IPF)被错误分类。表3列出了在IPF对NSIP分类器中使用的30个基因系列的生物标记物。表3基因标识符EnsemblIDTCIDLogFCP值FDRp值ASPMENSG000000662797923086-1.033.83E-141.28E-09BUB1ENSG000001696798054580-0.997.17E-132.72E-09PTTG1ENSG000001646118109639-1.121.49E-123.65E-09SHCBP1ENSG000001712418001133-0.821.57E-123.65E-09NUSAP1ENSG000001378047982889-0.887.51E-121.19E-08MKI67ENSG000001487737937020-0.921.13E-111.57E-08HJURPENSG000001234858059838-0.551.71E-112.27E-08CDCA3ENSG000001116657960702-0.554.03E-114.47E-08PLK1ENSG000001668517994109-0.618.94E-118.53E-08PRR11ENSG000000684898008784-0.674.01E-102.90E-07BRCA2ENSG000001396187968484-0.671.07E-096.84E-07ORM1ENSG000002293148157446-1.492.09E-091.24E-06CCNB2ENSG000001574567983969-0.651.81E-086.84E-06SMC4ENSG000001138108083709-0.512.76E-089.10E-06HM13ENSG000001012948061542-0.375.02E-081.41E-05DMDENSG0000019894781719210.736.76E-081.72E-05FHL1ENSG0000002226781701190.704.33E-076.83E-05ORM2ENSG000002282788157450-0.801.54E-061.79E-04NDUFC2-KCTD14ENSG000001513647950641-0.681.71E-061.91E-04NCAPHENSG000001211528043602-0.442.52E-062.50E-04TTLL7ENSG0000013794179171990.671.09E-057.44E-04DEPDC1BENSG000000354998112260-0.461.24E-058.06E-04CNTN4ENSG0000014461980773230.521.29E-043.90E-03PRKAA2ENSG0000016240979017200.641.52E-044.39E-03PRKCQENSG000000656757931930-0.502.00E-045.24E-03CDC42BPAENSG0000014377679247730.288.24E-041.30E-02PARD3BENSG0000011611780477090.222.55E-032.56E-02SCTRENSG000000802938054846-0.433.53E-033.12E-02CSF3RENSG000001195357914950-0.347.16E-034.84E-02MPDZENSG0000010718681600880.271.24E-026.84E-02图6A和6B提供了基于显著性(FDRp<0.05)的标记物综合列表。在该分析中总共有495个标记物被发现是显著的。这里列出的基因在IPF中是过表达的或者低表达的。图6A和6B中列出的基因在IPF和NSIP之间差异性表达。图7提供了使用RNA-Seq在IPF和NSIP之间差异性表达的基因。图7提供了根据RNASeq数据的EdgeR分析的标记物的综合列表。在该分析中总共有296个标记物被发现是显著的。基因根据FDRp-值排列。图8提供了使用RNA-Seq在IPF和NSIP之间差异性表达的基因。提供了根据RNASeq数据的NPSeq分析的标记物的综合列表。在该分析中总共有160个标记物被发现是显著的。基因根据FDRp-值排列。这里提供的生物标记物是通过使用NugenWT扩增系统扩增的RNA的AffymetrixGeneST微阵列分析获得的。差异性基因表达和特征选择使用Limma模型(引用Smyth)。特征选择策略可以细分为如下步骤:1)选择数据集中上面50%的最可变转录本集群ID(TCID,aka基因)(即在两组之间,例如IPF对NSIP,表达差异最高的),和步骤2)通过Limma以10%的FDR截止对这些TCID进行分析。在交叉验证期间使用弃一方法对分类性能进行评估。表4提供了在IPF对正常分类器中使用的生物标记物的列表。图3和4提供的数据显示了使用表4中列出的50个基因的生物标记物标识的结果。图3.使用优选的50个基因标识的IPF对正常的分类错误率。图4.使用50个基因标识的IPF对正常的分类。图4X-轴从左至右,前13个样品的结果对应正常样品,其余结果对应IPF样品。在该分类器上,正常肺样品得分低而IPF样品得分高。在本实施例中只有3个样品(1个正常和2个IPF)被错误分类。表4基因标识符EnsemblIDTCIDLogFCp值FDRp值THY1ENSG0000015409679522681.803.25E-201.08E-16GALNT13ENSG000001442788045776-1.283.59E-186.29E-15CFHENSG0000000097179084590.943.88E-186.47E-15CRTAC1ENSG000000957137935535-1.145.62E-177.49E-14CHD3ENSG0000017000480046990.458.73E-171.08E-13TSHZ2ENSG0000018246380634371.221.39E-161.66E-13NAENSG000001231198147244-1.792.01E-162.23E-13ISM1ENSG0000010123080610131.221.95E-151.58E-12NAENSG000002369727971998-0.652.59E-151.96E-12PDE7BENSG0000017140881222221.264.76E-153.30E-12SULF1ENSG0000013757381468631.495.66E-153.84E-12FABP5ENSG000001646877948420-0.751.04E-146.77E-12FABP5ENSG000001646878147049-0.741.49E-148.57E-12PTGFRNENSG0000013424779042930.751.40E-136.76E-11表3基因标识符EnsemblIDTCIDLogFCP值FDRp值IGFBP5ENSG0000011546180588571.188.20E-133.03E-10CFHR1ENSG0000024441479084880.731.79E-125.90E-10MS4A15ENSG000001669617940333-1.133.22E-121.00E-09FAM13CENSG0000014854179337331.072.39E-115.00E-09STC1ENSG000001591678149825-1.001.23E-101.91E-08RCAN2ENSG0000017234881267600.742.24E-103.09E-08LGI2ENSG0000015301280996850.801.13E-091.14E-07CCND2ENSG0000011897179532000.494.00E-093.13E-07DCLK1ENSG0000013308379709540.889.45E-096.27E-07C22orf46ENSG0000018420880734700.321.32E-088.19E-07IGF1ENSG0000001742779658731.043.77E-081.97E-06CSF3RENSG000001195357914950-0.645.85E-082.78E-06PPP4R4ENSG000001196987976451-0.581.85E-077.36E-06CEBPDENSG000002218698150592-0.424.41E-071.53E-05NMNAT2ENSG0000015706479227560.681.63E-064.48E-05EPB41L5ENSG000001151098044882-0.622.62E-066.67E-05ZNF385DENSG0000015178980857741.043.68E-068.68E-05FCN3ENSG000001427487914075-1.415.96E-061.30E-04CNTN6ENSG000001341158077299-0.575.22E-057.77E-04DGKAENSG0000006535779560460.448.10E-051.12E-03CSGALNACT1ENSG0000014740881495740.470.000103161.36E-03SYT15NA7933298-0.340.0001256931.59E-03STX11ENSG000001356048122457-0.440.0001946712.25E-03ITSN1ENSG0000020572680683050.230.0011608149.50E-03TMEM100ENSG000001662928016841-0.890.0015406231.20E-02EGFLAMENSG0000016431881050130.250.0016099431.24E-02C13orf15ENSG000001027607968789-0.430.0044028732.75E-02NAENSG000001820107933855-0.950.008049484.40E-02ERRFI1ENSG000001162857912157-0.460.0085957024.63E-02RGS16ENSG000001433337922717-0.310.0090734534.82E-02SLNENSG0000017029079514791.040.0114018335.77E-02NAENSG0000014637481219160.560.0115223245.82E-02NANA8066275-0.380.0291163781.15E-01CXCL2ENSG000000810418100994-0.550.0376626641.39E-01ITLN1ENSG0000017991479216900.930.214561734.45E-01PDE2AENSG0000018664279501620.100.3773321516.18E-01图9A-9D提供了使用微阵列数据在IPF对“其余”中差异性表达的基因。图9A-D中的“其余”是指除IPF之外的ILD的组合;例如在图9A-D中,“其余”是指如下的ILD例如HP、NSIP和结节病。在图9A-D中,根据对错误发现率(FDR)进行修正之后的显著性(p<0.05)对标记进行排序。使用这一分析总共有1342个标记物被发现是显著的。列出了在IPF中过表达的基因和在IPF中低表达的基因。图10A-10G提供了使用微阵列数据在IPF对正常中差异性表达的基因。在图10A-10G中,根据对FDR进行Benjamini和Hochberg修正之后的显著性(p<0.05)对标记物进行排序。使用这种分析总共有2521个标记物被发现是显著的。这里列出的基因包括在IPF中过表达的基因和在IPF中低表达的基因。图11A-11F提供了使用微阵列数据在NSIP对正常中差异性表达的基因。在图11A-F中,根据对FDR进行Benjamini和Hochberg修正之后的显著性(p<0.05)对标记物进行排序。使用这种分析总共有2253个标记物被发现是显著的。这里列出的基因包括在NSIP中过表达的基因和在NSIP中低表达的基因。图12提供了使用微阵列数据在NSIP对HP中差异性表达的基因。在图12中,根据对错误发现率(FDR)进行Benjamini和Hochberg修正之后的显著性(p<0.05)对标记物进行排序。使用这种分析总共有13个标记物被发现是显著的。这里列出的基因包括在NSIP中过表达的基因和在NSIP中低表达的基因。图13A-13F提供了使用微阵列数据在正常(NML)对“其余”中差异性表达的基因。在图13A-13F中,根据对FDR进行Benjamini和Hochberg修正之后的显著性(p<0.05)对标记物进行排序。使用这种分析总共有2297个标记物被发现是显著的。这里列出的基因包括在NML(logFC列)中过表达的基因和在NML中低表达的基因。图14提供了使用微阵列数据在NP对NML中差异性表达的基因。在图14中,根据对FDR进行Benjamini和Hochberg修正之后的显著性(p<0.05)对标记物进行排序。使用这种分析总共有311个标记物被发现是显著的。这里列出的基因包括在HP中过表达的基因和在HP中低表达的基因。表5总结了使用RNA-Seq和微阵列数据的显著基因的数目。图15A-27E提供了其它基因表达分析的结果。实施例2-数据分析和算法数据收集ILD样品通过视频辅助胸腔镜手术(VATS)收集,而正常肺(NML)在肺移植期间或之后从切除后的癌旁正常组织收集。两者都放在干冰上并贮存于-80℃直至使用。RNA分离、扩增、微阵列杂交使用AllPrep微量试剂盒(Qiagen)从VATS样品提取RNA。RNA的量使用Quant-ITRNA试剂盒(Invitrogen,Carlsbad,CA)确定,RNA质量用BioanalyzerPicochip系统(AgilentTechnologies,SantaClara,CA)确定,以生成RNA完整数(RNAintegritynumber)(RIN)。15纳克总RNA用NuGEN(SanCarlos,CA)WTAOvation扩增系统(WTAFFPEOvation)扩增,产生5.0pg生物素标记的cDNA,用于微阵列杂交。随后按照制造商的方案进行清洗、染色、和在GeneChipFluidics450/Scanner30007G系统和/或GeneChip系统(Affymetrix,SantaClara,CA)上扫描。扩增的样品使用标准程序与人基因1.0ST微阵列(Affymetrix)杂交。杂交后、质量控制和标准化使用R/BioconductorOligo包(1.22.0版)处理、标准化和总结输出(杂交后)微阵列数据(.CEL)文件,通过背景校正、分位数标准化,和强大的多芯片平均(RMA)。这种自动化处理程序产生一个探针系列-水平强度矩阵和基因-水平强度矩阵。杂交后的质量控制包括检测高于背景(pDET或DABG,>=0.21)和对照探针的管家-抗基因组信号AUC(HAAUC,>=0.88)。准确分类可能涉及多种技术因素,包括失败或不理想的杂交。杂交后的QC量度与鉴定技术因素的预杂交QC变量有关,其可能会掩盖或偏置信号强度。训练系列的组成用于初步IPF对NSIP或IPF对正常分类器的训练系列使用如表1所列的标记样品。用于ILD亚型的训练标签根据患者手术切除活检(VATS)的专家组织病理学诊断加以定义。分类器训练和特征选择每一个ILD分类器均是二元分类器,试图将个人样品分类成显示IPF或其它类型:正常肺组织或者存在NSIP病理模式的肺组织的证据。使用嵌套交叉验证(详见下文)对分类器性能进行评估,其在每一个交叉验证循环内使用顺次的特征选择程序,以鉴定可区分各个亚型的标记物。亚型特异性表达的Limma分析被应用到这些数据系列中(Smyth,G.K.(2005).Limma:linearmodelsformicroarraydata.收载于:'BioinformaticsandComputationalBiologySolutionsusingRandBioconductor'.R.Gentleman,V.Carey,S.Dudoit,R.Irizarry,W.Huber(编),Springer,NewYork,397-420页)。来自limma分析的Top标记物(按照错误发现率顺序排名)包含在初始特征系列中。这些标记物用多种分类方法进行评估,包括使用线性核函数的支持向量机(SVM线性)(C.Cortes和V.Vapnik.Supportvectornetworks.MachineLearning,20:273-297,1995),k最近邻(KNN),线性判别分析(LDADIAG)和Up/DOWN分类器(updown)。所有分类使用公众可得到的软件包在R中运行,并且交叉验证参数在本地编辑(即,30-倍弃一(leave-one-out)交叉验证)。性能评估和模型选择对于每一个目标分类任务(例如,IPF对正常;IPF对NSIP),使用弃一(LOO)交叉验证策略在训练数据上对性能进行评估。这种性能数据用于生成用于回顾的ROC曲线。为了确保性能估计的有效性,与模型构建有关的所有组件(包括特征选择和分类器训练)均包含在交叉验证程序的内部循环中。对整个训练系列进行交叉验证。使用这种方法进行性能评估,分类的比较结果选出了具有如上所述通过limma选出的30个(IPF对NSIP)或50个(IPF对NML)转录本集群的线性SVM。然后,这些所选分类器的每一个在一系列外植体正常、IPF和NSIP样品上进行测试,导致与在LOOCV训练中所见的相似的性能。表6列出了在开发ILD分类器期间使用的软件。实施例3-在诊断IPF和其他肺病中有用的生物标记物用于开发临床和商业可用分类器的机器学习方法是本领域已知的。然而,使用独立样品队列对这些分类进行训练和后续验证可能具有挑战性。在本实施例中,描述了差异性表达的生物标记物,其显示可以在交叉验证期间精确地预测VATS肺组织活检的IPF状态(图28),而与所检验的比较子组无关。图28.高AUC证明ILD分类器的高准确度。使用弃一患者(leave-one-patient-out)(LOPO)或10倍交叉验证对每一个不同的分类器进行训练和评估。每一个分析中受试者工作特征(ROC)的曲线下面积(AUC)超过0.96,而与所用的方法无关,这指示在商业应用中可以预期高准确度的结果。图7提供了通过微阵列研究的VATS肺组织样品队列。样品根据使用专家标签的病理分类加以列出。样品是通过视频辅助胸腔镜手术(VATS)或支气管镜获得的。表7病理标签病理简写样品总数毛细支气管炎BRONCH1未分类的慢性间质性纤维化CIF-NOC8超敏感性肺炎HP16特发性肺纤维化IPF46其它OTHER6非特异性间质性肺炎NSIP26机化性肺炎OP2呼吸性细支气管炎RB4结节病SARC2吸烟相关的间质纤维化SRIF1总计112这些分类器使用IPF训练标签开发,这些训练标签只有在IPF诊断中有至少两个病理学家表示同意时才产生(2Path)。将2Path分类器应用于具有单个病理学家训练标签的独立样品队列(1Path),并且显示尽管有可能对这些样品的一部分进行分类,但是大部分被错误分类(图29)。图29.分类器比较。使用具有两个病理学家一致标签的样品训练的分类器(2Path,图A)优于使用来自单个病理学家的标签(1Path)或两个样品队列的组合训练的分类器(图B)。分类器得分在1Path或组合的分类器中分布更广(图C)。而且,当组合两个队列(2Path和1Path)时,所得分类器的准确度降低,判定边界更难以确定。这些数据强调了在分类器训练期间获得MDT(多学科团队;一组医学专家)金标准标签的重要性。可以解释所观察数据的一种假说是,在开发本发明中发现的生物标记物如此灵敏,以致于对于病理学家而言还没有显示IPF迹象的样品已经显示出了疾病的分子标识(图30)。图30.IPF表达信号假说。可以解释在尚未显示严重IPF大体病理的样品中能够检测到强IPF分子标识的观察数据的假说的图形表示。尽管假阳性结果在分类器开发期间并不少见,但是观察到的数据表明,可检测的信号先于IPF疾病的爆发(full-blown)。开发在这里发现的分子标识以训练其它的分类器,旨在不仅评估肺VATS组织活检,而且评估支气管活检(TBB)、支气管肺泡灌洗(BAL)和冷冻活检(cryobiopsy)样品。这些样品类型(VATS,TBB,BAL或冷冻活检)样品中的每一个具有不同的细胞隔室,并且可以预期在单一患者体内,这些样品中的每一个会产生其自身的疾病标识,它一般与其它样品类型仅有部分重叠。新的分类器使用VATS和TBB,或VATS和BAL,TBB和BAL,TBB和冷冻活检,VATS和冷冻活检的组合,或者仅单一样品类型(或者1、2、3或4个任意组合),以便获得特异性>95%、PPV>95%且灵敏度>70%的分类的分子标识。还包括其它分类器,其利用来自同一患者的样品的进一步的组合,包括但不仅限于血浆、血清、唾液和痰。而且,虽然使用来自同一患者的VATS、TBB、BAL、血清、血浆、唾液和/或痰的组合可以对最佳分类器进行训练,但是该方法也可使用来自不同患者的这些样品类型的任意组合(例如,VATS来自患者1,血清来自患者2,唾液来自患者3等)开发分类器。此外,此外,该方法可以用于开发分类器,其中对来自单个患者的2个或更多个样品类型同时进行评估,以便准确检测、预测或诊断疾病(例如,BAL和唾液来自患者1,或者VATS和TBB来自患者1,或者TBB和血浆来自患者1,或者它们的任意组合)。这些方法还可用于疾病严重程度的预后,并且在用药、呼吸康复训练、或其他治疗之前、期间或之后对治疗响应进行评估。例如,这些方法可用于鉴定作为特定药物靶治疗的候选者的患者,或者排除那些不适合用特定药物靶治疗的患者。这些方法已经为所有主要的ILD亚型鉴定了了分子标识(表27),并且这些方法可能对于每种特定的亚型应用较窄并且较难,或者对于亚型的组合或组群更加广泛。例如,炎症是HP、NSIP、结节病和机化性肺炎(OP)的标志,并且作为一组(ILD炎症),这些亚型可以和IPF准确区分(图28,表8,并在下文列出);并且IPF可以和这些亚型区分,并且与ILD炎症单独分类。尽管这些方法旨在分类ILD疾病并可用于鉴定特定的ILD亚型,但是预期在临床环境中以高准确度、灵敏度、特异性和重复性执行的分类器训练确实需要利用略微处于ILD疾病谱之外的样品。例如,分类器训练可以包括来自患有COPD、肺动脉高压、结缔组织病、肺结节等的患者的样品,因为这些症状可以模拟ILD,并且重要的是能够训练可以区分ILD和这些其它病症的分类器。在本发明中鉴定的分子标识指示了参与肌肉生理学并作为IPF重要生物标记物的基因。肌肉基因在IPF中被上调,而在其它ILD亚型中则没有,类似地,炎症基因在IPF中被下调,而在HP、NSIP、OP和结节病中被大大上调。尽管这些方法不受基因本体、分子功能或特异通路的限制,但是也应当理解,肌肉和炎症分类中的任何生物标记物均可以使用。IPF对NSIP生物标记物图31描述了使用9个基因标识的IPF对NSIP的分类错误率。在弃一患者(LOPO)交叉验证期间,三种不同的分类器(KNN,SVMlinear,和SVMradial)显示相似的性能,低于10%的整体分类。图32描述了使用15个基因标识的IPF对NSIP的分类错误率。在10倍交叉验证期间,三种不同的分类器(KNN,SVMlinear,和SVMradial)显示相似的性能,低于10%的整体分类。表8提供了在IPF对NSIP分类中使用的示例生物标记物。如表8中“x”所指示的,一些生物标记物可用于使用任意数目的分类方法和弃一患者(LOPO)交叉验证,和/或10倍交叉验证(10倍),和/或任何其它分类和交叉验证方法(任意)进行分类。表8TCID标识符任意LOPO10倍8101031CDKL2XXX8037205CEACAM1XX8127234DSTXXX8112980EDIL3XXX8179019HLA-FXXX8177717HLA-FXXX8117760HLA-FXXX7947248KIF18AXX7923386LMOD1XX7956856MSRB3XXX7999674MYH11XX8090098MYLKXX7934997PPP1R3CXX8126853PTCHD4XX8109639PTTG1XX8172022TMEM47XX7917199TTLL7XX下面列出了一系列250个差异表达(过表达;低表达)的生物标记物,其满足分析标准,指示用于使用微阵列数据的IPF对NSIP分类中。在IPF中过表达的基因(n=101)的Log2倍数变化范围是0.22至1.37。在IPF中低表达的基因(n=149)的Log2倍数变化范围是-2.20至-0.20。本分析中全部250个基因的FDRp-值范围是2.21E-11至2.46E-06。如果HUGO基因符号不可得,则给出Affymetrix转录本集群鉴定子(TCID)来详明基因。过表达:ACTA2,ACTG2,AHNAK,AHNAK2,AKT3,ANO2,AOC3,ARHGEF25,ATP1A2,CALD1,CAMK2N1,CD109,CDH13,CNKSR2,CNN1,COL21A1,COPZ2,COX7A1,CRIM1,CRYAB,CSRP1,DENND2A,DES,DGKG,DIXDC1,DMD,DNAJB4,DPYSL3,DST,DTNA,EDIL3,EOGT,EPB41L2,FGF14,FHL1,FMO2,FMO3,GARNL3,HOXA-AS2,HOXA4,HOXA6,HPSE2,LAMA4,LARP6,LHFP,LMCD1,LMOD1,LRRFIP1,MAP1B,MARK1,MCAM,MFAP4,MPDZ,MSRB3,MXRA7,MYH10,MYH11,MYL9,MYLK,MYOCD,NEXN,PALLD,PCDHB10,PCDHGC5,PDE1C,PDE5A,PDLIM3,PEAK1,PGM5,PGM5P2,PHLDB2,PKD2,PKIG,PLCB4,PLCE1,PLN,PPP1R3C,PREX2,PRKAA2,PRKAB2,PRKG1,PRUNE2,PTCHD4,PTPRB,REEP1,RERG,SBF2,SORBS1,SYNM,SYNPO2,TAGLN,TIMP2,TIMP3,TMEM47,TMOD1,TPM1,TPM2,TRPC1,TTLL7,UACA,ZC3H12B。低表达:ABCA3,ACADSB,ACOXL,ADAR,APOL6,ARHGEF38,ARPC5L,ASPM,ATP11A,ATP2C2,ATP8A1,BUB1,C18orf8,C2,CASC5,CCL4,CCL4L1,CCNA2,CCNB1,CCNB2,CCR5,CD38,CDC45,CDK1,CDKL2,CEACAM1,CFTR,CISH,CLINT1,CNDP2,CRTAC1,CSF3R,CXCL10,CXCL11,CXCL9,CXCR6,DGKD,DLGAP5,DRAM1,DUSP16,EDEM1,EFNA1,EPSTI1,ESRP2,ETV7,EZH2,FHDC1,FOXM1,FZD5,GALNT3,GBP1,GBP5,GPR98,GRAMD1A,GUCD1,HAS3,HERC6,HIST1H2BI,HIST1H2BM,HIST1H3E,HIST1H3J,HLA-A,HLA-B,HLA-C,HLA-DOA,HLA-F,HLA-H,HMMR,IFI35,IRF1,IRF9,KCNJ15,KCNQ3,KCTD14,KIF11,KIF14,KIF18A,KIF4A,LARP4B,LGALS3BP,LNX2,MAP3K13,MAPK13,MARK2,METTL7B,MKI67,MTUS1,NPC1,NUSAP1,OAS2,ORM1,ORM2,PARP14,PARP9,PLAGL2,PRKCQ,PSMB10,PSMB8,PSMB9,PSME1,PSME2,PTTG1,PXMP4,RABGAP1L,RAD51AP1,RAP1GAP,RBM47,RCOR1,RFX5,RGS16,RNF145,RNF213,SCTR,SDC4,SDR16C5,SEMA4A,SFTPD,SLC16A13,SLC22A3,SMC4,SNX30,SQSTM1,SREBF2,STAT1,STIL,TAPI,TAPBP,TCID-7896714,TCF19,TKT,TLR2,TMED6,TMEM164,TMEM41B,TOP1,TOP2A,TOX,TRAFD1,TRIM26,TYMP,UBD,UBE2S,USP44,VDR,WARS,WWC1,YARS,ZDHHC16,ZNF385B。IPF对其余/非IPF生物标记物图33A-B提供了可用于IPF对其余/非IPF分类的生物标记物。如表中x所示,一些生物标记物可用于使用任意数目的分类方法和弃一患者(LOPO)交叉验证,和/或10倍交叉验证(10倍),和/或任何其它分类和交叉验证方法(任意)进行分类。下面列出了一系列500个差异表达(过表达;低表达)的生物标记物,其在使用微阵列数据的IPF对其余/非IPF分类中具有令人满意的分析标准。在IPF中过表达的基因(n=202)的Log2倍数变化范围是0.17至1.41。在IPF中低表达的基因(n=298)的Log2倍数变化范围是-2.08至-0.15。本分析中全部500个基因的FDRp-值范围是1.47E-12至9.87E-06。如果HUGO基因符号不可得,则给出Affymetrix转录本集群鉴定子(TCID)来详明基因。过表达:ABCA6,ABLIM3,ACTA2,ACTG2,ADCY5,AHNAK2,AKAP12,ANO1,ANO2,ARHGEF25,ATP1A2,ATP1B2,BAG2,BHMT2,BMX,C16orf45,C3orf55,C3orf70,CACNA1C,CACNB2,CALD1,CAMK2N1,CCDC3,CDH6,CDR1,CLIP3,CLU,CNN1,COCH,COL21A1,COPZ2,COX7A1,CRYAB,CSRP1,CTTNBP2,DACT1,DDR2,DENND2A,DES,DIXDC1,DMD,DST,DTNA,DYNC1I1,DZIP1,EBF1,EDIL3,EFHD1,F10,FAM124B,FAM13C,FBLIM1,FEZ1,FGF10,FGF14,FGF2,FGFR1,FHL1,FHL2,FLNC,GADL1,GARNL3,GAS7,GNG12,GRIA3,GRIN2A,HOXA2,HOXA6,HOXA7,HPSE2,HRC,HRH1,HSPA2,HSPB6,HSPB7,IGFBP5,ITGB4,ITIH5,KALRN,LAMA4,LAMC1,LARP6,LDB3,LGI4,LMOD1,LPP,LTBP1,MAP1B,MAP7D3,MARK1,MCAM,MEIS1,MEOX2,MPDZ,MRGPRF,MRVI1,MSRB3,MUSTN1,MXRA7,MYH11,MYL9,MYLK,MYOCD,MYOM1,NCAM1,NEXN,NFASC,NPR2,NR2F1,NR2F2,NTRK3,OSR2,PALLD,PALMD,PARVA,PBX1,PCDH7,PCDHB10,PCDHB12,PCDHB13,PCDHB14,PCDHB18,PCDHB3,PCDHB7,PCDHGC5,PDE10A,PDE1A,PDE2A,PDE3A,PDE5A,PDE7B,PDGFRB,PDLIM3,PDZRN4,PEG3,PFKM,PGM5,PGM5P2,PHYHIPL,PKD2,PLA2R1,PLCB4,PLN,PLXNA4,PODN,PPP1R3C,PRKAA2,PRKG1,PRSS23,PRUNE2,PTCHD4,PYGM,RAB9B,RASD2,RBM24,RCAN2,RERG,RGS5,RGS7BP,RYR3,S1PR3,SBSPON,SCRG1,SCUBE1,SEMA3D,SETBP1,SGCA,SLC38A11,SLIT3,SLN,SMIM10,SNED1,SNORD116-17,SNORD116-21,SNX9,SOGA1,SORBS1,SPARCL1,SSPN,SYNM,SYNPO2,SYTL2,TAGLN,TCEAL4,TCEAL6,TIMP2,TMEM252,TMEM47,TMOD1,TPM1,TPM2,TRPC1,TTLL7,WISP2,ZAK,ZC3H12B,ZCCHC24,ZEB2,ZHX3,ZNF135,ZNF154,ZNF521。低表达:ACADL,ACOXL,ACSF2,AHCYL2,ANK3,AP1M2,APOL1,APOL4,APOL6,AQP4,ARAP2,ARHGEF38,ARSD,ASPM,ATP1A1,ATP2C2,ATP8A1,BATF2,BAZ1A,BMP3,BST2,BTG3,BTN3A3,BUB1,C18orf8,C2,CASP1,CASP4,CCL4,CCL4L1,CCL5,CCNA2,CCR5,CD274,CD40,CD47,CD74,CD8A,CDCA7L,CDK1,CDKL2,CEACAM1,CFTR,CKAP2,CLDN4,CLINT1,CNDP2,CNKSR1,CRTAC1,CRTAM,CSF3R,CXCL10,CXCL11,CXCL9,CXCR6,CYB5A,CYP2B6,CYP2B7P1,DAPK1,DBI,DDX60,DENND1B,DHCR24,DNASE2,DOCK8,DRAM1,DTNB,DTX3L,DUSP16,DYNLT1,EDEM1,EFNA1,EML4,ENTPD3,EPSTI1,ERAP1,ERBB3,ESRP1,ESRP2,ETV7,FAM111A,FCGR1A,FCGR1B,FDFT1,FGFR2,FHDC1,FLRT3,FNIP2,FREM2,FZD5,GALNT3,GBP1,GBP4,GBP5,GBP7,GCH1,GCNT2,GK,GNPTAB,GPR98,GRAMD1B,GRHL2,GSAP,GUCD1,GZMB,GZMH,HAS3,HCP5,HIST1H2AI,HIST1H2BI,HIST1H3B,HLA-A,HLA-B,HLA-C,HLA-DMA,HLA-DOA,HLA-DPA1,HLA-DPB1,HLA-DQA2,HLA-DRA,HLA-E,HLA-F,HLA-G,HLA-H,HLA-J,HLA-L,HMGCL,HMGCR,HMMR,HN1,HNF1B,HPS5,ICOS,IDI1,IDO1,IFI27,IFI35,IFIH1,IFIT3,IFIT5,IGSF3,IL10RB,IL32,IL6R,INADL,IRF1,IRF9,ITGAE,ITGAL,JPH1,KCNJ15,KCTD14,KIAA0247,KIAA0319L,KIAA1958,KIF18A,KLF5,L3MBTL4,LAMP3,LAP3,LARP4B,LCP2,LIMD1,LNX2,LPIN2,MAGI3,MAP3K13,MAPK13,MARK2,MB21D1,MBIP,MIA2,MICALCL,MID1IP1,MREG,MRPL14,MTMR14,MTRR,MYL1,MYO5B,N4BP1,NAV2,NEDD4L,NMI,NPC1,NUB1,NUSAP1,OAS2,OCLN,ORM1,PARP12,PARP14,PARP9,PCK2,PCLO,PDZK1IP1,PEBP4,PFKFB3,PHACTR1,PI4K2B,PLA2G12B,PLAGL2,PLCH1,PLS1,PPP1R9A,PPP2R5A,PRKCQ,PRKCZ,PRRG4,PRSS8,PSMB10,PSMB8,PSMB9,PSME1,PSME2,PTP4A1,PTPN1,PTPRJ,PTTG1,PXMP4,RAB20,RAB3IP,RABGAP1L,RANBP17,RARRES3,RBM47,RCOR1,RFC1,RFX5,RGS16,RNF19B,RNF213,S100A14,SAMD9L,SCN1A,SCTR,SDC4,SELENBP1,SEMA4A,SFTPD,SH2D4A,SHANK2,SLAMF8,SLC15A3,SLC16A13,SLC22A3,SLC37A1,SLC04C1,SMARCA5,SMC4,SQLE,SQRDL,SREBF2,ST7,STARD10,STAT1,STX11,STX19,SYT15,TAPI,TAP2,TAPBP,TAPT1,TC2N,TCID-7895602,TCID-7896651,TCID-7896695,TCID-7951593,TCID-8113717,TDRKH,THEMIS,TKT,TLR2,TLR3,TMEM164,TMEM180,TMEM41B,TMEM87A,TMPRSS2,TMPRSS3,TNFAIP3,TOX,TRAFD1,TRIM21,TRIM24,TTLL4,UBALD2,UBD,UBE2L6,USP38,USP44,USP54,WARS,WHSC1,WWC1,ZDHHC16,ZDHHC2,ZNF385B。IPF对HP生物标记物表9提供了可用于IPF对HP分类的生物标记物。如表中x所示,一些生物标记物可用于使用任意数目的分类方法和弃一患者(LOPO)交叉验证,和/或10倍交叉验证(10倍),和/或任何其它分类和交叉验证方法(任意)进行分类。表9TCID标识符任意LOPO10倍8179019HLA-FXXX8177717HLA-FXXX8117760HLA-FXXX8079377CXCR6XX下面列出了一系列250个差异表达(过表达;低表达)的生物标记物,其在使用微阵列数据的IPF对HP分类中具有令人满意的分析标准。在IPF中过表达的基因(n=43)的Log2倍数变化范围是0.23至1.21。在IPF中低表达的基因(n=207)的Log2倍数变化范围是-2.71至-0.21。本分析中全部250个基因的FDRp-值范围是1.62E-13至2.02E-04。如果HUGO基因符号不可得,则给出Affymetrix转录本集群鉴定子(TCID)来详明基因。过表达:ACTA2,ACTG2,ARHGEF25,CACNA1C,CALD1,CNN1,COL21A1,DST,EDIL3,GPC6,HERC2P2,HSPA2,KALRN,LINC00328,LMOD1,MAP1B,MEIS1,MEOX2,MYH11,MYLK,MYOCD,NBPF3,NEXN,OSMR,PAPPA,PCDHB18,PDE3A,PLXNA4,PRUNE2,PTCHD4,PTGFRN,SCRG1,SLC25A27,SLIT3,SOGA1,SORBS1,SYNPO2,TAGLN,TCID-7906969,TPM1,TPM2,VCAN,ZNF154。低表达:ADAMDEC1,ANKRD22,APOBEC3C,APOBEC3F,APOBEC3G,APOBEC3H,APOL1,APOL3,APOL4,APOL6,ASCL2,BATF,BATF2,BST2,BTN2A2,BTN3A1,BTN3A2,BTN3A3,C17orf49,CAMK4,CASP1,CASP4,CCL4,CCL4L1,CCL5,CCR5,CD2,CD226,CD244,CD247,CD274,CD3D,CD3E,CD3G,CD40,CD40LG,CD5,CD6,CD72,CD74,CD8A,CD96,CIITA,CLEC6A,CMTM1,COROIA,CRTAM,CST7,CTLA4,CXCL10,CXCL11,CXCL9,CXCR3,CXCR6,DDX60,DNASE2,EBB,EIF4E3,EPSTI1,ETV7,FAM26F,FAM78A,FASLG,FGL2,FYB,GATA3,GBP1,GBP2,GBP3,GBP4,GBP5,GBP7,GCH1,GPR171,GPR174,GPR68,GRAMD1B,GZMA,GZMB,GZMH,HCP5,HCST,HIST1H2BI,HLA-A,HLA-B,HLA-C,HLA-DMA,HLA-DMB,HLA-DOA,HLA-DPA1,HLA-DPB1,HLA-DPB2,HLA-E,HLA-F,HLA-G,HLA-H,HLA-J,HLA-L,ICOS,IDO1,IFI27,IFI27L2,IFI35,IFNG,IL12RB2,IL23A,IL26,IL27RA,IL2RB,IL2RG,IL32,IL6R,IRF1,IRF9,ITGA4,ITGAE,ITGAL,ITGB2,ITGB7,ITK,JAKMIP1,KIAA1324,KIF18A,KLRC2,KLRK1,L3MBTL4,LAP3,LAT,LCK,LCP2,LGALS2,LGR5,MIA2,NAGK,NFATC2,PAQR8,PARP12,PARP14,PARP9,PDCD1LG2,PLA2G12B,PLXNC1,PRKCQ,PSMB10,PSMB8,PSMB9,PSME1,PSME2,PTPN22,PTPRJ,PTTG1,PYCARD,PYHIN1,RABGAP1L,RARRES3,RASGRP1,RFX5,RGS10,RNF167,RNF19B,RNF213,RTP4,RUNX3,SAMD9L,SEMA4D,SEPT1,SH2D1A,SH2D2A,SKAP1,SLA2,SLAMF8,SLC35D2,STAT1,STAT4,TAPI,TAP2,TAPBP,TARP,TCID-7896691,TCID-7896701,TCID-7896702,TCID-7896719,TCID-7896720,TCID-7917530,TCID-7948502,TCID-8117739,TCID-8163000,TDRKH,THEMIS,TLR3,TLR8,TNF,TRAFD1,TRAT1,TRAV8-3,TRDV2,TRERF1,TUBA4A,UBASH3A,UBD,UBE2L6,VAMP5,WARS,XCL1,ZAP70,ZNF683,ZNF831。IPF对ILD炎症生物标记物图34A和34B提供了可用于IPF对ILD炎症分类的生物标记物。如图34A和34B中提供的表中x所示,一些生物标记物可用于使用任意数目的分类方法和弃一患者(LOPO)交叉验证,和/或10倍交叉验证(10倍),和/或任何其它分类和交叉验证方法(任意)进行分类。下面列出了一系列250个差异表达(过表达;低表达)的生物标记物,其在使用微阵列数据的IPF对ILD炎症分类中具有令人满意的分析标准。在IPF中过表达的基因(n=100)的Log2倍数变化范围是0.20至1.30。在IPF中低表达的基因(n=150)的Log2倍数变化范围是-2.46至-0.18。本分析中全部250个基因的FDRp-值范围是3.48E-18至4.05E-07。如果HUGO基因符号不可得,则给出Affymetrix转录本集群鉴定子(TCID)来详明基因。过表达:ABCA6,ACTA2,ACTG2,ADCY5,AHNAK2,ANKRD20A8P,ANO2,ARHGEF25,ATP1A2,C16orf45,CALD1,CAMK2N1,CNN1,COL21A1,CRYAB,CSRP1,CTTNBP2,DES,DGKG,DIXDC1,DMD,DST,DTNA,DZIP1,EDIL3,FAM124B,FAM13C,FHL1,GARNL3,HPSE2,HSPA2,KALRN,LAMA4,LAMC1,LDB3,LMOD1,LPP,MAP1B,MAP7D3,MARK1,MCAM,MEIS1,MPDZ,MRVI1,MSRB3,MUSTN1,MXRA7,MYH10,MYH11,MYL9,MYLK,MYOCD,MYOM1,NEXN,NFASC,NTRK3,PALLD,PBX1,PCDHB10,PCDHB13,PCDHGC5,PDE1C,PDE5A,PDLIM3,PGM5,PGM5P2,PKD2,PLA2R1,PLCB4,PLN,PPP1R3C,PREX2,PRKAA2,PRKG1,PRUNE2,PTCHD4,PWAR5,RAB9B,SBSPON,SCRG1,SNORD116-21,SORBS1,STON1-GTF2A1L,SYNM,SYNPO2,SYTL4,TAGLN,TCEAL4,TCEAL6,TCID-7919139,TIMP2,TIMP3,TMEM47,TMOD1,TPM1,TPM2,TRPC1,TTLL7,ZC3H12B,ZNF154。低表达:ACSF2,ANKRD22,AP1M2,APOBEC3F,APOBEC3G,APOL1,APOL4,APOL6,ARHGEF38,ASPM,ATP2C2,ATP8A1,BATF2,BST2,BTN3A3,BUB1,C18orf8,C2,CCL4,CCL4L1,CCL5,CCR5,CD2,CD274,CD38,CD74,CD8A,CDK1,CDKL2,CEACAM1,CFTR,CKS2,CNDP2,CRTAM,CTLA4,CXCL10,CXCL11,CXCL9,CXCR6,DDX60,DRAM1,DUSP16,EFNA1,EPSTI1,ESRP2,ETV7,FAM26F,FHDC1,FPR3,FZD5,GBP1,GBP4,GBP5,GCH1,GPR98,GRAMD1A,GUCD1,GZMB,GZMH,HAS3,HCP5,HIST1H2AI,HIST1H2BH,HIST1H2BI,HIST1H3B,HIST1H3J,HLA-A,HLA-B,HLA-C,HLA-DMA,HLA-DOA,HLA-DPB1,HLA-E,HLA-F,HLA-G,HLA-H,HLA-J,HLA-L,HN1,IFI35,IFIH1,IFNG,IL32,IL6R,IRF1,IRF9,ITGAE,ITGAL,KCNJ15,KCTD14,KIF18A,LAP3,LARP4B,LCP2,LGALS3BP,MAP3K13,MOV10,MREG,NUSAP1,OAS2,PARP12,PARP14,PARP9,PFKFB3,PRKCQ,PSMB10,PSMB8,PSMB9,PSME1,PSME2,PTPRJ,PTTG1,PXMP4,RABGAP1L,RARRES3,RASGRP1,RBM47,RFX5,RGS16,RNF213,SAMD9L,SCTR,SDC4,SEMA4A,SFTPD,SLAMF8,SLC37A1,SMC4,SQRDL,SREBF2,STAT1,TAPI,TAP2,TAPBP,TCID-7896714,TCID-8107094,THEMIS,TLR2,TLR3,TMEM164,TNFAIP3,TOX,TRAFD1,TRIM59,TYMP,UBD,UBE2L6,USP44,WARS,ZNF385B。表10提供了在使用微阵列数据的ILD亚系列分类中有用的示例生物标记物的总结。表10尽管本发明参考其特定的实施方案进行了描述,但是本领域技术人员应当理解,在不背离本发明精神和范围的前提下可以进行各种改变和等价物替换。此外,可以进行许多修饰以将特定的情况、材料、材料组合物、处理、处理步骤适应于本发明目标、精神和范围。所有这些修饰均意图涵盖在本文所附权利要求的范围内。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1