富含甘油三酯的脂蛋白中的胆固醇的定量方法以及定量试剂与流程
本发明涉及富含甘油三酯的脂蛋白(下文有时称为trl)中的胆固醇(下文表示为“脂蛋白名称”胆固醇或“脂蛋白名称”-c时,意味着“”内记载的脂蛋白中的胆固醇)的定量方法以及定量试剂。
背景技术:
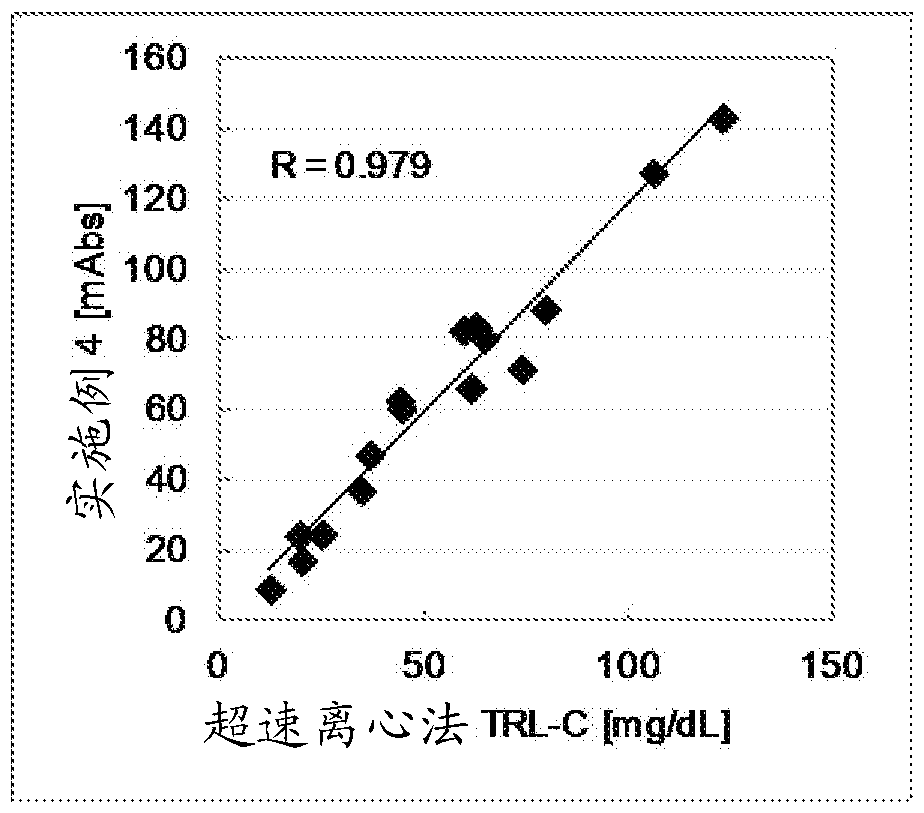
:根据利用超速离心分离的密度的差异,血液中包含的脂蛋白分为乳糜微粒、极低密度脂蛋白(下文有时称为vldl)、中间密度脂蛋白(下文有时称为idl)、低密度脂蛋白(下文有时称为ldl)、高密度脂蛋白(下文有时称为hdl)。已知这些脂蛋白的甘油三酯、胆固醇等脂质、蛋白等的含量不同,各自在体内显示不同的作用。trl是甘油三酯的含量多的脂蛋白的总称,包含乳糜微粒、vldl、它们的中间代谢产物、残粒(レムナント)样脂蛋白(rlp),有时也进一步地包含idl。一直以来已知ldl、rlp与动脉硬化性疾病的相关性,主要在欧美报告了包含idl的trl与动脉硬化性疾病的进展更加深入地相关,其受到关注。迄今为止已知的trl的测定法存在超速离心法、nmr法等。超速离心是通过离心利用脂蛋白的密度差分级的方法,存在需要操作熟练、花费时日、此外费用也变高的缺点。nmr法是通过核磁共振测量脂蛋白的粒子数的方法,需要特殊的机器,不具一般性。trl-c的其它测定方法可举出计算法。由于trl也可称为ldl、hdl以外的脂蛋白,因此从总胆固醇值中减去ldl-c和hdl-c而求得。作为ldl-c的测定法,美国疾病管理中心的β-定量法(β-quantification法,bq法)成为国际基准法,该方法将密度1.006-1.063g/cm3的脂蛋白作为ldl,因此bq法的ldl-c中包含idl-c。因此,在通过计算求得trl-c时,在应用由bq法测定的ldl-c的情况下,idl-c也作为ldl-c被减去。以bq法为基准开发的其它ldl-c测定法、例如应用friedewald公式等的情况也同样。在应用这些ldl-c的测定方法的情况下,算出的trl-c中不含idl-c,称不上测定所谓的临床意义更高的包含idl的trl。因此,需要简便且正确地定量包含idl的trl-c的方法以及试剂的发明。下文在仅仅记载trl、trl-c的情况下,各自意味着包含idl的trl、包含idl-c的trl-c。另外,专利文献1-3报告了作为trl-c的一部分的rlp-c的测定方法。它们都是可通过通用自动分析装置测定的方法,但仅测定rlp,与测定全体trl的本发明不同。现有技术文献专利文献专利文献1:专利4456715号公报专利文献2:专利5027648号公报专利文献3:专利5766426号公报。发明概述发明要解决的课题本发明的目的是,提供不需要繁杂的操作、更特异性地定量被检试样中的trl-c的方法以及试剂。用于解决课题的手段本申请发明人进行深入研究,结果发现,通过在表面活性剂存在下、使分子量超过50kda的胆固醇酯酶作用于包含各种脂蛋白的被检体试样,trl以外的脂蛋白特异性地产生反应。通过利用这一知识,想到可以不进行分离操作、简便且正确地定量trl-c,并完成本发明。也即,本发明如下。[1]trl-c的定量方法,其包含:通过使分子量超过50kda的胆固醇酯酶和表面活性剂产生作用、选择性地消除富含甘油三酯的脂蛋白(trl)以外的脂蛋白中的胆固醇的步骤(1),和特异性地定量残存的trl中的胆固醇(trl-c)的步骤(2)。[2][1]中记载的方法,其中,前述步骤(1)中应用的前述表面活性剂包含选自聚氧乙烯多环苯基醚的至少1种。[3][1]或[2]中记载的方法,其中,在前述步骤(1)中应用的前述表面活性剂是1种的情况下,该表面活性剂是选自hlb值为12-14的聚氧乙烯多环苯基醚的1种,在前述表面活性剂是2种以上的情况下,该表面活性剂包含选自聚氧乙烯多环苯基醚的至少1种,并且以2种以上表面活性剂全体的hlb值成为12-14的方式组合2种以上的表面活性剂。[4][1]-[3]的任一项中记载的方法,其中,前述步骤(2)在表面活性剂存在下进行,该表面活性剂包含选自聚氧乙烯烷基醚、聚氧乙烯月桂醚、月桂醇烷氧基化物(ラウリルアルコールアルコキシレート)、聚氧乙烯多环苯基醚的至少1种。[5][2]-[4]的任一项中记载的方法,其中,前述聚氧乙烯多环苯基醚是选自聚氧乙烯苯乙烯化苯基醚的至少1种。[6][5]中记载的方法,其中,前述聚氧乙烯苯乙烯化苯基醚是选自聚氧乙烯二苯乙烯化苯基醚的至少1种。[7][1]-[6]的任一项中记载的方法,其中,前述步骤(1)包含使胆固醇酯酶与胆固醇氧化酶产生作用、消除生成的过氧化氢,前述步骤(2)包含使胆固醇酯酶与胆固醇氧化酶产生作用、定量生成的过氧化氢。[8]trl-c的定量试剂盒,其为用于1-7的任一项中记载的方法的trl-c的定量试剂盒,其包含用于前述步骤(1)的分子量超过50kda的胆固醇酯酶、和表面活性剂。[9][8]中记载的试剂盒,其中,前述步骤(1)中应用的前述表面活性剂包含选自聚氧乙烯多环苯基醚的至少1种。[10][8]或[9]中记载的试剂盒,其中,在前述步骤(1)中应用的前述表面活性剂是1种的情况下,该表面活性剂是选自hlb值为12-14的聚氧乙烯多环苯基醚的1种,在前述表面活性剂是2种以上的情况下,该表面活性剂包含选自聚氧乙烯多环苯基醚的至少1种,并且以2种以上表面活性剂全体的hlb值成为12-14的方式组合2种以上的表面活性剂。[11][8]-[10]的任一项中记载的试剂盒,其中,前述步骤(2)在表面活性剂存在下进行,前述试剂盒进一步包含选自聚氧乙烯烷基醚、聚氧乙烯月桂醚、月桂醇烷氧基化物、聚氧乙烯多环苯基醚的至少1种的前述表面活性剂。[12][9]-[11]的任一项中记载的试剂盒,其中,前述聚氧乙烯多环苯基醚是选自聚氧乙烯苯乙烯化苯基醚的至少1种。[13][12]中记载的试剂盒,其中,前述聚氧乙烯苯乙烯化苯基醚是选自聚氧乙烯二苯乙烯化苯基醚的至少1种。发明的效果通过本发明,提供了不需要分离操作、能够利用自动分析装置简便且正确地定量被检试样中的trl-c的新方法,以及用于该方法的试剂盒。附图简述[图1]是显示利用下述实施例4中记载的本发明方法的trl-c、与利用超速离心法求得的trl-c的相关关系的图。用于实施发明的方式脂蛋白中包含的胆固醇有酯型胆固醇(胆固醇酯)以及游离型胆固醇。本发明中仅称为“胆固醇”的情况下包含这两者。欲利用本发明的方法定量的trl-c意味着,合并乳糜微粒(包含乳糜微粒残粒)、vldl(包含vldl残粒)和idl的脂蛋白中的胆固醇,也即密度不足1.019g/cm3的脂蛋白中的胆固醇。供给本发明方法的被检试样没有特别限定,只要是欲定量其试样中的trl-c即可,通常是血液(包含全血、血清以及血浆)等的体液、其稀释物。在应用与本发明中的脂蛋白“反应”的表述的情况下,其意味着利用表面活性剂、酶改变脂蛋白的构造,使酶容易作用于内部的胆固醇。对于本发明中的步骤(1),选择性地消除trl以外的脂蛋白中的胆固醇。此处的“消除”意味着分解胆固醇并且其分解物在随后的步骤(2)中检测不到。选择性地消除trl以外的脂蛋白中包含的胆固醇的方法可举出,例如,使胆固醇氧化酶、特定的胆固醇酯酶(后述)作用于被检体试样、除去生成的过氧化氢的方法。除去过氧化氢的方法可举出,使过氧化氢酶产生作用、分解为水和氧的方法,或利用过氧化物酶的作用、将例如与过氧化氢反应生成无色醌的氢供体化合物转化为无色醌的方法等,但不限于这些。此外,“选择性地消除”意味着消除后残存的胆固醇的90%以上、优选地94%以上、进一步优选地97%以上是trl中的胆固醇。消除后残存的胆固醇中的trl中的胆固醇的比例可通过在下述实施例中具体记载的、与依照超速离心法的测定结果的相关关系而测定,在该相关关系是0.9以上的情况下,认为消除后残存的胆固醇中的trl中的胆固醇的比例是90%以上。另外,第1步骤中选择性地消除特定的脂蛋白中的胆固醇的方法在ldl胆固醇的定量方法(例如wo98/47005等)、hdl胆固醇的定量方法(例如wo98/26090等)等中广泛采用,其为公知的。除使用后述特定的胆固醇酯酶以外,本发明的步骤(1)也可通过这些公知的方法实施。接着对于步骤(2),对前述步骤(1)中未消除而残存的trl中的胆固醇进行酶定量。胆固醇的酶定量方法本身是本领域中公知的,例如可举出下列方法:使胆固醇氧化酶和胆固醇酯酶作用于胆固醇,利用过氧化物酶与氢供体和氢受体将生成的过氧化氢转变为醌色素,对该色素进行吸光度测定而定量。这些是广泛应用的公知的方法,上述wo98/47005、wo98/26090中也有记载。另外,在用过氧化氢酶分解步骤(1)中生成的过氧化氢、在步骤(2)中需要抑制该过氧化氢酶的情况下,在步骤(2)中,使用例如叠氮化钠这样的过氧化氢酶抑制剂来抑制过氧化氢酶。本发明具有下列最大特征,在表面活性剂存在下,使用分子量超过50kda的胆固醇酯酶,消除trl以外的脂蛋白中的胆固醇。trl内部大量存在甘油三酯连同酯型胆固醇,小型的分子量小的胆固醇酯酶能够侵入至粒子内部产生作用,但对于大型的分子量大的胆固醇酯酶,甘油三酯成为立体障碍,其无法到达粒子内部的酯型胆固醇,认为可能无法产生作用。胆固醇酯酶以及其亚基的分子量通过常规方法sds-聚丙烯酰胺电泳(sds-page)测定。如公知的,sds-page是还原条件下的电泳,因此在胆固醇酯酶由多数亚基构成的情况下,胆固醇酯酶解离为各亚基,因此测定各亚基的分子量。另一方面,在胆固醇酯酶不具有亚基的情况下,测定胆固醇酯酶的分子量。也即,本发明中规定的胆固醇酯酶的分子量在胆固醇酯酶具有亚基的情况下是该亚基的分子量,在不具有亚基的情况下是胆固醇酯酶的分子量。分子量超过50kda的胆固醇酯酶由旭化成制药公司(旭化成ファーマ社)、kikkoman公司(キッコーマン社)等市售,可用于本发明。另外,分子量为50kda以下的胆固醇酯酶也有各种市售,因此如果本发明中应用市售品,需要选择和应用分子量超过50kda的胆固醇酯酶。对于本发明中的胆固醇酯酶,至少本发明的步骤(1)中包含分子量超过50kda的胆固醇酯酶即可,对于步骤(2),可原样应用步骤(1)中使用的酶,也可追加新的相同胆固醇酯酶,也可追加不同分子量的胆固醇酯酶。本发明的步骤(1)和步骤(2)中包含至少1种表面活性剂。如果应用适当的表面活性剂,可促进各步骤中的酶反应。本发明的步骤(1)中适当的表面活性剂可举出选自聚氧乙烯多环苯基醚的至少1种。聚氧乙烯多环苯基醚中优选聚氧乙烯苯乙烯化苯基醚,进一步更优选聚氧乙烯二苯乙烯化苯基醚,但只要选自聚氧乙烯多环苯基醚,则不限于这些。作为可用于本发明的步骤(1)的表面活性剂的具体例,作为聚氧乙烯多环苯基醚可举出newcol707(ニューコール707)、newcol708、newcol709、adekatolsp-12(アデカトールsp-12)(adeka(アデカ)制造),作为聚氧乙烯苯乙烯化苯基醚可举出blaunondsp-12.5(ブラウノンdsp-12.5)、blaunontsp-16(以上为青木油脂制造)、noigenea-137(ノイゲンea-137)(第一工业制药制造),作为聚氧乙烯二苯乙烯化苯基醚可举出emulgena60(エマルゲンa60)(花王制造)。这些表面活性剂可单独应用,也可组合应用2种以上。优选本发明的步骤(1)中应用的表面活性剂的hlb值为12-14,可为1种表面活性剂且hlb值为12-14,也可组合含有hlb值不是12-14的2种以上表面活性剂、且使表面活性剂全体的hlb值成为12-14。前述表面活性剂的具体例是hlb值为12-14范围内的全部,在组合2种以上的表面活性剂的情况下,可包含表面活性剂的hlb值为12-14的表面活性剂、也可不包含表面活性剂的hlb值为12-14的表面活性剂,能够在本发明的步骤(1)中应用的表面活性剂不限于前述具体例。作为本发明的步骤(2)中适当的表面活性剂,优选对所有脂蛋白产生反应的表面活性剂,例如,可举出选自聚氧乙烯烷基醚、聚氧乙烯月桂醚、月桂醇烷氧基化物、聚氧乙烯多环苯基醚的至少1种。更具体地,可举出emulgen707、emulgen709、emulgen108(以上为花王制造)、adekatollb83、adekatollb103、adekatollb720(以上为adeka制造)、blaunondsp-9(青木油脂制造)、noigenea-87(第一工业制药制造)等。本发明中应用的表面活性剂在反应液中的浓度优选为0.05%-5%,更优选0.1%-1%,进一步优选0.1%-0.75%。另外,在本说明书中,%在没有特别说明的情况下意味着质量%。可在本发明中使用的胆固醇氧化酶是具有氧化胆固醇、生成过氧化氢的能力的酶即可,没有特别限定,例如,可举出来自动物或微生物的胆固醇氧化酶。它们可通过基因操作制备,有无化学修饰均可。对于本发明的步骤(1),可应用磷脂酶,也可不应用磷脂酶,磷脂酶的具体例可举出,磷脂酶c(plc)、鞘磷脂酶(spc)、磷脂酰肌醇特异性磷脂酶c(pi-plc,以上为旭化成制药公司制造)、鞘磷脂酶(来自蜡样芽胞杆菌(bacilluscereus))、鞘磷脂酶(来自金黄色葡萄球菌(staphylococcusaureus))、磷脂酰肌醇特异性磷脂酶c(来自蜡样芽胞杆菌,以上为sigma公司制造)等,但不限于这些。另外,通过应用磷脂酶,在步骤(1)中,可以促进trl以外的脂蛋白中胆固醇的消除。本发明中使用的胆固醇酯酶、胆固醇氧化酶以及磷脂酶等各酶的使用量没有特别限制,可适当设定,通常以0.001u-2000u/ml、优选地0.1-1000u/ml使用。本发明中使用的氢供体优选苯胺衍生物,苯胺衍生物可举出n-乙基-n-(2-羟基-3-磺丙基)-3-甲基苯胺(toos)、n-乙基-n-(2-羟基-3-磺丙基)-3,5-二甲基苯胺(maos)、n-乙基-n-(3-磺丙基)-3-甲基苯胺(tops)、n-(2-羟基-3-磺丙基)-3,5-二甲氧基苯胺(hdaos)、n-(3-磺丙基)苯胺(halps)、n-(3-磺丙基)-3-甲氧基-5-苯胺(hmmps)等。氢受体可应用4-氨基安替比林(4-アミノアンチピリン)、甲基苯并噻唑酮腙(メチルベンゾチアゾロンヒドラゾン)等。本发明中的各步骤优选地在ph5-ph10进行,进一步优选地在ph6-ph8进行。对于反应温度,各步骤均优选在2℃-45℃进行,进一步优选在25℃-40℃进行。对于反应时间,各步骤均优选进行1-10分钟,进一步优选进行3-7分钟。实施本发明的定量方法时,可将使用的试剂分为众多试剂组合物。在本发明中,试剂可配制为两种试剂组合物,例如:用于进行消除trl以外的脂蛋白中的胆固醇的步骤(也即步骤(1))的试剂组合物、与用于进行测定trl中的胆固醇的步骤(也即步骤(2))的试剂组合物。用于进行步骤(1)的试剂组合物中至少包含分子量超过50kda的胆固醇酯酶和上述表面活性剂。该试剂组合物中可进一步包含胆固醇氧化酶、苯胺衍生物等氢供体、消除过氧化氢的过氧化氢酶等。用于进行步骤(2)的试剂组合物中至少包含上述表面活性剂。该试剂组合物中可进一步包含4-氨基安替比林等氢受体、过氧化物酶等。在用于进行步骤(1)的试剂组合物以及用于进行步骤(2)的试剂组合物中,按需要可添加1价阳离子(例如一价金属离子)、2价阳离子(例如二价金属离子)或它们的盐、聚阴离子(例如肝素、葡聚糖硫酸盐、磷钨酸盐)、血清白蛋白。此外,各试剂组合物的ph为中性附近,例如ph5-ph9,优选地ph6-8,添加缓冲液调整ph即可。在通过本发明的方法定量trl中的胆固醇中,通过向被检体试样添加用于进行步骤(1)的试剂组合物并使其反应、随后添加用于进行步骤(2)的试剂组合物并使其反应、测定吸光度而实施即可。下文,基于实施例具体地对本发明进行说明,但本发明不限于下述实施例。实施例实施例1如下述配制用于进行步骤(1)的试剂组合物a(实施例2以后也将用于进行步骤(1)的试剂组合物称为“试剂组合物a”)、用于进行步骤(2)的试剂组合物b(实施例2以后也将用于进行步骤(2)的试剂组合物称为“试剂组合物b”)。试剂组合物apipes缓冲液,ph6.8 50mmol/l各种胆固醇酯酶(参照表1) 3u/ml胆固醇氧化酶 3u/ml过氧化氢酶 1200u/mltoos 2.0mmol/l聚氧乙烯二苯乙烯化苯基醚[hlb:12.8] 0.25%(w/v)试剂组合物bpipes缓冲液,ph6.8 50mmol/l4-氨基安替比林 4.0mmol/l过氧化物酶 20单位/ml叠氮化钠 0.05%(w/v)聚氧乙烯烷基醚 0.5%(w/v)在3μl血清试样中加入150μl试剂组合物a,在37℃反应5分钟后,加入50μl试剂组合物b使其反应5分钟,测定主波长600nm、副波长700nm下的吸光度。与通过作为比较对象法的超速离心法测定的trl-c浓度进行比较,得到的相关系数在表1中示出。表1胆固醇酯酶的分子量相关系数62kda0.96854kda0.96829.5kda0.595(胆固醇酯酶都是市售品)如表1所示,在步骤(1)中应用超过50kda的胆固醇酯酶的情况下,显示与超速离心法良好的相关性。实施例2如下述配制试剂组合物a和试剂组合物b。试剂组合物apipes缓冲液,ph6.8 50mmol/l胆固醇酯酶[62kda] 3u/ml胆固醇氧化酶 3u/ml过氧化氢酶 1200u/mltoos 2.0mmol/l各种表面活性剂(参照表2)※ 0.25%(w/v)※在组合2种以上的情况下,合计0.25%(w/v)试剂组合物bpipes缓冲液,ph6.8 50mmol/l4-氨基安替比林 4.0mmol/l过氧化物酶 20单位/ml叠氮化钠 0.05%(w/v)聚氧乙烯烷基醚 0.5%(w/v)在3μl血清试样中加入150μl试剂组合物a,在37℃反应5分钟后,加入50μl试剂组合物b使其反应5分钟,测定主波长600nm、副波长700nm下的吸光度。与通过作为比较对象法的超速离心法测定的trl-c浓度进行比较,得到的相关系数在表2中示出。表2如表2所示,在步骤(1)中应用选自hlb值为12-14的聚氧乙烯多环苯基醚的表面活性剂的情况下,显示与超速离心法的良好相关性。此外,即使是选自单独情况下得不到良好相关性的、hlb值不是12-14的聚氧乙烯多环苯基醚的表面活性剂,在以全体的hlb值成为12-14的方式组合的情况下,也显示与超速离心法良好的相关性。实施例3如下述配制试剂组合物a和试剂组合物b。试剂组合物apipes缓冲液,ph6.8 50mmol/l胆固醇酯酶[62kda] 3u/ml胆固醇氧化酶 3u/ml过氧化氢酶 1200u/mltoos 2.0mmol/l聚氧乙烯多环苯基醚[hlb:12.8] 各种浓度(参照表3)试剂组合物bpipes缓冲液,ph6.8 50mmol/l4-氨基安替比林 4.0mmol/l过氧化物酶 20单位/ml叠氮化钠 0.05w/v%聚氧乙烯烷基醚 0.5w/v%在3μl血清试样中加入150μl试剂组合物a,在37℃反应5分钟后,加入50μl试剂组合物b使其反应5分钟,测定主波长600nm、副波长700nm下的吸光度。与通过作为比较对象法的超速离心法测定的trl-c浓度进行比较,得到的相关系数在表3中示出。表3如表3所示,在步骤(1)中应用选自0.1-1.0w/v%的聚氧乙烯多环苯基醚的表面活性剂的情况下,显示与超速离心法良好的相关性。进一步,该表面活性剂的浓度为0.1-0.75w/v%显示与超速离心法更好的相关性。实施例4如下配制试剂组合物a和试剂组合物b。试剂组合物apipes缓冲液,ph6.8 50mmol/l胆固醇酯酶[62kda] 3u/ml胆固醇氧化酶 3u/ml过氧化氢酶 1200u/mltoos 2.0mmol/l聚氧乙烯二苯乙烯化苯基醚[hlb:12.8] 0.4%(w/v)试剂组合物bpipes缓冲液,ph6.8 50mmol/l4-氨基安替比林 4.0mmol/l过氧化物酶 20单位/ml叠氮化钠 0.05%(w/v)聚氧乙烯烷基醚 0.5%(w/v)在3μl血清试样中加入150μl试剂组合物a,在37℃反应5分钟后,加入50μl试剂组合物b使其反应5分钟,测定主波长600nm、副波长700nm下的吸光度。与通过作为比较对象法的超速离心法测定的trl-c浓度进行比较,得到的相关图在图1中示出。如图1所示,本发明中测定的trl-c显示与超速离心法良好的相关性。实施例5如下配制试剂组合物a和试剂组合物b。试剂组合物apipes缓冲液,ph6.8 50mmol/l胆固醇酯酶[62kda] 3u/ml胆固醇氧化酶 3u/ml过氧化氢酶 1200u/mltoos 2.0mmol/l聚氧乙烯二苯乙烯化苯基醚[hlb:12.8] 0.25%(w/v)试剂组合物bpipes缓冲液,ph6.8 50mmol/l4-氨基安替比林 4.0mmol/l过氧化物酶 20单位/ml叠氮化钠 0.05%(w/v)各种表面活性剂(参照表4) 各种浓度(参照表4)在3μl血清试样中加入150μl试剂组合物a,在37℃反应5分钟后,加入50μl试剂组合物b使其反应5分钟,测定主波长600nm、副波长700nm下的吸光度。与通过作为比较对象法的超速离心法测定的trl-c浓度进行比较,得到的相关系数在表4中示出。表4如表4所示,在步骤(2)中应用选自聚氧乙烯烷基醚、聚氧乙烯月桂醚、月桂醇烷氧基化物的表面活性剂的情况下,显示与超速离心法良好的相关性。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1