CD38蛋白抗体及其应用的制作方法
本申请涉及生物医药领域,具体涉及一种能与cd38蛋白结合的抗体。
背景技术:
cd38蛋白是可以催化nad+转化为环状adp核糖(cadpr,cyclicadp-ribose)并将cadpr水解成adp核糖的双功能外切酶。通常情况下,cd38由造血细胞和实体组织表达。大多数髓质胸腺细胞为cd38+,静止和循环的t和b细胞为cd38-,活化的细胞为cd38+。cd38蛋白是恶性浆细胞上表达的抗原之一,在各种恶性血液病细胞中表达,包括但不限于多发性骨髓瘤细胞,b细胞慢性淋巴细胞白血病细胞,b细胞急性淋巴细胞性白血病细胞。从功能上来看,cd38蛋白参与受体介导,作用于粘附,信号传递以及外部(ecto-)酶活等活动。cd38具有多种环化酶活性作用,它能够催化细胞代谢的中间产物nad+转化成第二信使环化二磷酸腺苷核糖(cadpr),后者可激活理阿诺碱受体(ryanodinereceptors,ryrs),而促进ca2+释放。同时,cd38蛋白分子还具有脱氢酶活性,催化cadpr生成二磷酸腺苷核糖(adpr)。除通过ca2+传递信号外,cd38蛋白还可通过与t和b细胞的抗体-受体复合物或其他类型的受体复合物,例如mhc分子,进行信号交叉传递。通过这种方式,cd38蛋白参与了多种细胞反应以及免疫球蛋白g1(immunoglobuling1,igg1)的转化与分泌。
然而,目前已研发的cd38抗体识别活性有限,细胞毒性活性有限,且对肿瘤的抑制能力有限,因此亟待开发新的cd38抗体以用于新药研发。
技术实现要素:
本申请提供了一种cd38抗体及其应用。本申请提供的cd38抗体具有下列性质中的一种或多种:1)能够以较高的亲和力和特异性结合cd38蛋白;2)能够通过抗体依赖的细胞介导的细胞毒性adcc、补体依赖的细胞毒性cdc和/或细胞凋亡杀死cd38+细胞;3)能够杀伤肿瘤细胞和/或抑制肿瘤生长;4)能够用于预防或治疗肿瘤;5)能够抑制cd38蛋白与cd38配体结合。本申请还提供所述cd38抗体的制备方法和应用。
一方面,本申请提供了一种抗体、其抗原结合片段或变体,其以1×10-9m或更低的kd与cd38蛋白相结合。
在某些实施方式中,本申请的抗体、其抗原结合片段或变体能够通过与cd38蛋白特异性结合而杀伤肿瘤细胞和/或抑制肿瘤生长。
在某些实施方式中,本申请的抗体、其抗原结合片段或变体能够通过抗体依赖的细胞介导的细胞毒性adcc、补体依赖的细胞毒性cdc和/或细胞凋亡杀死cd38+细胞。
在某些实施方式中,本申请的抗体、其抗原结合片段或变体不结合或基本上不结合bsa、cd19、trop2、cd47、axl或gas6等不相关抗原。
在某些实施方式中,所述肿瘤包括cd38阳性的肿瘤。在某些实施方式中,所述cd38阳性的肿瘤选自以下组:多发性骨髓瘤、淋巴瘤和白血病。
在某些实施方式中,所述肿瘤选自以下组:非霍奇金淋巴瘤和霍奇金淋巴瘤。
在某些实施方式中,所述肿瘤的细胞包括选自下组的细胞:raji细胞、daudi细胞、ramos细胞和rpmi8226细胞。
在某些实施方式中,当所述的抗体、其抗原结合片段或变体与cd38蛋白结合时,其结合所述cd38蛋白第220位至第241位氨基酸残基中的一个或多个残基(cd38蛋白第220位至第241位的氨基酸序列如seqidno:15所示)。
在某些实施方式中,所述抗体选自下组:单克隆抗体、单链抗体、嵌合抗体、人源化抗体和全人源抗体。
在某些实施方式中,所述抗原结合片段选自下组:fab,fab’,f(ab)2和fv片段。
在某些实施方式中,所述变体选自下组:1)在所述抗体或所述其抗原结合片段中经过取代、缺失或添加一个或多个氨基酸的蛋白质或多肽;和2)与所述抗体或所述其抗原结合片段具有至少90%序列同源性的蛋白质或多肽。
在某些实施方式中,所述cd38蛋白为人cd38蛋白或猴cd38蛋白。例如,所述cd38蛋白可以不为小鼠cd38蛋白,或者可以不为大鼠cd38蛋白。
在某些实施方式中,本申请的抗体、其抗原结合片段或变体,其与参比抗体竞争结合所述cd38蛋白,其中所述参比抗体包含轻链可变区和重链可变区,所述参比抗体的轻链可变区包含lcdr1-3,所述lcdr1-3的氨基酸序列依次为seqidno:1、seqidno:2和seqidno:3,所述参比抗体的重链可变区包含hcdr1-3,所述hcdr1-3的氨基酸序列依次为seqidno:4、seqidno:5和seqidno:6。
在某些实施方式中,所述参比抗体的轻链可变区的氨基酸序列为:seqidno:7,且所述参比抗体的重链可变区的氨基酸序列为:seqidno:8。
在某些实施方式中,所述参比抗体的轻链包含如seqidno:11、所示的氨基酸序列;且所述参比抗体的重链包含如seqidno:13所示的氨基酸序列。
在某些实施方式中,本申请的抗体、其抗原结合片段或变体,其与参比抗体竞争结合所述cd38蛋白,其中所述参比抗体包含轻链和重链,所述参比抗体的轻链包含选自下组的氨基酸序列:seqidno:16、seqidno:18和seqidno:20;且所述参比抗体的重链包含选自下组的氨基酸序列:seqidno:17、seqidno:19和seqidno:21。
在某些实施方式中,本申请所述的抗体、其抗原结合片段或变体,其中所述抗体包含抗体轻链或其片段。在某些实施方式中,所述抗体轻链或其片段包含lcdr1,且所述lcdr1包含选自下组的氨基酸序列:seqidno:1。在某些实施方式中,所述抗体轻链或其片段包含lcdr2,且所述lcdr2包含选自下组的氨基酸序列:seqidno:2。在某些实施方式中,所述抗体轻链或其片段包含lcdr3,且所述lcdr3包含选自下组的氨基酸序列:seqidno:3。在某些实施方式中,所述抗体轻链或其片段包含轻链可变区vl,且所述轻链可变区vl包含选自下组的氨基酸序列:seqidno:7。
在某些实施方式中,所述抗体轻链或其片段还包含人恒定区。在某些实施方式中,所述人恒定区包括人igκ恒定区。
在某些实施方式中,所述抗体轻链或其片段包含选自下组的氨基酸序列:seqidno:11、seqidno:16、seqidno:18和seqidno:20。
在某些实施方式中,所述抗体包含抗体重链或其片段。在某些实施方式中,所述抗体重链或其片段包含hcdr1,且所述hcdr1包含选自下组的氨基酸序列:seqidno:4。在某些实施方式中,所述抗体重链或其片段包含hcdr2,且所述hcdr2包含选自下组的氨基酸序列:seqidno:5。在某些实施方式中,所述抗体重链或其片段包含hcdr3,且所述hcdr3包含选自下组的氨基酸序列:seqidno:6。在某些实施方式中,所述抗体重链或其片段包含重链可变区vh,且所述重链可变区vh包含选自下组的氨基酸序列:seqidno:8。
在某些实施方式中,所述抗体重链或其片段还包含人恒定区。在某些实施方式中,人恒定区包括人igg恒定区。在某些实施方式中,所述igg恒定区包含人igg1恒定区。
在某些实施方式中,所述抗体重链包含选自下组的氨基酸序列:seqidno:13、seqidno:17、seqidno:19和seqidno:21。
另一方面,本申请提供了分离的一种或多种核酸分子,其编码本申请所述的抗体、其抗原结合片段或变体。
在某些实施方式中,所述的核酸分子中的至少一种经密码子优化。
在某些实施方式中,所述的核酸分子包含一个或多个选自下组的核苷酸序列:seqidno:9、seqidno:10、seqidno:12和seqidno:14。
另一方面,本申请提供了载体,其包含本申请所述的核酸分子。
另一方面,本申请提供了宿主细胞,其包含本申请所述的核酸分子或本申请所述的载体。
另一方面,本申请提供了制备所述的抗体、其抗原结合片段或变体的方法。所述方法包括在使得所述抗体、其抗原结合片段或变体表达的条件下,培养本申请所述的宿主细胞。
另一方面,本申请提供了药物组合物,其包含本申请所述的抗体、其抗原结合片段或变体、所述的核酸分子、所述的载体和/或所述的宿主细胞,以及任选地药学上可接受的佐剂。
另一方面,本申请提供了所述的抗体、其抗原结合片段或变体在制备预防或治疗肿瘤的药物中的用途。
在某些实施方式中,所述肿瘤包括cd38阳性的肿瘤。在某些实施方式中,所述cd38阳性的肿瘤选自以下组:多发性骨髓瘤、淋巴瘤和白血病。在某些实施方式中,所述肿瘤选自以下组:非霍奇金淋巴瘤和霍奇金淋巴瘤。
另一方面,本申请提供的所述抗体、其抗原结合片段或变体可用于预防或治疗肿瘤。
在某些实施方式中,所述肿瘤包括cd38阳性的肿瘤。在某些实施方式中,所述cd38阳性的肿瘤选自以下组:多发性骨髓瘤、淋巴瘤和白血病。在某些实施方式中,所述肿瘤选自以下组:非霍奇金淋巴瘤和霍奇金淋巴瘤。
另一方面,本申请提供了预防或治疗肿瘤的方法,所述方法包括向有需要的受试者施用本申请所述的抗体、其抗原结合片段或变体、所述的分子核酸、所述的载体、所述的宿主细胞和/或所述的药物组合物。
在某些实施方式中,所述肿瘤包括cd38阳性的肿瘤。在某些实施方式中,所述cd38阳性的肿瘤选自以下组:多发性骨髓瘤、淋巴瘤和白血病。在某些实施方式中,所述肿瘤选自以下组:非霍奇金淋巴瘤和霍奇金淋巴瘤。
另一方面,本申请提供了抑制cd38蛋白与cd38配体结合的方法,所述方法包括施用本申请所述的抗体、其抗原结合片段或变体、所述的核酸分子、所述的载体和/或所述的宿主细胞。
在某些实施方式中,所述cd38配体包括cd31。
本领域技术人员能够从下文的详细描述中容易地洞察到本公开的其它方面和优势。下文的详细描述中仅显示和描述了本公开的示例性实施方式。如本领域技术人员将认识到的,本公开的内容使得本领域技术人员能够对所公开的具体实施方式进行改动而不脱离本申请所涉及发明的精神和范围。相应地,本申请的附图和说明书中的描述仅仅是示例性的,而非为限制性的。
附图说明
本申请所涉及的发明的具体特征如所附权利要求书所显示。通过参考下文中详细描述的示例性实施方式和附图能够更好地理解本申请所涉及发明的特点和优势。对附图简要说明书如下:
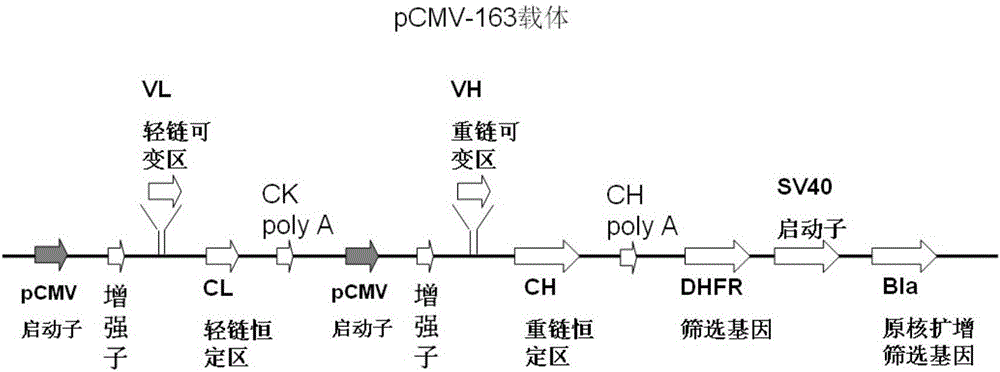
图1显示的是将本申请所述抗体sg003构建全抗体表达载体的物理图谱。
图2显示的是本申请所述抗体sg003与cd38蛋白的结合能力。
图3显示的是本申请所述抗体sg003特异性识别cd38蛋白的结果。
图4a-4d显示的是本申请所述抗体sg003与代表性细胞表面的cd38蛋白结合的能力。
图5a-5d显示的是本申请所述抗体sg003对代表性细胞的adcc活性。
图6显示的是本申请所述抗体sg003对肿瘤生长的抑制效果。
图7显示的是施用本申请所述抗体sg003对小鼠生存率的影响。
图8a-8b显示的是施用本申请所述抗体sg003与不同属来源的cd38分子结合能力。
图9显示的是施用本申请所述抗体sg003进行随机突变后与cd38分子的结合能力。
具体实施方式
以下由特定的具体实施例说明本申请发明的实施方式,熟悉此技术的人士可由本说明书所公开的内容容易地了解本申请发明的其他优点及效果。
在本申请中,术语“抗体”通常是指一种能够特异性识别和/或中和特定抗原的多肽分子。例如,抗体可包含通过二硫键相互连接的至少两条重(h)链和两条轻(l)链组成的免疫球蛋白,并且包括任何包含其抗原结合部分的分子。术语“抗体”包括单克隆抗体、抗体片段或抗体衍生物,包括但不限于人抗体(全人源抗体)、人源化抗体、嵌合抗体、单链抗体(例如,scfv),以及与抗原结合的抗体片段(例如,fab、fab’和(fab)2片段)。术语“抗体”还包括抗体的所有重组体形式,例如在原核细胞中表达的抗体、未糖基化的抗体以及本文所述的任何与抗原结合的抗体片段及其衍生物。每条重链可由重链可变区(vh)和重链恒定区构成。每条轻链可由轻链可变区(vl)和轻链恒定区构成。vh和vl区可进一步被区分为称为互补决定区(cdr)的高变区,它们散布在称为构架区(fr)的更保守的区域中。每个vh和vl可由三个cdr和四个fr区构成,它们从氨基端至羧基端可按以下顺序排列:fr1、cdr1、fr2、cdr2、fr3、cdr3和fr4。重链和轻链的可变区含有与抗原相互作用的结合结构域。抗体的恒定区可介导该免疫球蛋白与宿主组织或因子的结合,所述宿主组织或因子包括免疫系统的多种细胞(例如,效应细胞)和经典补体系统的第一成分(clq)。
在本申请中,术语“抗体结合片段”通常是指抗体中发挥特异性结合抗原功能的一个或多个片段。抗体的抗原结合功能可通过抗体的全长片段来实现。抗体的抗原结合功能也可通过以下来实现:包括fv、scfv、dsfv、fab、fab’或f(ab’)2的片段的重链,或者,包括fv、scfv、dsfv、fab、fab’或f(ab’)2的片段的轻链。(1)fab片段,即由vl、vh、cl和ch结构域组成的一价片段;(2)f(ab’)2片段,包含通过铰链区处的二硫键连接的两个fab片段的二价片段;(3)由vh和ch结构域组成的fd片段;(4)由抗体单臂的vl和vh结构域组成的fv片段;(5)由vh结构域组成的dab片段(ward等,(1989)nature341:544-546);(6)分离的互补决定区(cdr)和(7)可任选地通过接头连接的两个或以上分离的cdr的组合。此外,还可包括由vl和vh配对形成的一价单链分子fv(scfv)(参见bird等(1988)science242:423-426;以及huston等(1988)proc.natl.acad.sci.85:5879-5883)。所述“抗原结合部分”还可包括免疫球蛋白融合蛋白,所述融合蛋白包含选自以下的结合结构域:(1)与免疫球蛋白铰链区多肽融合的结合结构域多肽;(2)与铰链区融合的免疫球蛋白重链ch2恒定区;和(3)与ch2恒定区融合的免疫球蛋白重链ch3恒定区。
在本申请中,术语“cd38蛋白”和“cd38抗原”在本文中可互换使用,并且包括人cd38的任何变体,同种型和物种同系物,其由细胞天然表达或在用cd38基因转染的细胞上表达。本领域公认的cd38蛋白的同义词包括adp核糖基环化酶1,cadpr水解酶1,cd38-rs1,环状adp-核糖水解酶1,i-19,nim-r5抗原。“cd38+细胞”通常是指表达cd38蛋白的细胞。也可称之为cd38阳性细胞。“cd38-细胞”是指不表达cd38蛋白的细胞。cd38由造血细胞和实体组织表达。造血细胞和大多数髓质胸腺细胞是cd38+,静息和循环t和b细胞是cd38-,活化细胞是cd38+。cd38也在约80%的静息nk细胞和单核细胞上以及在淋巴结生发中心淋巴母细胞,血浆b细胞和一些滤泡内细胞上表达。cd38蛋白也可以由树突细胞表达。有显著比例的正常骨髓细胞(特别是前体细胞)的表达cd38蛋白。此外,50-80%的脐带血细胞是cd38+,并且在新生命开始的前两到三年仍然存在于人类血液中。除了淋巴前体细胞之外,cd38蛋白也在红细胞和血小板上表达。
在本申请中,术语“cd31蛋白”通常是指在血小板表面,培养的内皮细胞间连接处和骨髓细胞系中发现的130-140kda大小的跨膜糖蛋白,又称血小板-内皮细胞粘附分子(plateletendothelialcelladhesionmolecule-1,pecam-1/cd31)。cd31是cd38的配体,在血栓形成和血管生成中发挥作用。cd31蛋白通常在血小板,血管内皮细胞,单核细胞和嗜中性粒细胞上表达,此外,骨髓,干细胞和骨髓和巨核细胞谱系的转化细胞系也会表达cd31蛋白。
在本申请中,术语“adcc”是抗体依赖性细胞介导的细胞毒性(antibody-dependentcell-mediatedcytotoxicity,adcc),通常是指是指具有杀伤活性的细胞通过其表面表达的fc受体(fcr)识别包被于靶抗原上的fc段,由此免疫系统的效应细胞主动溶解其膜表面抗原已被特异性抗体结合的靶细胞。
在本申请中,术语“cdc”是补体依赖型细胞毒性(complementdependentcytotoxicity,cdc),通常是指补体参与的细胞毒作用,即通过特异性抗体与细胞膜表面相应抗原结合,形成复合物而激活补体经典途径,所形成的攻膜复合物对靶细胞发挥裂解效应。
在本申请中,术语“淋巴瘤”通常是指一种淋巴系统的恶性肿瘤。淋巴瘤的发生是由于淋巴结细胞或淋巴细胞开始无法控制地繁殖,并产生具有异常能力,可以侵入整个身体其他组织的癌细胞。患者体征和症状可能包括淋巴结肿大,发热,盗汗,消瘦,瘙痒,并持续感到疲倦。淋巴瘤有多种亚型,其中两种主要的类型为霍奇金淋巴瘤和非霍奇金淋巴瘤。在本申请中,术语“霍奇金淋巴瘤”(hodgkin'slymphoma,hl)通常是指一种由淋巴细胞类白细胞产生的一种淋巴瘤。约有一半的霍奇金淋巴瘤病例是由epstein-barr病毒引起的。在本申请中,术语“非霍奇金淋巴瘤”(non-hodgkinlymphoma,nhl)通常是指除了霍奇金淋巴瘤外其他类型的淋巴瘤。
在本申请中,术语“癌症”通常是指或描述哺乳动物的生理状况,其典型特征在于细胞增殖或存活失调。癌症的例子包括但不限于癌,淋巴瘤,母细胞瘤,肉瘤和白血病以及淋巴恶性肿瘤。例如,可以为淋巴瘤。
在本申请中,术语“白血病”通常是指一种造血系统恶性增殖性疾病,通常指因白血病细胞大量增殖、累积所引起的一类疾病。克隆性白血病细胞因为增殖失控、分化障碍、凋亡受阻等机制在骨髓和其他造血组织中大量增殖累积,并浸润其他非造血组织和器官,同时抑制正常造血功能。临床可见不同程度的贫血、出血、感染发热以及肝、脾、淋巴结肿大和骨骼疼痛。
在本申请中,术语“多发性骨髓瘤”(multiplemyeloma,mm)通常是指一种浆细胞不正常增生致使侵犯骨髓的一种恶性肿瘤。多发性骨髓瘤导致癌细胞在骨髓中聚集,使得健康的血细胞被排除。癌细胞产生可导致并发症的异常蛋白质而不是正常的抗体。多发性骨髓瘤的发病率在老年人群中增加,平均诊断年龄约为61岁。其化学治疗方案细胞增殖速率低和药物抗药性强,限制了其化疗效果。超过90%的多发性骨髓瘤患者有化疗抗药性。
在本申请中,术语“raji细胞”通常是指能产生epstein-barr病毒株的连续的人类细胞系。病毒将转化脐带淋巴细胞并且在raji细胞中诱导早期抗原。raji细胞被广泛用作转染宿主,也被用于了解造血细胞和其他细胞恶性肿瘤。此外,因为其具有和表达某些补体成分的几种受体以及免疫球蛋白g的fc受体,因而还被用于检测免疫复合物。
在本申请中,术语“daudi细胞”通常是指来源于burkitt淋巴瘤的细胞系。尽管daudi细胞存在胞内i类重链,但其表面无i类人类白血球抗原(humanleukocyteantigen,hla)分子表达,这是因为其编码β2-微球蛋白(β2m)的基因存在缺陷,导致该蛋白质缺乏可翻译的mrna。
在本申请中,术语“ramos细胞”通常是指一种burkitt淋巴瘤的细胞系。该细胞不带有epstein-barr病毒株,会分泌igm。
在本申请中,术语“rpmi8226细胞”通常是指一种人多发性骨髓瘤的细胞系。
在本申请中,术语“kd”可与“kd”互换使用,通常是指特定的抗体-抗原相互作用的解离平衡常数,单位为m(mol/l)。kd可通过物质ab和其解离得到的物质a和物质b的浓度来计算:kd=c(a)*c(b)/c(ab)。由该公式可知,kd值越大,说明解离越多,代表物质a、b之间的亲和力越弱;反之,kd值越小,说明解离越少,代表物质a、b之间的亲和力越强。
在本申请中,术语“单克隆抗体”通常是指一群基本同源的抗体的抗体,即包含该群的各个抗体除了可能的以微量存在的天然发生的突变之外是相同的。单克隆抗体是高度特异性的,直接针对单个抗原性位点。此外,与包括针对不同决定簇(表位)的不同抗体的多克隆抗体制备物相反,每个单克隆抗体针对抗原上的单一决定簇修饰语"单克隆"不是被解释为需要通过任何特殊方法产生抗体。例如,所述单克隆抗体可以通过杂交瘤技术制备或者通过使用重组dna方法在细菌、真核动物或植物细胞中产生单克隆抗体也可以得自噬菌体抗体文库,使用例如clacksonetal.,nature,352:624-628(1991)和marksetal.,mol.biol.,222:581-597(1991)所述的技术进行。
在本申请中,术语“单链抗体”(scfv)通常是指通常是指是由抗体重链可变区和轻链可变区通过短肽连接子(linker)连接而成的分子。
在本申请中,术语“嵌合抗体”通常是指这样的抗体,其中每个重链或轻链氨基酸序列的一部分与来自特定物种的抗体中相应氨基酸序列同源,或者属于特定的类别,而该链的其余区段则与另一物种中的相应序列同源。例如,轻链和重链的可变区均来自一个动物物种(如小鼠、大鼠等)的抗体的可变区,而恒定部分则与来自另一物种(如人)的抗体序列同源。例如,为获得嵌合抗体,可利用非人源的b细胞或杂交瘤细胞产生可变区,而与其组合的恒定区则来自人。所述可变区具有易于制备的优点,并且其特异性不受与其组合的恒定区的来源的影响。同时,由于嵌合抗体的恒定区可来源于人类,因此嵌合在注射时抗体引发免疫应答的可能性会低于使用恒定区为非人来源的抗体。
在本申请中,术语“人源化抗体”通常是指一种嵌合抗体,其含有较少的来自非人免疫球蛋白的序列,从而降低异种抗体引入到人类中时的免疫原性,同时保持抗体的完全抗原结合亲和力和特异性。例如,可以使用cdr移植(jonesetal.,nature321:522(1986))及其变体;包括“重塑”(reshaping),(verhoeyen,etal.,1988science239:1534-1536;riechmann,etal.,1988nature332:323-337;tempest,etal.,bio/technol19919:266-271),“高度加成”(hyperchimerization),(queen,etal.,1989procnatlacadsciusa86:10029-10033;co,etal.,1991procnatlacadsciusa88:2869-2873;co,etal.,1992jimmunol148:1149-1154)和“贴面”(veneering),(mark,etal.,“derivationoftherapeuticallyactivehumanizedandveneeredanti-cd18antibodies.”in:metcalfbw,daltonbj,eds.cellularadhesion:moleculardefinitiontotherapeuticpotential.newyork:plenumpress,1994:291-312)、表面重建(美国专利us5639641)等技术手段,对非人源的结合域进行人源化。如果其他区域,例如铰链区和恒定区结构域也源自非人来源,则这些区域也可以被人源化。
在本申请中,术语“序列同源性”通常是指同源蛋白质的氨基酸序列具有明显的相似性。
在本申请中,术语“表位”通常是指抗原决定簇,即指分子中被免疫系统识别(例如被抗体识别)的部分。例如,表位是被免疫系统识别的抗原上不连续的三维位点。表位通常由分子的化学活性表面基团(例如氨基酸或糖侧链)组成,并通常具有特定的三维结构特征以及特定的电荷特征。表位根据结构,可分为构象表位和非构象表位(线性表位)。构象表位与非构象表位的区别在于在变性溶剂存在下前者丧失结合,而后者则不会。只位于抗原物质表面、易与抗原识别受体或抗体结合的表位可称为功能性表位;位于分子内部、无免疫原性的表位可称为隐藏性表位。表位可以由连续的残基构成,或者由被抗原聚合物的折叠造成领近的不连续残基形成。在蛋白质中连续氨基酸所形成的表位通常在暴露到变性溶剂时仍被保持,然而不连续氨基酸所形成的表位通常会在所述暴露后丧失。
在本申请中,术语“igg”通常是指免疫球蛋白g(immunoglobuling)。igg是人的免疫球蛋白之一,其他还有lga、lgm、igd和lge。igg是血清主要的抗体成分,约占血清ig的75%。根据igg分子中的γ链抗原性差异,人igg有四个亚型:igg1、igg2、igg3、igg4。igg在免疫中发挥重要的作用。在本申请中,术语“igg1”通常是指igg中占比最高的一类亚型,与fc受体有较高亲和性。
在本申请中,术语“核酸分子”通常是指从其天然环境中分离的或人工合成的任何长度的分离形式的核苷酸、脱氧核糖核苷酸或核糖核苷酸或其类似物。
在本申请中,术语“载体”通常是指能够在合适的宿主中自我复制的核酸分子,其将插入的核酸分子转移到宿主细胞中和/或宿主细胞之间。所述载体可包括主要用于将dna或rna插入细胞中的载体、主要用于复制dna或rna的载体,以及主要用于dna或rna的转录和/或翻译的表达的载体。所述载体还包括具有多种上述功能的载体。所述载体可以是当引入合适的宿主细胞时能够转录并翻译成多肽的多核苷酸。通常,通过培养包含所述载体的合适的宿主细胞,所述载体可以产生期望的表达产物。
在本申请中,术语“宿主细胞”通常是指可以或已经含有包括本申请所述的核酸分子的质粒或载体,或者能够表达本申请所述的抗体或其抗原结合片段的个体细胞,细胞系或细胞培养物。所述宿主细胞可以包括单个宿主细胞的子代。由于天然的,意外的或故意的突变,子代细胞与原始亲本细胞在形态上或在基因组上可能不一定完全相同,但能够表达本申请所述的抗体或其抗原结合片段即可。所述宿主细胞可以通过使用本申请所述的载体体外转染细胞而得到。所述宿主细胞可以是原核细胞(例如大肠杆菌),也可以是真核细胞(例如酵母细胞,例如cos细胞,中国仓鼠卵巢(cho)细胞,hela细胞,hek293细胞,cos-1细胞,ns0细胞或骨髓瘤细胞)。在一些实施方案中,所述宿主细胞是哺乳动物细胞。例如,所述哺乳动物细胞可以是cho-k1细胞。在本申请中,术语“重组宿主细胞”通常指在其中引入了重组表达载体的细胞。所述重组宿主细胞不仅包括某种特定的细胞,还包括这些细胞的后代。
在本申请中,术语“蛋白a”和“proa”在本文中可互换使用,并且包括从其天然来源回收的蛋白a,合成产生的蛋白a(例如通过肽合成或通过重组技术),以及保留蛋白质结合能力的变体其具有ch2/ch3区,如fc区。蛋白质a可以从repligen,pharmacia和fermatech购买。蛋白质a通常固定在固相载体材料上。术语“proa”还指亲和层析树脂或含有与其共价连接的蛋白a的色谱固体支持基质的柱。
在本申请中,术语“约”通常是指在指定数值以上或以下0.5%-10%的范围内变动,例如在指定数值以上或以下0.5%、1%、1.5%、2%、2.5%、3%、3.5%、4%、4.5%、5%、5.5%、6%、6.5%、7%、7.5%、8%、8.5%、9%、9.5%、或10%的范围内变动。
在本申请中,术语“包括”通常是指包含、总括、含有或包涵的含义。在某些情况下,也表示“为”、“由……组成”的含义。
抗体、其抗体结合片段或变体
在一个方面,本申请提供了一种抗体或其抗原结合片段或变体,其以1×10-9m以下(例如,所述kd的值不高于约1×10-9m、不高于约9×10-10m、不高于约8×10-10m、不高于约7×10-10m、不高于约6×10-10m、不高于约5×10-10m、不高于约4×10-10m、不高于约3×10-10m、不高于约2×10-10m、不高于1×10-10m或不高于约1x10-11m或以下)的kd值与cd38蛋白相结合。
本申请所述的抗体、其抗原结合片段或变体,可通过抗体依赖的细胞介导的细胞毒性adcc、补体依赖的细胞毒性cdc和/或细胞凋亡杀死cd38+细胞。
本申请所述的抗体或其抗原结合片段或变体,可通过与cd38蛋白特异性结合而杀伤肿瘤细胞和/或抑制肿瘤生长。例如,所述肿瘤可以包括cd38阳性的肿瘤。如,所述cd38阳性的肿瘤可以选自以下组:多发性骨髓瘤、淋巴瘤和白血病。又例如,所述肿瘤选自以下组:非霍奇金淋巴瘤和霍奇金淋巴瘤。所述肿瘤的细胞可以选自下组:raji细胞、daudi细胞、ramos细胞和rpmi8226细胞。在本申请中,所述抗体、其抗原结合片段或变体可以杀伤多发性骨髓瘤、淋巴瘤、白血病、非霍奇金淋巴瘤和霍奇金淋巴瘤细胞或抑制多发性骨髓瘤、淋巴瘤、白血病、非霍奇金淋巴瘤和霍奇金淋巴瘤生长。
本申请所述的抗体、其抗原结合片段或变体,当与cd38蛋白结合时,其可结合所述cd38蛋白第220位至第241位氨基酸残基中的一个或多个残基。所述cd38蛋白第220位至第241位氨基酸的序列可以如seqidno:15所示。
本申请所述的抗体可选自下组:单克隆抗体、单链抗体、嵌合抗体、人源化抗体和全人源抗体。
本申请所述的抗原结合片段可选自下组:fab,fab’,f(ab)2和fv片段。
本申请所述的变体可选自下组:1)在所述抗体或所述其抗原结合片段中经过取代、缺失或添加一个或多个氨基酸的蛋白质或多肽;和2)与所述抗体或所述其抗原结合片段具有至少约85%(例如,具有至少约85%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或更高的)序列同源性的蛋白质或多肽。
本申请所述的cd38蛋白可为人cd38蛋白或猴cd38蛋白。例如,所述的cd38蛋白可以不为小鼠cd38蛋白,或者可以不为大鼠cd38蛋白。在某些实施方式中,本申请所述的抗体、其抗原结合片段或变体基本上不结合小鼠cd38蛋白或大鼠cd38蛋白。
本申请所述的抗体、其抗原结合片段或变体,可以与参比抗体竞争结合所述cd38蛋白。所述参比抗体可以包含轻链可变区和重链可变区。例如,所述参比抗体的轻链可变区可包含lcdr1-3,所述lcdr1-3的氨基酸序列依次为seqidno:1、seqidno:2和seqidno:3。所述参比抗体的重链可变区可包含hcdr1-3,所述hcdr1-3的氨基酸序列依次为seqidno:4、seqidno:5和seqidno:6。
例如,所述参比抗体的轻链可变区的氨基酸序列可以为:seqidno:7,且所述参比抗体的重链可变区的氨基酸序列可以为:seqidno:8。又例如,所述参比抗体的轻链可包含选自下组的氨基酸序列:seqidno:11、seqidno:16、seqidno:18和seqidno:20;且所述参比抗体的重链可包含选自下组的氨基酸序列:seqidno:13、seqidno:17、seqidno:19和seqidno:21。例如,所述参比抗体的轻链可包含如seqidno:11所示的氨基酸序列,且所述参比抗体的重链可包含如seqidno:13所示的氨基酸序列。例如,所述参比抗体的轻链可包含如seqidno:16所示的氨基酸序列,且所述参比抗体的重链可包含如seqidno:17所示的氨基酸序列。例如,所述参比抗体的轻链可包含如seqidno:18所示的氨基酸序列,且所述参比抗体的重链可包含如seqidno:19所示的氨基酸序列。例如,所述参比抗体的轻链可包含如seqidno:20所示的氨基酸序列,且所述参比抗体的重链可包含如seqidno:21所示的氨基酸序列。
本申请所述的抗体、其抗原结合片段或变体可包含抗体轻链或其片段。例如,所述抗体轻链或其片段可包括igκ恒定区,例如可包含人igκ恒定区。
例如,所述抗体轻链或其片段可包含lcdr1,且所述lcdr1可包含选自下组的氨基酸序列:seqidno:1。所述抗体轻链或其片段可包含lcdr2,且所述lcdr2可包含选自下组的氨基酸序列:seqidno:2。所述抗体轻链或其片段可包含lcdr3,且所述lcdr3可包含选自下组的氨基酸序列:seqidno:3。所述氨基酸序列的变体为与其具有基本上相同的功能(例如,能够特异性结合cd38蛋白),且与其具有至少约85%(例如,具有至少约85%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或更高的)序列同一性的氨基酸序列。在某些实施方式中,所述氨基酸序列的变体为与其具有基本上相同的功能(例如,能够特异性结合cd38蛋白),且在其基础上包含一个或多个(例如,1-2个、1-3个、1-4个、1-5个、1-6个、1-7个、1-8个、1-9个、1-10个或更多个)氨基酸的添加、缺失或置换的氨基酸序列。
本申请所述抗体的轻链或其片段可包含轻链可变区vl,且所述轻链可变区vl可包含选自下组的氨基酸序列:seqidno:7。在某些实施方式中,所述抗体轻链或其片段可包含选自下组的氨基酸序列:seqidno:11、seqidno:16、seqidno:18和seqidno:20。所述氨基酸序列的变体可以为与其具有基本上相同的功能(例如,能够特异性结合cd38),且与其具有至少约85%(例如,具有至少约85%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或更高的)序列同一性的氨基酸序列。在某些实施方式中,所述氨基酸序列的变体为与其具有基本上相同的功能(例如,能够特异性结合cd38蛋白),且在其基础上包含一个或多个(例如,1-2个、1-3个、1-4个、1-5个、1-6个、1-7个、1-8个、1-9个、1-10个或更多个)氨基酸的添加、缺失或置换的氨基酸序列。
本申请所述的抗体或其抗原结合片段可包含抗体重链或其片段。例如,所述抗体重链或其片段还包含人恒定区。其中,所述人恒定区可包括人igg恒定区。其中,所述igg恒定区可包含人igg1恒定区。
例如,所述抗体重链或其片段可包含hcdr1,且所述hcdr1可包含选自下组的氨基酸序列:seqidno:4。所述抗体重链或其片段可包含hcdr2,且所述hcdr2可包含选自下组的氨基酸序列:seqidno:5。又例如,所述抗体重链或其片段可包含hcdr3,且所述hcdr3可包含选自下组的氨基酸序列:seqidno:6。所述氨基酸序列的变体可为与其具有基本上相同的功能(例如,能够特异性结合cd38蛋白),且与其具有至少约85%(例如,具有至少约85%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或更高的)序列同一性的氨基酸序列。在某些实施方式中,所述氨基酸序列的变体为与其具有基本上相同的功能(例如,能够特异性结合cd38蛋白),且在其基础上包含一个或多个(例如,1-2个、1-3个、1-4个、1-5个、1-6个、1-7个、1-8个、1-9个、1-10个或更多个)氨基酸的添加、缺失或置换的氨基酸序列。
所述抗体重链或其片段可包含重链可变区vh,且所述重链可变区vh可包含选自下组的氨基酸序列:seqidno:8。在某些实施方式中,所述抗体重链包含选自下组的氨基酸序列:seqidno:13、seqidno:17、seqidno:19和seqidno:21。所述氨基酸序列的变体可为与其具有基本上相同的功能(例如,能够特异性结合cd38蛋白),且与其具有至少约85%(例如,具有至少约85%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或更高的)序列同一性的氨基酸序列。在某些实施方式中,所述氨基酸序列的变体为与其具有基本上相同的功能(例如,能够特异性结合cd38蛋白),且在其基础上包含一个或多个(例如,1-2个、1-3个、1-4个、1-5个、1-6个、1-7个、1-8个、1-9个、1-10个或更多个)氨基酸的添加、缺失或置换的氨基酸序列。
在某些实施方式中,本申请所述的抗体或其抗原结合片段中lcdr1的氨基酸序列可包括seqidno:1或其变体;lcdr2的氨基酸序列可包括seqidno:2或其变体;lcdr3的氨基酸序列可包括seqidno:3或其变体;且hcdr1的氨基酸序列可包括seqidno:4或其变体;hcdr2的氨基酸序列可包括seqidno:5或其变体;hcdr3的氨基酸序列可包括seqidno:6或其变体。例如,该抗体或其抗原结合片段可包括抗体sg003或与其具有相同的lcdr1-3及hcdr1-3的抗体。在某些实施方式中,本申请所述的抗体或其抗原结合片段的轻链可包含轻链可变区,所述轻链可变区的氨基酸序列可包括seqidno:7或其变体;且其中重链可包含重链可变区,所述重链可变区的氨基酸序列可包括seqidno:8或其变体。例如,该抗体或其抗原结合片段可包括抗体sg003或与其具有相同的轻链可变区及重链可变区的抗体。在某些实施方式中,本申请所述的抗体或其抗原结合片段可包含轻链和重链,所述轻链的轻链氨基酸序列如seqidno:11所示且所述重链氨基酸序列如seqidno:13所示。例如,该抗体或其抗原结合片段可包括抗体sg003或与其具有相同的轻链及重链氨基酸序列。
在某些实施方式中,本申请所述的抗体可以为sg003。抗体sg003的lcdr1-3的氨基酸序列分别如seqidno.1、seqidno.2和seqidno.3所示;vl的氨基酸序列如seqidno.7所示;hcdr1-3的氨基酸序列分别如seqidno.4、seqidno.5和seqidno.6所示;vh的氨基酸序列如seqidno.8所示;轻链的氨基酸序列如seqidno.11所示;重链的氨基酸序列如seqidno.13所示。
在某些实施方式中,本申请所述的抗体或其抗原结合片段与参比抗体竞争结合cd38蛋白(例如,人cd38蛋白或猴cd38蛋白)。所述参比抗体可包含lcdr1-3和hcdr1-3,且其lcdr1的氨基酸序列可包括seqidno:1或其变体;lcdr2的氨基酸序列可包括seqidno:2或其变体;lcdr3的氨基酸序列可包括seqidno:3或其变体;其hcdr1的氨基酸序列可包括seqidno:4或其变体;hcdr2的氨基酸序列可包括seqidno:5或其变体;hcdr3的氨基酸序列可包括seqidno:6或其变体。在某些实施方式中,所述参比抗体可包括抗体sg003或与其具有相同的lcdr1-3及hcdr1-3的抗体。在某些实施方式中,所述参比抗体可包含轻链可变区和重链可变区,所述轻链可变区的氨基酸序列可包括seqidno:7或其变体;且所述重链可变区的氨基酸序列可包括seqidno:8或其变体。例如,该抗体或其抗原结合片段可包括抗体sg003或与其具有相同的轻链可变区及重链可变区的抗体。在某些实施方式中,所述参比抗体可包含轻链和重链,所述轻链的轻链氨基酸序列可如seqidno:11所示且所述重链氨基酸序列可如seqidno:13所示。例如,该参比抗体或其抗原结合片段可包括抗体sg003或与其具有相同的轻链及重链。
本申请所述的抗体或其抗原结合片段或变体,还可以在其轻链和/或重链的氨基酸序列中包含一个或多个随机突变(例如,一个或多个、如一个或数个氨基酸取代)。例如,所述抗体、其抗原结合片段或变体可在其轻链可变区的框架区l-fr1-4的一个或多个位点包含一个或多个随机突变(例如,一个或多个,如一个或数个氨基酸取代),和/或在其重链可变区的框架区h-fr1-4的一个或多个位点包含一个或多个随机突变(例如,一个或多个,如一个或数个氨基酸取代)。例如,发生随机突变后,所述的抗体或其抗原结合片段或变体的轻链可包含选自下组的氨基酸序列:seqidno:16、seqidno:18和seqidno:20;和/或所述的抗体或其抗原结合片段或变体的重链可包含选自下组的氨基酸序列:seqidno:17、seqidno:19和seqidno:21。发生随机突变后的cd38抗体或其抗原结合片段或变体,仍具有特异性结合人cd38蛋白和猴cd38蛋白的能力。
在某些实施方式中,本申请所述的抗体或其抗原结合片段的轻链的氨基酸序列包括seqidno:16或其变体;并且其重链的氨基酸序列包括seqidno:17或其变体;或者,本申请所述的抗体或其抗原结合片段的轻链的氨基酸序列包括seqidno:18或其变体;并且其重链的氨基酸序列包括seqidno:19或其变体;或者,本申请所述的抗体或其抗原结合片段的轻链的氨基酸序列包括seqidno:20或其变体;并且其重链的氨基酸序列包括seqidno:21或其变体。
核酸、载体、宿主细胞和制备方法
在另一个方面,本申请还提供了分离的一种或多种核酸分子。所述一种或多种核酸分子可编码本申请所述的抗体、其抗原结合片段或变体。例如,所述一种或多种核酸分子中的每一个核酸分子可以编码完整的所述抗体、其抗原结合片段或变体,也可以编码其中的一部分(例如,hcdr1-3、lcdr1-3、vl、vh、轻链或重链中的一种或多种)。
本申请所述的核酸分子中的至少一种所述核酸分子可经密码子优化。例如,所述密码子优化的方法包括但不限于:消除稀有密码子、调整gc含量、增加mrna的稳定性、调整mrna的二级结构、合理设计接头和调整起始密码子环境。
在某些实施方式中,所述核酸分子包含一个或多个选自下组的核苷酸序列:seqidno:9、seqidno:10、seqidno:12和seqidno:14。其中,seqidno:9可编码本申请所述抗体sg003的轻链可变区。seqidno:10可编码本申请所述抗体sg003的重链可变区。seqidno:12可编码本申请所述抗体sg003的轻链。seqidno:14可编码本申请所述抗体sg003的重链。
本申请所述的核酸分子可以为分离的。例如,其可以是通过以下方法产生或合成的:(i)在体外扩增的,例如通过聚合酶链式反应(pcr)扩增产生的,(ii)通过克隆重组产生的,(iii)纯化的,例如通过酶切和凝胶电泳分级分离,或者(iv)合成的,例如通过化学合成。在某些实施方式中,所述分离的核酸是通过重组dna技术制备的核酸分子。
在本申请中,可以通过本领域已知的多种方法来制备编码所述的抗体、其抗原结合片段或变体的核酸,这些方法包括但不限于,采用限制性片段操作或采用合成性寡核苷酸的重叠延伸pcr,具体操作可参见sambrook等人,molecularcloning,alaboratorymanual,coldspringharborlaboratorypress,coldspringharbor,n.y.,1989;和ausube等人currentprotocolsinmolecularbiology,greenepublishingandwiley-interscience,newyorkn.y.,1993。
在另一个方面,本申请提供了一种或多种载体,其包含本申请所述的一种或多种核酸分子。每种载体中可包含一种或多种所述核酸分子。此外,所述载体中还可包含其他基因,例如允许在适当的宿主细胞中和在适当的条件下选择该载体的标记基因。此外,所述载体还可包含允许编码区在适当宿主中正确表达的表达控制元件。这样的控制元件为本领域技术人员所熟知的,例如,可包括启动子、核糖体结合位点、增强子和调节基因转录或mrna翻译的其他控制元件等。在某些实施方式中,所述表达控制序列为可调的元件。所述表达控制序列的具体结构可根据物种或细胞类型的功能而变化,但通常包含分别参与转录和翻译起始的5’非转录序列和5’及3’非翻译序列,例如tata盒、加帽序列、caat序列等。例如,5’非转录表达控制序列可包含启动子区,启动子区可包含用于转录控制功能性连接核酸的启动子序列。所述表达控制序列还可包括增强子序列或上游活化子序列。本申请所述的一种或多种核酸分子可以与所述表达控制元件可操作地连接。
所述载体可以包括,例如质粒、粘粒、病毒、噬菌体或者在例如遗传工程中通常使用的其他载体。例如,所述载体为表达载体。例如,所述表达载体可以为t-easy。
在另一个方面,本申请提供了宿主细胞,所述宿主细胞可包含本申请所述的一种或多种核酸分子和/或本申请所述的一种或多种载体。在某些实施方式中,每种或每个宿主细胞可包含一个或一种本申请所述的核酸分子或载体。在某些实施方式中,每种或每个宿主细胞可包含多个(例如,2个或以上)或多种(例如,2种或以上)本申请所述的核酸分子或载体。例如,可将本申请所述的载体引入所述宿主细胞中,例如真核细胞,如来自植物的细胞、真菌或酵母细胞等。可通过本领域已知的方法将本申请所述的载体引入所述宿主细胞中,例如电穿孔、lipofectine转染、lipofectamin转染等。例如,所述宿主细胞可以为cho-s。
在另一个方面,本申请提供了制备所述的抗体、其抗原结合片段或变体的方法。所述方法可包括,在使得所述的抗体、其抗原结合片段或变体表达的条件下,培养所述本申请所述的宿主细胞。例如,可通过使用适当的培养基、适当的温度和培养时间等,这些方法是本领域普通技术人员所了解的。
在某些情形中,所述方法还可包括分离和/或纯化所述抗体或其抗原结合片段的步骤。例如,可以采用蛋白g-琼脂糖或蛋白a-琼脂糖进行亲和层析,还可通过凝胶电泳和/或高效液相色谱等来纯化和分离本申请所述的抗体或其抗原结合片段。例如,还可以使用proteina亲和纯化。
药物组合物、应用
在另一个方面,本申请提供了一种药物组合物,其可包含本申请所述的抗体、其抗体结合片段或变体,所述的核酸分子,所述的载体,所述的宿主细胞,以及任选地药学上可接受的佐剂。
所述药学上可接受的佐剂可以包括可以包括缓冲剂、抗氧化剂、防腐剂、低分子量多肽、蛋白质、亲水聚合物、氨基酸、糖、螯合剂、反离子、金属复合物和/或非离子表面活性剂等。
在本申请中,所述药物组合物可被配制用于口服给药,静脉内给药,肌肉内给药,在肿瘤部位的原位给药,吸入,直肠给药,阴道给药,经皮给药或通过皮下储存库给药。
所述药物组合物可以用于抑制肿瘤生长。例如,本申请的药物组合物可以抑制或延缓疾病的发展或进展,可以减小肿瘤大小(甚至基本消除肿瘤),和/或可以减轻和/或稳定疾病状态。
本申请所述的药物组合物可以包含治疗有效量的所述抗体或其抗原结合片段。所述治疗有效量是能够预防和/或治疗(至少部分治疗)患有或具有发展风险的受试者中的病症或病症(例如癌症)和/或其任何并发症而所需的剂量。
另一方面,本申请提供了所述的抗体、其抗原结合片段或变体在制备预防或治疗肿瘤的药物中的用途。
另一方面,本申请提供了用于预防或治疗肿瘤的所述的抗体、其抗原结合片段或变体。
另一方面,本申请提供了预防或治疗肿瘤的方法,其包括向有需要的受试者施用本申请所述的抗体、其抗原结合片段或变体、所述的分子核酸、所述的载体、所述的宿主细胞和/或所述的药物组合物。
在本申请中,所述肿瘤可包括cd38阳性的肿瘤。例如,所述cd38阳性的肿瘤可以选自以下组:多发性骨髓瘤、淋巴瘤和白血病。
在某些实施方式中,所述肿瘤选自以下组:非霍奇金淋巴瘤和霍奇金淋巴瘤。
另一方面,本申请提供了抑制cd38蛋白与cd38配体结合的方法,其包括施用本申请所述的抗体、其抗原结合片段或变体、所述的核酸分子、所述的载体和/或所述的宿主细胞。
在本申请中,所述cd38配体可以包括cd31蛋白。
在某些实施方式中,所述抑制cd38蛋白与cd38配体结合的方法为体外或离体方法。
本申请可包括以下的实施方案:
1.抗体、其抗原结合片段或变体,其以1×10-9m或更低的kd与cd38蛋白相结合。
2.根据实施方案1所述的抗体、其抗原结合片段或变体,其能够通过与cd38蛋白特异性结合而杀伤肿瘤细胞和/或抑制肿瘤生长。
3.根据实施方案1-2中任一项所述的抗体、其抗原结合片段或变体,其能够通过抗体依赖的细胞介导的细胞毒性adcc、补体依赖的细胞毒性cdc和/或细胞凋亡杀死cd38+细胞。
4.根据实施方案3所述的抗体、其抗原结合片段或变体,其中所述肿瘤包括cd38阳性的肿瘤。
5.根据实施方案4所述的抗体、其抗原结合片段或变体,其中所述cd38阳性的选自以下组:多发性骨髓瘤、淋巴瘤和白血病。
6.根据实施方案3-5中任一项所述的抗体、其抗原结合片段或变体,其中所述肿瘤选自以下组:非霍奇金淋巴瘤和霍奇金淋巴瘤。
7.根据实施方案3-6中任一项所述的抗体、其抗原结合片段或变体,其中所述肿瘤的细胞包括选自下组的细胞:raji细胞、daudi细胞、ramos细胞和rpmi8226细胞。
8.根据实施方案1-7中任一项所述的抗体、其抗原结合片段或变体,当其与cd38蛋白结合时,其结合所述cd38蛋白第220位至第241位氨基酸残基中的一个或多个残基。
9.根据实施方案1-8中任一项所述的抗体、其抗原结合片段或变体,其中所述抗体选自下组:单克隆抗体、单链抗体、嵌合抗体、人源化抗体和全人源抗体。
10.根据实施方案1-9中任一项所述的抗体、其抗原结合片段或变体,其中所述抗原结合片段选自下组:fab,fab’,f(ab)2和fv片段。
11.根据实施方案1-10中任一项所述的抗体、其抗原结合片段或变体,其中所述变体选自下组:
a)在所述抗体或所述其抗原结合片段中经过取代、缺失或添加一个或多个氨基酸的蛋白质或多肽;和
b)与所述抗体或所述其抗原结合片段具有至少90%序列同源性的蛋白质或多肽。
12.根据实施方案1-10中任一项所述的抗体、其抗原结合片段或变体,其中所述cd38蛋白为人cd38蛋白或猴cd38蛋白。
13.根据实施方案1-12中任一项所述的抗体、其抗原结合片段或变体,其与参比抗体竞争结合所述cd38蛋白,其中所述参比抗体包含轻链可变区和重链可变区,所述参比抗体的轻链可变区包含lcdr1-3,所述lcdr1-3的氨基酸序列依次为seqidno:1、seqidno:2和seqidno:3,所述参比抗体的重链可变区包含hcdr1-3,所述hcdr1-3的氨基酸序列依次为seqidno:4、seqidno:5和seqidno:6。
14.根据实施方案13所述的抗体、其抗原结合片段或变体,其中所述参比抗体的轻链可变区的氨基酸序列为:seqidno:7且所述参比抗体的重链可变区的氨基酸序列为:seqidno:8。
15.根据实施方案13-14中任一项所述的抗体、其抗原结合片段或变体,其中所述参比抗体的轻链包含如seqidno:11所示的氨基酸序列;且所述参比抗体的重链包含如seqidno:13所示的氨基酸序列。
16.根据实施方案1-12中任一项所述的抗体、其抗原结合片段或变体,其与参比抗体竞争结合所述cd38蛋白,其中所述参比抗体包含轻链和重链,其中所述参比抗体的轻链包含选自下组的氨基酸序列:seqidno:16、seqidno:18和seqidno:20;且所述参比抗体的重链包含选自下组的氨基酸序列:seqidno:17、seqidno:19和seqidno:21。
17.根据实施方案1-16中任一项所述的抗体、其抗原结合片段或变体,其中所述抗体包含抗体轻链或其片段。
18.根据实施方案17所述的抗体、其抗原结合片段或变体,其中所述抗体轻链或其片段包含lcdr1,且所述lcdr1包含选自下组的氨基酸序列:seqidno:1。
19.根据实施方案17-18中任一项所述的抗体、其抗原结合片段或变体,其中所述抗体轻链或其片段包含lcdr2,且所述lcdr2包含选自下组的氨基酸序列:seqidno:2。
20.根据实施方案17-19中任一项所述的抗体、其抗原结合片段或变体,其中所述抗体轻链或其片段包含lcdr3,且所述lcdr3包含选自下组的氨基酸序列:seqidno:3。
21.根据实施方案17-20中任一项所述的抗体、其抗原结合片段或变体,其中所述抗体轻链或其片段包含轻链可变区vl,且所述轻链可变区vl包含选自下组的氨基酸序列:seqidno:7。
22.根据实施方案17-21中任一项所述的抗体、其抗原结合片段或变体,其中所述抗体轻链或其片段还包含人恒定区。
23.根据实施方案22所述的抗体、其抗原结合片段或变体,其中所述人恒定区包括人igκ恒定区。
24.根据实施方案17-23中任一项所述的抗体、其抗原结合片段或变体,其中所述抗体轻链或其片段包含选自下组的氨基酸序列:seqidno:11、seqidno:16、seqidno:18和seqidno:20。
25.根据实施方案1-24中任一项所述的抗体、其抗原结合片段或变体,其中所述抗体包含抗体重链或其片段。
26.根据实施方案25所述的抗体、其抗原结合片段或变体,其中所述抗体重链或其片段包含hcdr1,且所述hcdr1包含选自下组的氨基酸序列:seqidno:4。
27.根据实施方案25-26中任一项所述的抗体、其抗原结合片段或变体,其中所述抗体重链或其片段包含hcdr2,且所述hcdr2包含选自下组的氨基酸序列:seqidno:5。
28.根据实施方案25-27中任一项所述的抗体、其抗原结合片段或变体,其中所述抗体重链或其片段包含hcdr3,且所述hcdr3包含选自下组的氨基酸序列:seqidno:6。
29.根据实施方案25-28中任一项所述的抗体、其抗原结合片段或变体,其中,所述抗体重链或其片段包含重链可变区vh,且所述重链可变区vh包含选自下组的氨基酸序列:seqidno:8。
30.根据实施方案25-29中任一项所述的抗体、其抗原结合片段或变体,其中所述抗体重链或其片段还包含人恒定区。
31.根据实施方案30所述的抗体、其抗原结合片段或变体,所述人恒定区包括人igg恒定区。
32.根据实施方案31所述的抗体、其抗原结合片段或变体,其中所述igg恒定区包含人igg1恒定区。
33.根据实施方案25-32中任一项所述的抗体、其抗原结合片段或变体,其中,所述抗体重链包含选自下组的氨基酸序列:seqidno:13、seqidno:17、seqidno:19和seqidno:21。
34.分离的一种或多种核酸分子,其编码实施方案1-33中任一项所述的抗体、其抗原结合片段或变体。
35.根据实施方案34所述的核酸分子,其中至少一种所述核酸分子经密码子优化。
36.根据实施方案34-35中任一项所述的核酸分子,其中所述核酸分子包含一个或多个选自下组的核苷酸序列:seqidno:9、seqidno:10、seqidno:12和seqidno:14。
37.载体,其包含实施方案34-36中任一项所述的核酸分子。
38.宿主细胞,其包含实施方案34-36中任一项所述的核酸分子或实施方案37所述的载体。
39.制备实施方案1-33中任一项所述的抗体、其抗原结合片段或变体的方法,所述方法包括在使得所述抗体、其抗原结合片段或变体表达的条件下,培养实施方案38所述的宿主细胞。
40.药物组合物,其包含实施方案1-33中任一项所述的抗体、其抗原结合片段或变体、实施方案34-36中任一项所述的核酸分子、实施方案37所述的载体和/或实施方案38所述的宿主细胞,以及任选地药学上可接受的佐剂。
41.实施方案1-33中任一项所述的抗体、其抗原结合片段或变体在制备预防或治疗肿瘤的药物中的用途。
42.根据实施方案41所述的用途,其中所述肿瘤包括cd38阳性的肿瘤。
43.根据实施方案42所述的用途,其中所述cd38阳性的肿瘤选自以下组:多发性骨髓瘤、淋巴瘤和白血病。
44.根据实施方案41-43中任一项所述的用途,其中所述肿瘤选自以下组:非霍奇金淋巴瘤和霍奇金淋巴瘤。
45.实施方案1-33中任一项所述的抗体、其抗原结合片段或变体,其用于预防或治疗肿瘤。
46.根据实施方案45所述的抗体、其抗原结合片段或变体,其中所述肿瘤包括cd38阳性的肿瘤。
47.根据实施方案46所述的抗体、其抗原结合片段或变体,其中所述cd38阳性的肿瘤选自以下组:多发性骨髓瘤、淋巴瘤和白血病。
48.根据实施方案45-47中任一项所述的用途,其中所述肿瘤选自以下组:非霍奇金淋巴瘤和霍奇金淋巴瘤。
49.预防或治疗有需要的受试者中的肿瘤的方法,其包括向所述受试者施用实施方案1-33中任一项所述的抗体、其抗原结合片段或变体、实施方案34-36中任一项所述的分子核酸、实施方案37所述的载体、实施方案38所述的宿主细胞和/或实施方案39所述的药物组合物。
50.根据实施方案49所述的方法,其中所述肿瘤包括cd38阳性的肿瘤。
51.根据实施方案50所述的方法,其中所述cd38阳性的肿瘤选自以下组:多发性骨髓瘤、淋巴瘤和白血病。
52.根据实施方案49-51中任一项所述的方法,其中所述肿瘤选自以下组:非霍奇金淋巴瘤和霍奇金淋巴瘤。
53.抑制cd38蛋白与cd38配体结合的方法,所述方法包括施用实施方案1-33中任一项所述的抗体、其抗原结合片段或变体、实施方案34-36中任一项所述的核酸分子、实施方案37所述的载体和/或实施方案38所述的宿主细胞。
54.根据实施方案53所述的方法,其中所述cd38配体包括cd31。
不欲被任何理论所限,下文中的实施例仅仅是为了阐释本申请的产品、方法或系统的工作方式,而不用于限制本申请发明的范围。
实施例
实施例1杂交瘤抗体制备及基因克隆
小鼠免疫:balb/c小鼠(购自北京维通利华实验动物技术有限公司)经皮下(s.c.)用弗氏佐剂或弗氏不完全佐剂混合100μg可溶性cd38抗原(购自北京义翘神州生物技术有限公司)免疫3次。在第0天用弗氏完全佐剂,在第14天和第28天用弗氏不完全佐剂。将免疫小鼠的脾细胞根据标准方法融合于小鼠骨髓瘤细胞sp2/0(atcc)。
杂交瘤融合:按现有常规杂交瘤融合方法融合小鼠脾脏,hat筛选法筛选融合后的杂交瘤细胞(每个孔105个细胞)。在12天后,取上清用cd38抗原包被的酶标板进行elisa检测。优选克隆通过有限稀释法进行第二轮亚克隆。获得稳定表达目的抗体的杂交瘤株后进行保种建库。
制备rna:使用rna提取试剂盒trizolreagent(购自lifetechnologies)制备rna。用反转录试剂盒(购自北京全式金生物技术有限公司)制备编码抗体基因的cdna,以cdna为模板做pcr扩增抗体可变区基因,克隆t-easy载体,将克隆得到的抗体重链和轻链可变区序列测序,并进一步获得对应的氨基酸序列。
实施例2抗体人源化改造及制备
在实施例1获得鼠源抗体可变区重、轻链序列的基础上,通过ncbi提供的在线序列比对方法(igblast)与ncbi数据库中已有人源抗体序列进行比对,确定潜在的人源化位;进一步通过swissmodel搭建鼠源抗体可变区三维结构,确定人源化位点;针对相应的人源化位点,开展人源化改造,获得人源化抗体序列。
将人源化改造后的抗体命名为sg003,测序结果显示,抗体sg003的lcdr1-3的氨基酸序列分别如seqidno.1、seqidno.2和seqidno.3所示;vl的氨基酸序列如seqidno.7所示;经优化密码子,反向翻译获得的编码vl的核苷酸序列如seqidno.9所示;抗体sg003的hcdr1-3的氨基酸序列分别如seqidno.4、seqidno.5和seqidno.6所示;vh的氨基酸序列如seqidno.8所示;经优化密码子,反向翻译获得的编码vh的核苷酸序列如seqidno.10所示。
抗体sg003的轻链的氨基酸序列如seqidno.11所示;编码其的核苷酸序列如seqidno.12所示。抗体sg003的重链的氨基酸序列如seqidno.13所示;编码其的核苷酸序列如seqidno.14所示。
将获得的人源化改造后的抗体可变区基因克隆进含有人igg恒定区基因的真核表达载体pcmv-163中,构建全抗体表达载体,其物理图谱如图1所示。图1中,真核表达载体pcmv-163的各个组成成分均为本领域已知的成分,按照所示次序重组而成。
使用expichotmexpressionsystem试剂盒(购自thermofisherscientific),将获得的编码抗体sg003的真核表达载体转染至cho-s细胞中进行表达,收集含有目的蛋白的细胞培养上清,利用常规的proteina亲和纯化目标抗体。
实施例3人源化抗体结合靶抗原
用含有1μg/mlcd38-his融合蛋白的pbs溶液在4℃包被elisa板过夜。该板随后用含有0.01%吐温-20的pbs溶液(pbst)洗涤,向pbst加入10%的胎牛血清在37℃封闭1小时,然后加入不同浓度的sg003抗体、对照抗体daratumumab,在37℃反应1小时。用pbst洗涤后,加入辣根过氧化物酶标记的羊抗人igg二抗(goatantihumanigghrp,购自thermofisherscientific),在37℃反应30分钟。然后用pbst重复洗板5遍,在吸水纸上尽量拍干残留液滴,向每孔加入100μltmb(购自ebioscience),在室温(20±5℃)避光放置1-5min。向每孔加入100μl2nh2so4终止液终止底物反应,用酶标仪在450nm处读取od值,分析抗体与靶抗原cd38-his结合能力。结果显示,sg003抗体与对照抗体daratumumab相比,显示出更强的结合活性,结果如图2所示。图2中,ec50值为35.1±10.5ng/ml,daratumumab抗体的ec50值为150.9±105.8ng/ml。
实施例4人源化抗体亲和力测定
采用biacore生物大分子相互作用仪(ge公司)分析抗体亲和力。在芯片上偶联抗人igg-fab抗体(购自abcam),利用抗人igg抗体捕获sg003抗体,抗体浓度定为1μg/ml,进样时间为60-150秒;以抗原cd38为流动相,使用6个浓度梯度(3.125、6.25、12.5、25、50、100nm),结合时间为120秒;解离时间为1200秒;使用10mm甘氨酸-盐酸缓冲液(ph2.1)进行再生,时间为60秒。结果显示sg003抗体亲和力如表1所示。
表1sg003抗体亲和力
实施例5人源化抗体特异性识别靶抗原
将牛奶(北京博迈德生物技术有限公司)、bsa(bovogen)、cd19(北京义翘神州生物技术有限公司)、trop2(北京义翘神州生物技术有限公司)、cd47(北京麦格珀尔生物科技有限公司)、cd38(北京义翘神州生物技术有限公司)、gas6(r&d)等各蛋白以及axl(acrobiosystems)分别包被elisa板条,1mg/ml,4℃过夜;pbst洗涤后,加入10%的胎牛血清,37℃封闭1小时;加入sg003抗体,37℃反应1小时;pbst洗涤后,加入辣根过氧化物酶标记的羊抗人igg二抗(goatantihumanigghrp,thermofisherscientific),室温反应30分钟;pbst重复洗板5遍,在吸水纸上尽量拍干残留液滴;每孔加入100mltmb(ebioscience),室温(20±5℃)避光放置1-5min;每孔加入100ml2nh2so4终止液终止底物反应,酶标仪450nm处读取od值,分析抗体与蛋白结合能力。
结果如图3所示,图3的结果显示,sg003抗体均能特异性识别靶抗原cd38,但与牛奶、bsa、cd19、trop2、cd47、axl、gas6等蛋白均无显著的结合反应。
实施例6人源化抗体与细胞表面抗原的结合
利用流式分析技术检测raji细胞、daudi细胞、ramos细胞和rpmi8226细胞表面cd38蛋白与sg003抗体及对照抗体daratumumab的结合。收集对数生长期细胞,调整细胞密度到5×106个细胞/ml,在冰上预冷。用含2%fbs预冷的生理盐水将sg003抗体、对照抗体daratumumab稀释成不同浓度。取100μl细胞,加入等体积所述稀释抗体,于4℃避光反应30min。反应结束后,洗涤细胞两次。用稀释后的pe标记小鼠抗人igg二抗(pemouseanti-humanigg,购自bdpharmingen)100μl重悬细胞,4℃避光反应30min。反应结束后,用2%fbs预冷的生理盐水洗涤细胞两次。用400μl1%多聚甲醛重悬细胞。用流式细胞仪(bdcalibur)分析抗体与细胞表面抗原的结合能力。
结果显示,sg003抗体能特异性识别raji细胞、daudi细胞、ramos细胞和rpmi8226细胞表面cd38,该识别活性明显高于对照抗体daratumumab且呈剂量依赖性,其中与raji细胞结合(图4a)的ec50值sg003为34.4ng/ml,daratumumab为49.3ng/ml。与daudi细胞结合(图4b)的ec50值sg003为36.7ng/ml,daratumumab为50.9ng/ml。与ramos细胞结合(图4c)的ec50值sg003为81.5ng/ml,daratumumab为95.1ng/ml。与rpmi8226细胞结合(图4d)的ec50值sg003为140.3ng/ml,daratumumab为176.5ng/ml。
实施例7人源化抗体的抗体依赖性细胞介导的细胞毒性(adcc)活性
首先将实验所需靶细胞(raji细胞、daudi细胞、ramos细胞和rpmi8226细胞)调整密度至2×105个细胞/ml重悬在adcc缓冲液(无酚红mem培养液+1%fbs)中,并加入96孔板(50μl/孔)。随后向每孔中加入100μl不同浓度的sg003抗体,混匀后在37℃,含5%co2的培养箱中孵育30min。再将实验所需效应细胞nk92mi-cd16a(购自华博生物)调整密度至1.2×106cell/ml,加入有靶细胞的孔中,使得靶细胞:效应细胞=1:6。混匀后在37℃,含5%co2的培养箱中孵育4-6h后,移除96孔板内部分原液(100μl/孔),加入ldh检测试剂盒(cytotoxicitydetectionkit,购自roche)中ldh反应混合物(100μl/孔),于37℃反应10min。再加入终止液(50μl/孔),轻微混匀。用酶标仪在492nm时读取od值,同时以650nm处的od值为背景值。实验中同时设置如下对照组,其中对照1为adcc缓冲液,对照2为靶细胞+adcc缓冲液,对照3为靶细胞+裂解液+adcc缓冲液,对照4为靶细胞+效应细胞+adcc缓冲液。特异性杀伤率%=((实验组-对照4)/(对照3-对照2))×100%。量效曲线采用graphpadprismversion5进行数据分析。
结果显示,使用raji靶细胞和nk92mi-cd16a效应细胞检测时,sg003抗体显示了非常有效的adcc活性(参见图5a),ec50值sg003为6.97ng/ml,daratumumab为17.0ng/ml。daudi作为靶细胞时,ec50值sg003为0.72ng/ml,daratumumab为4.6ng/ml(参见图5b)。同时sg003抗体还显示出对ramos细胞有效的adcc活性(参见图5c),ec50值sg003为0.69±0.007ng/ml,daratumumab为3.01ng/ml。sg003抗体还显示出对rpmi8226细胞有效的adcc活性(参见图5d),ec50值sg003为1.46ng/ml,daratumumab为4.94ng/ml。
实施例8人源化抗体体内抑制肿瘤活性
通过向cb17scid小鼠接种raji-luc细胞建立肿瘤模型,来评价sg003抗体抑制肿瘤活性的效果。
选择雌性,5~8周龄的cb17scid小鼠(购自北京百奥赛图基因生物技术有限公司)进行试验。raji-luc细胞为北京百奥赛图基因生物技术有限公司在raji细胞的基础上,转入荧光素报告基因后获得的稳定细胞系。复苏培养至所需数量后,收集对数期生长细胞悬浮至5×106个/0.2ml浓度,以0.2ml/只的数量通过尾静脉接种到cb17scid小鼠,接种后于第0天、第7天用小动物成像仪观察肿瘤生长情况及体重,并于第7天挑选肿瘤成像信号适中的18只小鼠入组,随机分组分配到3个组中,每组6只。然后开始对动物进行给药,设生理盐水对照组、阳性对照组(daratumumab,购自强生公司)以及实验组(sg003),给药剂量为200μg/kg,两周给药一次,共给药2次,观察小鼠体重、肿瘤生长情况以及小鼠生存率。
结果显示,daratumumab以及sg003抗体均可为实验动物所耐受。各组给药动物和溶剂对照组比较有明显肿瘤生长抑制效果(参见图6),第一次给药后第七天,daratumumab以及sg003抗体治疗组的平均荧光强度分别为(平均3.92e+07,标准误4.04e+06)、(平均3.19e+07,标准误:9.32e+06),显著低于对照组平均肿瘤荧光强度为(平均3.04e+08,标准误4.29e+07)。
然后,进一步观察动物生存率,对照组的中位生存时间为分组后12天,daratumumab为21天,而sg003组为28天。sg003组优效于daratumumab组(参见图7)。
实施例9嵌合抗体种属识别特异性
将人(human)、小鼠(mouse)、大鼠(rat)、食蟹猴(cynomolgus)等不同种属的cd38胞外段蛋白(北京义翘神州生物技术有限公司)分别包被elisa板条,1mg/ml,4℃过夜;pbst洗涤后,加入10%的胎牛血清,于37℃封闭1小时;分别加入待测sg003抗体、对照抗体daratumumab,37℃反应1小时;pbst洗涤后,加入辣根过氧化物酶标记的羊抗人igg二抗(goatantihumanigghrp,购自thermofisherscientific),室温反应30分钟;pbst重复洗板5遍,在吸水纸上尽量拍干残留液滴;每孔加入100mltmb(购自ebioscience),室温(20±5℃)避光放置1-5min;每孔加入100ml2nh2so4终止液终止底物反应,用酶标仪在450nm处读取od值,分析抗体与不同种属cd38蛋白的结合能力。
结果显示,sg003抗体能识别人和食蟹猴的cd38蛋白分子,但与小鼠和大鼠的cd38蛋白分子无结合反应;结果如图8a所示。
而对照抗体daratumumab只识别人cd38蛋白分子,与小鼠、大鼠及食蟹猴的cd38蛋白分子均无结合反应。结果如图8b所示。
实施例10人源化抗体突变后保持生物学活性
借助基因工程技术,可以对sg003抗体可变区序列进行随机突变,获得新的抗体可变区序列,并进一步获得新的抗体轻链和重链序列。例如,在sg003抗体基础上进行随机突变后获得的抗体,其轻链氨基酸序列可为seqidno:16,且重链氨基酸序列可为seqidno:17;或者,其轻链氨基酸序列可为seqidno:18,且重链氨基酸序列可为seqidno:19;或者,其轻链氨基酸序列可为seqidno:20,且重链氨基酸序列可为seqidno:21。将分别包含上述突变后轻链和重链的组合的抗体依次命名为sg003m1-3(例如,sg003m1抗体的轻链氨基酸序列为seqidno:16,且重链氨基酸序列为seqidno:17)。
参考实施例2的方法制备新抗体,参考实施例4的方法评价抗体活性。随机突变后的抗体sg003m1-3可以识别cd38抗原(参见图9)。经测定,sg003m1的ec50值为15.72ng/ml、sg003m2的ec50值为27.75ng/ml、sg003m3的ec50值为6.10ng/ml。随机选择sg003m1,测定亲和力结果如表2所示。
表2sg003突变体亲和力分析
前述详细说明是以解释和举例的方式提供的,并非要限制所附权利要求的范围。目前本文所列举的实施方式的多种变化对本领域普通技术人员来说是显而易见的,且保留在所附的权利要求和其等同方案的范围内。
序列表
<110>杭州尚健生物技术有限公司;尚健单抗(北京)生物技术有限公司
<120>cd38蛋白抗体及其应用
<130>0070-pa-001
<160>21
<170>siposequencelisting1.0
<210>1
<211>15
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>lcdr1
<400>1
argalaserserservalserserseralaphesertyrvalhis
151015
<210>2
<211>7
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>lcdr2
<400>2
leualaserasnleugluser
15
<210>3
<211>9
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>lcdr3
<400>3
hishisserarggluleuprophethr
15
<210>4
<211>5
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>hcdr1
<400>4
leutyrtrpmetasn
15
<210>5
<211>17
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>hcdr2
<400>5
lysileasnproaspserserthrileasntyrthrproserleulys
151015
asp
<210>6
<211>10
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>hcdr3
<400>6
leutrpilealathrglyglypheasptyr
1510
<210>7
<211>111
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>vl
<400>7
gluilevalmetthrglnserproalaserleuseralaserleugly
151015
glnargalathrilesercysargalaserserservalserserser
202530
alaphesertyrvalhistrptyrglnglnlysserglyglnpropro
354045
lysleuleuiletyrleualaserasnleugluserglyvalproala
505560
argpheserglyserglyserglythraspphethrleuthrilehis
65707580
provalglusergluaspvalalathrtyrtyrcyshishisserarg
859095
gluleuprophethrpheglyserglythrlysleugluilelys
100105110
<210>8
<211>119
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>vh
<400>8
glnvalglnleuleugluserglyglyglyleuvalglnproglygly
151015
serleulysleusercysvalalaserglypheasppheserleutyr
202530
trpmetasntrpvalargglnalaproglylysglyleuglutrpile
354045
glylysileasnproaspserserthrileasntyrthrproserleu
505560
lysasplysphepheileserargaspasnalalysasnthrleutyr
65707580
leuglnmetthrlysvalargsergluaspthralaleutyrtyrcys
859095
alaargleutrpilealathrglyglypheasptyrtrpglyglngly
100105110
thrthrleuthrvalserser
115
<210>9
<211>333
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>密码子优化后的vl核苷酸
<400>9
gagatcgtgatgacccagagccctgccagcctgagcgccagcctgggccagagggccacc60
atcagctgcagggccagcagcagcgtgagcagcagcgccttcagctacgtgcactggtac120
cagcagaagagcggccagcctcctaagctgctgatctacctggccagcaacctggagagc180
ggcgtgcctgccaggttcagcggcagcggcagcggcaccgacttcaccctgaccatccac240
cctgtggagagcgaggacgtggccacctactactgccaccacagcagggagctgcctttc300
accttcggcagcggcaccaagctggagatcaag343
<210>10
<211>357
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>密码子优化后的vh核苷酸
<400>10
caggtgcagctgctggagagcggcggcggcctggtgcagcctggcggcagcctgaagctg60
agctgcgtggccagcggcttcgacttcagcctgtactggatgaactgggtgaggcaggcc120
cctggcaagggcctggagtggatcggcaagatcaaccctgacagcagcaccatcaactac180
acccctagcctgaaggacaagttcttcatcagcagggacaacgccaagaacaccctgtac240
ctgcagatgaccaaggtgaggagcgaggacaccgccctgtactactgcgccaggctgtgg300
atcgccaccggcggcttcgactactggggccagggcaccaccctgaccgtgagcagc367
<210>11
<211>218
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>sg003轻链
<400>11
gluilevalmetthrglnserproalaserleuseralaserleugly
151015
glnargalathrilesercysargalaserserservalserserser
202530
alaphesertyrvalhistrptyrglnglnlysserglyglnpropro
354045
lysleuleuiletyrleualaserasnleugluserglyvalproala
505560
argpheserglyserglyserglythraspphethrleuthrilehis
65707580
provalglusergluaspvalalathrtyrtyrcyshishisserarg
859095
gluleuprophethrpheglyserglythrlysleugluilelysarg
100105110
thrvalalaalaproservalpheilepheproproseraspglugln
115120125
leulysserglythralaservalvalcysleuleuasnasnphetyr
130135140
proargglualalysvalglntrplysvalaspasnalaleuglnser
145150155160
glyasnserglngluservalthrgluglnaspserlysaspserthr
165170175
tyrserleuserserthrleuthrleuserlysalaasptyrglulys
180185190
hislysvaltyralacysgluvalthrhisglnglyleuserserpro
195200205
valthrlysserpheasnargglyglucys
210215
<210>12
<211>657
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>sg003轻链核苷酸
<400>12
gagatcgtgatgacccagagccctgccagcctgagcgccagcctgggccagagggccacc60
atcagctgcagggccagcagcagcgtgagcagcagcgccttcagctacgtgcactggtac120
cagcagaagagcggccagcctcctaagctgctgatctacctggccagcaacctggagagc180
ggcgtgcctgccaggttcagcggcagcggcagcggcaccgacttcaccctgaccatccac240
cctgtggagagcgaggacgtggccacctactactgccaccacagcagggagctgcctttc300
accttcggcagcggcaccaagctggagatcaagcgtacggtggctgcaccatctgtcttc360
atcttcccgccatctgatgagcagttgaaatctggaactgcctctgttgtgtgcctgctg420
aataacttctatcccagagaggccaaagtacagtggaaggtggataacgccctccaatcg480
ggtaactcccaggagagtgtcacagagcaggacagcaaggacagcacctacagcctcagc540
agcaccctgacgctgagcaaagcagactacgagaaacacaaagtctacgcctgcgaagtc600
acccatcagggcctgagctcgcccgtcacaaagagcttcaacaggggagagtgttag677
<210>13
<211>449
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>sg003重链
<400>13
glnvalglnleuleugluserglyglyglyleuvalglnproglygly
151015
serleulysleusercysvalalaserglypheasppheserleutyr
202530
trpmetasntrpvalargglnalaproglylysglyleuglutrpile
354045
glylysileasnproaspserserthrileasntyrthrproserleu
505560
lysasplysphepheileserargaspasnalalysasnthrleutyr
65707580
leuglnmetthrlysvalargsergluaspthralaleutyrtyrcys
859095
alaargleutrpilealathrglyglypheasptyrtrpglyglngly
100105110
thrthrleuthrvalserseralaserthrlysglyproservalphe
115120125
proleualaproserserlysserthrserglyglythralaalaleu
130135140
glycysleuvallysasptyrpheprogluprovalthrvalsertrp
145150155160
asnserglyalaleuthrserglyvalhisthrpheproalavalleu
165170175
glnserserglyleutyrserleuserservalvalthrvalproser
180185190
serserleuglythrglnthrtyrilecysasnvalasnhislyspro
195200205
serasnthrlysvalasplyslysvalgluprolyssercysasplys
210215220
thrhisthrcysproprocysproalaprogluleuleuglyglypro
225230235240
servalpheleupheproprolysprolysaspthrleumetileser
245250255
argthrprogluvalthrcysvalvalvalaspvalserhisgluasp
260265270
progluvallyspheasntrptyrvalaspglyvalgluvalhisasn
275280285
alalysthrlysproargglugluglntyrasnserthrtyrargval
290295300
valservalleuthrvalleuhisglnasptrpleuasnglylysglu
305310315320
tyrlyscyslysvalserasnlysalaleuproalaproileglulys
325330335
thrileserlysalalysglyglnproarggluproglnvaltyrthr
340345350
leuproproserargaspgluleuthrlysasnglnvalserleuthr
355360365
cysleuvallysglyphetyrproseraspilealavalglutrpglu
370375380
serasnglyglnprogluasnasntyrlysthrthrproprovalleu
385390395400
aspseraspglyserphepheleutyrserlysleuthrvalasplys
405410415
serargtrpglnglnglyasnvalphesercysservalmethisglu
420425430
alaleuhisasnhistyrthrglnlysserleuserleuserprogly
435440445
lys
<210>14
<211>1350
<212>dna
<213>人工序列(artificialsequence)
<220>
<223>sg003重链核苷酸
<400>14
caggtgcagctgctggagagcggcggcggcctggtgcagcctggcggcagcctgaagctg60
agctgcgtggccagcggcttcgacttcagcctgtactggatgaactgggtgaggcaggcc120
cctggcaagggcctggagtggatcggcaagatcaaccctgacagcagcaccatcaactac180
acccctagcctgaaggacaagttcttcatcagcagggacaacgccaagaacaccctgtac240
ctgcagatgaccaaggtgaggagcgaggacaccgccctgtactactgcgccaggctgtgg300
atcgccaccggcggcttcgactactggggccagggcaccaccctgaccgtgagcagcgct360
agcaccaagggcccatcggtcttccccctggcaccctcctccaagagcacctctgggggc420
acagcggccctgggctgcctggtcaaggactacttccccgaaccggtgacggtgtcgtgg480
aactcaggcgccctgaccagcggcgtgcacaccttcccggctgtcctacagtcctcagga540
ctctactccctcagcagcgtggtgaccgtgccctccagcagcttgggcacccagacctac600
atctgcaacgtgaatcacaagcccagcaacaccaaggtggacaagaaagttgagcccaaa660
tcttgtgacaaaactcacacatgcccaccgtgcccagcacctgaactcctggggggaccg720
tcagtcttcctcttccccccaaaacccaaggacaccctcatgatctcccggacccctgag780
gtcacgtgcgtggtggtggacgtgagccacgaagaccccgaggtcaagttcaactggtac840
gtggacggcgtggaggtgcataatgccaagacaaagccgcgggaggagcagtacaacagc900
acgtaccgtgtggtcagcgtcctcaccgtcctgcaccaggactggctgaatggcaaggag960
tacaagtgcaaggtctccaacaaagccctcccagcccccatcgagaaaaccatctccaaa1020
gccaaagggcagccccgagaaccacaggtgtacaccctgcccccatcccgggatgagctg1080
accaagaaccaggtcagcctgacctgcctggtcaaaggcttctatcccagcgacatcgcc1140
gtggagtgggagagcaatgggcagccggagaacaactacaagaccacgcctcccgtgctg1200
gactccgacggctccttcttcctctacagcaagctcaccgtggacaagagcaggtggcag1260
caggggaacgtcttctcatgctccgtgatgcatgaggctctgcacaaccactacacgcag1320
aagagcctctccctgtctccgggtaaatga1394
<210>15
<211>22
<212>prt
<213>homosapiens
<400>15
serthrpheglyservalgluvalhisasnleuglnproglulysval
151015
glnthrleuglualatrp
20
<210>16
<211>218
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>突变后的轻链1
<400>16
gluilevalmetthrglnserproalaserleuseralaserleugly
151015
glnargalaserilesercysargalaserasnservalserserser
202530
alatyrsertyrvalhistrptyrglnglnlysserglyglnpropro
354045
lysleuleuiletyrleualaserasnileglnserglyvalproala
505560
argpheserglyserglyserglythraspphethrleuthrilehis
65707580
provalglusergluaspvalalathrtyrtyrcyshishisserarg
859095
glnleuproserthrpheglyserglythrlysleugluilelysarg
100105110
thrvalalaalaproservalpheilepheproproseraspglugln
115120125
leulysserglythralaservalvalcysleuleuasnasnphetyr
130135140
proargglualalysvalglntrplysvalaspasnalaleuglnser
145150155160
glyasnserglngluservalthrgluglnaspserlysaspserthr
165170175
tyrserleuserserthrleuthrleuserlysalaasptyrglulys
180185190
hislysvaltyralacysgluvalthrhisglnglyleuserserpro
195200205
valthrlysserpheasnargglyglucys
210215
<210>17
<211>449
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>突变后的重链1
<400>17
glnvalglnleuleugluserglyglyglyleuvalglnproglygly
151015
serleulysleusercysvalalaserglytyrasnpheserleutyr
202530
tyrmetasntrpvalargglnalaproglylysglyleuglutrpile
354045
glylysileglnprogluserserthrileglntyrthrproserleu
505560
lysasplysphepheileserargaspasnalalysasnthrleutyr
65707580
leuglnmetthrlysvalargsergluaspthralaleutyrtyrcys
859095
alaargleutrpileglyserglyglypheasptyrtrpglyglngly
100105110
thrthrleuthrvalserseralaserthrlysglyproservalphe
115120125
proleualaproserserlysserthrserglyglythralaalaleu
130135140
glycysleuvallysasptyrpheprogluprovalthrvalsertrp
145150155160
asnserglyalaleuthrserglyvalhisthrpheproalavalleu
165170175
glnserserglyleutyrserleuserservalvalthrvalproser
180185190
serserleuglythrglnthrtyrilecysasnvalasnhislyspro
195200205
serasnthrlysvalasplyslysvalgluprolyssercysasplys
210215220
thrhisthrcysproprocysproalaprogluleuleuglyglypro
225230235240
servalpheleupheproprolysprolysaspthrleumetileser
245250255
argthrprogluvalthrcysvalvalvalaspvalserhisgluasp
260265270
progluvallyspheasntrptyrvalaspglyvalgluvalhisasn
275280285
alalysthrlysproargglugluglntyrasnserthrtyrargval
290295300
valservalleuthrvalleuhisglnasptrpleuasnglylysglu
305310315320
tyrlyscyslysvalserasnlysalaleuproalaproileglulys
325330335
thrileserlysalalysglyglnproarggluproglnvaltyrthr
340345350
leuproproserargaspgluleuthrlysasnglnvalserleuthr
355360365
cysleuvallysglyphetyrproseraspilealavalglutrpglu
370375380
serasnglyglnprogluasnasntyrlysthrthrproprovalleu
385390395400
aspseraspglyserphepheleutyrserlysleuthrvalasplys
405410415
serargtrpglnglnglyasnvalphesercysservalmethisglu
420425430
alaleuhisasnhistyrthrglnlysserleuserleuserprogly
435440445
lys
<210>18
<211>218
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>突变后的轻链2
<400>18
gluilevalmetthrglnserproalaserleuseralaserleugly
151015
glnargalathrilesercysargalaserserservalserserser
202530
alatyrsertyrvalhistrptyrglnglnlysserglyglnpropro
354045
lysleuleuiletyrleualaseraspleuglnserglyvalproala
505560
argpheserglyserglyserglythraspphethrleuthrilehis
65707580
provalglusergluaspvalalathrtyrtyrcyshishisserarg
859095
gluleuprotyrserpheglyserglythrlysleugluilelysarg
100105110
thrvalalaalaproservalpheilepheproproseraspglugln
115120125
leulysserglythralaservalvalcysleuleuasnasnphetyr
130135140
proargglualalysvalglntrplysvalaspasnalaleuglnser
145150155160
glyasnserglngluservalthrgluglnaspserlysaspserthr
165170175
tyrserleuserserthrleuthrleuserlysalaasptyrglulys
180185190
hislysvaltyralacysgluvalthrhisglnglyleuserserpro
195200205
valthrlysserpheasnargglyglucys
210215
<210>19
<211>449
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>突变后的重链2
<400>19
glnvalglnleuleugluserglyglyglyleuvalglnproglygly
151015
serleulysleusercysvalalaserglypheasppheserleutyr
202530
trpmetasntrpvalargglnalaproglylysglyleuglutrpile
354045
glylysileserproasnserserthrileasntyrserproserleu
505560
lysasplysphepheileserargaspasnalalysasnthrleutyr
65707580
leuglnmetthrlysvalargsergluaspthralaleutyrtyrcys
859095
alaargleutyrilealaserglyglypheasptyrtrpglyglngly
100105110
thrthrleuthrvalserseralaserthrlysglyproservalphe
115120125
proleualaproserserlysserthrserglyglythralaalaleu
130135140
glycysleuvallysasptyrpheprogluprovalthrvalsertrp
145150155160
asnserglyalaleuthrserglyvalhisthrpheproalavalleu
165170175
glnserserglyleutyrserleuserservalvalthrvalproser
180185190
serserleuglythrglnthrtyrilecysasnvalasnhislyspro
195200205
serasnthrlysvalasplyslysvalgluprolyssercysasplys
210215220
thrhisthrcysproprocysproalaprogluleuleuglyglypro
225230235240
servalpheleupheproprolysprolysaspthrleumetileser
245250255
argthrprogluvalthrcysvalvalvalaspvalserhisgluasp
260265270
progluvallyspheasntrptyrvalaspglyvalgluvalhisasn
275280285
alalysthrlysproargglugluglntyrasnserthrtyrargval
290295300
valservalleuthrvalleuhisglnasptrpleuasnglylysglu
305310315320
tyrlyscyslysvalserasnlysalaleuproalaproileglulys
325330335
thrileserlysalalysglyglnproarggluproglnvaltyrthr
340345350
leuproproserargaspgluleuthrlysasnglnvalserleuthr
355360365
cysleuvallysglyphetyrproseraspilealavalglutrpglu
370375380
serasnglyglnprogluasnasntyrlysthrthrproprovalleu
385390395400
aspseraspglyserphepheleutyrserlysleuthrvalasplys
405410415
serargtrpglnglnglyasnvalphesercysservalmethisglu
420425430
alaleuhisasnhistyrthrglnlysserleuserleuserprogly
435440445
lys
<210>20
<211>218
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>突变后的轻链3
<400>20
gluilevalmetthrglnserproalaserleuseralaserleugly
151015
glnargalathrilesercysargalaserasnservalserthrser
202530
alaphesertyrvalhistrptyrglnglnlysserglyglnpropro
354045
lysleuleuiletyrleualaserasnleugluserglyvalproala
505560
argpheserglyserglyserglythraspphethrleuthrilehis
65707580
provalglusergluaspvalalathrtyrtyrcyshishisserarg
859095
gluvalprophethrpheglyserglythrlysleugluilelysarg
100105110
thrvalalaalaproservalpheilepheproproseraspglugln
115120125
leulysserglythralaservalvalcysleuleuasnasnphetyr
130135140
proargglualalysvalglntrplysvalaspasnalaleuglnser
145150155160
glyasnserglngluservalthrgluglnaspserlysaspserthr
165170175
tyrserleuserserthrleuthrleuserlysalaasptyrglulys
180185190
hislysvaltyralacysgluvalthrhisglnglyleuserserpro
195200205
valthrlysserpheasnargglyglucys
210215
<210>21
<211>449
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>突变后的重链3
<400>21
glnvalglnleuleugluserglyglyglyleuvalglnproglygly
151015
serleulysleusercysvalalaserglypheasppheserleutyr
202530
trpmetasntrpvalargglnalaproglylysglyleuglutrpile
354045
glylysileserproaspserserserleuasntyrthrproserval
505560
lysasplysphepheileserargaspasnalalysasnthrleutyr
65707580
leuglnmetthrlysvalargsergluaspthralaleutyrtyrcys
859095
alaargleutrpilealathrglyglytyrasntyrtrpglyglngly
100105110
thrthrleuthrvalserseralaserthrlysglyproservalphe
115120125
proleualaproserserlysserthrserglyglythralaalaleu
130135140
glycysleuvallysasptyrpheprogluprovalthrvalsertrp
145150155160
asnserglyalaleuthrserglyvalhisthrpheproalavalleu
165170175
glnserserglyleutyrserleuserservalvalthrvalproser
180185190
serserleuglythrglnthrtyrilecysasnvalasnhislyspro
195200205
serasnthrlysvalasplyslysvalgluprolyssercysasplys
210215220
thrhisthrcysproprocysproalaprogluleuleuglyglypro
225230235240
servalpheleupheproprolysprolysaspthrleumetileser
245250255
argthrprogluvalthrcysvalvalvalaspvalserhisgluasp
260265270
progluvallyspheasntrptyrvalaspglyvalgluvalhisasn
275280285
alalysthrlysproargglugluglntyrasnserthrtyrargval
290295300
valservalleuthrvalleuhisglnasptrpleuasnglylysglu
305310315320
tyrlyscyslysvalserasnlysalaleuproalaproileglulys
325330335
thrileserlysalalysglyglnproarggluproglnvaltyrthr
340345350
leuproproserargaspgluleuthrlysasnglnvalserleuthr
355360365
cysleuvallysglyphetyrproseraspilealavalglutrpglu
370375380
serasnglyglnprogluasnasntyrlysthrthrproprovalleu
385390395400
aspseraspglyserphepheleutyrserlysleuthrvalasplys
405410415
serargtrpglnglnglyasnvalphesercysservalmethisglu
420425430
alaleuhisasnhistyrthrglnlysserleuserleuserprogly
435440445
lys
- 还没有人留言评论。精彩留言会获得点赞!