一种含芳杂环亚甲基吲嗪衍生物的制备方法与流程
本发明属于有机药物合成技术领域,具体是一种合成吡嗪衍生物的方法。
背景技术:
在有机化合成和药物合成中,吡嗪及其衍生物是合成活性天然产物的重要原料,具有抗菌、抗高血压、抗肿瘤以及抗心律失常等重要的生物和药理活性,因此受到广泛的重视。然而,如何经济有效地合成吡嗪及其衍生物是合成热点。目前,对吡嗪及其衍生物的制备方法有很多,其主要方法是在吲嗪的3-位引入新的基团,如:(1)Org. Lett.,6(7), 1159- 1162,2004
又如:(2)Org. Biomol. Chem., 13, 10986–10994,2015
还如:(3)Org. Biomol. Chem., 10, 7108–7119, 2012
再如(4)Org. Lett.,13(6), 1342- 1345,2011
上述几种合成方法均能在吲嗪3-位引入新的取代基,得到吲嗪衍生物。但存在两个共性的缺陷,一是区域选择性差,二是昂贵的金属催化剂导致合成成本居高不下。中国专利201180042948.8中公开了一些3-位氧代的吲嗪衍生物制备方法,其步骤(1)将化合物与化合物进行缩合,但并未公开该缩合的反应条件和产率;(2)进行碱水解反应;(3)进行酯化反应;(4)再与N- 溴代琥珀酰亚胺进行反应;(5)经历三光气的作用,得到相应的异氰酸酯,再进行胺缩合,得到相应的脲;(6)在碱性介质中对得到的脲进行环化反应;(7)最后在钯催化剂、配体和碱的存在下,与苯基硼酸衍生物或杂芳基硼酸衍生物或苯基硼酸酯衍生物或杂芳基硼酸酯衍生物发生苏楚基偶联反应,得到相应的吲嗪衍生物。该技术方案存在的问题是收率较低,操作繁琐复杂,合成成本高,不能满足规模化生产要求。
因此,亟待研发一种原料易得、产率高、成本低的芳杂环亚甲基吲嗪衍生物合成方法。
技术实现要素:
针对现有技术存在的问题,本发明提供一种含芳杂环亚甲基吲嗪衍生物及其合成方法。
本发明的反应机理为:
根据上述反应机理,本发明采用如下技术方案:
一种含芳杂环亚甲基吲嗪衍生物,其结构式为:
其中R1为H、CH3;R2为吡啶基、呋喃基、噻吩基、吡咯基、吲哚基、喹啉基等杂环基。
本发明的含芳杂环亚甲基吲嗪衍生物的制备方法,包括如下步骤:
(1)按摩尔比称取原料,1份5-甲基-2-苯基吲嗪,1份芳杂醛,1.3份汉斯酯,47-94份甲苯,0.05-0.1份对甲基苯磺酸;
(2)将5-甲基-2-苯基吲嗪、芳杂醛和汉斯酯依次溶于甲苯中,再加入催化剂对甲基苯磺酸, 60℃搅拌12~24h;
(3)将(2)得到的溶液冷却至室温,减压旋干溶剂;
(4)将(3)得到的固相经柱层析分离得芳杂环亚甲基吲嗪衍生物。
所述的吲嗪原料的结构式为:。
所述的芳杂醛包括不同取代位的吡啶甲醛、噻吩甲醛、呋喃甲醛、吡咯甲醛、吲哚甲醛、喹啉甲醛,其结构式为:。
所述的汉斯酯的结构式为:。
本发明使用的原料或试剂均市售可得。
与现有技术相比,本发明的优点在于:(1)原料易得且经济;本发明合成方所需的原料包括吲嗪衍生物、芳杂醛、汉斯酯、对甲基苯磺酸和甲苯,上述原料都是市场易于购置的化学品,且与现有技术所需的原料相比,原料经济、实惠,初步核算,本发明合成芳杂环亚甲基吲嗪衍生物的成本只有现有技术的50%。(2)省去使用贵金属做催化剂,一方面进一步降低了合成成本,另一方面没有可能的重金属污染,属于环境友好型合成方法。(3)操作简单,本发明为三组分一锅合成法,步骤简单,易于操作,对操作人员的要求较低,易于推广应用。(4)收率高,实验证明,本发明合成方法的收率在90%以上。
附图说明
图1 为5-甲基2-苯基-3-(吡啶-3-亚甲基)吲嗪的核磁共振氢谱。
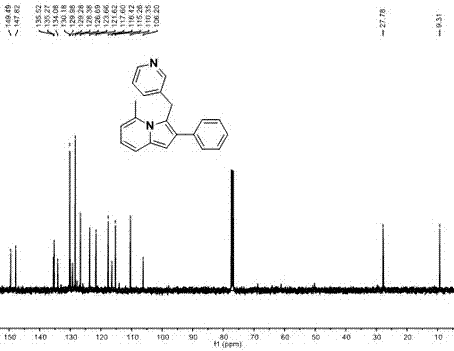
图 2为5-甲基2-苯基-3-(吡啶-3-亚甲基)吲嗪的核磁共振碳谱。
图3为5-甲基2-苯基-3-(吡啶-4-亚甲基)吲嗪的核磁共振氢谱。
图4为5-甲基2-苯基-3-(吡啶-4-亚甲基)吲嗪的核磁共振碳谱。
图5为5-甲基2-苯基-3-(吡啶-2-亚甲基)吲嗪的核磁共振氢谱。
图6为5-甲基2-苯基-3-(吡啶-2-亚甲基)吲嗪的核磁共振碳谱。
图7为5-甲基2-苯基-3-(噻吩-3-亚甲基)吲嗪的核磁共振氢谱。
图8为5-甲基2-苯基-3-(噻吩-3-亚甲基)吲嗪的核磁共振碳谱。
图9为5-甲基2-苯基-3-(呋喃-2-亚甲基)吲嗪的核磁共振氢谱。
图10为5-甲基2-苯基-3-(呋喃-2-亚甲基)吲嗪的核磁共振碳谱。
实施例1
在50 mL圆底烧瓶中加入1 mmol 5-甲基-2-苯基吲嗪(207 mg)、1 mmolβ-吡啶甲醛(107 mg)、1.3 mmol汉斯酯(330 mg)、 94mmol甲苯(10 mL),搅拌溶解后再加入0.1 mmol对甲基苯磺酸(17 mg),60℃搅拌反应24h,冷却至室温,减压旋干溶剂,柱层析分离得棕色产物277 mg,产率93%。结构式:
中文名称:5-甲基2-苯基-3-(吡啶-3-亚甲基)吲嗪
外观:棕色固体
熔点:159-162 ℃
核磁共振氢谱(400MHz , CDCl3, 内标: TMS); δ: 8.51 – 8.36 (m, 2H), 7.45 (dt, J = 15.8, 7.8 Hz, 4H), 7.39 – 7.33 (m, 3H), 7.25 (d, J = 7.8 Hz, 1H), 7.17 (dd, J = 7.7, 4.7 Hz, 1H), 6.66 (dd, J = 8.9, 6.6 Hz, 1H), 6.42 (t, J = 6.7 Hz, 1H), 4.30 (s, 2H), 2.38 (s, 3H);结果见图1。
核磁共振碳谱(400MHz , CDCl3, 内标: TMS); δ:149.49, 147.82, 135.52, 135.27, 134.08, 130.18, 129.98, 129.28, 128.38, 126.69, 123.66, 121.62, 117.60, 116.42, 115.26, 110.35, 106.20, 27.78, 9.31;结果见图2。
实施例2
在50 mL圆底烧瓶中加入1 mmol 5-甲基-2-苯基吲嗪(207 mg)、 1 mmol γ-吡啶甲醛(107 mg)、1.3 mmol汉斯酯(330 mg)、47mmol甲苯(5 mL),搅拌溶解后再加入0.1mmol对甲基苯磺酸(17 mg),60℃搅拌反应18h,冷却至室温,旋干溶剂,柱层析分离得棕色固体产物283 mg,产率95%。结构式:
中文名称:5-甲基2-苯基-3-(吡啶-4-亚甲基)吲嗪
外观:棕色固体
熔点: 168-171 ℃
核磁共振氢谱(400MHz , CDCl3, 内标: TMS);δ:8.50 (d, J = 5.9 Hz, 2H), 7.51 – 7.34 (m, 7H), 6.99 (d, J = 5.5 Hz, 2H), 6.68 (dd, J = 8.8, 6.5 Hz, 1H), 6.43 (t, J = 6.8 Hz, 1H), 4.28 (s, 2H), 2.39 (s, 3H);结果见图3。
核磁共振碳谱(400MHz , CDCl3, 内标: TMS);δ:150.06, 147.89, 135.43, 130.12, 129.47, 128.40, 126.73, 123.19, 121.65, 117.63, 115.83, 115.38, 110.39, 106.22, 29.94, 9.34;结果见图4。
实施例3
在50 mL圆底烧瓶中加入1 mmol 5-甲基-2-苯基吲嗪(207 mg)、 1 mmolα-吡啶甲醛(107 mg)、1.3 mmol汉斯酯(330 mg,)、 65.8mmol甲苯(7 mL),搅拌溶解后再加入0.05 mmol对甲基苯磺酸(8.5mg,),60℃搅拌反应12h,冷却至室温,旋干溶剂,柱层析分离得棕色固体产物269 mg,产率90%。结构式
中文名称:5-甲基2-苯基-3-(吡啶-2-亚甲基)吲嗪
外观:棕色固体
熔点:164-166 ℃
核磁共振氢谱(400MHz , CDCl3, 内标: TMS); δ:8.59 (d, J = 4.2 Hz, 1H), 7.71 (d, J = 7.0 Hz, 1H), 7.60 – 7.35 (m, 7H), 7.19 – 7.02 (m, 1H), 6.82 (d, J = 7.8 Hz, 1H), 6.69 – 6.61 (m, 1H), 6.42 (t, J = 6.7 Hz, 1H), 4.49 (s, 2H), 2.40 (s, 3H);结果见图5。
核磁共振碳谱(400MHz , CDCl3, 内标: TMS);δ:158.94, 149.38, 136.80, 135.73, 130.30, 129.87, 128.91, 128.33, 126.57, 122.31, 122.02, 121.47, 117.38, 117.12, 115.21, 110.04, 106.06, 33.68, 9.39; HRMS (ESI): calcd. For C24H24NO2 (M+H): 358.1807; found: 358.1800;结果见图6。
实施例4
在50 mL圆底烧瓶中加入1 mmol 5-甲基-2-苯基吲嗪(207 mg)、1 mmolβ-噻吩甲醛(112 mg)、1.3 mmol汉斯酯(330 mg)、 56.4mmol甲苯(6 mL),搅拌溶解后再加入0.08 mmol对甲基苯磺酸(13.6 mg,),60℃搅拌反应16h,冷却至室温,旋干溶剂,柱层析分离得棕色固体产物270 mg,产率91%。结构式:
中文名称:5-甲基2-苯基-3-(噻吩-3-亚甲基)吲嗪
外观:棕色固体
熔点:149-151 ℃
核磁共振氢谱(400MHz , CDCl3, 内标: TMS);δ:7.59 (d, J = 7.1 Hz, 1H), 7.50 – 7.41 (m, 5H), 7.37 (t, J = 7.0 Hz, 1H), 7.29 (t, J = 3.9 Hz, 1H), 6.88 (d, J = 4.9 Hz, 1H), 6.81 (d, J = 1.6 Hz, 1H), 6.67 (dd, J = 8.9, 6.5 Hz, 1H), 6.44 (t, J = 6.7 Hz, 1H), 4.27 (s, 2H), 2.41 (s, 3H);结果见图7。
核磁共振碳谱(400MHz , CDCl3, 内标: TMS);δ:139.06, 135.78, 130.24, 129.71, 128.27, 127.71, 126.47, 126.00, 122.06, 120.83, 118.16, 117.44, 114.95, 109.98, 105.83, 25.80, 9.41; HRMS (ESI): calcd. For C20H18NS (M+H): 304.1162; found: 304.1169;结果见图8。
实施例5
在50 mL圆底烧瓶中加入1 mmol 5-甲基-2-苯基吲嗪(207 mg)、 1 mmolα-呋喃甲醛(96 mg)、1.3 mmol汉斯酯(330 mg)、 84.6mmol无水甲苯(9 mL),搅拌溶解后再加入0.1 mmol对甲基苯磺酸(17 mg),60℃搅拌反应22h,冷却至室温,旋干溶剂,柱层析分离得棕色固体产物261 mg,产率91%。结构式
中文名称:5-甲基2-苯基-3-(呋喃-2-亚甲基)吲嗪
外观:棕色固体
熔点:178-180℃;
核磁共振氢谱(400MHz , CDCl3, 内标: TMS);δ:7.77 (d, J = 7.1 Hz, 1H), 7.55 – 7.47 (m, 4H), 7.46 – 7.39 (m, 3H), 6.71 (dd, J = 8.7, 6.7 Hz, 1H), 6.52 (t, J = 6.3 Hz, 1H), 6.41 – 6.27 (m, 1H), 5.98 (d, J = 2.4 Hz, 1H), 4.27 (s, 2H), 2.42 (s, 3H);结果见图9。
核磁共振碳谱(400MHz,CDCl3,内标: TMS);δ:152.25, 141.55, 135.58, 130.38, 129.91, 128.59, 128.27, 126.56, 122.12, 117.45, 115.59, 115.15, 110.42, 110.06, 106.19, 105.94, 24.26, 9.39; HRMS (ESI): calcd. For C20H18NO (M+H): 288.1383; found: 238.1389;结果见图10。
- 还没有人留言评论。精彩留言会获得点赞!