一步法实时荧光RT-PCR反应缓冲液及其反应体系和PCR方法与流程
本发明涉及生物
技术领域:
,更具体地说,涉及一种一步法实时荧光rt-pcr反应缓冲液及其反应体系和pcr方法。
背景技术:
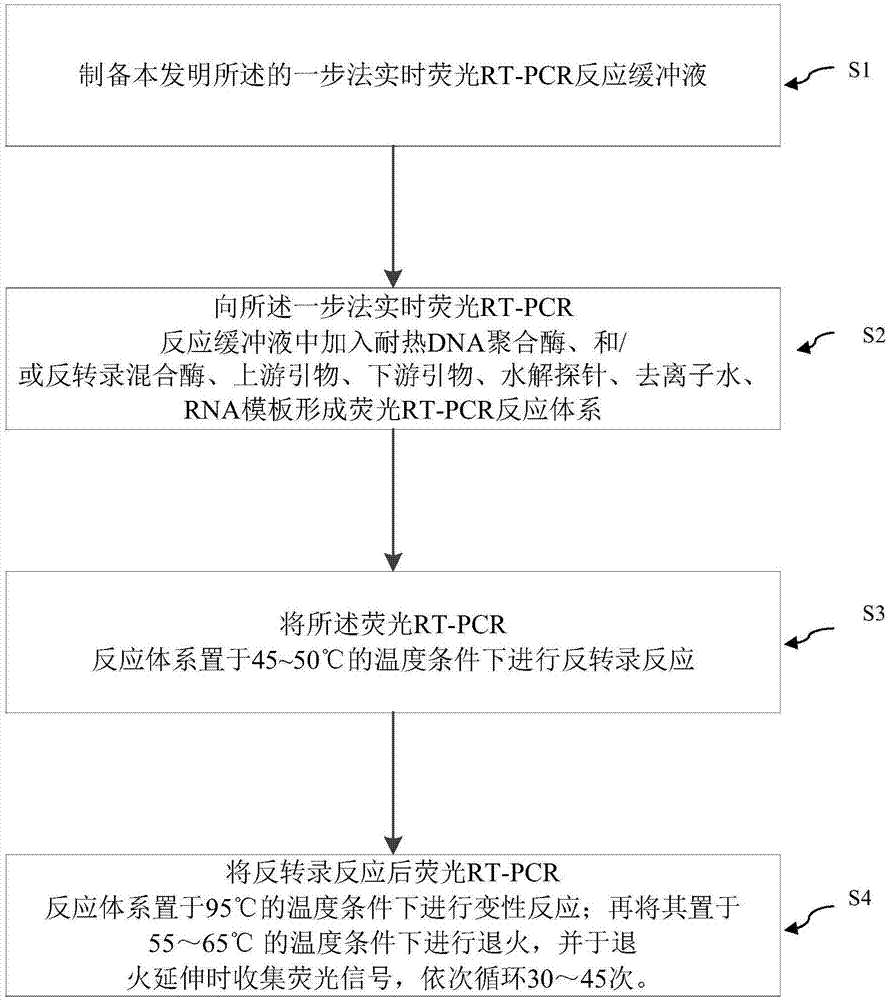
实时荧光pcr技术是近年来应用最广泛的一种实时在线的检测技术,既能够定性,又能够定量,是近年来进行检测的新的“黄金标准”。实时荧光pcr根据化学原理的不同可分为探针法和染料法。其中taqman实时荧光技术以taqman水解探针为基础。当探针完整时,5’端荧光基团发射的荧光信号被3’端淬灭基团吸收而不发光;当探针被具有5’-3’外切酶活性的taq酶降解时,荧光基团和淬灭基团分离,发射出的荧光就可以被荧光pcr检测到。在荧光pcr的检测中,rna的荧光rt-pcr检测应用最广泛。荧光rt-pcr检测步骤首先是逆转录酶将rna逆转录成cdna,taq酶可以催化5’至3’方向的依赖于cdna模板的脱氧核苷酸的聚合,同时具有5’-3’外切酶活性的taq酶在进行pcr扩增时将探针进行剪切,同时释放出荧光信号。《一种荧光定量pcr反应液及荧光定量pcr方法》,申请号为cn201010538264.4,公开了在常规的pcr反应液中增加了包括二甲基亚砜、甘油、牛血清白蛋白、甲酰胺、聚乙二醇6000、亚精胺、硫酸铵和甜菜碱中的一种或多种作为荧光pcr的反应增强剂。《荧光定量pcr反应液及试剂盒和荧光定量pcr方法》,申请号为cn201410578009.0,公开了在sybr染料荧光pcr反应液中加入了酶的保护剂和稳定剂二甲基亚砜、牛血清蛋白和甘油。《一种荧光定量pcr反应液及方法》,申请号为cn201610958965公开了在常规的pcr缓冲液中加入了荧光稳定剂(np-40、tritonx100、nacl和kcl)和荧光增强剂(牛血清白蛋白、二甲基亚砜、甲酰胺、亚精胺和甜菜碱)。以上专利申请文件其存在pcr反应效率低的问题。技术实现要素:本发明要解决的技术问题在于,提供一种能够解决pcr反应效率低的一步法实时荧光rt-pcr反应缓冲液及其反应体系和实时荧光pcr方法。本发明解决其技术问题所采用的技术方案是:构造一种一步法实时荧光rt-pcr反应缓冲液,包括如下体积比的原料:优选地,各所述原料的终浓度为:优选地,所述一步法实时荧光rt-pcr反应缓冲液的ph值为6.5~8.5。本发明还构造一种一步法实时荧光rt-pcr反应体系,包括本发明所述的一步法实时荧光rt-pcr反应缓冲液,还包括耐热dna聚合酶、和/或反转录混合酶,上游引物,下游引物,水解探针,去离子水,rna模板。优选地,所述耐热dna聚合酶为2~10u/μl。优选地,所述反转录混合酶为50~300u/μl。优选地,所述耐热dna聚合酶为化学修饰的热启动耐热dna酶、抗体修饰的热启动耐热dna酶的一种或多种。优选地,反转录混合酶为amv反转录酶、m-mlv反转录酶、superscriptiii逆转录酶的混合酶。发明还构造一种实时荧光pcr方法,包括以下步骤:s1、制备本发明所述的一步法实时荧光rt-pcr反应缓冲液;s2、向所述一步法实时荧光rt-pcr反应缓冲液中加入耐热dna聚合酶、和/或反转录混合酶,上游引物,下游引物,水解探针,去离子水,rna模板形成荧光rt-pcr反应体系;s3、将所述荧光rt-pcr反应体系置于45~50℃的温度条件下进行反转录反应;s4、将反转录反应后荧光rt-pcr反应体系置于95℃的温度条件下进行变性反应;再将其置于55~65℃的温度条件下进行退火,并于退火延伸时收集荧光信号,依次循环30~45次。实施本发明的一步法实时荧光rt-pcr反应缓冲液及其实时荧光rt-pcr反应体系和实时荧光pcr方法,具有以下有益效果:该一步法实时荧光rt-pcr反应缓冲液由三羟甲基氨基甲烷-盐酸缓冲液、氯化钾、氯化镁、硫酸铵、二甲基亚砜、脱氧核糖核苷三磷酸、甘油、牛血清蛋白、吐温20、三氮化钠、rox参比染料、去离子配置而成,其在常规的荧光稳定剂、荧光增强剂、taq酶的保护剂和稳定剂的基础上,增加了硫酸铵、三氮化钠,从而增加了nh4+和n3-,提高pcr反应效率,适用于pcr技术的高效扩增型和灵敏检测,其不仅具有稳定性好,荧光效果佳、灵敏度高的优点,而且具有反应效率快的优点。且其在常规实时荧光rt-pcr母液成份的基础上,形成了一步法实时荧光rt-pcr反应缓冲液,该反应缓冲液温度兼容性强,基本上所有荧光rt-pcr的反应均在同一个温度进行,保证了反应的均一性。该实时荧光rt-pcr反应体系,向本发明的一步法实时荧光rt-pcr反应缓冲液加入耐热dna聚合酶、反转录混合酶、上游引物、下游引物、水解探针、去离子水、rna模板形成,其具有结果可靠和准确灵敏的优点。该实时荧光pcr方法,通过采用一步法实时荧光rt-pcr反应缓冲液配置成荧光rt-pcr反应体系,其具有结果可靠和准确灵敏、操作简单、省时省力、降低检测成本,提高检查效率等优点,特别适合大规模样品的快速检测以及紧急疫情的快速诊断。附图说明下面将结合附图及实施例对本发明作进一步说明,附图中:图1是本发明一步法实时荧光rt-pcr反应缓冲液及其实时荧光pcr方法中的实时荧光pcr方法的工艺流程图;图2是本发明一步法实时荧光rt-pcr反应缓冲液及其实时荧光pcr方法的对比例1的扩增效果图;图3是本发明一步法实时荧光rt-pcr反应缓冲液及其实时荧光pcr方法的实施例1的扩增效果图;图4是本发明一步法实时荧光rt-pcr反应缓冲液及其实时荧光pcr方法的对比例1中用商品化反应体系进行实时荧光rt-pcr实验的标准曲线图;图5是本发明一步法实时荧光rt-pcr反应缓冲液及其实时荧光pcr方法的实施例1的实时荧光rt-pcr实验的标准曲线图;图6是本发明一步法实时荧光rt-pcr反应缓冲液及其实时荧光pcr方法的实施例1中一步法实时荧光rt-pcr反应缓冲液用于检测检测肠道病毒通用型、柯萨奇病毒a组16型和肠道病毒71型的扩增效果图;图7是本发明一步法实时荧光rt-pcr反应缓冲液及其实时荧光pcr方法中对比例2商品化实时荧光rt-pcr试剂盒的反应体系用于检测检测肠道病毒通用型、柯萨奇病毒a组16型和肠道病毒71型的扩增效果图;图8是本发明一步法实时荧光rt-pcr反应缓冲液及其实时荧光pcr方法的检测实施例1的扩增效果图;图9是本发明一步法实时荧光rt-pcr反应缓冲液及其实时荧光pcr方法的检测实施例2的扩增效果图。具体实施方式为了对本发明的技术特征、目的和效果有更加清楚的理解,现对照附图详细说明本发明的具体实施方式。实施例中,未注明具体条件者,按照常规条件或制造商建议的调节进行,所以试剂或仪器未注明生产厂商者,均为可通过市购获得的常规产品。实施例中,1m=1mol/l,1mm=10-3mol/l,1nm=10-9mol/l,本发明所涉及的百分比为体积百分比或质量百分比。本发明的一步法实时荧光rt-pcr反应缓冲液,增加了nh4+和n3-,提高pcr反应效率,适用于pcr技术的高效扩增型和灵敏检测。且其在常规实时荧光rt-pcr母液成份的基础上,形成了一步法实时荧光rt-pcr反应缓冲液,该反应缓冲液温度兼容性强,基本上所有荧光rt-pcr的反应均在同一个温度进行,保证了反应的均一性。本发明的一步法实时荧光rt-pcr反应缓冲液,包括如下原料:三羟甲基氨基甲烷-盐酸缓冲液(tris-hcl)、氯化钾(kcl)、氯化镁(mgcl2)、硫酸铵((nh4)2so4)、二甲基亚砜(dmso)、脱氧核糖核苷三磷酸(dntps)、甘油、牛血清蛋白(bsa)、吐温20(tween20)、三氮化钠(nan3)、rox参比染料(roxreferencedye)、去离子水;以上原料均配置成相应浓度的溶液,所得到的一步法实时荧光rt-pcr反应缓冲液的ph值优选为6.5~8.5。其中,优选地,该tris-hcl的浓度为20~40mm,且可由母液浓度为1m的tris-hcl溶液配置而成,其在该一步法实时荧光rt-pcr反应缓冲液的配比优选为2%~4%,其可用于调节该一步法实时荧光rt-pcr反应缓冲液的ph值,稳定该一步法实时荧光rt-pcr反应缓冲液的ph值。其中,优选地,该kcl溶液的浓度为100~200mm,且其可由母液浓度为1m的kcl溶液配置而成,其在该一步法实时荧光rt-pcr反应缓冲液的配比优选为1%~2%,其可用于稳定基础荧光值,从而使得荧光值在上升前能够保持稳定。其中,优选地,该mgcl2的浓度为3~6mm,其可以由母液浓度为1m的mgcl2溶液配置而成,其在该一步法实时荧光rt-pcr反应缓冲液的配比优选为0.3%~0.6%,其可用于稳定基础荧光值,从而使得荧光值在上升前能够保持稳定。其中,优选地,该(nh4)2so4的浓度为20~40mm,其可以由母液浓度为3.2m的(nh4)2so4配置而成,其在该一步法实时荧光rt-pcr反应缓冲液的配比优选为0.625%~1.25%,其可为该实时荧光rt-pcr反应缓冲液提供nh4+,从而增强了一步法实时荧光rt-pcr反应缓冲液的灵敏度,提高该一步法实时荧光rt-pcr反应缓冲液的反应效率。其中,优选地,该dmso的浓度为0.07~0.14mm,其可由该dmso的原液配置而成,其在该一步法实时荧光rt-pcr反应缓冲液的配比优选为5%~10%,其可与该bsa配合,用于增强该一步法实时荧光rt-pcr反应缓冲液中耐热dna聚合酶的稳定性和活性,可减少引物二聚体的形成。其中,优选地,dntps其可包括datp、dgtp、dctp以及dttp,其中,每一组分的浓度均为2~4mm,且其均可由母液浓度为100mm的母液配置而成,每一组分在该一步法实时荧光rt-pcr反应缓冲液的配比优选为2%~4%。其中,优选地,甘油的浓度为0.05~0.1mm,其可由其原液配置而成,其在该一步法实时荧光rt-pcr反应缓冲液的配比优选为5%~10%,其可用于提高该一步法实时荧光rt-pcr反应缓冲液中耐热dna聚合酶的稳定性,其到保护耐热dna聚合酶的作用。其中,优选地,bsa其浓度可以为1.5×10-7~3×10-7mm,其可由浓度为1.5×10-5mm的bsa溶液配置而成,其在该一步法实时荧光rt-pcr反应缓冲液的配比优选为1%~2%,其可与dmso配合,增强该一步法实时荧光rt-pcr反应体系中耐热dna聚合酶的稳定性和活性,可减少引物二聚体的形成。其中,优选地,tween20的浓度可以为1.8×10-6~3.6×10-6mm,其可由其原液配置而成,其在该一步法实时荧光rt-pcr反应缓冲液的配比优选为0.2%~0.4%,其可以起到增溶的作用。其中,优选地,该nan3溶液的浓度为4.5×10-2~9×10-2mm,其可以由浓度为4.5mm的nan3溶液配置而成,其在该一步法实时荧光rt-pcr反应缓冲液的配比优选为0.3%~0.6%,其能够为该一步法实时荧光rt-pcr反应缓冲液提供n3-,从而提高一步法实时荧光rt-pcr反应缓冲液的pcr反应效率。其中,优选地,该rox参比染料的浓度为70~140nm,其可由浓度为25μm的rox参比染料配置而成,其在该一步法实时荧光rt-pcr反应缓冲液的配比优选为0.28%~0.56%,其可用于调整pcr加样误差所引起的pcr管与管之间的荧光差异。本发明的一步法实时荧光rt-pcr反应体系,其包括本发明的一步法实时荧光rt-pcr反应缓冲液,还包括耐热dna聚合酶(taq聚合酶)、和/或反转录混合酶,上游引物,下游引物,水解探针,去离子水,rna模板;该一步法实时荧光rt-pcr反应缓冲液见前述,在此不再赘述。当所检测的被测物中只含有dna时,只需采用taq聚合酶,反转录混合酶可以省去;当所检测的被测物中含有rna时,则需要添加taq聚合酶和反转录混合酶。其中,该taq聚合酶为2~10u/μl,其可包括化学修饰的热启动taq聚合酶、抗体修饰的热启动taq聚合酶的一种或多种;在本实施例中,优选地,该taq聚合酶为5u/μl,且其为化学修饰的热启动taq聚合酶;当然,可以理解地,在其他实施例中,其也可以为常规的taq聚合酶。其中,该反转录混合酶为50~300u/μl,其可包括amv反转录酶、m-mlv反转录酶、superscriptiii逆转录酶的混合酶;在本实施例中,优选地,200u/μl,且其可以为superscriptiii逆转录酶。在其它一些实施例中,其可以省去。图1示出了本发明实时荧光pcr方法的一个优选实施例。该实时荧光pcr方法,通过采用一步法实时荧光rt-pcr反应缓冲液配置成荧光rt-pcr反应体系,其具有结果可靠和准确灵敏、操作简单、省时省力、降低检测成本,提高检查效率等优点,特别适合大规模样品的快速检测以及紧急疫情的快速诊断。如图1所示该实时荧光pcr方法包括以下步骤:s1、制备本发明所述的一步法实时荧光rt-pcr反应缓冲液。具体地,首先配置浓度为20~40mm的tris-hcl,浓度为100~200mm的kcl溶液,浓度为3~6mm的mgcl2溶液,浓度为20~40mm的(nh4)2so4溶液,浓度为0.07~0.14mm的dmso,浓度为2~4mm的datp、dgtp、dctp以及dttp,浓度为0.05~0.1mm的甘油,浓度为1.5×10-7~3×10-7mm的bsa,浓度为1.8×10-6~3.6×10-6mm的tween20,浓度为4.5×10-2~9×10-2mm的nan3溶液,浓度为70~140nm的roxreferencedye;并按照本发明所述的配比量取上述溶液,并置于反应容器中混合均匀,形成一步法实时荧光rt-pcr反应缓冲液。s2、向所述一步法实时荧光rt-pcr反应缓冲液中加入反转录混合酶(enzymemix)、上游引物、下游引物、水解探针、去离子水、rna模板形成荧光rt-pcr反应体系。taq聚合酶浓度优选为5u/μl;反转录混合酶的浓度优选为200u/μl;当所检测的被测物中只含有dna时,只需采用taq聚合酶,反转录混合酶可以省去;当所检测的被测物中含有rna时,则需要添加taq聚合酶和反转录混合酶。本发明配制的一步法实时荧光rt-pcr反应缓冲液(2×)所形成的反应体系如下:25μl荧光rt-pcr反应体系:s3、将所述荧光rt-pcr反应体系置于45~50℃的温度条件下进行反转录反应;具体地,将步骤2形成的荧光rt-pcr反应体系置于荧光定量pcr仪中进行反应,并控制在45~50℃的温度条件下反应15~30min。s4、将反转录反应后荧光rt-pcr反应体系置于95℃的温度条件下进行变性反应;再将其置于55~65℃的温度条件下进行退火,并于退火延伸时收集荧光信号,依次循环30~45次。具体地,置于95℃的温度条件下进行变性反应的时间为35s,在55~65℃的温度条件下进行退火的时间为40s。以下结合具体地实施例对本发明实时荧光pcr方法做进一步阐述。模板的制备:取从哈尔滨兽医研究所购置的h5n6灭活hi抗原200μl,参照magmax核酸抽提试剂盒操作说明书,于全自动核酸抽提工作站中抽提病毒rna。将抽提的模板从100连续10倍系列稀释至10-10,作为反应模板。水解探针h5-p序列:5’-fam-gggtgattatttattattgttgttgttgggytggt-3’-bhq1(seqidno:1),在其5’端带有荧光基团5’-fam(5’-羧基荧光素),3’端带有淬灭基团bhq1。上游引物h5-f序列:5’-aaattattctgagggtgattatttattattgt-3’(seqidno:2)下游引物h5-r序列:5’-atcggtagtaagcctgctaatagga-3’(seqidno:3)2)试剂浓度为1m的三羟甲基氨基甲烷-盐酸缓冲液(tris-hcl)、浓度为1m的氯化钾(kcl)、1m氯化镁(mgcl2)、浓度为3.2m的硫酸铵((nh4)2so4)、二甲基亚砜(dmso)、浓度为25mm脱氧核糖核苷三磷酸(dntps)、甘油、浓度为1.5×10-5mm的牛血清蛋白(bsa)、吐温20(tween20)、三氮化钠(nan3)和rox参比染料(roxreferencedye)均购自上海sigma-aldrich公司。耐热dna聚合酶(taq聚合酶)(5u/μl)和superscriptiii逆转录酶反转录酶(200u/μl)均购自赛默飞世尔中国公司。引物和探针由上海基康生物技术有限公司合成。商品化试剂的反应预混液,购自appliedbiosystems,成分为amplitaqgolddna聚合酶、amperaseung、dntps、rox参比染料及优化的缓冲液组分(具体可参见产品说明书)。实施例11)配置一步法实时荧光rt-pcr反应缓冲液;将tris-hcl、kcl溶液、mgcl2溶液、(nh4)2so4溶液、dmso、datp、dgtp、dctp、dttp、甘油、bsa、tween20、nan3溶液、roxreferencedye、去离子水按以下表中的浓度和配比加入反应容器中,配置100ml的一步法实时荧光rt-pcr反应缓冲液。表1:实施例1中的原料浓度及配比成分母液浓度配制100ml所用量2×反应液的终浓度tris-hcl1m2ml20mmkcl1m1ml100mmmgcl21m300μl3mm(nh4)2so43.2m625μl20mm二甲基亚砜(dmso)原液5ml0.07mmdatp100mm2ml2mmdgtp100mm2ml2mmdctp100mm2ml2mmdttp100mm2ml2mm甘油原液5ml0.05mmbsa1.5×10-5mm1ml1.5×10-7mmtween20原液200μl1.8×10-6mmnan34.5mm300μl4.5×10-2mmroxreferencedye25μm280~560μl45~70nm去离子水定容至100ml其中(2×)表示浓度浓缩为一倍2)利用本发明配制的一步法实时荧光rt-pcr反应缓冲液所形成的反应体系如下:25μl荧光rt-pcr反应体系:3)将该荧光rt-pcr反应体系置于荧光定量pcr仪中进行反应,控制在45℃的温度条件下反应20min4)将反转录反应后荧光rt-pcr反应体系置于95℃的温度条件下进行变性反应35s;再将其置于55℃的温度条件下进行退火40s,并于退火延伸时收集荧光信号,依次循环40次。实施例21)配置一步法实时荧光rt-pcr反应缓冲液;将tris-hcl、kcl溶液、mgcl2溶液、(nh4)2so4溶液、dmso、datp、dgtp、dctp、dttp、甘油、bsa、tween20、nan3溶液、roxreferencedye、去离子水按以下表中的浓度和配比加入反应容器中,配置100ml的一步法实时荧光rt-pcr反应缓冲液。表2:实施例2中的原料浓度及配比成分母液浓度配制100ml所用量2×反应液的终浓度tris-hcl1m3ml30mmkcl1m1.5ml150mmmgcl21m450μl4.5mm(nh4)2so43.2m937.5μl30mm二甲基亚砜(dmso)原液7.5ml0.105mmdatp100mm3ml3mmdgtp100mm3ml3mmdctp100mm3ml3mmdttp100mm3ml3mm甘油原液7.5ml0.075mmbsa1.5×10-5mm1.5ml2.25×10-7mmtween20原液300μl2.7×10-6mmnan34.5mm450μl6×10-2mmroxreferencedye25μm420μl105nm去离子水定容至100ml其中(2×)表示浓度浓缩为一倍2)利用本发明配制的一步法实时荧光rt-pcr反应缓冲液所形成的反应体系如下:25μl荧光rt-pcr反应体系:2×rt-pcrbuffer12.5μltaq聚合酶1μl上游引物(10μmol/ml)1μl下游引物(10μmol/ml)1μltaqman探针(5μmol/ml)1μl去离子水3.5μlrna模板5μltotal25μl3)将该荧光rt-pcr反应体系置于荧光定量pcr仪中进行反应,控制在95℃的温度条件下进行变性反应35s;再将其置于60℃的温度条件下进行退火40s,并于退火延伸时收集荧光信号,依次循环40次。实施例31)配置一步法实时荧光rt-pcr反应缓冲液;将tris-hcl、kcl溶液、mgcl2溶液、(nh4)2so4溶液、dmso、datp、dgtp、dctp、dttp、甘油、bsa、tween20、nan3溶液、roxreferencedye、去离子水按以下表中的浓度和配比加入反应容器中,配置100ml的一步法实时荧光rt-pcr反应缓冲液。表3:实施例3中的原料浓度及配比成分母液浓度配制100ml所用量2×反应液的终浓度tris-hcl1m4ml40mmkcl1m2ml200mmmgcl21m600μl6mm(nh4)2so43.2m1250μl40mm二甲基亚砜(dmso)原液10ml0.14mmdatp100mm4ml4mmdgtp100mm4ml4mmdctp100mm4ml4mmdttp100mm4ml4mm甘油原液10ml0.1mmbsa1.5×10-5mm2ml3×10-7mmtween20原液400μl3.6×10-6mmnan34.5mm600μl9×10-2mmroxreferencedye25μm560μl140nm去离子水定容至100ml其中(2×)表示浓度浓缩为一倍。2)利用本发明配制的一步法实时荧光rt-pcr反应缓冲液所形成的反应体系如下:25μl荧光rt-pcr反应体系:3)将该荧光rt-pcr反应体系置于荧光定量pcr仪中进行反应,控制在50℃的温度条件下反应30min4)将反转录反应后荧光rt-pcr反应体系置于95℃的温度条件下进行变性反应35s;再将其置于65℃的温度条件下进行退火40s,并于退火延伸时收集荧光信号,依次循环40次。对比例11)appliedbiosystems商品化实时荧光rt-pcr的反应体系。25μlrt-pcr反应体系:2×rt-pcrbuffer12.5μlenzymemix1μl上游引物(10μmol/ml)1μl下游引物(10μmol/ml)1μltaqman探针(5μmol/ml)1μl去离子水3.5μlrna模板5μltotal25μl2)实时荧光rt-pcr反应条件。55℃延伸时收集荧光信号fam。3)图2至图5示出了将实施例1以及对比例1用于实时荧光rt-pcr检测结果。在25μl本发明的一步法实时荧光rt-pcr反应缓冲液反应体系和appliedbiosystems商品化实时荧光rt-pcr反应体系中,利用针对h5n6流感病毒的特异性引物和探针进行实时荧光rt-pcr,检测含有h5n6流感病毒基因组rna的阳性样品,结果可以得到特异性的荧光曲线。图2是对比例1appliedbiosystems商品化实时荧光rt-pcr反应体系的扩增效果图,图3是本发明实施例1一步法实时荧光rt-pcr反应缓冲液反应体系检测扩增效果图。其中横坐标为循环数,纵坐标为荧光强度,曲线1-11为将抽提的h5核酸模板从100连续10倍系列稀释至10-10,图4为商品化反应体系进行实时荧光rt-pcr实验的标准曲线,其是取图2的1-8个点所制作的标准曲线图;图5为本发明的反应体系的实时荧光rt-pcr实验的标准曲线,其是取图3的1-8个点所制作的标准曲线图。其中横坐标为样品起始浓度logod值,纵坐标为ct值。如图4所示,商品化反应体系进行实时荧光rt-pcr实验的标准曲线的斜率为-2.483995,相关系数为0.989357(介于0.95~1.05之间),说明存在良好的线性关系。如图5所示,本发明反应体系进行实时荧光rt-pcr实验的标准曲线的斜率为-2.820370,相关系数为0.988249(介于0.95~1.05之间),说明存在良好的线性关系,则本发明反应体系进行实时荧光rt-pcr实验,其能够达到商品话反应体系所进行的实时荧光rt-pcr实验效果。对比例2本发明实施例1制得的一步法实时荧光rt-pcr反应缓冲液配置为实时荧光rt-pcr反应体系,以及appliedbiosystems商品化实时荧光rt-pcr的反应体系分别用于检测检测肠道病毒通用型、柯萨奇病毒a组16型和肠道病毒71型;模板、探针和引物模板的制备:1)合成并纯化的含肠道病毒通用型(eu)、柯萨奇病毒a组16型(ca16)和肠道病毒71型(ev71)的体外转录rna,通过紫外分光光度计测定浓度,计算rna拷贝数,并将rna用去离子稀释至5×102copies/ml标准品进行检测。1、水解探针eu-p序列:5'-cy5-cctccggcccctgaatgcg-3'-bhq2(seqidno:1),在其5’端带有荧光基团5’-cy5(5’-羧基荧光素),3’端带有淬灭基团bhq2。上游引物eu-f序列:5'-ggtgygaagagyctaytgagcta-3'(seqidno:2)。下游引物eu-r序列:5'-caaagtagtcggttccgc-3'(seqidno:3)。2、水解探针ca16-p序列:5'-fam-taccagcactrcaagcygcggag-3'-bhq1(seqidno:1),在其5’端带有荧光基团5’-fam(5’-羧基荧光素),3’端带有淬灭基团bhq1。上游引物ca16-f序列:5'-caagtaytacctacrgctgccaa-3'(seqidno:2)。下游引物ca16-r序列:5'-caacacacatctmgtctcaatgag-3'(seqidno:3)。3、水解探针ev71-p序列:5'-vic-tggatacctcgbccratgcgcaa-3'-bhq1(seqidno:1),在其5’端带有荧光基团5’-vic(5’-羧基荧光素),3’端带有淬灭基团bhq1。上游引物ev71-f序列:5'-atrgccccagaytgctgacc-3'(seqidno:2)。下游引物ev71-r序列:5'-caacacacatctmgtctcaatgag-3'(seqidno:3)。1)采用本发明实施例1配制的一步法实时荧光pcr反应缓冲液,配制25μl实时荧光pcr反应体系。实时荧光rt-pcr反应条件。55℃延伸时收集荧光信号fam、vic、cy5。2)appliedbiosystems商品化实时荧光rt-pcr的反应体系。25μlrt-pcr反应体系2×rt-pcrbuffer12.5μlenzymemix1μl上游引物ca16-f(50μmol/ml)0.2μl下游引物ca16-r(50μmol/ml)0.2μltaqman探针ca16-p(50μmol/ml)0.1μl上游引物ev71-f(50μmol/ml)0.2μl下游引物ev71-r(50μmol/ml)0.2μltaqman探针ev71-p(50μmol/ml)0.1μl上游引物eu-f(50μmol/ml)0.2μl下游引物eu-r(50μmol/ml)0.2μltaqman探针eu-p(50μmol/ml)0.1μl去离子水5μlrna模板5μltotal25μl实时荧光rt-pcr反应条件。55℃延伸时收集荧光信号fam、vic、cy5。3)图6及图7示出了将本实施例1以及对比例2用于实时荧光rt-pcr检测结果。在25μl本发明的一步法实时荧光rt-pcr反应缓冲液反应体系和appliedbiosystems商品化实时荧光rt-pcr试剂盒反应体系中,利用针对肠道病毒通用型、柯萨奇病毒a组16型和肠道病毒71型的特异性引物和探针进行实时荧光rt-pcr,检测含有肠道病毒通用型、柯萨奇病毒a组16型和肠道病毒71型基因组rna的阳性标准品,结果如图6及图7所示,本发明的反应缓冲液及反应体系扩增效果较商品化好,有明显的特异性的荧光曲线,曲线较平滑。注:其中曲线1-6分别为:1:柯萨奇病毒a组16型标准品;2:肠道病毒71型标准品;3:肠道病毒通用型标准品;4:柯萨奇病毒a组16型阴性对照;5:肠道病毒71型阴性对照;6:肠道病毒通用型阴性对照。检测实施例1:本发明实时荧光pcr反应缓冲溶液检测转基因dna。2)模板、探针和引物模板的制备:购置转基因大豆标准品,参照国家标准《转基因产品检测-核酸提取纯化方法》(gb/t19495.3-2004)方法抽提基因组dna,按照《转基因产品检测-核酸定量pcr检测方法》(gb/t19495.5-2004)方法进行转基因gts-40-3-2定量检测。水解探针序列:5'-fam-cgcaaccgcccgcaaatcc-3'-bhq1(seqidno:1),在其5’端带有荧光基团5’-fam(5’-羧基荧光素),3’端带有淬灭基团bhq1。上游引物:5'-cctttaggatttcagcatcagtgg-3'(seqidno:2)下游引物:5'-gacttgtcgccgggaatg-3'(seqidno:3)2)采用本发明实施例2配制的一步法实时荧光pcr反应缓冲液,配制25μl实时荧光pcr反应体系。25μl实时荧光pcr反应体系2×rt-pcrbuffer12.5μltaq聚合酶1μl(5u)上游引物(10μmol/ml)1μl下游引物(10μmol/ml)1μltaqman探针(5μmol/ml)1μl去离子水3.5μldna模板5μltotal25μl实时荧光pcr反应条件。60℃延伸时收集荧光信号fam。3)实时荧光pcr定量检测结果如图8所示如图8所示,在25μl本发明的一步法实时荧光pcr反应缓冲液反应体系中,利用针对转基因大豆gts-40-3-2的定量检测,可达到标准要求的检测底限20拷贝。注:其中横坐标为循环数,纵坐标为荧光强度,曲线1-9为转基因大豆gts-40-3-2核酸模板从2×108copies/ml~2×100copies/ml连续10倍的标准品。检测实施例2:本发明实施例3实时荧光rt-pcr反应缓冲溶液检测甲型h1n1流感病毒。1)模板、探针和引物模板的制备:合成并纯化的甲型h1n1流感病毒基因的体外转录rna,通过紫外分光光度计测定浓度,计算rna拷贝数,并将rna用去离子水按100倍稀释法稀释至1×100copies/ml,取1×108copies/ml~1×100copies/ml标准品进行检测。水解探针序列:5’-fam-ccgagatatgckttcgcaatgga-3’-bhq1(seqidno:1),在其5’端带有荧光基团5’-fam(5’-羧基荧光素),3’端带有淬灭基团bhq1。上游引物:5'-cctttaggatttcagcatcagtgg-3'(seqidno:2)下游引物:5’-gtrttrcaatcgtggactgg-3’(seqidno:3)2)采用本发明配制的一步法实时荧光rt-pcr反应缓冲液,配制25μl实时荧光rt-pcr反应体系。25μl实时荧光pcr反应体系实时荧光pcr反应条件。65℃延伸时收集荧光信号fam。3)实时荧光pcr定量检测结果如图9如图9所示,在25μl本发明的一步法实时荧光rt-pcr反应缓冲液反应体系中,利用针对甲型h1n1流感病毒核酸标准品定量检测,可达到标准要求的检测底限100拷贝。注:其中横坐标为循环数,纵坐标为荧光强度,曲线1-5为将抽提的甲型h1n1流感病毒核酸模板从1×108copies/ml~1×100copies/ml连续100倍的标准品。可以理解的,以上实施例仅表达了本发明的优选实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制;应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,可以对上述技术特点进行自由组合,还可以做出若干变形和改进,这些都属于本发明的保护范围;因此,凡跟本发明权利要求范围所做的等同变换与修饰,均应属于本发明权利要求的涵盖范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1