一种宝乐果单体、提取物及其制备方法和应用与流程
本发明属于天然药物化学领域,具体涉及一种宝乐果中单体化合物、提取物及其制备方法和应用。
背景技术:
宝乐果是茜草科林果属植物borojoapatinoicuatrec和borojoasorbiliscuatrec的成熟果实。分布在亚马逊河流域厄瓜多尔热带雨林,原产于哥伦比亚、厄瓜多尔和巴拿马。宝乐果富含果糖和葡萄糖,水溶性的b族维生素,氨基酸和蛋白质,极具开发利用价值。当地土著居民认为食用宝乐果能够消除疲劳、增强免疫、壮阳、改善呼吸道炎症症状及抗炎。文献报道宝乐果具有抗氧化(国际药学研究杂志,2013:817-821)和降血糖活性,也有文献报道宝乐果中的多糖成分能够增强免疫力,但目前未见文献报道宝乐果中单体化合物的抗炎、抗氧化及降血糖作用。
技术实现要素:
本发明的目的在于提供一种宝乐果提取物及其单体化合物的制备方法及用途。
本发明的目的通过下述技术方案实现:
宝乐果提取物及其单体化合物,具体制备步骤如下:
(1)宝乐果粉用水混悬后,过滤,滤液通过大孔树脂吸附,可选用ab-8、d101、d102、ztc-1或1300-i型大孔树脂;
(2)用水或10%以下乙醇洗脱除去杂质,再用20%-80%乙醇水洗脱,收集洗脱液,浓缩至干;即得宝乐果提取物
(3)将宝乐果提取物经硅胶柱层析(石油醚-乙酸乙酯梯度洗脱,100:0→0:100),经tlc分析并合并成分相似的流分,得到10个主流分(fr.1~fr.10)。fr.4经中低压ods柱层析,甲醇-水梯度洗脱(90:10→100:0),得到7个亚流分(fr.4a~fr.4g)。其中fr.4c、fr.4d和fr.4e分别经sephadexlh-20凝胶柱层析、制备型hplc及重结晶得到化合物宝乐果酸-1、宝乐果酸-2、宝乐果酸-7、宝乐果酸-10。fr.6经中低压ods柱层析,甲醇-水梯度洗脱(95:5→100:0)得到6个亚流分(fr.6a~fr.6f)。fr.6c和fr.6d分别经sephadexlh-20凝胶柱层析及制备型hplc得到化合物宝乐果酸-8、宝乐果酸-9。fr.7经中低压ods柱层析,甲醇-水梯度洗脱(95:5→100:0)得到8个亚流分(fr.7a~7j)。fr.7d、fr.7e和fr.7f分别经sephadexlh-20凝胶柱
本发明宝乐果提取物成分分析:上述的宝乐果提取物中的主要成分已进行了结构鉴定,明确其主要成分为11个新化合物和2个已知的环烯醚萜苷,其化学式为:
本发明还提供宝乐果提取物或单体作为制备抗炎或降血糖药物的用途。
本发明还提供宝乐果提取物或单体作为制备抗氧化/防衰老或降血糖类功能性食品的用途。
本发明还提供一种宝乐果的宝乐果酸提取物,其包含以下化合物:
该提取物还进一步包括以下化合物:
本发明还提供一种宝乐果的宝乐果酸提取物,包括以下制备步骤:
取新鲜的宝乐果为原料,加水混匀磨浆或取宝乐果冻干粉加水混匀,过滤,滤液加乙酸乙酯萃取,合并乙酸乙酯层,减压浓缩至干得宝乐果的宝乐果酸提取物。
本发明的宝乐果是来源于茜草科林果属植物borojoapatinoicuatrec和borojoasorbiliscuatrec的成熟果实。
附图说明
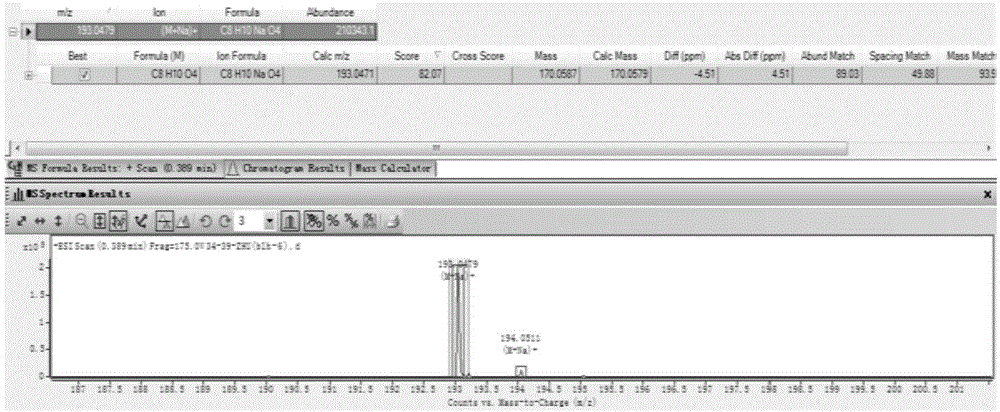
图1宝乐果酸-1的高分辨质谱图
图2宝乐果酸-1的核磁共振氢谱
图3宝乐果酸-1的核磁共振碳谱
图4宝乐果酸-2的高分辨质谱图
图5宝乐果酸-2的核磁共振氢谱
图6宝乐果酸-2的核磁共振碳谱
图7宝乐果酸-3的高分辨质谱图
图8宝乐果酸-3的核磁共振氢谱
图9宝乐果酸-3的核磁共振碳谱
图10宝乐果酸-4的高分辨质谱图
图11宝乐果酸-4的核磁共振氢谱
图12宝乐果酸-4的核磁共振碳谱
图13宝乐果酸-5的高分辨质谱图
图14宝乐果酸-5的核磁共振氢谱
图15宝乐果酸-5的核磁共振碳谱
图16宝乐果酸-6的高分辨质谱图
图17宝乐果酸-6的核磁共振氢谱
图18宝乐果酸-6的核磁共振碳谱
图19宝乐果酸-7的高分辨质谱图
图20宝乐果酸-7的核磁共振氢谱
图21宝乐果酸-7的核磁共振碳谱
图22宝乐果酸-8的高分辨质谱图
图23宝乐果酸-8的核磁共振氢谱
图24宝乐果酸-8的核磁共振碳谱
图25宝乐果酸-9的高分辨质谱图
图26宝乐果酸-9的核磁共振氢谱
图27宝乐果酸-9的核磁共振碳谱
图28宝乐果酸-10的高分辨质谱图
图29宝乐果酸-10的核磁共振氢谱
图30宝乐果酸-10的核磁共振碳谱
图31宝乐果酸-11的高分辨质谱图
图32宝乐果酸-11的核磁共振氢谱
图33宝乐果酸-11的核磁共振碳谱
图34宝乐果酸-1的单晶x衍射结构
图35宝乐果酸-12的单晶x衍射结构
具体实施方式
下面结合实施例及附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。
实施例1宝乐果提取物的制备
取新鲜的宝乐果50kg,去皮和种子,果肉加水200l搅拌,磨浆混匀,过滤。果渣再加入100l水搅拌,磨浆混匀,过滤。
合并两次滤液,加300l的乙酸乙酯萃取,分取乙酸乙酯层。水层加300l乙酸乙酯,分取乙酸乙酯层。水层再加300l乙酸乙酯萃取,分取乙酸乙酯层。
合并3次乙酸乙酯层,减压浓缩至干,得宝乐果提取物650g。
实施例2宝乐果提取物的制备
取宝乐果粉5kg,加水50l搅拌,混匀,过滤。滤渣再加入50l水搅拌,混匀,过滤。
合并两次滤液,加100l的乙酸乙酯萃取,分取乙酸乙酯层。水层每次加100l乙酸乙酯再萃取3次,每次分取乙酸乙酯层。
合并4次乙酸乙酯层,减压浓缩至干,得宝乐果提取物480g。
实施例3化合物制备与结构鉴定
宝乐果提取物500g加入甲醇复溶,用80-100目的硅胶拌样后,经200-300目的硅胶柱层析,依次用95:5、90:10、85:115、80:20、75:25、70:30、60:40、50:50、0:100的石油醚-乙酸乙酯梯度洗脱,根据tlc检测,合并薄层斑点相类似的流分,得到fr.1-fr.9共9个组分。
fr.4经中低压ods柱层析,甲醇-水梯度洗脱(90:10→100:0),得到7个亚流分(fr.4a~fr.4g)。其中fr.4c、fr.4d和fr.4e分别经sephadexlh-20、pre-hplc及重结晶得到化合物宝乐果酸1(171mg)、宝乐果酸2(163mg)、宝乐果酸7(201mg)和宝乐果酸10(167mg)。
fr.6经中低压ods柱层析,甲醇-水梯度洗脱(95:5→100:0)得到6个亚流分(fr.6a~fr.6f)。fr.6c和fr.6d分别经sephadexlh-20、pre-hplc得到化合物宝乐果酸8(195mg)和宝乐果酸9(218mg)。
fr.7(2.5g)经中低压ods柱层析,甲醇-水梯度洗脱(95:5→100:0)得到8个亚流分(fr.7a~7j)。fr.7d、fr.7e和fr.7f分别经sephadexlh-20、pre-hplc得到化合物宝乐果酸3(146mg)、宝乐果酸4(160mg)、宝乐果酸5(185mg)、宝乐果酸6(260mg)、宝乐果酸11(136mg)、宝乐果酸12(564mg)和宝乐果酸13(428mg)。
宝乐果酸-1((1r,5s)-5-methylcyclopent-2-ene-1,2-dicarboxylicacid)无色细针状晶体,化学结构式为:
光谱数据如下:hr-esi-msm/z193.0479[m+na]+,esi-ms如图1所示。1hnmr(cd3od,400mhz)δ:1.19(3h,d,j=6.5hz,h-8),2.16(1h,ddt,j=18.5,5.5,2.5hz,h-4a),2.81(1h,ddt,j=18.5,8.0,2.5hz,h-4b),2.57(1h,m,h-1),3.26(1h,qd,j=5.7,2.0hz,h-5),6.83(1h,dd,j=4.5,2.4hz,h-3),核磁共振氢谱如图2所示。13cnmr(cd3od,100mhz)δ:21.4(c-8),40.1(c-5),41.7(c-4),58.8(c-1),136.4(c-2),146.4(c-3),167.9(c-7),178.2(c-6),核磁共振碳谱如图3所示。通过单晶x衍射法对宝乐果酸-1的绝对构型进行了确定,见图34。
根据以上光谱数据鉴定宝乐果酸-1为一新的环戊烯类化合物并命名为(1r,5s)-5-methylcyclopent-2-ene-1,2-dicarboxylicacid。
宝乐果酸-2((1s,5s)-5-methylcyclopent-2-ene-1,2-dicarboxylicacid)白色无定形粉末,化学结构式为:
光谱数据如下:hr-esi-ms:m/z193.0479[m+na]+,esi-ms如图4所示。1hnmr(cd3od,500mhz)δ:1.10(3h,d,j=7.1hz,h-8),2.25(1h,ddt,j=18.0,8.2,2.4hz,h-4a),2.65(1h,ddd,j=18.0,8.1,2.8hz,h-4b),2.78(1h,dq,j=16.1,7.1hz,h-5),3.64(1h,d,j=9.3hz,h-1),6.92(1h,brs,h-3),核磁共振氢谱如图5所示。13cnmr(cd3od,125mhz)δ:16.6(c-8),37.1(c-5),41.6(c-4),54.7(c-1),136.9(c-2),148.1(c-3),167.8(c-7),176.3(c-6),核磁共振碳谱如图6所示。
根据以上光谱数据鉴定宝乐果酸-2为一新的环戊烯类化合物并命名为(1s,5s)-5-methylcyclopent-2-ene-1,2-dicarboxylicacid。
宝乐果酸-3((1r,5r)-5-(carboxymethyl)cyclopent-2-ene-1,2-dicarboxylicacid)黄色油状物,化学结构式为:
光谱数据如下:hr-esi-ms:m/z237.0377[m+na]+,esi-ms如图7所示。1hnmr(cd3od,400mhz)δ:2.31(1h,dt,j=13.1,2.3hz,h-4b),2.48(1h,dd,j=16.0,8.3hz,h-8b),2.61(1h,dd,j=16.0,5.6hz,h-8a),2.86(1h,m,h-5),2.93(1h,dt,j=8.3,2.5hz,h-4a),3.44(1h,m,h-1),6.85(1h,m,h-3),核磁共振氢谱如图8所示。13cnmr(cd3od,100mhz)δ:39.7(c-4),40.3(c-8),41.2(c-5),56.5(c-1),136.1(c-2),146.2(c-3),167.5(c-7),175.6(c-9),177.6(c-6),核磁共振碳谱如图9所示。
根据以上光谱数据鉴定宝乐果酸-3为一新的环戊烯类化合物并命名为(3r,4r)-4-(carboxymethyl)cyclopent-1-ene-1,3-dicarboxylicacid。
宝乐果酸-4((1r,5s)-5-(carboxymethyl)cyclopent-2-ene-1,2-dicarboxylicacid)棕色无定形粉末,化学结构式为:
光谱数据如下:hr-esi-ms:m/z237.0377[m+na]+,esi-ms如图10所示。1hnmr(cd3od,400mhz)δ:2.33(1h,dd,j=18.0,9.4hz,h-4b),2.42(1h,dd,j=16.6,8.6hz,h-8b),2.57(1h,dd,j=16.6,6.9hz,h-8a),2.74(1h,ddd,j=18.0,8.1,2.8hz,h-4a),3.05(1h,m,h-5),3.75(1h,d,j=9.0hz,h-1),6.95(1h,brs,h-3),核磁共振氢谱如图11所示。13cnmr(cd3od,100mhz)δ:36.7(c-8),39.0(c-5),39.5(c-4),53.5(c-1),137.5(c-2),147.5(c-3),167.5(c-7),175.7(c-9),175.8(c-6),核磁共振碳谱如图12所示。
根据以上光谱数据鉴定宝乐果酸-4为一新的环戊烯类化合物并命名为(1r,5s)-5-(carboxymethyl)cyclopent-2-ene-1,2-dicarboxylicacid。
宝乐果酸-5((1r,5r)-5-(2-methoxy-2-oxoethyl)cyclopent-2-ene-1,2-dicarboxylicacid)黄色油状物,化学结构式为:
光谱数据如下:hr-esi-ms:m/z251.0520[m+na]+,esi-ms如图13所示。1hnmr(cd3od,400mhz)δ:2.31(1h,m,h-4b),2.50(1h,dd,j=16.0,7.7hz,h-8b),2.57(1h,dd,j=16.0,6.0hz,h-8a),2.84(1h,m,h-5),2.86(1h,m,h-4a),3.48(1h,m,h-1),3.68(3h,s,h-10),6.86(1h,brs,h-3),核磁共振氢谱如图14所示。13cnmr(cd3od,100mhz)δ:39.7(c-4),40.1(c-8),41.4(c-5),52.6(c-10),56.5(c-1),136.1(c-2),146.4(c-3),167.2(c-7),175.5(c-6),176.3(c-9),核磁共振碳谱如图15所示。
根据以上光谱数据鉴定宝乐果酸-5为一新的环戊烯类化合物并命名为(1r,5r)-5-(2-methoxy-2-oxoethyl)cyclopent-2-ene-1,2-dicarboxylicacid。
宝乐果酸-6((1s,5r)-5-(2-methoxy-2-oxoethyl)cyclopent-2-ene-1,2-dicarboxylicacid)棕黄色无定形粉末,化学结构式为:
光谱数据如下:hr-esi-ms:m/z251.0520[m+na]+,esi-ms如图16所示。1hnmr(cd3od,300mhz)δ:2.32(1h,ddt,j=18.0,9.4,2.4hz,h-4b),2.54(2h,qd,j=16.6,7.8hz,h-8),2.73(1h,ddd,j=18.0,8.1,3.0hz,h-4a),3.07(1h,m,h-5),3.68(3h,s,h-10),3.74(1h,dd,j=9.3,1.5hz,h-1),6.94(1h,brs,h-3),核磁共振氢谱如图17所示。13cnmr(cd3od,75mhz)δ:36.6(c-8),39.0(c-5),39.3(c-4),52.1(c-10),53.5(c-1),137.3(c-2),147.1(c-3),167.5(c-7),174.2(c-9),175.7(c-6),核磁共振碳谱如图18所示。
根据以上光谱数据鉴定宝乐果酸-6为一新的环戊烯类化合物并命名为(1s,5r)-5-(2-methoxy-2-oxoethyl)cyclopent-2-ene-1,2-dicarboxylicacid。
宝乐果酸-7((1r,5s)-1-methoxycarbonyl-5-methylcyclopent-2-enecarboxylicacid)黄色油状物,化学结构式为:
光谱数据如下:hr-esi-ms:m/z207.0635[m+na]+,esi-ms如图19所示。1hnmr(cd3od,500mhz)δ:1.18(3h,d,j=6.0hz,h-8),2.16(1h,ddt,j=18.4,5.8,2.3hz,h-4b),2.53(1h,m,h-5),2.81(1h,ddt,j=18.4,8.2,2.5hz,h-4),3.30(1h,m,h-1),3.68(3h,s,h-9),6.83(1h,dd,j=4.2,2.4hz,h-3),核磁共振氢谱如图20所示。13cnmr(cd3od,125mhz)δ:21.3(c-8),40.2(c-5),41.8(c-4),52.5(c-9),53.8(c-1),136.7(c-2),146.4(c-3),168.4(c-7),176.8(c-6),核磁共振碳谱如图21所示。
根据以上光谱数据鉴定宝乐果酸-7为一新的环戊烯类化合物并命名为(1r,5s)-1-methoxycarbonyl-5-methylcyclopent-2-enecarboxylicacid。
宝乐果酸-8(tans-2-oxo-3,3a,4,6a-tetrahydro-2h-cyclopenta[b]furan-5-carboxylicacid)淡黄色无定形粉末,化学结构式为:
光谱数据如下:hr-esi-ms:m/z191.0316[m+na]+,esi-ms如图22所示。1hnmr(cd3od,500mhz)δ:2.56(1h,ddt,j=19.0,4.0,2.5hz,h-4′),2.95(1h,dddd,j=19.0,9.0,2.5,1.5hz,h-4″),3.47(1h,m,h-3a),3.95(1h,ddd,j=9.0,4.2,1.8hz,h-6a),4.05(1h,dd,j=9.5,5.0hz,h-3′),4.56(1h,dd,j=9.5,8.0hz,h-3″),6.83(1h,dd,j=4.5,2.4hz,h-6),核磁共振氢谱如图23所示。13cnmr(cd3od,125mhz)δ:39.8(c-4),40.2(c-3a),51.4(c-6a),74.7(c-3),134.6(c-5),146.2(c-6),166.7(c-7),178.1(c-1),核磁共振碳谱如图24所示。
根据以上光谱数据鉴定宝乐果酸-8为一新的稠环化合物并命名为tans-2-oxo-3,3a,4,6a-tetrahydro-2h-cyclopenta[b]furan-5-carboxylicacid。
宝乐果酸-9(cis-2-oxo-3,3a,4,6a-tetrahydro-2h-cyclopenta[b]furan-5-carboxylicacid)黄色油状物,化学结构式为:
光谱数据如下:hr-esi-ms:m/z191.0318[m+na]+,esi-ms如图25所示。1hnmr(cd3od,500mhz)δ:2.43(1h,dd,j=18.5,4.2hz,h-3′),2.49(1h,m,h-4),2.96(1h,dd,j=18.5,10.5hz,h-3″),3.31(1h,m,h-3a),2.97(1h,ddd,j=19.6,8.8,2.4hz,h-4),5.69(1h,dd,j=7.5,2.1hz,h-6a),7.10(1h,t,j=2.4hz,h-5),核磁共振氢谱如图26所示。13cnmr(cd3od,125mhz)δ:36.3(c-3),37.1(c-3a),40.5(c-4),89.2(c-6a),136.3(c-6),151.0(c-5),166.6(c-7),179.6(c-2),核磁共振碳谱如图27所示。
根据以上光谱数据鉴定宝乐果酸-9为一新的稠环化合物并命名为cis-2-oxo-3,3a,4,6a-tetrahydro-2h-cyclopenta[b]furan-5-carboxylicacid。
宝乐果酸-10(cis-3,3a,4,6a-tetrahydro-2h-cyclopenta[b]furan-6-carboxylicacid)黄色无定形粉末,化学结构式为:
光谱数据如下:hr-esi-ms:m/z177.0529[m+na]+,esi-ms如图28所示。1hnmr(cd3od,500mhz)δ:1.68(1h,m,h-3′),2.07(1h,m,h-3″),2.81(1h,ddd,j=19.6,8.8,2.2hz,h-4′),2.32(1h,m,h-4),3.05(1h,m,h-3a),3.56(1h,m,h-2′),3.81(1h,m,h-2″),5.22(1h,d,j=6.0hz,h-6a),6.87(1h,t,j=2.4hz,h-5),核磁共振氢谱如图29所示。13cnmr(cd3od,125mhz)δ:35.7(c-3),40.1(c-4),41.3(c-3a),67.1(c-2),88.0(c-6a),137.2(c-6),148.1(c-5),168.3(c-7),核磁共振碳谱如图30所示。
根据以上光谱数据鉴定宝乐果酸-10为一新的稠环类化合物并命名为cis-3,3a,4,6a-tetrahydro-2h-cyclopenta[b]furan-6-carboxylicacid。
宝乐果酸-11(bicyclo[3.1.0]hex-3-ene-1,3-dicarboxylicacid)黄色油状物,化学结构式为:
光谱数据如下:m/z191.0316[m+na]+,esi-ms如图31所示。1hnmr(cd3od,500mhz)δ:0.67(1h,t,j=5.0hz,h-6′),1.84(1h,dd,j=8.5,4.2hz,h-6″),2.19(1h,m,h-5),2.50(1h,dd,j=19.7,2.0hz,h-2′),2.84(1h,ddd,j=19.7,7.0,2.0hz,h-2″),6.43(1h,m,h-4),核磁共振氢谱如图32所示。13cnmr(cd3od,125mhz)δ:24.1(c-6),29.7(c-5),35.9(c-2),37.4(c-1),140.1(c-3),143.1(c-4),167.4(c-8),175.7(c-7),核磁共振碳谱如图33所示。
以上光谱数据与文献(prinzbachh,etal.chemischeberichte,1965,98(7):2201-2220)报道一致,故鉴定宝乐果酸-11为bicyclo[3.1.0]hex-3-ene-1,3-dicarboxylicacid。
宝乐果酸-12(ixoside)淡黄色针状晶体,化学结构式为:
光谱数据如下:hr-esi-msm/z411.0903[m+na]+。1hnmr(cd3od,300mhz)δ:2.45(1h,brd,j=18.6hz,h-6b),2.95(1h,dd,j=18.6,8.1hz,h-6a),3.22(2h,m,h-5,h-9),5.67(1h,d,j=5.1hz,h-1),6.93(1h,m,h-7),7.51(1h,s,h-3),3.22(1h,m,h-2′),3.34(1h,m,h-4′),3.36(1h,m,h-5′),3.37(1h,m,h-3′),3.71(1h,m,h-6′),3.87(1h,d,j=11.4hz,h-6′)和4.65(1h,d,j=7.8hz,h-1′)。13cnmr(cd3od,75mhz)δ:35.0(c-5),40.1(c-6),47.2(c-9),96.3(c-1),112.4(c-4),136.1(c-8),147.8(c-7),153.6(c-3),168.1(c-10),170.5(c-11),62.5(c-6′),71.2(c-4′),74.4(c-2′),77.6(c-5′),78.0(c-3′)和100.2(c-1′)。通过单晶x衍射法对宝乐果酸-12的绝对构型进行了确定,见图35。
以上光谱数据与文献(yoshiot,etal.chemicalpharmaceuticalbulletin,1976,24(6):1216-1218)报道一致,故鉴定宝乐果酸-12为ixoside。
宝乐果酸-13黄色油状物,化学结构式为:
光谱数据如下:hr-esi-ms:m/z415.1218[m+na]+。1hnmr(cd3od,400mhz)δ:1.28(1h,s,h-10),1.85(1h,dd,j=13.2,6.0hz,h-7a),2.05(1h,dd,j=13.2,6.8hz,h-7b),2.62(1h,dd,j=10.0,2.4hz,h-9),2.97(1h,dd,j=10.0,3.2hz,h-5),5.57(1h,d,j=2.4hz,h-1),7.42(1h,s,h-3),3.19(1h,m,h-2′),3.27(1h,m,h-4′),3.33(1h,m,h-5′),3.38(1h,m,h-3′),3.65(1h,d,j=12.0,1.6hz,h-6′a),3.87(1h,d,j=12.0,6.0hz,h-6′b)和4.66(1h,d,j=8.0hz,h-1′)。13cnmr(cd3od,100mhz)δ:24.8(c-10),41.4(c-5),49.1(c-7),51.4(c-9),77.7(c-6),79.0(c-8),94.8(c-1),111.6(c-4),152.6(c-3),171.3(c-11),62.9(c-6′),71.7(c-4′),74.5(c-2′),78.0(c-3′),78.3(c-5′)和99.8(c-1′)。
以上光谱数据与文献(masateruo,etal.chemicalpharmaceuticalbulletin,2007,55(4):632-634)报道一致,故鉴定宝乐果酸-13为shanzhiside。
实施例4体外抗氧化实验
1.材料和方法
1.1材料:
待测样品:实施例1制备得到的宝乐果提取物及13种单体化合物,标准抗氧化剂维生素c。
试剂:abts(2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐)、dpph(二苯基苦基苯肼)购自sigma公司。其他试剂为国产分析纯。
1.2对dpph的自由基的清除作用
dpph·一种稳定的以氮为中心的自由基,在517nm处有强吸收。当反应系统中存在抗氧化剂时,它可以和dpph·的单电子配对而使517nm处的吸收峰渐渐消退,吸光度值下降。而且,这种下降的程度与自由基被清除的程度呈定量关系。
取dpph0.0246g溶于约100ml溶剂甲醇中,超声5min,充分振摇,务使上下各部分均匀。将样品用甲醇配制成一系列浓度,取0.1ml的样品溶液加入2mldpph甲醇溶液,混匀,30min后测定其在515nm处的吸光度;同法以甲醇替代样品测定空白对照的吸光度值。每份样品平行操作3次,取平均值计算。
dpph清除率(%)=[(a空白-a样品)/a空白]×100%
ic50:半抑制量,表示清除50%自由基或抑制50%的氧化作用所需要的样品浓度,该值常用来表示抗氧化活性大小。
1.3对abts+清除能力测定
abts经活性氧氧化后生成稳定的蓝绿色阳离子自由基abts·+,当向其中加入抗氧化剂,该物质会与abts·+发生反应而使反应体系颜色褪去,即吸光度值会下降,下降的程度可反映抗氧化剂的抗氧化能力。
将0.4ml的7.4mmol/labts和1.43ml的2.6mmol/l过硫酸钾混合,于室温、避光的条件下反应,静置过夜,最终形成abts+自由基储备液。将样品用甲醇配制成一系列浓度,取0.2ml的样品溶液加入0.8mlabts+自由基工作液,均匀振荡10s,30℃水浴反应10min,测定其在734nm处的吸光度值;同法以甲醇替代样品测定空白对照的吸光度值。每份样品平行操作3次,取平均值计算。
abts清除率(%)=[(a空白-a样品)/a空白]×100%
ic50:半抑制量,表示清除50%自由基或抑制50%的氧化作用所需要的样品浓度,该值常用来表示抗氧化活性大小。
1.4对超氧自由基的清除作用
利用邻苯三酚在碱性环境中发生自氧化链式反应并释放出大量的·o2-,·o2-又进一步加速邻苯三酚的氧化,生成一系列在可见光区有特征吸收的中间产物。而若在反应体系中加入抗氧化物质可降低邻苯三酚的自氧化速率,清除产生的·o2-,抑制中间产物的生成,使反应溶液在320nm处的吸光度减小,减小的程度可反映抗氧化剂的抗氧化能力。
将样品用甲醇配制成一系列浓度,取0.2ml的样品溶液加入一定浓度的样品溶液4ml,0.1mol/ltris-hcl缓冲溶液(ph=8.2)4.5ml,在25℃水浴20min后,加入0.2ml3mmol/l邻苯三酚溶液,混匀后于25℃水浴中反应5min,加入1mol/lhcl终止反应,于325nm处测定吸光度;同法以蒸馏水替代样品测定空白对照的吸光度值。
清除率(%)=[(a空白-a样品)/a空白]×100%
ic50:半抑制量,表示清除50%自由基或抑制50%的氧化作用所需要的样品浓度,该值常用来表示抗氧化活性大小。
2.统计学处理
实验结果以
3.结果
采用ic50值来评估宝乐果提取物及13种单体化合物的抗氧化活性。抗氧化结果见下表。
表1宝乐果提取物及其单体化合物的抗氧化活性
由上表可知,与维生素c相比,单体化合物均表现出良好的抗氧化活性,且活性均好于宝乐果提取物。
实施例5抗炎实验
样品:实施例1和实施例3所制的宝乐果提取物及13种单体化合物
1.实验方法
利用脂多糖(lps)刺激raw264.7细胞,建立体外炎症模型,探讨了宝乐果提取物及14种单体化合物对炎症因子tnf-α产生的影响,具体操作如下:
(1)细胞培养:raw264.7细胞培养于含10%胎牛血清、青霉素100u/ml、链霉素100u/ml的dmem培养基中,在37℃、5%co2条件下传代培养。细胞生长至70~80%融合后进行传代,1~2天换液一次,4~6天传代一次。
(2)将raw264.7细胞悬液按1×105/ml、100μl/孔接种于96孔板内,置于37℃,5%co2培养箱中培养12h,加入不同浓度的待测样品,每个浓度的样品平行接种4孔,置于37℃继续培养24h后,加入100ng/ml的lps,再继续培养9小时,每孔取200μl上清液,按tnf-αelisa试剂盒操作方法检测tnf-α的含量。同时,设立lps对照组。
2.统计学处理
实验结果以
3.结果
结果见下表。
表2.宝乐果提取物及其单体化合物对lps致raw264.7细胞tnf-α炎症因子产生的抑制作用
与lps单独作用组相比,**p<0.01;***p<0.001。
由上表可知,与宝乐果提取物相比,单体化合物均表现出良好的抗炎活性。
实施例6降血糖实验
样品:实施例1和实施例3所制的宝乐果提取物及13种单体化合物
1.实验方法
将170只icr雄性小鼠(6周龄,体重30~35g)随机分为正常对照组10只和糖尿病模型组160只,正常组给予基础饲料,模型组给予高脂饲料。喂养4周,禁食12h,按100mg/kg(溶剂为柠檬酸-柠檬酸钠缓冲液,ph=4.5)腹腔注射链脲佐菌素,3天后测小鼠2h葡萄糖耐受量,筛选血糖值大于11.1mmol/ml的小鼠为造模成功的小鼠。将成模的小鼠随机分为1组模型组和14组实验组。实验组每天按照2mg/kg口服灌胃给药1次,连续2周。实验结束后,检测隔夜禁食小鼠空腹血糖值和空腹体重。
2.统计学处理
实验结果以
3.结果
实验结果见下表:
表3.宝乐果提取物及单体化合物降血糖作用
与正常组相比,##p<0.01;###p<0.001;与模型组相比,*p<0.05;**p<0.01;**p<0.001。
由上表可知,与宝乐果提取物相比,单体化合物均表现出良好的降血糖活性。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、代替、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!