一种生物芯片及其制备方法与流程
本发明一般涉及用于生物或化学分析的测定系统中,用于检测和分析感兴趣的分子,属于微细加工技术领域,同时也是生物芯片技术的范畴,具体涉及一种生物芯片及其制备方法。
背景技术:
生物芯片,用于生物或化学研究的各种测定方案涉及进行大量的受控反应;在某些情况下,这些受控反应在支撑表面上进行,然后操作人员可以观测并分析所需的反应,以帮助确定所需的反应中涉及的化学品的属性或特征;例如:在一些方案中,在受控条件下,包含可识别的标记(例如荧光标记)的化学组成部分可以选择性地结合至另一化学组成部分,通过辐射激发标记并检测来自标记的光发射可以观测到这些化学反应,也可以通过其他方式(如化学发光)提供光发射。
这类方案的例子包括dna测序,在一个边合成边测序(sbs)方案中,通过桥式pcr在流道的表面上形成克隆扩增子簇。在生成克隆扩增子簇后,可以将扩增子“线性化”,以产生单链dna(sstdna),将一系列的试剂流入流动池,以完成测序循环。每个测序循环通过具有独特的荧光标记的单核普酸(例如a,t,g,c)延伸sstdna。每个核酸具有只允许一个循环内发生单碱基掺入的可逆终止子,核酸被添加到sstdna簇后,在流道内成像(即,每个荧光标记一个),成像后,荧光标记和终止子被从sstdna化学裂解,而不断增长的dna链准备用于另一循环,可以重复几个循环的试剂输送和光学检测,以确定克隆扩增子的序列。
然而,被配置以执行这些方案的系统可能能力有限以及可能不符合成本效益,因此,一般需要能够以具有成本效益的、更简易的或者以其他方式改进的方式执行测定方案或能够用于测定方案过程的改进的系统、方法和装置。
生物芯片在上述测序过程中作为耗材大量使用,作为生物芯片一部分的流通池,其加工方法应用最多的掩膜加工方法(bulknanomachining),首先在基片上通过光刻、刻蚀形成通道,然后用另一块盖片与其封合形成芯片;这种方法原理简单,可用于复杂结构的制作;但制得的纳米通道易变形塌陷或堵塞,且无论用何种材料,芯片的封合始终是一个难点;为了得到更小宽度的通道,在这些方法中多使用精密的光刻技术,如电子束光刻(electron.beamlithography,ebl)、聚焦离子束光刻(focused.ionbeam,fib)等,但这些技术大多成本昂贵,且不适用于多维纳米通道的加工制作。
表面加工方法(surfacenanomachining)也称牺牲层技术(sacrificiallayertechnology),是一种先形成闭合的芯片,然后除去牺牲层,在芯片中形成纳米通道的加工技术;但这种方法步骤繁琐而且耗时,牺牲层的刻蚀时间通常达数小时甚至数十小时;另外已报道的方法如纳米压印光刻方法(nanoimprintlithography),只能加工简单设计的芯片;掩埋通道技术(buriedchanneltechnology)制作复杂,且要用到气相沉积(chernicalvapordeposition,cvo)真空技术;化学机械抛光技术(chemicalmechanicalpolishing)制作步骤较多,繁琐耗时;这些加工技术在制作纳米结构时,可以根据所要分析研究的物质及需要来制作相应尺寸、形态的纳米结构,使分析更有针对性,而且几种方法相结合,可以取长补短,虽然繁琐也能满足分析的要求,但这样将使成本更高,因此找到一种更简便、更低廉的方法来制作微结构通道将显得非常必要。
键合是流通池加工中一个关键的工艺环节,玻璃流通池的键合方法一般分为静电(阳极或场助)键合、热键合和粘接键合;高温键合工艺,需要将玻片在马弗炉中加热至550℃,然后保温6h,再缓慢降温,整个过程不但能耗高,而且往往整个工艺过程耗时十几个小时以上,生产效率低;低温键合工艺,所需温度相对较低,但一般也在100℃以上,室温下的低温键合技术目前还处于科研阶段;阳极键合需要复杂的设备,键合过程中也对玻璃加热(键合时温度在370~420℃),然后加高直流电压(键合时直流电压控制在1000~1500v)使玻璃中的正离子(如钠、钾、钙离子)在强电场的作用下向负极运动,同时玻璃中的偶极子在强电场作用下,产生极化取向,在界面形成电子的积聚过程中,然后,在玻璃中固定的束缚负离子保持不动,并在硅的表面感应形成一层空间正电荷层,使得硅片和玻璃之间产生静电力完成键合。
技术实现要素:
本发明的目的在于提供一种生物芯片及其制备方法,以解决现有技术中的问题。
为实现上述目的,本发明提供如下技术方案:
一种生物芯片,所述生物芯片包括上基底、填充层和下基底,所述填充层分别与下基底、上基底键合,所述填充层的上表面设置有流道,所述填充层上表面的流道与上基底的下表面键合形成流动池,所述上基底上设置有若干个孔,所述孔包括若干个进液孔和若干个出液孔,所述流道两端分别与进液孔、出液孔连通。
较优化地,所述流道包括第一流通段和第二流通段,所述第一流通段的两端分别与进液孔、出液孔连通;所述第二流通段的两端分别与进液孔、出液孔连通。
较优化地,所述流道为u型流道,所述u型流道的两端分别与进液孔、出液孔连通。
一种生物芯片的制备方法,包括以下步骤:
1)加工:
a)切片:分别对上基底(3)、下基底(1)进行切片,得到的上基底(3)、下基底(1)的长l1为0-75mm,宽w为0-25mm,所述上基底(3)、下基底(1)的厚度分别为0.1mm-1.5mm;
b)打孔:对上基底(3)进行打孔,孔(5)的数量为0-40个;
2)清洗:
a)将上基底(3)、下基底(1)分别放入氢氟酸中,超声波清洗1-1.5h,然后用70℃去离子水冲洗干净;
b)再用去离子水超声波清洗2-2.5h,每30-35min更换一次去离子水,然后用冷、热去离子水交替冲洗四遍;
c)分别对上基底(3)、下基底(1)进行干燥;
3)加工流道(4):
a)喷墨:首先将制备填充层(2)的聚合物颗粒与分散剂在反应管中混合,升温至70-100℃,搅拌1-5min至混合物为透明溶液,控制混合液表面张力为20-40mn/m,粘度为50-100cps;并将液滴从喷嘴压电喷出;再用红外线照射到所述液滴上,使所述液滴中含有的溶剂蒸发,且所述液滴中含有的聚合物颗粒熔化,熔化的聚合物颗粒在进行堆积,制备得到填充层(2),所述填充层(2)的厚度为0.01mm-1.5mm;
b)溅射:对制备得到的填充层(2)进行溅射刻蚀,抽真空至1×10-4pa,溅射时间为20-30min,得到流道(4);
c)夹层填充:将制备好的填充层(2)填充至上基底(3)、下基底(1)之间;
4)键合:将填充层(2)、上基底(3)、下基底(1)进行键合,得到所述生物芯片。
较优化地,包括以下步骤:
1)加工:
a)切片:分别对上基底(3)、下基底(1)进行切片,得到的上基底(3)、下基底(1)的长l1为0-75mm,宽w为0-25mm,所述上基底(3)、下基底(1)的厚度分别为0.1mm-1.5mm;
b)打孔:对上基底(3)进行打孔,孔(5)的数量为0-40个;
2)清洗:
a)将上基底(3)、下基底(1)分别放入氢氟酸中,超声波清洗1-1.5h,然后用70℃去离子水冲洗干净;
b)再用去离子水超声波清洗2-2.5h,每30-35min更换一次去离子水,然后用冷、热去离子水交替冲洗四遍;
c)分别对上基底(3)、下基底(1)进行干燥;
3)加工流道(4):
a)喷墨:首先将制备填充层(2)的聚合物颗粒与分散剂在反应管中混合,升温至70-100℃,搅拌1-5min至混合物为透明溶液,控制混合液表面张力为20-40mn/m,粘度为50-100cps;并将液滴从喷嘴压电喷出;再用红外线照射到所述液滴上,使所述液滴中含有的溶剂蒸发,且所述液滴中含有的聚合物颗粒熔化,熔化的聚合物颗粒在进行堆积,制备得到填充层(2),所述填充层(2)的厚度为0.01mm-1.5mm;
b)溅射:对制备得到的填充层(2)进行溅射刻蚀,抽真空至1×10-4pa,溅射时间为20-30min,得到流道(4);
c)夹层填充:将制备好的填充层(2)填充至上基底(3)、下基底(1)之间;
4)键合:将填充层(2)、上基底(3)、下基底(1)进行键合,得到所述生物芯片;
5)修饰:将制备得到的生物芯片放入配制好的硅烷偶联剂溶液中,在0-25℃,相对湿度为30-50%的恒温恒湿箱中放置7-12h,取出后用无水乙醇清洗,110-140℃烘干15-30min。
较优化地,包括以下步骤:
1)加工:
a)切片:分别对上基底(3)、下基底(1)进行切片,得到的上基底(3)、下基底(1)的长l1为0-75mm,宽w为0-25mm,所述上基底(3)、下基底(1)的厚度分别为0.1mm-1.5mm;
b)打孔:对上基底(3)进行打孔,孔(5)的数量为0-40个;
2)清洗:
a)将上基底(3)、下基底(1)分别放入氢氟酸中,超声波清洗1-1.5h,然后用70℃去离子水冲洗干净;
b)再用去离子水超声波清洗2-2.5h,每30-35min更换一次去离子水,然后用冷、热去离子水交替冲洗四遍;
c)分别对上基底(3)、下基底(1)进行干燥;
3)加工流道(4):
a)喷墨:首先将制备填充层(2)的聚合物颗粒与分散剂在反应管中混合,升温至70-100℃,搅拌1-5min至混合物为透明溶液,控制混合液表面张力为20-40mn/m,粘度为50-100cps;并将液滴从喷嘴压电喷出;再用红外线照射到所述液滴上,使所述液滴中含有的溶剂蒸发,且所述液滴中含有的聚合物颗粒熔化,熔化的聚合物颗粒在进行堆积,制备得到填充层(2),所述填充层(2)的厚度为0.01mm-1.5mm;
b)溅射:对制备得到的填充层(2)进行溅射刻蚀,抽真空至1×10-4pa,溅射时间为20-30min,得到流道(4);
c)夹层填充:将制备好的填充层(2)填充至上基底(3)、下基底(1)之间;
4)修饰:将制备得到的填充层(2)、上基底(3)、下基底(1)分别放入配制好的硅烷偶联剂溶液中,在0-25℃,相对湿度为30-50%的恒温恒湿箱中放置7-12h,取出后用无水乙醇清洗,110-140℃烘干15-30min;
5)键合:将填充层(2)、上基底(3)、下基底(1)进行键合,得到所述生物芯片。
较优化地,所述填充层通过物理气相沉积(pvd)、化学气相沉积(cvd)、液相沉积、离子束沉积(ibd)、溅射沉积(rfsandms)、涂覆、打印、机械加工中的任意一种方式加工形成。
较优化地,所述填充层的材料为类金刚石薄膜(dlc)、尼龙膜、聚丙烯膜、硝酸纤维膜、uv墨水、环氧胶、丙烯酸胶、聚四氟乙烯、碳氟化合物、聚对二甲苯、全氟聚合物、金属、金属氧化物或其他类型的钝化聚合物中的任意一种。
较优化地,所述填充层与上基底、下基底之间的键合方式为粘接键合、热键合、激光辅助键合中的任意一种。
较优化地,所述上基底、下基底的材料分别为玻璃、聚合物材料、硅、石英、蓝宝石、瓷片、铝、钛中的任意一种。
现如今,常用的玻璃材质流通池在制作微流道过程中常用光刻工艺,一般的光刻工艺要经历表面清洗烘干、涂底、旋涂光刻胶、软烘、对准曝光、后烘、显影、硬烘、刻蚀等工序,可见整个过程较为繁琐,并且在刻蚀过程中有时会用到一些具有毒性的试剂,比如氢氟酸,不环保,也存在安全问题,所以本专利的目的就是尽量避免刻蚀工艺,同时尽量减少工艺流程,降低生产成本。
本发明中的生物芯片的流道是通过增材技术,即通过增加填充层形成的,通过在基底上增加填充层,在填充层上制作流道,然后键合形成完整的流通池;填充层材质的可选择范围大,且往往比玻璃更易加工,通过这个方法避开玻璃的刻蚀工艺,增加的工艺的选择性和降低了生产成本。
与玻璃光刻工艺相比较,增材技术刻蚀的宽度较大,不能做到科研追求的纳米级,但是在实际应用中,考虑到试剂在流道中的流体性质和生产成本,微米级流道甚至毫米级流道的应用范围更广,所以利用增材技术制备的生物芯片更加适合实际的生产。
另外,增材技术制作流道后采用粘接键合,有利于手工制作,所以,可以说此方法制作的流通池同pdms、pdma材质制作的流通池工艺一样简单,容易掌握,也适用性于在实验室手工制作。
本发明中还进行生物芯片的修饰,可以有效提高生物分子在生物芯片表面的固定量,使原来很难检测到的小分子药物能够检测出来。
本发明中流道、上基底之间键合形成流通池,流道用于保持有关样品,样品被示为在sbs方案过程中可以成像的多个dna簇,但其他样品可用于替代性的实施方式中。虽然只示出单一的双流道,替代性的实施方式可包括具有带有不同形状的路径的多流道的流动池。流动池可以与射流系统(未显示)流体连通,射流系统被配置以递送试剂至流道中的样品。
在一些实施方式中,所需的反应发生后,样品可提供可检测的特征(例如通过荧光或化学发光),例如:流动池可以具有光信号从其中发出的一个或多个样品区域或部分(即样品所处的区域或部分)。
在一些实施方式中,流动池也可用于生成样品,以执行生物或化学测定,例如:在sbs方案执行前,流动池可用于生成dna簇。
流动池的所述长度l1可以是约75mm或更小;在具体的实施方式中,长度l1是约75mm或更小;在一些实施方式中,宽度w,可以是约25mm或更小;此外,图2所示的合并或总高度h可以是约2.1mm或更小;更具体地,高度h可以是约1.5mm或更小。
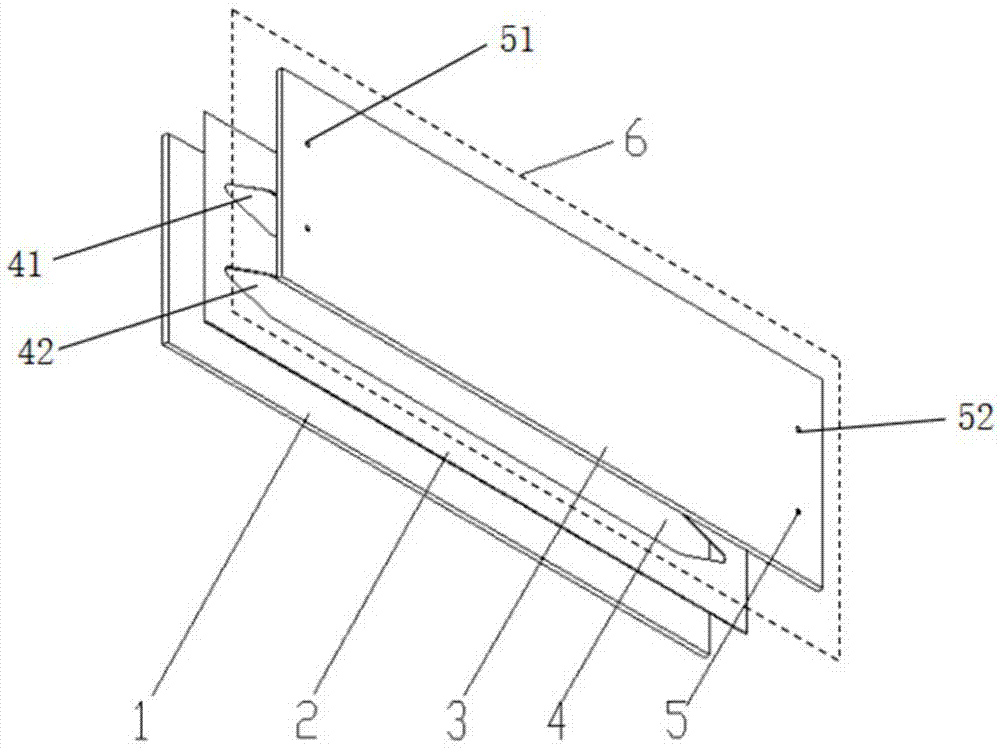
如图1所示,填充层由喷墨打印形成,填充层厚度h2可以是0.1或者更小,在具体的实施方式中,厚度h2是约0.06mm或更小。
在所示的实施方式中,流道可以如图1、图2所示,也可以如图3所示,流道各自的横截面,其通过垂直于流动方向,在一些实施方式中,横截面可以是不同大小的(即不同的截面积)。
在替代性的实施方式中,流道可以具有不同的路径,以便试剂出入口在流动池中具有不同的位置,例如:试剂出入口可以同时在一层基底上或者同时在两层基底上。
与现有技术相比,本发明的有益效果是:本发明中不再对玻璃进行刻蚀加工形成流道,而是通过增加填充层方式形成流道,在制作生物芯片过程中,填充层采用材质的材质可以具有生物相容性或者不具有生物相容性,当填充层材质不具有生物相容性时,可以在填充层形成的流道表面涂覆一层生物相容性涂层解决生物相容性问题,设计这种增加涂层的工艺,不但扩大了填充层材质选用范围,降低物料成本,甚至具有降低背景光,固定核酸探针,蛋白质分子等作用。
本发明通过增加填充层构建流道,避免了复杂的蚀刻工艺,大大降低成本和工时,有利于商业化制作流通池。
本发明的芯片具有以下优点:1、密封性能好,能承受较高正负压,密封过程中没有高温等极端工况,适用于把样品、核酸探针固定到流道,再进行密封;2、散热性好,实验过程中能进行升降温工序;3、上基底、下基底的平面度好、透光性佳,适用于光学检测;4、本发明适于生物芯片领域,具有成本低、工艺简单、易于大批量商业化生产。
附图说明
为了使本发明的内容更容易被清楚地理解,下面根据具体实施例并结合附图,对本发明作进一步详细的说明。
图1为本发明的实施例结构爆炸图;
图2为本发明的实施例结构正视图;
图3为本发明的可存在的结构正视图;
图4为本发明的实施例填充层区域图;
图5为本发明的实施例工艺路线图;
图6为本发明的可实施工艺路线图a;
图7为本发明的可实施工艺路线图b。
图中:1-下基底、2-填充层、3-上基底、4-流道、41-第一流通段、42-第二流通段、5-孔、51-进液孔、52出液孔、6-流动池、7-样品。
具体实施方式
下面结合附图与具体实施方式对本发明作进一步详细描述。
实施例1:
首先分别对上基底3、下基底1进行切片,得到的上基底3、下基底1的长l1为75mm,宽w为25mm,所述上基底3、下基底1的厚度分别为0.1mm;再对上基底3进行打孔,孔5的数量为40个;接着将上基底3、下基底1分别放入氢氟酸中,超声波清洗1h,然后用70℃去离子水冲洗干净;再用去离子水超声波清洗2h,每30min更换一次去离子水,然后用冷、热去离子水交替冲洗四遍;分别对上基底3、下基底1进行干燥;
再将制备填充层2的聚合物颗粒与分散剂在反应管中混合,升温至70℃,搅拌3min至混合物为透明溶液,控制混合液表面张力为20mn/m,粘度为50cps;并将液滴从喷嘴压电喷出;再用红外线照射到所述液滴上,使所述液滴中含有的溶剂蒸发,且所述液滴中含有的聚合物颗粒熔化,熔化的聚合物颗粒在进行堆积,制备得到填充层2,填充层2的厚度为0.01mm;对制备得到的填充层2进行溅射刻蚀,抽真空至1×10-4pa,溅射时间为20min,得到流道4;将制备好的填充层2填充至上基底3、下基底1之间;最后将填充层2、上基底3、下基底1进行键合,得到所述生物芯片。
实施例2:
首先分别对上基底3、下基底1进行切片,得到的上基底3、下基底1的长l1为75mm,宽w为25mm,所述上基底3、下基底1的厚度分别为0.5mm;再对上基底3进行打孔,孔5的数量为40个;接着将上基底3、下基底1分别放入氢氟酸中,超声波清洗1.5h,然后用70℃去离子水冲洗干净;再用去离子水超声波清洗2.5h,每35min更换一次去离子水,然后用冷、热去离子水交替冲洗四遍;分别对上基底3、下基底1进行干燥;
再将制备填充层2的聚合物颗粒与分散剂在反应管中混合,升温至100℃,搅拌5min至混合物为透明溶液,控制混合液表面张力为40mn/m,粘度为100cps;并将液滴从喷嘴压电喷出;再用红外线照射到所述液滴上,使所述液滴中含有的溶剂蒸发,且所述液滴中含有的聚合物颗粒熔化,熔化的聚合物颗粒在进行堆积,制备得到填充层2,填充层2的厚度为0.05mm;对制备得到的填充层2进行溅射刻蚀,抽真空至1×10-4pa,溅射时间为30min,得到流道4;将制备好的填充层2填充至上基底3、下基底1之间;最后将填充层2、上基底3、下基底1进行键合,得到所述生物芯片。
实施例3:
首先分别对上基底3、下基底1进行切片,得到的上基底3、下基底1的长l1为75mm,宽w为25mm,所述上基底3、下基底1的厚度分别为1mm;再对上基底3进行打孔,孔5的数量为40个;接着将上基底3、下基底1分别放入氢氟酸中,超声波清洗1.2h,然后用70℃去离子水冲洗干净;再用去离子水超声波清洗2.3h,每30min更换一次去离子水,然后用冷、热去离子水交替冲洗四遍;分别对上基底3、下基底1进行干燥;
再将制备填充层2的聚合物颗粒与分散剂在反应管中混合,升温至100℃,搅拌3min至混合物为透明溶液,控制混合液表面张力为30mn/m,粘度为80cps;并将液滴从喷嘴压电喷出;再用红外线照射到所述液滴上,使所述液滴中含有的溶剂蒸发,且所述液滴中含有的聚合物颗粒熔化,熔化的聚合物颗粒在进行堆积,制备得到填充层2,填充层2的厚度为0.05mm;对制备得到的填充层2进行溅射刻蚀,抽真空至1×10-4pa,溅射时间为25min,得到流道4;将制备好的填充层2填充至上基底3、下基底1之间;再将填充层2、上基底3、下基底1进行键合,得到所述生物芯片;
最后将制备得到的生物芯片放入配制好的硅烷偶联剂溶液中,在15℃,相对湿度为30%的恒温恒湿箱中放置7h,取出后用无水乙醇清洗,110℃烘干15min。
实施例4:
首先分别对上基底3、下基底1进行切片,得到的上基底3、下基底1的长l1为75mm,宽w为25mm,所述上基底3、下基底1的厚度分别为1mm;再对上基底3进行打孔,孔5的数量为40个;接着将上基底3、下基底1分别放入氢氟酸中,超声波清洗1.5h,然后用70℃去离子水冲洗干净;再用去离子水超声波清洗2h,每35min更换一次去离子水,然后用冷、热去离子水交替冲洗四遍;分别对上基底3、下基底1进行干燥;
再将制备填充层2的聚合物颗粒与分散剂在反应管中混合,升温至80℃,搅拌5min至混合物为透明溶液,控制混合液表面张力为30mn/m,粘度为100cps;并将液滴从喷嘴压电喷出;再用红外线照射到所述液滴上,使所述液滴中含有的溶剂蒸发,且所述液滴中含有的聚合物颗粒熔化,熔化的聚合物颗粒在进行堆积,制备得到填充层2,填充层2的厚度为0.02mm;对制备得到的填充层2进行溅射刻蚀,抽真空至1×10-4pa,溅射时间为20min,得到流道4;将制备好的填充层2填充至上基底3、下基底1之间;再将填充层2、上基底3、下基底1进行键合,得到所述生物芯片;
最后将制备得到的生物芯片放入配制好的硅烷偶联剂溶液中,在20℃,相对湿度为50%的恒温恒湿箱中放置12h,取出后用无水乙醇清洗,140℃烘干30min。
实施例5:
首先分别对上基底3、下基底1进行切片,得到的上基底3、下基底1的长l1为75mm,宽w为25mm,所述上基底3、下基底1的厚度分别为1mm;再对上基底3进行打孔,孔5的数量为40个;接着将上基底3、下基底1分别放入氢氟酸中,超声波清洗1.5h,然后用70℃去离子水冲洗干净;再用去离子水超声波清洗2.5h,每30min更换一次去离子水,然后用冷、热去离子水交替冲洗四遍;分别对上基底3、下基底1进行干燥;
再将制备填充层2的聚合物颗粒与分散剂在反应管中混合,升温至100℃,搅拌5min至混合物为透明溶液,控制混合液表面张力为40mn/m,粘度为100cps;并将液滴从喷嘴压电喷出;再用红外线照射到所述液滴上,使所述液滴中含有的溶剂蒸发,且所述液滴中含有的聚合物颗粒熔化,熔化的聚合物颗粒在进行堆积,制备得到填充层2,填充层2的厚度为0.01mm;对制备得到的填充层2进行溅射刻蚀,抽真空至1×10-4pa,溅射时间为30min,得到流道4;将制备好的填充层2填充至上基底3、下基底1之间;再将制备得到的填充层2、上基底3、下基底1分别放入配制好的硅烷偶联剂溶液中,在25℃,相对湿度为50%的恒温恒湿箱中放置12h,取出后用无水乙醇清洗,140℃烘干30min;
最后将填充层2、上基底3、下基底1进行键合,得到所述生物芯片。
实施例6:
首先分别对上基底3、下基底1进行切片,得到的上基底3、下基底1的长l1为75mm,宽w为25mm,所述上基底3、下基底1的厚度分别为1mm;再对上基底3进行打孔,孔5的数量为40个;接着将上基底3、下基底1分别放入氢氟酸中,超声波清洗1.5h,然后用70℃去离子水冲洗干净;再用去离子水超声波清洗2.5h,每35min更换一次去离子水,然后用冷、热去离子水交替冲洗四遍;分别对上基底3、下基底1进行干燥;
再将制备填充层2的聚合物颗粒与分散剂在反应管中混合,升温至70℃,搅拌5min至混合物为透明溶液,控制混合液表面张力为20mn/m,粘度为50cps;并将液滴从喷嘴压电喷出;再用红外线照射到所述液滴上,使所述液滴中含有的溶剂蒸发,且所述液滴中含有的聚合物颗粒熔化,熔化的聚合物颗粒在进行堆积,制备得到填充层2,填充层2的厚度为0.02mm;对制备得到的填充层2进行溅射刻蚀,抽真空至1×10-4pa,溅射时间为30min,得到流道4;将制备好的填充层2填充至上基底3、下基底1之间;再将制备得到的填充层2、上基底3、下基底1分别放入配制好的硅烷偶联剂溶液中,在15℃,相对湿度为50%的恒温恒湿箱中放置7h,取出后用无水乙醇清洗,140℃烘干30min;
最后将填充层2、上基底3、下基底1进行键合,得到所述生物芯片。
通过对实施例1-6制备得到的生物芯片进行检测,我们得到以下结论:
本发明所公开的技术方案可以与任何己知的组合化学或生物化学测定方法一起使用,并且尤其适用于具有固相固定化的测定,例如药物研发、功能化底物、生物学、蛋白质组学、组合化学和任何测定或多重实验;常见测定的例子是snp(单核普酸多态性)检测、dna/基因组序列分析、基因分型、基因表达测定、蛋白质组学测定、肤测定、抗原/抗体测定(免疫测定)、配体/受体测定、dna分析标记以及分子标记、生物颗粒、细胞鉴定和分选、基质支持材料、受体结合测定、放射性或非放射性邻近测定以及其它测定、高通量药物/基因组筛选或大规模平行测定应用。
如本文所用,术语“生物或化学物质”可以包括各种适于用本文所述的光学系统成像或检验的生物或化学物质。例如,生物或化学物质包括生物分子,如核普、核酸、多核普酸、寡核普酸、蛋白质、酶、多肤、抗体、抗原、配体、受体、多糖、碳水化合物、多磷酸盐、纳米孔、细胞器、脂质层、细胞、组织、生物体和生物活性化合物(如上述种类的类似物或拟态物)。其他化学物质包括可以用于标识的标记,其例子包括荧光标记和下文进一步详述的其他标记。
不同类型的样品可包括以不同的方式影响入射光的不同光学基底或支撑结构,在具体的实施方式中,待检测的样品7可被连接到基底或支撑结构的一个或多个表面,例如:流动池6可包括一个或多个流道4,在流动池6中,流道4可以通过流动池6的顶层和底层与周围环境分隔,因此,待检测的光信号投射自支撑结构的内部并可以传输通过具有不同折射率的多个材料层。例如:当检测来自流道4的内底面的光信号以及当检测来自流道4上面的光信号时,希望待检测的光信号可传播通过具有一种折射率的流体、通过流动池6的具有不同的折射率的一个或多个层并通过具有一种不同折射率的周围环境。
本发明在具体的实施方式中,流体池具有微流体尺寸的流道4,在这样的通道中,流动穿过其中的液体的表面张力和内聚力以及液体和通道的表面之间的粘合力至少对液体的流动有实质影响。例如:流道4的横截面面积(垂直于流动方向截取)可以是约10μm2或更小。
本发明可以用于本领域已知的各种微阵列的任何一种。典型的微阵列包含位点(有时也被称为功能部件),每个具有一组探针,每个位点上的探针组通常具有单一品种的探针,是同质的,但在一些实施方式中,组中每个可以是异质的,阵列的位点或功能部件通常是离散的、被隔开的;单独的位点可以是连续的,或者它们彼此之间可以有间隔,探针位点的大小和位点之间的间距可以不同,以便阵列可以是高密度、中密度或较低密度:高密度阵列的特点是位点间隔小于约15μm;中密度阵列的位点间隔约15至30μm;而低密度阵列的位点间隔大于30μm;用于本发明的阵列可以具有间隔小于100μm、50μm、l0μm、5μm、lμm或0.5μm的位点,本发明实施方式的装置或方法可用来以足以辨别上述密度或密度范围的位点的分辨率使阵列成像。
本发明可以应用的市售微阵列的进一步的例子包括,例如affymetrix微阵列或其他按照有时被称为vls工pstm(超大规模固定化聚合物合成)技术的方法合成的微阵列,点状微阵列也可用于根据本发明的实施方式的方法中,示例性的点状微阵列是来自amershambiosciences的codelinktm阵列,另一有用的微阵列是一种使用喷墨印刷方法(来自agilenttechnologies的sureprinttm技术)制造的微阵列。
在一些本专利的实施方式中,核酸可在测序之前或期间被附到表面并扩增,例如:可以使用桥式扩增进行扩增,以在表面上形成核酸簇;另一有用的用于扩增表面上的核酸的方法是滚环扩增;珠上乳液pcr也可以使用。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明保护的范围之内。
- 还没有人留言评论。精彩留言会获得点赞!