一种柠檬酸单酯的选择性合成方法与流程
本发明涉及化工合成工艺技术领域,具体为一种柠檬酸单酯的选择性合成方法。
背景技术:
柠檬酸(2-羟基-丙三羧酸)是当前以微生物发酵法生产量最大的有机酸,由于其特殊的结构,具有酸性、缓冲、络合等多种功能。我国是农业大国,生产柠檬酸的原料来源丰富,是世界上最大的柠檬酸生产和出口国。但目前,世界柠檬酸供大于求,市场价格更处于逐年下降的趋势,适时开发柠檬酸的多种应用途径,大力发展柠檬酸衍生物的应用研究领域,具有重要的现实意义。
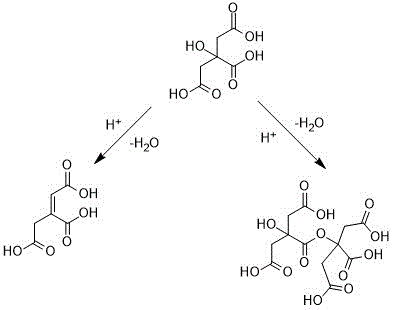
柠檬酸作为羟基酸,含有三个羧基和一个羟基,同时具有醇和酸两种性质,可以成醚、成酯等。其反应特征是酸性条件下失水,柠檬酸作为β-羟基酸时,极易分子内脱水生成α,β-不饱和酸,或分子间失水交联(如图1所示)。
当前广泛使用的柠檬酸酯化方法有直接酯化法和间接酯化法两种,得到的产物是柠檬酸单、双、三酯的混合物,因此,如何控制条件生成含量较高的柠檬酸单酯是一个关键问题。
针对这一问题,gooding等将柠檬酸溶解在无水吡啶中,再与十八醇反应,由于十八醇在吡啶中溶解度不大,少量的脂肪醇和过量的柠檬酸反应,有利于柠檬酸单酯的生成。但随醇的相对摩尔数的增加,双酯、三酯相对含量增加,且吡啶等毒害试剂的应用对柠檬酸单酯生产工艺的安全性能及环保要求提出了较大挑战。weil等利用柠檬酸酐与含有10~18个碳原子的直链脂肪醇反应,得到单酯含量达到95%以上。但通过柠檬酸酐制备柠檬酸单酯的过程中不可避免的会因为反应条件的酸性、高温、避水导致柠檬酸脱水异构的发生,进而导致后处理复杂、原料转化率低、原子经济效率差。
因此,开发一种选择性好、原子经济效率高、原料转化率高且制备条件相对温和环保的柠檬酸单酯的制备方法就成为了本领域技术人员亟需解决的问题。
技术实现要素:
有鉴于此,本发明的目的是针对现有技术中存在的问题,提供一种可以选择性合成柠檬酸单酯的方法。
为解决上述技术问题,本发明采用如下技术方案:
本发明提供一种柠檬酸单酯的选择性合成方法,通过柠檬酸、碳原子数为2-18的单羟基化合物及耦合剂反应得到柠檬酸单酯,所述耦合剂包括碳二亚胺和n-羟基二酰亚胺。
值得说明的是,柠檬酸作为羟基酸,含有三个羧基和一个羟基,同时具有醇和酸两种性质,可以成醚、成酯等。现有技术中,为了规避柠檬酸的自交联或内交联,制备得到柠檬酸单酯,或是通过控制醇与柠檬酸的反应比例,在酸大大过量的条件下制备单酯;或是通过控制柠檬酸的活性基团,利用柠檬酸酐使柠檬酸有且仅有一个羧基可进行酯化反应,从而制备单酯。而本发明利用包括碳二亚胺和n-羟基二酰亚胺的耦合剂,构建了一个空间位阻较大的柠檬酸衍生中间体,利用该中间体稳定的活性位点、合适的空间位阻,反应得到了柠檬酸单酯。
优选地,所述n-羟基二酰亚胺包括n-羟基邻苯二甲酰亚胺或n-羟基丁二酰亚胺。
优选地,所述碳二亚胺包括n,n’-二环己基碳二亚胺。
值得说明的是,n,n’-二环己基碳二亚胺较大的空间位阻使活性中间体更为稳定,不易发生重排异构等反应,利于反应的正向进行。
优选地,反应体系还包括溶剂。
优选地,所述溶剂包括二氯甲烷、二氯甲烷/丙酮、二氯甲烷/丁酮、二氯甲烷/1,4-二氧六环中的任意一种。
值得说明的是,二氯甲烷对单羟基化合物及耦合剂都具有良好的溶解性。不同于通过吡啶等不良溶剂控制反应体系中羟基与羧基的比例,进而控制柠檬酸单酯的生成,本发明无需限定反应体系中羟基的相对摩尔数远少于羧基,在单羟基化合物与柠檬酸的相对摩尔数大致相当时,也可以得到产率较高的柠檬酸单酯。并且,良溶剂的应用也提高了反应物的原子转化率,有效提高了反应的原子经济效率。
优选地,反应条件为:25℃-100℃的条件下,常压控温搅拌反应10min-48h。
值得说明的是,无论是利用吡啶限制脂肪醇的溶解,还是采用酸酐法制备单酯,为了酯化反应的正向进行,都需要在酸性环境下严格避水,并辅以高温、高压等较为严苛的反应条件。与之不同的,本发明利用耦合剂首先得到柠檬酸衍生中间体,再通过该中间体与醇反应得到单酯,降低了反应过程的能量壁垒,无需高温、高压等条件,有效解决了柠檬酸分子间、分子内脱水的问题,提高了柠檬酸的反应效率,无需分离由柠檬酸分子间、分子内脱水产生的酯、醚,后处理简便高效。
优选地,所述单羟基化合物包括脂肪醇或酚。
与现有技术相比,本发明利用耦合剂常温控压反应选择性合成了柠檬酸单酯,该方法反应条件温和,安全环保。并且,通过柠檬酸衍生中间体的构建,在保证了反应正向进行的同时,产物选择性较好、原子转化率高且安全风险性低,后处理简便高效,可以适用于自动化连续式生产工艺,符合绿色化工、高效经济的发展理念。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
图1为柠檬酸在酸性条件下失水,分子内脱水生成的α,β-不饱和酸,或分子间失水交联的产物结构式;
图2为负离子模式下,实施例1的柠檬酸单乙酯通过液相色谱质谱联用仪lc-ms检测得到的质谱图;
图3为负离子模式下,实施例5的柠檬酸单癸酯通过液相色谱质谱联用仪lc-ms检测得到的质谱图;
图4为负离子模式下,实施例6的柠檬酸单硬脂醇酯通过液相色谱质谱联用仪lc-ms检测得到的质谱图;
图5为负离子模式下,实施例7的柠檬酸单苯酚酯通过液相色谱质谱联用仪lc-ms检测得到的质谱图。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
为更好地理解本发明,下面通过以下实施例对本发明作进一步具体的阐述,但不可理解为对本发明的限定,对于本领域的技术人员根据上述发明内容所作的一些非本质的改进与调整,也视为落在本发明的保护范围内。
实施例1,在反应釜中加入8×10-6moln-羟基丁二酰亚胺、12.8×10-6moln,n’-二环己基碳二亚胺、3×10-6mol柠檬酸、86µl乙醇和914µl二氯甲烷,常温搅拌10min。反应完毕,得到柠檬酸单乙酯。将反应体系稀释104倍,通过液相色谱质谱联用仪lc-ms测得柠檬酸单乙酯的质谱图如图2所示,且柠檬酸单乙酯的产率为72%。
实施例2,在反应釜中加入12.5×10-5moln-羟基邻苯二甲酰亚胺、20×10-5moln,n’-二环己基碳二亚胺、4.7×10-5mol柠檬酸、4.7×10-5mol正丁醇和23ml1,4-二氧六环/二氯甲烷混合溶液,35℃搅拌30min。反应完毕,通过lc-ms检测显示反应生成柠檬酸单丁酯,且柠檬酸单丁酯的产率为76%。
实施例3,在反应釜中加入8×10-6moln-羟基邻苯二甲酰亚胺、12.8×10-6moln,n’-二环己基碳二亚胺、3×10-6mol柠檬酸、86µl正己醇和914µl二氯甲烷,40℃搅拌90min。反应完毕,通过lc-ms检测显示反应生成柠檬酸单己酯,且柠檬酸单己酯的产率为83%。
实施例4,在反应釜中加入12.5×10-5moln-羟基丁二酰亚胺、20×10-5moln,n’-二环己基碳二亚胺、4.7×10-5mol柠檬酸、4.7×10-5mol正辛醇和30ml丁酮/二氯甲烷,50℃搅拌12h。反应完毕,通过lc-ms检测显示反应生成柠檬酸单辛酯,且柠檬酸单辛酯的产率为83%。
实施例5,在反应釜中加入8×10-6moln-羟基丁二酰亚胺、12.8×10-6moln,n’-二环己基碳二亚胺、3×10-6mol柠檬酸、3×10-6mol正癸醇和1ml丙酮/二氯甲烷混合溶液,80℃搅拌24h。反应完毕,得到柠檬酸单癸酯。将反应体系稀释104倍,通过lc-ms测得柠檬酸单癸酯的质谱图如图3所示,且柠檬酸单癸酯的产率为81%。
实施例6,在反应釜中加入8×10-5moln-羟基邻苯二甲酰亚胺、12.8×10-5moln,n’-二环己基碳二亚胺、3×10-5mol柠檬酸、3×10-5mol十八醇和15ml二氧六环/二氯甲烷混合溶液,100℃搅拌48h。反应完毕,得到柠檬酸单十八醇酯。将反应体系稀释105倍,通过lc-ms测得柠檬酸单十八醇酯的质谱图如图4所示,且柠檬酸单十八醇酯的产率为78%。
实施例7,在反应釜中加入2.1×10-4moln-羟基丁二酰亚胺、3.4×10-4moln,n’-二环己基碳二亚胺、7.8×10-5mol柠檬酸、7.8×10-5mol苯酚和50ml二氧六环/二氯甲烷,70℃搅拌30h。反应完毕,得到柠檬酸单苯酚酯。将反应体系稀释105倍,通过lc-ms测得柠檬酸单苯酚酯的质谱图如图5所示,且柠檬酸单苯酚酯的产率为72%。
实施例8,在反应釜中加入2.1×10-4moln-羟基丁二酰亚胺、3.4×10-4moln,n’-二环己基碳二亚胺、7.8×10-5mol柠檬酸、7.8×10-5mol环己醇和50ml二氧六环/二氯甲烷,70℃搅拌30h。反应完毕,通过lc-ms检测显示反应生成柠檬酸单环己醇酯,且柠檬酸单环己醇酯的产率为85%。
实施例9,在反应釜中加入8×10-6moln-羟基丁二酰亚胺、12.8×10-6moln,n’-二环己基碳二亚胺、3×10-6mol柠檬酸、1000µl乙醇,常温搅拌10min。反应完毕,通过lc-ms检测显示反应生成柠檬酸单乙酯,且柠檬酸单乙酯的产率为88%。
为了进一步证明本发明的有益效果以更好地理解本发明,下面通过以下对比例进一步阐明本发明所述柠檬酸单酯选择性合成方法具有的性质及适用条件,但不可理解为对本发明的限定,对于本领域的技术人员根据上述发明内容所作的其他正相关实验或对比实验得到的制备性质及根据上述性质进行的制备应用,也视为落在本发明的保护范围内。
对比例1,与实施例1反应原料相同,改变溶剂体系。在反应釜中加入8×10-6moln-羟基丁二酰亚胺、12.8×10-6moln,n’-二环己基碳二亚胺、3×10-6mol柠檬酸、86µl乙醇和914µl乙酸乙酯,常温搅拌10min。反应完毕,得到柠檬酸单乙酯、柠檬酸二乙酯和柠檬酸三乙酯混合物。将反应体系稀释104倍,通过气相色谱质谱联用仪gc-ms测得柠檬酸三乙酯的产率为72%,该合成条件不具有选择性。
对比例2,与实施例2反应原料相同,改变溶剂体系。在反应釜中加入12.5×10-5moln-羟基邻苯二甲酰亚胺、20×10-5moln,n’-二环己基碳二亚胺、4.7×10-5mol柠檬酸、4.7×10-5mol正丁醇和23ml石油醚/二氯甲烷混合溶液,35℃搅拌30min。反应完毕,将体系稀释104倍,通过lc-ms测得的色谱图显示柠檬酸量未见明显减少,即反应并未进行。
对比例3,与实施例3反应原料相同,改变溶剂体系。在反应釜中加入8×10-6moln-羟基丁二酰亚胺、12.8×10-6moln,n’-二环己基碳二亚胺、3×10-6mol柠檬酸、86µl正己醇和914µl氯仿,40℃搅拌90min。反应完毕,未检测到柠檬酸酯生成。
对比例4,与实施例4反应原料比例相同,改变溶剂体系。在反应釜中加入12.5×10-5moln-羟基丁二酰亚胺、20×10-5moln,n’-二环己基碳二亚胺、4.7×10-5mol柠檬酸、4.7×10-5mol正辛醇和30ml水/二氯甲烷,50℃搅拌12h。反应完毕,未检测到柠檬酸酯生成。
对比例5,与实施例5反应原料相同,改变溶剂体系。在反应釜中加入8×10-6moln-羟基丁二酰亚胺、12.8×10-6moln,n’-二环己基碳二亚胺、3×10-6mol柠檬酸、86µl正癸醇和914µl乙酸丁酯/二氯甲烷混合溶液,40℃搅拌90min。反应完毕,得到柠檬酸单癸酯、柠檬酸二癸酯和柠檬酸三癸酯混合物。将反应体系稀释104倍,通过gc-ms测得柠檬酸三癸酯的产率为62%,该合成条件不具有选择性。
对比例6,与实施例6反应原料相同,改变溶剂体系。在反应釜中加入8×10-5moln-羟基邻苯二甲酰亚胺、12.8×10-5moln,n’-二环己基碳二亚胺、3×10-5mol柠檬酸、3×10-5mol硬脂醇和15ml乙腈/二氯甲烷混合溶液,90℃搅拌24h。反应完毕,未检测到柠檬酸酯生成。
对比例7,与实施例7反应原料相同,改变溶剂体系。在反应釜中加入2.1×10-4moln-羟基邻苯二甲酰亚胺、3.4×10-4moln,n’-二环己基碳二亚胺、7.8×10-5mol柠檬酸、7.8×10-5mol苯酚和50mldmf/二氯甲烷混合溶液,50℃搅拌30h。反应完毕,未检测到柠檬酸酯生成。
对比例8,与实施例1反应原料相同,改变反应温度。在反应釜中加入8×10-6moln-羟基丁二酰亚胺、12.8×10-6moln,n’-二环己基碳二亚胺、3×10-6mol柠檬酸、86µl乙醇和914µl二氯甲烷,0℃搅拌10min。反应完毕,未检测到柠檬酸酯生成。
对比例9,与实施例6反应原料相同,改变反应温度。在反应釜中加入8×10-5moln-羟基丁二酰亚胺、12.8×10-5moln,n’-二环己基碳二亚胺、3×10-5mol柠檬酸、3×10-5mol硬脂醇和15ml丙酮/二氯甲烷混合溶液,110℃搅拌24h。反应完毕,lc-ms检测到柠檬酸脱水自交联,转化率为97%,仅有极少量柠檬酸三酯生成。
对比例10,与实施例6反应原料相同,改变反应时间。在反应釜中加入8×10-5moln-羟基丁二酰亚胺、12.8×10-5moln,n’-二环己基碳二亚胺、3×10-5mol柠檬酸、3×10-5mol硬脂醇和15ml丙酮/二氯甲烷混合溶液,100℃搅拌72h。反应完毕,lc-ms检测到柠檬酸脱水自交联的转化率为75%,柠檬酸酯产量极低。
对所公开的实施例的上述说明,使本领域专业技术人员能够实现或使用本发明。对这些实施例的多种修改对本领域的专业技术人员来说将是显而易见的,本文中所定义的一般原理可以在不脱离本发明的精神或范围的情况下,在其它实施例中实现。因此,本发明将不会被限制于本文所示的这些实施例,而是要符合与本文所公开的原理和新颖特点相一致的最宽的范围。
- 还没有人留言评论。精彩留言会获得点赞!