一种含锌和钼酸根离子的金属基配合物及其合成方法与流程
1.本发明涉及一种含锌和钼酸根离子的金属基配合物及其合成方法。
背景技术:
2.1890年l.mond等在研究一氧化碳对金属镍的腐蚀的过程中,发现了第一个金属基配合物
‑
四羧基合镍ni(co)4,随后人们又进一步研究发现了含有负价态以及含正一价、二价、三价、四价过渡金属的金属羰基阴离子。到目前,已经发现了几千种金属基配合物。常见的为二元的单核或多核金属炭基配合物,即只含有一种金属元素及co一种配体的电中性配合物。
3.金属离子配合物具有优异的特性,其结构确定,含有多功能基团,同时具有大分子特性和金属离子特性。由于金属离子配合物在构型上的特殊性使其在催化剂合成、药物合成、电化学运用、与阻燃抑烟剂复配等方面有着广泛的应用,特别是在超分子化学、生物和医学等领域具有更加广阔的应用前景。一直以来,金属基配合物的金属离子与大分子之间的相互作用是国内外研究热点之一。然而,至今为止,对于金属离子配合物的合成仍然是化学领域的重大挑战。除了研究广泛的金属羟基配合物,对于其他金属基阴离子配合物的合成鲜少见于报道。
技术实现要素:
4.针对上述的目前对于金属离子配合物的研究存在的问题,本发明提出一种含锌和钼酸根离子的金属基配合物[zn(dn)mo]及其合成方法,该配合物是以对苯乙烯磺酸钠,丙烯酰氧乙基三甲基氯化铵溶液,n,n
’‑
亚甲基双丙烯酰胺、α
‑
酮戊二酸、钼酸钠和氯化锌为原料运用化学法合成。具体技术方案如下:
[0005]
首先,本发明提供一种含锌和钼酸根离子的金属基配合物,该金属基配合物是由含c6h5o3s
‑
和n,n,n
‑
三甲基乙铵根离子的有机物基体与锌离子和钼酸根离子配合形成的离子配合物,其分子结构式为:
[0006][0007]
其次,本发明提供一种前述的含锌和钼酸根离子的金属基配合物的合成方法,包含如下步骤:
[0008]
1)原料溶解:将用于制备含有c6h5o3s
‑
和n,n,n
‑
三甲基乙铵根离子的有机物基体
原料混合后加入合适的溶剂在水浴条件下进行完全溶解,获得有机物基体溶液;
[0009]
2)光照交联:将步骤1)中制备的有机物基体溶液加入模具中于光照条件下进行光照交联,形成有机物基体;
[0010]
3)离子交换:将步骤2)中光照交联获得的有机物基体,先后浸泡于锌离子和钼酸根离子溶液中一定时间,进行离子交换,获得离子配合物初成品;
[0011]
4)干燥研磨:将步骤3)中离子交换获得的离子配合物初成品于一定的干燥条件下干燥后,研磨成粉,即获得成品的含锌和钼酸根离子的金属基配合物。
[0012]
作为优选的技术方案的,步骤1)中,所述含有c6h5o3s
‑
和n,n,n
‑
三甲基乙铵根离子的有机物基体原料包括:对苯乙烯磺酸钠,丙烯酰氧乙基三甲基氯化铵溶液,n,n
’‑
亚甲基双丙烯酰胺和α
‑
酮戊二酸;其溶解的溶剂为蒸馏水,所述水浴的温度为55~65℃。
[0013]
作为进一步优选的技术方案的,所述含有c6h5o3s
‑
和n,n,n
‑
三甲基乙铵根离子的有机物基体原料的各组分按重量份计为:对苯乙烯磺酸钠255~265份,丙烯酰氧乙基三甲基氯化铵溶液285~295份,n,n
’‑
亚甲基双丙烯酰胺0.34~0.45份,α
‑
酮戊二酸0.34~0.45份。
[0014]
作为优选的技术方案的,步骤2)中,所述光照交联的光照条件为紫外灯下照射12~16h。
[0015]
作为优选的技术方案的,步骤3)中,所述离子交换的具体操作为:
[0016]
先将有机物基体浸泡于zncl2溶液中3天以上,使zn
2+
与有机物基体的c6h5o3s
‑
形成稳定的离子键;再将其浸泡于na2moo4溶液中3天以上,使moo
42
‑
与有机物基体的n,n,n
‑
三甲基乙铵根离子形成稳定的离子键。
[0017]
其中,所述离子交换所用的锌离子溶液为优选为zncl2溶液,其浓度优选为0.5~2mol/l;所用的钼酸根离子溶液优选为na2moo4溶液,其浓度优选为0.5~2mol/l。
[0018]
作为优选的技术方案的,步骤3)中,所述干燥条件为70~90℃温度下干燥8~10h;所述研磨成粉的粒径大小为小于100目。
[0019]
前述的含锌和钼酸根离子的金属基配合物的合成方法,还包括检测步骤,即将干燥研磨获得的含锌和钼酸根离子的金属基配合物分别进行x
‑
射线光电子能谱,x射线衍射,红外光谱和热失重检测分析,判定锌元素和钼元素是否成功引入有机物基体中。
[0020]
各检测分析的判断标准分别为:
[0021]
x
‑
射线光电子能谱数据:分别在164ev、232.1ev、285ev、402ev、530.6ev和1021.8ev处有xps信号。
[0022]
xrd能谱图数据:zn(dn)mo的xrd曲线杂乱无序,结晶度很低,zncl2,na2moo4和znmoo4等为晶体,说明合成了无序的非晶态结构zn(dn)mo。
[0023]
ftir光谱图数据:用红外特征峰验证合成的物质是zn(dn)mo。
[0024]
tg图数据:根据结构分析其tg特性,用样品tg加以对比,进一步验证合成了zn(dn)mo。同时检测zn(dn)mo的热稳定性能。
[0025]
本发明的有益效果是:
[0026]
本发明通过以对苯乙烯磺酸钠,丙烯酰氧乙基三甲基氯化铵溶液,n,n
’‑
亚甲基双丙烯酰胺、α
‑
酮戊二酸为原料制备成有机物基体,然后将该有机物基体先后分别浸泡于锌离子和钼酸根离子溶液中使其进行离子交换,将zn2+和moo42
‑
分别与有机物基体的
c6h5o3s
‑
和n,n,n
‑
三甲基乙铵根离子形成稳定的离子键,制成含锌和钼酸根离子的金属基配合物。
[0027]
本发明制备方法简单,反应物原料价格便宜,得率较高。制备金属基配合物弥补除了金属羟基配合物之外金属配合物空白,可用于催化剂合成、药物合成、电化学运用、阻燃剂复配、超分子化学、生物和医学等领域,具有广阔的应用前景及实用价值。
附图说明
[0028]
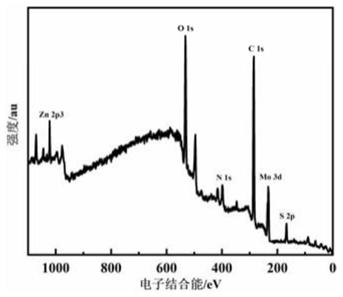
图1为本发明含锌和钼酸根离子的金属基配合物的xps信号图;
[0029]
图2为本发明含锌和钼酸根离子的金属基配合物的xrd能谱图;
[0030]
图3为本发明含锌和钼酸根离子的金属基配合物的ftir光谱图;
[0031]
图4为本发明含锌和钼酸根离子的金属基配合物的tg图。
具体实施方式
[0032]
为使本发明的目的、技术方案和优点更加清楚,下面将结合实施例,对本发明的技术方案进行清楚、完整地描述。其中实施例1为一种含锌和钼酸根离子的金属基配合物,实施例2~4为合成含锌和钼酸根离子的金属基配合物,实施例5为检测合成的含锌和钼酸根离子的金属基配合物。
[0033]
实施例1
[0034]
本实施例提供一种含锌和钼酸根离子的金属基配合物,该金属基配合物是由含c6h5o3s
‑
和n,n,n
‑
三甲基乙铵根离子的有机物基体与锌离子和钼酸根离子配合形成的离子配合物,其分子结构式为:
[0035][0036]
实施例2
[0037]
本实施例是合成一种含锌和钼酸根离子的金属基配合物,具体步骤如下:
[0038]
首先,按一定的摩尔配比称取对苯乙烯磺酸钠(nass),丙烯酰氧乙基三甲基氯化铵溶液(dmaea
‑
q),n,n
’‑
亚甲基双丙烯酰胺(mbaa)以及α
‑
酮戊二酸(ka)合成一种可以引入金属离子的有机物基体。具体操作如下:称取nass 2.6062g,dmaea
‑
q 2.9055g,mbaa 0.0039g,ka 0.0037g;将以上物质混合后加入蒸馏水定容到10ml,放入60℃水浴锅中不停搅拌直至完全溶解,获得有机物基体溶液。
[0039]
将上述有机物基体溶液加入模具中,放在紫外灯下照射12h进行光照交联,形成有机物基体;然后先将该有机物基体浸泡于zncl2溶液中(1mol/l,50ml)中3天,使zn
2+
与有机物基体的c6h5o3s
‑
形成稳定的离子键;再将其浸泡于na2moo4溶液(1mol/l,50ml)中3天,使
moo
42
‑
和n,n,n
‑
三甲基乙铵根离子(c4h
11
n
+
)形成稳定的离子键;最后于80℃温度下干燥8h,再将其研磨粒径为110目的粉末,即获得含锌和钼酸根离子的金属基配合物。
[0040]
实施例3
[0041]
本实施例也是合成一种含锌和钼酸根离子的金属基配合物,其合成步骤与实施例1一致,具体如下:
[0042]
分别称取nass 260.62g,dmaea
‑
q 290.55g,mbaa 0.39g,ka 0.37g;将以上物质混合后加入蒸馏水定容到1000ml,放入58℃水浴锅中不停搅拌直至完全溶解,获得有机物基体溶液。
[0043]
将上述有机物基体溶液加入模具中,放在紫外灯下照射14h进行光照交联,形成有机物基体;然后先将该有机物基体浸泡于zncl2溶液中(1.5mol/l,500ml)中5天,使zn
2+
与有机物基体的c6h5o3s
‑
形成稳定的离子键;再将其浸泡于na2moo4溶液(1.5mol/l,5000ml)中5天,使moo
42
‑
和n,n,n
‑
三甲基乙铵根离子(c4h
11
n
+
)形成稳定的离子键;最后于75℃温度下干燥10h,再将其研磨粒径为105目的粉末,即获得含锌和钼酸根离子的金属基配合物。
[0044]
实施例4
[0045]
本实施例同样是合成一种含锌和钼酸根离子的金属基配合物,其合成步骤也与实施例1一致,具体如下:
[0046]
分别称取nass 130.31g,dmaea
‑
q 145.275g,mbaa 0.195g,ka 0.185g;将以上物质混合后加入蒸馏水定容到500ml,放入62℃水浴锅中不停搅拌直至完全溶解,获得有机物基体溶液。
[0047]
将上述有机物基体溶液加入模具中,放在紫外灯下照射12h进行光照交联,形成有机物基体;然后先将该有机物基体浸泡于zncl2溶液中(1mol/l,2500ml)中3天,使zn
2+
与有机物基体的c6h5o3s
‑
形成稳定的离子键;再将其浸泡于na2moo4溶液(1mol/l,2500ml)中4天,使moo
42
‑
和n,n,n
‑
三甲基乙铵根离子(c4h
11
n
+
)形成稳定的离子键;最后于85℃温度下干燥9h,再将其研磨粒径为120目的粉末,即获得含锌和钼酸根离子的金属基配合物。
[0048]
实施例5
[0049]
任意取实施例2~4合成含锌和钼酸根离子的金属基配合物进行x
‑
射线光电子能谱,x射线衍射,红外光谱和热失重检测分析,判定锌元素和钼元素是否成功引入有机物基体中。
[0050]
经检测,在164ev、285ev、402ev和530.6ev处存在xps信号,其分别对应zn(dn)mo中有机物基体的s2p、c1s、n1s和o1s元素;另外在232.1ev和1021.8ev处存在xps信号,其分别对应zn(dn)mo中mo3d和zn2p3元素,这说明锌元素和钼元素成功引入有机物基体中(见附图1)。
[0051]
xrd能谱图数据:zn(dn)mo的xrd曲线杂乱无序,结晶度很低,图表面生成zn(dn)mo,不含有zncl2,na2moo4和znmoo4等晶体(见附图2)。
[0052]
ftir光谱图数据:zn(dn)mo与有机配合物的红外光谱图,zn(dn)mo在3418.78cm
‑1和1639.38cm
‑1处的吸收峰未消失,说明产物中还存在
‑
oh键,因此合成的fe(dn)mo中还含有结晶水。有机配合物在1185.9cm
‑1处有吸收峰,该产物存在na
‑
o
‑
s网络。zn(dn)mo在1182.7cm
‑1处有一条宽吸收峰,说明产物中形成了zn
‑
o
‑
s网络。此外,zn(dn)mo在838.09cm
‑1有一条较强的吸收峰,而mo=o键的吸收峰位于964cm
‑1左右,则表明该产物的强吸收峰是
由mo
‑
n键的拉伸振动形成的(见附图3)。
[0053]
tg图数据:由于zn(dn)mo中含有少量的水分和小分子,随着温度不断上升时会形成水蒸气和低分子气态化合物,因此在30℃
‑
300℃之间曲线都有轻微的下降趋势。在320℃
‑
480℃之间阻燃抑烟剂中的有机配合物开始分解,此外zn(dn)mo的残余量为64.1%。曲线与分析抑制,进一步验证合成了zn(dn)mo,而且具有良好的热稳定性能(见附图4)。
[0054]
本发明含锌和钼酸根离子的金属基配合物弥补除了金属羟基配合物之外金属配合物空白,可用于催化剂合成、药物合成、电化学运用、阻燃抑烟剂复配、超分子化学、生物和医学等领域。
[0055]
本发明方法通过以对苯乙烯磺酸钠,丙烯酰氧乙基三甲基氯化铵溶液,n,n
’‑
亚甲基双丙烯酰胺、α
‑
酮戊二酸为原料制备成有机物基体,然后将该有机物基体先后分别浸泡于锌离子和钼酸根离子溶液中使其进行离子交换,将zn
2+
和moo
42
‑
分别与有机物基体的c6h5o3s
‑
和n,n,n
‑
三甲基乙铵根离子形成稳定的离子键,制成含锌和钼酸根离子的金属基配合物,方法简单,反应物原料价格便宜,且得率较高,具有广阔的应用前景及实用价值。
[0056]
对于本领域技术人员而言,显然本发明不限于上述示范性实施例的细节,而且在不背离本发明的精神或基本特征的情况下,能够以其他的具体形式实现本发明。因此,无论从哪一点来看,均应将实施例看作是示范性的,而且是非限制性的。此外,应当理解,虽然本说明书按照实施方式加以描述,但并非只包含这些的技术方案,说明书的这种叙述方式仅仅是为清楚起见,本领域技术人员应当将说明书作为一个整体,实施例中的技术方案也可以经适当组合,形成本领域技术人员可以理解的其他实施方式。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1