生物标志物在肺动脉高压诊疗中的应用的制作方法
1.本发明涉及生物医学领域,涉及生物标志物在肺动脉高压诊疗中的应用。
背景技术:
2.肺动脉高压(pulmonaryhypertension,ph)是以肺动脉压力和肺小血管阻力进行性增加为特征的临床
‑
病理生理综合征(hoepermm,bogaardhj,condliffer,etal.definitionsanddiagnosisofpulmonaryhypertension[j].jamcollcardio1,2013,62:42
‑
50),主要表现为肺血管过度收缩、肺小动脉重构,从而引起肺血管阻力的增加来实现肺动脉压力的逐渐升高,最终导致心力衰竭而危及生命。美国流行病学统计资料表明,ph患病率至少为10.6/100万,ph年发病率至少为2/100万(mcgoonmichaeld,benzaraymondl,escribano
‑
subiaspilar,eta1.pulmonaryarterialhypertension:epidemiologyandregistries[j].turkkardiyoldernars,2014,null:67
‑
77)。ph患者临床预后极差,目前全球约有1亿人受到ph的威胁,由于治疗效果差和疾病不可逆性的迅速进展,其死亡率居高不下,如确诊的ph不及时控制,患者预期中位生存期仅2.8年(hoepermm,mclvv,dalaanam,eta1,treatmentofpulmonaryhypertension[j].lancetrespirmed,2016,4(4):323
‑
336.)。
[0003]
ph的发生与遗传、个体、环境等多种因素相关,其定义是指在静息状态下平均肺动脉压)25mmhg,欧洲心脏病学会/欧洲呼吸病学会(esc/ers于2015年发布了最新版《肺动脉高压诊断和治疗指南》,将肺动脉高压分为动脉性ph、左心疾病相关性ph、肺部疾病和(或)缺氧导致ph、慢性血栓栓塞性ph及机制不明和/或多因素所致ph五大类,但目前研究发现不同类型的ph发生发展存在共同的病理基础,包括:肺血管收缩、肺血管重构、原位血栓形成,其中肺小动脉重构是主要环节(bujakr,mateoj,blancoi,etal.newbiochemicalinsightsintothemechanismsofpulmonaryarterialhypertensioninhumans[j].plosone,2016,11:e0160505.)。
[0004]
在ph出现症状前,相当比例的肺血管床已经消失,甚至在症状轻微的ph患者中肺血管阻力已显著增加。现有的心导管检查及影像学检查对早期ph的诊断较为困难。因此寻找新的生物标记物具有重要的临床意义。
技术实现要素:
[0005]
为了弥补现有技术的不足,本发明基于基因在肺动脉高压的发生发展中的作用,研究与肺动脉高压发生发展相关的生物标志物,从而为肺动脉高压的诊断和治疗提供新的手段。
[0006]
本发明提供了检测生物标志物的试剂在制备诊断肺动脉高压的产品中的应用,生物标志物包括clec2l、spns3和/或fam86b1。
[0007]
进一步,与正常对照相比,clec2l、fam86b1在肺动脉高压患者中的表达水平上调,spns3在肺动脉高压患者中的表达水平下调。
[0008]
进一步,所述试剂包括:特异性识别clec2l、spns3或fam86b1基因的探针;特异性扩增clec2l、spns3或fam86b1基因的引物;或特异性结合clec2l、spns3或fam86b1编码的蛋白的结合剂。
[0009]
进一步,所述样本选自组织、血液。
[0010]
进一步,所述样本选自血液。
[0011]
本发明提供了一种诊断肺动脉高压的产品,所述产品包括检测生物标志物clec2l、spns3和/或fam86b1水平的试剂。
[0012]
进一步,所述试剂包括在mrna水平或蛋白水平上检测生物标志物clec2l、spns3和/或fam86b1表达水平的试剂。
[0013]
进一步,所述产品包括通过聚合酶链反应、实时荧光定量逆转录多聚酶链反应、逆转录聚合酶链反应、竞争性聚合酶链反应、核酸酶保护分析、原位杂交法、核酸微阵列、rna印迹或dna芯片的方法进行检测mrna水平的试剂。
[0014]
进一步,所述产品包括通过免疫印迹、酶联免疫吸附试验、放射免疫分析、放射免疫扩散法、免疫电泳、组织免疫染色、免疫沉淀分析法、补体固定分析法、荧光激活细胞分选、质量分析或蛋白质微阵列的方法进行检测蛋白水平的试剂。
[0015]
本发明提供了生物标志物在构建预测肺动脉高压的计算模型中的应用,所述生物标志物包括clec2l、spns3和/或fam86b1。
[0016]
本发明提供了一种预测肺动脉高压的装置,所述装置包括:处理器;输入模块,用于输入生物样品中生物标志物的水平,所述生物标志物选自clec2l、spns3和/或fam86b1。
[0017]
包含指令的计算机可读介质,所述指令在由所述处理器执行时在生物标志物的输入水平上执行算法;以及输出模块,指示受试者是否患有肺动脉高压或者存在患肺动脉高压的风险。
[0018]
本发明的有益效果:本发明通过检测clec2l、spns3和/或fam86b1的表达水平,可以实现肺动脉高压的早期诊断,增加检测的敏感度,提高检测能力和效率,积极采取干预措施,不仅可以延缓ph的进展、降低致残致死率,甚至可能达到早期治愈的效果。
附图说明
[0019]
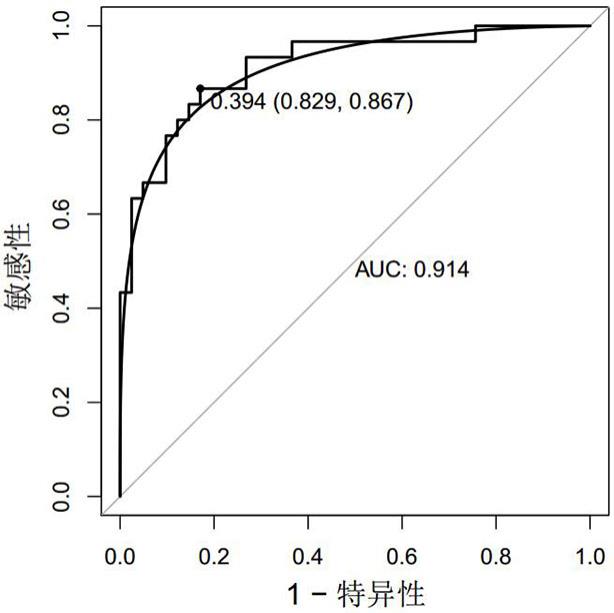
图1显示clec2l基因表达图;图2显示spns3基因表达图;图3显示fam86b1基因表达图;图4显示clec2l基因诊断肺动脉高压的roc曲线图;图5显示spns3基因诊断肺动脉高压的roc曲线图;图6显示fam86b1基因诊断肺动脉高压的roc曲线图;图7显示clec2l+spns3基因诊断肺动脉高压的roc曲线图;图8显示clec2l+fam86b1基因诊断肺动脉高压的roc曲线图;
图9显示spns3+fam86b1基因诊断肺动脉高压的roc曲线图;图10显示clec2l+spns3+fam86b1联合诊断肺动脉高压的roc曲线图。
[0020]
具体实施方式
[0021]
以下将对本发明进一步详细说明,应理解,所述用语旨在描述目的,而非限制本发明。
[0022]
术语“和/或”是指并且包括一个或多个相关联的所列项目的任何和所有可能的组合,以及在备选方案(或)中解释时缺少组合。
[0023]
术语
ꢀ“
样本
”ꢀ
或
ꢀ“
测试样本
”ꢀ
指获自或衍生自目的个体的生物试样,生物试样的供给源可以是新鲜、冷冻和/或保存的器官或组织样品或从活检或引物产生的固体组织;血液或任意血液组分。术语
ꢀ“
样本
”ꢀ
或
ꢀ“
测试样本
”ꢀ
包括在其获得后以任意方式操作过的生物样本,如通过试剂处理、稳定化、或针对某些成分(如蛋白质或多核苷酸)富集、或包埋在用于切片目的的半固体或固体基质中。在本发明的一实施例中,将组织组分用作试样。
[0024]
术语“生物标志物”宽泛地是指存在于或源自样品的任何可检测化合物,如蛋白质、肽、蛋白聚糖、糖蛋白、脂蛋白、碳水化合物、脂质、核酸(例如dna,诸如cdna或扩增的dna,或rna,诸如mrna)、有机或无机化学物质、天然或合成的聚合物、小分子(例如,代谢物)或上述任何物质的区分分子或区分片段。如这段内容中使用的
ꢀ“
源自
”ꢀ
是指检测时指示存在于样品中的特定分子的化合物。例如,特定cdna的检测可以指示样品中特定rna转录物的存在。作为另一个实例,特定抗体的检测或与特定抗体的结合可以指示样品中特定抗原(例如,蛋白质)的存在。在此,区分分子或片段是检测时指示以上鉴定的化合物的存在或丰度的分子或片段。生物标志物例如可以分离自样品、直接在样品中测量,或在样品中检测或测定。生物标志物可以例如是功能性的、部分功能性的或非功能性的。
[0025]
在本发明中,所述生物标志物包括clec2l、spns3和/或fam86b1。生物标志物例如clec2l(c
‑
type lectin domain family 2 member l,gene id:154790)、spns3(sphingolipid transporter 3,gene id:201305)、fam86b1(family with sequence similarity 86 member b1,gene id:85002);包括基因及其编码的蛋白及其同源物,突变,和同等型。该术语涵盖全长,未加工的生物标志物,以及源自细胞中加工的任何形式的生物标志物。该术语涵盖生物标志物的天然发生变体(例如剪接变体或等位变体)。gene id可在https://www.ncbi.nlm.nih.gov/gene/获得。
[0026]
术语
ꢀ“
引物
”ꢀ
是指短核酸序列,其具有短的游离3 羟基的核酸序列,能够与互补的模板形成碱基对,其充当用于模板链复制的起点。引物可以在适当的缓冲液及温度下,在用于聚合反应(即,dna聚合酶或逆转录酶)的试剂及不同的4种核苷三磷酸的存在下诱发dna合成。
[0027]
术语
ꢀ“
探针
”ꢀ
是指对应于能够特异性结合mrna的数个碱基至数百个碱基的核酸片段,例如rna或dna等。由于被标记,因而可以确认是否存在特定的mrna。探针能够以寡核苷酸探针、单链dna探针、双链dna探针、rna探针等形式制造。在本发明中,利用与clec2l、spns3和/或fam86b1基因互补的探针进行杂交,并且可通过是否杂交来诊断上述基因的表达水平。可以基于本技术领域中公知的技术来更改用于合适探针的选择及杂交条件,在本
发明中,对此没有特别限制。
[0028]
本发明的引物或探针可以使用亚磷酰胺固相载体方法或其他公知的方法化学合成。这种核酸序列可以利用本领域中公知的多种手段来进行变形。这种变形的非限制性实施例包括甲基化、封装、天然核苷酸的一种以上的同源物的取代以及核苷酸之间的变形,例如,变形为不带电的连接体(例:膦酸甲酯、磷酸三酯、氨基磷酸酯、氨基甲酸酯等)或带电的连接体(例:硫代磷酸酯,二硫代磷酸酯等)。
[0029]
在本发明中,可通过优化步骤在一系列过程中确定使探针与cdna分子杂交的合适条件。该步骤由本领域普通技术人员通过一系列过程进行,以建立用于在研究室中使用的协议。例如,温度、成分浓度、杂交及洗涤时间、缓冲液成分及其ph以及离子强度等条件取决于探针的长度、gc量及靶核苷酸序列等各种因素。
[0030]
术语
ꢀ“
表达的水平
”ꢀ
或
ꢀ“
表达水平
”ꢀ
一般可互换使用,通常指生物样品中多核苷酸或氨基酸产物或蛋白质的量。
ꢀ“
表达
”ꢀ
通常指基因编码的信息转化为在细胞中存在和运转的结构的过程。因此,本文所用的基因的
ꢀ“
表达
”ꢀ
指转录为多核苷酸、翻译为蛋白质、或甚至蛋白质的翻译后修饰。转录的多核苷酸、翻译的蛋白质或翻译后修饰的蛋白质的片段也视为表达的,无论它们是源自通过选择性剪接产生的转录物或降解的转录物,还是源自蛋白质的翻译后加工(例如,通过蛋白水解)。“表达的基因
”ꢀ
包括转录为多核苷酸(如mrna)然后翻译为蛋白质的那些,以及转录为rna但不翻译为蛋白质的那些(例如,转运rna和核糖体rna)。
[0031]
本文用术语
ꢀ“
诊断”来指分子或病理学状态、疾病或病症的鉴定或分类。例如,“诊断
”ꢀ
可以指,通过所累及的组织/器官(例如,肺动脉高压),或通过分子特征(例如,表征为特定基因或该基因所编码的蛋白质之一或其组合的表达),鉴定患肺动脉高压的风险。
[0032]“辅助诊断”来指辅助就症状或病症的具体类型的存在或性质作出临床决定的方法。例如,辅助诊断肺动脉高压方法可以包括测量某些基因在来自个体的生物样品中的表达。
[0033]
术语“抗体”在本文中以最广泛的含义使用,且包括单克隆抗体( 例如,全长或完整的单克隆抗体)、多克隆抗体、多价抗体、多特异性抗体( 例如,双特异性抗体,只要它们显示希望的生物学活性),且也可以包括某些抗体片段( 如本文更详细地描述)。抗体可以是人、人源化和/或亲和力成熟的抗体。
[0034]“抗体片段
”ꢀ
仅包含完整抗体的部分,其中该部分优选保留与该部分存在于完整抗体中时通常相关的功能的至少一种,优选多数或全部。在一个实施方案中,抗体片段包含完整抗体的抗原结合部位,从而保持结合抗原的能力。在另一实施方案中,抗体片段( 例如包含fc区的抗体片段)保留通常与该fc区存在于完整抗体中时相关的生物学功能的至少一种,如fcrn结合、adcc功能和补体结合。在一个实施方案中,抗体片段是单价抗体,其具有基本上类似于完整抗体的体内半衰期。例如,这种抗体片段可以包含与能够赋予该片段体内稳定性的fc序列连接的抗原结合臂。
[0035]
本文所用的术语
ꢀ“
单克隆抗体
”ꢀ
指从基本上同质的抗体群体获得的抗体,即除了可以少量存在的可能的天然存在的突变外,包含该群体的单种抗体是相同的。单克隆抗体高度特异,针对单一抗原。此外,与通常包括针对不同决定簇(表位)的不同抗体的多克隆抗体制剂不同,每种单克隆抗体针对抗原上的单个决定簇。
[0036]
本文的单克隆抗体特别包括
ꢀ“
嵌合
”ꢀ
抗体,其中重链和/或轻链的一部分与衍生自特定物种或隶属于特定抗体种类或亚类的抗体中对应的序列相同或同源,一条或多条链的其余部分与衍生自另一物种或隶属于另一抗体种类或亚类的抗体中对应的序列相同或同源,以及这类抗体的片段,只要它们显示希望的生物学活性。
[0037]
术语
ꢀ“
双抗体
”ꢀ
指具有两个抗原结合部位的小的抗体片段,该片段包含在同一条多肽链中与可变轻链结构域(vl)连接的可变重链结构域(vh)( vh
‑
vl)。通过使用太短而不允许同一条链上的两个结构域之间配对的接头,迫使结构域与另一条链上的互补结构域配对,并产生两个抗原结合部位。
[0038]
本文所述的基因表达水平的检测可以采用本领域已知的测定方法,包括但不限于检测所述生物标志物的rna转录物的量或所述生物标志物编码的多肽的量的方法。
[0039]
生物标志物的rna转录物可通过本领域已知的方法转化为与其互补的cdna,通过测定互补cdna的量可以获得rna转录物的量。生物标志物的rna转录物或与其互补的cdna的量,可以针对样本中总rna或总cdna的量或者针对一组看家基因的rna转录物或与其互补的cdna的量来标准化。
[0040]
在本文中,rna转录物可以通过例如杂交、扩增、测序的方法来检测和量化,包括但不限于将rna转录物与探针或者引物杂交的方法,通过基于聚合酶链式反应(pcr)的各种定量pcr技术或测序技术检测rna转录物或其对应cdna产物的量的方法。所述定量pcr技术包括但不限于荧光定量pcr、实时pcr或半定量pcr技术。所述测序技术包括但不限于sanger测序、二代测序、三代测序和单细胞测序等。优选地,所述测序技术为二代测序,更优选地为靶向rna
‑
seq技术。
[0041]
在本文中,多肽的量可以通过例如蛋白组学或试剂来检测。优选地,所述试剂为抗体、抗体片段或者亲和性蛋白。在本文提供的方法中可以使用任何合适的蛋白质定量方法。在某些实施方案中,使用基于抗体的方法。可使用的示例性方法包括但不限于免疫印迹法(蛋白质印迹(western blot))、酶联免疫吸附测定(elisa)、免疫组织化学、流式细胞术、流式细胞术微珠阵列和质谱法。elisa的一些类型是常用的,包括直接elisa、间接elisa和夹心elisa。
[0042]
应用本发明涉及用于测定样品中生物标志物的试剂在制备肺动脉高压的诊断产品中的应用,所述生物标志物包括clec2l、spns3和/或fam86b1。
[0043]
优选地,所述诊断产品包括检测样品中clec2l、spns3和/或fam86b1表达水平的试剂。
[0044]
作为可选择的实施方案,所述试剂包括:特异性识别clec2l、spns3或fam86b1基因的探针;特异性扩增clec2l、spns3或fam86b1基因的引物;或特异性结合clec2l、spns3或fam86b1编码的蛋白的结合剂。
[0045]
作为可选择的实施方案,蛋白的结合剂包括但不限于是肽、肽模拟物、aptamer、spiegelmer、darpin、锚蛋白重复蛋白、kunitz型域、抗体、单域抗体和单价抗体片段。
[0046]
作为一种优选地实施方案,蛋白的结合剂为抗体。
[0047]
作为可选择的实施方案,样本包含来自受试者的血浆、血清或血液抽取物、刷洗
物、活组织检查物或外科手术切除的组织或液体样品。
[0048]
(诊断)产品本发明涉及一种诊断肺动脉高压的产品,所述产品包括检测生物标志物clec2l、spns3和/或fam86b1的试剂。
[0049]
在一实施方案中,所述试剂为检测所述生物标志物表达水平的试剂。
[0050]
在一实施方案中,所述诊断产品为体外诊断产品的形式。
[0051]
在一具体的实施方案中,所述诊断产品为诊断试剂盒。
[0052]
在一实施方案中,所述试剂为检测所述生物标志物转录的rna,特别是mrna的量的试剂。在又一实施方案中,所述试剂为检测与所述mrna互补的cdna的量的试剂。
[0053]
在一优选的实施方案中,所述诊断产品还包括总rna抽提试剂、逆转录试剂和/或二代测序试剂。
[0054]
所述总rna抽提试剂可以为本领域常规的总rna抽提试剂。
[0055]
所述逆转录试剂可以为本领域常规的逆转录试剂,并且优选地包括dntp溶液和/或rna逆转录酶。
[0056]
所述二代测序试剂可以为本领域常规使用的试剂,只要能够满足对所得序列进行二代测序的要求即可。二代测序试剂可以为市售产品,其实例包括但不限于illumina公司miseq
®ꢀ
reagent kit v3(150cycle)(ms
‑
102
‑
3001)、truseq
®ꢀ
targeted rna index kita
‑
96indices(384samples)(rt
‑
402
‑
1001)。二代测序为本领域常规的二代测序,例如为靶向rna
‑
seq技术。因此,二代测序试剂还可以包括可供构建靶向rna
‑
seq的文库illumina定制的试剂,例如targeted rna custom panel kit(96samples)(rt
‑
102
‑
1001)。
[0057]
在优选的实施方案中,所述试剂为探针或引物。
[0058]
在可选的实施方案中,所述试剂为检测所述生物标志物编码的多肽的量的试剂。
[0059]
在具体的实施方案中,所述试剂为抗体、抗体片段或者亲和性蛋白。
[0060]“试剂盒
”ꢀ
是包含至用于特异性检测本发明的生物标志基因或蛋白质的探针的制成品(例如,包装或容器)。在某些实施方案中,该制成品作为用于进行本发明的方法的单位推销、分销或销售。
[0061]
这类试剂盒可以包含区室化来紧密限制地容纳一个或多个容器手段(如小瓶、管等)的载体手段,每个容器手段包含将要在方法中使用的分开的组成部分之一。例如,容器手段之一可以包含进行可检测标或可以进行可检测标记的探针。这种探针可以是对包含基因表达特征的一个或多个基因的多核苷酸特异的多核苷酸。在试剂盒利用核酸杂交来检测靶核酸时,试剂盒还可以具有包含用于扩增靶核酸序列的一种或多种核酸的容器和/或包含报道手段的容器,如生物素结合蛋白,如抗生物素蛋白或链霉抗生物素蛋白,结合于报道分子,如酶、荧光或放射性同位素标记。
[0062]
试剂盒通常将包含上述容器和一个或多个其他容器,该其他容器包含商业和用户角度希望的物质,包括缓冲液、稀释液、滤器、针头、注射器和含有使用说明的包装说明书。容器上可以存在标签来指示该组合物用于具体的治疗或非治疗性应用,且还可以指示体内或体外使用的方向,如上文所述的那些。试剂盒中的其他可选成分包括一种或多种缓冲液( 例如封闭缓冲液、洗涤缓冲液、底物缓冲液等)、其他试剂(如通过酶标记发生化学改变的底物)、表位修复溶液、对照样品(阳性和/或阴性对照)、对照切片等。
0.5(两个组的测试值之间没有明显分布差异)之间。面积不仅取决于线图的特定部分诸如最接近对角线的点或 90% 特异性处的灵敏度,而且还取决于整个线图。这是 roc 线图如何接近完美者(面积 =1.0)的一种定量、描述性表述。
[0070]
装置本发明提供了一种诊断/预测肺动脉高压的装置,所述装置包括:处理器;输入模块,用于输入生物样品中生物标志物的水平,所述生物标志物选自clec2l、spns3和/或fam86b1;包含指令的计算机可读介质,所述指令在由所述处理器执行时在生物标志物的输入水平上执行算法;以及输出模块,指示受试者是否患有肺动脉高压或者存在患肺动脉高压的风险。
[0071]
如本文应用的装置应至少包括上述模块。装置的模块可操作地彼此连接。如何以操作方式链接将取决于装置中包含的模块的类型。
[0072]
所述处理器可以执行一系列的机器可读指令,该机器可读指令可以以程序或软件来体现。指令可以被存储于存储器位置,诸如存储器中。指令可以被导向处理器,该指令可以随后编程或以其他方式配置处理器以实现本公开内容。由处理器进行的操作的实例可以包括读取、解码、执行和写回。
[0073]
下面结合附图和实施例对本发明作进一步详细的说明。以下实施例仅用于说明本发明而不用于限制本发明的范围。实施例中未注明具体条件的实验方法,通常按照常规条件,或按照制造厂商所建议的条件。
[0074] 实施例1与肺动脉高压相关的生物标志物的检测1、样本采集收集7例慢性血栓栓塞性肺动脉高压(cteph)患者和5例健康人群对照组的血液样本,在收集样本时详细记录患者以及健康对照组的基本信息,包括年龄,性别,bmi等,其中疾病组和健康组在年龄、性别、bmi等无统计学差异。
[0075]
疾病组纳入标准:经右心导管置入术、肺通气灌注扫描或ct肺血管造影(ctpa)诊断为cteph。cteph的诊断需同时满足以下3 条:
①
至少已行3个月的有效抗凝治疗, 以排除亚急性 pte;
②
v/q 显像扫描显示至少1个肺段灌注缺损,或多层螺旋ct肺动脉成像(computed tomography pul
‑
monaryangiography, ctpa)、mri 或直接肺血管造影等检查发现cteph的特异性征象,如环状狭窄、网格征及缝隙征和动脉闭塞;
③
右心导管测定肺循环血流动力学指标符合肺高压诊断标准 [平均肺动脉压≥25 mm hg(1 mm hg=0.133 k pa)、肺小动脉楔压≤15 mm hg)]。
[0076]
疾病组排除标准:存在循环系统疾病,如恶性肿瘤、高血压、糖尿病、冠心病或脑血管疾病。
[0077]
健康组纳入标准:包括与cteph组年龄、性别相匹配的健康对照组和正常血常规/尿常规/生化试验/癌胚抗原(cea)/甲胎蛋白(afp)/血沉(esr)/胸透。
[0078]
健康组排除标准:排除既往该疾病病史、头部外伤及手术史、心脏手术史或神经系统疾病的人群。
[0079]
2、实验方法
2.1 血液总rna的提取使用bd公司出产的paxgene blood rna kit试剂盒提取血液总rna,操作步骤按说明书进行。
[0080]
2.2样品检测使用 agilent 2100 bioanalyzer (agilent rna 6000 nano kit)检测 total rna 的浓度、rin值、28s/18s 和片段大小。
[0081]
2.3文库的构建与转录组测序1)dnase 消化去除dna:利用dnase i 消化total rna 样品中存在的dna 片段,磁珠纯化回收反应产物,最后溶解于depc 水;2)去除 rrna:取消化好的total rna 样品,使用试剂盒去除rrna,去除之后进行agilent 2100 检测,验证rrna 去除效果;3) rna 打断:取上一步样品,加入打断buffer,置于pcr 仪中进行热打断,打断到130
‑
160nt;4)反转录一链的合成:向打断后的样品中加入适量引物,充分混匀后在 thermomixer 适温反应一定时间,使之打开二级结构并与引物结合,再加入提前配制的一链合成反应体系 mix,在 pcr仪上按相应程序合成一链 cdna;5) 反转录二链的合成:配制二链合成反应体系,在thermomixer 上适温反应一定时间,合成二链 cdna,反应产物用磁珠进行纯化回收。产物用磁珠进行纯化回收;6)末端修复:配制末端修复反应体系,在thermomixer 中适温反应一定时间,在酶的作用下,对反转录得到的cdna 双链的粘性末端进行修复。末端修复产物用磁珠进行纯化回收,最后将样品溶于eb solution ;7)cdna 末端加
ꢀ“
a”:配制加“a”反应体系,在 thermomixer 中适温反应一定时间,在酶的作用下,使末端修复的产物 cdna 的 3’末端加上 a 碱基;8)cdna adapter 的连接:配制接头连接反应体系,在thermomixer 中适温反应一定时间,在酶的作用下,使接头与a 碱基连接,产物用磁珠进行纯化回收;9)pcr 反应及产物回收:配制pcr 反应体系,选择适当的pcr 反应程序,对上步骤得到的产物进行扩增。对pcr产物进行磁珠纯化回收。回收产物溶于eb 溶液中。贴上标签,文库制备至此完成;10)文库质量检测:使用agilent 2100 bioanalyzer (agilent dna 1000 reagents)检测文库的片段大小及浓度;11) pcr 产物环化:将pcr 产物变性为单链后,配制环化反应体系,充分混匀适温反应一定时间,得到单链环形产物,消化掉未被环化的线性dna 分子后,即得到最终的文库;12)上机测序:单链环状 dna 分子通过滚环复制,形成一个包含 200 多个拷贝的 dna 纳米球(dnb)。将得到的 dnbs 采用高密度 dna 纳米芯片技术,加到芯片上的网状小孔内。通过边合成边测序的方法,得到50bp/100bp 的测序读长。
[0082]
2.4测序数据质量控制对原始测序数据进行过滤,从而得到高质量的测序数据(clean data),步骤如下:去除reads中的adapter序列;剪切前去除5’端含有非agct的碱基;修剪测序质量较低的
reads末端 (测序质量值小于q20);去除含n的比例达到10%的reads;舍弃去adapter及质量修剪后长度小于25bp的小片段。
[0083]
2.5 与参考基因组比对使用hisat2分析软件价格测序数据比对到参考基因组上。参考基因组来自于ensembl数据库,基因组版本grch38,基因注释信息为ensemble 92。
[0084]
2.6基因表达水平分析通过比对到参考基因组区域的序列(clean reads)的数量来计算基因的表达水平。使用stringtie根据hisat2软件的比对结果,计算每个基因/转录本在样本中的fpkm值,以该值作为基因/转录本在样本中的表达量。
[0085]
2.7mrna差异表达分析使用deseq2比较对照组跟疾病组mrna的表达差异,差异分析步骤如下:首先对原始的read count进行标准化(normalization),主要是对测序深度的校正;通过统计学模型进行假设检验概率(p
‑
value)的计算,进行多重假设检验校正(bh),得到padj值(错误发现率),差异表达基因的筛选标准为:pvalue<0.05 和 |log2foldchange|>1。
[0086]
3、结果与分析3.1对数据质控后的序列进行数据量统计,结果如表1所示。
[0087]
表1 测序数据统计表(1) sample id:样品信息; (2) total_reads:统计原始序列数据的条数; (3) total_bases:raw reads的条数乘以长度,并转化为以g为单位; (4) q20、q30:分别计算 phred 数值大于20、30的碱基占总体碱基的百分比; (5) gc content:计算碱基g和c的数量总和占总的碱基数量的百分比。
[0088]
3.2 差异表达基因分析对疾病组和健康对照全部样本进行高通量测序分析,与健康对照相比,呈现显著性差异的基因有437个,其中表达上调基因233个,表达下调的基因有204个。
[0089]
其中,fam86b1、clec2l肺动脉高压患者中表达显著上调,spns3在肺动脉高压患者中表达显著下调,具体表达情况如表2所示。
[0090]
表2 基因的差异表达
实施例2差异基因的验证及诊断效能检测1、数据和预处理从geo数据库下载肺动脉高压及其对照的数据集gse33463的基因表达数据,并利用注释文件对其注释,多个探针对应同一个基因的取平均值作为其表达量,然后获得基因表达矩阵文件。
[0091]
2、差异表达分析使用r软件中的“limma”包进行差异基因的表达分析。
[0092]
分析结果显示,fam86b1、clec2l肺动脉高压患者中表达显著上调,spns3在肺动脉高压患者中表达显著下调,其表达情况如图1
‑
3所示,其中,*:p<0.05;**:p<0.01;***:p<0.001。
[0093]
3、诊断效能分析使用r包“proc”roc曲线,分析差异表达基因作为检测变量的auc值、敏感性和特异性,判断其诊断效能。在判断每个基因的诊断效能时,直接使用基因的表达量进行分析。首先调用proc包,然后读入目的基因构建的表达量矩阵,运行绘制roc曲线的命令,同时涉及添加auc,thres(阈值)、smooth(拟合曲线)的命令。在判断基因联合的诊断效能时,首先是使用glmnet对基因进行logistics回归,利用建立的logistic回归模型,使用predict(预测)函数观察某个预测变量在各个水平对结果概率的影响,计算预测概率,绘制预测结果的roc曲线。
[0094]
结果如表3和图4
‑
10所示,从表中可以看出clec2l、spns3、fam86b1及其组合应用于肺动脉高压的诊断具有较高的准确性,尤其是三者的组合,具有较高的准确性、敏感性以及特异性。
[0095]
表3差异表达基因诊断效能分析以上结合附图详细描述了本技术的优选实施方式,但是,本技术并不限于上述实施方式中的具体细节,在本技术的技术构思范围内,可以对本技术的技术方案进行多种简单变型,这些简单变型均属于本技术的保护范围。
[0096]
另外需要说明的是,在上述具体实施方式中所描述的各个具体技术特征,在不矛盾的情况下,可以通过任何合适的方式进行组合,为了避免不必要的重复,本技术对各种可能的组合方式不再另行说明。
[0097]
此外,本技术的各种不同的实施方式之间也可以进行任意组合,只要其不违背本技术的思想,其同样应当视为本技术所公开的内容。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1