一种基于草酸强化的NaBH4快速还原六价铬离子的方法与流程
本发明属于污水处理技术领域,具体涉及一种基于草酸强化的nabh4快速还原六价铬离子的方法。
背景技术:
铬及其化合物是一种重要的化工产品,广泛应用于木材防腐、皮革鞣制、电镀和金属加工等领域。cr(vi)被认为是所有铬化合物中毒性最大的,其毒性大约是cr(iii)的300倍。在水环境中,cr(vi)在整个ph范围内都是可溶的,因此具有很高的迁移率,这加剧了其潜在的危害。此外,cr(vi)在强酸性条件下是一种强氧化剂,当与还原剂或具有可氧化官能团的有机分子共存时,cr(vi)很容易变得不稳定并转化为cr(iii)。在特定的反应条件下,水环境中存在许多可以降低cr(vi)的有机化合物,包括醛、酮、酚、羧酸和芳香烃。但对于大多数有机化合物,由于其还原能力有限,cr(vi)的还原速率非常缓慢。此外,天然水体的酸性不足,即使存在还原性物质,cr(vi)转化为cr(iii)的速度也很慢。因此,一旦cr(vi)进入水体,就会成为一种持久性无机污染物。尽管人们认为环境中绝大多数的cr(vi)来自人类活动,然而,在自然条件下,cr(iii)氧化为cr(vi)也会助力于增加环境中cr(vi)的含量。因此,有必要对含cr(vi)和cr(iii)的废水进行人为干预,以降低cr(vi)和总铬(crt)排放量。
草酸是一种具有还原性的小分子二元羧酸([e0(co2/h2c2o4)]=-0.49),是自然界中最常见的小分子酸。草酸及其盐类通常存在于天然水中,用于许多工业过程,包括制药,木材防腐,化学合成,金属表面清理与处理,纺织印染,皮革加工,催化剂制备,冶金。它们与某些过渡金属元素结合时也表现出很强的配位性,从而形成可溶性配合物,从而大大提高了它们的溶解度。草酸和草酸盐作为还原剂或促进剂处理cr(vi)已得到广泛的研究。尽管如此,与其他有机化合物类似,草酸或草酸盐单独还原cr(vi)的速度非常缓慢。mn2+、fe3+、al3+、光照和光催化材料能够促进草酸或草酸盐对cr(vi)的还原。通常利用电子供体来增强cr(vi)的光催化还原,即利用太阳光或紫外光的诱导作用,建立“cr(vi)–草酸–还原材料”体系。然而,即使在较低的ph下,低浓度cr(vi)的完全还原也需要几十分钟到几个小时,式(1)给出了cr(vi)还原为cr(iii)和草酸氧化为co2的总反应式。
nabh4作为一种反应条件温和的还原剂,在中性甚至弱碱性条件下都能还原cr(vi),nabh4的水解能自然提高溶液体系的ph,无需添加沉淀剂即可完成cr(iii)的自然沉降。此外,nabh4水解可以被催化,这样在较高的ph条件下几乎可以完全去除cr(vi),并且可以产生大量可回收的h2。因此,nabh4对高浓度cr(vi)的处理具有一定的应用潜力。
目前,高浓度cr(vi)废水处理策略主要是将cr(vi)转化为低价态的cr(iii),常见的化学还原法以铁及其亚铁盐或硫化物、亚硫酸盐和水合肼为还原剂。硫系还原剂的问题主要是对ph要求极为苛刻,初始ph需控制在1.0~3.0;此外,还原剂需要过量投加3.5~5倍,直接导致成本增加和产生浓度较高的含硫废水;尤其值得指出的是,还原剂局部浓度过高可产生有毒的so2气体,导致严重的二次污染。
技术实现要素:
本发明的目的是为了进一步强化水体中cr(vi)的处理效果,提供一种基于草酸强化的nabh4快速还原六价铬离子的方法。
为实现上述目的,本发明采取的技术方案如下:
一种基于草酸强化的nabh4快速还原六价铬离子的方法,所述方法步骤如下:
步骤一:将草酸钠加入含有cr(vi)的溶液中,混合均匀后形成混合溶液,控制所述混合溶液中草酸钠的浓度为0.1~10mm;所述含有cr(vi)的混合溶液中cr(vi)的浓度为1~100mg/l;
步骤二:调节混合溶液的ph为3~7,控制溶液中cr(vi)与草酸的摩尔浓度比为1.92:0.1~10;
步骤三:在650r/min的搅拌情况下,加入粉末状的nabh4还原剂,搅拌均匀5min,所述nabh4还原剂与含有cr(vi)的溶液的添加比例为0.02~0.12g:550ml;
步骤四:沉降15min或20h。
本发明相对于现有技术的有益效果为:采用化学还原技术将cr(vi)转化为cr(ⅲ)是解决高浓度cr(vi)废水的有效途径,也是工业废水常用的处理方法。尽管化学还原方法在理论和技术上都比较成熟,但它们需要过量的还原剂和强酸环境,才能取得良好的效果。常见的还原剂为na2s2o5和na2so3,两者在强酸条件下使用易生成so2而造成空气污染,在ph大于3的条件下,又表现为对cr(vi)的还原速率缓慢和还原率有限。nabh4作为一种反应条件温和的还原剂,水解的副产物之一是h2,安全无毒且回收价值高。因此,以nabh4代替硫还原剂,可以减轻so2和硫酸根离子对环境的潜在释放,具有潜在的应用价值。本发明基于nabh4水解反应可被催化,经催化后的nabh4还原能力有较大幅度提升,故选用草酸为强化剂,在适量的草酸浓度下,强化nabh4还原cr(vi),结果表明cr(vi)还原率得到有效提高,5min可实现cr(vi)的快速完全还原,此过程中草酸并未被消耗而可循环利用。
本发明使用的还原剂和强化剂具有无毒、安全、环保等优点,操作简单、方便。通过草酸对nabh4水解的催化作用,使得nabh4的还原能力大幅度提高,在适量的草酸浓度下,具有强化nabh4还原cr(vi),cr(vi)还原率得到有效提高,在ph3.0条件下,5min即可实现100mg/lcr(vi)的快速且完全还原,此过程中草酸并未被消耗而可循环利用。
本发明中,相比于硫系还原剂,nabh4还原cr(vi)的同时可产生高纯度高附加值的h2能源,这相比于na2s2o5、na2so3等所产生副产物so2具有更加明显的优势,可以减轻so2和硫酸根离子对环境的潜在释放,具有一定的应用前景。通过nabh4与草酸的配合使用,使得草酸对nabh4水解起到促进作用,可提高nabh4在较高ph条件下对cr(vi)的还原率,解决nabh4还原。
附图说明
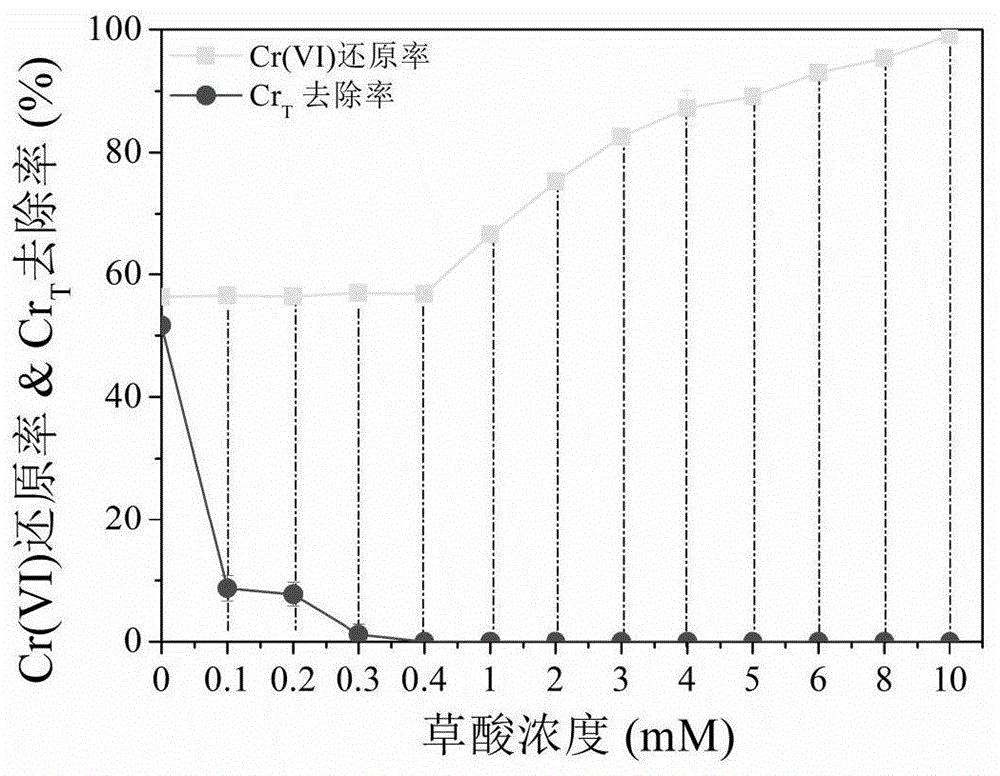
图1为草酸浓度对cr(vi)–草酸–nabh4中cr(vi)还原和crt去除的影响示意图;[cr(vi)]0=100mg/l,[草酸]=0~10mm,ph=3.0,0.10gnabh4,650r/min搅拌5min,静沉15min;
图2为草酸浓度对nabh4-cao处理cr(vi)时的crt去除和浊度的影响示意图;[cr(vi)]0=100mg/l,[草酸]=0~2.0mm,ph=3.0,0.10gnabh4,650r/min搅拌5min,0.3cao,继续以650r/min搅拌0.5min,静沉15min;
图3为草酸浓度对nabh4-cao处理cr(vi)时的cr(iii)沉淀的影响示意图;[cr(vi)]0=100mg/l,[草酸]=0~2.0mm,ph=3.0,0.10gnabh4,650r/min搅拌5min,0.3cao,继续以650r/min搅拌0.5min,静沉15min;
图4为nabh4投加量对cr(vi)–草酸–nabh4体系中cr(vi)还原的影响;[cr(vi)]0=100mg/l,[草酸]=0~10.0mm,ph=3.0,0.02~0.12gnabh4,650r/min搅拌5min,静沉15min;
图5为初始ph对cr(vi)–草酸–nabh4体系中cr(vi)还原的影响示意图;[cr(vi)]0=100mg/l,[草酸]=0,0.20,2.0,10.0mm,ph=3.0~8.0,0.10gnabh4,以650r/min搅拌5min,静沉15min;
图6为离子形态分布图;[草酸]=10mm,温度25℃,离子强度i=0.01;
图7为ph变化曲线图;[草酸]=0~10mm;
图8为草酸浓度对草酸–cr(vi)–na2s2o5体系中cr(vi)还原的影响示意图;[cr(vi)]0=100mg/l,[草酸]=0~10mm,ph=3.0,0.10~0.30gna2s2o5和na2so3,650r/min搅拌5min,静沉15min;
图9为草酸浓度对草酸–cr(vi)–na2so3体系中cr(vi)还原的影响示意图;[cr(vi)]0=100mg/l,[草酸]=0~10mm,ph=3.0,0.10~0.30gna2s2o5和na2so3,650r/min搅拌5min,静沉15min;
图10为草酸浓度对nabh4水解产h2的影响示意图;[草酸]=0~10mm,ph=3.0,0.10gnabh4,650r/min搅拌20min;
图11为浊度与吸光度的关系图;
图12为浊度变化曲线图;[cr(vi)]0=100mg/l,[草酸]=0,0.10,0.20,0.30,0.40mm,ph=3.0,0.10gnabh4,650r/min搅拌5min,静沉时间0~20h;
图13为草酸浓度对cr(iii)在固液两相分布的影响图,静沉15min;
图14为草酸浓度对cr(iii)在固液两相分布的影响图,静沉20h;
图15为na2c2o4和cr(oh)3的红外光谱图;cr(oh)3制备:1mnaoh逐滴滴入crcl3溶液中,得到的絮体经过滤干燥步骤;
图16为不同体系得到沉淀物的xrd衍射图;
图17为红外光谱图对比图;(a)cr(vi)–nabh4体系获得的沉淀物;(b)0.10mm草酸–cr(vi)–nabh4体系获得的沉淀物;(c)0.20mm草酸–cr(vi)–nabh4体系获得的沉淀物;(d)0.30mm草酸–cr(vi)–nabh4体系获得的沉淀物;
图18为絮体或胶体afm图像,cr(vi)–0.10gnabh4体系,静沉15min;
图19为絮体或胶体afm图像,cr(vi)–0.10gnabh4体系,静沉20h;
图20为絮体或胶体afm图像,0.10mm草酸–cr(vi)–0.10gnabh4,静沉15min;
图21为絮体或胶体afm图像,0.10mm草酸–cr(vi)–0.10gnabh4,静沉20h;
图22为絮体或胶体afm图像,0.40mm草酸–cr(vi)–0.10gnabh4,静沉15min;
图23为絮体或胶体afm图像,0.40mm草酸–cr(vi)–0.10gnabh4,静沉20h。
具体实施方式
下面结合附图和实施例对本发明的技术方案作进一步的说明,但并不局限于此,凡是对本发明技术方案进行修改或者等同替换,而不脱离本发明技术方案的精神和范围,均应涵盖在本发明的保护范围中。
具体实施方式一:本实施方式记载的是一种基于草酸强化的nabh4快速还原六价铬离子的方法,所述方法步骤如下:
步骤一:将草酸钠加入含有cr(vi)的溶液中,混合均匀后形成混合溶液,控制所述混合溶液中草酸钠的浓度为0.1~10mm;所述含有cr(vi)的混合溶液中cr(vi)的浓度为1~100mg/l;
步骤二:调节混合溶液的ph为3~7,控制溶液中cr(vi)与草酸的摩尔浓度比为1.92:0.1~10;
步骤三:在650r/min的搅拌情况下,加入粉末状的nabh4还原剂,搅拌均匀5min,以实现cr(vi)与还原剂的充分接触;所述nabh4还原剂与含有cr(vi)的溶液的添加比例为0.02~0.12g:550ml;
步骤四:沉降15min或20h。
具体实施方式二:具体实施方式一所述的一种基于草酸强化的nabh4快速还原六价铬离子的方法,步骤二中,使用1.2m盐酸调节溶液ph。
具体实施方式三:具体实施方式一所述的一种基于草酸强化的nabh4快速还原六价铬离子的方法,步骤二中,当cr(vi)与草酸的摩尔浓度比为1.92:0.10~2.0时,加入cao作为絮凝剂和沉淀剂,去除还原得到的三价铬,以650r/min搅拌0.5min,以确保cao完全分散;在300r/min的慢速搅拌模式下混凝5min,然后沉降15min。
具体实施方式四:具体实施方式一所述的一种基于草酸强化的nabh4快速还原六价铬离子的方法,步骤三中,所述nabh4还原剂与含有cr(vi)的混合溶液的添加比例为0.10~0.12g:550ml。
实施例1:
向100mg/l高浓度cr(vi)废水中加入草酸,使得cr(vi)与草酸的摩尔比为1.92:10,采用1.2mhcl调节上述含草酸的cr(vi)废水的ph至3.0,然后向废水中投加0.10~0.12gnabh4,此时,cr(vi)、草酸和nabh4的摩尔比例为1.92:10:4.8~5.7(0.10~0.12g),cr(vi)的还原率在99.1%以上。
液相部分用于分析浊度、crt和cr(vi)浓度等。沉淀物进行ftir、afm和xrd表征。一定浓度的na2c2o4(cmm)加入到溶液中,根据体系的ph,溶液中主要存在的离子类型为hc2o4-、c2o42-和h2c2o4,因此,当以总离子浓度c,可表示为c=[hc2o4-]+[c2o42-]+[h2c2o4]。为了便于表达,在不区分离子类型的情况下,本发明中将这三种离子统称为草酸。
采用美国perkinelmer的5300dv型电感耦合等离子体发射光谱仪(icp–oes)测定液相中crt的浓度。在测量之前,需调整样品的酸度,以确保呈胶体态的cr(iii)完全溶解。采用标准的1,5–二苯碳酰二肼法测定了液相中cr(vi)的浓度,该法基于在酸性条件下形成的红紫色络合物,该络合物可在540nm波长处利用分光光度法定量。采用德国wtw的turb555ir型浊度仪对不连续时间点的液体样品浊度进行测定。采用日本岛津的uv-2550型紫外可见分光光度计连续测定液体样品的浊度曲线。利用德国bruker的bioscope型原子力显微镜(afm)在tapping模式下观察絮体的形态。利用分辨率为4cm-1的美国perkinelmer的spectrumone型红外光谱仪(ftir)表征了固体样品的功能性质。采用传统的kbr压片法制备固体样品。波数范围为4000~400cm-1。采用德国bruker的d8-advance型x射线衍射仪(xrd),测定了固体样品的物相,散射角设置为10°~90°,扫描速度设置为6°/min。
(1)草酸浓度对cr(vi)还原和crt去除的影响
在含有不同浓度草酸的cr(vi)溶液中添加0.10gnabh4,草酸浓度对cr(vi)还原和crt去除的影响如图1所示。由图可知,当草酸的浓度由0增加至0.40mm时,cr(vi)的还原率几乎保持不变,这意味着草酸在这些实验条件下不起任何作用,进一步表明草酸在此体系中未能起到还原剂的作用,这与草酸还原cr(vi)速率缓慢有关。然而,crt的去除率却表现为逐渐降低,说明该体系产生的cr(iii)不能通过自沉淀而去除,当草酸浓度增加至0.4mm时,cr(iii)的沉降率接近于零。随着草酸浓度由1.0增加至10mm,cr(vi)的还原率逐渐升高,可显著提高至最高99.1%。然而,由于cr(iii)几乎没有沉淀,crt去除率接近于零,这与草酸和cr(iii)形成络合物有关。在cr(oh)3·(h2o)3的八面体结构中,作为配体的h2o通过氢键与相邻的cr(iii)结合,随着cr(oh)3逐渐老化,两个相邻且相同的cr(iii)中心将协同释放水分子,然后由相邻cr(iii)的oh配体取代,两个单体将结合形成一个羟基二聚体。然而,由于溶液中存在草酸配体,这些配体可能会填补水分子留下的空位,阻止相邻cr(iii)中心的oh配体加入空位,从而减少二聚体甚至聚合物的形成,使沉降更加困难。
在cr(vi)还原反应进行5min时,加入一定量的cao,crt去除结果如图2所示,与图1相比,cao的加入提高了0~2.0mm草酸–cr(vi)–nabh4体系中crt的去除率,并在一定程度上降低了反应体系的浊度,这原于还原生成的cr(iii)在0~2.0mm草酸溶液几乎完全沉降,如图3所示。当cao加入溶液中时,与水解产物ca(oh)2(s)之间存在溶解平衡,生成oh-(aq)和溶解性的ca2+(aq)。一些研究表明,高电荷的阳离子是一种有效的胶体破坏剂。因此,cr(iii)的快速沉降可能是由多价ca2+离子对胶体的破坏作用所引起的。此外,ca2+和草酸很容易形成几乎不溶的草酸钙(ksp=2.32×10-9),这也可能有助于从cr(iii)–草酸络合物中释放草酸,减少草酸与cr(iii)的结合。
综上所述,1.0~10mm草酸可强化nabh4对cr(vi)的还原,且当草酸浓度处于0~2.0mm范围时,由还原所生成的cr(iii),可采用cao为沉淀剂,以实现cr(iii)的快速沉降。
(2)nabh4投加量对草酸存在下cr(vi)还原的影响
将不同投加量的nabh4添加到草酸–cr(vi)溶液中,cr(vi)还原效果如图4所示。当草酸浓度为0.20mm时,cr(vi)的还原率与对照组相比无显著性差异,说明低浓度草酸根对nabh4还原cr(vi)无影响。当草酸浓度为2.0mm时,随着nabh4投加量的增加,cr(vi)还原率逐渐增大。此外,当草酸浓度为10mm时,它也表现出类似的趋势。通过比较相同投加量nabh4对cr(vi)还原的影响,结果表明,当nabh4投加量大于0.06g时,10mm草酸比在2.0mm草酸更能促进nabh4对cr(vi)的还原。同时,当nabh4投加量从0.02g增加到0.04g时,10mm草酸对nabh4还原cr(vi)的强化作用弱于对2.0mm草酸。因此,草酸和nabh4的比例影响cr(vi)的还原。当草酸和nabh4的摩尔浓度比例在10:3.8~5.7(0.08~0.12g)时,cr(vi)的还原率在97.8%以上;当草酸和nabh4的摩尔浓度比例在10:4.8~5.7(0.10~0.12g)时,cr(vi)的还原率在99.1%以上。
(3)初始ph对草酸存在下cr(vi)还原和crt去除的影响
不同ph条件下,草酸对nabh4还原cr(vi)的影响如图5所示。如图可知,当初始ph大于或等于6.0时,草酸对cr(vi)的还原没有明显的影响;当初始ph为5.0时,10mm草酸对cr(vi)的还原有强化作用,而在初始ph为3.0和4.0时,2.0mm和10mm草酸对cr(vi)的还原均有强化作用。以上结果表明,初始ph对草酸强化nabh4的还原行为有一定的影响,这可能与草酸在水溶液中的缓冲行为有关。
在水溶液中,草酸以h2c2o4、hc2o4-和c2o42-离子形态存在,其分布取决于ph,如图6所示。ph在1.23~4.19之间,溶液中以hc2o4-为主,而c2o42-在ph大于4.19情况下占优势。图7显示了将naoh逐滴加入不同浓度的草酸溶液后,每个体系的ph变化。随着各溶液体系ph从3.0增加到10.0,ph曲线呈现由缓变到陡的变化趋势。草酸浓度越高,平缓区越宽,说明溶液体系对naoh的缓冲能力随着草酸浓度的增加而增强(>1mm)。这可归因于溶液中共轭酸碱对hc2o4-–c2o42-的存在,如式(2)所示。hc2o4-因加入的oh-逐渐电离生成c2o42-,直到c2o42-的浓度足够大,从而产生了抑制hc2o4-电离的同离子效应。当溶液体系中碱的引入并没有引起过大的ph变化,因此草酸对nabh4还原cr(vi)的影响可以归因于hc2o4-–c2o42-所组成的缓冲体系,使cr(vi)还原环境保持在较低的ph水平,cr(vi)的氧化还原电位与ph密切相关,ph越低对cr(vi)还原越有利。另一方面,ph越低,nabh4作为还原剂的水解能力越强。
草酸浓度越高,缓冲能力越强,能抵抗nabh4水解和cr(vi)还原反应引起的ph升高,对cr(vi)还原反应的促进作用越强,这可以解释图1所示的现象,由于草酸浓度较低,缓冲容量相对较弱,导致强化效果较差。此外,如图7所示,0.20mm和2.0mm草酸溶液在ph大于5.0时的缓冲能力基本上消失,因此处于此ph条件下的草酸起不到强化cr(vi)还原的作用,如图5所示的结果正好说明了这一点。
综上所述,草酸对nabh4还原cr(vi)的强化作用受初始ph的影响。在ph3.0和4.0时,高浓度的草酸(10mm)对cr(vi)还原的强化作用较强,cr(vi)还原率可达到88.6%以上,而当ph小于5.0时,即使是高浓度的草酸(10mm),对cr(vi)还原的强化作用不明显。这与hc2o4-–c2o42-缓冲行为有关,较高的ph不利于其发挥缓冲作用。
(4)nabh4与硫系还原剂的对比研究
图8和图9分别显示了两种还原剂,包括na2s2o5和na2so3,对草酸-cr(ⅵ)溶液体系中cr(vi)还原的影响。如图8所示,当草酸浓度从2.0增加至10mm时,其对0.10gna2s2o5还原cr(vi)的强化作用很小。cr(vi)的还原率可从45.4%(0mm草酸)提高到52.7%(10mm草酸),而0.10gnabh4处理的10mm草酸–cr(vi)溶液中,cr(vi)的还原率达到99.1%,如图1所示。当na2s2o5用量为0.20g时,6~10mm草酸对cr(vi)还原率有较弱的强化作用,最大可达98.9%。而0.30gna2s2o5本身对cr(vi)的还原程度较高,因此表现为草酸对cr(vi)还原的强化作用不明显。从图9可以看出,在草酸–cr(vi)溶液体系中,用0.10~0.30g的na2so3作为还原剂,2.0~10mm草酸的存在可以显著提高cr(vi)的还原率。采用0.30gna2so3处理草酸–cr(vi)溶液,cr(vi)的最高还原率可达99.7%,与相同剂量的na2s2o5的还原率相近,这与以往的研究不同。
表1显示了草酸–cr(vi)–na2s2o5和草酸–cr(vi)–na2so3两个体系的在20min时的ph。草酸–cr(vi)–0.10gna2s2o5体系的ph随草酸浓度的增加而降低。已知na2s2o5还原cr(vi)是一个消耗h+的过程。如图8所示,随着草酸浓度的增加,cr(vi)的还原率增加,因此,溶液体系中h+的消耗会逐渐增加,导致体系ph呈上升趋势。然而,这一趋势与表1所示的实际测量值相反,由此可推断溶液体系中的其他因素会影响体系的ph,一方面,ph降低可能是na2s2o5自水解生成h+的结果,另一方面,来源于hc2o4-–c2o42-的缓冲作用。草酸–cr(vi)–0.10gna2so3体系的ph也遵循这一规律,即随着溶液中草酸浓度的增加,ph变小。这一现象与hc2o4-–c2o42-的缓冲作用有关,它减缓了na2so3水解产生的oh-对cr(vi)还原的负面影响,这与用nabh4观察到的结果相似。
通过nabh4与两种常见cr(vi)还原剂对比可知,草酸对na2s2o5还原cr(vi)的强化作用不明显,而对高投加量的na2so3强化作用明显,然而达到99%以上的去除率,na2so3投加量是nabh4的三倍,从节省还原剂的角度讲,草酸用于强化nabh4更适合。
表1na2s2o5和na2so3处理草酸–cr(vi)溶液后体系的ph(20min)
(5)草酸强化nabh4还原去除cr(vi)的潜在机制
a.草酸与nabh4间的相互作用规律
通过向不同浓度的草酸水溶液中加入一定量的nabh4,研究草酸与nabh4的相互作用,结果如图10所示。当草酸浓度大于0.40mm时,nabh4水解产h2的速率增加,说明草酸对nabh4水解有一定的强化作用。nabh4水解伴随着氧化还原反应,因此,水解能力提升的同时也强化了nabh4的还原cr(vi)的能力,并由此可以解释随着草酸浓度的增加cr(vi)还原率的增加这一现象,如图1所示。
b.固相沉淀物的表征
制备了一系列浊度标准溶液。图11显示了浊度与吸光度之间的关系。由图可知,在600nm、650nm、680nm和700nm处,浊度与吸光度均呈良好的线性关系,因此,利用吸光度的变化来评价浊度的变化是可行的。图12显示了停止搅拌后0~0.40mm草酸–cr(vi)–0.10gnabh4反应系统的浊度变化。对于cr(vi)–0.10gnabh4对照体系,搅拌后0min浊度最高,然后在短时间内浊度迅速下降。这可能表明,所制备的cr(iii)是不溶性的cr(oh)3,在停止搅拌前便大量生成,停止搅拌后迅速沉淀。而对于0~0.30mm草酸–cr(vi)–0.10gnabh4体系,出现最大浑浊的时间发生延迟。特别是对于0.3mm草酸–cr(vi)–0.10gnabh4体系,浊度从8h开始上升,然后在19h时达到最大值。如前所述,由此可以推断,0.30mm草酸的存在导致溶液中cr(iii)在前8h以稳定的胶体形式存在,胶体在凝聚成絮状物后,逐渐失稳并沉淀下来。不稳定过程可以解释为cr(oh)3老化过程中,悬浮液在不同ph下的总含量变化。在碱性条件下,cr(oh)3单体含量随老化时间的延长而降低,而低聚物和高低聚物含量则增加。对于0.40mm草酸–cr(vi)–0.10g体系,浊度始终保持在较低水平,这表明生成的cr(iii)在0.40mm草酸溶液中稳定,很难形成胶体,这可归因于cr(iii)与草酸配体形成不易水解的可溶性或不溶性cr(iii)配合物。
图13和图14分别显示了在停止搅拌后的15min和20h时,0~0.40mm草酸–cr(vi)–0.10gnabh4体系中的cr(iii)在固液相中的分布。由cr(vi)–0.10gnabh4体系中获得的cr(iii)基本上在15min内完全沉淀,从图13可以看出,从0.10~0.20mm草酸–cr(vi)–0.10g体系中获得的cr(iii)在静止15min后呈现少量沉淀,但沉降持续20h可分别达到84.3%和95.8%的沉淀率,如图14所示。0.30~0.40mm草酸–cr(vi)–0.10gnabh4体系生成的cr(iii)在15min时几乎没有沉淀,但在20h时分别达到15.3%和8.8%的沉淀率。由以上结果可以推断,随着草酸浓度的增加,草酸阻止cr(iii)沉淀的能力增强。然而,浓度为0.10~0.40mm的草酸不足以完全结合液相中的生成的cr(iii);作用在cr(iii)上的分子间作用力会使其逐渐聚集,直至随时间变化而沉淀,而其沉淀速率和程度取决于草酸浓度。
c.沉淀物形态和结构特征
图15显示了na2c2o4、制备的cr(oh)3和来自cr(vi)–nabh4体系的沉淀物的ftir光谱。由于–coo-是一个多电子共轭物,其两个氧原子之间没有差别,因此没有观察到c–o弯曲振动吸收峰。当两个c=o振动耦合时,在1610~1560cm-1处会出现反对称拉伸振动,而在1440~1360cm-1处,由于对称拉伸振动会出现两个或三个吸收带,其强度比前者弱。因此,光谱中1637cm-1和1345cm-1处的c2o42-吸收带分别对应于c=o伸缩振动和781cm-1处的o–c=o弯曲振动。对于制备的cr(oh)3,1633cm-1处的吸收峰可归因于与cr(iii)相连自由水的弯曲振动。在1560~1300cm-1区域有两条谱带,这可能来源于cr(iii)与羟基的相互作用,为羟基化合物的cr–oh弯曲振动。860和500cm-1处的谱带归因于束缚水分子的弯曲振动。对于来自cr(vi)–nabh4体系的沉淀,其ftir光谱与制备的cr(oh)3相似。两个红外光谱的区别在于,制备的cr(oh)3处于结晶状态,如图16所示,但cr(vi)–nabh4体系得到的沉淀为非晶态cr(oh)3。已有研究表明,在含有结晶水的cr(iii)以cr(oh)3·3h2o的形式存在。结晶态cr(oh)3经加热干燥后,易失去结晶水,转变为非晶态。无定cr(oh)3可表示为cr(oh)3·xh2o,其中x小于3。因此,这些样品具有不同的结晶度,可能导致它们的红外光谱略有不同。
图17显示了0~0.30mm草酸–cr(vi)–0.10gnabh4体系静沉20h后获得的沉淀物的红外光谱图。比较cr(vi)–0.10gnabh4体系和0.10~0.30mm草酸–cr(vi)–0.10gnabh4体系产生的沉淀物,从草酸存在的体系中获得的沉淀物显示出五个新吸收峰,分别位于1708cm-1,1685cm-1,1407cm-1,1275cm-1和805cm-1。随着草酸浓度的增加,1483cm-1(仅归属于cr(oh)3·xh2o)与1708cm-1,1685cm-1,1407cm-1,1275cm-1和805cm-1的峰强比值也逐渐增大。从这两类沉淀物的来源来看,它们之间唯一的区别是草酸的存在与否。由此可以推断,在这些沉淀物中观察到的新吸附峰来自草酸。这五条谱带与草酸谱图不一致的原因与草酸与cr(iii)配合物的形成有关。当cr(iii)与草酸配合时,o–c=o的电子云密度降低,多电子共轭体系消失,与c相连的两个o原子不再相同。因此,o–c=o的弯曲振动由781cm-1变为805cm-1,其中一个c=o的伸缩振动峰出现在1708cm-1和1685cm-1处,另一个c=o在1345cm-1处的伸缩振动峰变成了c–o,导致在1275cm-1处观察到吸收峰。1407cm-1处的新吸收峰可能是由cr(iii)与草酸配合形成的cr–o振动,但由于这条谱带与1379cm-1处的cr–oh弯曲振动非常接近,两个位置的峰都变成了复合峰,而且更宽。随着沉淀物中草酸含量的增加,cr–o在沉淀物中的比例增加,1407cm-1处的峰值更明显。图16显示出了每个体系的沉淀物的xrd衍射图。相比之下,草酸–cr(vi)–0.10g–nabh4体系生成的沉淀物没有发现草酸结晶相,说明cr(iii)与草酸的配合作用破坏了草酸的晶体结构。
图18~23显示了静沉15min和20h后不同体系中的絮体或胶体的afm图像。静沉15min的cr(vi)–0.10gnabh4体系产生的絮体小而致密,20h时絮体的形态变化不大。而0.10mm草酸–cr(vi)–0.10g–nabh4体系的胶体颗粒在15min时较疏松,沉淀困难,故形成较大的浊度,20h时颗粒结构致密,可能表现为由胶体向絮体转变的过程,从而形成沉淀。对于0.40mm草酸–cr(vi)–0.10gnabh4体系,在15min和20h时絮体的大小和形态没有显著变化,因此在20h时cr(iii)的沉淀率是有限的,如图14所示。
采用草酸强化nabh4处理cr(vi),cr(vi)的还原率与初始ph、草酸浓度和nabh4投加量有关。低浓度(0.10~0.40mm)草酸对nabh4还原cr(vi)几乎没有影响,但生成的cr(iii)的自沉降效应受到阻碍,这是由沉淀15min后cr(iii)的自沉降速率受到限制而决定的。然而,当自沉降时间延长到20h时,0.10~0.20mm草酸溶液中cr(iii)的沉淀率分别达到84.3%和95.8%,且草酸与可参与到cr(iii)沉淀物中。当草酸浓度大于或等于1.0mm时,草酸强化了nabh4对cr(vi)的还原。共轭酸碱对hc2o4-–c2o42-缓冲作用强化了nabh4水解生成oh-的过程,而oh-的生成同样促进了形态c2o42-的浓度,有利于共轭酸碱对的形成。具有较强缓冲作用的共轭酸碱对的总浓度越大,cr(vi)的还原率越高。na2so3水解生成oh-的特性与nabh4相似,这使hc2o4-–c2o42-在促进cr(vi)还原方面所发挥的作用更明显。而初始ph和nabh4投加量影响体系的ph,影响hc2o4-–c2o42-缓冲对中hc2o4-和c2o42-分配比例的,对缓冲能力产生影响,从而影响nabh4对cr(vi)的还原。
- 还没有人留言评论。精彩留言会获得点赞!