一种锂锡氧化物多金属掺杂光催化剂及其在药物降解中的用途的制作方法
1.本发明涉及环境功能材料技术领域,具体涉及一种锂锡氧化物多金属掺杂光催化剂及其制备方法。
背景技术:
2.酚氯作为剧毒有机污染物,广泛应用于农药、杀菌剂、杀虫剂、除草剂和木材防腐剂。特别是2,4-dcp是一种典型的氯酚,由于其高稳定性和致癌性,迫切需要从污染水体中去除。同时,医药工业废水中的的残留药物排放量逐渐增加,针对卤代酚污染物和医药废水废药,如四环素药物,传统的生物和电催化技术已被广泛探索。然而,这些技术总是涉及稳定性差、催化剂中毒和电极腐蚀。然而光催化技术是一种新型的污染物治理技术,通过将太阳能转化为化学能,实现对污染物的降解转化。
3.现有技术中,针对污水、空气的有害有机物进行光催化的光催化剂多为半导体催化剂,例如tio2、ceo2、g-c3n4、sno2、mos2、tio2等,但是,针对水中的卤代酚污染物和医药废水中的残留废药如四环素,现有的光催化剂对该类有机物的降解效率低下,无法满足实际应用的需求。
技术实现要素:
4.针对现有技术中所存在的不足,本发明提供了一种锂锡复合氧化物多金属掺杂光催化剂,以解决相关技术中传统光催化剂对污水中卤代酚污染物和医药废水中的残留药物(废药)的光催化降解效率低的技术问题。
5.在一实施方案中,本发明的一种锂锡氧化物多金属掺杂光催化剂,为式(i) 所示化合物,
6.li2sn
xay
o3(i),且a=sb、ge、pb、in,
7.式中,a选自sb、ge、pb和in,0《x+y≤1,且x不能为0。
8.在上述实施方案中,本发明的掺杂光催化剂,优选的,所述a为sb或ge。
9.在一些优选的实施方案中,本发明的掺杂光催化剂,选自以下化合物,
10.li2sn
0.95
in
0.05
o3、li2sn
0.90
in
0.10
o3、li2sn
0.95
ge
0.05
o3、li2sn
0.9
ge
0.10
o3、 li2sn
0.95
sb
0.05
o3、li2sn
0.90
sb
0.10
o3、li2sn
0.90
pb
0.10
o3、li2sn
0.95
pb
0.05
o3。
11.更优选的,所述的掺杂光催化剂,选自以下化合物,
12.li2sn
0.95
ge
0.05
o3、li2sn
0.9
ge
0.10
o3、li2sn
0.95
sb
0.05
o3和li2sn
0.90
sb
0.10
o3。
13.在又一实施方案中,本发明还提供了一种制备上述本发明的锂锡氧化物多金属掺杂光催化剂,包括以下步骤:
14.1)按1.1(li2co3):x:y的摩尔比称取li2co3、sno2和in2o3或geo2或sb2o3或pbo;
15.2)将li2co3和sno2与in2o3或geo2或sb2o3或pbo混合,研磨;
16.3)研磨混合均匀后,加热烧结,冷却至室温即得。
17.上述本发明的方法,优选的,x:y为0.95:0.05~0.9:0.1。
18.优选的,上述本发明的方法,步骤2)中所述的研磨,研磨时间为10~60 分钟,更优选为30分钟。步骤3)中所述加热烧结,加热升温速率为4~6℃/min,烧结温度为850℃~950℃,或者烧结时间为8-12h,更优选的,加热升温速率为 5℃/min,烧结温度为850℃,或者烧结时间为10h。
19.在另一实施方案中,本发明还提供一种本发明的锂锡氧化物多金属掺杂光催化剂以及li2sno3用于光催化降解卤代酚污染物的用途,尤其是光催化降解水中的卤代酚污染物的用途。
20.优选的,所述的用途,所述为卤代酚为2,4-二氯苯酚。
21.具体来说,提供li2sno3、li2sn
0.95
in
0.05
o3、li2sn
0.90
in
0.10
o3、li2sn
0.95
ge
0.05
o3、 li2sn
0.9
ge
0.10
o3、li2sn
0.95
sb
0.05
o3、li2sn
0.90
sb
0.10
o3、li2sn
0.90
pb
0.10
o3、 li2sn
0.95
pb
0.05
o3用于光催化降解卤代酚污染物的用途,尤其是光催化降解水中的卤代酚污染物的用途。优选的所述为卤代酚为2,4-二氯苯酚。
22.在一具体实施方案中,本发明的一种锂锡复合氧化物多金属掺杂光催化剂的制备方法,包括如下步骤:
23.1)按1.1(li2co3):x:y的摩尔比称取原料li2co3、sno2和in2o3或geo2或sb2o3或pbo,备用;
24.2)将步骤1)称取的li2co3和sno2与in2o3或geo2或sb2o3或pbo混合研磨、得到混合研磨物;
25.3)将步骤2)的混合研磨物置于反应装置中,加热烧结反应,然后自然冷却至室温,制得光催化剂li2sn
xay
o3。
26.其中,x:y为0.95:0.05~0.9:0.1。
27.相比于现有技术,本发明具有如下有益效果:
28.1、本发明的光催化剂针对卤代酚污染物具体较高的光催化降解效率,与现有的半导体催化剂比较而言,比如sno2,紫外光照射下,80分钟降解甲基橙溶液20%;in2o3,在可见光照射下,180分钟降解2,4-二氯苯酚60%。本发明的光催化剂降解速率高、降解效果良好,特别是针对2,4-dcp具有接近100%的降解效率,使得本发明的光催化剂能应用于农药、杀菌剂、杀虫剂、除草剂和木材防腐剂等行业中,实现对污水中不易处理的酚类污染物的高效处理,避免添加外加化学添加剂对污水中的酚类污染物进行处理带来的附加问题,并且,不同于外加化学反应原料,还能减少污水在该有机酚类处理过程中的成本,使得污水处理工艺更加节能。
29.2、本发明提供的新型光催化剂的制备原料简单易得,且该光催化剂的制备方法简单、便捷、成本低下,适合规模化生产。
30.3、本发明通过设计添加不同的金属原料及其不同的加入量等得到不同金属掺入量的光催化剂,掺不同金属的光催化剂对不同波长的光具有不同的吸收效果,以有效调控光催化剂的带隙从而实现光催化剂对不同光源的吸收,进而提高光催化剂对酚类化合物的降解效率。
31.总之,本发明的催化剂对卤代酚污染物具体较高的光催化降解效率,可广泛应用于印染、药物、造纸以及塑料等行业中,实现对污水中不易处理的酚类污染物的高效处理,
避免添加外加化学添加剂对污水中的酚类污染物进行处理带来的附加问题,而且还能减少污水在该有机酚类处理过程中的成本,使得污水处理工艺更加节能。
附图说明
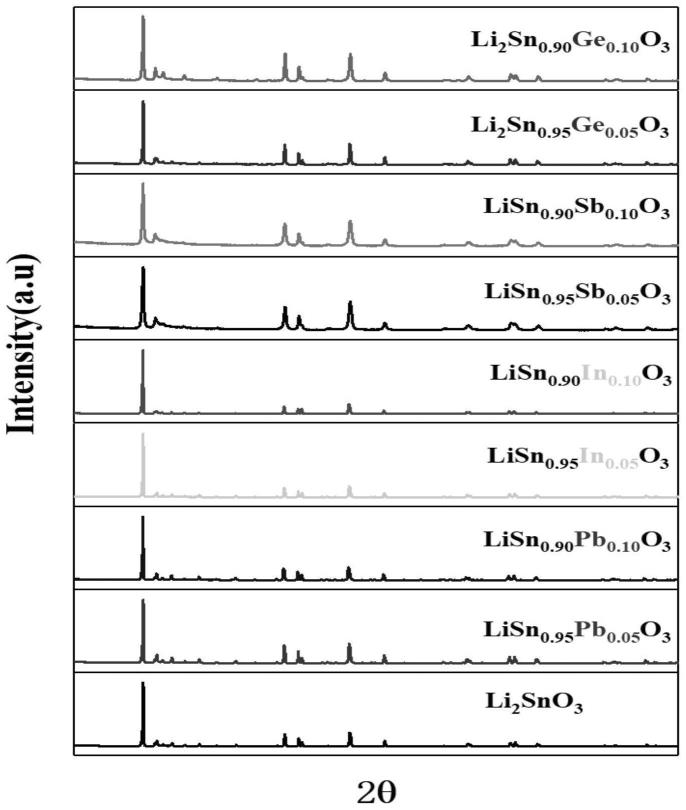
32.图1为本发明的光催化剂li2sno3、li2sn
0.95
in
0.05
o3、li2sn
0.90
in
0.10
o3、 li2sn
0.95
ge
0.05
o3、li2sn
0.9
ge
0.10
o3、li2sn
0.95
sb
0.05
o3、li2sn
0.90
sb
0.10
o3、 li2sn
0.90
pb
0.10
o3、li2sn
0.95
pb
0.05
o3的xrd图;
33.图2为本发明的光催化剂li2sno3的sem图;
34.图3为本发明的光催化剂li2sn
0.9
ge
0.10
o3的sem图;
35.图4为本发明的光催化剂li2sn
0.90
sb
0.10
o3的sem图;
36.图5为本发明的光催化剂li2sno3、li2sn
0.95
in
0.05
o3、li2sn
0.90
in
0.10
o3、 li2sn
0.95
ge
0.05
o3、li2sn
0.9
ge
0.10
o3、li2sn
0.95
sb
0.05
o3、li2sn
0.90
sb
0.10
o3、 li2sn
0.90
pb
0.10
o3、li2sn
0.95
pb
0.05
o3的降解2,4-dcp的效果图;
37.图6中本发明制备的光催化剂li2sno3、li2sn
0.95
in
0.05
o3、li2sn
0.90
in
0.10
o3、 li2sn
0.95
ge
0.05
o3、li2sn
0.9
ge
0.10
o3、li2sn
0.95
sb
0.05
o3、li2sn
0.90
sb
0.10
o3、 li2sn
0.90
pb
0.10
o3、li2sn
0.95
pb
0.05
o3的降解四环素的效果图;
38.图7为本发明的光催化剂li2sn
0.9
ge
0.10
o3的循环实验图;
39.图8为本发明的光催化剂li2sno3的漫反射对比图谱;
40.图9为本发明的光催化剂li2sn
0.90
in
0.10
o3的漫反射对比图谱;
41.图10为本发明的光催化剂li2sn
0.9
ge
0.10
o3的漫反射对比图谱;
42.图11为本发明的光催化剂li2sn
0.90
sb
0.10
o3的漫反射对比图谱;
43.图12为本发明的光催化剂li2sn
0.90
pb
0.10
o3的漫反射对比图谱。
具体实施方式
44.下面结合实施例对本发明中的技术方案进一步说明。
45.本发明提供了一种锂锡复合氧化物多金属掺杂光催化剂,所述光催化剂的化学式为li2sn
xay
o3,且a=sb、ge、pb、in,0《x+y≤1,且x不能为0。并且,该光催化剂li2sn
xay
o3(a=sb、ge、pb、in)可通过如下方法制得:
46.1)按照摩尔比为1:x:y的比值称取原料li2co3、sno2、in2o3或geo2或 sb2o3或pbo,备用;
47.2)将步骤1)中称取的li2co3、tio2、in2o3或geo2或sb2o3或pbo混合、研磨30min得到混合研磨物;
48.3)将步骤2)中的混合研磨物置于反应装置中,烧结,然后自然冷却至室温,制得光催化剂li2sn
xay
o3(a=sb、ge、pb、in,0《x+y≤1)。
49.根据原料的不同以及不同掺杂量可以制得li2sno3、li2sn
0.95
in
0.05
o3、 li2sn
0.90
in
0.10
o3、li2sn
0.95
ge
0.05
o3、li2sn
0.9
ge
0.10
o3、li2sn
0.95
sb
0.05
o3、 li2sn
0.90
sb
0.10
o3、li2sn
0.90
pb
0.10
o3、li2sn
0.95
pb
0.05
o3九种光催化剂,分别通过实施例1-9制得。
50.需要说明的是,下述实施例中所使用的实验方法如无特殊说明,均为常规方法;下述实施例中所用的材料、试剂、器材等,如无特殊说明,均可从商业途径获得。
51.下述施例中用到的li2co3纯度为99.90%,来自阿拉丁;sno2纯度为99.50%,来自阿拉丁;in2o3纯度为99.90%,来自阿拉丁;geo2纯度为99.99%,来自阿拉丁;sb2o3纯度为99.5%,来自阿拉丁;pbo2纯度为99.9%,来自阿拉丁。
52.实施例1
53.li2sno3光催化剂的制备方法,包括如下步骤:
54.1)按照摩尔比为3.3:3的比值称取原料li2co3和sno2,备用;
55.2)将步骤1)中称取的li2co3、sno2混合,研磨30min,得到混合研磨物;
56.3)将步骤2)中的混合研磨物置于反应装置中,控制升温速率为5℃/min,升温至反应温度为850℃,在该反应温度下烧结10h,然后自然冷却至室温,制得光催化剂li2sno3(标号为样品1)。
57.实施例2
58.li2sn
0.95
in
0.05
o3光催化剂的制备方法,包括如下步骤:
59.1)按照摩尔比为3.3:2.85:0.075的比值称取原料li2co3、sno2、in2o3,备用;
60.2)将步骤1)中称取的li2co3、sno2、in2o3混合,研磨30min,得到混合研磨物;
61.3)将步骤2)中的混合研磨物置于反应装置中,控制升温速率为5℃/min,升温至反应温度为850℃,在该反应温度下烧结10h,然后自然冷却至室温,制得光催化剂li2sn
0.95
in
0.05
o3(标号为样品2)。
62.实施例3
63.li2sn
0.9
in
0.10
o3光催化剂的制备方法,包括如下步骤:
64.1)按照摩尔比为3.3:2.70:0.15的比值称取原料li2co3、sno2、in2o3,备用;
65.2)将步骤1)中称取的li2co3、sno2、in2o3混合,研磨30min,得到混合研磨物;
66.3)将步骤2)中的混合研磨物置于反应装置中,控制升温速率为5℃/min,升温至反应温度为850℃,在该反应温度下烧结10h,然后自然冷却至室温,制得光催化剂li2sn
0.9
in
0.10
o3(标号为样品3)。
67.实施例4
68.li2sn
0.95
ge
0.05
o3光催化剂的制备方法,包括如下步骤:
69.1)按照摩尔比为3.3:2.85:0.15的比值称取原料li2co3、sno2、geo2,备用;
70.2)将步骤1)中称取的li2co3、sno2、geo2混合,研磨30min,得到混合研磨物;
71.3)将步骤2)中的混合研磨物置于反应装置中,控制升温速率为5℃/min,升温至反应温度为850℃,在该反应温度下烧结10h,然后自然冷却至室温,制得光催化剂li2sn
0.95
ge
0.05
o3(标号为样品4)。
72.实施例5
73.li2sn
0.90
ge
0.10
o3光催化剂的制备方法,包括如下步骤:
74.1)按照摩尔比为3.3:2.7:0.3的比值称取原料li2co3、sno2、geo2,备用;
75.2)将步骤1)中称取的li2co3、sno2、in2o3混合,研磨30min,得到混合研磨物;
76.3)将步骤2)中的混合研磨物置于反应装置中,控制升温速率为5℃/min,升温至反应温度为850℃,在该反应温度下烧结10h,然后自然冷却至室温,制得光催化剂li2sn
0.90
ge
0.10
o3(标号为样品5)。
77.实施例6
li2sn
0.95
ge
0.05
o3、li2sn
0.9
ge
0.10
o3、li2sn
0.95
sb
0.05
o3、li2sn
0.90
sb
0.10
o3、 li2sn
0.90
pb
0.10
o3、li2sn
0.95
pb
0.05
o3的xrd图谱。
100.2、结果分析
101.分别将测验得到的光催化剂li2sno3、li2sn
0.95
in
0.05
o3、li2sn
0.90
in
0.10
o3、 li2sn
0.95
ge
0.05
o3、li2sn
0.9
ge
0.10
o3、li2sn
0.95
sb
0.05
o3、li2sn
0.90
sb
0.10
o3、li2sn
0.90
pb
0.10
o3、li2sn
0.95
pb
0.05
o3的xrd图谱与li2tio3标准xrd图谱进行比较,发现通过实施例1、2、3、4、5、6、7、8、9中记载的方法分别制得的光催化剂为目标产物。
102.说明,本发明能通过控制原料的添加量得到目标光催化剂,本光催化剂的制备方法简单、便捷、成本低下,适合规模化生产。
103.光催化效果试验
104.本发明的光催化剂li2sno3(样品1)、li2sn
0.95
in
0.05
o3(样品2)、 li2sn
0.90
in
0.10
o3(样品3)、li2sn
0.95
ge
0.05
o3、(样品4)li2sn
0.9
ge
0.10
o3(样品 5)、li2sn
0.95
sb
0.05
o3(样品6)、li2sn
0.90
sb
0.10
o3(样品7)、li2sn
0.95
pb
0.05o3 (样品8)、li2sn
0.90
pb
0.10
o3(样品9)的光催化降解效果测试
105.1、光催化降解2,4-dcp的光催化实验操作
106.分别取样品1-9各50mg,将样品1-9分别进行光催化试验,操作均如下:
107.将50mg样品加入100ml浓度为10mg/l的2,4-dcp溶液中,暗吸附60min,至吸附-脱附平衡,然后在500w的紫外高压汞灯下光照20min,每隔4min取上清液3ml,过滤后用高效液相色谱仪(安捷伦1260)测定其浓度,得到表1和图 5的数据。
108.2、结果分析
109.样品1-9光催化降解2,4-dcp溶液30min后的降解效率的最终数据由如表 1所示:
110.表1样品1-9对2,4-dcp的降解效率
111.项目样品1样品2样品3与原始含量的比值83.1%87.1%100%项目样品4样品5样品6与原始含量的比值100%100%100%项目样品7样品8样品9与原始含量的比值100%55.9%72.4%
112.由表1中的数据可以看出,本发明掺入不同的金属及比例的光催化剂(光催化剂li2sno3、li2sn
0.95
in
0.05
o3、li2sn
0.90
in
0.10
o3、li2sn
0.95
ge
0.05
o3、li2sn
0.9
ge
0.10
o3、 li2sn
0.95
sb
0.05
o3、li2sn
0.90
sb
0.10
o3、li2sn
0.95
pb
0.05
o3、li2sn
0.90
pb
0.10
o3)对2,4-dcp 均具有良好的降解效率,并且,样品3、4、5、6、7的光催化剂在仅仅20分钟内对2,4-dcp的降解效率几乎为100%,证明本发明制得的光催化剂对污水中卤代酚污染物,特别是对2,4-dcp的降解效果良好;同时,不同掺杂金属对 2,4-dcp的降解效果不同,表明掺杂的金属改变了母体li2sno3对的结构,特别是催化剂的能级排列。说明本发明的催化剂更能适用于印染、药物、造纸以及塑料等行业中,实现对污水中不易处理的酚类污染物的高效处理,避免添加外加化学添加剂对污水中的酚类污染物进行处理带来的附加问题。
113.同时,分析图5和表1,通过样品2、3对比可以看出,样品2的光催化剂对2,4-dcp的降解效率低于样品3对2,4-dcp的降解效率,说明光催化剂的掺杂in的量的选取对得到的光
催化剂的催化效果也具有一定影响,说明样品3 对应的掺杂量为最优的反应参数;对比样品1-9,发现掺杂不同金属的降解效果差异明显,其中掺杂pb后,效果比母体差,掺杂in,ge,sb后,效果比母体li2sno3更好,其中ge和sb效果最好,说明样品4-7对应的掺杂金属类型为最优的反应参数。
114.1、光催化降解四环素的光催化实验操作
115.分别取样品1-9各30mg,将样品1-9分别进行光催化试验,操作均如下:将30mg样品加入100ml浓度为20mg/l的四环素溶液中,暗吸附60min,至吸附-脱附平衡,然后在500w的紫外高压汞灯下光照30min,每隔4min取上清液 3ml,过滤后用岛津紫外测定其浓度,得到表2和图6的数据
116.2、结果分析
117.样品1-9光催化降解四环素溶液30min后的降解效率的最终数据由如表2所示:
118.表2所得样品光降解四环素的降解率
119.项目样品1样品2样品3与原始含量的比值28.542%35.465%37.527%项目样品4样品5样品6与原始含量的比值64.978%74.394%66.127%项目样品7样品8样品9与原始含量的比值73.975%25.762%31.818%
120.由表2中的数据可以看出,本发明掺入不同的金属及比例的光催化剂(光催化剂li2sno3、li2sn
0.95
in
0.05
o3、li2sn
0.90
in
0.10
o3、li2sn
0.95
ge
0.05
o3、li2sn
0.9
ge
0.10
o3、 li2sn
0.95
sb
0.05
o3、li2sn
0.90
sb
0.10
o3、li2sn
0.95
pb
0.05
o3、li2sn
0.90
pb
0.10
o3)对四环素均具有良好的降解效率,并且,样品5、7的光催化剂在仅仅30分钟内对四环素的降解效率为73%和75%,证明本发明制得的光催化剂对医药废水污染物,特别是对四环素的降解效果良好;同时,不同掺杂金属对2,4-dcp的降解效果不同,表明掺杂的金属改变了母体li2sno3对的结构,特别是催化剂的能级排列。
121.本发明的光催化剂的稳定性测试
122.为进一步研究光催化剂的光催化降解稳定性,便于拓宽光催化剂的应用领域,本发明对光催化剂进行稳定性分析。
123.光催化剂li2sno3(样品1)、li2sn
0.95
in
0.05
o3(样品2)、li2sn
0.90
in
0.10o3 (样品3)、li2sn
0.95
ge
0.05
o3(样品4)、li2sn
0.9
ge
0.10
o3(样品5)、li2sn
0.95
sb
0.05o3 (样品6)、li2sn
0.90
sb
0.10
o3(样品7)、li2sn
0.95
pb
0.05
o3(样品8)、li2sn
0.90
pb
0.10o3 (样品9)的稳定性分析
124.1、循环实验操作
125.取样品5的光催化剂li2sn
0.9
ge
0.10o3 50mg加入100ml浓度为10mg/l的2, 4-dcp溶液的烧杯中,暗吸附60min,至吸附-脱附平衡;再在500w的紫外高压汞灯下光照20min,每隔4min取上清液3ml,过滤后用高效液相色谱仪(安捷伦1260)测定其浓度,回收光照后的样品,静置沉淀后用纯水洗涤三次,烘箱40℃烘干,得到循环第一次的样品。再用回收的样品进行相同的实验,以此类推,进行四次循环实验,得到如图7所示的结果数据。
126.2、结果分析
127.对li2sn
0.9
ge
0.10
o3进行循环实验,该催化剂对2,4-dcp的降解效果仍能达到100%,
表明该催化剂对2,4-dcp有良好的催化效果以及稳定性良好。
128.本发明的光催化剂的漫反射试验
129.为进一步研究li2sno3、li2sn
0.90
in
0.10
o3、li2sn
0.9
ge
0.10
o3、li2sn
0.90
sb
0.10
o3、 li2sn
0.90
pb
0.10
o3对2,4-dcp光催化效率的区别,本发明对样品1-9的光催化剂进行了漫反射表征试验。
130.光催化剂li2sno3(样品1)、li2sn
0.95
in
0.05
o3(样品2)、li2sn
0.90
in
0.10o3 (样品3)、li2sn
0.95
ge
0.05
o3(样品4)、li2sn
0.9
ge
0.10
o3(样品5)、li2sn
0.95
sb
0.05o3 (样品6)、li2sn
0.90
sb
0.10
o3(样品7)、li2sn
0.95
pb
0.05
o3(样品8)、li2sn
0.90
pb
0.10o3 (样品9)漫反射表征试验
131.1、实验操作
132.取样品1、样品2、样品3、样品4、样品5、样品6、样品7、样品8、样品的光催化剂li2sno3、li2sn
0.95
in
0.05
o3、li2sn
0.90
in
0.10
o3、li2sn
0.95
ge
0.05
o3、 li2sn
0.9
ge
0.10
o3、li2sn
0.95
sb
0.05
o3、li2sn
0.90
sb
0.10
o3、li2sn
0.95
pb
0.05
o3、 li2sn
0.90
pb
0.10
o3分别于玛瑙研钵中充分研磨后,将研磨好的样品制片后放于置于岛津uv-2700i漫反射仪进行表征,得到如图6所示的光催化剂li2sno3、 li2sn
0.95
in
0.05
o3、li2sn
0.90
in
0.10
o3、li2sn
0.95
ge
0.05
o3、li2sn
0.9
ge
0.10
o3、 li2sn
0.95
sb
0.05
o3、li2sn
0.90
sb
0.10
o3、li2sn
0.95
pb
0.05
o3、li2sn
0.90
pb
0.10
o3的漫反射图谱。
133.根据漫反射吸收计算出催化剂的带隙、价带、导带值如表3所示。
134.表3样品1-9的漫反射吸收的带隙、价带、导带值
135.样品带隙导带价带li2sno3(样品1)3.55ev-1.22 ev2.33evli2sn
0.95
in
0.05
o3(样品2)3.08ev-0.99ev2.08evli2sn
0.90
in
0.10
o3(样品3)3.44ev-1.19ev2.24evli2sn
0.95
ge
0.05
o3(样品4)3.81ev-1.35ev2.46evli2sn
0.9
ge
0.10
o3(样品5)3.92ev-1.39ev2.52evli2sn
0.95
sb
0.05
o3(样品6)3.83ev-1.35ev2.48evli2sn
0.90
sb
0.10
o3(样品7)3.89ev-1.38 ev2.5evli2sn
0.95
pb
0.05
o3(样品8)3.35ev-1.12ev2.23evli2sn
0.90
pb
0.10
o3(样品9)3.49ev-1.18ev2.30ev
136.2、结果分析
137.由表2可知,li2sno3(样品1)、li2sn
0.95
in
0.05
o3(样品2),li2sn
0.90
in
0.10o3 (样品3)的带隙随掺in量增加在逐渐增加,有经验公式计算出的价带导带值也在增加,表明随掺in量增加,催化剂的氧化还原能力在增强;同理,li2sno3中分别掺杂pb、ge、sb的量增加后的样品的带隙值在增加,同时价带导带值也在增加,说明催化剂的氧化还原能力在增强。
138.如图8、9、10、11、12可知,li2sno3(样品1)、li2sn
0.90
in
0.10
o3(样品3)、 li2sn
0.90
ge
0.10
o3(样品5)、li2sn
0.90
sb
0.10
o3(样品7)、li2sn
0.90
pb
0.10
o3(样品 9)对不同波长的光具有不同的吸收效果,通过对比发现,li2sn
0.90
sb
0.10
o3和 li2sn
0.90
pb
0.10
o3较li2sno3相比,在可见光范围里有两个吸收边,会增强其对光的吸收,可能是其光催化降解效率增大的原因之一;
139.结合表3与图8-12可以得到,掺sb和ge的样品的带隙值高于母体li2sno3,掺in和pb的样品的带隙值低于母体li2sno3,其中能对较宽范围的可见光进行吸收,能在可见光的作用下进行催化反应,并且li2sn
0.95
in
0.05
o3的带隙比li2sno3的小且小于3.1ev,更有利于在可用于可见光下降解其他的污染物;并且,通过 li2sno3、li2sn
0.90
in
0.10
o3、li2sn
0.90
ge
0.10
o3、li2sn
0.90
sb
0.10
o3四种催化剂比较还可以看出含有不同掺杂金属、相同掺杂量的催化剂在光催化降解污染物的效率、可见光的吸收范围上都有所区别,根据该规律得到其他可预见的li2sn
xaz
o3光催化剂。
140.最后说明的是,以上实施例仅用以说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的宗旨和范围,其均应涵盖在本发明的权利要求范围当中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1