可视灵敏活组织切片检查法用于癌症早期诊断的制作方法
本发明属于纳米技术和分析疾病诊断领域,涉及纳米材料中的H2O2响应聚碳酸酯胶束的合成方法及应用于癌症早期诊断的诊断方法。
背景技术:
H2O2作为一种潜在的癌症诊断指标,它产生于细胞外存在各种刺激时中无吞噬细胞的响应。(Crit.Rev.Eukar.Gene.2008,18,35–45)NADPH氧化酶产生毫克量的H2O2,并且在细胞范围内杀死入侵细菌及病毒。在病理学的情况下,细胞外的浓度高达10-50μM,(Cell.1994,77,817–827;Brain Res.1995,671,181–186;Chest.1989,96,606–612;Cancer Res.1991,51,794–798.)用于抗炎响应。重要的是,NOX氧化酶所产生的细胞微摩尔含量的H2O2对炎症相关癌症产生起着极其重要的作用(Sci.2009,100,1382–1388.)。并且无吞噬细胞产生的H2O2对肿瘤的发生起着极其重要的作用。它会增强肿瘤细胞或薄壁细胞的增殖和血管再生来为即将形成的肿瘤提供氧气和营养物质。H2O2含量增加主要存在于肿瘤细胞中,并且它对原癌基因的转移较周围的正常细胞更为重要。由此可见,将它作为一种癌症相关的指标对于人类的癌症诊断具有非常重要的意义。
现有的癌症早期诊断的主要方法为一些传统的仪器方法,例如:血清蛋白组学蛋白微阵列分析方法、单光子发射计算机断层扫描(PET)、实时聚合酶链式反应(RT-PCR)尽管它们在癌症诊断中有着解剖学的特征且拥有高时空分辨率。但复杂的样品制备过程及昂贵的仪器设备限制了它们的广泛使用。(Nat.Rev.Drug Discovery.2008,7,591-607;Chem.Soc.Rev.2012,41,2656-2672.)
活检是一种医学诊断方法,它通常由一名外科医生,介入放射科医生或介入心脏病学家通过提取细胞或组织样品来确定疾病或疾病存在的程度。最早的活检技术是由安德森等人于1987年开发的早期诊断的甲状腺肿的帮助下通过刺穿一个如针的材料(Brit.J.surg.1987,74,292-296.)。在安德森的开创性工作指导下,另一些活检技术包括:针吸活组织检查(Endocrine.2016,52,305-312.)、切除活组织检查(J.Am.Acad.Dermatol..2016,74,102-107.)、切口活组织检查(Tech.coloproctol.2015,19,159-164.)已经成为最常见的的癌症和炎症检查方法。组织病理学切片,作为一种切除式活组织检查法,它是一种对病人癌症显微组织结构进行检查的技术。曙红和苏木精染色(Hematoxylin-Eosin)作为经典的组织病理学方法已被用于一个几十年。由于悠久的历史和行之有效的方法,诊断的结果对许多许多病理学家来说更可信。然而,这些癌症检测过程主要包括对病理学切片根据切片中细胞及组织的不同的特征,如形状、颜色、大小、比例进行分类,并由细胞学技术员来对细胞质等显微切片图像分析,最终确定是否癌症(J.Med.Imag.Health.In.2015,5,877-892.)。因为病理学家不同的专业知识和主观的检测,病理诊断结果可能是错误的。更重要的是,这种策略缺乏足够信息底层代谢物的生物学特性,去识别最优治疗癌症疾病的早期阶段。最重要的肿瘤标记物,也是一些癌细胞代谢产物,它通常由各种各样的蛋白质,RNA或DNA异常产生的肿瘤细胞或机体对癌症的免疫反应所产生的(Annu.Rev.Med.2014,65,95–110.)。近年来,一些信号分子(H2O2(Crit.Rev.Eukar.Gene.2008,18,35–45.)、H2S(Antioxid.redox.sign.2010,12,1101-1109.)、NO(Adv.Healthc.mater.2015,4,1153-1158.))被发现可以作为潜在的癌症恶化的临床指标。然而肿瘤标志物的含量非常低和并且在癌症早期阶段更加低。因此,发展一种信号放大的组织活检技术,可视化高灵敏度识别肿瘤标志物对癌症早期诊断有着极其重要的意义。
胶束是由具有疏水性基团和亲水性基团的聚合物在水溶液中形成的,其为具有独特的核壳结构即疏水内核和亲水外壳的分子聚集体。胶束形成的主要原因是亲水基团相互排斥和疏水基团相互吸引(Macromolecules,2006,39,473-475)。疏水区的疏水内核即药物在胶束中所形成的微环境,用于包载疏水性物质,胶束的极性决定疏水物在胶束中的具体空间位置;而亲水区形成的亲水外壳可提高胶束的稳定性。聚碳酸酯作为一种生物可降解的高分子材料,它不仅有着良好的生物相容性和物理机械性能,而且品种繁多。通过改变主链化学结构或者在侧链中引入功能基团,可以使聚碳酸酯材料具有特殊的物理、化学和生物学性质。当对其疏水端进行功能化,在外界刺激情况下,聚合物疏水端可以转化为亲水端,从而使胶束破裂达到控制释放的目的。由于稳定,合成简单,灵敏度高,成本较低,和存储方便,刺激响应胶束放大体系具有独特的优势用于生物传感器研究。最常用的引发靶物质主要有:pH(Angew.Chem.2010,122,4342-4345.)、生物大分子(J.Am.Chem.Soc.2015,137,1412–1415.)、酶(J.Am.Chem.Soc.2012,134,10244–10250.)、氧化还原(J.Am.Chem.Soc.2013,136,574–577.)、电势(Angew.Chem.Int.Ed.2013,52,6926–6929.)、气体(J.Am.Chem.Soc.2013,135,16300–16303.)、温度(Macro.Lett.2014,3,1235–1239.)及光(J.Am.Chem.Soc.2013,135,4765–4770.)等。在响应过程中,将大量包载物释放导致响应信号呈指数提升,实现对超微含量分析物实现探测感知。
本发明结合了新型功能化的聚碳酸酯,利用了合成的带有识别位点的聚合物胶束对H2O2的响应特性,以及胶束响应后释放的淀粉与随后加入的碘变蓝的络合化学反应,设计了一种信号放大的组织活检技术,并用于可视化高灵敏度识别早期含量较少的肿瘤标志物,实现对癌症早期诊断。同时也是对传统组织病理学活检方法缺乏足够代谢物信息的一个重大突破。
技术实现要素:
本发明的目的在于,为了克服现有癌症诊断中组织病理学活检方法缺乏信号放大的不足,结合响应聚合物纳米材料的优势,提出了一种具有信号放大功能的H2O2响应的包载淀粉的聚合物纳米胶束。以此作为癌症早期诊断的新方法。从而达到对癌症早期诊断的目的。本发明的癌症诊断方法方便简单快速,无需昂贵仪器,花费低廉,检测灵敏度高,同时也是对传统组织病理学活检方法缺乏足够代谢物信息的一个重要突破,具有良好的实际应用前景。
为实现上述目的,本发明的技术方案是:
一种基于信号放大的可视、灵敏活组织切片检查法。尽管癌症组织中含有比正常组织中更多的H2O2,但在癌症早期,组织切片中H2O2含量较少。所以本发明可以在癌症早期组织切片上释放出包载的大量淀粉,形成信号放大。随后,在组织切片上滴加碘溶液,会产生碘与淀粉形成大量的蓝色络合物。从变蓝程度就可以直观的指示组织中H2O2的含量。以此为癌症早期诊断的新方法。
具体为:将包载有淀粉的H2O2响应胶束分散在PBS缓冲溶液中,定容。然后,将一定量的胶束溶液滴加到已知面积的癌症组织切片上面,使胶束与组织切片充分作用一段时间。随后加入碘,使组织切片上胶束响应后释放出来的淀粉变蓝。通过普通显微镜放大可以直观地对组织切片变蓝的程度及组织学特征进行观察,实现对癌症早期诊断。
所述淀粉包载量与H2O2响应胶束的质量比为1:5-5.1,且最终浓度定为0.48-0.51mg/mL
所述PBS缓冲溶液的pH为7.2-7.4。
所述胶束溶液为0.48-0.51mg/mL。
所述癌症组织切片厚度为28-30μm。面积为:0.25-0.30cm2。
所述胶束与组织切片作用时间为:90-105min,所述加入碘的含量为:1mM/L-1.2mM/L,所述普通显微镜型号为:尼康TE 2000显微镜,所用的镜头100×。
H2O2响应胶束PMPC-Bpe中主链PMPC的合成方法为现有方法,本发明所述响应胶束的合成过程优选为:
(1)4-羟甲基苯硼酸嚬呐醇酯的合成
向50mL反应管中,加入(3.81g,25mmol)4-羟甲基苯硼酸,频哪醇(3.54g,30mmol),加入甲苯10mL,加热回流2小时。当反应产物冷却至室温后,用水洗(3×150mL)有机层减压蒸馏蒸出溶剂后,加入CH2Cl2100mL。所得CH2Cl2溶液用饱和氯化钠溶液洗涤(3×150mL),再用无水MgSO4干燥,过滤,滤液收集,除去溶剂得白色固体4-羟甲基苯硼酸嚬呐醇酯(4.84g,82.7%)。
(2)4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环)-2-苄基-3-溴-丙酸酯的合成
在500毫升圆底烧瓶中加入,三乙胺(6.07g,60mmol)、4-羟甲基苯硼酸嚬呐醇酯(9.36g,40mmol)和干燥的THF(200mL)在冰水浴冷却到0℃,然后将3-溴丙酰氯(6.84g,40mmol)溶解在100mL干燥的THF中,滴加入烧瓶中,在持续搅拌1h。滴毕,反应混合物在室温下搅拌过夜。经过过滤和蒸发后,残留物用乙酸乙酯稀释,并分别用水和盐水洗两次。有机层在无水干MgSO4、过滤、浓缩,最后通过硅胶柱色谱纯化使用乙酸乙酯/石油醚(1/3v/v)作为洗脱液。得到淡黄色的液体(9.48g,yield:71.6%)。
(3)4-(4,4,5,5-四甲基-1,3,2-二氧硼戊环)-2-苄基-3-叠氮-丙酸酯的合成(Bpe-N3)
化合物2(4.43g,12.0mmol)和叠氮化钠(1.56g,24.0mmol)溶解在DMF中(15mL),混合物在室温下搅拌24小时。待反应完全,向瓶中加入CH2Cl2(100mL)、分液,水相用CH2Cl2(100mL×3)萃取三次。合并有机相,并在无水MgSO4中干燥、过滤和蒸发干燥。得到的产品为黄色固体粉末。产量:3.58g(90.1%)。
(4)2,2-二羟甲基丙酸丙炔酯的合成
向50mL圆底烧瓶中,加入2.24g 2,2-二羟甲基丙酸,1.01g氢氧化钾,再加入20mL DMF,于100℃下反应2h,再逐滴加入2.13g溴丙炔,半小时滴毕,反应72h,停止反应,过滤,减压旋干溶剂,加CH2Cl2溶解,饱和的盐水溶液萃取(20mL×3),收集有机相得粗产物,过柱分离(PE:EA=5∶1),得到产物,产率45.14%。
(5)MPC的合成
向50mL两口圆底烧瓶中,加入1.18g化合物2,1.48g氯甲酸乙酯,再加入20mL DMF,氮气保护下于冰浴下搅拌1h,再逐滴加入1.39g三乙胺,半小时滴毕,反应3h后于室温下过夜反应,过滤,减压旋干溶剂,粗产物用乙酸乙酯:乙醚=1:1重结晶,得到白色结晶产物,产率91.05%。
(6)PEG-b-poly(MPC)的合成
MPC的开环聚合是采用标准的希莱克技术,在氮气保护下进行的。向50mLSchlenk瓶中,加入0.594g MPC,0.601g PEG5k,0.055g TU,0.005g DBU,再加入10mL CH2Cl2,橡胶塞封口,再经过冷冻为固态-抽真空-解冻三次循环,室温搅拌7h,加冰乙醚析出沉淀,离心分离,过滤,旋干溶剂,得到白色粉末产物,产率92.0%。
PMPC-Bpe胶束制备及相关参数的测试为现有方法,本发明所述的过程优选为:
(1)胶束制备为现有方法,本发明所述的过程优选为:
PEG-b-poly(MPC)和PMPC-Bpe的胶束通过透析法制备。取25.0mg共聚物溶解在四氢呋喃中,搅拌下缓慢加入10mL去离子水。室温搅拌2h,制得胶束,然后用去离子水透析24h除去DMF(MWCO 1KDa),再加去离子水调节最终聚合物浓度为0.5mg mL-1。
(2)临界胶束浓度的测定(CMC)为现有方法,本发明所述的过程优选为:
MPC聚合物和PMPC-Bpe两亲聚合物的临界胶束浓度(CMC)是以尼罗红(NR)作为探针分子通过染料增溶法来测定的。用微量调节注射器将溶在THF中的尼罗红(0.1mg mL-1,30μL)注入一个小玻璃瓶中,蒸干THF,再加入2mL的胶束溶液,搅拌5h,胶束溶液的浓度为0.1~5×10-4mg mL-1。在550nm的激发波长下进行荧光检测,收集570nm到750nm的发射波。
(3)细胞毒性的检测为现有方法,本发明所述的过程优选为:
胶束对作为模型的海拉细胞的细胞毒性的评估使用了标准的细胞活性检测法即MTT比色法测定。Hela细胞接种于96孔板,并在浓度为5×103细胞的含10%胎牛血清的100μL MEM培养基中,在5%CO2并在37℃下孵化24小时。然后,将培养基用200μL聚合物胶束取代。用DMEM培养基稀释法分别制备了每个配方的总浓度。细胞培养的培养基为对照。细胞用PBS洗三次,然后将100μL MTT溶液(在0.5mg mL-1PBS中)添加到每个小孔中。加入DMSO(150μL/well)后,检测板在室温下摇动10分钟。该实验平行做三次。基于570nm测定紫外-可见吸收,并使用以下公式计算细胞存活率,OD570代表光密度。
Cell viability=[OD570(sample)-OD570(blank)]/[OD570(control)-OD570(blank)]
以下对本发明做进一步说明:
本发明的原理是:将包载有淀粉的H2O2响应胶束分散在PBS缓冲溶液中,定容。然后,将一定量的胶束溶液滴加到已知面积的癌症组织切片上面,使胶束与组织切片充分作用一段时间。随后加入碘,使组织切片上胶束响应后释放出来的淀粉变蓝。通过普通显微镜放大可以直观地对组织切片变蓝的程度及组织学特征进行观察,实现对癌症早期诊断。
本发明进行癌症早期诊断所用到的淀粉包载量与H2O2响应胶束的质量比为1:5-5.1,且最终浓度定为0.48-0.51mg/mL;PBS缓冲溶液的pH为7.2-7.4;胶束溶液为0.48-0.51mg/mL;癌症组织切片厚度为28-30μm;面积为:0.25-0.30cm2;胶束与组织切片作用时间为:90-105min;碘的含量为:1mM/L-1.2mM/L,所用普通显微镜型号为:尼康TE 2000显微镜,所用的镜头100×。
与现有技术相比,本发明的优势在于:
提出了一种基于信号放大的H2O2响应的包载淀粉的聚合物纳米胶束。以此为癌症早期诊断的新方法,达到对癌症早期诊断的目的。本发明的癌症诊断方法方便简单快速,无需昂贵仪器,花费低廉,检测灵敏度高,同时也是对传统组织病理学活检方法缺乏足够代谢物信息的一个重要突破,具有良好的实际应用前景。
【附图说明】
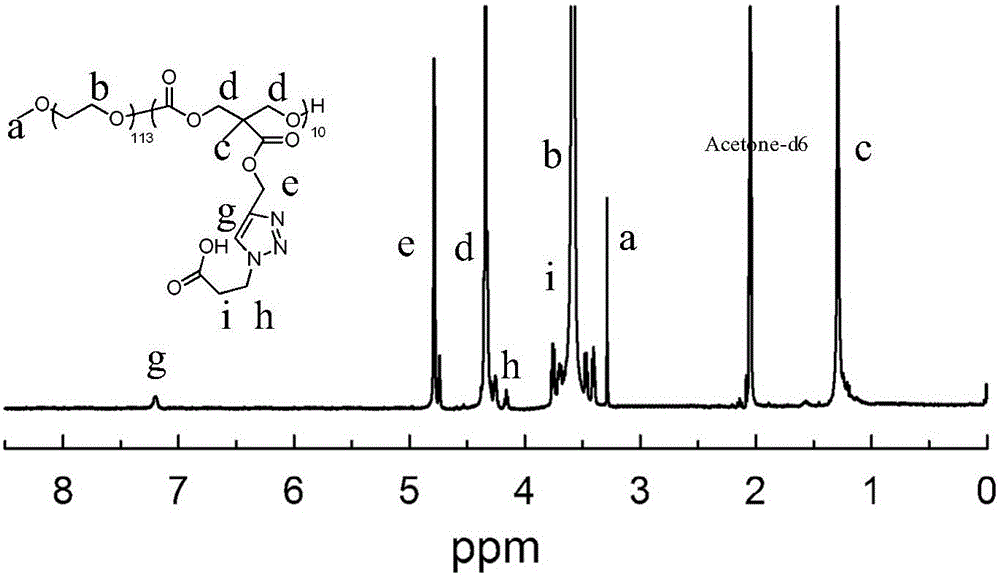
图1-1为实施例1中制得的以H2O2响应聚合物PMPC-Bpe的1HNMR分析;
图2-1为实施例2中PMPC-Bpe胶束对H2O2检测的工作原理;
图2-2为实施例2中PMPC-Bpe胶束对H2O2的可行性。
图3-1为实施例3中H2O2识别的灵敏度;
图3-2为实施例3中H2O2识别的选择性。
图4-1为实施例4中PMPC-Bpe@amylose/I2胶束体系用于癌症组织早期诊断中测试响应时间;
图4-2为实施例4中PMPC-Bpe@amylose/I2胶束体系用于癌症组织不同(早、中、晚期)时期癌症诊断;
图4-3为实施例4中PMPC-Bpe@amylose/I2胶束体系用于癌症组织癌旁组织诊断。
【具体实施方式】
以下结合附图对本发明的实施例作详细说明:本实施例在以本发明技术方案为前提下进行实施,给出了详细的实施方式和过程,旨在易于理解本发明的技术方案特征,对本发明的保护范围不构成任何限制。凡采用等同变换或者是等效替换而形成的技术方案,均落在本发明权利保护范围之内。
实施例1H2O2响应胶束PMPC-Bpe的点击化学合成
向50mL Schlenk瓶中,加入200mg PEG-b-poly(MPC),76.13mg Bpe-N3,4.50mg抗坏血酸钠,再加入4mL DMF,橡胶塞封口,再经过冷冻为固态-抽真空-解冻三次循环后,加入DMF溶解的2.8mg硫酸铜,室温搅拌反应24h,用去离子水透析3天(透析袋3500MWCO),冰冻法得产物,产率81.30%。
核磁1H NMR谱图分析:从图1-1可以看出,PMPC-Bpe的合成是在MPC的开环聚合是基础上,采用标准的希莱克技术,在氮气保护下进行的。向50mL Schlenk瓶中,加入0.594g MPC,0.601g PEG5k,0.055g TU,0.005g DBU,再加入10mL CH2Cl2,橡胶塞封口,再经过冷冻为固态-抽真空-解冻三次循环,室温搅拌7h,加冰乙醚析出沉淀,离心分离,过滤,旋干溶剂,得到白色粉末产物,产率92.0%。1H NMR(400MHz,CDCl3):δ=4.73(d,OCH2CCH),4.28-4.32(m,OC(O)OCH2),3.65(s,OCH2CH2O),3.38(s,CH3O),2.55(s,CH2CCH),2.19(s,OH),1.29(s,CH3).GPC(THF,RI):Mn(PDI)=7263g mol-1(1.04).
实施例2PMPC-Bpe胶束对H2O2检测的工作原理及可行性
H2O2的识别位点4-羟甲基苯硼酸嚬呐醇酯与聚碳酸酯主链的疏水端发生开环聚合。当PMPC-Bpe共聚物和淀粉置于水溶液中,胶束发生自组装,并且疏水的淀粉被包裹在胶束中。在没有H2O2时,H2O2的识别位点在生理条件下是稳定的,这使得胶束也是稳定的。相反,当有H2O2时,识别位点与H2O2发生反应导致4-羟甲基苯硼酸嚬呐醇酯断裂,且疏水端变为亲水性的羧基端,使胶束解离。胶束的解离释放出包裹的淀粉,与随后加入的碘,形成碘与淀粉络合物,在可见光处574nm处呈现明显的蓝色。因此,可以用荧核磁1H NMR来验证胶束对H2O2检测的工作原理(图2-1)。
核磁1H NMR谱图分析:在1H NMR分析中,一个可以看到信号δ=5.25,7.36和7.88消失和出现微弱信号在δ=3.76和4.17,这意味着反应顺利进行,并且成功脱去了H2O2识别位点。
为了验证共聚胶束对H2O2检测的可行性,制备了包裹淀粉的H2O2响应的PMPC-Bpe胶束。当在胶束溶液(0.5mg mL-1)中加入H2O2响应90min后,直接加入碘,溶液变蓝且在574nm有吸收。当在空白组胶束溶液(0.5mg mL-1)中加入碘后,溶液没变蓝且在574nm没有吸收见图2-2。这些实验明确的表明,成功地合成了对H2O2响应的PMPC-Bpe胶束。
吸收谱图分析:在加入1μM过氧化氢,PMPC-Bpe胶束分离直链淀粉释放到解决方案,然后处理KI/I2,表现出明显的变化从无色到蓝色,且吸收峰在574nm处明显增强。相反,如果没有加入没有过氧化氢或加了H2O2,但是没有加入KI/I2吸光度在574nm没有明显变化。
实施例3H2O2识别的灵敏度和选择性
为了验证所提出的对H2O2定量检测方法的适用性,我们测量了一系列在PBS缓冲溶液中含不同H2O2浓度的PMPC-Bpe胶束反应后加入碘的吸收光谱(图3-1)。增加H2O2的浓度造成更多的4-羟甲基苯硼酸嚬呐醇酯发生重排、裂解使胶束的不稳定,从而提高胶束的裂解并释放出淀粉,随着H2O2浓度的增加,吸收强度明显增加,且呈浓度依赖性。其线性范围在0.5-80μM之间。随着H2O2浓度的进一步增加,胶束分解完并且加入KI/I2吸收强度达到一个最高值。基于3σ规则,其检测限为0.1μM。
吸收谱图分析:如图3-1,过氧化氢浓度的增加导致更多硼酸酯裂解反应和胶束的不稳定,从而提高胶束的离解和。在添加以后的KI/I2,所形成复合物在574nm处有一个独特吸收峰,且随着过氧化氢浓度的增加吸光度大大增加。如插图所示,获得的线性范围是0.5-80μM之间。检测极限计算是基于3σ规则,其检测限为0.1μM。这个值是检测组织中过氧化氢浓度足够低。
由于4-羟甲基苯硼酸嚬呐醇酯对H2O2的识别具有高的选择性,所以PMPC-Bpe胶束对H2O2的检测也具高选择性(图3-2)。然后对PMPC-Bpe对H2O2的选择性进行了确定。在各种高浓度氧化剂的存在下,包括过氧乙酸(CH3COOOH),单线态氧(1O2),叔丁基自由基(tBuO·),羟基自由基(HO·),次氯酸(HClO/-OCl),三价铁离子(Fe3+),亚硝基(NO2-),硝基(NO3-),叔丁基过氧化氢(TBHP)及一氧化氮(NO)等进行了检测,无明显吸收变化表明其对探针没有响应。这表明胶束对上述的还原剂没有响应并且只对H2O2具有高选择性。
吸收谱图分析:如图3-2,PMPC-Bpe胶束的选择性(0.5mg mL-1)对各种活性氧包括过氧乙酸(CH3COOOH),单线态氧(1O2),叔丁基自由基(tBuO·),羟基自由基(HO·),次氯酸(HClO/-OCl),三价铁离子(Fe3+),亚硝基(NO2-),硝基(NO3-),叔丁基过氧化氢(TBHP)及一氧化氮(NO)等进行了检测。从图中可以明显看出,加入H2O2,后574nm处吸收峰明显增强,说明此体系对于H2O2有着较高的选择性。
实施例4PMPC-Bpe@amylose/I2胶束体系用于癌症组织早期诊断
(1)在癌症诊断之前,体系长期稳定性非常重要。因此我们测定了在人类细胞裂解液及高浓度的牛血清白蛋白中的稳定性。这些研究通过胶束响应后加入碘,在不同存储时间测试其收光谱。结果表明,胶束PMPC-Bpe@Amylose在生物条件下24小时都非常稳定。
(2)实际样品测试响应时间
在一组组织切片中,加入同一浓度的PMPC-Bpe@Amylose(0.5mg mL-1)。在同不同时间时加入KI/I2。图4-1中,成像清楚地表明,颜色开始变化出现在45分钟时。在90到105分钟的时候颜色基本不再改变。说明实际测试时间为90-105分钟之间。
显微镜图像分析:乳腺癌组织切片后用PMPC-Bpe@Amylose(0.5mg mL-1)孵育。然后加入KI/I2和拍摄时间为15,30,45,60,75,90和105分钟。从TE2000显微镜获得图像(日本尼康仪器公司)(100×)。标尺:20nm。
(3)不同(早、中、晚期)癌症诊断
肿瘤异种移植小鼠模型用于癌症不同阶段诊断(图4-2)。癌组织冰冻切片加入PMPC-Bpe@amylose(0.5mg mL-1)后,在不同时间段(0、6、12、18、24、30)中,用KI/I2处理,蓝色的明显增强。意味着PMPC-Bpe@Amylose系统可以用于癌症诊断的不同阶段并且此方法能完全测试到早期癌症。
显微镜图像分析:异种移植肿瘤在不同时间的乳腺癌肿瘤切片。冷冻癌组织切片MPC-Bpe@amylose(0.5mg mL-1)后,在0,6,12,18,24,30天分别测试。然后,然后用KI/I2处理和拍照。从TE2000显微镜获得图像(日本尼康仪器公司)(100×)。标尺:20nm
(4)实际样本诊断
我们将上述方法应用在实际样品的诊断方面。三种来自湖南省肿瘤医院的癌症患者投入调查(图4-3)。将所取得的肿瘤样本冰冻切片后,进行诊断。在控制组中,癌组织切片分别用PMPC-Bpe@Amylose、KI/I2、以及空白样本。发现个控制组中没有颜色变化。然而,组织切片PMPC-Bpe@Amylose孵育,然后用KI/I2处理发现癌症组织中有明显的颜色变化。且变化的深度为宫颈癌<结肠癌<乳腺癌。说明胶束探针可以识别不同癌症组织中的H2O2,并且在癌症组织中三种病人所产生的H2O2是不一样的。并且与相关文献报道相符合。
显微镜图像分析:三位癌症病人组织样本经过冷冻切片后,分别孵育:分别用PMPC-Bpe@Amylose、KI/I2、以及空白样本。发现个控制组中没有颜色变化。然而,组织切片PMPC-Bpe@Amylose孵育,然后用KI/I2处理发现癌症组织中有明显的颜色变化。且变化的深度为宫颈癌<结肠癌<乳腺癌。PMPC-Bpe@Amylose胶束浓度为0.5mg mL-1,KI/I2(1μM)处理和拍照。从TE2000显微镜获得图像(日本尼康仪器公司)(100×)。标尺:20nm。
- 还没有人留言评论。精彩留言会获得点赞!
- 癌症病理演变前期microrna-330水平原位杂交检测试剂盒及检测方法和应用的制作方法
- 癌症病理演变前期microrna-16-1水平原位杂交检测试剂盒及检测方法和应用的制作方法
- 各种癌症病理演变前期microrna-10b水平原位杂交检测试剂盒及检测方法和应用的制作方法
- 各种癌症病理演变前期microrna-520水平原位杂交检测试剂盒及检测方法和应用的制作方法
- 各种癌症病理演变前期microrna-373水平原位杂交检测试剂盒及检测方法和应用的制作方法
- 各种癌症病理演变前期microrna-372水平原位杂交检测试剂盒及检测方法和应用的制作方法
- 各种癌症病理演变前期microrna-21原位杂交检测试剂盒及检测方法和应用的制作方法