一种醒脑降压丸的含量测定方法与流程
本发明涉及一种醒脑降压丸的含量测定方法,属于中药制剂含量测定技术领域。
背景技术:
高血压病是一种不明原因的以动脉血压增高为主要表现的心血管疾病,不加治疗,可导致脑、心和肾等重要脏器的严重损害,甚至致残或致死。许多大规模的临床研究结果显示,高血压病人注意自我保健,规则服用降压药,有效控制高血压可显著降低脑卒中和死亡率。
醒脑降压丸由黄芩、黄连、郁金、栀子、玄精石、珍珠母、辛夷、零陵香、朱砂、雄黄、冰片等共11味药材组成。具有通窍醒脑,清心镇静,抗热消炎之功效。现行质量标准收载于“《卫生部药品标准》中药成方制剂第二册”,该标准无含量测定项目,缺乏控制药品质量的手段。为提高该药品质量控制水平,对醒脑降压丸质量标准进行了提高、完善,起草制定了醒脑降压丸的质量标准。
技术实现要素:
本发明公开了一种醒脑降压丸的含量测定方法,其特征在于按如下的步骤进行:
(1)确定色谱条件:以十八烷基硅烷键合硅胶为填充剂;以甲醇-水-磷酸体积比为40:60:0.2做为本品的流动相;检测波长为280nm;柱温35℃;流速1ml/min,理论塔板数按厚朴酚峰计算应不低于7000;
(2)对照品溶液的制备: 取黄芩苷对照品适量,精密称定,加甲醇制成每1ml含0.1mg的溶液,即得;
(3)供试品溶液的制备:取同一批号样品,研细,取0.3g,精密称定,分别精密加入甲醇、70%甲醇摇匀,称定重量,超声处理,功率150W,频率20kHz,45分钟,取出,放冷,再称定重量,用各自得溶液补足减失的重量,摇匀,滤过,取续滤液,即得;所测含量为13.9~17.5mg/g;
(4)测定法:分别精密吸取对照品溶液与供试品溶液各10μl,注入液相色谱仪,测定,每1g含黄芩以黄芩苷(C21H18O11)计,不得少于11.5mg。
本明更加详细的方法如下:
1仪器与试药
仪器:SHIMADZU LC-20AD高效液相色谱仪,二极管阵列检测器,LC solution工作站。色谱柱:Phenomenex C18(250×4.6 mm,5μm);Venusil C18 (250×4.6 mm,5μm);SepaxSappire C18(250×4.6mm,5μm)。
试剂:甲醇(色谱纯,天津市康科德科技有限公司),磷酸(分析纯,天津化学试剂厂),水为去离子水。
对照品:黄芩苷(中国药品生物制品检定所购置,批号:110715-201117;为含量测定用对照品,纯度91.7%)。
样品:天津中新药业集团股份有限公司乐仁堂制药厂提供(批号:2012001、 C130040、B130033、D130045、无批号)。
2、色谱条件的确定
2.1 检测波长的确定
根据《中国药典》2010年版一部有关黄芩苷含量测定方法,采用280nm波长为本试验的检测波长。
2.2 流动相的考察
本品采用了:甲醇-水-磷酸(40:60:0.2);甲醇-水-冰醋酸(40:60:1);
甲醇-水(45:55)三种不同的流动相予以比较,结果加入少量酸的二种流动相色谱峰的峰形较好,和杂质峰能得到较好分离。结果选择流动相甲醇-水-磷酸(40:60:0.2)做为本品的流动相。
2.3 色谱条件与系统使用性试验:参照《中国药典》2010年版一部有关含量测定方法并根据以上考察制定了本含量测定方法的色谱条件。以十八烷基硅烷键合硅胶为填充剂;以甲醇-水-磷酸(40:60:0.2)为流动相;检测波长为280nm,柱温:35℃;流速:1ml/分钟。理论板数按黄芩苷峰计算应不低于7000。
3、提取方法的选择
3.1提取溶剂的考察:取同一批号(2012001)样品,研细,取约0.3g,精密称定,分别精密加入甲醇、70%甲醇、50%甲醇25ml,摇匀,称定重量,超声处理(功率150W,频率20kHz)60分钟,取出,放冷,再称定重量,用各自得溶液补足减失的重量,摇匀,滤过,取续滤液,即得。测定样品中黄芩苷含量,结果见表(1);表(1)提取溶剂的选择
表(1)显示,提取溶剂使用单纯的甲醇提取,含量测定结果较低;而采用加有水的不同比例的甲醇,测定结果基本相同(除甲醇提取的外,其他4种提取方法测定结果的RSD为2.3%),采用70%甲醇提取,测定的含量最高,故本试验提取溶剂定为70%甲醇。
3.2提取方式的考察:取同一批号(2012001)样品,研细,取约0.3g,精密称定,精密加入70%甲醇25 ml,摇匀,称定重量,分别超声处理(功率150W,频率20kHz)或加热回流60分钟,取出,放冷,再称定重量,用70%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。测定样品中黄芩苷含量。结果见表(2)。
表(2) 提取方式的选择
如表(2)所示,采用超声提取与回流提取不同的提取方式,其测定结果基本相同,不同提取方式的样品测定结果的RSD均为0.97%。为试验操作方便简捷,故将超声提取定为本提取方法。
3.3提取时间的考察:取同一批号(2012001)样品,研细,取约0.3g,精密称定,精密加入70%甲醇25 ml,摇匀,称定重量,分别超声处理(功率150W,频率20kHz)30、45、60分钟,取出,放冷,再称定重量,用70%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。测定样品中黄芩苷含量,结果见表(3)。
表(3) 提取时间的选择
表(3)显示,提取时间30分钟~60分钟,其含量测定结果无明显差异,3种不同提取时间测定结果的RSD为2.01%),提取时间为45分钟的测定结果较高故选定超声处理时间为45分钟。
3.4取样量的考察:取同一批号(2012001)样品,研细,分别取约0.1g、0.2g、0.3g,精密称定,精密加入70%甲醇25ml,摇匀,称定重量,分别超声处理(功率150W, 频率20kHz )45分钟,取出,放冷,再称定重量,用70%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。测定样品中黄芩苷含量。结果见表(4)
表(4) 取样量的选择
表(4)显示,取样量0.1 g、0.2g、0.3 g,测定结果基本相同(RSD=0.96%),故本试验将取样量定为0.3 g为取样量 。
4 、溶液的制备
4.1对照品溶液的制备: 取黄芩苷对照品适量,精密称定,加甲醇制成每1ml含0.1mg的溶液,即得。
4.2供试品溶液的制备:取本品适量,研细,取约0.3g,精密称定,精密加入70%甲醇25ml,摇匀,称定重量,超声处理(功率150W, 频率20kHz )45分钟,取出,放冷,再称定重量,用70%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
4.3阴性样品溶液的制备:按处方取除黄芩的各味药材,按【制法】制得样品,再按供试品溶液制备方法,制得阴性样品溶液。
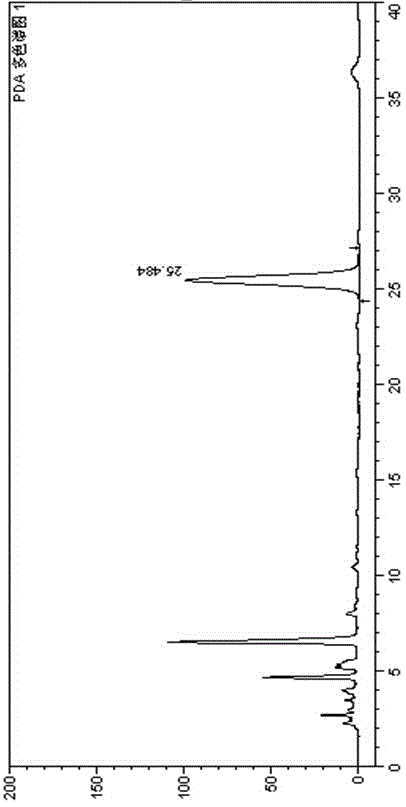
4.4 测定: 将各种溶液,分别精密吸取10μl,注入高效液相色谱仪中,按色谱条件分析。得到的色谱图如下,对照品溶液色谱图见图1,供试品溶液色谱图见图2,阴性样品溶液色谱图见图3。如图可见,阴性样品在黄芩苷色谱峰处无干扰。二极管阵列检测器从样品色谱和黄芩苷对照品色谱相应的色谱峰中提取出的光谱图,光谱特征一致,峰纯度指数为0.9999,未检出不纯峰。专属性考察符合规定。对照品黄芩苷色谱峰光谱图见图4,样品黄芩苷色谱峰光谱图见图5。
5、标准曲线的制备
取黄芩苷对照品适量,精密称定,加甲醇制成每ml含0.191415mg的溶液,作为对照品溶液,分别精密吸取上述对照品溶液各2μl ,5μl ,10μl,15μl,20μl,25μl注入液相色谱仪,按色谱条件分析,测定各自峰面积,以对照品进样量(μg)为横坐标,峰面积值为纵坐标,求得回归方程:Y=3.315255×106 x + 5.2682×104 r=0.9999。结果表明黄芩苷在0.38283μg~4.78538μg范围内线性良好,结果见表(5)。
表(5) 黄芩苷标准曲线
5.1进样重复性(精密度)试验
取同一批号(2012001)样品,研细,取约0.3g,按照供试品溶液制备操作,按色谱条件分析,连续进样6次,测定样品中黄芩苷峰面积,测得峰面积平均值:7594232;峰面积的RSD为0.10%,符合要求,结果见表(6)。
表(6) 进样重复性试验
5.2重现性试验
取同一批号(2012001)样品6份,研细,取约0.3g,按照供试品溶液制备操作,按色谱条件分析,测定每份样品中黄芩苷含量。结果样品中黄芩苷平均含量为17.1550mg/g,RSD为1.38%,符合要求,结果见表(7)。
表(7) 重现性试验
5.3稳定性试验
取同一批号(2012001)样品,研细,取约0.3g,按照供试品溶液制备操作,按色谱条件分析,分别在0、3、6、9、12、15小时,测定样品中黄芩苷峰面积,测得峰面积值的RSD为0.73%,说明样品溶液在15小时内稳定,符合试验要求,结果见表(8)。
表(8) 稳定性试验
5.4回收率试验
取同一批号(2012001)样品,研细,取约0.15g,共6份,精密称定,分别精密加入黄芩苷对照品70%甲醇溶液(0.15951mg/ml)15ml,再分别精密加入70%甲醇溶液10ml,再按照供试品溶液制备操作,制得供回收率用供试品溶液,按色谱条件分析,计算回收率,结果平均回收率为96.9%,RSD为1.04%。符合试验要求。结果见表(9)。
表(9) 回收率试验
5.5样品测定
取5个批号的样品,按照供试品溶液制备操作,按色谱条件测定样品中黄芩苷含量。结果见表(10)。
表(10) 5批样品含量测定结果
5.6同色谱柱及不同仪器对含量测定的影响
5.6.1不同色谱柱对含量测定的影响
取同一批号(2012001),按照供试品溶液制备操作,使用日本SHIMADZU LC-20AD高效液相色谱仪,LC solution工作站。分别使用Phenomenex C18(250×4.6 mm,5μm),SepaxSappire C18(250×4.6 mm,5μm),Venusil C18(250×4.6 mm,5μm),色谱柱,按色谱条件分析,测定样品中黄芩苷含量。结果见表(11)。
表(11) 不同色谱柱对含量测定的影响
测定结果显示,不同色谱柱对含量测定的影响很小,不同色谱柱测定的6份数据的RSD为0.68%。
5.6.2度的制定
处方中,黄芩占处方总量的20.51%,制剂中每g样品约含黄芩生粉205mg。参照《中国药典》2010年版一部黄芩饮片项下含量限度(8.0% )计算,每g样品含黄芩苷应为16.4mg。本制剂黄芩采用部分生粉入药,部分用60%乙醇提取的工艺,按70%转移率计算,为每g含黄芩以黄芩苷(C21H18O11)计,为11.5mg。表(11)显示,天津中新药业集团股份有限公司乐仁堂制药厂生产的5批样品,1批含量较低外,其他4批均可达到上述规定,所测含量为13.9~17.5mg/g。故含量限度制定为每1g含黄芩以黄芩苷(C21H18O11)计,不得少于11.5mg。
本发明公开的醒脑降压丸含量测定方法所具有的积极效果在于:
(1)发明了醒脑降压丸中黄芩苷的测定方法。
(2)增加了含量测定项目,提高了控制药品质量的手段。
附图说明:
图1对照品溶液色谱图;
图2 样品溶液色谱图;
图3阴性样品色谱图;
图4对照品溶液黄芩苷色谱峰光谱图;
图5样品溶液黄芩苷色谱峰光谱图。
具体实施方式
下面通过具体的实施方案叙述本发明。除非特别说明,本发明中所用的技术手段均为本领域技术人员所公知的方法。另外,实施方案应理解为说明性的,而非限制本发明的范围,本发明的实质和范围仅由权利要求书所限定。对于本领域技术人员而言,在不背离本发明实质和范围的前提下,对这些实施方案中的物料成分和用量进行的各种改变或改动也属于本发明的保护范围。本发明所用药材均有市售。
实施例1
【处方】黄芩 184g 黄连 92g 郁金 92g
栀子 92g 玄精石 92g 珍珠母 69g
辛夷 38g 零陵香 8g 朱砂 92g
雄黄 92g 冰片 46 g
【制法】以上十一味,朱砂、雄黄分别水飞或粉碎成极细粉;冰片研细;取黄芩92g与黄连等七味粉碎成细粉,其余黄芩用60%乙醇加热回流提取,提取液回收乙醇后浓缩成膏,干燥,粉碎成细粉,加入黄芩等粉末,混匀,再与朱砂、雄黄、冰片粉末配研,过筛,混匀。用水泛丸,干燥;即得。
【用法与用量】口服,一次10~15粒,一日1~2次。
【注意】孕妇及胃肠溃疡者忌用。
【规格】每10粒重2.2g
【贮藏】密封。
实施例2
醒脑降压丸的含量测定方法:
一种醒脑降压丸的含量测定方法,其特征在于按如下的步骤进行:
(1)确定色谱条件:以十八烷基硅烷键合硅胶为填充剂;以甲醇-水-磷酸体积比为40:60:0.2做为本品的流动相;检测波长为280nm;柱温35℃;流速1ml/min,理论塔板数按厚朴酚峰计算应不低于7000;
(2)对照品溶液的制备: 取黄芩苷对照品适量,精密称定,加甲醇制成每1ml含0.1mg的溶液,即得;
(3)供试品溶液的制备:取同一批号样品,研细,取0.3g,精密称定,分别精密加入甲醇、70%甲醇摇匀,称定重量,超声处理,功率150W,频率20kHz,45分钟,取出,放冷,再称定重量,用各自得溶液补足减失的重量,摇匀,滤过,取续滤液,即得;所测含量为13.9~17.5mg/g;
(4)测定法:分别精密吸取对照品溶液与供试品溶液各10μl,注入液相色谱仪,测定,每1g含黄芩以黄芩苷(C21H18O11)计为11.9mg。
- 还没有人留言评论。精彩留言会获得点赞!