盐酸帕洛诺司琼合成中间产物的HPLC分析方法与流程
本发明属于药物分析领域,涉及药物中间体的反应监控,具体涉及n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺及其异构体的hplc分析方法。
背景技术:
盐酸帕洛诺司琼是由瑞士mgipharma及helsinnhealthcare公司研制开发的高效、高选择性的5-ht3受体拮抗剂,于2003年7月首先在美国获准上市,临床上用于放、化疗所致的急性和延迟性恶心、呕吐。因其具有疗效高、毒副作用小、半衰期长、用药剂量小等特点而备受关注(palonosetronforthepreventionofchemotherapy-inducednauseaandvomiting:approvalandefficacy,cancermanagres,2009)。
盐酸帕洛诺司琼的合成工艺较多,但是这些工艺步骤多,副产物多,有些步骤反应条件甚为苛刻,需要特别的试剂,不适合于工业化生产。朱阳等提供了一种盐酸帕洛诺司琼盐酸盐的合成工艺(盐酸帕洛诺司琼的合成,中国医药工业杂志,2009,40),其反应条件温和,无需特殊试剂和设备,但是存在以下两个不足:(1)收率过低,盐酸帕洛诺司琼(即ss型)的总收率仅有12%;(2)由n-[(3,4-二氢萘-1-基)甲基]-1-氮杂二环[2.2.2]-辛烷-3-胺二盐酸盐制备n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺的步骤中需要进行手性拆分。
为了提高收率,同时进一步简化工艺,申请人对朱阳等的工艺进行了改进,工艺如下:
步骤s1,以3,4-二氢-1-萘甲胺盐酸盐和3-奎宁环酮盐酸盐为原料缩合还原制备得到n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺的正丁醇溶液;
步骤s2,直接在n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺的正丁醇溶液中加入催化剂氢化还原得到n-[(1,2,3,4-四氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺;
步骤s3,将n-[(1,2,3,4-四氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺环合成盐得到盐酸帕洛诺司琼盐酸盐;
其中,步骤s1操作如下:将3,4-二氢-1-萘甲胺盐酸盐、3-奎宁环酮盐酸盐和甲苯在搅拌下加入三乙胺加热回流反应,减压蒸除溶剂,剩余物中加入正丁醇,加入硼氢化钠常温反应,减压蒸除正丁醇,剩余物中加入水,用水饱和的正丁醇萃取,合并正丁醇萃取液体,干燥,过滤,即可得到n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺的正丁醇溶液。
经过申请人改进之后,n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺产物中,其r型异构体的含量显著降低(由改进前的32%降为现在的2%以内),因而不需要进行手性拆分即可直接用作下一步反应的原料,大大简化了工艺,提高了收率。
n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺及其异构体结构式如下:
n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺产物r型异构体的含量监控依然是申请人必须要做的工作之一,以确保r型异构体不要超过2%,降低下一步反应的副产物。前述朱阳等使用手性色谱柱对n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺及其r型异构体进行分离检测(hplc法:daicelod-h手性柱,流动相为正己烷:异丙醇=95:5,检测波长254nm)。但是,daicelod-h手性柱价格昂贵,且柱效极为容易降低,而中间反应液杂质多,对手性柱损伤较大,成本太高。为了降低中间产物监控过程中色谱柱耗材的成本,申请人旨在开发一种使用常规c18色谱柱分离分析n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺及其异构体的hplc检测方法。
技术实现要素:
为了降低中间产物反应监控过程中色谱柱耗材的成本,申请人旨在开发一种使用常规c18色谱柱分离分析n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺及其r型异构体的hplc检测方法,以用于盐酸帕洛诺司琼合成工艺的中间产物反应监控。
本发明通过下面的技术方案得以实现:
如下化学结构式所示的n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺及其r型异构体的hplc分析方法,固定相为十八烷基硅烷键合硅胶,流动相为乙腈-水,在含有n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺及其r型异构体的对照品溶液或供试品溶液中添加有效量的异佛尔酮二胺,摇匀后并至少静置30分钟后再注入液相色谱仪分析;所述异佛尔酮二胺为顺反异构体混和物;
优选地,添加异佛尔酮二胺后避光静置。
优选地,所述的hplc分析方法包括如下色谱参数:
色谱柱:十八烷基硅烷键合硅胶(c18)色谱柱;
流动相及洗脱方式:乙腈水溶液等度洗脱,乙腈的体积百分浓度为21-25%;
柱温:28-32℃;检测波长:252-256nm。
优选地,乙腈的体积百分浓度为23%。
优选地,将乙腈和水按比例混合后,由液相色谱单泵洗脱;或将乙腈、水由二元泵按照设定的比例混合洗脱。
优选地,柱温为30℃。
优选地,检测波长为254nm。
优选地,所述色谱柱的规格为长250mm,内径4.6mm,填料粒径5μm。
优选地,色谱柱为zorbaxextend-c18。
本发明的优点:
1、本发明提供的hplc分析方法仅使用普通的c18色谱柱、普通的乙腈-水混合溶剂即可实现对n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺及其r型异构体的有效分离,成本低;2、本发明流动相简单,不需要添加离子对,不需要调节ph,配制简单,而添加了离子对等复杂成分的流动相多数需要临用现配,本发明节省了大量配制流动相的时间;3、本发明分析时间短,10分钟内即可完成s型、r型异构体的有效分离,适用于合成反应监控。
附图说明
图1为n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺(s型异构体)及其r型异构体的化学结构式;
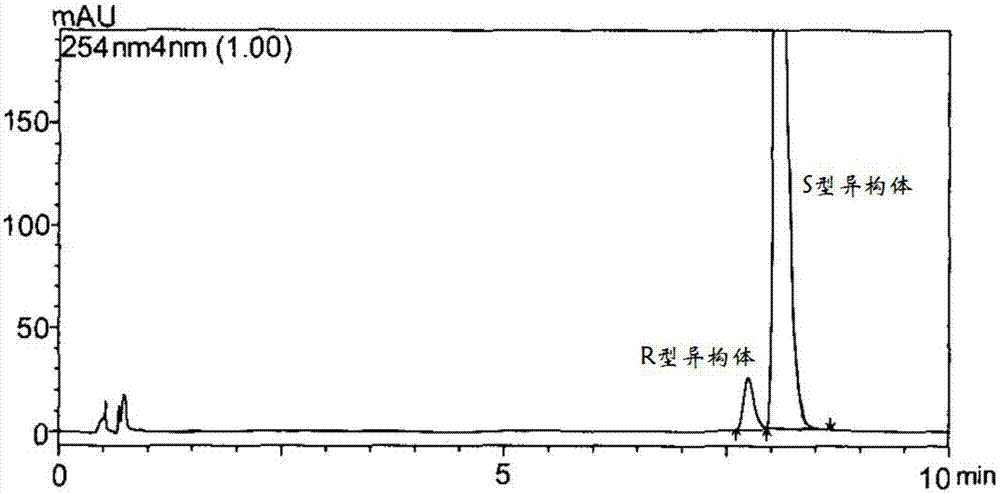
图2为混合对照品溶液使用本发明hplc方法分析结果图;
图3为供试品溶液使用本发明hplc方法分析结果图;
图4为对比试验hplc分析结果图(取s型异构体10mg、r型异构体对照品1mg,精密称定,用不含有异佛尔酮二胺的样品稀释剂溶解并稀释至10ml,摇匀,其他同实施例1)。
具体实施方式
下面结合具体实施例进一步介绍本发明的技术方案。
实施例1n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺及其r型异构体分离
一、实验材料
岛津lc-20a高效液相色谱仪;
cpa225d电子天平(北京赛多利斯仪器系统有限公司);
色谱柱:zorbaxextend-c18柱(安捷伦);
n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺(s型异构体)及其r型异构体自制,化学结构及构型经过确证,化学结构式如图1所示;
异佛尔酮二胺为市售顺反异构体混合物(cas:2855-13-2,以顺反异构体合计的纯度>99%),购于百灵威科技有限公司;
乙腈为色谱纯,水为去离子水,其余试剂均为分析纯。
二、实验方法和结果
1、溶液配制
样品稀释剂:体积百分浓度为20%的乙腈水溶液,其中含有异佛尔酮二胺2mg/ml。
混合对照品溶液:分别称取s型异构体10mg、r型异构体对照品1mg,精密称定,分别加上述样品稀释剂溶解并稀释至10ml,摇匀,静置30分钟后再进样分析。
供试品溶液:取3,4-二氢-1-萘甲胺盐酸盐和3-奎宁环酮盐酸盐为原料缩合还原制备得到n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺的正丁醇溶液【具体步骤为:将3,4-二氢-1-萘甲胺盐酸盐(含量大于99%,35g,0.18mol)、3-奎宁环酮盐酸盐(含量大于99%,29g,0.18mol)和甲苯(300ml)在搅拌下加入三乙胺(45g,0.45mol),加热回流反应4h,减压蒸除溶剂,剩余物中加入正丁醇(200ml),冷却至0℃,分批加入硼氢化钠(7.5g,0.2mol),室温反应4h。减压蒸除正丁醇,剩余物中加入水(200ml),用水饱和的正丁醇(200ml×2)萃取,合并有机相,无水硫酸镁干燥,过滤,得n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺的正丁醇溶液】适量,浓缩至干后用上述样品稀释剂溶解并稀释配制成s型异构体浓度约为1mg/ml的溶液,摇匀,静置30分钟后再进样分析。
2、色谱条件
色谱柱:agilentzorbaxextend-c18色谱柱(250mm×4.6mm,5μm);
流动相及洗脱方式:乙腈水溶液等度洗脱,乙腈的体积百分浓度为23%;
柱温:30℃;
检测波长:254nm;
进样量:20μl。
3、分离度考察
精密量取混合对照品溶液20μl注入液相色谱仪,记录色谱图,色谱图见图2。结果在该色谱条件下s型异构体、r型异构体可较好分离,出峰顺序为r型异构体、s型异构体,分离度大于1.5,分离效果好。
4、线性关系考察
分别精密称取r型异构体、s型异构体,分别配制成标准溶液,s型异构体标准溶液终浓度分别为0.5、0.8、1.0、1.2、1.5mg/ml,r型异构体标准溶液终浓度分别为1、2、5、10、20、40μg/ml。分别精密量取各标准溶液20μl注入液相色谱仪,记录色谱图。以浓度对峰面积作图,r型异构体、s型异构体在上述浓度范围内线性关系良好,r2大于0.9999。
r型异构体、s型异构体的回归曲线基本一致,斜率和截距基本相同,这也符合本领域发展规律,即光学异构体的紫外吸收光谱性质几近相同。因此,在测定供试品溶液中r型异构体的含量时,使用r型异构体的峰面积除以s型异构体的峰面积即可准确知道r型异构体相对于s型异构体的重量百分含量。
5、灵敏度考察
精密称取r型异构体、s型异构体对照品各适量,加样品稀释剂溶解并稀释至峰高约为基线噪音的3倍。r型异构体、s型异构体的最低检出限均约为1.2×10-3μg,灵敏度高。
6、精密度考察
取线性关系考察试验中浓度为1.0mg/ml的s型异构体标准溶液、浓度为20μg/ml的r型异构体标准溶液,精密量取20μl注入液相色谱仪,连续进样5针,记录色谱图。r型异构体、s型异构体峰面积的rsd均小于1%,证明本发明提供的液相分析方法精密度良好。
7、溶液稳定性考察
精密称取r型异构体、s型异构体各适量,加样品稀释剂溶解并稀释成每1ml含1mgs型异构体和20μgr型异构体的溶液,分别于0.5、4.5、8.5、12.5、24.5h进样分析。2个异构体不同时间峰面积的rsd均小于1.5%。结果表明,异构体在样品稀释剂中室温放24.5h稳定。
8、加样回收率
r型异构体、s型异构体的平均回收率分别为99.8%(rsd=1.3%)、100.1%(rsd=0.6%)。结果表明,本发明分析方法回收率良好。
9、供试品溶液中异构体含量测定
精密量取混合对照品溶液、供试品溶液20μl注入液相色谱仪,记录色谱图。供试品溶液色谱图中如有与r型异构体保留时间相同的杂质峰,按峰面积归一化法计算r型异构体的含量。供试品溶液色谱图见图3。
3批样品中检出r异构体分别为s型异构体重量的1.67%、1.59%、1.63%。
实施例2对比实施例,样品稀释剂中不添加异佛尔酮二胺
一、实验材料
岛津lc-20a高效液相色谱仪;
cpa225d电子天平(北京赛多利斯仪器系统有限公司);
色谱柱:zorbaxextend-c18柱(安捷伦);
n-[(3,4-二氢萘-1-基)甲基]-(s)-1-氮杂二环[2.2.2]辛烷-3-胺(s型异构体)及其r型异构体自制,化学结构及构型经过确证,化学结构式如图1所示;
乙腈为色谱纯,水为去离子水,其余试剂均为分析纯。
二、实验方法和结果
1、溶液配制
样品稀释剂:体积百分浓度为20%的乙腈水溶液。
混合对照品溶液:分别称取s型异构体10mg、r型异构体对照品1mg,精密称定,分别加上述样品稀释剂溶解并稀释至10ml,摇匀。
2、色谱条件
色谱柱:agilentzorbaxextend-c18色谱柱(250mm×4.6mm,5μm);
流动相及洗脱方式:乙腈水溶液等度洗脱,乙腈的体积百分浓度为23%;
柱温:30℃;
检测波长:254nm;
进样量:20μl。
3、分离度考察
精密量取混合对照品溶液20μl注入液相色谱仪,记录色谱图,色谱图见图4。结果在该色谱条件下s型异构体、r型异构体共洗脱,10分钟内无法实现有效分离。
- 还没有人留言评论。精彩留言会获得点赞!