用于流体分析的盒和分析仪的制作方法
本发明的实施例一般地涉及半导体技术领域,更具体地,涉及用于流体分析的盒和分析仪。
背景技术:
生物传感器是用于感测和检测生物分子并基于电子、电化学、光学和机械检测原理操作的器件。包括晶体管的生物传感器是电感测生物实体或生物分子的电荷、光子或机械性能的传感器。通过检测生物实体或生物分子自身或通过特定反应物和生物实体/生物分子之间的相互作用和反应来来实施检测。这样的生物传感器可以使用半导体工艺进行制造,可以很快地转换电信号,以及可以容易地应用至集成电路(ic)和mems。
生物样本本身和生物传感器的相互作用可能是一个挑战。通常,将包括生物样本的流体直接吸移至生物传感器的感测部分上方。该方法导致流体样本的大部分无法使用,并且手动加载每个感测区是耗时的。
技术实现要素:
根据本发明的一方面,提供了一种流体盒,包括:衬底,包括多个接触焊盘,配置为与分析仪电连接,半导体芯片,具有传感器阵列,以及参考电极;第一流体沟道,具有第一入口,并且连接至第二流体沟道,对准所述第二流体沟道使得所述传感器阵列和所述参考电极设置在所述第二流体沟道内;样本入口,用于将样本放置在所述第一流体沟道或所述第二流体沟道的路径内;第一插塞,设置在所述第一入口处并且包括配置为被毛细管穿过而不会使流体通过所述第一插塞泄漏的柔性材料。
根据本发明的另一方面,提供了一种流体盒,包括:第一流体沟道,具有第一入口,并且连接至第二流体沟道,对准所述第二流体沟道使得传感器阵列和参考电极设置在所述第二流体沟道内;样本入口,用于将样本放置在所述第一流体沟道或所述第二流体沟道的路径内;第一插塞,设置在所述第一入口处并且包括配置为被毛细管穿过而不会使流体通过所述第一插塞泄漏的柔性材料,其中,所述毛细管连接至分析仪,并且当所述流体盒与所述分析仪物理接触时,所述毛细管穿过所述第一插塞。
根据本发明的又一方面,提供了一种分析仪,配置为与流体盒连接,所述分析仪包括:注射器,布置成使得当所述流体盒物理连接至所述分析仪时,所述注射器的针与所述流体盒的对应输入端口对准;致动器,配置为控制所述注射器的操作;感测模块,配置为当所述流体盒物理连接至所述分析仪时,经由多个导电焊盘向所述流体盒发送信号并从所述流体盒接收信号,其中,所述多个导电焊盘接触所述流体盒上的对应的多个导电焊盘;以及处理器,电连接至所述感测模块,并且配置为基于从所述流体盒接收的信号来确定来自所述流体盒中的样本的给定分析物的浓度水平。
附图说明
当结合附图进行阅读时,从以下详细描述可最佳地理解本发明的各个方面。应该注意,根据工业中的标准实践,各个部件未按比例绘制。实际上,为了清楚的讨论,各种部件的尺寸可以被任意增大或减小。
图1示出示例性生物感测盒的组件的图。
图2是示例性双栅背侧感测fet传感器的截面图。
图3是在示例性可寻址阵列中配置的多个fet传感器的电路图。
图4是双栅fet传感器和加热器的示例性可寻址阵列的电路图。
图5是配置为ph传感器的示例性双栅背侧感测fet传感器的截面图。
图6a示出离子与受体层结合的实例。
图6b示出在基于ph的示例性fet传感器中的阈值电压的变化。
图7是示例性生物传感器芯片的平面图。
图8示出用于将示例性生物传感器芯片安装至处理(handle)层的制造工艺的一系列截面图。
图9是具有安装至衬底的示例性生物传感器芯片的手柄层的顶视图。
图10是具有集成的生物传感器芯片的示例性流体盒的示意图。
图11是在示例性流体盒中的一些流体沟道的示意图。
图12是连接至分析仪的示例性流体盒的示意图。
图13是使用流体盒的示例性方法的流程图。
图14是检测dna的示例性双栅背侧感测生物fet的截面图。
图15a示出受体表面上的dna的结合力。
图15b示出基于配对的分析物结合的示例性双栅背侧感测生物fet的阈值电压的变化。
图16是具有固定在其感测层上的抗体的示例性双栅背侧感测生物fet的截面图。
图17示出受体表面上的抗原和抗体的结合力。
图18是根据本公开的一个或多个方面的制造biofet器件的方法2100的实施例的流程图。
具体实施方式
以下公开内容提供了许多用于实现所提供主题的不同特征的不同实施例或实例。下面描述了组件和布置的具体实例以简化本发明。当然,这些仅仅是实例,而不旨在限制本发明。例如,在以下描述中,在第二部件上方或者上形成第一部件可以包括第一部件和第二部件以直接接触的方式形成的实施例,并且也可以包括在第一部件和第二部件之间可以形成和/或设置附加的部件,从而使得第一部件和第二部件可以不直接接触的实施例。此外,本发明可在各个实例中重复参考标号和/或字符。该重复本身不指示所讨论的各个实施例和/或配置之间的关系。
而且,为了便于描述,在此可以使用诸如“在…下方”、“在…下面”、“下部”、“在…之上”、“上部”等空间相对术语以描述如图所示的一个元件或部件与另一个(或另一些)元件或部件的关系。除了图中所示的方位外,空间相对术语旨在包括器件在使用或操作中的不同方位。装置可以以其他方式定向(旋转90度或在其他方位上),并且在此使用的空间相对描述符可以同样地作出相应的解释。
术语
除非另有规定,本文中使用的所有技术和科学术语具有如本发明所属领域的普通技术人员通常理解的相同的含义。与本文所描述的那些类似或等同的任何方法和材料根据本发明的实施例可以应用于实践或测试中;现在描述方法、器件和材料。本文中所提及的所有专利和出版物结合于此作为参考,从而用于描述和公开在与本发明结合使用的出版物中报道的材料和方法。
本文所用的首字母缩写“fet”是指场效应晶体管。一种非常常见的fet类型是指金属氧化物半导体场效应晶体管(mosfet)。历史上,mosfet已经是在诸如半导体晶圆的衬底的平坦表面中和上创建的平面结构。但是半导体制造的最新进展已经导致三维鳍式mosfet结构。
术语“生物fet”是指包括固定的捕获试剂层的fet,该捕获试剂层用作表面受体以检测生物源的目标分析物的存在。根据实施例,生物fet是具有半导体变换器的场效应传感器。生物fet的一个优势是具有无标记操作的前景。特别地,生物fet使得能够避免诸如利用例如荧光或放射性探针标记分析物的昂贵且费时的标记操作。本文描述的一种特定类型的生物fet是双栅背侧感测生物fet。由生物fet检测的分析物通常是生物源诸如但不限于蛋白质、碳水化合物、脂质、组织碎片或它们的部分。然而,在更一般的意义上,生物fet是更广泛的fet传感器种类的部分,其还可以检测任何化学化合物(本领域中称为化学fet)或包括诸如质子或金属离子的离子的任何其他元素(在本领域中称为isfet)。本发明意在适用于所有类型的基于fet的传感器(“fet传感器”)。本文的一种特定类型的fet传感器是双栅背侧感测fet传感器(“dgbssfet传感器”)。
“s/d”是指形成fet四个端子中的两个端子的源极/漏极结。
表述“高k”是指高介电常数。在半导体器件结构和制造工艺的领域中,高k是指大于sio2的介电常数(即,大于3.9)的介电常数。
术语“分析”通常是指涉及物理、化学、生物化学或生物分析的包括但不限于表征、测试、测量、优化、分离、合成、添加、过滤、溶解或混合的工艺或步骤。
术语“测定(assay)”通常是指涉及化学物质或目标分析物的分析的的工艺或步骤,并且包括但不限于基于细胞的测定、生物化学测定、高通量测定和筛选、诊断测定、ph确定、核酸杂交测定、聚合酶活性测定、核酸和蛋白测序、免疫测定(例如,抗体-抗原结合测定、elisa和iqpcr)、用于检测基因甲基化模式的亚硫酸氢盐甲基化测定、蛋白质测定、蛋白质结合测定(例如蛋白质-蛋白质、蛋白-核酸和蛋白-配体结合测定)、酶测定、偶联酶测定、动力学测量(例如,蛋白质折叠动力学和酶反应动力学)、酶抑制剂和活化剂筛选、化学发光和电化学发光测定、荧光测定、荧光偏振和各向异性测定、吸光度和比色测定(例如,bradford测定、lowry测定、hartree-lowry测定、biuret测定和bca测定),化学测定(例如,用于检测环境污染物和致污物、纳米颗粒或聚合物)和药物发现测定。本文描述的装置、系统和方法可以使用或采用将与fet传感器描述的任何设计一起使用的这些测定中的一种或多种。
术语“液体活检”通常是指与受试者的组织样本相比,从受试者的体液中获得的活检样本。与使用组织样本相比,通常更期望有能力使用体液样本实施测定。使用体液样本的微创方法在患者福利、进行纵向疾病监测的能力以及甚至当在组织细胞不易于接近的情况下(例如在前列腺中)获得表达谱的能力的方面具有广泛的意义。用于检测液体活检样本中的目标分析物的测定包括但不限于上述那些。作为非限制性实例,可以对液体活检样本进行循环肿瘤细胞(ctc)测定。
例如,固定在fet传感器上的捕获试剂(例如,抗体)可以用于使用ctc测定来检测液体活检样本中的目标分析物(例如,肿瘤细胞标记物)。ctc是从肿瘤流入脉管系统并在例如血液中循环的细胞。通常,ctc以非常低的浓度存在于血液循环中。为了测定ctc,通过本领域已知的各种技术从患者血液或血浆中富集ctc。可以使用本领域已知的方法对ctc进行染色以用于特定标记,所述方法包括但不限于基于细胞计数(例如,流式细胞仪)的方法和基于ihc的方法。对于本文所述的装置、系统和方法,可以使用捕获试剂捕获或检测ctc,或者可以将来自ctc的核酸、蛋白质或其他细胞环境作为目标分析物的目标,从而用于结合捕获试剂或通过捕获试剂检测。
当在ctc上或从ctc中检测到目标分析物时,例如,表达或包括ctc的目标分析物的增加可能有助于将受试者鉴定为具有可能对特定治疗做出反应的癌症(例如,与目标分析物相关的癌症)或允许优化具有例如针对目标分析物的抗体的治疗方案。ctc测量和定量可以提供关于例如肿瘤的阶段、对治疗的反应、疾病进展或它们的组合的信息。从检测ctc的目标分析物获得的信息可以用作例如预诊断的、预测的或药效动力学的生物标记物。此外,用于液体活检样本的ctc测定可以单独使用或与固体活检样本的附加的肿瘤标记物分析结合使用。
术语“鉴定”通常是指基于目标分析物与其特征(identity)已知的捕获试剂的结合来确定目标分析物的特征的过程。
术语“测量”通常是指基于目标分析物与捕获试剂的结合来确定目标分析物的量、数量、质量或性质的过程。
术语“定量”通常是指基于目标分析物与捕获试剂的结合来确定目标分析物的数量或浓度的过程。
术语“检测”通常是指基于目标分析物与捕获试剂的结合来确定目标分析物的存在或不存在的过程。检测包括但不限于鉴定、测量和定量。
术语“化学”是指物质、化合物、混合物、溶液、乳液、分散剂、分子、离子、二聚体、诸如聚合物或蛋白质的大分子、生物分子、沉淀物、晶体、化学组成部分或基团、颗粒、纳米颗粒、试剂、反应产物、溶剂或流体,其中的任何一种可以固态、液态或气态状态存在,并且通常是分析对象。
术语“反应”是指涉及至少一种化学物质,并且通常涉及(在化学、生物化学和生物转化的情况下)破坏或形成一种或多种键的物理、化学、生物化学或生物转化,诸如共价键、非共价键、范德华键、氢键或离子键。该术语包括典型的化学反应,诸如合成反应、中和反应、分解反应、置换反应、还原-氧化反应、沉淀、结晶、燃烧反应和聚合反应,以及共价和非共价结合、相变、颜色变化、相形成、结晶、溶解、发光、光吸收或发射性质的变化、温度变化或热吸收或发射、构象变化(conformationalchange)以及诸如蛋白质的大分子的折叠或解折叠。
本文所用的“捕获试剂”是能够结合目标分析物或目标试剂的分子或化合物,其可直接或间接地附接到基本固体的材料。捕获试剂可以是化学物质,具体地是天然存在的目标分析物(例如,抗体、多肽、dna、rna、细胞、病毒等)或可以制备目标分析物的任何物质,并且捕获试剂在测定中可以结合一种或多种目标分析物。
本文所用的“目标分析物”是在测试样本中要使用本发明检测的物质。目标分析物可以是化学物质,具体地是天然存在的捕获试剂(例如抗体、多肽、dna、rna、细胞、病毒等)或可以制备捕获试剂的任何物质,并且目标分析物在测定中可以结合一种或多种捕获试剂。“目标分析物”还包括任何抗原物质、抗体和它们的组合。目标分析物可以包括蛋白质、肽、氨基酸、碳水化合物、激素、类固醇、维生素,包括用于治疗目的而管理的那些药物以及用于非法目的而管理的那些药物、细菌、病毒、以及任何上述物质的代谢物或抗体。
本文所用的“测试样本”是指使用本发明检测和测定的包括目标分析物的组合物、溶液、物质、气体或液体。测试样本可以包括除了目标分析物之外的其他组分,其可以具有液体或气体的物理属性,并且可以是任何尺寸或体积,包括例如液体或气体的移动流。只要其他物质不干扰目标分析物与捕获试剂的结合或第一结合成分(member)与第二结合成分的特异性结合,则测试样本可以包括除目标分析物以外的任何物质。测试样本的实例包括但不限于天然存在和非天然存在的样本或它们的组合。天然存在的测试样本可以是合成物或合成的。天然存在的测试样本包括从受试者体内或体上的任何位置分离的身体液或体液,包括但不限于血液、血浆、血清、尿液、唾液或痰液、脊髓液、脑脊液、胸膜液、乳头吸入液、淋巴液、呼吸道、肠道和泌尿生殖道液、泪液、唾液、母乳、淋巴系统液、精液、脑脊液、器官内系统液、腹水、肿瘤囊肿液、羊水和它们的组合,以及诸如地下废水或废水、土壤提取物、空气和农药残留物的环境样本或食品相关的样本。
检测到的物质可以包括例如核酸(包括dna和rna)、激素、不同的病原体(包括引起其宿主疾病或病的生物试剂,诸如病毒(例如h7n9或hiv)、原生动物(例如,导致疟原虫的疟疾)或细菌(例如大肠杆菌或结核分枝杆菌))、蛋白质、抗体、各种药物或治疗剂、或包括氢或其他离子的其他化学或生物物质、非离子分子或化合物、多糖、诸如化学组合库成分(member)等的小化学化合物等。检测或确定的参数可以包括但不限于例如ph变化、乳糖变化、浓度变化、每单位时间内的颗粒和其他参数,其中,流体在一段时间内在器件上方流动以检测颗粒,例如稀疏的颗粒。
如本文所用的,相对于例如捕获试剂使用的术语“固定”包括将分子层级的捕获试剂大致附接至表面。例如,可以使用包括非共价相互作用(例如,静电力、范德华力和疏水界面的脱水)的吸附技术以及共价键合技术将捕获试剂固定到衬底材料的表面,其中官能团或接头(linker)有助于将捕获试剂附接至表面。可以基于衬底表面的性质、携带捕获试剂的介质和捕获试剂的性质将捕获试剂固定至衬底材料的表面。在一些情况下,可以首先改变(modify)衬底表面以具有与表面接合的官能团。然后官能团可以结合生物分子或生物或化学物质以将它们固定在其上。
术语“核酸”通常是指通过磷酸二酯键彼此连接的一组核苷酸,并且是指天然存在的核酸,其中,自然界存在的天然存在的核苷酸连接至该核酸,该核酸可以是诸如dna和/或rna,其中,dna包括具有彼此连接的腺嘌呤、鸟嘌呤、胞嘧啶和胸腺嘧啶中的任何一种的脱氧核糖核苷酸和/或rna包括具有彼此连接的腺嘌呤、鸟嘌呤、胞嘧啶和尿嘧啶的任何一种的核糖核苷酸。此外,非天然存在的核苷酸和非天然存在的核酸在本发明的核酸的范围内。实例包括肽核酸(pna)、具有磷酸基团的肽核酸(phona)、桥连核酸/锁定核酸(bna/lna)和吗啉代核酸。另一实例包括化学改变的核酸和核酸类似物,诸如甲基膦酸酯dna/rna、硫代磷酸酯dna/rna、氨基磷酸酯dna/rna和2'-o-甲基dna/rna。核酸包括可以改变的那些。例如,可以根据需要标记核酸中的磷酸基团、糖和/或碱基。本领域已知的用于核酸标记的任何物质都可用于标记。其实例包括但不限于放射性同位素(例如,32p、3h和14c)、dig、生物素、荧光染料(例如fitc、texas、cy3、cy5、cy7、fam、hex、vic、joe、rox、tet、bodipy493、nbd和tamra)和发光物质(例如,吖啶酯)。
本文所用的适配体是指结合至特定目标分子的低聚核酸或肽分子。最初在1990年(ellington和szostak1990,1992;tuerk和gold1990)公开了使用单链核酸(适配体)作为亲和分子以用于蛋白质结合的概念,并且在目标存在的情况下,该适配体基于短序列的能力折叠成为与具有高亲和力和特异性的目标结合的独特的三维结构。eugenew.mng等人在2006年公开了适配体是选择用于高亲和力结合至分子目标的寡核苷酸配体。
本文所用的术语“抗体”是指能够非共价、可逆地且以特定方式结合对应的抗原的免疫球蛋白家族的多肽。例如,天然存在的igg抗体是包括通过二硫键相互连接的至少两个重(h)链和两个轻(l)链的四聚体。每个重链由重链可变区(本文缩写为vh)和重链恒定区组成。重链恒定区由三个域ch1、ch2和ch3组成。每个轻链由轻链可变区(本文缩写为vl)和轻链恒定区组成。轻链恒定区由一个域cl组成。vh和vl区可以进一步细分为随着更保守的区域(称为框架区(fr))散布的超可变区(称为互补性决定区(cdr))。每个vh和vl以以下顺序由从氨基末端至羧基末端排列的三个cdr和四个fr组成:fr1、cdr1、fr2、cdr2、fr3、cdr3和fr4。三个cdr构成可变域的约15-20%。重链和轻链的可变区包括与抗原相互作用的结合域。抗体的恒定区可以调节免疫球蛋白与宿主组织或因子(包括免疫系统的各种细胞(例如效应细胞))和典型的补充系统的第一组分(c1q)的结合(kuby,immunology,4thed.,chapter4.w.h.freeman&co.,newyork,2000)。
术语“抗体”包括但不限于单克隆抗体、人抗体、人源化抗体、嵌合抗体和抗独特型(抗-id)抗体(包括例如针对本发明抗体的抗-id抗体)。抗体可以是任何同种型/类(例如igg、ige、igm、igd、iga和igy)或亚类(例如,igg1、igg2、igg3、igg4、iga1和iga2)。
术语“聚合物”是指由两个或多个彼此重复连接的合成砌块(buildingblocks)(“mers”)组成的任何物质或化合物。例如,“二聚体”是其中两个合成砌块已经结合在一起的化合物。聚合物包括缩聚物和加聚物两者。缩聚物的典型实例包括聚酰胺、聚酯、蛋白质、羊毛、丝绸、聚氨酯、纤维素和聚硅氧烷。加聚物的实例是聚乙烯、聚异丁烯、聚丙烯腈、聚(氯乙烯)和聚苯乙烯。其他实例包括诸如导电或光折射聚合物的具有增强的电学或光学特性(例如非线性光学特性)的聚合物。聚合物包括直链和支链聚合物两者。
生物感测盒概述
图1示出集成在一起以形成示例性生物感测盒102的各个组件的概述。生物感测盒102可以包括多个流体沟道,其配置为控制流体朝向和远离可以检测到目标分析物存在的感测位置的流动。
在该示例性实施例中,生物感测盒102包括fet传感器104的阵列。fet传感器104构成生物感测盒102的传感器组件。fet传感器104可以布置成阵列并进行单独寻址以检测fet传感器感测层的表面处的结合事件。在一个实施例中,fet传感器104包括双栅背侧fet传感器。在可选实施例中,可以使用其他类型的基于fet传感器的传感器。
生物感测盒102包括生物界面106。生物界面106可以连接至双栅背侧感测fet传感器104,以便于在双栅背侧感测fet传感器104的表面处进行可以被检测到的结合反应。各种类型的生物分子可以形成诸如dna或rna适配体和抗体(仅举几个实例)的生物界面106的部分。将在本文中详细讨论有关生物界面及其相关的化学和生物力的更多细节。
生物感测盒102包括各个级别(level)的芯片封装件108,以将双栅背侧感测fet传感器芯片集成到流体环境中。生物感测盒102还包括具有微流体沟道的流体组件110,以用于管理向fet传感器104输送液体。流体组件110还包括流体入口,以用于与从生物感测盒102的外部输送的流体连接。
生物感测盒102中的各个组件的集成产生了可用于许多各个生物感测应用的紧凑且便携的平台。使用具有集成流体组件的fet传感器可以在使用低样本体积时产生精确的结果。此外,生物感测盒102可以配置为通过分析仪以完全自主的方式操作,然后在使用后进行处置。
本文的描述分为四个主要部分,以更详细地描述生物感测盒102的组件。第一部分将描述双栅背侧生物fet传感器104的布置和制造。第二部分将描述封装工艺。第三部分将描述流体组件110,并进一步描述生物感测盒102和分析仪之间的相互作用。最后一部分将提供使用双栅背侧fet传感器104的关于生物学和各个生物感测应用的细节。
双栅背侧fet传感器
双栅背侧fet传感器利用半导体制造技术和生物捕获试剂形成灵敏且易于排列的传感器。虽然传统的mosfet具有连接至单个电节点的单个栅电极,但是双栅背侧感测fet传感器具有两个栅电极,每个栅电极连接至不同的电节点。两个栅电极中的第一个在本文中称为前侧栅极,并且两个栅电极中的第二个在本文中称为后侧栅极。前侧栅极和后侧栅极两者配置为使得在操作中每个可以充电和/或放电,并且从而每个都影响双栅背侧感测fet传感器的源极/漏极端之间的电场。前侧栅极是导电的,其通过前侧栅极电介质与沟道区分离,并且配置为由与其连接的电路进行充电和放电。背侧栅极通常通过背侧栅极电介质与沟道区分离,并且包括设置在背侧栅极电介质上的生物功能化感测层。背侧栅极上的电荷量为是否发生生物识别反应的函数。在双栅背侧感测fet传感器的典型操作中,将前侧栅极充电至预定的电压范围内的电压。前侧栅极的电压决定了fet传感器的沟道区的对应电导率。背侧栅极上的电荷的相对少量的变化改变了沟道区的电导率。电导率的这种变化表明生物识别反应。
fet传感器的一个优势是具有无标记操作的前景。特别地,fet传感器使得能够避免诸如用例如荧光或放射性探针标记分析物的昂贵且费时的标记操作。
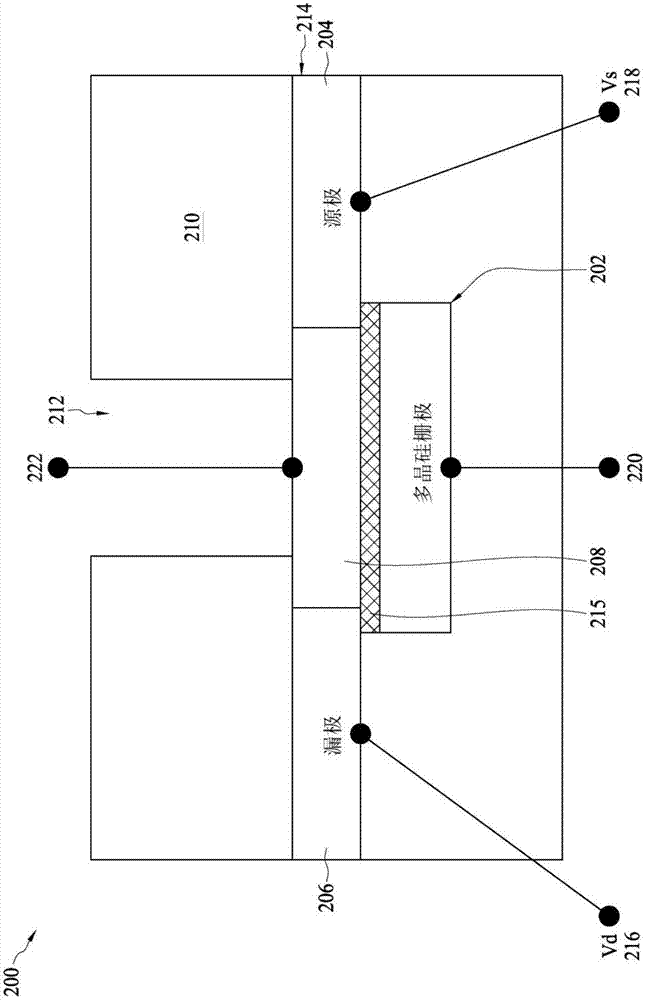
参考图2,示出示例性双栅背侧感测fet传感器200。双栅背侧感测fet传感器200包括形成在衬底214上方的控制栅极202,并通过设置在衬底214上的中间电介质215与衬底214分离。衬底214还包括源极区204、漏极区206以及位于源极区204和漏极区206之间的沟道区208。在实施例中,衬底214具有介于约100nm和约130nm之间的厚度。可以使用合适的cmos工艺技术形成栅极202、源极区204、漏极区206和沟道区208。栅极202、源极区204、漏极区206和沟道区208形成fet。在衬底214的与栅极202相对的一侧上设置隔离层210。在一个实施例中,隔离层210具有约1μm的厚度。在本发明中,其上设置有栅极202的衬底214的一侧称为衬底214的“前侧”。类似地,在其上设置有隔离层210的衬底214的一侧称为“背侧”。
在隔离层210中提供开口212。开口212可以与栅极202大致对准。在其他实施例中,开口212大于栅极202,并且可以在多个双栅背侧感测fet传感器的上方延伸。可以在位于沟道区208的表面上的开口212中设置界面层(未示出)。可操作界面层以提供用于定位和固定一个或多个受体的界面,从而用于检测生物分子或生物实体。本文提供了关于界面层的更多细节。
双栅背侧感测fet传感器200包括至漏极区206(vd216)、源极区204(vs218)、栅极结构202(前侧栅极220)和/或有源区208(例如,背侧栅极222)的电接触件。应当注意,背侧栅极222不需要物理接触衬底214或衬底214上方的任何界面层。因此,虽然传统的fet使用栅极接触件来控制源极和漏极之间(例如,沟道)的半导体的电导,但是双栅背侧感测fet传感器200允许形成在fet器件的相对侧上的受体来控制电导,而栅极结构202提供另一栅极来控制电导。因此,双栅背侧感测fet传感器200可用于检测周围环境中和/或开口212中的一个或多个特定的生物分子或生物实体,如本文中使用的各个实施例更详细地讨论的。
双栅背侧感测fet传感器200可以连接至附加的无源组件,诸如电阻器、电容器、电感器和/或熔丝之类;和其他有源组件,包括p沟道场效应晶体管(pfet)、n沟道场效应晶体管(nfet)、金属氧化物半导体场效应晶体管(mosfet)、高压晶体管和/或高频晶体管;其他合适的组件;和/或它们的组合。还应理解,对于双栅背侧感测fet传感器200的附加的实施例,可以在双栅背侧感测fet传感器200中添加附加的部件,并且可以替换或去除所描述的一些部件。共同拥有的公开号为第2013/0200438号的美国专利申请和公开号为第2014/0252421号美国专利申请可以找到关于双栅背侧感测fet传感器200的示例性制造程序的更多细节。
图18是根据本公开的一个或多个方面的制造biofet器件的方法2100的实施例的流程图。方法2100开始于框2102,其中提供衬底。衬底可以是半导体衬底(例如,晶圆)。半导体衬底可以是硅衬底。可选地,衬底可以包括其他元素半导体,例如锗;包括碳化硅、砷化镓、磷化镓、磷化铟、砷化铟和/或锑化铟的化合物半导体;包括sige,gaasp,alinas,algaas,gainas,gainp和/或gainasp的合金半导体;或其组合。在一个实施例中,衬底是绝缘体上半导体(soi)衬底。soi衬底可以包括通过诸如通过注氧隔离(simox)的工艺形成的掩埋氧化物(box)层和/或其它合适的工艺。衬底可以包括掺杂区域,例如p阱和n阱。
方法2100然后进行到框2104,其中场效应晶体管(fet)形成在衬底上。fet可以包括栅极结构,源极区域、漏极区域和插入源极区域和漏极区域的沟道区域。源极、漏极和/或沟道区可以形成在半导体衬底的有源区上。fet可以是n型fet(nfet)或p型fet(pfet)。例如,源极/漏极区域可以包括取决于fet配置的n型掺杂剂或p型掺杂剂。栅极结构可以包括栅极介电层,栅极电极层和/或其它合适的层。在一个实施例中,栅电极是多晶硅。其他示例性的栅电极包括金属栅电极,其包括诸如cu、w、ti、ta、cr、pt、ag、au等材料;合适的金属化合物如tin、tan、nisi、cosi;其组合;和/或其它合适的导电材料。在一个实施例中,栅极电介质是氧化硅。其它示例性栅极电介质包括氮化硅,氮氧化硅,具有高介电常数(高k)的电介质,和/或其组合。
方法2100然后进行到框2106,其中在衬底的背面形成开口。开口可以包括形成在包括fet器件的衬底背面上的一个或多个层中的沟槽。开口可以暴露栅极和体结构下方的区域(例如,邻近fet的沟道)。在一个实施例中,开口暴露fet器件的栅极和有源/沟道区下面的有源区(例如,硅有源区)。可以使用合适的光刻工艺形成开口,以在衬底上提供图案和蚀刻工艺以从背面去除材料,直到fet器件的体结构暴露。蚀刻工艺包括湿式蚀刻,干蚀刻,等离子体蚀刻和/或其它合适的工艺。
然后,方法2100进行到框2108,其中在开口中形成界面层。界面层可以形成在fet的栅极结构下面的暴露的有源区上。界面层可以与生物分子或生物实体结合相容(例如,友好的)。例如,界面层可为生物分子或生物实体提供结合界面。界面层可以包括介电材料,导电材料和/或用于保持受体的其它合适的材料。示例性界面材料包括高k电介质膜、金属、金属氧化物、电介质和/或其它合适的材料。作为另一示例,示例性界面材料包括hfo2、ta2o5、pt、au、w、ti、al、cu、这些金属的氧化物、sio2、si3n4、al2o3、tio2、tin、sno、sno2、srtio3、zro2、la2o3;和/或其它合适的材料。可以使用例如物理气相沉积(pvd)(溅射)、化学气相沉积(cvd)、等离子体增强化学气相沉积(pecvd)、大气压化学气相沉积(apcvd))等cmos工艺形成界面层。低压cvd(lpcvd)、高密度等离子体cvd(hdpcvd)或原子层沉积(ald)。在实施例中,界面层包括多个层。
方法2100然后进行到框2110,其中受体例如酶、抗体、配体、肽、核苷酸、器官细胞、生物体或组织片段被放置在界面层上以用于检测目标生物分子。
参考图3,示出连接至位线306和字线308的fet传感器304的示例性可寻址阵列300的示意图。应当注意,术语位线和字线在本文中用于指示与存储器件中的阵列结构的类似物,然而,并不表明存储器件或存储阵列必须包括在阵列中。可寻址阵列300可具有在诸如动态随机存取存储器(dram)阵列的其他半导体器件中所采用的具有类似物。例如,上文参考图2描述的双栅背侧感测fet传感器200可以形成在电容器存在于dram阵列中的位置处。示意图300仅是示例性的,并且可以意识到其他配置是可能的。
fet传感器304均大致类似于双栅背侧感测fet传感器200。fet302配置为提供介于fet传感器304的漏极端子和位线306之间的连接。以这种方式,fet302类似于dram阵列中的存取晶体管。在该示例性实施例中,fet传感器304是双栅背侧感测fet传感器,并且包括:感测栅极,由设置在fet有源区上方的介电层上的受体材料提供,该fet有源区设置在反应位置处;和控制栅极,由设置在fet有源区上方的介电层上的栅电极(例如,多晶硅)提供。
示意图300示出阵列形成,该阵列可能有利于检测由引入到fet传感器304的最小生物分子或生物实体所提供的小信号变化。使用位线306和字线308的阵列格式允许减少输入/输出焊盘的数量。可以使用放大器来增强信号强度,以提高具有示意图300的电路布置的器件的检测能力。在实施例中,当置位特定字线308和位线306时,对应的存取晶体管302将导通(例如,像开关)。当相关的fet传感器304的栅极(例如,诸如双栅背侧感测fet传感器200的背侧栅极222)具有由生物分子的存在而影响的电荷时,fet传感器304将传递电子并诱导器件的场效应充电,从而调制电流(例如ids)。电流(例如,ids)或阈值电压(vt)的变化可用于指示相关生物分子或生物实体的检测。因此,具有示意图300的器件可以实现生物传感器应用,包括具有差分感测的应用,从而用于提高灵敏度。
参考图4,呈现示例性布局400。示例性布局400包括配置为单独可寻址像素402的阵列401的访问晶体管302和fet传感器304。阵列401可以包括任何数量的像素402。例如,阵列401可以包括128×128像素。其他布置可以包括256×256像素或诸如128×256像素的非矩形阵列。
每个像素402包括:存取晶体管302和双栅背侧感测fet传感器304;以及其他组件,可包括一个或多个加热器408和温度传感器410。在该实例中,存取晶体管302是n沟道fet。n沟道fet412还可以用作温度传感器410的存取晶体管。在该示例性实例中,尽管这不是必需的,但是fet302和412的栅极共同连接。可以使用列解码器404和行解码器406来单独寻址每个像素402(以及其相关的组分)。在一个实例中,每个像素402具有约10微米×约10微米的尺寸。在另一实例中,每个像素402具有约5微米×约5微米的尺寸,或具有约2微米×约2微米的尺寸。
列解码器406和行解码器404可用于确定n沟道fet302和412的导通/截止(on/off)状态。导通n沟道fet302向双栅背侧感测fet传感器304的s/d区提供电流。当导通这些器件时,电流ids流过fet传感器304,并且可以测量该电流ids。
加热器408可以用于局部地增加双栅背侧感测fet传感器304周围的温度。可以使用诸如形成具有穿过其中的高电流的金属图案的任何已知的技术来构造加热器408。加热器408还可以是热电加热器/冷却器,如peltier器件。可以在特定的生物测试期间(诸如使dna或rna变性,或为特定的生物分子提供更理想的结合环境)使用加热器408。温度传感器410可用于测量双栅背侧感测fet传感器304周围的局部温度。在一个实施例中,可以创建控制回路以使用加热器408控制温度并且从温度传感器410接收反馈。在另一实施例中,加热器408可以是热电加热器/冷却器,该冷却器允许像素402内的组件局部主动冷却。
参考图5,提供了示例性双栅背侧感测fet传感器500的截面图。双栅背侧感测fet传感器500是双栅背侧感测fet传感器200的一个实施方案,因此用图2的元件符号来标记先前描述的图2的元件,并且它们的描述在此不再重复。双栅背侧感测fet传感器500包括栅极202、源极区204、漏极区206和沟道区208,其中源极区204和漏极区206形成在衬底214内。栅极202、源极区204、漏极区206和沟道区208形成fet。应当注意,如相关领域技术人员将理解的那样,图5的各个组件不旨在按比例绘制并且为了视觉上的方便被放大。
在示例性实施例中,双栅背侧感测fet传感器500连接至各个金属互连层502,金属互连层502与形成在衬底214内的各个掺杂区和其他器件形成电连接。可以使用相关领域的技术人员熟知的制造工艺来制造金属互连层502。
双栅背侧fet传感器500可以包括与源极区204和漏极区206分离的主体区504。主体区504可用于偏置介于源极区204和漏极区206之间的有源区208中的载流子浓度。因此,负电压偏置可以施加到主体区504以提高双栅背侧fet传感器500的灵敏度。在一个实施例中,主体区504与源极区204电连接。在另一实施例中,主体区504电接地。
双栅背侧fet传感器500可以连接至在衬底214内制造的附加的电路506。电路506可以包括任何数量的mosfet器件、电阻器、电容器或电感器,以形成辅助操作双栅背侧感测fet传感器500的电路。例如,可以在电路506中形成列解码器406和行解码器404。电路506可以包括任何放大器、模数转换器(adc)、数模转换器(dac)、电压发生器、逻辑电路和dram存储器(仅列举几个实例)。可以在与双栅背侧fet传感器500相同的衬底214中集成附加的电路506的全部或部分组件。应当理解,每个大致类似于双栅背侧fet传感器500的多个fet传感器可以集成到衬底214上并连接至附加的电路506。在另一实例中,在与衬底214分离的另一半导体衬底上提供附加的电路506的全部或部分组件。在又一实例中,在与双栅背侧fet传感器500相同的衬底214中集成附加的电路506的一些组件,并且在与衬底214分离的另一半导体衬底上提供附加的电路506的一些组件。
仍参考图5的示例性实例,双栅背侧感测fet传感器500包括沉积在隔离层210上方和沟道区208上方的开口内的界面层508。在一个实施例中,界面层508具有介于约
现在将描述用作ph传感器的双栅背侧fet传感器500的示例性操作。简而言之,流体栅极510用于提供至双栅背侧感测fet传感器的“第二栅极”的电接触。在双栅背侧感测fet传感器500的反应位置上方提供具有给定ph值的溶液512,并且在溶液512内放置流体栅极510。溶液的ph通常与溶液中的氢离子[h+]的浓度有关。在沟道区208之上的界面层508的表面附近的离子的积聚将影响沟道区208内反型层的形成,该沟道区208在源极区204和漏极区206之间形成导电通路。这可以通过fet传感器的电导率的变化来测量。在一个实施例中,在感测期间,流体栅极510用作晶体管的栅极,而栅极202保持浮置。在另一实施例中,在感测期间,流体栅极510用作晶体管的栅极,而栅极202以给定电压偏置。例如,栅极202可以根据应用以-2v和2v之间的电压偏置,而在一定的电压范围之间扫描流体栅极510。在另一实施例中,在感测期间,流体栅极510以给定电压(或接地)偏置,而栅极202用作晶体管的栅极(例如,其电压扫过一定的电压范围)。流体栅极510可以由铂形成,或者可以由电化学分析中用于参考电极的任何其他通常使用的材料形成。最常见的参考电极是稳定电压值为约0.230v的ag/agcl电极。
图6a示出溶液中结合至界面层508的表面的离子。界面层508的最顶部原子层描述为各种悬空[o-]、[oh]和[oh2+]键。当离子积聚在表面上时,总表面电荷影响晶体管的阈值电压。如本文所用的,阈值电压是在fet传感器的源极和漏极之间形成少数载流子的导电路径所需的介于fet传感器的栅极和源极之间的最小电势。总电荷还直接与溶液的ph值有关,因为较高的正电荷累积表明低ph值,而较高的负电荷累积则表明高ph值。图6b示出由于n沟道fet传感器中不同的ph值导致的阈值电压的变化。从图中可以看出,阈值电压增加59mv大致表明溶液的ph值增加1。换言之,当测量导通晶体管所需的电压时,一个ph变化导致总表面等效电荷为59mv。
芯片封装
参考图7,示出半导体芯片702的示例性平面图。芯片702包括传感器阵列704、可选参考电极706、模拟电路708和i/o焊盘716。芯片702可以是硅、砷化镓或磷化铟(仅举几个实例)。芯片702可具有约3mm×约2.5mm的尺寸。
诸如上文在图2和图5所示,传感器阵列704表示双栅背侧感测fet传感器的阵列。例如,在图4中,该阵列可以布置为如图所示的像素的行-列矩阵。可以用相同或不同的捕获试剂功能化传感器阵列704中的各个fet传感器,以对各个分析物实施生物感测。
可以在包括传感器阵列704的相同芯片702上图案化参考电极706。参考电极706可以沿着x或y方向与传感器阵列704大致对准,使得可以在传感器阵列704和参考电极706两者上方放置流体沟道。在另一实施例中,在芯片702之外的其他地方提供参考电极706。
参考电极706可以包括具有相对稳定电势的任何材料。示例性参考电极材料包括铂或ag/agcl。所描述的在衬底表面上制造ag/agcl电极是本领域公知的,例如通过moschou等人于2015年在《传感器》上第15(8)卷第18102-18113页的文章“利用市售的pcb技术制造的ag/agcl伪参考电极的表面和电学表征”。
模拟电路708可以包括与传感器阵列704的操作有关的电路。因此,模拟电路708可以配置为在与各个i/o焊盘716接口连接的同时向传感器阵列704提供信号并且测量来自该传感器阵列的信号。在一个实施例中,模拟电路708包括串联外围接口(spi)712和传感器阵列电路714。在该实施例中,传感器阵列704和传感器阵列电路714之间的间隔不小于约135微米。
spi712可以是串行接口电路,以促进下面更详细地描述的传感器阵列电路714和分析仪单元之间的数据传输。对于相关领域的技术人员来说,将很好地理解的spi的一般操作。传感器阵列电路714可以包括任何数量的参考电压发生器、运算放大器、低通滤波器、adc和dac,以向传感器阵列704提供信号并且从传感器阵列704接收信号。
在一个实例中,可以使用传感器阵列电路714产生偏置参考电压,以向传感器阵列704中的给定fet传感器或一组fet传感器的主体区提供约-0.24伏特的负偏置电压。当实施感测时,还可以向传感器阵列704中的给定fet传感器或一组fet传感器的流体栅极提供可调电压。
当测量从传感器阵列704中的给定fet传感器或一组fet传感器接收到的信号(例如ids)时,在将所得到的信号输出至i/o焊盘716之前,传感器阵列电路714可以接收测量的信号并将这些信号通过跨阻抗放大器进行传输,即电流-至-电压转换器、接着是一个或多个附加的放大级、低通滤波器和最终的adc。在放大测量信号之前,还可以通过从测量信号中减去背景ac信号来减小测量信号中的噪声。在温度信号输出至i/o焊盘716之前,还可以放大、滤波并通过adc传输温度信号(从传感器阵列704中的一个或多个温度传感器接收到的)。
在各个实施例中,可以沿着芯片702的外围图案化多个i/o焊盘716。可以提供比由芯片702的各个组件所使用的实际的输入和输出更多的i/o焊盘。在一个实施例中,引线接合技术可用于将各个i/o焊盘716连接至与芯片702接合的另一衬底或封装件。在一个特定实施例中,可以围绕芯片702的外围图案化32个i/o焊盘。给定i/o焊盘716的尺寸可以为约80微米×约70微米,并且i/o焊盘716之间的间距可以为约150微米。传感器阵列704和最接近的i/o焊盘716之间的间隔可以不短于约400微米,而i/o焊盘716和芯片702的最外边缘之间的间隔可以不短于约177.5微米。
参考图8,示出芯片702的示例性封装方案。将具有i/o焊盘716的芯片702结合至载体层802。载体层802可以是诸如硅衬底的另一半导体衬底。在另一实例中,载体层802是诸如硬塑料材料的绝缘体。可以使用诸如通过使用焊料或粘合剂的任何已知的接合技术,将芯片702接合至载体层802。
在一个实施例中,载体层802包括填充有导电材料804的多个贯通孔。导电材料804可以是诸如但不限于锡、铜、铝、金或它们的任何合金的任何金属。导电材料804可以包括位于载体层802的底面805处的焊料凸块或焊球。焊料可以延伸超出表面805。
根据实施例,芯片封装件还包括邻接芯片702的侧面的第一绝缘层806。第一绝缘层806还可以是填充芯片702周围区域的塑料材料或树脂,并且可以帮助将芯片702固定在合适的位置处。在示例性实施例中,第一绝缘层806包括还填充有导电插塞808的贯通孔。导电插塞808可以是与导电材料804相同的材料。导电插塞808在导电材料804的对应区域上方大致对准,从而使得在导电插塞808和导电材料804之间形成欧姆接触。
一旦已经将芯片702固定至载体层802,并且在其周围具有第一绝缘层806,则可以在i/o焊盘716和导电插塞808之间形成电连接812。相关领域的技术人员将理解,可以使用引线接合技术形成电连接812。在另一实例中,使用光刻图案化技术形成电连接812,其中,该光刻图案化技术图案化导电迹线以电连接i/o焊盘716与相应的导电插塞808。一旦形成电连接812,则可以沉积第二绝缘层810以保护电连接812免受环境的损坏。第二绝缘层810可以是与第一绝缘层806相同的材料。第二绝缘层810可以是树脂材料,该树脂材料在电连接812周围流动然后硬化以形成保护壳。在第二绝缘层810内形成开口814,以创建朝向存在于芯片702上的传感器阵列的通路。在芯片702上还图案化参考电极的实施例中,则开口814将创建朝向传感器阵列和参考电极的通路。
最终的芯片封装件816包括结合至载体层802并且电连接至位于载体层802的底面805上的各个导电焊点或金属焊盘的芯片702。还通过第一绝缘层806和第二绝缘层810来保护芯片702免受环境的损坏。芯片封装件816可以更容易地处理并连接至诸如印刷电路板(pcb)的较大的衬底。在一些实施例中,芯片封装件816可以连接至一个或多个散热器,以提供从芯片702进入到周围空气中或进入到芯片封装件816附接的衬底中的更有效的散热路径。在其他实施例中,芯片封装件816可以连接至peltier器件以提供热电加热和/或冷却。
参考图9的说明性实施例,芯片封装件816与衬底902接合。衬底902可以是pcb,该pcb包括导电接触焊盘以制造与载体层802的底面上的焊料或导电焊盘的电接触。可以实施倒装芯片接合技术以将芯片封装件816接合到衬底902的表面上。简而言之,沿着载体层802的底面的焊料或导电焊盘与衬底902上图案化的对应的导电焊盘对准,并且接合在一起以将芯片封装件816物理地附接至衬底902,并且将来自芯片702的i/o焊盘电连接至存在于衬底902上的导电迹线。衬底902上的导电迹线终止于边缘连接件908中。
一个或多个边缘连接件908可以提供至芯片702的电连接。一个或多个其他边缘连接件908可以提供至在衬底902的表面上图案化的参考电极906的电连接。使用参考电极906可以消除在芯片702上提供参考电极的需要。可以使用诸如但不限于铜、金或铝的金属来图案化一个或多个边缘连接件908中的每个。可以使用上文讨论的与用于芯片702上的参考电极706相同的技术来制造参考电极906。
示例性芯片封装件816的尺寸可以介于约1至2厘米×1至2厘米之间或更小,而衬底902的尺寸可以介于3至4厘米×3至4厘米之间或更小。
开口814示出为位于芯片702上方,至少暴露芯片702的传感器阵列。在示例性实施例中,开口814沿x或y方向与参考电极906大致对准,从而使得流体沟道可以放置在开口814和参考电极906两者上方。
流体设计
参考图10,提供示例性流体盒1000的示意图。示意图示出盒1000的自上向下的视图,并且应当注意,并非所示的所有元件都在相同的水平面上。此外,为了提高可视化,有目的地未按比例绘制各个流体沟道的特定尺寸和比例。盒1000包括壳体1002。可以使用注塑、铸造或3-d印刷技术(仅举几个实例)由诸如聚甲基丙烯酸甲酯(pmma)的任何塑料材料形成壳体1002。可以由机械地或通过使用粘合剂连接在一起的一个以上的区段形成壳体1002。在一个实施例中,可以在壳体1002的一个或多个组件内模制各个流体沟道和室。在另一实施例中,由诸如聚二甲基硅氧烷(pdms)的不同的模制聚合物材料形成各个流体沟道和室。壳体1002的总体尺寸可以介于约4厘米至约7厘米×约4厘米至约7厘米之间。随着技术的进步,壳体1002可以变得更小。在一个实施例中,在壳体1002内设置具有封装芯片802的衬底902。在一个实例中,仅将衬底902的部分封装在壳体1002内,而边缘连接件908暴露在壳体1002的外部。
示例性壳体1002的流体设计包括至少第一沟道1004、第二沟道1006和第三沟道1008。第一沟道1004和第二沟道1006均分别包括对应的流体入口1010a和1010b。流体入口提供将流体从盒1000的外部注入到盒1000中的区域。流体入口还提供将流体从盒1000排出到盒1000外部的区域。第三沟道1008可以在接合至衬底902的封装芯片802上方对准。在一个实施例中,传感器阵列上方的开口814大致位于第三沟道1008内。根据实施例,在衬底902上图案化的参考电极906也在第三沟道1008内对准。
第一沟道1004、第二沟道1006和第三沟道1008均可以具有介于约1毫米和3毫米之间的沟道宽度。沟道高度可能为约1毫米。在另一实施例中,第一沟道1004、第二沟道1006和第三沟道1008中的一个或多个是宽度和高度尺寸小于1mm的微流体沟道。第一沟道1004、第二沟道1006和第三沟道1008均可以具有矩形、正方形或半圆形的截面。
在一些实施例中,第一沟道1004和第二沟道1006中的一个或多个与第三沟道1008连接。以这种方式,流过第一沟道1004的流体将最终流过第三沟道1008,并且类似地流过第二沟道1006的流体将最终流过第三沟道1008。在一些实施例中,第三沟道1008最终流入废物室1016,其收集流过盒1000的所有流体。废物室1016可以包括至大气中的排气口(未示出),以避免流体系统内的背压积聚。
在一些实施例中,入口1010a和1010b分别地包括插塞1012a和1012b。插塞1012a/1012b可以是柔软的柔性材料,其紧密地安装到入口1010a/1010b内,以将入口密封从而防止任何流体泄漏。插塞1012a/1012b可以是诸如聚四氟乙烯(ptfe)或软木塞的聚合物材料。插塞1012a/1012b可以密封入口1010a/1010b,同时允许毛细管穿过插塞1012a/1012b而不损坏流体密封。毛细管可以是诸如注射器针的针状管。毛细管可以包括诸如金属或硬塑料的硬的刚性材料。在讨论盒1000与分析仪的连接时,稍后将更详细地描述毛细管与盒1000的连接。
盒1000包括样本入口1014,其布置为将样本引入第一沟道1004(如图10所示)或第二沟道1006。在一个实例中,可以通过样本入口1014将血液样本放置到流体系统中。一旦已经引入样本,可以使用盖或任何其他类似的结构密封样本入口1014,以在样本入口1014周围提供防漏密封。在图10所示的沟道布置中,从入口1010a流过第一沟道1004的流体将与通过样本入口1014引入的样本混合,并且混合物将在第三沟道1008中的开口814和参考电极906上方流动。一旦已经将样本传送至由开口814暴露的传感器阵列,则可能发生生物分子之间的相互作用,并且fetsensor传感器可用于检测样本中特定分析物的存在或测量样本中特定分析物的浓度。仅举几个实例,可以使用压力驱动流使流体沿着各个沟道并且在各个沟道之间移动。压力可能是由注射器迫使液体或空气通过盒1000导致的,或通过推压液体的加压空气导致的。用于通过盒1000输送液体的技术的其他实例包括电润湿或使用芯片上蠕动泵。在一些实施例中,可以使用本领域已知的各个芯片上混合方法中的任何一种在盒1000内进行流体混合。盒1000的流体沟道的尺寸可以足够大,使得由于液体移动通过沟道时液体的紊流进行一些流体混合。应当理解,样本入口1014的位置可以变化。例如,样本入口1014可以直接位于开口814上方,从而使得引入到样本入口1014中的样本还引入到通过开口814暴露的传感器阵列上方。
一旦衬底902已经集成到壳体1002中,根据实施例,可以利用各种捕获试剂功能化通过开口814访问的传感器阵列。该工艺可能涉及通过第三沟道1008流动的包括捕获试剂的液体缓冲液,从而使得捕获试剂有机会结合至传感器阵列中的各个fet传感器。在另一实例中,当样本入口1014位于开口814上方时,在开口814的上方直接设置捕获试剂。在已经固定捕获试剂之后,可以密封样本入口1014,从而使得可以储存盒1000直到准备好实施生物感测测试。捕获试剂可以保留在其初始的缓冲溶液中,或者可以引入新的缓冲溶液以保存捕获试剂,同时盒1000等待测试。本文提供了不同的捕获试剂和利用捕获试剂实施测试的实例。
参考图11,示出用于盒1000的各个流体通沟道的另一设计。在该设计中,具有第一入口1102a的第一沟道1104和具有入口1102b的第二沟道1106会聚在具有样本入口1110的区域处。具有在其内对准的开口814的第三沟道1108在样本入口1110处与第一沟道1104和第二沟道1106连接。开口814提供了一个向下至芯片的通路,以至少将芯片上的传感器阵列暴露于第三沟道1108中的流体。从第一沟道1104或第二沟道1106流过第三沟道1108的流体最终收集在废物室1112内。可以基于各个沟道的几何形状或者通过使用阀关闭特定沟道来朝向废物室1112引导流体。样本入口1110还可以位于开口814上方。
第一沟道1104、第二沟道1106和第三沟道1108中的一个或多个可以包括气泡阱1114。气泡阱1114可以表示具有突然更大的截面(或较高的“天花板”)的流体沟道的区域,从而使得存在于溶液中的任何空气可以上升到在气泡阱1114处创建的附加的空间中。相关领域的技术人员应该理解,可以使用其他气泡阱设计。在溶液到达开口814下面的传感器阵列之前从溶液中除去气泡对于确保精确的感测结果非常重要。
参考图12,盒1000示出为连接至分析仪1200,从而用于实施生物感测。可以通过例如向着分析仪1200的接收端口按压盒1000来使盒1000与分析仪1200物理接触。分析仪1200的接收端口可以包括用于形成与边缘连接件908的一些或全部的欧姆接触的电焊盘。衬底902的边缘可以紧密地安装到分析仪1200的接收端口中,从而使得边缘连接件908贴着(pressagainst)分析仪1200的对应的导电焊盘。此外,组装盒1000和分析仪1200的其他方法包括将它们夹在一起,将一个插入另一个中。分析仪1200可以足够小以便于携带并且可以适合于成年人手掌。
在一些实施例中,分析仪1200至少包括第一注射器1202a和第二注射器1202b。第一注射器1202a和第二注射器1202b均可以包括在盒1000的操作期间使用的缓冲液或其他流体。注射器1202a/1202b均包括对准的针1204a/1204b,以延伸到远离分析仪1200的剩余部分的间隔中。在一些实施例中,可以对准针1204a/1204b,从而使得向着分析仪1200的接收端口按压盒1000可导致针1204a/1204b穿过对应的插塞1012a/1012b并进入入口1010a/1010b中。在该实施例中,针1204a/1204b是穿过对应的插塞1012a/1012b的毛细管的一个实例。因此,创建防漏密封以将溶液从每个注射器1202a/1202b转移到盒1000的对应入口1010a/1010b中。应当理解,尽管说明书仅描述了与两个输入端口对准的两个注射器,但是可以使用任何数量的注射器和流体输入端口,包括仅使用一个注射器与单个入口连接的实例。每个注射器1202a/1202b可以预先装有用于各个测试的溶液。在另一实施例中,使用者可以容易地将每个注射器1202a/1202b去除并替换为不同的注射器。
每个注射器1202a/1202b可以具有通过对应的致动器1206a/1206b控制的与其相关的活塞。致动器1206a/1206b的实例包括步进电机或感应电机。致动器1206a/1206b按压注射器1202a/1202b的活塞的速度将直接影响盒1000的流体沟道内溶液的流速。可以通过电机控制模块1208a/1208b来控制致动器1206a/1206b。相关领域的技术人员将理解,电机控制模块1208a/1208b包括生成用于控制致动器1206a/1206b的速度和操作的电压所需的电路。
制造的与盒1000的边缘连接件908的所有电连接可以布线至感测电子设备1210。感测电子设备1210可以包括任何数量的分立电路、集成电路和分立模拟电路组件,其设计成在感测电子设备1210和边缘连接件908之间提供和接收许多不同的电信号。例如,感测电子设备1210可以配置为向边缘连接件908提供电源信号、接地信号和时钟信号,后续可用于供电和操作传感器阵列和芯片702上的其他电子设备。感测电子设备1210还可以提供用于激活传感器阵列内的特定fet传感器的栅极的各种电压偏置电平。感测电子设备1210可以接收表示从特定fet传感器测量的漏极电流的信号,以及表示从芯片702上的温度传感器的输出的信号。感测电子设备1210可以将该接收到的数据存储在存储器中,或者可以使用所接收的数据来改变电压偏置电平,或改变由芯片702上的加热器产生的热量。通常,感测电子设备1210控制与由盒1000的传感器阵列实施的生物感测相关的所有信令。
在一些实施例中,分析仪1200还包括处理器1212,其控制分析仪1200的诸如电机控制模块1208a/1208b和感测电子设备1210的每个其他模块的功能和定时。处理器1212可以是任何类型的中央处理单元(cpu)或微控制器,并且可以由用户编程以实施与分析仪1200的操作相关的特定功能。处理器1212可以配置为分析从感测电子设备1210接收的信号,以确定来自盒1000中的样本的给定分析物的浓度水平。与确定的浓度水平相关的数据可以存储在分析仪1200的存储器中。在另一实施例中,感测电子设备1210确定来自盒1000中的样本的给定分析物的浓度水平,并且还配置为将与所确定的浓度水平相关的数据存储在分析仪1200的存储器中。
在一些实施例中,分析仪1200包括设计为使数据与外部处理器件通信的通信模块1214。处理器1212可以与通信模块1214电连接以控制数据传输。通信可以是有线或无线的。有线通信的实例包括通过网络电缆或通用串联总线(usb)电缆的数据传输。无线通信可以包括无线rf传输、蓝牙、wifi、3g或4g。通信模块1214还可以设计成从外部处理器件接收数据。例如,可以将用于如何操作分析仪1200的各个组件的程序发送到通信模块1214并由处理器1212执行。通信模块1214可以包括任何数量的公知的硬件元件以促进模拟数据和/或数字数据传输和接收。
在已经实施生物感测测试之后,盒1000可以从分析仪1200中去除并丢弃。此外,注射器1202a/1202b可以从分析仪1200中去除并丢弃。因此,所有试剂保留包括在盒1000或注射器1202a/1202b中,并且不发生分析仪1200的任何其他部分的污染。以这种方式,可以重新使用单个分析仪1200来测试任何数量的附加的盒,其中可以用不同的捕获试剂单独地功能化每个盒以实施不同的生物感测测试。
在另一实施例中,注射器1202a/1202b集成到盒1000上,并且盒1000和分析仪1200之间的连接将注射器1202a/1202b的相关活塞与分析仪1200上的致动器1206a/1206b对准。在该实施例中,分析仪1200完全没有任何试剂携带容器。
在另一实施例中,盒1000包括穿过对应插塞1012a/1012b的一个或多个毛细管。在该实施例中,当在盒1000和分析仪1200之间发生连接时,毛细管与分析仪1200中的其余注射器1202a/1202b流畅地连接。在已经实施生物感测测试之后,盒1000以及其毛细管可以从分析仪1200中去除并丢弃。
参考图13,示出示例性方法1300。可以在盒1000已经连接至分析仪1200之后由分析仪1200实施方法1300。可以在方法1300的所示操作之前、之间或之后实施在方法1300中未示出的与流体处理和电测量有关的其他操作。以与所示的一个顺序的不同顺序实施方法1300的各个操作。在实施例中,在已经将捕获试剂固定在盒1000内之后实施方法1300。
在框1302处,第一溶液流过盒的第一沟道。第一溶液可以通过连接至第一沟道的入口进入盒。可以由注射器提供第一溶液,该注射器具有穿过设置在第一沟道的入口处的插塞的针。第一溶液可以包括缓冲溶液以提供稳定的ph环境。
在框1304处,在第一溶液中校准传感器阵列的双栅背侧感测fet传感器。可以实施校准以测量各个fet传感器的噪声或背景信号。可以存储该测量值并且稍后在检测生物分子时,从测量信号中减去该测量值以尝试并降低噪声并且获得更清晰的检测信号。第一溶液必须存在于传感器阵列和在主检测沟道内图案化的参考电极上方,以实施校准。在一些实施例中,第一溶液在校准测量期间不流动。在一些实施例中,校准测量表示fet传感器的基准阈值电压。
在框1306处,样本通过样本入口输入到盒的流体网络中。样本可以是包括血液样本的任何液体样本。在一些实施例中,样本是在溶液中分解的半固体样本。在已经通过样本入口输入样本之后,可以通过使用盖子或其他类似的结构密封样本入口。
在框1308处,第二溶液流过盒的第二沟道。第二溶液可能是与第一溶液相同的溶液。第二溶液可以与在框1306处将样本输入到流体系统的路径交叉,并与样本混合。然后,样本和第二溶液的混合物可以流过第二沟道并进入传感器阵列所在的主检测沟道中。第二溶液可以是缓冲溶液。在一个实例中,第二溶液是分解的缓冲溶液。可以使用压力驱动流使第二溶液沿着各个沟道且在各个沟道之间移动。仅举几个实例,压力可能是由注射器迫使液体或空气通过盒导致的,或通过向着第二溶液推压的加压空气导致的。用于通过盒输送第二液体的技术的其他实例包括电润湿或使用芯片上蠕动泵。
在框1310处,存在于样本内的生物分子在传感器阵列上方培养。培养可以持续例如介于30秒至10分钟之间的任何给定的时间。在培养期间,与第二溶液混合的样本可以不流动,或者可以以非常慢的流速流动。可以设计流速,从而使得新鲜溶液随时间出现在传感器阵列上方,但是流动不太强以免对捕获试剂造成损坏或使结合反应不能发生。
在框1312处,在培养时间到期后,第三溶液流过盒的第一沟道并通过主检测沟道,以将与第二溶液混合的全部样本基本推入废物室。可以在给定时间段内通过主检测沟道注入第三溶液,以确保样本已经从主检测沟道中清除。理想情况下,框1312中使用的第三溶液是与第一溶液相同的溶液。在另一实施例中,第三溶液与第一溶液不同。第三溶液可以是缓冲溶液。
在框1314处,测量传感器阵列的输出以确定是否发生任何结合反应。传感器输出可以是从传感器阵列中的一个或多个双栅背侧感测fet传感器测量的漏极电流。测量的漏极电流可以与在框1304中的相同传感器的校准期间测量的漏极电流进行比较。如果阈值电压(例如,大致对应于导通fet并导致漏极电流流动所需的电压)已经在校准传感器时发生变化,则可以确定发生了结合反应,并且目标分析物存在于样本中。阈值电压变化的量和符号可能取决于以下许多因素:诸如双栅背侧感测fet传感器是n沟道器件还是p沟道器件,检测的分析物的类型和与分析物相关的正电荷或负电荷的量。在另一实例中,来自传感器阵列的测量输出是阈值电压本身,其可以与在框1304中的相同传感器的校准期间测量的阈值电压进行比较。
化学、生物学和界面
本申请中描述的本发明的装置、系统和方法可用于检测和/或监测各个实体之间的相互作用。这些相互作用包括生物和化学反应以检测测试样本中的目标分析物。作为实例,可以监测包括物理、化学、生物化学或生物转化的反应,以检测中间体、副产物、产物及它们的组合的产生。此外,本发明的装置、系统和方法可以用于在本文所述的各个测定中检测这些反应,包括但不限于,用于液体活检的循环肿瘤细胞测定和螯合测定(chelationassay)以检测重金属和其他环境污染物的存在。可以以单一格式或阵列格式监测这样的测定和反应,以检测例如多种目标分析物。
具有dgbssfet传感器的生物传感实例
参考图14,使用上述双栅背侧感测fet传感器实施示例性生物感测测试。探针dna1404(捕获试剂的实例)通过连接分子1402接合至界面层508。连接分子1402可以具有结合至界面层508的部分的反应性化学基团。连接分子的实例包括硫醇。还可以通过界面层508的表面的硅烷化或通过将界面层508的表面暴露于氨(nh3)等离子体以在表面上形成反应性nh2基团来形成连接分子。如相关领域的技术人员通常所理解的,硅烷化工艺涉及将界面层508的表面依次暴露于不同的化学品,以在界面层508的表面上建立共价结合的分子。探针dna1404表示单链dna。根据实施例,在实施方法1300的任何步骤之前,将连接分子1402接合至界面层508。在实施方法1300的任何步骤之前,探针dna1404也可以结合至连接分子1402。在另一实例中,在方法1300的框1302处探针dna1404接合至连接分子1402。
根据实施例,图14所示的双栅背侧感测fet传感器是将存在于诸如上述芯片702的芯片上的传感器阵列内的一个fet。在切割包括芯片702的晶圆以将芯片702与晶圆分离之前,连接分子1402可以接合至界面层508。
可以在使fet传感器经受样本1401之前将探针dna1404固定在界面层508上。样本1401可以包括强有力地结合至与其配对的探针dna1404的配对的单链dna序列1406。附加的dna的结合会增加界面层508上存在的负电荷,并且该附加的dna的结合直接位于fet传感器的沟道区208上方。
在图15a中概念性地示出dna结合。这里具有核酸序列tcga的探针dna结合至具有核酸序列agct的其互补配对的链。任何未配对的序列都不会与探针dna序列杂交。配对的dna的结合增加了累积在界面层508的界面处的负电荷。在图15a所示的实例中,界面层508是氧化铪。
图15b示出当配对的dna结合至界面层508的表面时双栅背侧感测fet传感器的阈值电压偏移。简而言之,电压施加到流体栅极510直到fet传感器“导通”,并且电流在漏极区206和源极区204之间流动。当由于互补dna结合而在界面层508上存在更多的负电荷时,需要较高的电压以在沟道区208内形成导电反型层。因此,根据实施例,在fet传感器导通和ids电流流动之前,可以将较高的电压施加到流体栅极510。可以测量阈值电压的这种差异,并用于确定目标配对的dna序列的存在,以及确定其浓度。应当理解,界面层508处的净正累积电荷将导致阈值电压降低而不是增加。另外地,与p沟道fet相比,n沟道fet的阈值电压的变化将具有相反的符号。
参考图16,使用双栅背侧感测fet传感器实施另一示例性生物感测测试。探针抗体1604(捕获试剂的另一实例)通过连接分子1602结合至界面层508。连接分子1602可以具有结合至界面层508的部分的反应性化学基团。可以在探针抗体1604上方提供样本溶液1601,以确定配对的抗原是否存在于样本溶液1601内。根据实施例,在实施方法1300的任何步骤之前,将连接分子1602结合至界面层508。在实施方法1300的任何步骤之前,探针抗体1604还可以结合至连接分子1602。在另一实例中,探针抗体1604在方法1300的框1302处接合至结合分子1602。
参考图17,示出配对抗原与探针抗体1604的结合过程。这里,配对的抗原将结合至固定的探针抗体,而未配对的抗原不结合。与上述dna杂交过程类似,配对的抗原将改变在界面层508处存在的累积电荷。以与上文参考图15b已经讨论的大致相同的方式测量由于来自结合至探针抗体的配对抗体的累积电荷而引起的阈值电压的偏移。
在实施例中,提供了一种流体盒,包括:衬底,包括多个接触焊盘,配置为与分析仪电连接,半导体芯片,具有传感器阵列,以及参考电极;第一流体沟道,具有第一入口,并且连接至第二流体沟道,对准所述第二流体沟道使得所述传感器阵列和所述参考电极设置在所述第二流体沟道内;样本入口,用于将样本放置在所述第一流体沟道或所述第二流体沟道的路径内;第一插塞,设置在所述第一入口处并且包括配置为被毛细管穿过而不会使流体通过所述第一插塞泄漏的柔性材料。
在实施例中,流体盒还包括具有第二入口的第三流体沟道。
在实施例中,所述第三流体沟道连接至所述第二流体沟道。
在实施例中,流体盒还包括第二插塞,设置在所述第二入口处,并且包括配置为被所述毛细管穿过而不会使所述流体通过所述第二插塞泄漏的柔性材料。
在实施例中,所述第一插塞和所述第二插塞配置为与连接至所述分析仪的第一毛细管和第二毛细管对准,并且当所述流体盒和所述分析仪物理接触时,多个接触焊盘与所述分析仪连接。
在实施例中,当所述流体盒和所述分析仪物理接触时,所述第一毛细管和所述第二毛细管分别穿过所述第一插塞和所述第二插塞。
在实施例中,所述衬底是印刷电路板。
在实施例中,流体盒还包括连接至所述第二流体沟道的废物室。
在实施例中,所述传感器阵列中的一个或多个传感器包括配置为结合至存在于所述样本中的目标分子的多个探针分子。
在实施例中,所述传感器阵列包括双栅背侧感测fet传感器阵列。
在实施例中,提供了一种流体盒,包括:第一流体沟道,具有第一入口,并且连接至第二流体沟道,对准所述第二流体沟道使得传感器阵列和参考电极设置在所述第二流体沟道内;样本入口,用于将样本放置在所述第一流体沟道或所述第二流体沟道的路径内;第一插塞,设置在所述第一入口处并且包括配置为被毛细管穿过而不会使流体通过所述第一插塞泄漏的柔性材料,其中,所述毛细管连接至分析仪,并且当所述流体盒与所述分析仪物理接触时,所述毛细管穿过所述第一插塞。
在实施例中,所述传感器阵列包括双栅背侧感测fet传感器阵列。
在实施例中,所述传感器阵列中的一个或多个传感器包括配置为结合至存在于所述样本中的目标分子的多个探针分子。
在实施例中,所述多个探针分子包括dna、rna和抗体中的一种或多种。
在实施例中,流体盒还包括:具有配置为与所述分析仪电连接的多个接触焊盘,具有所述传感器阵列的半导体芯片,和参考电极。
在实施例中,提供了一种分析仪配置为与流体盒连接,所述分析仪包括:
注射器,布置成使得当所述流体盒物理连接至所述分析仪时,所述注射器的针与所述流体盒的对应输入端口对准;
致动器,配置为控制所述注射器的操作;
感测模块,配置为当所述流体盒物理连接至所述分析仪时,经由多个导电焊盘向所述流体盒发送信号并从所述流体盒接收信号,其中,所述多个导电焊盘接触所述流体盒上的对应的多个导电焊盘;以及处理器,电连接至所述感测模块,并且配置为基于从所述流体盒接收的信号来确定来自所述流体盒中的样本的给定分析物的浓度水平。
在实施例中,分析仪还包括致动器控制器,配置为控制所述致动器的操作。
在实施例中,所述处理器还电连接至所述致动器控制器。
在实施例中,分析仪还包括至少一个其他注射器,布置成使得当所述流体盒物理连接至所述分析仪时,所述至少一个其他注射器的针与所述流体盒的对应输入端口对准。
在实施例中,分析仪还包括存储器,配置为存储与由所述处理器确定的给定分析物的浓度水平有关的数据。
最终备注
应当理解,详细描述的部分,而不是公开部分的摘要,旨在用于解释权利要求。公开部分的摘要可以阐述发明人所预期的本发明的一个或多个但不是全部的示例性实施例,因此,不旨在以任何方式限制本发明和相关权利要求。
应当理解,本文的措辞或术语是为了描述而不是限制的目的,从而使得本说明书的术语或措辞由相关领域的技术人员在本文中根据教导和指导来解释。
本发明的广度和范围不应该由上述示例性实施例中的任何一个限制,而是应仅根据所附权利要求及其等同物来限定。
- 还没有人留言评论。精彩留言会获得点赞!