一种ST37型艰难梭菌及其单位点变异型ST81的鉴定方法与流程
本发明涉及一种菌种型别的鉴定方法,具体涉及一种st37型艰难梭菌及其单位点变异型st81的鉴定方法。
背景技术:
艰难梭菌(clostridiumdifficile,cd)是一种专性厌氧,革兰阳性的粗大芽孢杆菌,是抗生素相关性腹泻和伪膜性肠炎(pmc)的主要病原体,约30%的抗生素相关性腹泻以及90%以上的伪膜性肠炎由艰难梭菌引起。艰难梭菌相关性腹泻(clostridiumdifficile-associateddiarrhea,cdad)的临床表现差异较大,患者症状可为轻度腹泻或重度致死性的伪膜性肠炎。艰难梭菌基因型与患者病情相关,感染不同的基因型,疾病的发展和预后可能完全不同,如感染了高毒力基因型,例如艰难梭菌027/nap1/bi(pcr-核糖体分型为027,脉冲场凝胶电泳分型为nap1,限制性内切酶分型为bi)可导致严重后果,甚至死亡。
艰难梭菌导致人类腹泻的主要致病机制与该菌产生的两种毒素有关,即肠毒素a(tcda)和细胞毒素b(tcdb),rt027型艰难梭菌是一种毒素a+b+菌株,但是该菌株在我国并不常见,我国等亚洲地区国家较为广泛流行的是rt017型,也就是多位点序列分型37型(以下简称st37型),st3型和st54型也较为常见。st37型艰难梭菌是一种毒素a-b+菌株,即仅产生毒素b,不产生毒素a,却比a+b+菌株有更强的耐药特性和致病能力。近年来,由a-b+菌株引起的严重cdi症状和医院内爆发流行时有报道,来自韩国的一家三级医院的研究表明,相比a+b+菌株,a-b+菌株在伪膜性肠炎(pmc)患者中的检出率更高,对氟喹诺酮类、大环内脂类、林可霉素类等多种抗生素呈高水平耐药的特性更促使st37型艰难梭菌在医院内的广泛流行。st81型是st37型的单位点变异型,二者具有非常相近的亲缘关系和相似的生物学特性。st81型与st37型艰难梭菌均为a-b+变异株,且同样存在“耐多药”现象,具有同样的诊断价值。因此,st37型艰难梭菌及其单位点变异型st81型的快速鉴定对cdi的防控和治疗用药的选择具有极其重要的意义。
传统的mlst分型技术需要经过细菌基因组提取,扩增,测序,并将测序结果提交数据库比对后,才可知道分型结果,完整的mlst分型过程需要1~2天的时间,既耗时又耗力,并且操作繁琐,价格昂贵,无法在临床实验室中常规检测。当院内感染暴发时,mlst对引起院内感染的病原体的检测具有滞后性,无法满足快速鉴定的实际需求。
技术实现要素:
本发明的目的就是提供一种st37型艰难梭菌及其单位点变异型st81的鉴定方法,以解决现有鉴定方法操作繁琐、耗时长且无法用于常规检测的问题。
本发明的目的是这样实现的,一种st37型艰难梭菌及其单位点变异型st81的鉴定方法,包括以下步骤:提取待鉴定艰难梭菌菌株中的蛋白质,得到质谱测试样品;利用质谱检测设备对上述样品进行检测,所得质谱图中在m/z3235~3245和m/z3280~3290处同时存在特异性的蛋白峰的菌株为st37型艰难梭菌或其单位点变异型st81。
本发明方法中,采用乙醇/甲酸法提取待鉴定艰难梭菌菌株中的蛋白质。
本发明方法中,所述质谱测试样品按照以下步骤制备:取5~10mg新鲜培养的艰难梭菌菌株充分悬浮于300μl超纯水中,再加入900μl无水乙醇,充分混匀后,12000×g离心2min,弃去上清液,向沉淀中加入20μl70%甲酸水溶液(由70μl甲酸和30μl水配成)并混匀,再加入20μl乙腈,充分振荡混匀,12000×g离心2min,吸出上清放于干净的ep管(即离心管)中,将含有艰难梭菌蛋白质提取物的1μl上清液转移到样品靶板上,室温下干燥,之后,将1μlchca基质覆盖在样品靶板上,避风干燥,即得到质谱测试样品。
本发明方法中,所用的质谱检测设备为microflexlt基质辅助激光解吸电离飞行时间质谱仪或vitekms全自动快速微生物质谱检测系统。
本发明首次建立了一种基于maldi-tofms的st37型艰难梭菌及其单位点变异型st81的快速鉴定方法,通过检测质谱中是否存在一组特异性的蛋白峰(m/z3235~3245和m/z3280~3290),即可判定是否为st37型或其单位点变异型st81型艰难梭菌,该方法具有实时快速的特点,可以在菌种鉴定的同时将st37型及其单位点变异型st81实时筛选出来,鉴定过程不再需要其他的特殊仪器设备,也不需要额外的操作步骤,对疾病的快速诊断和提供及时的临床用药指导具有重要意义,适用于医院感染和暴发流行的监测。
本发明方法简单,操作简便,结果准确有效,重复性好,且所用设备均为常规实验设备,便于推广和应用。
附图说明
图1是实施例1中159株艰难梭菌菌株clinprotools软件分析的质谱图。
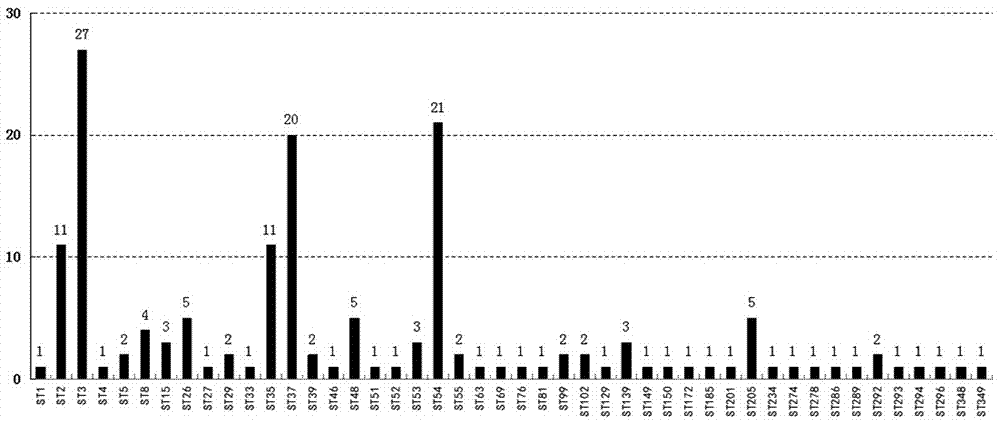
图2是实施例1中159株艰难梭菌菌株的mlst分型结果柱状图。
图3是实施例3中编号38-1样品的质谱图。
图4是实施例3中编号81-1样品的质谱图。
图5是实施例3中编号90-1样品的质谱图。
图6是实施例3中编号3-1样品的质谱图。
图7是实施例3中编号45-1样品的质谱图。
图8是实施例3中编号86-1样品的质谱图。
具体实施方式
下面结合具体实施例进一步阐述本发明,在以下实施例中,未详细描述的各种过程和方法是本领域中公知的常规方法,所用试剂为市售分析纯或化学纯。
实施例1
样品:159株艰难梭菌均来自河北省医学微生物菌种保藏中心(hbcmcc),其中152株艰难梭菌采用随机数字表的方法随机选取自2010到2014年收集的腹泻患者和健康人群分离菌株(65株收集于腹泻患者,87株收集于健康成人或儿童),另包含7株已知不同st型的艰难梭菌标准菌株(atccbaa-1870,atccbaa-1382,atccbaa-1812,atccbaa-1804,atcc9689,atcc43255和atcc43598)。
菌株保存于hbcmcc超低温冰箱,使用前进行菌株复苏,将菌株接种于哥伦比亚血琼脂平板(英国oxoid公司)中,37℃厌氧环境下培养48小时,48小时后,刮取形态典型的单个菌落进行第二次传代,相同条件下培养48小时后用于下面的实验。
所用试剂:
α-氰基-4-羟基肉桂酸(chca),美国sigma公司;色谱级无水乙醇,美国sigma公司;色谱级乙腈,美国sigma公司;色谱级甲酸,美国sigma公司;三氟乙酸(tfa),美国sigma公司;bruker细菌测试蛋白标准品,德国brukerdaltonics公司。
所用仪器:
vitekms全自动快速微生物质谱检测系统,法国biomérieux公司;
microflexlt基质辅助激光解吸电离飞行时间质谱仪,德国brukerdaltonics公司。
按照如下方法对各样品进行测试。
maldi-tof样品准备:
挑取适量(5-10mg)新鲜培养的细菌充分悬浮于300μl超纯水中,再加入900μl无水乙醇,充分混匀后,12000×g离心2min,弃去上清液(尽量去除乙醇和水),向沉淀中加入20μl70%甲酸水溶液,混匀,再加入20μl乙腈并充分混匀,12000×g离心2min,将含有细菌蛋白质提取物的1μl上清液转移到样品靶板上,室温下干燥,之后,将1μlchca基质覆盖在样品靶板上,避风干燥,即得到maldi-tofms测试样品。
数据获取:用vitekms全自动快速微生物质谱检测系统和microflexlt基质辅助激光解吸电离飞行时间质谱仪分别对159株艰难梭菌样品进行检测。
vitekms:n2激光,λ=337nm,线性阳离子模式,vitekms(2.0)软件用于质谱数据采集,釆集的质量范围为:2000-20000da;参数设定为:离子源电压,20kv;透镜电压,6kv;延时提取,200ns;激光频率,50.0hz;545shots叠加形成一张谱图;大肠杆菌atcc8739用于质量校准及仪器参数优化。
microflexlt:n2激光,λ=337nm,线性阳离子模式,flexcontrol3.0软件用于质谱数据采集,釆集的质量范围为2000-20000da;参数设定为:源1电压,20kv;源2电压,18.5kv;透镜电压,8.45kv;延时提取,320ns;激光频率,20.0hz;50shots釆集一个样品结晶点,平均每个样本结晶点釆集10次,500shots叠加形成一张谱图(保证每张总谱图峰强度达到10000以上);bruker细菌测试蛋白标准品用于质量校准及仪器参数优化。
数据分析:
检测质谱图中在m/z3235~3245和m/z3280~3290处是否存在蛋白峰,质谱图中信噪比大于4的峰为有效的蛋白峰,或者导出包含峰列表的txt文件,观察是否含有m/z3235~3245和m/z3280~3290蛋白峰。
鉴定结果:159株艰难梭菌中有21株菌的质谱图中同时在m/z3235~3245和m/z3280~3290处存在蛋白峰,由此确定,该21株菌为st37型艰难梭菌或其单位点变异型st81,且采用两种设备所测得的结果相同。将这21株艰难梭菌的质谱检测数据归为一组,将其余138株艰难梭菌的质谱检测数据归为另一组,将两组数据导入clinprotools软件中,得到159株艰难梭菌的clinprotools软件分析的质谱图,如图1,图1中可以看出,由上述21株艰难梭菌质谱检测数据得到的曲线中,在m/z3240和m/z3285处同时出现特异性蛋白峰,由上述138株艰难梭菌质谱检测数据得到的曲线中,在m/z3240和m/z3285处均不存在有效的蛋白峰。
对上述159株艰难梭菌进行mlst分型,以验证上述结果,具体步骤如下:
管家基因的扩增与测序:根据griffiths等的方案,选取7个管家基因(adk、atpa、dxr、glya、reca、sod、tpi)进行pcr扩增。反应体系:2×taqmastermix25μl,上、下游引物(10pmol/l)各1μl,dna模板2μl,ddh2o21μl。反应程序:94℃预变性15min,然后94℃变性30s,50℃退火40s,72℃延伸70s,共35个循环,最后72℃再延伸5min。扩增产物送上海生物工程有限公司和北京华大基因研究中心测序,测序峰图用chromas软件读取。
管家基因的比对:扩增序列提交到网络开源数据库(http://pubmlst.org/cdifficile/)中进行比对,每个位点得到相应的等位基因号,并形成相应的等位基因谱,判断该菌株的st。若出现新的等位基因型以及等位基因谱,则对相应的菌株进行2次以上重复试验,并送往不同公司测序,从而避免由于失误导致的假的新基因型。
结果显示,采用本发明方法鉴定出来的21株菌中有20株为st37型艰难梭菌和1株st81型艰难梭菌,其他的138株菌中均不是st37型或st81型菌株,由此可见,本发明方法将159株艰难梭菌中所有的st37型艰难梭菌及其单位点变异型st81型准确地鉴定出来,鉴定结果准确率高达100%。159株艰难梭菌的mlst分型结果见图2。
实施例2
样品:从收集于不同国家和地区(包括中国内地、中国香港、韩国、新加坡、澳大利亚)的艰难梭菌菌株中随机选取3株st35型艰难梭菌,4株st2型艰难梭菌,3株st3型艰难梭菌,1株st8型艰难梭菌,4株st54型艰难梭菌,1株st139型艰难梭菌,1株st81型艰难梭菌和22株st37型艰难梭菌,上述菌株均来自hbcmcc。
所用试剂:同实施例1。
所用仪器:vitekms全自动快速微生物质谱检测系统,法国biomérieux公司。
按照如下方法对各样品进行测试。
maldi-tof样品准备:方法同实施例1。
数据获取:
vitekms:同实施例1。
数据分析:检测质谱图中m/z3235~3245和m/z3280~3290处是否存在蛋白峰,或者导出包含峰列表的txt文件,观察是否含有m/z3235~3245和m/z3280~3290蛋白峰。
鉴定结果见表1,表中39株不同来源菌株的试验结果显示,21株st37型菌株和1株st81型菌株被正确鉴定出来,鉴定结果的准确率高达95.6%(22/23)。
表1各样品鉴定结果
注:“+”代表该菌株的质谱图中在m/z3235~3245和m/z3280~3290处存在的蛋白峰,“-”代表该菌株的质谱图中在m/z3235~3245和m/z3280~3290处不存在蛋白峰。
实施例3
样品:从收集于不同年份(2010年、2012年、2014年)的艰难梭菌菌株中随机选取2株st37型艰难梭菌(分别编号38、90)、1株st81型艰难梭菌(编号81)、1株st3型艰难梭菌(编号3)、1株st102型艰难梭菌(编号45)和1株st348型艰难梭菌(编号86),共6株菌株,上述菌株均来自hbcmcc,各菌株编号、型别和收集年份见表2。
表2菌株信息
由三位实验人员分别在不同时间重复对这6株艰难梭菌进行接种传代两次,培养条件都是37℃厌氧培养48h(厌氧培养系统,广州尤德公司)。在每个菌株的第二次传代的培养基中随机挑选三个菌落,总共采集54个艰难梭菌菌落,作为鉴定样品,编号分别为38-1~38-9、90-1~90-9、81-1~81-9、3-1~3-9、45-1~45-9、86-1~86-9。
所用仪器、试剂、maldi-tof样品准备方法、数据获取均同实施例2。
数据分析:总共得到54张质谱图,检测质谱图中m/z3235~3245和m/z3280~3290处是否存在蛋白峰,或者导出包含峰列表的txt文件,观察是否含有m/z3235~3245和m/z3280~3290蛋白峰,结果见表3。
表3样品检测结果
注:“+”代表该菌株的质谱图中在m/z3235~3245和m/z3280~3290处存在的蛋白峰,“-”代表该菌株的质谱图中在m/z3235~3245和m/z3280~3290处不存在蛋白峰。
结果显示:编号38-1~38-9、90-1~90-9、81-1~81-9的样品对应的质谱图中均同时在m/z3235~3245和m/z3280~3290处出现蛋白峰而被鉴定出来,编号3-1~3-9、45-1~45-9、86-1~86-9的样品对应的质谱图中均没有在m/z3235~3245和m/z3280~3290处同时出现蛋白峰而被区分出来。图3~8为部分样品的质谱图,图3为编号38-1样品的质谱图,图中在m/z3244处和m/z3286处同时出现特异性的蛋白峰,图4是编号81-1样品的质谱图,图中在m/z3243处和m/z3285处同时出现特异性的蛋白峰,图5是编号90-1样品的质谱图,图中在m/z3245处和m/z3284处同时出现特异性的蛋白峰;图6~8依次为编号3-1、45-1、86-1样品的质谱图,图中在m/z3235~3245和m/z3280~3290处均未出现蛋白峰。
上述试验表明:本发明方法能够准确地将st37型艰难梭菌及其单位点变异型st81鉴定出来,且不同操作人员和不同检测时间对鉴定结果没有影响,m/z3235~3245和m/z3280~3290蛋白峰有很高的重现性。
- 还没有人留言评论。精彩留言会获得点赞!