检测草甘膦残留的免疫层析试纸及其制备方法和应用与流程
本发明涉及草甘膦检测
技术领域:
,尤其是涉及一种检测草甘膦残留的免疫层析试纸及其制备方法和应用。
背景技术:
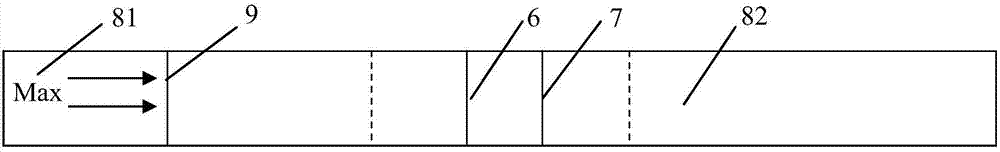
:草甘膦(glyphosate)是美国孟山都公司在1971年开发的一种广谱灭生性水溶性除草剂,能够非选择性的有效抑制多种一年生或多年生杂草。草甘膦化学名为n-膦羧甲基甘氨酸(n-phosphonomethyl-glycine,pmg),商品名为镇草宁、农达等,化学式为c3h8no5p,分子量为169。随着现代农业的迅速发展,农药的使用越来越广泛,农药残留对环境、动植物及人体健康造成的威胁越来越凸显。草甘膦目前已成为使用最广泛、用量最大的除草剂之一。虽然草甘膦的毒性较低,但长期大量使用会在环境和生物体内不断富集,并通过食物链进入人体,对人体健康造成潜在威胁。已有研究证实草甘膦具有一定的动物毒性作用。因此,很多国家和地区都将草甘膦的残留限量列入相关法规与标准中,我国以及美国的饮用水标准中都规定草甘膦的最大残留限量为0.7mg/l,我国2014年修订的食品安全国家标准《食品中农药最大残留限量》(gb2763-2014)中对草甘膦在食品中的最大残留限量作出了更为详细的规定。近年来,针对草甘膦残留的检测研究逐渐成为研究热点,目前较为成熟的检测方法包括气相色谱、液相色谱以及联用技术,但这些传统方法在样品处理、分析时间上都存在一些不足,不适宜于大批量快速筛查以及推广应用。因此,开发一种灵敏特异、简便省时的草甘膦残留的快速检测方法尤为重要。有鉴于此,特提出本发明。技术实现要素:本发明的第一个目的在于提供一种检测草甘膦残留的免疫层析试纸,以缓解现有技术中存在的在样品处理、分析时间上都存在一些不足,不适宜于大批量快速筛查以及推广应用的技术问题。本发明的第二个目的在于提供上述的免疫层析试纸在检测草甘膦残留中的应用。本发明的第三个目的在于提供上述免疫层析试纸的制备方法,以缓解现有技术中存在的对于草甘膦的检测仪器昂贵,操作复杂的技术问题。本发明提供了一种检测草甘膦残留的免疫层析试纸,所述免疫层析试纸包括吸附层,所述吸附层包括结合垫和印迹膜;所述结合垫包括草甘膦特异性抗体;所述印迹膜包括检测印迹和对照印迹。进一步的,所述免疫层析试纸还包括支撑板和保护膜;所述支撑板设于所述吸附层下方,用于粘结所述吸附层;所述保护膜设于所述吸附层上方,用于防止所述吸附层被外界污染。进一步的,所述吸附层还包括样品垫和吸水垫;所述样品垫与所述结合垫相接,用于与待测样品相接触;所述吸水垫与所述印迹膜相接,用于吸收待测样品溶液。进一步的,所述草甘膦特异性抗体为胶体金纳米颗粒标记的抗草甘膦兔源多克隆抗体。进一步的,所述检测印迹为草甘膦载体蛋白偶联物,所述对照印迹为抗小鼠igg抗体。本发明还提供了上述的免疫层析试纸在检测草甘膦残留中的应用。另外,本发明还提供了上述的免疫层析试纸的制备方法,所述制备方法包括:将所述草甘膦特异性抗体设于所述结合垫上,将所述检测印迹和对照印迹喷点于所述印迹膜上;在所述支撑板上依次固定所述样品垫、结合垫、印迹膜和吸水垫,并覆盖所述保护膜;优选地,所述草甘膦特异性抗体为胶体金纳米颗粒标记的草甘膦兔源多克隆抗体,所述检测印迹为草甘膦载体蛋白偶联物,所述对照印迹为抗小鼠igg抗体。进一步的,所述草甘膦载体蛋白偶联物制备方法包括:分别配置草甘膦溶液,1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐溶液和载体蛋白溶液;将所述草甘膦溶液和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐溶液混合并反应后,加入所述载体蛋白溶液混合并反应,得到反应产物;将所述反应产物透析后,离心取上清液,得到所述草甘膦载体蛋白偶联物。进一步的,所述草甘膦兔源多克隆抗体的制备方法包括:制备所述偶联物,应用所述偶联物作为免疫原对实验兔进行免疫,所述免疫完成后采血并提纯抗体,得到所述草甘膦兔源多克隆抗体。进一步的,所述胶体金纳米颗粒标记的草甘膦兔源多克隆抗体的制备方法包括:制备胶体金溶液,将所述草甘膦兔源多克隆抗体加入所述胶体金溶液中混合并反应,离心后得到沉淀,将所述沉淀复溶,再次离心得到胶体金纳米颗粒沉淀,将所述胶体金纳米颗粒沉淀用四硼酸钠溶液复溶,得到所述胶体金纳米颗粒标记的草甘膦兔源多克隆抗体。本发明提供的检测草甘膦残留的免疫层析试纸,包括设有草甘膦特异性抗体的结合垫及设有检测印迹和对照印迹的印迹膜。本发明提供的检测草甘膦残留的免疫层析试纸具有如下有益效果:(1)灵敏、特异。本发明提供的免疫层析试纸基于竞争性免疫反应原理,通过胶体金纳米颗粒标记的兔源多克隆抗体实现检测草甘膦的残留。胶体金纳米颗粒与抗体分子之间电荷间的范德华力相结合,对抗体的亲和力影响小。因此,该试纸具有较强的特异性和较高的灵敏度,目测检测限可达到1μg/ml左右。(2)简便、快速。使用本发明提供的免疫层析试纸,无需借助仪器判定检测结果,只需将试纸插入被检样品液中,5分钟内即可判定检测结果。(3)直观、准确。本发明提供的免疫层析试纸以显示胶体金自身红色的印迹作为检测的阴性和阳性标记,结果可裸眼直接判别,不易出现误判。(4)经济实用。本发明提供的免疫层析试纸可以对大批量样品进行同时检测,能够有效减少检测费用和检测时间,不需要昂贵仪器进行检测,能够有效减少设备费。(5)便于推广。本发明试纸由于其操作简便,能够满足检验检疫、环境监测、卫生监督、生产企业等多个单位的检测需求,适用性强,尤其能够在基层单位推广使用。本发明提供的免疫层析试纸为草甘膦在水质及食品等物质中的残留检测提供了新的途径,能够为保障环境检测和食品检测发挥重要作用,能够产生良好的经济效益。附图说明为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。图1为本发明实施例1提供的检测草甘膦残留的免疫层析试纸的侧视结构示意图;图2为本发明实施例1提供的检测草甘膦残留的免疫层析试纸的俯视图。图标:1-支撑板;2-样品垫;3-结合垫;4-印迹膜;5-吸水垫;6-检测印迹;7-对照印迹;81-第一保护膜;82-第二保护膜;9-标记线。具体实施方式下面将结合附图对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。在本发明的描述中,需要说明的是,如出现术语“中心”、“上”、“下”、“左”、“右”、“竖直”、“水平”、“内”、“外”等,其所指示的方位或位置关系为基于附图所示的方位或位置关系,仅是为了便于描述本发明和简化描述,而不是指示或暗示所指的装置或元件必须具有特定的方位、以特定的方位构造和操作,因此不能理解为对本发明的限制。此外,如出现术语“第一”、“第二”、“第三”仅用于描述目的,而不能理解为指示或暗示相对重要性。目前草甘膦残留的检测方法多采用气相色谱、液相色谱以及联用技术,但这些方法在样品处理上较为繁琐,分析时间较长,设备成本以及检测成本较高,不适宜于大批量快速筛查以及推广应用。为解决上述问题,本发明提供了一种检测草甘膦残留的免疫层析试纸,包括吸附层,该吸附层包括结合垫和印迹膜;结合垫包括草甘膦特异性抗体,该草甘膦特异性抗体用于与待测样品中的抗原特异性结合;印迹膜包括检测印迹和对照印迹,用于显示待测样品中是否有草甘膦残留。在一个优选的实施方式中,印迹膜上的检测印迹和对照印迹为平行排列的隐形直线印迹,或为其他类似形状印迹,两种印迹之间的距离为0.5cm。其中,结合垫例如可以为,但不限于玻璃纤维棉或尼龙膜。印迹膜例如可以为,但不限于纤维素膜,优选地,纤维素膜例如可以为,但不限于硝酸纤维素膜、纯纤维素膜或羧化纤维素膜。在一个优选的实施方式中,吸附层还包括样品垫和吸水垫;样品垫与所述结合垫相接,用于与待测样品相接触;吸水垫与所述印迹膜相接,用于吸收待测样品溶液。其中,样品垫例如可以为,但不限于玻璃纤维棉或尼龙膜。吸水垫例如可以为,但不限于吸水纯白滤纸。在一个优选的实施方式中,免疫层析试纸还包括支撑板和保护膜;支撑板设于所述吸附层下方,用于粘结所述吸附层;保护膜设于所述吸附层上方,用于防止所述吸附层被外界污染。其中,支撑板不吸水且表面有粘合剂。保护膜覆盖在样品垫、结合垫及吸水垫上。在样品垫与结合垫交界处对应保护膜的位置有样品标记线。在一个优选的实施方式中,草甘膦特异性抗体为胶体金纳米颗粒标记的抗草甘膦兔源多克隆抗体。在一个优选的实施方式中,检测印迹为草甘膦载体蛋白偶联物,对照印迹为抗小鼠igg抗体。本发明还提供了上述的免疫层析试纸在检测草甘膦残留中的应用。另外,本发明还提供了上述的免疫层析试纸的制备方法,包括:将草甘膦特异性抗体设于结合垫上,将检测印迹和对照印迹喷点于印迹膜上;在支撑板上依次固定样品垫、结合垫、印迹膜和吸水垫,并覆盖保护膜;优选地,草甘膦特异性抗体为胶体金纳米颗粒标记的草甘膦兔源多克隆抗体,检测印迹为草甘膦载体蛋白偶联物,对照印迹为抗小鼠igg抗体。在一个优选的实施方式中,草甘膦载体蛋白偶联物的载体蛋白例如可以为,但不限于牛血清白蛋白、鸡卵清蛋白或血蓝蛋白。草甘膦载体蛋白偶联物制备方法包括:分别配置草甘膦溶液,1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐溶液和载体蛋白溶液;将草甘膦溶液和1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐溶液混合并反应后,加入载体蛋白溶液混合并反应,得到反应产物;将反应产物透析后,离心取上清液,得到草甘膦载体蛋白偶联物。在一个更优选的实施方式中,草甘膦载体蛋白偶联物制备方法包括:(a)称取2mg草甘膦,用500μl磷酸盐缓冲液(pbs)溶解;(b)称取2mg1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐溶解于500μlpbs,然后在磁力搅拌的条件下,将其液逐滴缓慢加入步骤(a)得到的草甘膦溶液中反应10min左右;(c)称取3mg载体蛋白溶解于1000μlpbs,然后在磁力搅拌的条件下逐滴缓慢加入上述混合液中,在4℃避光条件下搅拌反应3h,然后将反应产物在pbs中透析,最后5000r/min离心5min取上清液,得到草甘膦载体蛋白偶联物。在一个优选的实施方式中,草甘膦兔源多克隆抗体的制备方法包括:制备偶联物,应用偶联物作为免疫原对实验兔进行免疫,免疫完成后采血并提纯抗体,得到草甘膦兔源多克隆抗体。在一个更优选的实施方式中,草甘膦兔源多克隆抗体的制备方法包括:(a)根据上述的偶联物制备方法制备偶联物并作为免疫原;(b)选取清洁级新西兰白兔,采用颈部皮下多点注射进行免疫,免疫剂量为200μg/ml/只,共免疫4次,每次间隔2-4周。首次免疫将免疫原用pbs稀释后与等体积的弗氏完全佐剂混合,25000r/min充分乳化10min,待溶液变为白色乳浊液后对新西兰白兔进行免疫,2-4次免疫为加强免疫,加强免疫剂量与首免相同,仅将弗氏完全佐剂换为弗氏不完全佐剂。(c)免疫程序完成后10-30天,进行耳缘静脉或心脏采血,首先置于37℃条件下2h,然后置于4℃条件下6-8h,5000-10000r/min离心5-10min,取出上清液。以饱和硫酸铵法提纯抗体,取血清加双倍pbs,然后加等体积饱和硫酸铵溶液混匀,置于4℃条件下过夜,然后5000-10000r/min离心5-10min,将沉淀用少量pbs溶解,然后加1/2体积饱和硫酸铵,混匀置于4℃条件下过夜,然后5000-10000r/min离心5-10min,将沉淀用少量pbs溶解,用pbs透析48~72h,换液5-10次,然后5000-10000r/min离心5-10min,取上清即为草甘膦兔源多克隆抗体。在一个优选的实施方式中,胶体金纳米颗粒标记的草甘膦兔源多克隆抗体的制备方法包括:制备胶体金溶液,将草甘膦兔源多克隆抗体加入胶体金溶液中混合并反应,离心后得到沉淀,将沉淀复溶,再次离心得到胶体金纳米颗粒沉淀,将胶体金纳米颗粒沉淀用四硼酸钠溶液复溶,得到胶体金纳米颗粒标记的草甘膦兔源多克隆抗体。其中,沉淀复溶可以用四硼酸钠溶液或pb溶液。在一个更优选的实施方式中,胶体金纳米颗粒标记的草甘膦兔源多克隆抗体的制备方法包括:通过柠檬酸三钠法首先制备直径10~20nm的胶体金溶液,以2μl/ml~3μl/ml的标记量将待标记的草甘膦兔源多克隆抗体加入ph为8.5~9.5的胶体金溶液中,反应30min后,加入10%(w/v)的bsa反应30min,4℃、15000rpm离心20min,沉淀用四硼酸钠溶液复溶,再次离心后将胶体金纳米颗粒沉淀用四硼酸钠溶液重悬,得到胶体金纳米颗粒标记的草甘膦兔源多克隆抗体。本发明提供的检测草甘膦残留的免疫层析试纸,利用了竞争性免疫反应的原理,当免疫层析试纸的测试端,即样品垫插入待测样品溶液后,待测样品溶液通过虹吸作用带动样品中的草甘膦及结合垫中的特异性抗体一起向印迹膜扩散,并最终渗入手柄端的吸水垫。在扩散过程中,样品中的草甘膦可先与特异性抗体相结合,进而使特异性抗体不能与印迹膜上喷点的草甘膦载体蛋白偶联物检测印迹结合,样品中的草甘膦与检测印迹的草甘膦载体蛋白偶联物竞争与草甘膦特异性抗体结合,即竞争免疫反应模式。如果样品中的草甘膦与特异性抗体完全结合,纤维素膜上则不显示红色检测印迹带;而印迹膜上喷点的抗小鼠igg抗体对照印迹仍可与特异性抗体结合,显示红色对照印迹带,即一条红色印迹带,表示为阳性;反之样品溶液中无草甘膦时,则不能与特异性抗体结合,特异性抗体便于草甘膦载体蛋白偶联物结合,在检测印迹处显示红色印迹带,而印迹膜上喷点的抗小鼠igg抗体对照印迹仍可与特异性抗体结合,显示红色对照印迹带,形成两条红色带表示为阴性。本发明提供的免疫层析试纸,基于竞争性免疫反应原理,通过胶体金纳米颗粒标记的兔源多克隆抗体实现检测草甘膦的残留,具有较强的特异性和较高的灵敏度,目测检测限可达到1μg/ml左右。使用本发明提供的免疫层析试纸,无需借助仪器判定检测结果,只需将试纸插入被检样品液中,5分钟内即可判定检测结果,简便、快速。并且,本发明提供的免疫层析试纸以显示胶体金自身红色的印迹作为检测的阴性和阳性标记,结果可裸眼直接判别,不易出现误判,直观、准确。在上述有益效果的基础上,本发明提供的免疫层析试纸还可以对大批量样品进行同时检测,能够有效减少检测费用和检测时间,不需要昂贵仪器进行检测,能够有效减少设备费,经济实用。由于其操作简便,能够满足检验检疫、环境监测、卫生监督、生产企业等多个单位的检测需求,适用性强,尤其能够在基层单位推广使用。本发明提供的免疫层析试纸为草甘膦在水质及食品等物质中的残留检测提供了新的途径,能够为保障环境检测和食品检测发挥重要作用,能够产生良好的经济效益。下面结合具体实施例和实验例,对本发明作进一步说明。实施例1本实施例提供了一种检测草甘膦残留的免疫层析试纸,如图1和图2所示,包括:支撑板1,吸附层和保护膜。支撑板1为塑料胶条,表面有粘合剂,用于粘结吸附层。吸附层包括依次相接的样品垫2、结合垫3、印迹膜4和吸水垫5。其中,样品垫2为玻璃纤维棉,用于与待测样品相接触;结合垫3为玻璃纤维棉,吸附有胶体金纳米颗粒标记的草甘膦兔源多抗;印迹膜4为纤维素膜,具体为硝酸纤维素膜;吸水垫5为吸水滤纸。在印迹膜4上喷点有隐形检测印迹6和隐形对照印迹7。隐形检测印迹6由草甘膦载体蛋白偶联物溶液制成;隐形对照印迹7由羊抗小鼠igg抗体溶液制成。隐形检测印迹6和隐形对照印迹7平行排列。保护膜分为第一保护膜81和第二保护膜82。第一保护膜81为覆盖在样品垫2和结合垫3上面的样品端保护膜;第二保护膜82为覆盖在吸水垫5上面的保护膜;设置第一保护膜81和第二保护膜82的颜色不同,以便区分。在本实施例中,第一保护膜81上还设有标记线9,用于提示试纸插入样品溶液的最深位置。该标记线9设于样品垫2接近结合垫3的位置,具体地,该标记线9设于样品垫2与结合垫3交界处对应的第一保护膜81上偏向样品垫2一侧0.5cm处。在本实施例中,在标记线9靠近样品垫2一侧的保护膜上印有箭头及max字样。在使用本实施例提供的检测草甘膦残留的免疫层析试纸时,包括以下步骤:检测水质:吸取1ml待测样品加入9mlpbs中,充分混匀10min,10000r/min离心5-10min,取上清用于检测。操作方法:将本实施例提供的检测草甘膦残留的免疫层析试纸的样品端,即样品垫2插入待测样品中,插入深度不超过标记线9,约10~20秒钟取出免疫层析试纸,水平放置,5min内观察判定检测结果。结果判定:(a)阴性,即在印迹膜4上显示两条红色印迹(检测印迹和对照印迹),表示被检样品中不含或含有低于检测限含量的草甘膦;(b)阳性,即在纤维素膜上显示一条红色印迹(对照印迹),表示被检样品中含有大于检测限的草甘膦;(c)失效,即在纤维素膜上没有红色带显示,则表明试纸已失效。实施例2本实施例提供了一种检测草甘膦残留的免疫层析试纸,与本发明实施例1的不同之处在于,样品垫2用尼龙膜制成,印迹膜4采用纯纤维素膜。操作方法和结果判定同本发明实施例1。实施例3本实施例提供了一种检测草甘膦残留的免疫层析试纸,与本发明实施例1的不同之处在于,隐形对照印迹7用兔抗小鼠igg抗体溶液在印迹膜4上制成,印迹膜4采用羧化纤维素膜。操作方法和结果判定同本发明实施例1。实施例4本实施例提供了一种检测草甘膦残留的免疫层析试纸,与本发明实施例1的不同之处在于,样品垫2用尼龙膜制成,隐形对照印迹7用兔抗小鼠igg抗体溶液在印迹膜4上制成。操作方法和结果判定同本发明实施例1。实施例5本实施例提供了上述实施例1至4提供的检测草甘膦残留的免疫层析试纸的制备方法,包括:a、草甘膦载体蛋白偶联物的制备草甘膦载体蛋白偶联物的载体蛋白为牛血清白蛋白,偶联物由以下方法制得:(1)称取2mg草甘膦,用500μl磷酸盐缓冲液(pbs)溶解;(2)称取2mg1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐溶解于500μlpbs,然后在磁力搅拌的条件下,将其液逐滴缓慢加入第一步溶液中反应10min左右;(3)称取3mg载体蛋白溶解于1000μlpbs,然后在磁力搅拌的条件下逐滴缓慢加入上述混合液中,在4℃避光条件下搅拌反应3h,然后将反应产物在pbs中透析,最后5000r/min离心5min取上清液,得到草甘膦载体蛋白偶联物。b、草甘膦兔源多克隆抗体的制备(1)根据上述的偶联物制备方法制备偶联物并作为免疫原;(2)选取清洁级新西兰白兔,采用颈部皮下多点注射进行免疫,免疫剂量为200μg/ml/只,共免疫4次,每次间隔2-4周。首次免疫将免疫原用pbs稀释后与等体积的弗氏完全佐剂混合,25000r/min充分乳化10min,待溶液变为白色乳浊液后对新西兰白兔进行免疫,2-4次免疫为加强免疫,加强免疫剂量与首免相同,仅将弗氏完全佐剂换为弗氏不完全佐剂。(3)免疫程序完成后10-30天,进行耳缘静脉或心脏采血,首先置于37℃条件下2h,然后置于4℃条件下6-8h,5000-10000r/min离心5-10min,取出上清液。以饱和硫酸铵法提纯抗体,取血清加双倍pbs,然后加等体积饱和硫酸铵溶液混匀,置于4℃条件下过夜,然后5000-10000r/min离心5-10min,将沉淀用少量pbs溶解,然后加1/2体积饱和硫酸铵,混匀置于4℃条件下过夜,然后5000-10000r/min离心5-10min,将沉淀用少量pbs溶解,用pbs透析48~72h,换液5-10次,然后5000-10000r/min离心5-10min,取上清即为草甘膦兔源多克隆抗体。c、样品垫2的制备样品垫2用玻璃纤维棉或尼龙膜等材料制备,将其裁成宽1.5cm规格的条带,放入封闭液中浸泡30min后,烘干备用。d、结合垫3的制备通过柠檬酸三钠法首先制备直径10~20nm的胶体金溶液,以2μl/ml~3μl/ml的标记量将待标记的草甘膦兔源多克隆抗体加入ph为8.5~9.5的胶体金溶液中,反应30min后,加入10%(w/v)的bsa反应30min,4℃、15000rpm离心20min,沉淀用四硼酸钠溶液复溶,再次离心后将胶体金纳米颗粒沉淀用四硼酸钠溶液重悬。将适当比例稀释的胶体金标记抗体喷点于玻璃纤维棉等材料的条带上,4℃低温真空干燥备用。e、印迹膜4的制备印迹膜4用硝酸纤维素膜、纯纤维素膜或羧化纤维素膜,裁成宽1.5cm规格的条带,用喷膜仪在印迹膜4上不同位置分别喷点草甘膦载体蛋白偶联物和抗小鼠igg抗体,两种印迹之间的距离为0.5cm,于37℃烘干后形成隐形的检测印迹和对照印迹。f、免疫层析试纸的组装将样品垫2、结合垫3、印迹膜4、吸水垫5黏贴在支撑板1上,各组件重叠2~3mm,然后经切条以切成3~4mm宽的试纸。本发明提供的免疫层析试纸的检测原理为:利用竞争性免疫反应的原理,当免疫层析试纸的测试端,即样品垫插入待测样品溶液后,待测样品溶液通过虹吸作用带动样品中的草甘膦及结合垫中的特异性抗体一起向印迹膜扩散,并最终渗入手柄端的吸水垫。在扩散过程中,样品中的草甘膦可先与特异性抗体相结合,进而使特异性抗体不能与印迹膜上喷点的草甘膦载体蛋白偶联物检测印迹结合,样品中的草甘膦与检测印迹的草甘膦载体蛋白偶联物竞争与草甘膦特异性抗体结合,即竞争免疫反应模式。如果样品中的草甘膦与特异性抗体完全结合,纤维素膜上则不显示红色检测印迹带;而印迹膜上喷点的抗小鼠igg抗体对照印迹仍可与特异性抗体结合,显示红色对照印迹带,即一条红色印迹带,表示为阳性;反之样品溶液中无草甘膦时,则不能与特异性抗体结合,特异性抗体便于草甘膦载体蛋白偶联物结合,在检测印迹处显示红色印迹带,而印迹膜上喷点的抗小鼠igg抗体对照印迹仍可与特异性抗体结合,显示红色对照印迹带,形成两条红色带表示为阴性。实验例1将草甘膦标准品配制成125ng/ml、250ng/ml、500ng/ml、1000ng/ml、2000ng/ml和4000ng/ml六个浓度的溶液,然后用本发明提供的免疫层析试纸进行检测,印迹膜上的检测印迹显色情况如下表所示:草甘膦浓度检测印迹显色情况125ng/ml红色250ng/ml红色500ng/ml微弱红色1000ng/ml无色2000ng/ml无色4000ng/ml无色从表中可以看出,草甘膦浓度大于1000ng/ml(1μg/ml)时,免疫层析试纸的检测印迹不显色;小于1000ng/ml(1μg/ml)时,免疫层析试纸的检测印迹开始显红色。这说明试纸具有较好的检测效果,目测检测限能够达到1μg/ml。实验例2使用其他常用农药亚胺磷、内吸磷、对硫磷、敌百虫、马拉硫磷以及载体蛋白作为检测物,每种物质标准品分别配置成1μg/ml、5μg/ml、25μg/ml、125μg/ml四个浓度的溶液,然后用免疫层析试纸进行检测,印迹膜上的检测印迹显色均为红色,结果表明试纸具有较强的特异性。综上所述,本发明提供的检测草甘膦残留的免疫层析试纸,操作快捷简便,检测特异性好,灵敏度高,检测结果直观准确,且适合大批量样品同时检测,有效减少了检测费用和检测时间,经济实用,满足多个检测领域的检测需求,适于大批量快速筛查和推广应用。最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1