一种用电位滴定法测定碳酸司维拉姆中总可滴定胺的方法与流程
本发明涉及化学分析技术领域,具体涉及一种用电位滴定法测定碳酸司维拉姆中总可滴定胺的方法。
背景技术:
碳酸司维拉姆是一种不会被人吸收的高分子聚合物,它携带多个氨基,由于本品分子中的氨基为弱碱,等当点的滴定突跃将不尖锐,传统的根据酸碱指示剂来判断反应终点的方法误差较大。而电位滴定仪是靠电极电位的突跃来指示滴定终点,可以有效监测滴定终点。本发明采用高灵敏度的全自动电位滴定仪,仔细设计滴定参数,可以有效监控等当点,实现本品的总可滴定胺测定。实验表明电位滴定突跃明显,精密度、准确度符合要求,可以有效的测定碳酸司维拉姆中总可滴定胺的含量。
技术实现要素:
由于常规的酸碱滴定无法准确判断碳酸司维拉姆总可滴定胺的滴定终点,针对这一难题,本发明提供了一种用电位滴定法测定碳酸司维拉姆中总可滴定胺的方法,本发明的目的是通过下述技术方案来实现的:
一种用电位滴定法测定碳酸司维拉姆中总可滴定胺含量的方法,其特征在于,包括以下步骤:
(1)取碳酸司维拉姆样品约1.0g,精密称定置于滴定杯中;
(2)用移液管精密量取1.0mol/l盐酸溶液15ml,加水35ml,搅拌40分钟;
(3)照电位滴定法,设置滴定参数,模式选择平衡控制模式,de为0.2mv,dt为1秒;阈值设为4~6mv/ml;等当点选择两个,其中一个等当点的电位值控制在150mv~250mv之间,另外一个等当点的电位值控制在-250mv~-280mv之间;采用玻璃电极,用1.0mol/l氢氧化钠滴定液滴定上述溶液;
所述的一种用电位滴定法测定碳酸司维拉姆中总可滴定胺含量的方法,其特征在于,所述步骤(2)中用移液管精密量取1.0mol/l盐酸溶液17ml,加水35ml,搅拌40分钟;
所述的一种用电位滴定法测定碳酸司维拉姆中总可滴定胺含量的方法,其特征在于,所述步骤(3)中模式选择平衡控制模式,de为0.2mv,dt为1秒,即电位变化控制在0.2mv/s的前提下,电位滴定仪可滴进下一滴;
所述的一种用电位滴定法测定碳酸司维拉姆中总可滴定胺含量的方法,其特征在于,所述步骤(3)中阈值设为4~6mv/ml;
所述的一种用电位滴定法测定碳酸司维拉姆中总可滴定胺含量的方法,其特征在于,所述步骤(3)中等当点选择两个,其中一个等当点的电位值控制在150mv~250mv之间,另外一个等当点的电位值控制在-250mv~-280mv之间。
一种用电位滴定法测定碳酸司维拉姆中总可滴定胺的方法,其实验过程如下:
一、实验原理
本品分子结构中含有氨基,分子中氨基以两种型态存在:游离氨基和铵离子。首先向样品中加入过量盐酸,使所有分子中的氨基转化为铵离子,然后用标准氢氧化钠溶液滴定上述酸性溶液,将会存在两个滴定等当点,游离酸完全中和时产生第一个等当点;铵离子完全中和转化为游离氨基时产生第二个等当点,两个等当点的差值即样品分子中氨基消耗滴定剂的量;
二、主要仪器及试剂
梅特勒t5电位滴定仪、mettlertoledo电子天平、mettlertoledodgi111-sc复合玻璃ph电极、1mol/l氢氧化钠滴定液、1mol/l盐酸溶液
三、样品的测定
(1)操作及计算过程
取碳酸司维拉姆(下称本品)约1.0g,精密称定置于滴定杯中,加入1.0mol/l盐酸溶液15ml,加水35ml,搅拌40分钟,照电位滴定法,仔细设置滴定参数,采用玻璃电极,用1.0mol/l氢氧化钠滴定液滴定上述溶液。
x=[(v2-v1)×c]/w
其中:x为总可滴定胺含量(mmol/g)
v2为第二个等当点消耗滴定液的体积数(ml)
v1为第一个等当点消耗滴定液的体积数(ml)
c为1.0mol/l氢氧化钠滴定液的浓度(mol/l)
w为样品称重(g),以干燥品计
(2)重复性实验
取本品约1.0g,精密称定置于滴定杯中,加入1.0mol/l盐酸溶液15ml,加水35ml,搅拌40分钟,照电位滴定法,仔细设置滴定参数,采用玻璃电极,用1.0mol/l氢氧化钠滴定液滴定上述溶液,重复滴定6份样品。结果见下表。
重复性实验结果
结论:由上表可知,重复测定6份样品,总可滴定胺品平均含量为12.23mmol/g,rsd为0.49%,小于2%,可见该方法重复性良好。
(3)中间精密度实验
按照“重复性试验方法”,有不同分析人员于不同日期,重复测定6份样品,考察12次测定结果的rsd。结果见下表。
精密度试验结果
结论:由上表可知,重复测定12份样品,总可滴定胺品平均含量为12.23mmol/g,rsd为0.42%,小于2%,可见该方法精密度良好。
采用上述技术方案,本发明的有益效果是:本发明的方法电位滴定突跃明显,精密度、准确度符合要求,与传统的酸碱滴定相比,具有高效率、操作简单、易掌握等优点。
附图说明
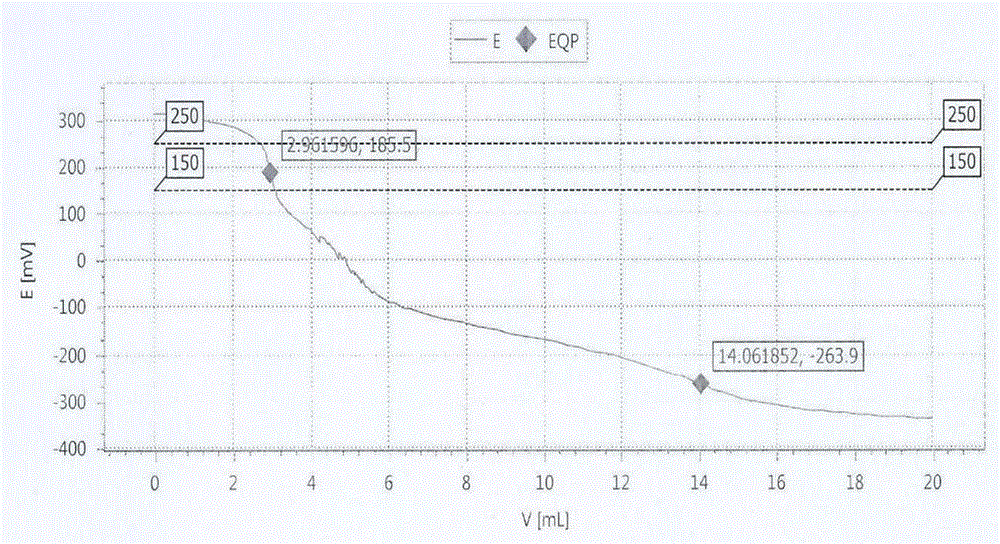
图1:电位值e(mv)随着滴定体积v(mv)的变化趋势;由图可以看出,电位值e(mv)随着滴定体积v(ml)的增加而变化,等当点有两个,分别为2.961596ml和14.061852ml;
图2:de/dv(mv/ml)随着滴定体积v(ml)的变化趋势;由图可以看出,de/dv(mv/ml)随着滴定体积v(ml)的增加而变化,等当点有两个即出现在de/dv(mv/ml)的峰值处即,分别为2.961596ml、14.061852ml。
具体实施方式
以下详细说明本发明,但不限定本发明的实施范围。
实施例1
(1)取碳酸司维拉姆(下称本品)约1.0g,精密称定置于滴定杯中;
(2)用移液管精密量取1.0mol/l盐酸溶液15ml,加水35ml,搅拌40分钟;
(3)照电位滴定法,仔细设置滴定参数,采用玻璃电极,用1.0mol/l氢氧化钠滴定液滴定上述溶液。
(4)滴定结束,通过计算得出总可滴定胺的含量。
实施例2
(1)取本品约1.0g,精密称定置于滴定杯中;
(2)用移液管精密量取1.0mol/l盐酸溶液13ml,加水35ml,搅拌40分钟;
(3)照电位滴定法,仔细设置滴定参数,采用玻璃电极,用1.0mol/l氢氧化钠滴定液滴定上述溶液。
(4)滴定结束,通过计算得出总可滴定胺的含量。
实施例3
(1)取本品约1.0g,精密称定置于滴定杯中;
(2)用移液管精密量取1.0mol/l盐酸溶液17ml,加水35ml,搅拌40分钟;
(3)照电位滴定法,仔细设置滴定参数,采用玻璃电极,用1.0mol/l氢氧化钠滴定液滴定上述溶液。
(4)滴定结束,通过计算得出总可滴定胺的含量。
实施例4
(1)取本品约1.0g,精密称定置于滴定杯中;
(2)用移液管精密量取1.0mol/l盐酸溶液15ml,加水35ml,搅拌30分钟;
(3)照电位滴定法,仔细设置滴定参数,采用玻璃电极,用1.0mol/l氢氧化钠滴定液滴定上述溶液。
(4)滴定结束,通过计算得出总可滴定胺的含量。
实施例5
(1)取本品约1.0g,精密称定置于滴定杯中;
(2)用移液管精密量取1.0mol/l盐酸溶液15ml,加水35ml,搅拌50分钟;
(3)照电位滴定法,仔细设置滴定参数,采用玻璃电极,用1.0mol/l氢氧化钠滴定液滴定上述溶液。
(4)滴定结束,通过计算得出总可滴定胺的含量。
实施例6
(1)取本品约1.0g,精密称定置于滴定杯中;
(2)用移液管精密量取1.0mol/l盐酸溶液15ml,加水30ml,搅拌40分钟;
(3)照电位滴定法,仔细设置滴定参数,采用玻璃电极,用1.0mol/l氢氧化钠滴定液滴定上述溶液。
实施例7
(1)取本品约1.0g,精密称定置于滴定杯中;
(2)用移液管精密量取1.0mol/l盐酸溶液15ml,加水40ml,搅拌40分钟;
(3)照电位滴定法,仔细设置滴定参数,采用玻璃电极,用1.0mol/l氢氧化钠滴定液滴定上述溶液。
(4)滴定结束,通过计算得出总可滴定胺的含量。
- 还没有人留言评论。精彩留言会获得点赞!