一种盐酸替罗非班注射液有关物质的检测方法与流程
本发明属于药物分析领域,涉及一种盐酸替罗非班注射液有关物质的检测方法。
背景技术:
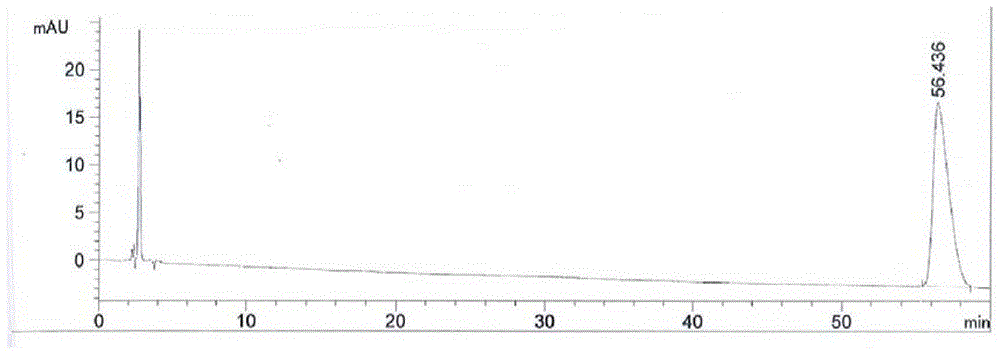
:盐酸替罗非班由美国merck公司研制开发,于1998年5月首次在美国上市,目前已在众多国家上市。盐酸替罗非班是一种高效、高选择性的gpⅱb/ⅲa受体拮抗剂,用于治疗不稳定型心绞痛或非q波心肌梗塞病人,预防心脏缺血事件,同时也适用于冠脉缺血综合征病人进行冠脉血管成形术或冠脉内斑块切除术,以预防与经治冠脉突然闭塞有关的心脏缺血并发症。杂质是影响药品质量的一个重要因素,在药品质量研究过程中,必须确认杂质的结构和控制杂质的含量。在药品申报注册中,根据fda及nmpa的要求必须对成品中的杂质进行严格的控制,对出现在最终产品的杂质必须进行结构分析及质量控制,其来源和去除需要在注册文件中进行描述。现有检测技术中,国家标准(标准号:ybh08272009)中所述的方法是以辛烷基硅烷键合硅胶为填充剂,以0.2%辛烷磺酸钠溶液(磷酸调节ph至3.0)和乙腈为流动相进行梯度洗脱,检测波长为227nm,注入适当浓度的供试品溶液和对照溶液进行分析检测,按不加校正因子的主成分自身对照法计算有关物质的含量。该方法所用辛烷基硅烷键合硅胶为填充剂的色谱柱,保留行为弱,不利于有关物质的分离,而且所用方法为梯度方法,在日常检测过程中基线易漂移,而且比较容易受到所用流动相纯度影响,如乙腈、甲醇等,可能引入不可预见的鬼峰,干扰有关物质的检测。另一现有检测技术,进口药品注册标准(标准号:jx20080265)中所述的方法是以十八烷基硅烷键合硅胶为填充剂,以0.01%磷酸二氢钾溶液(磷酸调节ph值至2.3)和乙腈(78:22)为流动相,流速为1.0ml/min;检测波长为227nm;柱温为35℃,等度洗脱。该方法要求主峰的拖尾因子不得过2.0,理论塔板数不小于7500,按照该方法筛选时,选用不同品牌的十八烷基硅烷键合硅胶色谱柱,主峰的保留时间很长,峰拖尾严重,不能满足系统要求。综上,提供一种简便、专属性好、准确度高的适用盐酸替罗非班注射液的有关物质检测方法是非常必要的。技术实现要素:针对现有技术存在的问题,本发明人通过多次试验,筛选不同的色谱柱以及组合其他不同的色谱条件,成功开发出一种更适合于检测盐酸替罗非班注射液有关物质的方法。本发明提供了一种盐酸替罗非班注射液有关物质检测的高效液相(hplc)质量控制方法,该方法较现有技术公开的方法更具有分离度更高,检出的杂质更多,专属性强,灵敏度高,准确性好。本发明提供一种盐酸替罗非班注射液有关物质检测方法。具体的,本发明采用如下技术方案:一种盐酸替罗非班注射液有关物质检测方法,采用hplc法进行检测,色谱条件如下:以十八烷基硅烷键合硅胶为色谱柱;流动相a为0.01mol/l磷酸二氢钾溶液(磷酸调节ph至2.5);流动相b为乙腈;等度洗脱条件如下:所述缓冲液中的无机盐为钾盐中的一种或多种,优选为磷酸二氢钾。所述缓冲液中无机盐的浓度为0.005mol/l~0.03mol/l,优选为0.005mol/l~0.015mol/l,更优选0.01mol/l。所述缓冲液ph的范围为2.0~3.0,优选为2.5。所述流动相b中有机溶剂为甲醇、乙腈中的一种或多种,更优选为乙腈。所述流动相为0.01mol/l磷酸二氢钾溶液-乙腈的混合溶液,二者体积比为68:32~75:25,优选70:30。等度洗脱条件如下:更优选的,所用柱温为30℃~40℃,优选为35℃。所用色谱柱为c18,apolloc18和agelavenusilmpc18,优选为agelavenusilmpc18,规格为4.6mm×250mm,5μm。所述流动相的流速为0.8ml/min~1.2ml/min,优选为1.0ml/min。进样量为20~50μl,优选为50μl。检测波长为222nm~240nm,更优选检测波长为227nm。进一步地,可将待测样品用溶剂稀释制成待测样品溶液,以浓度为25μg/ml。本发明方法可对存在的杂质进行有效分离并定量测定,从而有效控制产品的质量,专属性强,灵敏度高,准确度良好。附图说明图1供试品溶液高效液相色谱图(色谱柱agelavenusilmpc184.6×250mm5μm)图2供试品溶液高效液相色谱图(色谱柱apolloc184.6×250mm5μm)图3系统适用性试验溶液高效液相色谱图图4空白溶液高效液相色谱图图5供试品溶液高效液相色谱图图6供试品溶液(氧化破坏)高效液相色谱图图7自制制剂供试品溶液高效液相色谱图图8参比制剂供试品溶液高效液相色谱图具体实施方式以下是本发明的具体实施例,对本发明的技术方案做进一步作描述,但是本发明的保护范围并不限于这些实施例。本发明所使用的试剂均可以从市场上购得或者可以通过本发明所描述的方法制备而得。盐酸替罗非班对照品可在中国食品药品检定研究院购买。实施例1盐酸替罗非班注射液及制备制备方法为先将枸橼酸、枸橼酸钠溶于10~50%的水中制备成枸橼酸-枸橼酸钠缓冲液,然后将盐酸替罗非班、海藻酸钠溶于水中,两液混合;调节ph,然后过滤、分装、灭菌、灯检、包装即得。实施例2(对比实验1)采用进口药品注册标准(标准号:jx20080265)中有关物质检测方法,选择不同品牌的色谱柱测定实施例1所得盐酸替罗非班注射液,记录色谱图,如图1、图2。实施例3专属性试验系统适用性试验溶液:取盐酸替罗非班对照品与杂质a对照品适量,分别精密称定,加水稀释溶解并制成每1ml中约含替罗非班25μg,杂质a0.5μg的混合溶液,作为系统适用性试验溶液。空白溶液:量取空白辅料溶液5ml置25ml量瓶中,加水稀释至刻度,摇匀,滤过,取续滤液即得。取实施例1中的样品适量,用水稀释制成每1ml中约含替罗非班25μg的溶液,作为供试品溶液。供试品溶液(氧化破坏):精密量取样品溶液2ml,置20ml量瓶中,加10%的双氧水溶液2ml,混匀,95℃水浴加热30分钟,冷却,用水稀释至刻度,摇匀,滤过,即得。色谱条件:仪器:waterse2695检测器:dad检测器,检测波长为227nm色谱柱:agelavenusilmpc18,规格为4.6mm×250mm,5μm流速:1.0ml/min运行时间:40min柱温:35℃进样量:50μl流动相:0.01mol/l的磷酸二氢钾溶液(磷酸调节ph2.5):乙腈=70:30,等度洗脱分别注入系统适用性试验溶液、空白溶液、供试品溶液、供试品溶液(氧化破坏)测定,记录色谱图,检测图谱如图3、图4、图5、图6。实施例4精密度试验:精密称取盐酸替罗非班对照品和杂质a对照品适量,配制两者低浓度的混合溶液(约相当于供试品浓度的0.1%)、中浓度的混合溶液(约相当于供试品浓度的0.2%)、高浓度的混合溶液(约相当于供试品浓度的0.3%),按照实施条例4中的色谱条件进行检测,记录两种物质的峰面积,并计算其相对标准偏差(rsd)。实验结果见表1。表1杂质a及盐酸替罗非班精密度试验结果实施例5回收率实验:盐酸替罗非班对照品储备液的配制:取盐酸替罗非班对照品适量,精密称定,加水适量,超声溶解,稀释制成每1ml中约含替罗非班25μg的溶液,作为盐酸替罗非班对照品储备液①,精密量取上述储备液适量,加水稀释制成每1ml中约含替罗非班5μg的溶液,作为盐酸替罗非班对照品储备液②。杂质a对照品储备液的配制:取杂质a对照品适量,精密称定,加水适量,超声溶解,稀释制成每1ml中约含杂质a100μg的溶液,作为杂质a对照品储备液①,精密量取上述储备液适量,加水稀释制成每1ml中约含杂质a5μg的溶液,作为杂质a对照品储备液②。杂质对照品溶液:精密量取溶液稳定性项下盐酸替罗非班杂质a储备液②1ml,置100ml量瓶中,加水稀释至刻度,摇匀,即得。校正溶液:精密量取实施例1中的盐酸替罗非班注射液样品适量,用水稀释制成每1ml中约含替罗非班25μg的溶液,作为对比校正溶液。低浓度溶液:分别精密量取盐酸替罗非班杂质a储备液②0.25ml,置50ml量瓶中,加盐酸替罗非班注射液样品5ml,加水稀释至刻度,摇匀。同法配制三份。中浓度溶液:分别精密量取盐酸替罗非班杂质a储备液②0.50ml,置50ml量瓶中,加盐酸替罗非班注射液样品5ml,加水稀释至刻度,摇匀。同法配制三份。高浓度溶液:分别精密量取盐酸替罗非班杂质a储备液②0.75ml,置50ml量瓶中,加盐酸替罗非班注射液样品5ml,加水稀释至刻度,摇匀。同法配制三份。精密量取上述溶液各50μl,分别注入液相色谱仪,记录色谱图。采用外标法计算盐酸替罗非班杂质a的量,并将测得量扣除样品中已知的杂质量后与加入量进行比较,得到加样回收率,结果见表2。表2杂质a加样回收率试验结果实施例6定量限和检测限:取实施例5中的盐酸替罗非班对照品储备液②1.0ml,杂质a对照品储备液②1.0ml,置同一100ml量瓶中,用水稀释至刻度,摇匀,作为限度储备液,逐步稀释摸索定量限和检测限溶液浓度,结果见表3和表4。表3定量限试验结果表4检测限试验结果名称杂质a替罗非班峰面积246299s/n3.23.2浓度(μg/ml)0.003120.00317相当于供试品溶液(%)0.0120.013检测限(ng)0.1560.159实施例7样品检测:对照品溶液的配制:取盐酸替罗非班对照品适量,精密称定,加水溶解并稀释制成每1ml中约含替罗非班0.05μg的溶液,作为对照品溶液。供试品溶液的配制:取实施例1中的样品适量,用水稀释制成每1ml中约含替罗非班25μg的溶液,作为供试品溶液。取参比制剂的样品适量用水稀释制成每1ml中约含替罗非班25μg的溶液,作对比。分别精密量取对照品溶液和供试品溶液各50μl,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的3倍。供试品溶液的色谱图中如有杂质峰,按外标法以替罗非班峰面积计算,供试品溶液检测图谱为图7、图8,检测结果见表5。表5盐酸替罗非班注射液有关物质检测结果综上实施例1-7,经实施例2-3对比,本发明提供的盐酸替罗非班注射液有关物质检测方法具有更好的专属性。空白溶液对盐酸替罗非班注射液的有关物质检测无干扰,有关物质和盐酸替罗非班之间分离度良好。实施例4表明本发明提供的盐酸替罗非班注射液有关物质检测方法具有很好的精密度,3个浓度水平的杂质溶液,所得峰面积的相对标准偏差最大是3.40%,精密度良好。实施例5表明本发明提供的盐酸替罗非班注射有关物质检测方法准确度高,3个浓度水平的准确度溶液的回收率在96.55%~105.77%之间,平均回收率为100.8%,相对标准偏差为2.96%,符合中国药典的要求。实施例6表明本发明提供的盐酸替罗非班注射有关物质检测方法灵敏度高,检测限及定量限均能满足本品有关物质检查的要求。实施例7表明本发明提供的盐酸替罗非班注射液有关物质检测方法适用于检测盐酸替罗非班注射液的有关物质,灵敏度高,专属性强。总之,本发明提供的盐酸替罗非班注射液有关物质检测方法,具有操作简便、专属性强、精密度好和准确度高的特点,适合于盐酸替罗非班注射液有关物质的检测。本发明的方法已经通过较佳实施例进行了描述,相关人员明显能在本
发明内容、思路和范围内对本文所述的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1