一种人呼吸道病原体快速诊断的定量检测方法和试剂盒与流程
本发明属于病原体诊断
技术领域:
,具体涉及了一种人呼吸道病原体快速诊断的定量检测方法和试剂盒,以及该试剂盒的制备及使用方法。
背景技术:
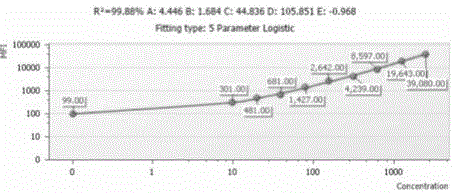
:呼吸道感染是我国最常见的传染性疾病,大多数由呼吸道病毒引起,可分为上呼吸道感染和下呼吸道感染,。流感病毒(ifv)、副流感病毒(piv)、腺病毒(hadv)、偏肺病毒(mpv)、冠状病毒(cov)、呼吸道合胞病毒(rsv)、鼻病毒(rhv)、肠道病毒(ev)、博卡病毒(hbov)、肺炎支原体、肺炎衣原体是常见的呼吸道病原体,因此快速检测病原体种类,对疾病的及时诊断、抗生素和抗病毒药物的合理使用和预防感染有着重要作用。流式细胞术是利用流式细胞仪快速定量分析细胞群的物理化学特征的技术,主要应用于检测外周血淋巴细胞及其亚群数量,监测hiv感染者疾病的进展;利用流式分选干细胞过继回输用于疾病的治疗,及其辅助白血病的诊断和分型。cba,微量样品多重蛋白定量技术,是基于流式细胞检测系统的多重蛋白定量检测方法。即利用微小、分散的颗粒微球捕获液体待测物,并利用流式细胞仪检测类似“三明治”的微球-待测物复合体所散发的荧光,从而测定待测物的数量。目前主要用于检测血液样本中的细胞因子、炎症因子的水平分析。目前呼吸道病毒感染诊断的金标准仍是病毒的的分离培养,但是细胞培养方法周期长,运输和储存易感染,实际应用受到限制。玻片直接免疫荧光法,则需要通过肉眼观察绿色荧光细胞的数量来判定结果,因此结果的判定具有主观性,且一次只能用单一荧光素标记的抗体,故一次只能鉴定一种病原体,检测效率低。目前市面上的利用流式细胞术检测呼吸道病原体的技术和产品主要是通过固体液固定住细胞,利用通透剂对细胞内的病毒进行荧光染色,染色效率受通透率影响大,还不能定量分析。技术实现要素:本发明提供了一种人呼吸道原体快速诊断的定量检测方法和试剂盒,以及该试剂盒的制备及使用方法。本发明检测快速准确,灵敏度高、重复性好,并且操作简便、自动化,可实现单样本的多重定量检测,且检测对象可灵活组合,能更真实的反映病原体的感染情况。本发明是通过以下技术方案来实现的:一种基于流式细胞检测和微量多重蛋白定量检测的人呼吸道病原体快速诊断和检测的方法,其特征在于:所述方法包括以下步骤:1)呼吸道病原体抗体和捕捉微球的共价耦合:将标记有apc荧光素的聚苯乙烯微球分别与人呼吸道病原体抗体偶联(其中人呼吸道病原体包括呼吸道合胞病毒、甲型流感病毒、乙型流感病毒、腺病毒、副流感病毒1型、副流感病毒2型和副流感病毒3型、偏肺病毒、博卡病毒、冠状病毒、鼻病毒、肠道病毒、支原体或衣原体),制得人呼吸道病原体抗体捕获微球;不同抗体结合的微球apc荧光强度不同,通过apc荧光强度可识别不同的病原体抗体。2)检测抗体的荧光标记:用pe荧光素标记检测抗体,所述检测抗体与捕获抗体为配对抗体。3)标准曲线的制备:将等比稀释的0-5000不同浓度的标准品蛋白与捕捉微球和检测抗体等体积混合后,室温避光孵育反应,加入清洗液后,将该复合物置于流式细胞仪,检测pe通道荧光强度,通过fsc和ssc确定微球位置后,再通过荧光强度的不同判定病原体的种类,分别绘制不同病原体蛋白的标准曲线,其中,曲线坐标为病原体浓度和检测平均荧光强度(mfi)。4)待测样品处理和检测:使用咽拭子收集呼吸道上皮细胞,将咽拭子放入含培养基的采样管中,4℃保存;检测时涡旋振荡采样管,取出拭子,离心后,小心吸去上清,加入4℃预冷的细胞裂解液,至细胞裂解完全,离心取上清,加入抗体捕获微球和pe检测抗体,混合孵育后,上流式细胞仪检测。5)检测结果分析:根据微球自带的apc和apc-cy7两种荧光,分别在apc和apc-cy7通道检测,通过二位矩阵识别捕获微球,确定微球的位置,划分微球门,再根据pe标记的检测抗体在pe通道来对目的病原体定量。6)检测法临界值的判定:分别检测30份阴性样本咽拭子的值,统计并计算出该样本的平均值和标准差。根据统计学原则,当样本值大于阴性样本值的平均值与3倍标准差之和时,便可在99%的水平上判定为阳性,计算出阴阳性临界值。一种基于流式细胞检测和微量多重蛋白定量检测的人呼吸道病原体快速诊断及检测试剂盒,包括人呼吸道病原体抗体的一种或多种组合捕捉微球,pe标记的检测抗体试剂(一种或多种组合),标准品蛋白(一种或多种组合),流式细胞仪校准微球,样品缓冲液,微球缓冲液,细胞裂解液,清洗液。其中所述的呼吸道病原体包括呼吸道合胞病毒、甲型流感病毒、乙型流感病毒、腺病毒、副流感病毒1型、副流感病毒2型和副流感病毒3型、偏肺病毒、博卡病毒、冠状病毒、鼻病毒、肠道病毒、支原体或衣原体中的至少一种。一种用于制备基于流式细胞检测和微量多重蛋白定量检测的人呼吸道病原体快速诊断及检测的试剂盒的方法,其特征在于:所述方法包括以下步骤:1)人呼吸道病原体抗体的捕捉微球制备:1.1)溶液配制buffera的配制:称取0.96g磷酸氢二钠,加去离子水600ml溶解,调节ph至6.0,再加水定容至800ml,0.45μm水系过滤膜过滤;bufferb的配制:称取甘氨酸7.5g,加水800ml溶解,调节ph至7.5,再加水定容至1000ml,0.45um水系过滤膜过滤;50mg/ml1-(3-二甲基氨基丙基)-3-乙基-碳二亚胺盐酸盐(edc)溶液配制:称取1gedc,加入50ml水溶解,0.45μm水系过滤膜过滤;1.2)微球共价结合抗体1.2.1)使用buffera悬浮标有apc荧光素的微球,使微球浓度为1%w/v1.2.2)每1ml微球悬液中加入20mg的edc,室温孵育20min,再加入20mg/ml的edc,室温孵育20min1.2.3)1000rpm/min离心5min,弃上清,加入等体积的bufferb缓冲液,反复清洗微球两次1.2.4)使用500ulbufferb重悬微球1.2.5)使用bufferb缓冲液溶解病原体抗体,至终浓度为1mg/ml1.2.6)将抗体加入微球缓冲液中,涡旋混匀,室温,避光孵育2-4h,1.2.7)使用微球缓冲液将标记后的微球抗体偶联物清洗两次后,重悬保存。2)检测抗体的荧光素标记:2.1)将5-10mg活化处理的荧光素pe,使用脱盐柱置换到ph6.0反应缓冲液中,调节浓度至5-10mg/ml,体积为1ml。2.2)取活化抗体0.8ml,加入活化pe溶液0.571ml,再加入0.137ml苯胺溶液。混匀后,避光,置于旋转混合仪上2h。2.3)用akta蛋白纯化仪进行纯化,用0.5倍柱体积的超声脱气纯化水进行平衡,流速为0.5-1ml/min,再用约1.5倍柱体积的0.05m洗脱缓冲液平衡,流速为0.5-1ml/min,上样,后用0.05洗脱缓冲液洗脱,收集所需峰值附近液体。2.4)使用紫外可见分光光度计检测抗体浓度和抗体量,得到检测抗体3)微球缓冲液:量取0.5-3.0%胎牛血清,0.1%-10%的吐温-20,0.05%-0.1%的叠氮化钠,加入到ph7.0-8.0的0.1mpbs缓冲液,混合均匀,0.45um水系过滤膜过滤.4)细胞裂解液:150mmnacl1%np-40,0.1%sds,2μlg/mlaprotinin,1mmpmsf,1.5mmedta,1mmnavanadate以上所有试剂均按比例溶于150mmnacl溶液中。5)清洗液:称取1%-5%的bsa,0.1-2.0%nan3,加入到phph7.0-8.0的0.1mpbs缓冲液中,混合均匀,0.45um水系过滤膜过滤。本发明相比现有技术具有以下优点:1、本发明利用捕获微球提供特定蛋白的捕获表面,捕获病原体抗体后呈悬浮态,能更有效捕获分析物,同时结合fcm的宽范围荧光检测特点,对样本需求量更少,检测更快速、更准确。2、本发明可同时对一个样本的多个病原体抗体进行精确定量,能够从多种呼吸道病原体中快速检测出感染的病原体种类,实现单样本多重检测,并且灵敏度高、检测范围广、重复性好。针对不同临床表现,检测对象可灵活组合,真实反映病原体的感染情况。3、操作简单,节省时间,软件自动分析,结果客观准确。附图说明图1为rsv标准曲线,其横坐标为细胞因子浓度(单位pg/ml),纵坐标为平均荧光强度值(mfi),图中各个点所标识的数字,为该检测浓度所对应的mfi;图2为adv标准曲线,其横坐标为细胞因子浓度(单位pg/ml),纵坐标为平均荧光强度值(mfi),图中各个点所标识的数字,为该检测浓度所对应的mfi;图3为ia标准曲线,其横坐标为细胞因子浓度(单位pg/ml),纵坐标为平均荧光强度值(mfi),图中各个点所标识的数字,为该检测浓度所对应的mfi;图4为ib标准曲线,其横坐标为细胞因子浓度(单位pg/ml),纵坐标为平均荧光强度值(mfi),图中各个点所标识的数字,为该检测浓度所对应的mfi。具体实施方式本方法是利用已知体积和荧光强度的微球捕获呼吸道病原体抗体,形成微球-病原体-检测抗体“三明治”夹心复合物,结合流式细胞仪宽范围荧光检测特点,建立了一种人呼吸道原体快速诊断及定量检测方法,从而达到早期诊断和检测呼吸道感染的目的。相对传统的elisa和流式检测,具有特异性强,灵敏度高,可实现单样本多重检测等优势。本发明通过以下实施例做进一步具体描述。实施例一:人呼吸道病原体快速诊断及检测试剂盒包括人呼吸道病原体rsv抗体捕捉微球,pe标记检测抗体试剂,rsv重组蛋白标准品,流式细胞仪校准微球,样品缓冲液,微球缓冲液,裂解液,清洗液。其中所述的呼吸道病原体还包括呼吸道合胞病毒(rsv)、甲型流感病毒(ia)、乙型流感病毒(ib)、腺病毒(adv)、副流感病毒1型、副流感病毒2型和副流感病毒3型、偏肺病毒、博卡病毒、冠状病毒、鼻病毒、肠道病毒、支原体或衣原体中的至少一种。实施例二:人呼吸道病原体检测试剂盒的制备本实施例为人呼吸道病原体单项rsv抗体检测试剂盒的制备,按如下步骤进行:1、rsv抗体捕获微球的制备1)溶液配制buffera的配制:称取0.96g磷酸氢二钠,加去离子水600ml溶解,调节ph至6.0,再加水定容至800ml,0.45um水系过滤膜过滤;bufferb的配制:称取甘氨酸7.5g,加水800ml溶解,调节ph至7.5,再加水定容至1000ml,0.45um水系过滤膜过滤;20mg/ml1-(3-二甲基氨基丙基)-3-乙基-碳二亚胺盐酸盐(edc)溶液配制;称取1gedc,加入50ml水溶解,0.45um水系过滤膜过滤;1.2)微球共价结合抗体1.2.1)使用buffera悬浮标有apc荧光素的微球,使微球浓度为1%w/v1.2.2)每1ml微球悬液中加入20mg/ml的edc20μl,室温孵育20min1.2.3)1000rpm/min离心5min,弃上清,加入等体积的bufferb缓冲液,反复清洗微球两次1.2.4)使用500ulbufferb重悬微球1.2.5)使用bufferb缓冲液溶解rsv抗体,至终浓度为1mg/ml1.2.6)将抗体加入微球缓冲液中,涡旋混匀,室温,避光孵育2-4h1.2.7)使用微球缓冲液将标记后的微球抗体偶联物清洗两次后,重悬保存2、检测抗体的荧光素标记取1-5mg活化处理的检测抗体(与捕捉抗体为配对抗体),使用超滤管将其置换到ph6.0反应缓冲液中,调节浓度至2-3mg/ml,体积为0.8ml,2.1)将5-10mg活化处理的荧光素pe,使用脱盐柱置换到ph6.0反应缓冲液中,调节浓度至5-10mg/ml,体积为1ml;2.2)取活化抗体0.8ml,加入活化pe溶液0.571ml,再加入0.137ml苯胺溶液。混匀后,避光,置于旋转混合仪上2h;2.3)用akta蛋白纯化仪进行纯化,用0.5倍柱体积的超声脱气纯化水进行平衡,流速为0.5-1ml/min,再用约1.5倍柱体积的0.05m洗脱缓冲液平衡,流速为0.5-1ml/min,上样,后用0.05洗脱缓冲液洗脱,收集所需峰值附近液体;2.4)使用紫外可见分光光度计检测抗体浓度和抗体量,得到检测抗体pe-svr3、微球缓冲液的制备:量取0.5-3.0%胎牛血清,0.1%-10%的吐温-20,0.05%-0.1%的叠氮化钠,加入到ph7.0-8.0的0.1mpbs缓冲液,混合均匀,0.45um水系过滤膜过滤4、细胞裂解夜:150mmnacl1%np-40,0.1%sds,2μg/mlaprotinin,1mmpmsf,1.5mmedta,1mmnavanadate以上所有试剂均按比例溶于150mmnacl溶液中。实施例三:人呼吸道病原体快速诊断及检测方法本实施例为利用实施例二中制备的试剂盒进行单项病原体(rsv)检测的方法,按如下步骤进行:1、标准曲线的绘制:取人重组rsv抗体标准品,加入2ml样品缓冲液,室温静置15min,使用移液枪轻轻吹打混匀标准品,此时标准品的浓度为每毫升5000个病毒量;取10根流式上样管,分别标记梯度稀释的倍数为1/2,1/4,1/8,1/16,1/32,1/64,1/128/,1/256,0;每管各加入200μl的样品缓冲液,从标准品管中取200ul液体到1/2管中,吹打混匀后取200μl液体到1/4管中,依次类推至1/256管;取实施例二中制备的rsv抗体捕获微球50ul,混匀后200g离心5min,吸去上清,加入250μl微球缓冲,室温避光孵育30min;分别取25ul梯度稀释的标准品,各加入25μlrsv抗体捕获微球,25ulpe检测抗体,轻轻混合均匀,室温避光孵育2.5h,每管加入500μl清洗液,200g离心5min,吸去上清,加入150μl清洗液重悬,上流式细胞仪检测。2、样本的处理及检测:口咽拭子采集:使用一次性压舌板将舌压下,暴露患者咽喉,取口试子迅速轻柔的擦拭两腭弓、咽喉及扁桃体至少3次,将拭子头浸入3ml采样液中,把拭子头部与管壁接触几下,使标本尽量多的保存在采样液中,弃去拭子手捏尾部部分。将所述采样管正立置于4℃保存;将上述采样管涡旋振荡10-20s,取出拭子,500g离心7min,小心吸去上清,加入100μl4℃预冷的细胞裂解液,手指轻弹以充分裂解细胞,4℃静置10min,至细胞裂解完全,5000g离心5min,取上清25μl,加入25μl抗体捕获微球,25ulpe检测抗体,轻轻混合均匀,室温避光孵育2.5h,每管加入500μl清洗液,200g离心5min,吸去上清,加入150μl清洗液重悬,上流式细胞仪检测。3、检测结果如下:根据rsv重组抗体标准品绘制的标准曲线如图1,可以计算出rsv病原体的值,其中标本为采自10位临床疑似呼吸道病原体rsv感染患者的口试子,其检测结果如表1。4、rsv检测法临界值的判定:分别检测30份临床诊断阴性样本咽拭子的值,统计并计算出该样本的平均值和标准差。根据统计学原则,当样本值大于阴性样本值的平均值与3倍标准差之和时,便可在99%的水平上判定为阳性;计算出rsv≤15.9时,为rsv阴性,反之为阳性。根据此判断,10份检测样本测定值均大于15.9,均为rsv阳性,与临床诊断结果一致。实施例四:多项呼吸道病原体组合检测方法本实施例为基于流式细胞检测和微量多重蛋白定量检测的多项人呼吸道病原体组合检测的实验。本实施例所用的人呼吸道病原体快速诊断及检测试剂盒与实施例一中的组成大部分相同,不同的是病原体抗体捕捉微球,检测二抗及标准品不同。本实例具体的试剂盒中,病原体抗体捕捉微球为:rsv抗体捕捉微球、ia抗体捕捉微球、adv抗体捕捉微球及ib抗体捕捉微球,各自对应的pe检测二抗混合液,及rsv、ia、ib、adv重组蛋白标准品,检测方法如下:1、标准曲线的绘制:取人重组rsv、ia、ib、adv抗体标准品,加入2ml样本缓冲液混匀,室温静置15min,使用移液枪轻轻吹打混匀标准品,此时标准品的浓度为每毫升5000个病毒量;取10根流式上样管,分别标记标记梯度稀释的倍数为1/2,1/4,1/8,1/16,1/32,1/64,1/128/,1/256,0;每管各加入200μl的实验稀释液,从标准品管中取200μl液体到1/2管中,吹打混匀后取200μl液体到1/4管中,依次类推至1/256管;取rsv、ia、ib、adv抗体混合捕获微球50μl,混匀后200g离心5min,吸去上清,加入250μl微球缓冲,室温避光孵育30min;分别取25μl梯度稀释的标准品,各加入25μl抗体捕获微球,25μlpe检测抗体,轻轻混合均匀,室温避光孵育2.5h,每管加入500μl清洗液,200g离心5min,吸去上清,加入150μl清洗液重悬,上流式细胞仪检测。2、样本的处理及检测:口咽拭子采集:使用一次性压舌板将舌压下,暴露患者咽喉,取口试子迅速轻柔的擦拭两腭弓、咽喉及扁桃体至少3次,将拭子头浸入3ml采样液中,把拭子头部与管壁接触几下,使标本尽量多的保存在采样液中,弃去拭子手捏尾部部分。将所述采样管正立置于4℃保存;将上述采样管涡旋振荡10-20s,取出拭子,500g离心7min,小心吸去上清,加入100ul4℃预冷的细胞裂解液,手指轻弹以充分裂解细胞,4℃静置10min,至细胞裂解完全,5000g离心5min,取上清25μl,加入25μl抗体捕获微球,25μlpe检测抗体,轻轻混合均匀,室温避光孵育2.5h,每管加入500ul清洗液,200g离心5min,吸去上清,加入150μl清洗液重悬,上流式细胞仪检测。3、检测结果如下:根据rsv、ia、ib、adv重组抗体标准品绘制的标准曲线如图1-图4,可以计算出各病原体的值,其中检测标本为采自10位临床诊断呼吸道病原体感染患者的口试子,其检测结果如表1-表5。4、rsv检测法临界值的判定:分别检测rsv、ia、ib、adv各30份临床诊断阴性样本咽拭子的值,计算出各病原体阴性判断区间为rsv≤15.9,ia≤8.64,ib≤17.5,adv≤22.56。根据此判断,10份检测样本中rsv阳性1例,adv阳性1例,ia阳性6例,ib阳性2例,与临床诊断结果一致。nameplatepositionnominalccfittedccfinalccstd0011-a10.000.000.00std0021-a29.778.028.02std0031-a319.5317.9717.97std0041-a439.0638.0838.08std0051-a578.1375.5675.56std0061-a6156.25153.38153.38std0071-a7312.50310.26310.26std0081-a8625.00638.11638.11std0091-a91,250.001,224.981,224.98std0101-a102,500.002,508.122,508.12test0011-b1n/a119.7119.7test0021-b2n/a41.2341.23test0031-b3n/a22.4222.42test0041-b4n/a37.0037.00test0051-b5n/a554.1554.1test0061-b6n/a218.47218.47test0071-b7n/a30.7930.79test0081-b8n/a319.2319.2test0091-b9n/a22.3122.31test0101-b10n/a172.00172.00表1本实施例的方法检测的rsv值nameplatepositionnominalccfittedccfinalccstd0011-a10.000.000.00std0021-a29.778.028.02std0031-a319.5317.9717.97std0041-a439.0638.0838.08std0051-a578.1375.5675.56std0061-a6156.25153.38153.38std0071-a7312.50310.26310.26std0081-a8625.00638.11638.11std0091-a91,250.001,224.981,224.98std0101-a102,500.002,508.122,508.12test0011-b1n/a1.351.35test0021-b2n/a0.000.00test0031-b3n/a10.3110.31test0041-b4n/a110.82110.82test0051-b5n/a0.000.00test0061-b6n/a0.000.00test0071-b7n/a1.251.25test0081-b8n/a0.000.00test0091-b9n/a0.000.00test0101-b10n/a0.000.00表2本实施例的方法检测的rsv值nameplatepositionnominalccfittedccfinalccstd0011-a10.000.000.00std0021-a29.776.516.51std0031-a319.5318.8518.85std0041-a439.0633.6133.61std0051-a578.1378.3578.35std0061-a6156.25151.65151.65std0071-a7312.50320.91320.91std0081-a8625.00613.63613.63std0091-a91,250.001,233.521,233.52std0101-a102,500.002,524.012,524.01test0011-b1n/a0.000.00test0021-b2n/a0.000.00test0031-b3n/a0.000.00test0041-b4n/a0.000.00test0051-b5n/a32.5732.57test0061-b6n/a0.000.00test0071-b7n/a0.000.00test0081-b8n/a0.000.00test0091-b9n/a0.000.00test0101-b10n/a0.000.00表3本实施例的方法检测adv值nameplatepositionnominalccfittedccfinalccstd0011-a10.000.000.00std0021-a29.777.457.45std0031-a319.5320.8420.84std0041-a439.0629.8929.89std0051-a578.1379.8879.88std0061-a6156.25146.54146.54std0071-a7312.50337.27337.27std0081-a8625.00660.31660.31std0091-a91,250.001,078.731,078.73std0101-a102,500.002,649.572,649.57test0011-b1n/a0.000.00test0021-b2n/a13.7513.75test0031-b3n/a24.8024.80test0041-b4n/a0.000.00test0051-b5n/a0.000.01test0061-b6n/a311.26311.26test0071-b7n/a0.000.00test0081-b8n/a121.77121.77test0091-b9n/a71.1471.14test0101-b10n/a35.3935.39表4本实施例的方法检测ia值nameplatepositionnominalccfittedccfinalccstd0011-a10.000.000.00std0021-a29.776.626.62std0031-a319.5315.2615.26std0041-a439.0637.5037.50std0051-a578.1374.9374.93std0061-a6156.25159.09159.09std0071-a7312.50306.39306.39std0081-a8625.00600.50600.50std0091-a91,250.001,252.371,252.37std0101-a102,500.002,524.552,524.55test0011-b1n/a39.539.5test0021-b2n/a0.000.00test0031-b3n/a0.000.00test0041-b4n/a1.221.22test0051-b5n/a0.000.00test0061-b6n/a1.651.65test0071-b7n/a411.56411.56test0081-b8n/a3.13.1test0091-b9n/a0.000.00test0101-b10n/a0.000.0表5本实施例的方法检测ib值。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1