一种沉积物中喹诺酮类抗生素的超高效液相色谱串联质谱检测方法与流程
1.本发明涉及沉积物污染检测技术领域,尤其是涉及一种沉积物中喹诺酮类抗生素的超高效液相色谱串联质谱检测方法。
背景技术:
2.喹诺酮类抗生素作为一种广泛应用于预防或治疗动物和人类传染病的药物,由于其在环境中的耐药性会对水生生态系统和人类健康造成不良影响而日益受到关注。因此,分析喹诺酮类抗生素的赋存、分布和风险成为环境监测的重要内容。然而,由于沉积物样品的复杂性、以及沉积物对喹诺酮类抗生素的强吸附性,准确地进行沉积物中喹诺酮类抗生素残留检测是一项艰巨的任务。
3.近年来,结合紫外、荧光、质谱或串联质谱的高效液相色谱法、毛细管电泳法等仪器分析技术,常用于沉积物中喹诺酮类抗生素的测定。由于喹诺酮类抗生素的含量相对较低和沉积物基体的复杂性,因此为提高灵敏度及分析结果的准确性,必须对沉积物样品进行前处理。
4.现有对沉积物的样品前处理方法主要是用单一有机溶剂(常用乙腈或甲醇)或混合溶剂(常用乙腈或甲醇与缓冲溶液和edta的混合液)进行萃取,也会同时采用超声辅助萃取、微波辅助萃取或加压流体萃取等技术提升萃取效率,萃取完成后则需要再加入200~500ml超纯水进行固相萃取。单一有机溶剂或混合溶剂对实际样品中的诺氟沙星、依诺沙星、环丙沙星、培氟沙星、恩诺沙星、氧氟沙星等萃取效果很差甚至不能萃取出来,不能反映样品的真实检出情况;同时,萃取完成后,加入200~500ml超纯水进行固相萃取,一方面对超纯水的需求量增加,另一方面大大增加了固相萃取时间(需要》130min),最重要的是,沉积物样品中对喹诺酮类抗生素的检测存在较为明显的基质效应,使得分析结果的准确性较低。
5.在大多数文献报道中,在分析多个抗生素时,只有少量的几种同位素标记内标用于基质效应的校正,这会导致某些化合物的回收率过高或过低。
6.因此,开发有效的沉积物中喹诺酮类抗生素前处理技术和检测技术是十分必要的。
技术实现要素:
7.本发明是为了解决现有技术的沉积物中喹诺酮类抗生素检测方法所存在的上述问题,提供了一种能快速完成样品前处理,操作简单,具有较高的灵敏度机准确性、令人满意的回收率及重现性的沉积物中喹诺酮类抗生素的超高效液相色谱串联质谱检测方法。
8.为了实现上述目的,本发明采用以下技术方案:本发明的一种沉积物中喹诺酮类抗生素的超高效液相色谱串联质谱检测方法,包括以下步骤:
9.(1)制样
10.将沉积物样品冷冻干燥后,研磨过筛,冷藏,得待测样品。
11.(2)超声提取
12.精密称取2.00g待测样品,加入15种喹诺酮类抗生素的同位素内标及5ml甲醇,涡旋、避光静置后,加入10ml提取剂,超声提取后,高速离心,取上清液,得一次提取液;再向提取液中加入10ml提取剂,重复上述过程,得二次提取液;将一次提取液和二次提取液合并,得混合提取液;15种喹诺酮类抗生素的同位素内标为恶喹酸-d5、氟甲喹-13
c3、诺氟沙星-d5、依诺沙星-d8、环丙沙星-d8、培氟沙星-d5、洛美沙星-d5、丹诺沙星-d3、恩诺沙星-d5、氧氟沙星-d3、氟罗沙星-d3、沙拉沙星-d8、司帕沙星-d4、奥比沙星-d4、双氟沙星-d3,15种喹诺酮类抗生素的同位素内标的加入量分别为12ng。合适的同位素内标可以弥补样品前处理、色谱进样及分离、离子化和检测中产生的误差,校正基质效应的影响,进行多分析物检测时,为每个分析物挑选合适的同位素内标可确保检测结果准确性,故本发明中选择上述15种同位素内标。在提取剂选择时,发明人分别考察了甲醇、乙腈、体积比为1:1的乙腈/mcilvaine缓冲液(ph=4)、体积比为1:1的甲醇/mcilvaine缓冲液(ph=4)、体积比为1:1的乙腈/edta-mcilvaine缓冲液(ph=4)、体积比为1:1的乙腈/0.2mol/l磷酸氢二钠溶液共六种萃取剂的提取效果,结果表明,体积比为1:1的乙腈/0.2mol/l磷酸氢二钠溶液的提取效果最好,外标法回收率为10.96%~69.51%,经同位素内标校正后,内标法回收率为77.08%~119.76%;体积比为1:1的乙腈/edta-mcilvaine缓冲液(ph=4)的萃取效果次之,外标法回收率为4.07%~66.13%,且诺氟沙星、依诺沙星、环丙沙星、培氟沙星、达诺沙星、恩诺沙星、氧氟沙星、氟罗沙星的外标法回收率均小于10%,内标法回收率为78.91%~128.88%;而其他提取剂对诺氟沙星、依诺沙星、环丙沙星、培氟沙星、丹诺沙星、恩诺沙星、氧氟沙星、氟罗沙星的萃取效果均极差,外标法回收率均《1%;因此本发明选择体积比为1:1的乙腈/0.2mol/l磷酸氢二钠溶液作为提取剂;同时为了保证15种喹诺酮类抗生素的同位素内标充分、均匀地被沉积物吸附,在一次提取时加入5ml甲醇,并静置至少1h。
13.(3)浓缩和稀释
14.将混合提取液在50℃水浴条件下,用氮气吹扫除去甲醇和乙腈后用稀释液稀释至45ml,得萃取稀释液。
15.(4)全自动固相萃取
16.对萃取稀释液进行全自动固相萃取,得洗脱液。
17.(5)浓缩定容
18.将洗脱液在50℃水浴条件下,氮气吹干,用初始流动相溶解后定容至600μl,有机相滤膜过滤,得上机溶液。
19.(6)超高效液相色谱-串联质谱检测
20.用进样针抽取上机溶液,按已设定的超高效液相色谱-串联质谱检测条件进行上样检测,得上机溶液的离子流色谱图。
21.(7)标准曲线绘制
22.采用mass-lynx软件4.1和计算机进行数据采集和处理,用多反应监测模式和保留时间进行定性:取浓度为1mg/l的恶喹酸、氟甲喹、诺氟沙星、依诺沙星、环丙沙星、培氟沙星、洛美沙星、丹诺沙星、恩诺沙星、氧氟沙星、氟罗沙星、沙拉沙星、司帕沙星、奥比沙星、双氟沙星的喹诺酮混合标准使用液12μl,以及与上述15种喹诺酮类抗生素相对应的1mg/l的
恶喹酸-d5、氟甲喹-13
c3、诺氟沙星-d5、依诺沙星-d8、环丙沙星-d8、培氟沙星-d5、洛美沙星-d5、丹诺沙星-d3、恩诺沙星-d5、氧氟沙星-d3、氟罗沙星-d3、沙拉沙星-d8、司帕沙星-d4、奥比沙星-d4、双氟沙星-d3的喹诺酮同位素内标混合溶液12μl,用初始流动相定容至0.6ml,得到标准工作液;将标准工作液按照上述步骤(6)的步骤进行操作,得标准工作液的离子流色谱图;将标准工作液的离子流色谱图与单种喹诺酮类抗生素和与之相对应的同位素内标的离子流色谱图进行定性离子、定量离子比较,同时结合保留时间,确定15种喹诺酮类抗生素;该15种喹诺酮类抗生素的定性离子、定量离子、保留时间和相对应的15种同位素内标的定量离子、保留时间用以作为同位素标记内标法定量时识别15种喹诺酮类抗生素色谱峰识别的依据;
23.用同位素标记内标法进行定量:同时取浓度为1μg/l的喹诺酮混合标准使用液30μl、浓度10μg/l的喹诺酮混合标准使用液60μl、浓度100μg/l的喹诺酮混合标准使用液30、120、300μl以及浓度1000μg/l的喹诺酮混合标准使用液60μl,分别加入与之对应的1mg/l的喹诺酮同位素内标混合溶液12μl,再分别用初始流动相定容至0.6ml,得到六次加标浓度范围均为0.05~100μg/l,且同位素内标浓度均为20μg/l的标准曲线系列溶液;将六种不同加标浓度的标准曲线系列溶液,根据加入的喹诺酮浓度和相应定量离子积分峰面积与对应同位素内标的定量离子积分峰面积的比值的对应关系建立标准曲线。
24.(8)样品分析
25.将步骤(6)中得到的上机溶液的离子流色谱图中的喹诺酮类抗生素的相应定量峰面积与相对应同位素内标的定量峰面积的比值,与步骤(7)中建立的标准曲线进行比较,通过换算即可得到样品中15种喹诺酮的实际含量。
26.作为优选,步骤(1)中,冷冻干燥后的沉积物样品研磨后过80~100目筛,于-18℃保藏。
27.作为优选,步骤(2)中,所述萃取剂为乙腈和0.2mol/l磷酸氢二钠溶液的混合液,乙腈和0.2mol/l磷酸氢二钠溶液的体积比为1:1;超声条件为:功率300w,温度38℃,提取时间10min;高速离心条件为:转速8000rpm,离心6min。
28.作为优选,步骤(3)中,所述稀释液为氯化钠/乙二胺四乙酸二钠二水合物的水溶液,稀释液通过以下方法制得:将15g氯化钠、0.25g乙二胺四乙酸二钠二水合物,溶于超纯水中并定容至500ml,加入浓盐酸调节ph为3。在稀释液选择时,发明人分别考察了不加稀释液、加超纯水、加氯化钠/乙二胺四乙酸二钠二水合物的水溶液对实验结果的影响,结果表明,加氯化钠/乙二胺四乙酸二钠二水合物的水溶液的提取效果最好,外标法回收率为10.96%~69.51%,经同位素内标校正后,内标法回收率为77.08%~119.76%;加超纯水和不加稀释水的萃取效果差不多,外标法回收率分别为3.35%~70.83%和2.24%~64.31%,且诺氟沙星、依诺沙星、洛美沙星的外标法回收率均小于10%,内标法回收率分别为57.82%~121.42%和48.09%~130.84%。
29.作为优选,步骤(4)中,采用全自动固相萃取仪进行全自动固相萃取,具体方法为:将cnw poly-sery hlb小柱,柱规格为500mg,6ml,依次用10ml甲醇和10ml、ph为3的超纯水进行活化,再以30s浸泡模式上样,上样结束后,用15ml、ph为3的超纯水分三次淋洗cnw poly-sery hlb小柱,在氮气流下干燥15min,最后用8ml甲醇洗脱,得到洗脱液。采用全自动固相萃取仪进行全自动固相萃取,整个过程只要28~30min,且可同时处理6个样品;ph为3
的超纯水,ph采用浓盐酸调节。
30.作为优选,步骤(5)中,所述初始流动相为乙腈和0.1%甲酸的mmol/l乙酸铵溶液的混合液,乙腈和0.1%甲酸的2mmol/l乙酸铵溶液的体积比1:9;0.22μm有机相滤膜过滤。
31.作为优选,步骤(6)中,色谱条件为:waters acquity uplc beh c18色谱柱,柱规格为2.1mm
×
100mm,1.7μm;柱温35℃,样品室温度10℃;进样量为5μl;流速为0.3ml/min;采用二元梯度洗脱,流动相a为0.1%甲酸的2mmol/l乙酸铵溶液,b为乙腈,梯度洗脱程序:0~1.5min,90%a;1.5~6.5min,90%~87.5%a;6.5~9.5min,87.5%~70%a;9.5~10.5min,70%~60%a;10.5~10.7min,60%~10%a;10.7~11.5min,10%a;11.5~11.8min,10%~90%a;11.8~15min,90%a。
32.作为优选,步骤(6)中,质谱条件为:电喷雾正电子(esi+)模式电离,多反应监测模式检测;离子源温度:150℃;脱溶剂气温度:600℃;毛细管电压:3.0kv;锥孔气流量:150l/h;脱溶剂气流量:800l/h。
33.作为优选,步骤(7)中,初始流动相为乙腈和0.1%甲酸的2mmol/l乙酸铵溶液的混合液,乙腈和0.1%甲酸的2mmol/l乙酸铵溶液的体积比1:9。
34.因此,本发明具有如下有益效果:以体积比为1:1的乙腈/0.2mol/l磷酸氢二钠溶液作为提取剂进行超声波提取、浓缩和稀释、全自动固相萃取、超高效液相色谱-串联质谱法测定沉积物中的喹诺酮类抗生素,操作简单,能快速完成沉积物样品前处理,其中全自动固相萃取过程只需要28~30min/6个样品,结果准确,15种抗生素检出限为0.002~0.015ng/g,回收率为82%~119%,相对标准偏差(n=5)为1.8~12.5%,具有较高的灵敏度和令人满意的回收率及重现性,适合用于沉积物中喹诺酮类抗生素的含量测定。
附图说明
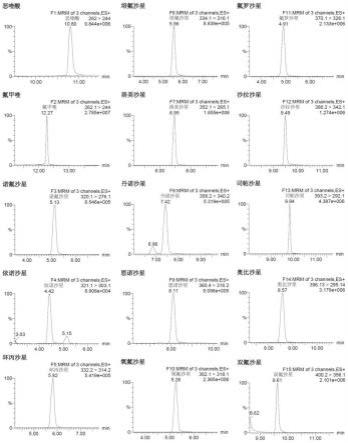
35.图1是浓度为20μg/l的15种喹诺酮类抗生素定量离子离子流色谱图。
36.图2是浓度为20μg/l的15种喹诺酮类抗生素定性离子离子流色谱图。
37.图3是浓度为20μg/l的15种同位素内标定量离子离子流色谱图。
具体实施方式
38.下面结合附图和具体实施方式对本发明做进一步的描述。
39.实施例1
40.舟山海域采集的沉积物样品中喹诺酮类抗生素检测
41.(1)制样
42.将沉积物样品冷冻干燥后,研磨过100目筛,-18℃冷藏,得待测样品。
43.(2)超声提取
44.精密称取2.00g待测样品,加入15种喹诺酮类抗生素的同位素内标及5ml甲醇,涡旋、避光静置后,加入10ml提取剂,超声提取后,高速离心,取上清液,得一次提取液;再向提取液中加入10ml提取剂,重复上述过程,得二次提取液;将一次提取液和二次提取液合并,得混合提取液;15种喹诺酮类抗生素的同位素内标为恶喹酸-d5、氟甲喹-13
c3、诺氟沙星-d5、依诺沙星-d8、环丙沙星-d8、培氟沙星-d5、洛美沙星-d5、丹诺沙星-d3、恩诺沙星-d5、氧氟沙星-d3、氟罗沙星-d3、沙拉沙星-d8、司帕沙星-d4、奥比沙星-d4、双氟沙星-d3,15种喹诺酮类
抗生素的同位素内标的加入量分别为12ng;提取剂为乙腈和0.2mol/l磷酸氢二钠溶液的混合液,乙腈和0.2mol/l磷酸氢二钠溶液的体积比为1:1;超声条件为:功率300w,温度38℃,提取时间10min;高速离心条件为:转速8000rpm,离心6min。
45.(3)浓缩和稀释
46.将混合提取液在50℃水浴条件下,用氮气吹扫除去甲醇和乙腈后用稀释液稀释至45ml,得萃取稀释液;所述稀释液为氯化钠/乙二胺四乙酸二钠二水合物的水溶液,稀释液通过以下方法制得:将15g氯化钠、0.25g乙二胺四乙酸二钠二水合物,溶于超纯水中并定容至500ml,加入浓盐酸调节ph为3。
47.(4)全自动固相萃取
48.采用全自动固相萃取仪(automatic cartridge-disk universal solid phase extraction system(labtech,china))进行全自动固相萃取,具体方法为:将cnw poly-sery hlb小柱,柱规格为500mg,6ml,依次用10ml甲醇和10ml、ph为3的超纯水进行活化,再以30s浸泡模式上样,上样结束后,用15ml、ph为3的超纯水分三次淋洗cnw poly-sery hlb小柱,在氮气流下干燥15min,最后用8ml甲醇洗脱,得到洗脱液。
49.(5)浓缩定容
50.将洗脱液在50℃水浴条件下,氮气吹干,用初始流动相溶解后定容至600μl,过0.22μm有机相滤膜,得上机溶液;初始流动相为乙腈和0.1%甲酸的2mmol/l乙酸铵溶液的混合液,乙腈和0.1%甲酸的2mmol/l乙酸铵溶液的体积比1:9。
51.(6)超高效液相色谱-串联质谱检测
52.用进样针抽取上机溶液,按已设定的超高效液相色谱-串联质谱检测条件进行上样检测,得上机溶液的离子流色谱图;色谱条件为:waters acquity uplc beh c18色谱柱,柱规格为2.1mm
×
100mm,1.7μm;柱温35℃,样品室温度10℃;进样量为5μl;流速为0.3ml/min;采用二元梯度洗脱,流动相a为0.1%甲酸的2mmol/l乙酸铵溶液,b为乙腈,梯度洗脱程序:0~1.5min,90%a;1.5~6.5min,90%~87.5%a;6.5~9.5min,87.5%~70%a;9.5~10.5min,70%~60%a;10.5~10.7min,60%~10%a;10.7~11.5min,10%a;11.5~11.8min,10%~90%a;11.8~15min,90%a;质谱条件为:电喷雾正电子(esi+)模式电离,多反应监测模式检测;离子源温度:150℃;脱溶剂气温度:600℃;毛细管电压:3.0kv;锥孔气流量:150l/h;脱溶剂气流量:800l/h。
53.(7)标准曲线绘制
54.采用mass-lynx软件4.1和计算机进行数据采集和处理,用多反应监测模式和保留时间进行定性:取浓度为1mg/l的恶喹酸、氟甲喹、诺氟沙星、依诺沙星、环丙沙星、培氟沙星、洛美沙星、丹诺沙星、恩诺沙星、氧氟沙星、氟罗沙星、沙拉沙星、司帕沙星、奥比沙星、双氟沙星的喹诺酮混合标准使用液12μl,以及与上述15种喹诺酮类抗生素相对应的1mg/l的恶喹酸-d5、氟甲喹-13
c3、诺氟沙星-d5、依诺沙星-d8、环丙沙星-d8、培氟沙星-d5、洛美沙星-d5、丹诺沙星-d3、恩诺沙星-d5、氧氟沙星-d3、氟罗沙星-d3、沙拉沙星-d8、司帕沙星-d4、奥比沙星-d4、双氟沙星-d3的喹诺酮同位素内标混合溶液12μl,用初始流动相定容至0.6ml,得到标准工作液,初始流动相为乙腈和0.1%甲酸的2mmol/l乙酸铵溶液的混合液,乙腈和0.1%甲酸的2mmol/l乙酸铵溶液的体积比1:9;将标准工作液按照上述步骤(6)的步骤进行操作,得标准工作液的离子流色谱图(如图1、图2、图3所示);将标准工作液的离子流色谱图与单
种喹诺酮类抗生素和与之相对应的同位素内标的离子流色谱图进行定性离子、定量离子比较,同时结合保留时间,确定15种喹诺酮类抗生素;该15种喹诺酮类抗生素的定性离子、定量离子、保留时间和相对应的15种同位素内标的定量离子、保留时间用以作为同位素标记内标法定量时识别15种喹诺酮类抗生素色谱峰识别的依据;15种喹诺酮类抗生素和相对应15种同位素内标的保留时间和多反应监测条件如表1所示;
55.用同位素标记内标法进行定量:同时取浓度为1μg/l的喹诺酮混合标准使用液30μl、浓度10μg/l的喹诺酮混合标准使用液60μl、浓度100μg/l的喹诺酮混合标准使用液30、120、300μl以及浓度1000μg/l的喹诺酮混合标准使用液60μl,分别加入与之对应的1mg/l的喹诺酮同位素内标混合溶液12μl,再分别用初始流动相定容至0.6ml,得到六次加标浓度范围均为0.05~100μg/l,且同位素内标浓度均为20μg/l的标准曲线系列溶液;将六种不同加标浓度的标准曲线系列溶液,根据加入的喹诺酮浓度和相应定量离子积分峰面积与对应同位素内标的定量离子积分峰面积的比值的对应关系建立标准曲线。标准曲线的线性回归方程、线性范围、相关系数和检出限如表2所示。
56.表1 15种喹诺酮类抗生素和相对应15种同位素内标的保留时间和多反应监测条件
57.[0058][0059]
注:*定量离子。
[0060]
表2 15种喹诺酮类抗生素的线性回归方程,线性范围,相关系数和检出限
[0061][0062]
其中,a:线性范围代表分析物在标准曲线系列溶液中的浓度;b:y和x分别代表分析物相应定量离子积分峰面积与对应同位素内标的定量离子积分峰面积的比值和分析物在初始流动相中的理论浓度。
[0063]
(8)样品分析
[0064]
将步骤(6)中得到的上机溶液的离子流色谱图中的喹诺酮类抗生素的相应定量峰面积与相对应同位素内标的定量峰面积的比值,与步骤(7)中建立的标准曲线进行比较,通过换算即可得到样品中15种喹诺酮的实际含量。
[0065]
使用上述舟山海域采集的沉积物样品,按照步骤(1)的要求处理后,取2.00g,分别加入6μl、120μl浓度为100μg/l的喹诺酮混合标准使用液和60μl浓度为1000μg/l的喹诺酮混合标准使用液,配制成低(0.3ng/g),中(6ng/g)和高(30ng/g)三种添加浓度水平的加标样品,再分别加入与之对应的1mg/l的喹诺酮同位素内标混合溶液12μl,涡旋混合均匀,按照上述步骤(2)~(6)的要求分别进行五次平行操作,并与上述步骤(7)得到的标准曲线比较,通过换算最终得到加标样品中15种喹诺酮的测定浓度;按照下式进行回收率计算:
[0066][0067]
式中:r——回收率,%;
[0068]cs
——加标样品中15种喹诺酮类抗生素的测定浓度,ng/g;
[0069]
c0——实际样品中15种喹诺酮类抗生素的浓度,ng/g;
[0070]
c——加标样品中15种喹诺酮类抗生素的理论加标浓度,ng/g。
[0071]
经检测,舟山海域采集的沉积物样品中检出氟甲喹、诺氟沙星、环丙沙星、培氟沙星、洛美沙星、恩诺沙星、氧氟沙星,浓度分别为0.316、0.367、0.372、0.046、0.012、0.216、0.406ng/g,加标舟山海域采集的沉积物样品中不同加标浓度水平的加标回收实验结果见表3。
[0072]
表3舟山海域采集的沉积物样品中15种喹诺酮类抗生素的背景值、加标回收率和方法的精密度(n=5)
[0073][0074]
[0075]
注:“nd”代表未检出。
[0076]
由表3可知,加标舟山海域采集的沉积物样品回收率为82~119%,相对标准偏差(n=5)为1.8~12.5%,满足分析方法对回收率和重现性要求。
[0077]
以上所述的实施例只是本发明的一种较佳的方案,并非对本发明作任何形式上的限制,在不超出权利要求所记载的技术方案的前提下还有其它的变体及改型。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1