用于控制待冰冻的生物样本中的冰核形成的装置的制作方法
发明领域
本发明大体涉及用于控制冰形成的装置、方法和系统。
发明背景
生物材料(例如,细胞、疫苗和蛋白质)通常需要保存。例如,生物材料可能需要保存,以便它们可以在以后的时间点在科学实验中被研究或使用。在另一示例中,作为体外受精(ivf)过程的一部分,可以保存人体卵母细胞或受精胚胎。在这些实施例中,以使对生物材料的损害或劣化最小化的方式保存生物材料是重要的。冰冻技术常用于保存生物材料。有不同的方式冰冻生物材料以保存它们。例如,冷冻保存为将生物材料冰冻并然后以冰冻状态储存的过程,而冰冻干燥(冻干)为将生物样本冰冻并在冰冻步骤之后,从样本中除去水,使得样本以干燥状态储存的过程。
冷冻保存是广泛采用的用于保持生物样本的长期生存力以便随后在医学、生物技术和兽医学领域应用的技术。为了在解冻时获得高生存力,有必要加入也称为冷冻保护性添加剂的保护性化合物,并且然后以受控的速率冷却样本。对于许多细胞类型,还有必要通过受控的成核而不是允许自发的冰核形成(icenucleation)来诱发冰形成。用于冷冻保存的样本通常放置在专门的冷冻容器中,诸如:
·为薄壁管的吸管,其直径通常为2mm至4mm,长度可达140mm,容量为0.2ml至0.5ml;
·冰冻瓶,其为直径较大(直径通常为12.5mm)且容量为0.5ml至5.0ml的短管;
·袋,容量从5ml到1000ml的一系列柔性袋可用于较大体积的冷冻保存;以及
·多套管板(multiwellplate)、基质管和在机器人技术、高通量筛选等中采用的其他sbs(生物分子科学学会)样式。
存在一系列器具以允许样本在冰冻容器中的受控速率冰冻;这些装置可采用液氮作为冷冻剂或通过机械冷藏来冷却。此外,存在许多无源冷却装置。在受控速率冰冻后,样本在通常为液氮温度(-196℃)的低温下保持冰冻。在此温度下,如果细胞在冷却阶段存活,则细胞生存力与储存期无关。当需要使用时,样本被快速解冻,通常被保持在37℃的水浴中,并且冷冻保护剂被去除。
冰冻干燥(冻干)广泛用于生物技术、医药和兽医科学,以用于长期稳定细胞、疫苗、蛋白质和其他生物活性化合物。冰冻干燥过程也用于生成结构化材料,诸如应用于再生医学和新型陶瓷生产的支架和基片。在冰冻干燥过程中,将含水样本置于通常为玻璃小瓶的专门容器中并被冰冻。通常,冰冻发生在冰冻干燥器的冷却架上。冰冻后,局部气体压力降低,然后冰冻样本内的冰升华。从样本中去除所有的水后,将小瓶在真空下升温并密封。样本可在环境温度下分布,并通过加水重构。
一致的冰核形成是冷冻保存中最大的挑战。当液体被冷却至其熔点时,不会立即发生冰核形成。样本可达到在其熔点以下20℃或更多,而不会发生冰核形成,这种情况被称为“过冷却”或“过冷”。随着样本的温度降低,在某一温度下会发生自发冰核形成并且冰将会在整个样本中扩展。
一些类型的细胞是坚固的,并且不会受过冷却的不利影响。但是许多类型的细胞可能被过度的过冷却损坏,这会在解冻后降低细胞生存力。由于冰核形成的可变性质,样本生存力之间可能存在很大差异。这产生各种不利的商业后果:
1.保证在冰冻和解冻后样本中存在一定数量的活细胞的公司必须过量填充样本以补偿存活力范围。如果可以减少细胞的变异性(variability),则需要较低的细胞数量,同时仍然保证最小的存活数目。这将大大降低成本。
2.除细胞的变异性之外,如果可以提高整体生存力,则对于相同生产成本而言,总产量将更高。
3.使用具有冰冻并解冻的贴壁细胞的多套管板(例如,96个套管的板和384个套管的板)进行高通量筛选对于许多感兴趣类型的细胞(肝细胞、肌细胞、干细胞系等)来说是不可能的。细胞的背景变异性导致“噪声”太多难以识别任何有意义的测试结果。这迫使公司使用制备有贴壁细胞(即未冰冻的)的“新鲜”的多套管板或从单个冰冻源对多套管板进行引晶。这两个选项都会花费大量时间和成本,同时使多套管测试的逻辑复杂化。
过冷的水溶液中的冰核形成可通过两种不同的过程发生:
1)同质冰核形成简单地通过水体内的随机密度波动发生,充分描述了此类分子簇的生长和消减的历程以及它们作为用于使冰结晶的核的能力。
2)异质或促进的冰核形成由与水接触的固态或液态基质催化,其允许吸附的水分子组呈现能够促成冰形成的构型。实际上,冷冻保存样本中的冰核形成通过异质机制发生。
为了降低冷冻保存期间经历的冰核形成温度的范围,已经采用了许多物理方法来诱发样本内的冰核形成。
1)“引晶”。在早期研究哺乳动物组织培养细胞的基础低温生物学和后来的ivf中,通过将小冰晶物理地引入过冷样本中,对样本进行引晶。为了消除与该程序相关的污染的可能性,现在通常的做法是通过在封闭式冷冻容器的外部手动生成冷点来诱发样本中的冰核形成,并且这仍然被错误地称为“引晶”。
2)电冰冻(electrofreezing)。已经表明施加到金属电极的高电压在过冷却的水中引起冰形成,并且这已经应用于冷冻保存。
3)机械方法。摇晃、轻敲、应用超声波可以非常有效地在过冷样本中引入冰。超声波冰核形成已被实现到实验性冰冻干燥器具中。
4)“冲击冷却”。在传统的缓慢冷却之后,样本被快速冷却,然后进一步暴露于一组复杂的温度斜坡。很可能在样本的壁处形成“冷点”,从而导致局部的冰核形成。一些速度受控的冷冻机的供应商将冲击冷却特征集成到其器具中。
5)压力偏移。该方法已经被应用于冰冻干燥,其中样本被容纳在可以控制压力的腔室中。将样本用氩气加压至28psig,并然后冷却至所需的成核温度,然后将压力降至1psig以诱发成核。
这些物理方法难以标准化并集成到常规冷却速率器具中,并且与大量样本或所有样本容器不兼容。另一种方法是使用冰的异质成核剂并将其并入样本容器或悬浮液中。冷冻保存期间的冰核形成已通过将特定的冰核催化剂包含在悬浮介质中得到证明。所检查的冰核剂包括细菌丁香假单胞菌(bacteriumpseudomonassyringae)、结晶胆固醇、包封的碘化银和长石。尽管这些材料是有效的冰核剂,但是它们难以制成符合动态药品生产管理规范(cgmp)的材料,或者不具有生物兼容性,并因此不能在许多应用中使用。此外,在冰冻和解冻之后,有必要去除冰核剂,否则它们可能干扰细胞生存力和功能。目前,没有能将样本中的冰核剂呈现出来以避免这些问题的装置。
因此,本申请人已经认识到对用于控制冰形成和冰核形成的改进的装置的需要。
发明概述
根据本发明的第一方面,提供了用于执行冰核形成的装置,该装置包括:至少一个壳体,该壳体包括空腔和至少一个可渗透壳体壁;以及包封在空腔内的冰核材料(icenucleatingmaterial)。
在实施例中,壳体包括第一可渗透壳体壁和第二可渗透壳体壁。具有两个可渗透壳体壁的优点在于液体接触冰核材料的机会增加,这可加速冰晶的形成。在实施例中,特别是在冰核材料以粉末形式提供的情况下,空腔内很可能存在空气。可渗透壳体壁允许液体进入空腔,并且允许空气从空腔逸出,使得空腔基本上充满液体和冰核材料。这减少了空腔内的压力积聚,并且增加了能够与冰核材料相互作用的液体的量(这从而可能加速冰形成)。
在实施例中,第一可渗透壳体壁由第一层形成,并且第二可渗透壳体壁由第二层形成,并且其中,空腔设置在第一层和第二层之间。
优选地,第一层和第二层至少在壳体的边缘部分处结合在一起,以将冰核材料包封在空腔内,边缘部分围绕空腔。
额外地或替代地,壳体可由具有第一部分和第二部分的可渗透材料层形成,其中,第一可渗透壳体壁由可渗透材料层的第一部分形成,并且第二可渗透壳体壁由可渗透材料层的第二部分形成,并且其中,空腔设置在可渗透材料层的第一部分和第二部分之间。
优选地,可渗透材料层被折叠以在可渗透材料层的第一部分和第二部分之间形成空腔,并且其中,第一部分和第二部分至少在壳体的边缘部分处结合在一起以将冰核材料包封在空腔内,边缘部分围绕空腔。
额外地或替代地,壳体可包括壳体主体和可渗透壳体壁,其中,空腔设置在壳体主体和可渗透壳体壁之间。
优选地,壳体主体包括在壳体主体的表面中的凹部,该凹部形成空腔,并且其中,可渗透壳体壁设置在凹部之上并且结合到壳体主体的表面,以将冰核材料包封在空腔内。
在替代实施例中,壳体可包括壳体主体、第一可渗透壳体壁和第二可渗透壳体壁,其中,壳体主体为包括通孔的盘状物,通孔形成空腔,并且其中,第一可渗透壳体壁设置在通孔之上并且结合到壳体主体的第一表面,以及第二可渗透壳体壁设置在通孔上方并且结合到壳体主体的第二表面,以将冰核材料包封在空腔内。
在任何上述实施例中,该装置还可包括耦接到壳体的杆。杆的优点在于它可用于控制装置在容器内的位置。此外,杆提高了在解冻之后将装置从容器中取出的容易性。
在任何上述实施例中,该装置还可包括具有第一端和第二端的杆,其中,第一端耦接到壳体,并且第二端耦接到用于容器的盖。有利地,这可使得装置能够被放置在每个容器内的预定的一致的位置,并且还可提高解冻之后从容器中取出装置的容易性。
在实施例中,该装置包括多套管板,该多套管板包括:多个套管和多个一体式壳体,其中,多个一体式壳体中的一个一体式壳体被集成到多个套管中的一个套管中。
优选地,一体式壳体包括:一体式壳体壁;一体式可渗透壳体壁;以及在一体式壳体壁和一体式可渗透壳体壁之间的一体式空腔,其中,一体式空腔容纳冰核材料。
在实施例中,一体式壳体壁由套管的侧壁的至少一部分形成。额外地或替代地,一体式壳体壁由套管的至少一个底壁形成。套管的底壁可包括在内表面中的凹部,凹部形成一体式空腔,并且其中,一体式可渗透壳体壁设置在凹部之上并且结合到底壁的内表面以将冰核材料包封在空腔内。
在优选实施例中,该装置包括用于具有多个套管的多套管板的插入板,该插入板包括:布置成阵列的多个腿部,每个腿部具有耦接到插入板并从插入板的表面延伸的第一近端;多个脚部,其中,每个脚部耦接到腿部的第二远端。
插入板可耦接到多套管板以将多个脚部设置在多套管板的多个套管中,并且从而将冰核材料输送到每个套管中。
在实施例中,插入板还包括布置成阵列的多个孔眼(hole),其中,每个腿部靠近孔眼耦接到插入板。
至少一个壳体可包括多个壳体,其中,每个壳体设置在脚部内,并且每个壳体包括空腔和至少一个可渗透壳体壁。
优选地,每个壳体包括第一可渗透壳体壁和第二可渗透壳体壁,其中,空腔设置在第一可渗透壳体壁和第二可渗透壳体壁之间。
在任何上述实施例中,壳体包括至少一个通气孔眼,以便当水通过可渗透壳体壁进入空腔时允许空腔中的空气逸出,由此减小空腔内的压力。
在实施例中,插入板可卡扣配合到多套管板上。在实施例中,插入板的每个腿部的长度小于多套管板的每个套管的深度。在实施例中,腿部和脚部的组合长度小于多套管板的每个套管的深度。在每种情况下,该布置可使得脚部(并因此冰核材料)能够靠近套管的基底(在该处施加冷却,并且更有可能形成冰)设置。此布置可防止脚部接触存在于套管基底处或附近的任何生物物质(例如,细胞),这否则可能造成对生物物质的损害。
所述或每个可渗透壳体壁或本文所述的实施例可由以下中的任一种形成:可渗透材料、包括一个或更多个孔眼的材料、海绵材料、包括海绵材料的材料、芯吸材料、过滤板、过滤材料、网状材料、可渗透膜、亲水性过滤物和亲水性膜材料。
在本文所述的任何实施例中,冰核材料可为革兰氏阴性细菌、丁香假单胞菌、结晶胆固醇、包封的碘化银和长石中的任何一种。
根据本发明的第二方面,提供了如本文所述的装置的用途,所述装置用于在容器中形成冰核,其中,该容器为以下中的任何一种:试管、小瓶、吸管、多套管板的套管、多套管板和袋。
根据本发明的第三方面,提供了如本文所述的装置的用途,所述装置用于在多套管板中形成冰核。
根据本发明的第四方面,提供了形成冰核的方法,该方法包括:将本文所述的装置插入容纳待冰冻的生物样本的容器中。
根据本发明的第五方面,提供了形成冰核的方法,该方法包括:将本文所述的装置插入具有多个套管的多套管板中,每个套管容纳待冰冻的生物样本。优选地,该装置与多套管板兼容。因此,优选地,插入多套管板中的装置包括腿部的n×m阵列,并且其中,多套管板的多个套管以n×m阵列布置。
根据本发明的第六方面,提供了用于执行冰核形成的系统,包括:用于容纳待冰冻的样本的容器;以及本文所述的装置。容器可为试管、小瓶、吸管、多套管板的套管、多套管板和袋中的任何一种。
附图简述
附图中通过举例示意性地示出了该技术,其中:
图1a示出了根据实施例的用于执行冰核形成的装置的侧视剖视图;
图1b示出了根据另一实施例的用于执行冰核形成的装置的侧视剖视图;
图2示出了根据另一实施例的用于执行冰核形成的装置的侧视剖视图;
图3示出了根据另一实施例的用于执行冰核形成的装置的侧视剖视图;
图4a示出了包括冰核装置的系统;
图4b示出了包括冰核装置的系统(左),和冰核装置的透视图(右);
图5a示出了包括具有杆的冰核装置的系统;
图5b示出了包括具有杆的冰核装置的系统(左),和冰核装置的透视图(右);
图6a示出了包括具有耦接到容器盖的杆的冰核装置的系统;
图6b示出了包括具有耦接到容器盖的杆的冰核装置的系统(左),和冰核装置的透视图(右);
图7a示出了典型多套管板的套管的剖视图;
图7b示出了在冰核装置采用多套管板的形式的实施例中冰核装置的一部分的剖视图;
图7c和7d示出了在冰核装置采用多套管板的形式的另外实施例中冰核装置的一部分的剖视图;
图8a示出了在冰核装置采用了用于多套管板的插入板的形式的实施例中冰核装置的一部分的侧视剖视图;
图8b示出了图8a的冰核装置的在多套管板的套管内的部分的剖视图;
图8c为示出了在图8a的冰核装置的部分中包封冰核材料的步骤的示意图;
图8d为示出了在冰核装置的实施例中包封冰核材料的步骤的示意图;
图9a示出了采用用于多套管板的插入板的形式的冰核装置的透视图,以及冰核装置的一部分的放大视图;
图9b示出了图9a的冰核装置的下侧的透视图;以及
图10为示出了对于(a)不含冰核材料的多个单独的样本,和(b)加入冰核材料的相同样本的溶液温度与时间的曲线图。
详细描述
广义而言,本技术的实施例提供了用于控制冰形成(诸如在冷冻保存和冰冻干燥过程中)的装置。具体地,该装置提供了将冰核材料输送到待保存的生物样本中而不允许冰核剂接触或污染样本内的生物物质的机制。有利地,该装置的实施例可被制造成与现有广泛使用的实验室器具,诸如小瓶、管、多套管板等兼容。该装置的另一优点是提高了样本冰冻和随后的解冻之后的细胞生存力。
本申请的装置使得能够控制冷冻保存和冰冻干燥中的冰冻过程(特别是用于控制冰形成),使得样本在接近样本的熔点的温度下冰冻。小体积液体可在低于液体熔点的温度下冰冻。例如,10升水冰冻(在一个大气压下)时的温度约为0℃,而较小体积的水,例如,几微升的水,通常在低得多的温度下冰冻,例如,-30℃(在一个大气压下)。此外,小体积的水冰冻的确切温度可能会有明显的变化。当冰冻样本包含生物物质(诸如细胞)时,生物物质的生存力取决于冰冻和解冻过程。通常,生物样本以小体积冰冻,因此将在低于包含生物材料的样本/液体的熔点的温度下冰冻。然而,如果生物样本在比样本的熔点低得多的温度下冰冻,则在冰冻和解冻过程中生物样本更可能被损坏或变性。因此,为了降低在冰冻期间损伤生物样本的风险,使用技术来提高样本冰冻的温度,诸如通过向样本中加入冰核材料。
冰核装置有利地将冰核材料输送到待冰冻的样本,同时防止冰核材料渗透通过样本并接触样本内的任何生物物质。如下文更详细地描述的,冰核装置可采取不同的形式,它可为可被添加到容纳样本的容器中的装置,它可为多套管板的形式,和/或它可为用于多套管板的插入板的形式。在每个实施例中,冰核装置包括具有空腔和至少一个可渗透壳体壁的壳体,以及包封在空腔中的冰核材料。可渗透壳体壁对于液体分子(例如水)来说是可渗透的,但是并非对于任何生物物质(例如,细胞、蛋白质、疫苗等)来说都是可渗透的,并且对于冰核材料来说是不可渗透的。因此,当待冰冻的样本与该装置接触时,样本中的液体能够渗透通过可渗透壳体壁,使得在样本冷却时由该装置诱发液态冰晶的形成。一旦样本的温度达到足够低的温度,冰核材料就会使冰晶形成。冰晶然后扩展通过液态样本。冰核装置保留在冰冻样本内,并且可在冰冻样本已经解冻后除去。在实施例中,冰核装置可以是可重复使用的。替代地,冰核装置为一次性装置,即,是用后即弃的。
在实施例中,可渗透壳体壁的孔径(poresize)可大于冰核材料颗粒的尺寸,但当冰核材料为粉末形式时,颗粒倾向于结合在一起并且不流动。当冰核材料被润湿时,往往更不愿意流动。因此,冰核材料通过孔隙(pore)离开空腔的可能性降低。在实施例中,可渗透壳体壁的孔径可大于容器内的生物物质(例如,细胞)的尺寸。然而,生物物质通常沉积在容器的基底上或位于容器的基底处,并且往往可基本上固定到基底,使得生物物质不可能直接接触该装置并渗透通过可渗透壳体壁。
术语“装置”在本文中可与术语“冰核装置”、“设备”和“容纳材料的设备”互换使用。
术语“冰核材料”在本文中可与术语“冰核剂”、“成核剂”和“冰冻剂”互换使用。
术语“样本”在本文中可与术语“生物样本”、“生物物质”、“生物材料”、“生物介质”、“液体”和“流体”互换使用。
如下文更详细地描述的,“样本”可被容纳在容器中。术语“容器”在本文中可与术语“器皿”、“样本器皿”、“试管”、“小瓶”、“吸管”、“多套管板”、“套管”、“袋状物”互换使用。
术语“可渗透壳体壁”在本文中可与术语“分隔屏障”、“屏障”、“可渗透膜”、“膜”、“膜材料”和“膜层”互换使用。然而,应理解,可渗透壳体壁可由任何合适的可渗透材料或物质形成,并且“膜”仅仅为示例材料。所述或每个可渗透壳体壁可由以下中的任何一种形成:可渗透材料、包括一个或更多个孔眼的材料、海绵材料、包括海绵材料的材料、芯吸材料、过滤板、过滤材料、网状材料、可渗透膜、亲水性过滤物和亲水性膜材料。
图1a示出了根据实施例的用于执行冰核形成的装置10的侧视剖视图。在此实施例中,装置10包括壳体部分/壳体12(由虚线示出)。壳体12包括壁14和壁16,并且包括空腔20。空腔20设置在(或形成在)壁14和壁16之间。如图所示,壁14和16可延伸超过壳体12。装置10包括包封在空腔20中的冰核材料(未示出)。壳体12包括至少一个边缘部分18。壁14和16在边缘部分18处结合在一起,以形成空腔20并将冰核材料包封在空腔内。
装置10是可被添加到容纳待冰冻样本的容器中的装置(如图4a和4b所示)。因此,壁14和壁16中的至少一个为可渗透壳体壁,这使得样本中的液体能够接触包封在空腔20中的冰核材料。在实施例中,壁14和壁16均为可渗透壳体壁,并且可由相同或不同的材料形成。如图1a所示,壁14和16可由分离的层形成,即,壁14由第一层形成并且壁16由第二层形成。第一层和第二层可至少在壳体12的边缘部分18处结合在一起,以将冰核材料包封在空腔内。在替代实施例(未示出)中,壳体12可由具有第一部分和第二部分的可渗透层形成,其中,壳体12的第一可渗透壳体壁14由可渗透材料层的第一部分形成,并且第二可渗透壳体壁16由可渗透材料层的第二部分形成。也就是说,单个可渗透材料层可被折叠以提供壳体12的壁14和壁16。在这种布置中,空腔20设置在可渗透材料层的第一部分和第二部分之间。可渗透材料层的第一部分和第二部分至少在壳体12的边缘部分18处结合在一起,以将冰核材料包封在空腔20内,其中,边缘部分18围绕空腔20。
可以使用任何合适的结合壁14和16(或单个可渗透层的第一部分和第二部分)的技术来将冰核材料包封在空腔20内。例如,壁14和16可在边缘部分18处被热密封在一起,或它们可使用粘合剂或机械结合技术结合。
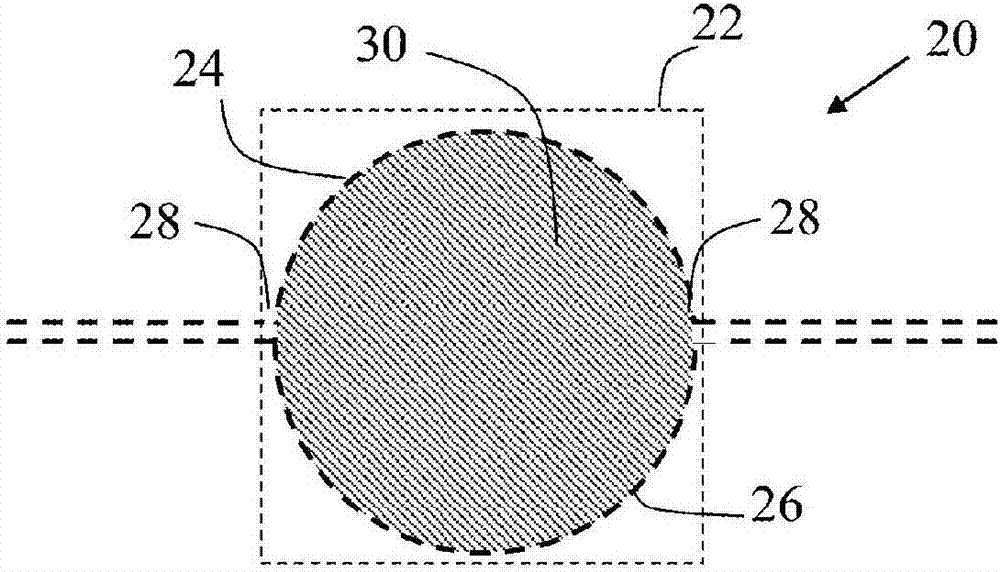
在图1a所示的实施例中,通过成形壳体12的壁中的一个,即壁14,来形成空腔。在此情况下,空腔20具有大致半球形形式,但也可采用任何其他形状。在替代实施例中,如图1b所示,可通过成形壳体壁14和16两者来形成空腔20。图1b示出了根据另一实施例的用于执行冰核形成的装置的侧视剖视图。这里,装置20包括壳体部分/壳体22(由虚线示出)。壳体22包括壁24和壁26,并且包括设置在(或形成在)壁24和壁26之间的空腔30。装置20包括包封在空腔30中的冰核材料(未示出)。壳体22包括至少一个边缘部分28。壁24和26在边缘部分28处结合在一起。以形成空腔30并将冰核材料包封在空腔内。在此实施例中,两个壁24和26被成形为形成空腔30。如图所示,空腔30可具有大致球形形式,但也可使用任何其他形状,并且每个壁24和26可具有不同的形状/形式。
用于形成图1b的装置20的技术和材料类似于上面关于图1a的装置10描述的技术和材料。具体地,壳体壁14和16中的至少一个并且壳体壁24和26中的至少一个是可渗透液体(例如,水)的。在实施例中,壳体壁14和16两者并且壳体壁24和26两者均可渗透水/液体。如上所述,可渗透壳体壁可由具有一个或更多个孔隙或孔眼的材料构成,所述孔隙/孔眼可渗透水和空气,但对于样本内存在的生物材料来说是不可渗透的,并且其对于包封在冰核装置内的冰核材料来说是不可渗透的。任何壳体壁可由包括以下材料的一系列材料制成:可渗透材料、包括一个或更多个孔眼的材料、海绵材料、包括海绵材料的材料、芯吸材料、过滤板、可渗透膜、亲水性过滤物和亲水性膜材料。
可渗透壳体壁的一个或更多个孔隙的典型孔径(例如直径)可在0.1μm至10μm的范围内,但孔隙可为任何合适的直径,该直径使得待冰冻样本中的液体能够渗透通过可渗透壳体壁,但防止冰核材料渗透出空腔(或减少其可能性)。在实施例中,所述或每个可渗透壳体壁可由标准实验室滤纸构成,标准实验室滤纸具有宽范围的孔径。
冰核装置的空腔(例如,空腔20和空腔30)可具有约1mm3的空腔体积。优选地,空腔具有适于在空腔内包封足够量的冰核材料的体积,以促进样本内的冰核形成或优化样本中的冰形成过程。在实施例中,空腔体积在0.1mm3-100mm3的范围内。
冰核材料可由包括呈任何物理形式(包括颗粒形式)的革兰氏阴性细菌、细菌丁香假单胞菌、结晶胆固醇、包封的碘化银和长石的一系列材料构成。颗粒形式相对于块形式的优点在于,与块形式相比,颗粒形式包括相对高的表面积,因此增加了冰核材料的冰核活性。优选地,用于冰冻样本的冰核材料是不会污染样本的材料。例如,如果冰核材料将要用于使生物样本的冰冻开始,则冰核材料不应该是有毒的、酸性或碱性过大的或生物活性的。
现在转向图2,其示出了根据另一实施例的用于执行冰核形成的装置40的侧视剖视图。在该实施例中,装置40包括壳体44。壳体44(由虚线指示)包括壳体主体42的全部或一部分、可渗透壳体壁48的全部或一部分和空腔46。空腔46设置在壳体主体42和可渗透壳体壁48之间。装置40是可被添加到容纳待冰冻样本的容器中的装置(如图4a和4b所示)。因此,可渗透壳体壁48使得样本中的液体能够接触包封在空腔46中的冰核材料(未示出)。在实施例中,壳体主体42可由不渗透材料形成,但是在特定实施例中,可由可渗透材料形成。壳体主体42和可渗透壳体壁48可由相同的材料形成,其中,该材料适于使其可渗透以形成可渗透壳体壁48(例如,通过在材料中形成孔隙/孔眼或通过其他方式)。
壳体主体42可由能够承受低温的任何合适的材料(例如聚合物)构成。在实施例中,壳体主体42以由聚丙烯形成,因为聚丙烯非常适合于低温应用,并且与通常用于制造装置40的热密封工艺(例如,将可渗透壳体壁48结合到壳体主体42)兼容。可渗透壳体壁48可由任何可渗透材料,例如以上提及的那些可渗透材料形成。
壳体壁48通过任何合适的结合技术(诸如热密封、在壳体44的边缘部分50处使用粘合剂或使用机械固定)至少在壳体44的边缘部分50处结合到壳体主体42上。空腔46可填充有任何合适的冰核材料,诸如上述那些冰核材料。
图3示出了根据另一实施例的用于执行冰核形成的装置60的侧视剖视图。在该实施例中,装置60包括壳体62。壳体62包括壳体主体68、第一可渗透壳体壁64和第二可渗透壳体壁66。壳体主体68可为包括通孔的盘状物,该通孔形成空腔72。第一可渗透壳体壁64设置在通孔之上并结合到壳体主体68的第一表面,并且第二可渗透壳体壁66设置在通孔之上并结合到壳体主体68的第二表面,以将冰核材料包封在空腔72内。
在此实施例中,壳体壁64和66可由分开的材料层形成(如图所示),或可由包裹壳体主体68的单个材料层形成(变型未示出)。两个壳体壁64和66优选是可渗透水的,但是在实施例中,壳体壁64和66中的一个可为不可渗透水的。壳体壁64和66可由具有孔隙的材料形成,如上所述,所述孔隙可渗透水和空气,但是对于样本内存在的生物材料来说是不可渗透的,并且对于冰核材料来说是不可渗透的。(也就是说,冰核材料的粉末颗粒倾向于结合在一起成为不太可能通过孔隙并且不太可能流动的簇或团块。生物物质通常沉积在样本容器的基底上或基本上固定到样本容器的基底,从而使得生物物质不可能直接接触该装置并渗透通过可渗透壳体壁。)壳体壁64和66可通过热密封技术、粘合剂或通过壳体62的边缘部分70处的机械固定而分别与壳体主体68的第一表面和第二表面结合。边缘部分70围绕空腔72。冰核材料设置在空腔72内。空腔72可具有适于在空腔内包封足够量的冰核材料的体积,以促进样本内发生冰核或优化样本中的冰形成过程。在实施例中,空腔体积在0.1mm3至100mm3的范围内。
图4a示出了包括冰核装置82和容器84的系统80。容器84可为用于储存冰冻样本的常用容器,诸如冷冻保存容器。容器84通常为用于保存和储存待冰冻并且随后解冻的样本的任何合适的容器,诸如但不限于:小瓶、吸管、多套管板和袋。冰核装置82可为例如上述参考图1a、1b、2和3描述的任何冰核装置。在所描绘的实施例中,冰核装置类似于图2的装置40,但这仅仅为系统的说明性示例。容器84包括盖86和主要主体88(也称为“主体”或“主体部分”)。盖86可为适于封闭/密封容器84的帽、塞子、顶部有螺旋的盖或任何其他盖。
为了冰冻样本,首先将样本放入容器84中。样本可以是包含生物物质,诸如细胞或蛋白质的液体。(在图4a中,示出了填充线89,仅仅是为了说明样本的存在。)冰核装置82被放置在容器的主要主体88中,使得其在样本内(即在填充线89下面)。容器84由冷却机构或装置(未示出)冷却,并且通常如图所示从容器84的下面施加冷却。如上所述,样本中的液体能够通过穿过所述或每个可渗透壳体壁而接触容纳在装置82内的冰核材料。与冰核材料接触的液体形成冰晶,冰晶在施加冷却时在样本中扩展并生长,从而使样本冰冻。装置82在样本中冰冻并保留在样本中(和容器84中)。当样本解冻时,装置82可从样本(和容器84)中取出。
图4b示出了图4a的系统80的图像(左)和冰核装置的图像(右)(未按相同的比例绘制)。在该示例中,容器84可包括顶部有螺旋的盖86。如图所示,冰核装置82优选被插入到容器84的主要主体88的底部,使得其最靠近向系统80施加冷却的冷却机构,以增加冰核化和冰冻速度。
图5a示出了包括容器96和冰核装置92的系统90。冰核装置92包括杆94(也称为“臂”或“棒”)。容器96包括盖98和主要主体100,并且类似于图4a所示且在上文中描述的容器。冰核装置92可为例如上述参考图1a、1b、2和3描述的任何冰核装置。在所描绘的实施例中,冰核装置92类似于图2的装置40,外加了杆94,但这仅仅为系统的说明性示例。
如上所述,为了冰冻样本,首先将样本放入容器96中。样本可为包含生物物质,诸如细胞或蛋白质的液体。在图5a中,示出了填充线99,仅仅是为了说明样本的存在。冰核装置92被放置在容器96的主要主体100中,使得其在样本内(即在填充线99下面)。如上面参考图4a所述,容器84由冷却机构或装置冷却。装置92在样本中冰冻并保留在样本中(和容器96中)。当样本解冻时,装置92可从样本(和容器96)中取出。图5a所示的冰核装置92的实施例的优点在于装置92的杆94允许控制装置92在容器96内的位置。在该实施例中,在解冻时可以通过拉动杆94容易且手动地取出该装置。
图5b示出了图5a的系统90的图像(左)和冰核装置92的图像(右)(未按相同比例绘制)。在该示例中,容器96可包括顶部有螺旋的盖98。如图所示,冰核装置92优选被插入到容器96的主要主体100的底部,使得其最靠近向系统90施加冷却的冷却机构,以增加冰核化和冰冻速度。
图6a示出了包括容器116和冰核装置112的系统110,该冰核装置112具有耦接到容器116的盖118的杆114。冰核装置112包括杆114(也称为“臂”或“棒”)。容器116包括盖118和主要主体111,并且类似于图4a和5a所示和上文中描述的容器。冰核装置112可为例如上述参考图1a、1b、2和3描述的任何冰核装置。在所描绘的实施例中,冰核装置112类似于图2的装置40,外加了耦接到盖118的杆114,但这仅仅为系统的说明性示例。杆114被附接到容器116(也称为“冷冻管”或“冷冻保存器皿”)的盖118的内表面(也称为“帽”)。
图6a所示的冰核装置的实施例的优点在于附接到盖118的杆114使得能够以可重复且准确的方式控制冰核装置112相对于容器116的位置。这种改进的控制的结果是一致的,并且在冰冻和解冻过程之后的样本生存力更高。该实施例的另一优点在于装置112被保持在冷冻管116中的相同位置,冷冻管116预期在冷却期间处于最低温度。这两者都优化了小瓶内的冰核形成,并确保了所有小瓶中的相同的热历史记录。当解冻时,在拧开盖118时,将装置112从样本中取出。
图6b示出了图6a的系统110的图像(左)和冰核装置112的图像(右)(未按相同比例绘制)。在该示例中,容器116可包括顶部有螺旋的盖118。如图所示,冰核装置112优选被插入到容器116的主要主体111的底部,使得其最靠近向系统100施加冷却的冷却机构,以增加冰核化和冰冻速度。
图7a示出了作为参考的典型多套管板的套管的剖视图。图7b示出了在冰核装置采用多套管板的形式的实施例中冰核装置的一部分130的剖视图。多套管板(未示出)包括套管阵列,并且通常可用的多套管板具有6、12、24、48、96、384和1536个套管。在装置为多套管板形式的实施例中,该装置包括多个套管和多个一体式壳体,其中,一个一体式壳体被集成在一个套管中。图7b示出了这种冰核装置的部分130(即,套管)。在图7b中,套管130包括主体132,并且主体132包括用于包封冰核材料的空腔134。主体132包括在套管130的基底处的底壁136。位于套管132的底壁136的一部分内的凹部形成空腔134。凹部位于底壁136的内表面中。可渗透壳体壁138位于空腔134之上并且结合在底壁的边缘部分140处,其中,边缘部分140围绕空腔134。在底壁136中具有空腔134和冰核材料的优点在于底壁136紧靠套管132内的样本的最冷部分和冷却机构(其通常在套管132下面)。
将可渗透壳体壁138结合到底壁的边缘部分140的过程类似于上述的结合方法,例如热密封、粘合剂和/或机械结合。
在实施例中,将冰冻剂加入到被模制成单个部件(例如,多套管板)的多个腔室(例如,套管)中,然后用多孔膜将该单个部件密封就位。每个腔室被放置成靠近多套管板上的单个套管的底部,并且允许在贴壁细胞的过冷却一致地低的情况下的高通量冷冻保存。
图7c和7d示出了在冰核装置采用多套管板的形式的另外实施例中冰核装置的部分150的剖视图。部分150包括套管152和用于包封冰核材料的空腔154。在图7c中,空腔154沿套管152的内侧壁(的全部或一部分)形成。空腔154形成在套管152的内侧壁(的全部或一部分)和可渗透壳体壁158之间。可渗透壳体壁可在结合点160处结合到套管152的内侧壁。
在图7d中,部分150包括套管152和用于包封冰核材料的空腔154。空腔154可以以至少两种方式形成。例如,套管152的侧壁152中的凹部可形成空腔154。凹部154位于侧壁152的内表面中。可渗透壳体壁158位于空腔154之上并且至少结合在侧壁152的边缘部分160处,边缘部分160围绕空腔154。在另一示例中,空腔154可形成在唇部156和底壁157的一部分之间。在此示例中,部分150包括如图所示部分地延伸到套管152中的唇部156。套管152包括至少一个侧壁152和底壁157。底壁157具有台阶部分159。空腔154形成在台阶部分159和唇部156之间。可渗透壳体壁158设置在空腔154之上并且在位置160处结合到台阶部分159的表面和唇部156。
图7d的实施例可优于图7c的实施例,因为与图7c的实施例中相比,图7d的实施例中的套管152的结构使得可渗透壳体壁158能够更有效地和/或更可靠地结合并结合到更大的表面区域。
图8a示出了在冰核装置包括用于多套管板的插入板的实施例中冰核装置的部分170的侧视剖视图。图9a示出了冰核装置190的透视图,冰核装置190包括用于多套管板(未示出)的插入板192,还示出了冰核装置190的一个节段的放大视图。图9b示出了图9a的冰核装置的底视透视图。
图9a和9b所示的冰核装置190包括孔眼198的阵列。孔眼198的数量和阵列中的孔眼的布置可改变以适应/匹配多套管板中的套管的数量和布置,使得当冰核装置190与多套管板一起使用时,孔眼198与多套管板的套管对准。例如,多套管板可包括套管的n×m阵列,并且冰核装置190可包括n×m个孔眼的阵列,使得装置190与多套管板兼容。可以将冰核装置190制造成与任何尺寸和类型的常用多套管板,例如具有6、12、24、48、96、384和1536个套管的多套管板兼容。因此,有利的是,冰核装置190与市售的多套管板兼容,并且不需要改造多套管板。在实施例中,冰核装置190可卡扣配合到多套管板上,以将装置190固定到多套管板。额外地或替代地,冰核可位于多套管板上,和/或使用任何合适的技术固定到多套管板上。
装置190包括多个脚部和多个腿部。多个腿部中的腿部196在第一端(或近端)处紧靠孔眼198耦接到插入板192。每个腿部196从插入板192的表面基本垂直地延伸,使得每个腿部196位于插入板192的相同侧上。每个腿部196在第二端(或远端)处耦接到多个脚部中的脚部194。脚部194包括具有空腔和至少一个可渗透壳体壁的壳体。冰核材料被包封在空腔内。多个腿部中的每个腿部196的长度基本相同,使得当装置190耦接到多套管板时,每个脚部194位于套管中基本相同的深度处。这使得冰核材料能够设置在多套管板的每个套管内的相同位置处,以保持冰形成的一致性并改进控制。腿部196的长度可小于多套管板的套管的长度(或深度),使得每个脚部194与套管的基底分离一定量。如下文更详细地描述的,每个脚部194和套管的基底之间的间隔可使得样本能够渗透穿过可渗透壳体壁并接触冰核材料。
装置190的孔眼198使得一旦装置190已耦接到多套管板就可将样本添加到多套管板中。在实施例中,在将样本添加到多套管板的套管中之后,装置190可耦接到多套管板。
装置190的一些部分(诸如插入板192、腿部196和脚部198)可由一件材料制成。在实施例中,装置190的一些部分可由聚合物或适合于容纳生物材料并用于冷冻保存/冰冻干燥的任何材料形成。诸如注射成型和3d打印的技术可用于制造装置190的一些部分。可使用下面关于图8c和8d描述的方法来制造装置190的一些部分。
返回图8a,更详细地描述了图9a和9b所示的冰核装置。图8a示出了冰核装置(例如,图9a所示的装置190)的部分170,该冰核装置包括插入板、多个腿部和多个脚部。部分170具有腿部171,其在第一端处耦接到插入板(未示出)并且在第二端处耦接到脚部178。脚部178包括壳体172。壳体172包括空腔182、第一壳体壁174和第二壳体壁176。空腔182可延伸穿过脚部178的一个节段,使得第一空腔开口设置在脚部178的顶表面上,并且第二空腔开口设置在脚部178的底表面上。第一空腔开口和第二空腔开口分别被第一壳体壁174和第二壳体壁176覆盖。第一壳体壁174和第二壳体壁176中的一个或两者可为可渗透壳体壁。优选地,第一壳体壁174和第二壳体壁176均为可渗透壳体壁。这增加了能够接触包封在空腔182中的冰核材料的液体的体积,这可经由形成冰核来增加冰晶形成的速度或效率。
壳体172包括从脚部178的表面突出并且分别定位在第一空腔开口和第二空腔开口附近(以及在实施例中,包围第一空腔开口和第二空腔开口)的密封唇部180和188。密封唇部180和188优选由与用于形成脚部178的材料相同的材料形成。在优选实施例中,脚部178和密封唇部180、188由适合在热密封工艺中使用的聚合物材料形成。如下文更详细地描述的,壳体壁174和176被结合到脚部178,优选地,经由热密封工艺,以将冰核材料包封在空腔182中。密封唇部180、188为脚部178的牺牲部分,其在热密封过程中熔化,以将壳体壁174和176结合到脚部178/壳体172。熔化密封唇部180、188会改善壁174、176和壳体172/脚部178之间的结合。壳体172包括通气孔184,当样本中的液体渗透通过壳体壁176时,通气孔184使得冰核材料内的空气能够从壳体172逸出(并且从而防止空腔182内的压力积聚)。
每个壳体壁174和176由单件材料形成。在实施例中,每个壳体壁174、176由单件可渗透材料形成。所述单件材料可为相同类型或不同类型的材料。每个壳体壁174和176与用于将每个壳体壁174和176结合到脚部178的密封唇部180或188接触。
图8b示出了在多套管板(未示出)的套管186内的图8a的冰核装置的部分170的剖视图。为了冰冻样本,将冰核装置的插入板耦接到多套管板,使得装置的每个脚部插入多套管板的套管中。可通过插入板中的孔眼将样本添加到套管中(参见图9a)。样本可为包含生物物质,诸如细胞或蛋白质的液体。图8b示出了填充线179,仅仅是为了说明样本的存在。添加到套管中的样本的体积可能需要使得样本至少与下部可渗透壳体壁176接触,但优选地也与上部可渗透壳体壁174接触。
为了将冰核材料包封在图8a的壳体172中,可遵循以下制造步骤。首先,将第一壳体壁174结合到壳体172以密封空腔182的第一开口。如上所述,热密封技术可用于将第一壳体壁174结合到壳体172,在此期间,唇部180被熔化以将第一壳体壁174固定就位。然后将冰核装置上下颠倒(即,使得脚部指向上),以使得冰核材料能够通过空腔的第二开口添加到空腔182中。将第二壳体壁176结合到壳体172/脚部178以密封空腔182的第二开口。热密封技术可用于将第二壳体壁176结合到壳体172,在此期间,唇部188被熔化以将第二壳体壁176固定就位。
图8c为示出了在图8a的冰核装置的壳体中包封冰核材料的步骤的示意图。图8c所示的壳体相对于图8a所示的壳体略有变化。具体地,相对于图8a的实施例,在图8c的实施例中第一壳体壁位于不同位置。在图8c的实施例中,第一壳体壁180'位于脚部178内,而不是在脚部178的外表面上。密封唇部174'位于脚部178内,而不是在脚部178的外表面上(如同图8a)。这是因为包封冰核材料的空腔182'不延伸通过脚部178,第一空腔开口通向通气孔184,而不是设置在脚部178的顶表面上,而第二空腔开口设置在脚部178的底表面上。图8c的布置的优点在于简化了将冰核材料包封在空腔182'内的过程,因为在将第一壳体壁180'结合到壳体172之后,不需要转动(旋转)所述装置,以便用冰核材料填充空腔182'。
因此,对于图8c的实施例,为了将冰核材料包封在壳体172'中,可遵循以下制造步骤。首先,将第一壳体壁174'结合到壳体172以密封空腔182'的第一开口。如上所述,热密封技术可用于将第一壳体壁174结合到壳体172,在此期间,唇部180'被熔化以将第一壳体壁174'固定就位。现在可将冰核材料通过空腔182'的第二开口加入空腔中(而不需要使该装置转动)。将第二壳体壁176结合到壳体172/脚部178以密封空腔182的第二开口。热密封技术可用于将第二壳体壁176结合到壳体172,在此期间,唇部188被熔化以将第二壳体壁176固定就位。如图8c所示,使壳体壁174'在脚部178内的优点在于,在包封冰核材料的步骤期间,不需要转动该装置,这可提高制造的容易性和效率(并且减少加工步骤)。
图8d是示出了在冰核装置的实施例中包封冰核材料的示例性步骤的示意图。首先,如图8d所示,将装置190定向成使得插入板被放置在对准架200上,其中,装置的多个脚部朝上。然后将装置190放置在对准架200上。对准架200包括钉202的阵列和一个或更多个对准销204。通过将插入板与对准销204对准,并将装置190的插入板的孔眼与架200的钉202对准,将装置沿所示的耦接方向放到架上。对准销194可用于使装置190与架192对准,并且对准在装置190的组件中使用的其他部件。然后第一壳体壁前体206被放置在装置190之上并且利用壳体壁前体206中的一个或更多个孔眼208与架200对准,其中在对准时,所述或每个孔眼208与对准架200的每个销204匹配。第一壳体壁前体206包括壳体壁材料片。第一壳体壁前体206包括穿孔218。使用热密封工具(未示出)向装置190施加热量以熔化与第一壳体壁材料接触的密封唇部,从而将壳体壁材料结合到壳体。一旦壳体壁材料已被热密封到装置190的每个脚部,则通过从装置190撕掉壳体材料将多余的未使用的壳体材料从装置190去除(穿孔218促进此过程)。
粉末掩模210被放置在装置190顶上,并且利用可与对准架200的所述或每个销204配合的一个或更多个孔眼212被对准。然后通过穿过粉末掩模210的孔眼213撒下冰核材料,将冰核材料加入到装置190的每个脚部的空腔中。从装置190中去除粉末掩模210。在实施例中,块形式的冰核材料的密度可为约2.6gcm-3,并且粉末形式的冰核材料的密度可为约1.0gcm-3。
第二可渗透壳体壁前体214被放置在装置190之上并且如上所述利用热密封被密封到装置190。第二可渗透壳体壁前体214包括穿孔216,其使得前体214的未使用节段能够在热密封过程之后容易地被去除。一旦膜材料被密封到装置190上,就将多余的膜材料去除。
如前所述,所述或每个可渗透壳体壁优选地具有以下功能和特性中的一些或全部:将冰核材料保持在空腔中,允许空气从空腔中逸出(并且防止压力在空腔中积聚),以及允许流体样本穿过壳体壁并接触冰核材料。
可渗透壳体壁可具有接近冰核材料的粒度的合适的孔径。通常,0.1μm至10μm的孔径(直径)是合适的。在实施例中,孔径可大于冰核材料颗粒的尺寸,但是当冰核材料为粉末形式时,颗粒倾向于粘结在一起并且不流动。当冰核材料被润湿时,往往更不愿意流动。因此,冰核材料通过孔隙从空腔离开的可能性降低。
优选地,可渗透壳体壁由吸收水并允许流体样本渗透通过该材料的亲水性材料形成,使得流体可以与冰核材料接合/接触。标准实验室滤纸是提供可渗透壳体壁的合适材料,并且可提供宽范围的孔径。标准实验室滤纸通常由纤维状纤维素材料制成。
在热密封过程中,可渗透壳体壁的纤维可与壳体粘结,特别是如果壳体由聚合物材料形成的话。
第一壳壁前体和第二壳体壁前体(用于将冰核材料包封在插入板的脚部中)优选为包括多个壳体壁区段的材料片,多个壳体壁区段被定位在正确的位置并且具有正确的尺寸,以使得区段能够被压印、激光切割或以其他方式从片材中被去除并施加到脚部上。有利地,这使得多个脚部的第一壳体壁能够在单个制造步骤中被结合到每个脚部(并且对于每个脚部的第二壳体壁也是这样)。壳体壁区段可被特定图案的穿孔围绕,穿孔有助于在热密封之前将壳体壁段与每个脚部对准。
图10是示出了对于(a)不含冰核材料的多个单独的样本,和(b)包含冰核材料的多个单独的样本的溶液温度与时间的曲线图。如对于(a)可以看出的,样本温度的自发尖峰(spontaneousspike)发生在不同的时间,并且尖峰通常为约10至15℃。已知样本温度的这种快速变化导致样本冰冻和解冻后生存力差。
标记为(b)的轨迹表示使用本发明的冰核装置获得的结果。可以看出,与不使用冰核装置的情况相比,在冷却阶段观察到的温度尖峰的振幅较低。这就解释了当使用冰核装置诱发冰核形成时为什么样本生存力得以改善。
在制造之后,任何上述实施例的冰核装置被封装成合适的密封容器。整个封装以及冰核装置被灭菌,特别是因为该装置可用于冰冻生物材料,灭菌会防止污染。γ射线灭菌是优选的,因为它很适合一次性对大量物品灭菌。在冰核材料为长石材料的实施例中,γ射线灭菌是合适的,因为长石不会受到γ射线灭菌的不利影响。
为了最大化冰核装置的有效性,需要合适的冰冻、解冻和恢复过程。
对于生物样本,冷冻保护剂,诸如dmso或甘油往往用于在冰冻过程中屏蔽细胞。冷冻保护剂通常占被冰冻的样本的5%。
在容纳样本的容器(例如容器、小瓶或套管)内,在仍然覆盖冰核材料的同时使用可能的最小体积是可取的。例如,在96个套管的板中,一个套管的体积为400微升,但可能仅需要填充至例如70微升,以使得样本能够接触冰核装置并基本上浸透冰核材料(即用冰核材料和来自样本流体基本上填满装置的空腔)。应理解,可使用能够使来自样本的流体基本上浸透冰核材料的任何填充体积,并且一般来说,该体积小于套管的体积。
在冰冻和解冻过程后,冷冻保护剂具有轻微的毒性作用,因此生物样本往往被“冲洗掉”。冷冻保护剂被稀释,然后被除去。通过在冰冻之前以尽可能小的体积填充器皿,可以以高的水与样本比例快速稀释有毒的冷冻保护剂。然后除去稀释的液体,并且如果需要,可以重复该“稀释和去除”步骤。
一旦生物样本已被添加到容器(例如,小瓶或多套管板的套管)中,就可以添加冰核装置。冰核装置在冰冻过程期间和之后保持就位。仅在解冻后才去除和处理掉冰核装置,时间可能是之后几天或几年。在实施例中,冰核装置为一次性装置。
冰核装置与asymptote有限公司制造的“viafreeze”器具一起工作最有效。传统的冰冻器具在样本之上吹冷气,这导致外侧的样本冷却得更快。via冰冻系统通过样本底侧上的传导进行冷却,并且每个样本经历相同的冷却分布。
在viafreeze系统中编程的冰冻协议具有用以最大限度地提高冰核装置的有效性的几个方面:
·低于理论冰点几度的保持期,以吸收从熔化潜热释放的能量。例如,如果理论冰点为-3℃,则在冰冻程序中可包括-10℃下8分钟的保持期。
·冰冻转变之后的冷却速率至关重要,并取决于被冰冻样本的性质。例如,对于一些细胞,冷却速率可为例如0.3℃/分钟,或者对于其他细胞为2℃/分钟。对冰核形成的控制对于安全地冷冻保存样本来说至关重要,但如果冰冻后的冷却速率过快或较慢,样本仍可能被破坏。
·一旦冰冻至例如-80℃或-100℃,样本就可以从viafreeze系统中被取出并放置在长期冰冻存储设备中。
样本优选以足够快的速度解冻以保护生物样本。通常,冰冻样本应在十分钟内完全解冻。
本发明的其他实施例在以下编号项目中列出:
1.容纳材料的装置,所述材料使在器皿内形成冰核,器皿的一些壁可渗透水。装置内的冰核剂与包围细胞的溶液接触,但是防止冰核剂的颗粒物污染生物材料。
2.根据项目1所述的装置,其中,冰核材料可包括但不限于任何物理形式的细菌丁香假单胞菌、结晶胆固醇、包封的碘化银和长石。
3.根据项目1所述的装置,其中,成核剂与样本溶液保持接触,而不会通过但不限于以下装置污染所述样本溶液内的生物介质:
a.具有孔眼的分隔屏障
b.具有一系列孔眼的分隔屏障
c.全部或部分由芯吸或海绵材料制成的分隔屏障
d.全部或部分由过滤物或膜材料制成的分隔屏障
e.全部或部分由亲水性过滤物或膜材料制成的分隔屏障
4.根据项目1所述的装置,其中,冰冻剂永久地是样本器皿的一部分。
5.根据项目1所述的装置,其中,冰冻剂可以与样本器皿分离。
6.根据项目1所述的装置,其中,样本器皿可为试管、小瓶、吸管、多套管板或袋。
7.根据项目1所述的装置,其中,可以将独立的多份冰冻剂作为一个整体来处理,因此可以并行处理多个样本,例如,96个套管的多套管板。
8.根据项目7所述的装置,其中,冰核剂被保持在样本的最冷部分附近。
9.在一个实施例中,冰冻剂是保持在腔室中的粉末,冰冻剂包含允许在困住粉末的同时进行液体和气体交换的膜材料。
10.根据上述项目所述的装置,其中,腔室为与样本容器分离的部件,并且可以被移除。
11.根据上述项目所述的装置,其中,多份冰冻剂被连结成一个部件并且可以与多个样本一起并行地使用。
本领域技术人员应理解,尽管已描述了被认为是最佳模式的前述内容,并且在适当的情况下执行本技术的其他模式,但是本技术不应限于本说明书中公开的优选实施例的具体配置和方法。本领域技术人员应认识到,本技术具有广泛的应用范围,并且在不脱离所附权利要求所限定的任何发明构思的情况下,实施例可以进行宽范围的修改。
- 还没有人留言评论。精彩留言会获得点赞!