一种NMOSD动物模型构建方法与流程
本发明涉及动物模型技术领域,具体涉及一种nmosd动物模型构建方法。
背景技术:
视神经脊髓炎谱系疾病(neuromyelitisopticaspectrumdisease,nmosd)是神经病学领域近十年来临床诊治更新和进展最迅速的疾病之一。nmosd是一类视神经与脊髓同时或相继受累的急性或亚急性自身免疫性脱髓鞘疾病,以其致残率高、易复发、预后差等特点严重威胁人类的健康。nmosd与视神经炎、多发性硬化(multiplesclerosis,ms)在临床症状、病程、累及的部位、实验室检查以及对各种治疗的反应性虽然各不相同,但却存在着极大的相似性、连续性和重叠性,仅依赖于以上特点很难将nmosd和ms等疾病区分开。
2004年lemmon和他的同事们首先描述视神经脊髓炎igg抗体(nmo-igg)为nmosd的一个特异性自身抗体标记物,并以其作为标志,诊断nmosd患者的敏感性和特异性分别达73%和91%,是nmosd与ms区别的重要依据。进一步研究证实其靶抗原是位于星形胶质细胞足突上的水通道蛋白4(aquaporin4,aqp4)。目前已经有许多研究表明,nmo-igg不但是nmosd特异的血清生物学标记物,而且在nmosd发病中具有重要作用。
到目前为止,国内外研究学者探索了很多nmo动物模型制作方法,总结主要有以下3种途径:由中枢神经系统髓鞘抗原肽诱导的实验性自身免疫性脑脊髓炎(experimentalautoimmuneencephalomyelitis,eae)模型、颅内注射抗体诱导的nmosd模型、由aqp4反应性t细胞诱导的nmosd模型。
1)由中枢神经系统髓鞘抗原肽诱导的eae模型:该模型的缺点是需要较高剂量的nmosd患者血清抗体(每只lewis大鼠需10mg/天,c57/b6小鼠则需2mg/天);虽然动物的血脑屏障被破坏,但浸润入中枢的t细胞极少,致病性有限,此模型难以模拟出nmosd病程中视神经及脊髓易受累的疾病特点。
2)颅内注射抗体诱导的脱髓鞘模型:该模型易建立,评价指标易检测,一定程度上模拟了人nmosd的特点,具有一定的研究价值。但该模型发病部位局限于注射区域,缺乏视神经及脊髓等好发部位的观察证据,此模型没能模拟出nmosd病程中视神经及脊髓易受累的疾病特点。
3)由aqp4反应性t细胞诱导的nmosd模型:此模型证实aqp4反应性t细胞导致行为障碍中枢少突胶质细胞损害的潜在作用,利于尝试针对aqp4抗原的特异性免疫治疗,但操作步骤较多,精细度要求较高,成功率较低。而且,很多nmosd患者(约40%)在患病前已经存在自身免疫性疾病(系统性红斑狼疮、干燥综合征、重症肌无力、i型糖尿病)等,nmosd患者体内存在多种特异性自身抗体,因此对于自身免疫的可能机制仍需进一步探索;目前约75%的nmosd患者血清中可检测到aqp4抗体,仍有nmo患者血清aqp4抗体阴性,这提示nmo-igg阳性与阴性患者可能具有不同的免疫遗传学背景或与不同的抗原靶标或者抗体检测不敏感等原因有关;不同aqp4分布、亚型及其膜结构是否影响其与nmo-igg的结合程度等。因此,关于nmosd与aqp4抗体关系的具体机制等问题仍需进一步挖掘。
综上所述,目前尚无普遍认可的nmosd动物模型解决更多的问题。因此建立一种有效的动物模型是探索视神经脊髓炎谱系疾病发病机制和病理特点的重要前提,对于进一步发掘治疗视神经脊髓炎谱系疾病可干预的药物治疗靶点具有重要意义。
技术实现要素:
基于以上问题,本发明提供一种nmosd动物模型构建方法,更好地模拟人类相关疾病的发病过程,更客观地反映了nmosd的病理过程及病理特征,为相关的研究提供了新的研究平台。
为解决以上技术问题,本发明提供了一种nmosd动物模型构建方法,包括如下步骤:
s1、建立小鼠eae模型;
s2、提取患者nmo-igg及正常人血清补体;
s3、开放eae模型小鼠血脑屏障:在小鼠eae发病高峰期,麻醉小鼠,颅顶部脱毛;经小鼠尾静脉注射声诺维微泡,用低频聚焦超声探头经颅骨辐照小鼠头部,辐照时间为1分钟;
s4、向eae模型小鼠注射人nmo-igg及补体:每只eae模型小鼠经辐照后立即通过尾静脉注射100μgnmo-igg及100μl补体。
进一步地,步骤s1中eae动物模型包括以下步骤:
1)制备mog抗原稀释液:称量适量mog35~55肽段冻干粉溶于磷酸盐缓冲液溶液中,使其浓度为2mg/ml;
2)制备完全弗氏佐剂:取适量不完全弗氏佐剂,加入灭活结核杆菌,使其浓度达到4mg/ml;
3)制备抗原乳剂:将mog抗原稀释液与完全弗氏佐剂等体积混合,于冰上充分乳化至油包水状态,此时mog35~55浓度为1mg/ml,灭活结核杆菌浓度为2mg/ml;
4)制备eae动物模型:麻醉小鼠,在小鼠背部分四点皮下注射抗原乳剂200μl,在免疫当天和48小时后每只小鼠腹腔注射百日咳毒素200ng。
进一步地,步骤s2中收集nmo-igg强阳性的nmosd患者的血浆,静置过夜后的血浆以1000转/分钟的速度离心10分钟,分离出上清液;利用igg提纯试剂盒分离出nmo-igg,具体操作为:将非igg抗体性蛋白结合胶体和纯化缓冲液分别在室温下放置15分钟;摇匀含有非igg抗体性蛋白结合胶体的瓶子,将100μl非igg抗体性蛋白结合胶体加入离心管里的离心柱;用纯化缓冲液洗涤非igg抗体性蛋白结合胶体两遍;取100μl患者血浆的上清液用300μl纯化缓冲液稀释后,加入到含有100μl非igg抗体性蛋白结合胶体的离心柱里上下颠倒混匀15分钟,之后将离心柱以5000g离心10分钟,收集纯化的igg。
进一步地,步骤s2中正常人血清补体提取步骤为:收集正常人血浆后,室温静置30分钟,以1000转/分钟的速度离心10分钟,分离出上清液,其中富含有活性的补体成分。
进一步地,步骤s3中经小鼠尾静脉注射声诺维微泡的剂量为0.2ml/25g;超声探头参数为:直径190mm,曲率半径150mm,最大压力幅度半值所形成焦斑的直径和长度分别是3和8mm;超声系统参数设定:频率1mhz,焦距2.5cm,辐射总时长为1分钟。
与现有技术相比,本发明的有益效果是:本发明通过采用视神经脊髓炎igg抗体及补体免疫诱导,并通过物理方法无创、短暂、可逆性开放血脑屏障,使nmo-igg及补体可以进入动物中枢诱发视神经脊髓炎谱系疾病,从而建立视神经脊髓炎谱系疾病动物模型;与现有其他动物模型相比,本发明更好地模拟人类相关疾病的发病过程,更客观地反映了nmosd的病理过程及病理特征,为相关的研究提供了新的研究平台。
附图说明
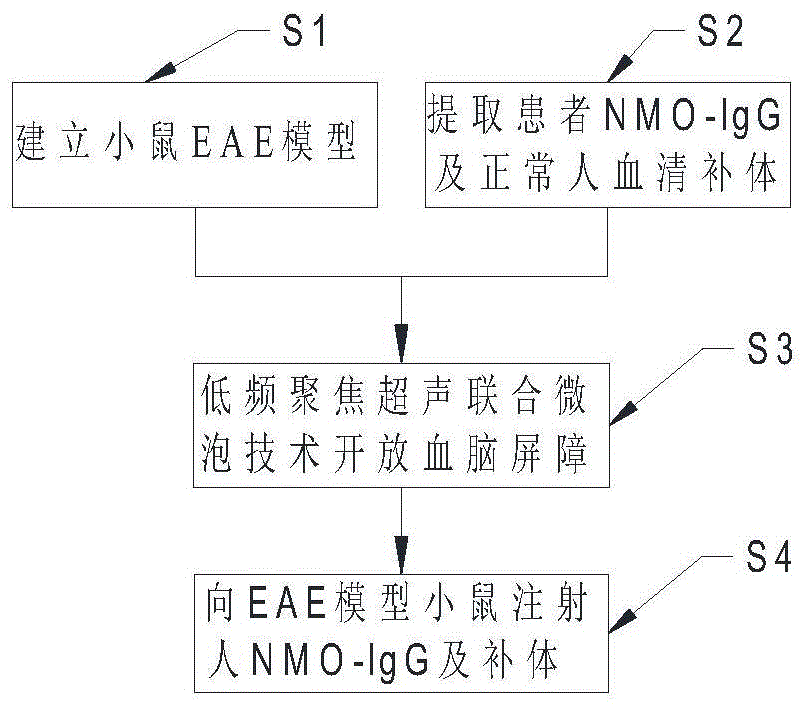
图1为实施例中nmosd动物模型构建方法流程图。
具体实施方式
为使本发明的目的、技术方案和优点更加清楚明白,下面结合实施例和附图,对本发明作进一步的详细说明,本发明的示意性实施方式及其说明仅用于解释本发明,并不作为对本发明的限定。
实施例1:
参见图1,一种nmosd动物模型构建方法,包括如下步骤:
s1、建立小鼠eae模型;
s2、提取患者nmo-igg及正常人血清补体;
s3、开放eae模型小鼠血脑屏障:在小鼠eae发病高峰期,麻醉小鼠,颅顶部脱毛;经小鼠尾静脉注射声诺维微泡作为造影剂,用低频聚焦超声探头经颅骨辐照小鼠头部,辐照时间为1分钟;
s4、向eae模型小鼠注射人nmo-igg及补体:每只eae模型小鼠经辐照后立即通过尾静脉注射100μgnmo-igg及100μl补体。
在本实施例中,采用视神经脊髓炎igg抗体及补体免疫诱导小鼠eae模型,利用低频聚焦超声联合微泡技术开放血脑屏障,使nmo-igg及补体可以进入动物中枢诱发视神经脊髓炎谱系疾病,从而建立视神经脊髓炎谱系疾病动物模型。血脑屏障开放采用了物理方法,具有无创、短暂、可逆性的特点,使nmo-igg及补体可以进入动物中枢诱发视神经脊髓炎谱系疾病,更客观地反映了nmosd的病理过程及病理特征,为相关的研究提供了新的研究平台。
同目前常用的颅内注射抗体诱导的nmosd模型相比,该方法预期可以模拟出nmosd病程中视神经及脊髓易受累的疾病特点;与现有其他动物模型相比,本发明更好地模拟人类相关疾病的发病过程,更客观地反映了nmosd的病理过程及病理特征,提高了动物nmosd模型的成功率,对于进一步发掘治疗视神经脊髓炎谱系疾病可干预的药物治疗靶点具有重要意义。
同时可应用于其他自身免疫性脑病的动物模型,有很大的基础研究价值与临床价值。
实施例2:
s1、建立小鼠eae模型:
1)制备mog抗原稀释液:称量适量mog35~55肽段冻干粉溶于磷酸盐缓冲液溶液中,使其浓度为2mg/ml;
2)制备完全弗氏佐剂:取适量不完全弗氏佐剂,加入灭活结核杆菌,使其浓度达到4mg/ml;
3)制备抗原乳剂:将mog抗原稀释液与完全弗氏佐剂等体积混合,于冰上充分乳化至油包水状态,此时mog35~55浓度为1mg/ml,灭活结核杆菌浓度为2mg/ml;
4)制备eae动物模型:麻醉小鼠,在小鼠背部分四点皮下注射抗原乳剂200μl,在免疫当天和48小时后每只小鼠腹腔注射百日咳毒素200ng。
s2、提取患者nmo-igg及正常人血清补体:
1)步骤s2中收集nmo-igg强阳性的nmosd患者的血浆,静置过夜后的血浆以1000转/分钟的速度离心10分钟,分离出上清液;利用igg提纯试剂盒分离出nmo-igg,具体操作为:将非igg抗体性蛋白结合胶体和纯化缓冲液分别在室温下放置15分钟;摇匀含有非igg抗体性蛋白结合胶体的瓶子,将100μl非igg抗体性蛋白结合胶体加入离心管里的离心柱;用纯化缓冲液洗涤非igg抗体性蛋白结合胶体两遍;取100μl患者血浆的上清液用300μl纯化缓冲液稀释后,加入到含有100μl非igg抗体性蛋白结合胶体的离心柱里上下颠倒混匀15分钟,之后将离心柱以5000g离心10分钟,收集纯化的igg。
本实施例中采用的是赛默飞公司生产的igg提纯试剂盒,包括一整套的试剂,主要有非igg抗体性蛋白结合胶体、纯化缓冲液和离心柱;其中,非igg抗体性蛋白结合胶体用于结合血清中非抗体性蛋白质,如白蛋白和转铁蛋白等;纯化缓冲液具有生理性ph,使得igg可以通过并储存在其中,并保证蛋白的活性和结构稳定。
2)正常人血清补体提取步骤为:收集正常人血浆后,室温静置30分钟,以1000转/分钟的速度离心10分钟,分离出上清液,其中富含有活性的补体成分。
s3、开放eae模型小鼠血脑屏障:在小鼠eae发病高峰期,麻醉小鼠,颅顶部脱毛;经小鼠尾静脉注射剂量为0.2ml/25g的声诺维微泡,用低频聚焦超声探头经颅骨辐照小鼠头部,辐照时间为1分钟;超声探头参数为:直径190mm,曲率半径150mm,最大压力幅度半值所形成焦斑的直径和长度分别是3和8mm;超声系统参数设定:频率1mhz,焦距2.5cm,辐射总时长为1分钟。
s4、向eae模型小鼠注射人nmo-igg及补体:每只eae模型小鼠经辐照后立即通过尾静脉注射100μgnmo-igg及100μl补体。
经上述步骤即可得到视神经脊髓炎谱系疾病动物模型,可通过临床评分、组织学染色、磁共振成像(mri)、视觉图样的记录和图片分析对小鼠视神经脊髓炎谱系疾病进行评估:具体评估方法或评估标准如下:
1.临床评分:在eae诱导后进行,由两名实验者各自分别对小鼠进行评分,采用6级5分制双盲评价,将两人对每只小鼠的评分结果取平均分视为当天小鼠的评分。具体标准如下:0分,小鼠无发病症状;1分,体重下降或小鼠尾巴肌张力减低;2分,小鼠尾巴瘫痪,出现轻度后肢或前肢无力;3分,小鼠出现重度后肢或前肢无力(出现肢体拖曳);4分,小鼠后肢完全瘫痪,并部分前肢瘫痪,人为翻身不能复位;5分,濒死。
2.组织学染色:在模型建立后第七天进行,包括小鼠大脑及视神经苏木精伊红染色及劳克坚牢蓝染色,观察炎细胞浸润、aqp4的脱失、视神经及脊髓髓鞘的破坏情况。
3.mri:在模型建立后第七天进行,通过mri检测小鼠视神经及脊髓的炎性病灶。所用mri为7tmri,扫描参数为tr=1.5s,te=50ms,field-of-view=3cm,imagematrix=192×192,slicethickness=0.4mm。
4.视觉图样的记录和图片分析:在模型建立后第七天进行,荧光显微镜下观察外侧膝状体和上丘整体观以及眼特化区域分离情况:观察小鼠球后视觉通路的缺损、外侧膝状体及上丘的形态及亮度相比于正常小鼠的改变。
如上即为本发明的实施例。上述实施例以及实施例中的具体参数仅是为了清楚表述发明验证过程,并非用以限制本发明的专利保护范围,本发明的专利保护范围仍然以其权利要求书为准,凡是运用本发明的说明书及附图内容所作的等同结构变化,同理均应包含在本发明的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!