电生理学导管设计的制作方法
本发明涉及一种可以减少的成本和复杂性制造的用于改进的标测和组织消融的装置和系统。
背景技术:
医疗过程可用于治疗多种心脏血管病症,例如,心律失常、心房颤动以及电脉冲穿过心脏传输时的其它不规则。作为开心手术的一个替代方案,许多医疗过程是使用微创手术技术执行的,其中一个或多个细长器具穿过一个或多个小切口插入到患者的身体中。此类过程可以涉及具有多个传感器、电极或其它测量和治疗组件的导管或探针的使用以治疗心脏、脉管系统或其它组织的患病区域。对于各种医疗和手术应用微创装置是所希望的,因为与手术相比它们允许较短的患者恢复时间,并且用于以其它方式难以进入的局部离散组织的精确治疗。举例来说,导管可以轻易地插入并且通过血管和动脉,从而允许以相对较少的损伤无创性地进入身体的区域,而其它微创探针或仪器可以插入到小开口中并且经引导穿过靶向身体结构而不会显著影响或扰乱周围组织。微创疗法的一个此类实例涉及心律失常或不规则心跳的治疗,其中医生采用专用心脏评估和治疗装置,例如,标测和/或消融导管,以进入患者的身体的内部区域。此类装置可以包含尖端电极或其它消融元件以形成破坏或阻断穿过靶向组织的电路径的伤口或其它解剖学影响。在心律失常的治疗中,通常在随后的治疗之前首先识别具有异常电活动(例如,局灶触发、缓慢导电、过快复极化、碎裂电图等)的心脏组织的特定区域。这种局部化或识别可以包含获得特定心脏区域的单相动作电位(“MAP”)电图。单相动作电位记录记载复极化期间局部组织去极化的开始和一般动作电位形态。所述MAP信号是通过两个电极之间的测量生成的,第一个电极与血液接触但是通常不接触心肌,并且第二个电极与心肌接触,具有较高的足够局部压力以对底层肌细胞进行去极化。这种增大的局部压力优选地通过相对重要的然而具有较小表面积的与心肌稳定接触的电极形成。MAP信号可以通过对选定的组织进行临时去极化而获得,其中响应性电活动得到记录或者以其它方式监测用于局部去极化计时、不应期持续时间和任何异常电活动的指示。在对异常组织进行标测和诊断之后,医生可以决定通过消融组织对患者进行治疗。心脏组织的精确标测可以减少治疗异常电路径所必需的消融的数目,并且可以使得所执行的消融更加有效。此外,MAP记录可以辅助局部组织激活的计时的确定,而这在使用标准心内电极进行记录时通常是不明确的。MAP信号测量的精确性很大程度上取决于一个或多个标测电极与心脏组织之间的接触的质量。举例来说,由跳动的心脏和非均一心室收缩引起的运动伪影可以使检测到的MAP信号显著失真,因为心脏的移动将改变心脏组织上的标测电极的压力(并且因此改变其间的接触)以及引起电极的不稳定滑动接触。目前已知的诊断性心脏电生理学导管无法精确且可靠地检测MAP信号。另外,组合标测和消融装置通过消除采用用于每个任务的单独标测和消融装置的必要减少了过程时间和复杂性。组合标测和消融装置还增大消融精确性,因为一旦发现异常组织(“目标组织”),可以紧接着开始消融而不需要移除标测装置以及通过消融装置重新定位目标组织。希望的是包含一个或多个较大电极用于射频(RF)消融,因此较大电极面积可以提供用于将从组织中吸收到的热消散到血池中的较大表面积。当使用较小电极并且因此使用较小活性表面积时,电极更有可能引发局部过热,这可以引起血液蛋白质的热变性,从而在电极和治疗位点的下游产生附着的或栓塞的凝结物或其它不希望的影响。相反地,更加精确的电图和MAP记录可以仅通过较小的标测电极获得。为了提供更加有效且高效的医学疗法,因此所希望的是优化所使用的设备和方法以确保在记录MAP信号时标测装置与心脏组织之间的更加均匀的接触。还希望的是拥有可以既记录单相动作电位且随后又根据需要消融局部组织的导管。进一步希望的是提供制造简单且经济的标测设备。
技术实现要素:
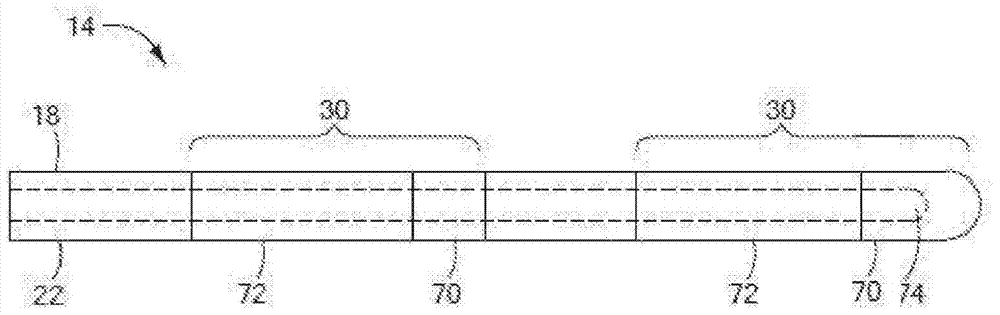
本发明涉及一种装置和系统,其中导电部分和非导电部分可以由相同材料组成。所述装置可以大体上包含:细长主体,所述细长主体具有外部表面;以及金属电极,所述金属电极具有近端部分、远端部分和外部表面,所述电极的近端部分的至少一部分安置在所述细长主体内并且所述电极的远端部分的至少一部分围绕所述细长主体的外部表面安置。所述电极可以由金属组成,例如,金、金合金、具有钽的涂层的金、具有钽的涂层的铜、具有金的涂层的铜、铝钨、钛、钽、铪、铌、锆,及其混合物,例如,钽。安置在细长主体内的电极的部分可以包含基本上绝缘的层,例如,氧化金属的层,例如,铝、钨、钛、钽、铪、铌、锆及其合金。举例来说,氧化金属的层可以是五氧化二钽。电极的远端部分可以围绕细长主体的远端部分的至少一部分的外部表面卷绕,并且卷绕部分可以包含每个大约360°的至少两个线圈。另外,所述电极可以是海波管电极,所述海波管电极具有含有生理盐水的用于在使用期间冷却电极的管腔。在另一实施例中,所述装置可以大体上包含:细长主体,所述细长主体具有外部表面、近端部分和远端部分;以及多个电极,所述电极由钽组成并且具有绝缘的近端部分、导电远端部分和外部表面,多个电极中的每一个的近端部分的至少一部分安置在细长主体内并且具有绝缘的氧化层,并且多个电极中的每一个的远端部分围绕细长主体的远端部分的至少一部分外部表面卷绕。举例来说,所述多个电极可以是海波管电极。在另一实施例中,装置远端组合件可以大体上包含:远端组合件外壳元件,所述元件具有纵轴和外部表面,所述远端组合件外壳元件由导电材料组成,所述导电材料具有在所述外部表面上的基本上上绝缘的层;以及多个电极,所述电极耦合到所述远端组合件外壳元件,所述多个电极由导电材料组成并且基本上具有围绕所述外壳元件纵轴的径向对称性,所述多个电极中的每一个包含整合的电极头部和电极导线,每个电极导线具有外部表面和所述外部表面上的基本上绝缘的层。所述导电材料可以选自由以下各者组成的群组:金属、掺杂半导体、导电聚合物、金属聚合物和金属陶瓷复合物。具体而言,所述导电材料可以是金属,例如,铂、铂合金、金、金合金、具有钽涂层的金、铜、具有钽涂层的铜、具有金涂层的铜、铝、钨、钛、钽、铪、铌、锆及其组合。所述基本上绝缘的层可以是热解石墨、石墨、石墨烯、金刚石、类金刚石碳(DLC)涂层、氧化铝、蓝宝石、氧化锆、钽酸盐、二氧化钛、氧化铍、含有导热粒子的聚合复合物、纳米粒子、自身组装纳米粒子、纳米材料和复合物、橄榄油、医学级聚硅氧油或其组合。举例来说,所述导电材料可以是钽并且所述基本上绝缘的层可以是五氧化二钽。所述系统可以大体上包含:射频能量来源;具有纵轴的远端组合件外壳元件,所述远端组合件外壳元件由导电材料组成并且与所述射频能量来源电连通;以及多个电极,所述电极耦合到所述远端组合件外壳元件并且与所述射频能量来源电连通,所述多个电极由导电材料组成并且基本上具有围绕所述外壳元件纵轴的径向对称性,所述多个电极中的每一个包含整合的电极头部和电极导线,每个电极导线具有外部表面和所述外部表面上的基本上绝缘的层。另外,基本上绝缘的层可以安置在所述远端组合件外壳元件与所述多个电极之间,使得所述远端组合件外壳元件和多个电极是彼此电绝缘的。附图说明通过在结合附图考虑时参考以下详细描述将更容易理解本发明的更完整的理解及其随附优势和特征,在附图中:图1示出了包含具有远端组合件的导管的医疗系统;图2示出了第一实施例远端组合件;图3示出了图2所示远端组合件的球茎式导线;图4示出了结合阳极氧化和退火的球茎式导线使用的电化学电池的示意图,例如,在钽表面上形成五氧化二钽层;图5示出了被适配成含有球茎式导线的固持器的简化描绘,所述球茎式导线用于结合将进一步防腐蚀性或选择性导电性赋予图2的球茎式导线的过程使用;图6A示出了远端组合件的第二实施例;图6B示出了远端组合件的第三实施例;图7A示出了远端组合件的第四实施例;图7B示出了远端组合件的第五实施例;图8示出了远端组合件的第六实施例;图9A示出了远端组合件的第七实施例;图9B示出了远端组合件的第八实施例;图9C示出了远端组合件的第九实施例;图10A-10H示出了远端组合件的第十实施例的各种配置;图11示出了远端组合件的第十一实施例;图12A示出了远端组合件的第十二实施例;以及图12B示出了图12A所示远端组合件的实施例的前部表面的视图。具体实施方式如本文中所使用,术语“远端组合件”是指具有标测和/或消融功能性的医疗装置的远端部分。如果所述医疗装置包含细长主体,那么远端组合件的至少一部分可以是细长主体的远端(例如,如图9A-10中所示出),或者远端组合件可以基本上固定在所述医疗装置的远端部分上,围绕所述医疗装置的远端部分安置或整合到所述医疗装置的远端部分(例如,如图2和6A-7B中所示出)。如本文所用,术语“选择性导电金属”是指具有氧化物形式或涂层的金属,其表现类似于电容器,使高频电流和脉冲能量通过但是阻断直流电和低频信号的传输。所述金属,例如,铝、钨、钛、钽、铪、铌、锆(及其合金),以及具有钽的薄膜的金或铜或具有金的薄膜的铜可以是完全导电的。另一方面,该金属的氧化物可以具有对高频电流的低阻抗,因此是选择性导电的,并且可以具有对低频或直流电流的高阻抗,因此具有选择性绝缘特性。现在参考图1,示出了医疗系统10,所述医疗系统包含导管12,所述导管具有远端组合件14。系统10通常可以包含耦合到控制台16或其它操作设备的医疗装置12(例如,导管或手术探针)。导管12具有可定位在目标组织区域处或附近的远端组合件14。导管12可以具有细长主体或具有近端部分20、远端部分22的导管轴杆18,并且可以在其间界定0管腔(在图1中未示出)。细长主体18的远端部分22可以包含与远端组合件14和控制台16电连通的一个或多个参比电极24。控制台16可以包含一个或多个计算机26,用于储存数据、解译从所述装置接收的信号(例如,确定接收到的信号是否指示患者的心脏内的异常电活动)、生成警示、控制所述系统等等,并且还可以包含一个或多个流体储槽27、真空装置、电源等等。细长主体18可以是柔韧的且具有弹性的,并且具有足够的管柱强度和扭转刚度以促进与组织的平稳接触从而在标测所接触的组织时改进信号保真度。导管12也可以具有固定到细长主体的近端部分20的手柄28,所述手柄可以包含一个或多个流体入口和出口端口、致动器、连接器以及其它控制和/或连接元件。远端组合件14耦合到细长主体18的远端部分22,并且包含一个或多个标测和/或消融电极30,每个电极包括电极头部32和电极导线34。一个或多个电极30可以永久地固定到电极组合件外壳36(如图2-5中所示和描述)。远端组合件14可以至少可操作用于标测目标组织区域,但是也可以可操作为治疗组合件。举例来说,控制台16可以包含与电极30或电极组合件外壳36中的一者或多者电连通的射频(RF)发生器或高压脉冲能量发生器38,使得远端组合件14也可以用于消融或电穿孔目标组织区域。导管12和系统10可以构造成通过多种能量形态中的任一种使用,包含冷冻消融、RF消融和电穿孔。另外,导管12和系统10可以构造成用于标测组织,例如,记录和处理来自心脏组织的电图。大体上参考图2-10,示出且描述了远端组合件14的实施例以及制造方法。在所有实施例中,远端组合件14提供优于目前已知装置的经济的且质量优的优势。举例来说,虽然所有实施例可以提供更精确的标测,但是图2的远端组合件14可以在具有较少组件和制造步骤的空间节约配置中提供组合的标测和消融功能性,而图6A、6B和8-10的远端组合件14可以进一步提供具有组合功能性而无需根据不同材料形成每一组件的优势。另外,图8-10的远端组合件14可以提供包含促进标测电极与组织之间的接触的特征的优势。最后,图7A和7B的远端组合件14可以提供包含具有标测和消融功能性的单个电极的优势。图2-10的远端组合件14可以包含由选择性导电材料组成的组件(例如,标测和/或电极和/或外壳组合件)。金属氧化物(例如,五氧化二钽)可被称为“选择性导电金属”。举例来说,五氧化二钽是选择性导电的。也就是说,它具有阻断直流电(DC)同时允许高频率电流传导(例如,射频能量)的独特能力。五氧化二钽优先传送高频率电流但是阻断DC传输。具有氧化物的钽、铝、钨、钛、铪、铌、锆及其混合物等金属是选择性导电的。另外,掺杂半导体,例如p型和n型掺杂硅和镓,以及由陶瓷和导电聚合物、金属聚合物制成的复合材料、金属陶瓷复合材料和一些纳米材料也可以选择性导电的。另外,钽(Ta)和钽化合物,例如,晶粒稳定化钽(TaKS)、五氧化二钽(Ta2O5)、钽钨(TaW)、电容器品质钽(TaK),或类似物是高度抗腐蚀的。钽化合物还显示出优良的冷延展性、高熔点(例如,钽具有3,017℃的熔点)、杰出的水溶液和金属熔化阻抗、超导性和高水平的生物相容性。另外,例如TaKS是不透射线的,使其较适合于在必须位于患者的身体内且通过患者的身体的导管中使用。钽和钽化合物甚至可以比MP35N(通常用于非磁性的导管导线等医学可植入装置的镍钴铬钼合金材料,其具有高抗张强度、良好的延展性和韧性以及优良的防腐蚀性)更耐久并且与铂相比不太昂贵。另外,如图7A和7B中所示出,远端组合件14可以包含单个电极30,其中所述电极的至少一部分由钽化合物(例如,Ta2O5)组成并且所述电极的至少一部分由不同材料(例如,金、金合金、涂覆有金的铜或铂)组成。因此,电极的钽部分可用于使用例如RF能量来消融或电穿孔组织(例如,肾、肝、或前列腺组织),而电极的非钽部分可用于将直流电刺激传递到组织或记录来自组织的直流电。现在参考图2,示出了远端组合件14的第一实施例。远端组合件14可以包含外壳36和一个或多个电极30,例如,单相动作电位(MAP)电极,每一电极放置在距离外壳36的纵轴40的径向距离处。如果使用两个电极30,那么电极30可以相对于彼此放置。如果使用三个或三个以上电极30(例如,图2中示出的四个电极),那么电极30可以具有围绕外壳纵轴40的径向对称性。图2中示出的远端组合件14可以已经根据图3-5中示出且描述的方法形成。举例来说,可以形成一个或多个球茎式导线42,所述球茎式导线包括球茎部分44和导线部分46(如图3中所示和描述)。每个球茎式导线42的导线部分46可以随后阳极化(如图4中所示和描述),并且每个球茎式导线42的球茎部分44可以由非阳极化材料组成或者电镀、溅镀或离子嵌入有防腐材料或具有其它有益特性的材料(如图5中所示和描述)。在一个或多个球茎式导线42已经得到处理(例如,阳极化和电镀)后,导线42可以放置到并且结合到电极组合件外壳(被称作“组合件外壳”)36中。举例来说,可以使用四个球茎式导线42。在此阶段(也就是说,当球茎式导线42安放在标测组合件外壳36内时),球茎式导线被称作电极30,包括电极头部32和电极导线34。在图2中所示的实施例中,电极30和电极组合件外壳36统称为远端组合件14。然而,并非所有实施例都包含外壳36(例如,图6A、6B、9和10A-10C的实施例)。组合件外壳36包含前部表面48,一个或多个电极头部32可以从所述前部表面突出。替代地,电极头部32可以安装在组合件外壳36内,使得电极头部32基本上与电极外壳36的前部表面48齐平。举例来说,组合件外壳36可以包含插座,所述插座经尺寸设定以接收每个电极30,使得在外壳耦合到细长主体后,电极头部32安放在插座内并且电极导线34穿过插座中的开口并且进入到细长主体中。可以使用粘合剂、热塑物或其它已知的技术将电极30固定到电极组合件外壳36。图2-5的远端组合件14可以尤其适用于诊断性目的,即,标测。然而,远端组合件14替代地可用作组合消融和标测装置12的一部分。举例来说,组合件外壳36可以与能量来源(例如,RF能量)电连通并且由导电材料组成,或涂覆或包覆有导电材料,因此电极30可用于标测并且外壳36(其可以具有与标测电极相比的较大“占据面积”)可用于消融。在这种情况下,可以并入薄绝缘层以将电极头部32与组合件外壳36电隔离。举例来说,绝缘层可以安置在组合件外壳36的插座内。替代地,组合件外壳36和电极30可以由导电材料组成,但是外壳36可以包含选择性导电材料的外层。额外地或替代地,组合件外壳36可以由低硬度计、弹性材料组成,例如,硅酮、聚合物或导电聚合物、充气球、凝胶、纤维复合物或其类似者,所述弹性材料与不规则的几何形状相符同时确保电极头部32与目标组织区域之间的接触。举例来说,随着心脏的跳动,可变形外壳可以吸收压力以保持电极头部与目标组织区域之间的接触。在组装后,远端组合件14可以耦合到细长主体18的远端部分22,其中电极导线34提供远端组合件14与导管12和/或系统10之间的电气连接。因此,整个远端组合件14可以包含少至两个组件(例如,如果使用单个电极和远端组合件外壳)。在一个非限制性实施例中,如图2中示出的远端组合件14可以包含六个组件:四个电极30、组合件外壳36和参比电极24。组合件外壳36和电极30可以由相同材料组成。至少在电极中此实施例包含与已知的标测组合件相比较少的组件,这降低了成本和组装时间同时提供较高的可靠性。现在参考图3,示出了图2的远端组合件14的球茎式导线42。球茎式导线42可以从一定体积的金属中制造或模制,使得球茎44或基本上球形的形状在一端(被称作“球茎”)处形成,例如,通过冷成型和/或挤压。球茎44可以变为电极头部32(例如,如图2、4和5中所示和描述),因此它可以具有适合于最终标测组合件的任何尺寸。具有单件电极头部32和电极导线34消除了将电极焊接到导线的必要。两件式系统也是可行的,但是将增大成本和制造时间以及复杂性。球茎式导线42可以由高度防腐材料组成,例如,钽或钽化合物(例如,Ta2O5或TaKS)。现在参考图4,示出了用于与阳极氧化且退火的球茎式导线42结合使用的电化学电池50的示意图。在形成图3的球茎式导线42后,导线部分46可以阳极化以在导线部分46的外部表面上形成薄氧化物层。举例来说,绝缘层可以大约1μm厚。在阳极氧化过程期间,将导线部分46放置到含有例如H3PO4、H2SO4、酒石酸铵或其类似者的电解质溶液54的容器52中。容器52还可以包含圆柱形网状电极56,并且将要氧化的导线部分46可以穿过圆柱形网状电极56的中心安置。网状物56和导线46可以耦合到可控制电源58。随后,电流(直流、交流或脉冲电流)可以通过溶液54,从而围绕导线46形成氧化物层。此氧化物层进一步保护导线以防止腐蚀并且使导电屏障能够电隔离导线与邻近组件和结构。多个球茎式导线42的导线部分46可以一次阳极化。虽然整个结构可以阳极化,但是优选实施例仅阳极化将邻近于其它导电结构的组合件的区域以提供绝缘屏障。举例来说,导线46和球茎44可以由钽组成,并且仅导线46可以随后阳极化以形成氧化物层。此过程可用于本文所示出和描述的包含氧化物层的任何远端组合件的组件。现在参考图5,示出了固持器60的示意图,所述固持器被适配成含有球茎式导线42,用于与向图3的球茎式导线42赋予进一步防腐蚀性的过程结合使用。在阳极化之后,一种或多种材料可以沉积在球茎44上以促进导电性、提供增加的防腐蚀性或赋予其它有益的品质。举例来说,氧化铱可以电沉积在球茎44上或者镍钛合金可以溅镀到球茎44上。额外地或替代地,溅镀可用于沉积镍钛合金、金、金合金、铂或基于铂的合金或其类似者。然而,也可以使用其它材料和技术。举例来说,导线42可以由具有钽涂层的金组成。球茎44上的钽涂层可以是蚀刻的,并且曝露的金可以随后得到阳极化或者电镀、溅镀或离子嵌入有铂-铱的涂层。在处理球茎44之前(例如,通过电沉积或溅镀),可以将一个或多个球茎式导线42放置到固持器或容器60中以将它们固持在适当位置。固持器或容器60可以被适配成固持任何数目的导线42,并且可以大体上固持导线42,使得球茎44在固持器60的顶部上是可进入的(如在图3中所示)。在导线42就位后,可以对球茎44进行处理。现在参考图6A和6B,示出了远端组合件14的第二和第三实施例。在两个实施例中,电极头部32(导电部分)和电极导线34(绝缘部分)不仅由相同材料组成,而且还由单件材料形成(统称为“电极”)。这可以减少制造成本和复杂性。另外,一个以上电极导线34可在导管主体18内使用而无需包含导线之间的绝缘材料。在图6A中示出的实施例中,多个(例如,三个)电极导线34安置在医疗装置内,例如,导管细长主体18。每个导线34可以由金属(例如,钽或TaKS)组成并且包含外部绝缘氧化物层(例如,五氧化二钽)。当低频率或DC电压流过导线时,导线34将充当能量的绝缘导体。因此,在医疗装置内不需要额外的绝缘材料来电隔离每个导线34与其它导线。这不仅可以增大医疗装置内用于拉线、推杆等其它组件的可供使用的空间,而且还可以减少制造成本和复杂性。每个导线34可以延伸穿过细长主体18的内部部分一段距离,并且随后在出口点62处离开细长主体18的壁。从出口点62,导线34可以随后围绕外部远端部分安置在一个或多个线圈64中,这可被称为电极头部32。不同于导线34,此外部卷绕部分64可不包含氧化层,并且因此可以是导电的。另外,卷绕部分64可以具有亲水涂层以减少在线圈的匝内收集空气的可能性。电极30可以如图3-5中所示和描述制得。另外,医疗装置的外壳或至少一部分(例如,细长主体)可以包覆模制到电极上以在出口点62处提供密封。细长主体18的远端尖端66可以具有非创伤性磨圆的或钝的配置以防止在标测和/或消融过程期间对患者造成损伤。图6B中示出的实施例具有与图6A中示出和描述的实施例基本上相同的配置,不同之处在于可以使用海波管68来代替导线。与图6A中的实施例的导线类似,海波管68可以包括电极30(导电部分)和“导线”34(绝缘部分);然而,不同于图6A中的实施例,海波管68可以含有一定体积的冷却剂或生理盐水溶液,用于在消融过程期间(例如,在RF消融期间)冷却海波管68的电极30部分。图6A和6B中示出的两个实施例的导电部分都可用于标测和/或消融。小直径海波管在任何取向上逆着心内膜提供增大的局部组织接触压力,从而提供可靠的MAP记录能力。现在参考图7A和7B,示出了远端组合件14的第四和第五实施例。这些实施例包含具有标测和消融功能性的电极30。如图7A中所示,一个或多个电极30可以围绕医疗装置的远端部分22安置,例如,导管的柔韧的细长主体18。虽然图7A示出了两个电极30,但是可以使用任何数目的电极30。每个电极30可以包含导电区域70和选择性导电的区域72。如本文所描述,电极30可以由高度导电的金属(例如,金)组成并且可以包含金属(例如,钽)的薄膜涂层,并且选择性导电区域72可以包含外部氧化物层,而导电区域70并不如此。氧化物层可以是铝、钨、钛、钽、铪、铌、锆(及其合金)的氧化物。在五氧化二钽的情况下氧化物层可以在大约10nm到大约5000nm之间,优选地在大约100nm到大约1000nm之间。另外,导电区域可以具有导电材料的层,例如,溅镀、离子嵌入或电沉积在外表面上的金或金合金。导电区域70可以具有与选择性导电区域72相比较小的表面积。作为非限制性实例,可以将两个电极30放置在装置远端上,使得导电区域70各自位于电极30的远端上,并且电极30是通过装置(例如,导管细长主体)的材料间隔开一定距离的,所述材料提供电极之间的绝缘。另外,流体管腔74可以安置在细长主体18内,所述细长主体与生理盐水或类似流体的来源流体连通,用于冷却电极30。在使用期间,通过低频心内电图或直流电电压的电极30的测量将仅来自导电区域70中的电极的部分,而选择性导电区域72通过氧化物层绝缘且并不测量电图。如上文所述,较小电极30不大可能在高压下发生腐蚀并且产生更加精确的电图。激活具有高频脉冲或RF能量的电极30可能引起整个电极30、导电区域70和选择性导电区域72充当消融电极,当在标测过程期间选择性导电区域72绝缘时所述消融电极具有与电极相比更大的占据面积。图7B中所示的实施例大体上以与图7A中所示的实施例相同的方式起作用。然而,图7B示出了围绕装置的远端部分22径向布置的两个电极30(然而可以使用任何数目的电极)。也就是说,每个电极30可以基本上安置在装置(例如,细长主体18)的远端区域22的离散圆形区段内。流体管腔74可以在装置的远端尖端66处界定开口76,并且每个电极30的导电区域70可以最接近于管腔开口76或远端尖端66以在选择性导电区域72绝缘时促进标测。当选择性导电区域72导电时,每个电极30的全部可以充当消融电极。在图7A和7B这两者中,含有生理盐水或类似无毒性流体的流体管腔74可以对于环境开放,并且可以允许生理盐水离开所述装置穿过管腔开口76进入到患者的血流中。替代地,流体管腔可以与制冷剂的来源连通,所述制冷剂膨胀以冷却电极30,并且在它在靠近电极30的装置的远端部分22中膨胀之后通过真空恢复。现在参考图8,示出了远端组合件的第六实施例。远端组合件14可以具有大体上圆锥形形状,但是可以包含一个或多个突出电极环78(例如,在图8中示出了三个突出电极环78)。突出电极环78可以具有磨圆的边缘以防止患者受到伤害。在突出电极环78之间可以是一个或多个凹陷绝缘部分80。突出电极环78和凹陷绝缘部分80可以由相同材料组成。举例来说,突出电极环78和凹陷绝缘部分80可以由金属组成(例如,钽),并且凹陷绝缘部分80可以具有氧化物层(例如,五氧化二钽)或者可以具有电绝缘和导热材料的涂层(例如,类金刚石碳)。作为非限制性实例,氧化物层或导热材料的层可以在大约10nm到大约5000nm之间。突出电极环78可以充当标测电极,并且突出可以促进环与组织之间的接触并且建立环与组织之间的较高局部压力,由此促进标测过程期间组织的去极化并且提供更加可靠且精确的标测(例如,MAP)信号记录。另外,如果绝缘部分80由选择性导电材料组成,突出电极环78和绝缘部分80这两者也可以能够充当单个较大消融电极。替代地,绝缘部分80可以由不同材料组成。尽管这可能添加制造成本和复杂性,但是远端组合件的配置将仍然起作用以产生更好的标测信号。现在参考图9A-9C,示出了第七、第八和第九实施例。所有三个实施例可以包含卷绕海波管电极68,所述电极围绕医疗装置的远端部分22安置,例如,标测和/或消融导管的细长主体18。将理解附图仅示出了单个卷绕,但是额外的更多近端卷绕可以包含在消融装置中。在此类实施例中,近端卷绕可以如先前所描述制成选择性导电的。在每个实施例中海波管68可以与生理盐水或类似流体的来源流体连通(如图7A和7B中所描述),或者与低温流体连通,用于冷却海波管电极68。小直径海波管可以提供抵靠心內膜的任何取向上的增大的局部组织接触压力,提供可靠的MAP记录能力。海波管68可以卷绕或缠绕细长主体18的远端部分22,海波管68围绕细长主体18的远端部分22卷绕至少大致上360°。替代地,海波管可以包含远离细长主体18的线圈或卷绕82(如图9A-9C中所示)。替代地,海波管可以包含围绕细长主体的远端部分安置的或远离细长主体18的多个线圈或卷绕82。另外,每个实施例的海波管68可以由金属(例如,钽或不锈钢镀覆的金或金合金)组成并且包含具有氧化物层(例如,五氧化二钽)的一个或多个交替的选择性导电区域72或更多近端海波管卷绕(未图示)。作为非限制性实例,氧化物层可以在大约10nm到大约5000nm之间,优选地在大约100nm到大约1000nm之间。曝露的(非氧化)导电区域70可以与氧化的选择性导电区域72相比较小(也就是说,具有较少表面积)以促进在记录心內电图时的标测期间的信号质量。最后,所有实施例可以包含与海波管68接触的一个或多个热电偶或热敏电阻84以监测海波管68的温度。图9A的海波管可以包含线圈82,所述线圈具有基本上平滑的圆周而没有任何凸块、隆脊或纹理。相反地,图9B的海波管68可以包含多个元件86,所述元件从海波管68的表面突显(或突出)以进一步促进在与每个突显元件86接触的位点处与组织的局部较小面积接触压力,因此通过增大突出元件86下方的组织上的局部压力促进MAP信号记录能力。每个突显元件86可以从海波管68的表面延伸,例如,海波管的外圆周或周长。虽然图9A中示出了四个突显元件86,但是将理解任何数目的突显元件86可用于促进海波管68与所关注的组织之间的接触。类似地,图9C的海波管68可以弯曲以包含一个或多个基本上有角度的弯曲88。每个弯曲88可以从海波管68的外圆周突显(或突出),因此围绕海波管68形成突显位点以进一步促进与组织的局部较小面积接触压力并且改进MAP信号记录能力。虽然图9C示出了三个突出的弯曲88,但是将理解可以包含任何数目的弯曲以促进当装置抵靠着所关注的组织放置在大部分的任何取向时MAP信号的记录能力。替代地,图9A-9C中所示的实施例可以制成完全具有导电表面而不具有选择性导电区域。现在参考图10A-10H,示出了远端组合件14的第十实施例的各种配置。图10A-10H中所示的实施例可以具有导管的一般外观,例如,由消融前沿(明尼苏达州、明尼阿波利斯的Medtronic有限公司)所销售的肺静脉消融导管(PVAC),所述导管是导线上方的圆形标测和消融导管。PVAC装置可以包含托架臂90,所述托架臂承载一个或多个电极,通常具有九个或十个电极30。虽然图10B-10H示出且描述了托架臂90上的仅两个电极30,所描述的电极30的特征也将适用于包含在托架臂90上的任何其它电极30。电极30可以是导电的,并且托架臂90可以由非导电材料91组成(如图10A中所示)。替代地,图10A-10H的实施例可不包含个体电极,而是实际上是柔韧的弯曲的托架臂90,所述托架臂由金属(例如,金)组成,所述金属是电绝缘的但是是导热涂覆的(例如,类金刚石碳)或者具有选择性导电涂层(例如,具有经氧化从而形成五氧化二钽的钽的薄膜涂层的金),具有一个或多个交替的未经涂覆的导电区域70。作为非限制性实例,氧化物层可以在大约10nm到大约5000nm之间,优选地在大约100nm到大约1000nm之间。曝露的或未经涂覆的导电区域70可以与氧化的选择性导电区域72相比较小(也就是说,具有较小表面积)(或是电绝缘的但是是导热区域)以促进在测量心內电图电压时标测期间的信号质量。替代地,导电区域70和选择性导电区域72可以是相同尺寸的。作为其中电极30承载在托架臂90上的非限制性实例,托架臂90可以具有大约25mm的直径,并且每个电极30和在电极30之间的托架臂90的部分可以是大约3mm宽。另外,托架臂90可以包含固定到其上的十个电极。托架臂90的第一端92可以固定到(例如)装置的细长主体18,而托架臂90的第二端94可以固定到可滑动地收纳在所述装置内的导引线护套96。因此,当导引线护套96收缩或部分地收缩时当导引线护套96延伸到弯曲治疗配置时,托架臂90可以是从基本上线性的输送配置可过渡的。举例来说,图10A示出了部分地收缩的导引线护套96,并且托架臂90在托架臂90的第一端92与第二端94之间延伸大约360°。图10B示出了托架臂90的一部分近距视图,其中导电区域70是完全导电的。整个托架臂90可以是非导电或选择性导电的,以便在应用高频率或脉冲电流(例如,RF电压)时对组织进行消融或电穿孔。替代地,托架臂90可以是电绝缘的且是导热的,如针对图10C-10H所描述。另外,虽然图10B示出了固定到托架臂90的电极30,但是电极30可以整合到托架臂90,如上文中在图10A中所述。在图10B中所示的实例中,导电电极30固定到托架臂90,并且托架臂90是选择性导电的72。另外,图10B中所示的导电70电极30可以一直围绕托架臂90的截面的圆周缠绕。图还示出了电图信号的一部分(插图)。图10C-10H示出了托架臂90部分的特写视图,其中电极30是部分导电的。也就是说,电极30仅在某些区域导电,具体而言是将接触目标组织的区域(例如,托架臂90的前部或面向组织的表面48)。举例来说,电极30可以由固定到托架臂90的外表面的材料(例如,金或金合金)组成(所述材料可以是非导电的91、选择性导电的72,或是电绝缘的但是是导热的97;在图中描绘为“92/72/97”),并且仅电极30的一部分可以未经涂覆或曝露(也就是说,导电的)。电极30的剩余的部分100可以选择性导电(例如,由具有已经氧化从而形成五氧化二钽的钽的薄膜外层的金组成)或是电绝缘的但是是导热的(例如,具有类金刚石碳的外层)。电绝缘的但是导热的层可以将热消散到血流中,然而防止到未组织接触的非面向组织表面的能量损失。电绝缘的但是导热的层可以是一种或多种材料的薄涂层,例如,热解石墨、石墨、石墨烯、金刚石、类金刚石碳(DLC)涂层、氧化铝、蓝宝石、氧化锆、钽酸盐、二氧化钛、氧化铍、含有导热粒子的聚合复合物、纳米粒子、自身组装纳米粒子、纳米材料和复合物、生物相容性导热流体状橄榄油、医学级聚硅氧油和类似材料。另外,此层可以在大约10nm和大约5000nm之间。替代地,电极30可以整合到托架臂90,其中导电区域70是曝露的或不具有外部氧化物层或是电绝缘的但是是导热材料(例如,类金刚石碳)的层。在任一配置中,电极30和托架臂90(例如,如果托架臂90选择性导电的话)这两者的非面向组织的表面可以包含电绝缘但是导热的层,其中仅电极30的前部或面向组织的表面是导电的。另外,在所有实施例中,导电区域70可以小于非导电或选择性导电部分,或者它们可以是相同尺寸的。本文中所示出的图可以都不按比例绘制。图10C-10H还示出了可以使用图10C-10H的装置获得的增强电图信号的一部分(插图)。在图10C-10E中,电极30的导电区域70可以是线性的。在图10F-10H中,导电区域70可以是基本上圆形的。在图10G和10H中,圆形导电区域70可以是升高的或者可以从托架臂90的表面以突显凸块102突出。如图9B和9C中所论述,此突显凸块102可以进一步促进电图信号质量。另外,当施加非常小或开放信号滤波时(例如,大约0.5Hz到大约1000Hz),突显凸块102可以在抵靠着非面向组织的参比电极24进行参考时产生单相动作电位,如图10H中所示。参比电极24可以位于细长主体17的远端部分上(如图10A中所示)或者位于托架臂90的非面向组织的表面上(未图示)。现在参考图11,示出了远端组合件的第十一实施例。所述装置可以是具有磨圆的远端尖端66的聚焦导管。标测和消融电极30可以安置在远端尖端66和细长主体18的远端部分22的部分上,如图所示。电极30可以包含导电区域70和非导电或选择性导电区域104。在一个配置中,区域104可以是选择性导电的。导电区域70和选择性导电区域104这两者可以由金属(例如,金或金合金)组成,并且选择性导电区域104可以(例如)具有金上方的钽的薄膜层并且钽层可以氧化成五氧化二钽。作为非限制性实例,氧化物层可以在大约10nm到大约5000nm之间,优选地在大约100nm到大约1000nm之间。在这种情况下,导电区域70可以用于标测过程并且整个电极30可以用于消融或电穿孔过程(例如,如图2中更详细描述的)。在另一配置中,区域104可以是非导电的。整个电极30可以由导电金属(例如,金或金合金)组成,但是非导电区域104可以具有带高度导热但是完全电绝缘的材料的涂层,例如,热解石墨、石墨、石墨烯、金刚石、类金刚石碳(DLC)涂层、氧化铝、蓝宝石、氧化锆、钽酸盐、二氧化钛、氧化铍、含有导热粒子的聚合复合物、纳米粒子、自身组装纳米粒子、纳米材料和复合物、生物相容性导热流体状橄榄油、医学级聚硅氧油和类似材料。在这种情况下,所述装置可以提供增强的电图信号质量(由于用于标测过程的电极30的较小区域和涂层的干扰减轻效果)、高冷却能力和到血流的消融或电穿孔能量的减少的损失。现在参考图12A和12B,示出了远端组合件的第十二实施例。远端组合件14可以包含一个或多个托架臂106,所述托架臂承载一个或多个标测和/或消融电极30。在图12A中为了简单起见示出了一个托架臂106,然而,可以使用两个或两个以上托架臂106。举例来说,图12B示出了包含两个托架臂106的远端组合件14的前部或面向组织的表面48。每个托架臂106可以包含位于托架臂106的前部或面向组织的表面48处的第一部分108和耦合到装置12的两个第二部分110,在所述第一部分上承载有一个或多个标测和/或消融电极30。远端组合件14可以进一步包含一个或多个参比电极24。电极30中的每一个可以包含导电区域70和电绝缘的但是高度导热的区域97。举例来说,导电区域70和绝缘区域97这两者可以由金或金合金组成,而绝缘区域97可以包含类金刚石碳(DLC)的薄膜涂层或层。虽然在图12A或12B中未示出,电极30可以由具有钽的薄膜表面的金组成,并且可以包含选择性导电区域72,其中钽层经氧化从而形成五氧化二钽。这些选择性导电区域72可以很大程度上对应于图12A和12B中所示的绝缘区域97。作为非限制性实例,氧化物层可以在大约10nm到大约5000nm之间,优选地在大约100nm到大约1000nm之间。每个托架臂106的第一部分108和第二部分110会合的点可以形成锐角。每个臂106的第二部分110可以固定到可在装置12的细长主体16内可滑动地移动的轴杆,或直接固定到细长主体18。另外,远端组合件14可以由弹性且可变形的材料组成,并且可以采用用于输送的第一位置(未图示)和用于标测和/或治疗的第二位置(如图12A中所示)。当在第二扩展位置时,每个臂106的第一部分108可以位于基本上正交于装置12的纵轴的平面上。再者,弹性和可变形的材料可以朝向第一或第二位置偏置并且可以通过一个或多个拉线、导引线、棒或在装置12的手柄28处或附近可控制的其它转向机构操纵。一个或多个电极30能够传输低频电流和高频电流这两者,并且可以适合于标测、消融和/或电穿孔。具体而言,在图10和12中所示出和描述的实施例可以适合于解剖学放置,使得电极30的某些区域将是接触组织的而同时其它区域将仅接触血液。Medtronic(美敦力)消融前沿肺静脉(PVAC)是在图10A-10H中所示和描述的此类装置的一个实例,并且Medtronic(美敦力)消融前沿多阵列(MAAC)是在图12A和12B中所示和描述的此类装置的一个实例。电极30的曝露的完全导电区域70专门放置于将接触心肌的电极30的区域中,所述区域将以电气方式标测和潜在地消融。在一些实施例中,电极30的非面向心肌的部分可以涂覆有电绝缘材料,所述电绝缘材料还高度导热。涂层所提供的两个重要功能是:在标测期间,面向表面的非心肌(组织)并不收集使局部电图的品质降级的远场电信号;以及在消融(例如,RF消融)或电穿孔期间,非面向肌肉的表面并不浪费能量所述血液,而是这些表面用来消散通过面向电极的侧面组织所收集的热,使热穿过电极并且到达流动的血液中。所属领域的技术人员将了解本发明并不限于上文中已经具体示出且描述的内容。此外,除非上文提及相反的内容,否则应注意所有的附图不是按比例的。鉴于以上教示在不脱离本发明的精神和范围的情况下多种修改和变化是可能的,所述修改和变化仅受所附权利要求书的限制。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1