菊粉山药多糖组合物在制备具有调节肠道内菌群功效的保健食品中的用途的制作方法
本发明涉及生物
技术领域:
,特别涉及菊粉山药多糖组合物在制备具有调节肠道内菌群功效的保健食品中的用途。
背景技术:
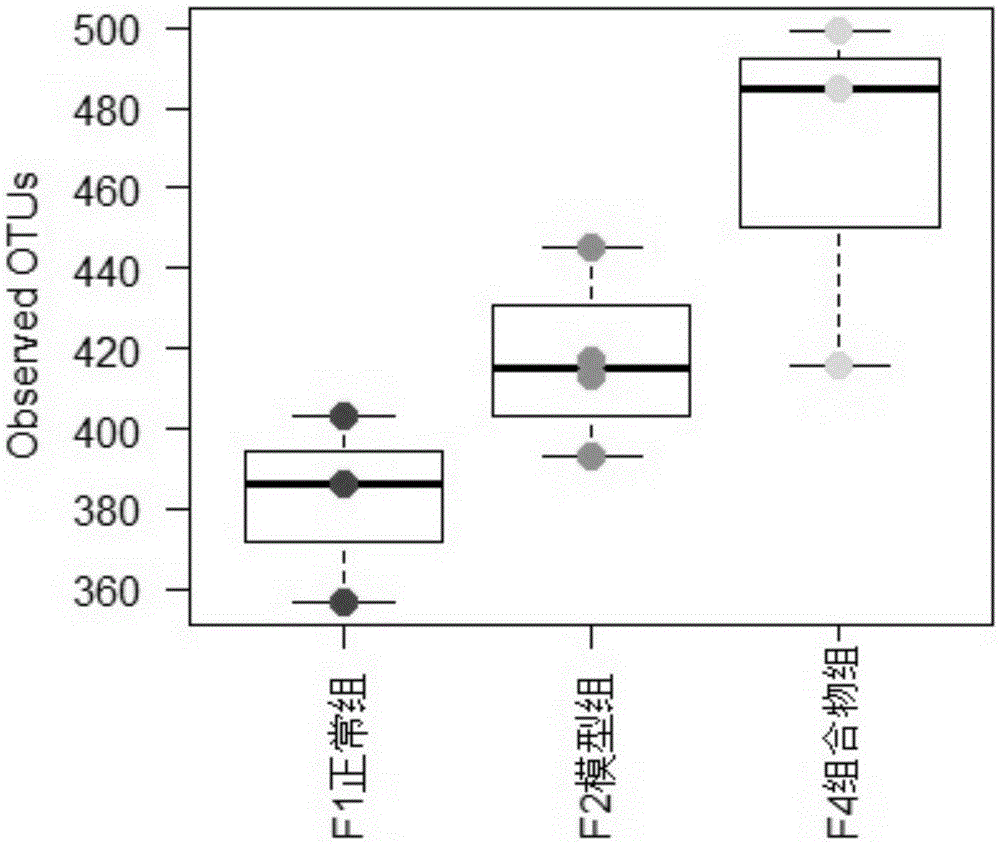
:人们的饮食习惯多偏好于高脂高糖高热量饮食,随着物质生活水平的提高,人们对于高脂饮食的需求也在增加。而高脂饮食也是肥胖、糖尿病等疾病的重要诱因之一。近年来的研究发现,一些富含多糖的食品药品在降糖、降脂方面有较好地效果。研究显示肠道菌群可以控制脂肪代谢、引发全身性的慢性低度炎症,诱发肥胖和胰岛素抵抗。饮食结构是决定肠道菌群组成的重要因素。保持肠道微生态平衡是维持人体健康所必需的。现有的微生态调节剂多是双歧杆菌、乳杆菌等活菌制剂,但是活菌制剂存在活菌数量难以保证、稳定性差等问题。近年来研究发现,一些中草药具有扶植正常菌群生长的作用,起到益生元的效果,是理想的微生态调节剂。而中药微生态调节剂与益生菌相比有许多优越性,如不存在保存活菌的技术难题,其稳定性强、有效期长和价格较低等。尤其是中药不仅扶植正常菌群生长,而且还可以提高机体的免疫功能,从而达到调整阴阳、扶正祛邪的目的。菊粉(Inulin或Alantin)是植物中储备性多糖,主要来源于植物,已发现有36000多种,包括双子叶植物中的菊科、桔梗科、龙胆科等11个科及单子叶植物中的百合科、禾木科。菊粉分子约由31个β-D-呋喃果糖和1~2个吡喃菊糖残基聚合而成,果糖残基之间能通过β-2,1-键连接。经研究发现菊粉能够降低血糖,控制血脂,促进矿物质吸收,调节肠道的作用。山药(yam或Chineseyam)又称薯蓣、土薯、山薯蓣、怀山药、淮山、白山药,是《中华本草》收载的草药,有滋养强壮,助消化,敛虚汗,止泻之功效。山药在食品业和加工业上大有发展前途,山药多糖是山药的主要成分。但未有菊粉和山药多糖对肠道菌群中能够调节的具体哪些有益有害菌的宏基因组学研究报道。技术实现要素:有鉴于此,本发明提供菊粉山药多糖组合物在制备具有调节肠道内菌群功效的保健食品中的用途。该组合物能够调节由饮食引起的肠道菌群紊乱,可明显改变肠道菌群的组成,使体内失衡的肠道菌群趋于正常,进而调节由饮食引起的肠道菌群紊乱所导致的肥胖的血脂和血糖指标,可明显降低血浆甘油三脂的含量,可以降低胆固醇、低密度脂蛋白和游离脂肪酸的含量。为了实现上述发明目的,本发明提供以下技术方案:本发明提供了一种组合物,包括菊粉和山药多糖。在本发明的一些具体实施方案中,所述组合物中所述菊粉与所述山药多糖的质量比为1:3~3:1。在本发明的另一些具体实施方案中,所述组合物中所述菊粉与所述山药多糖的质量比为1:1。本发明还提供了所述组合物在制备调节肠道菌群紊乱的药物和/或食品中的应用。在本发明中,所述食品指各种供人食用或者饮用的成品和原料以及按照传统既是食品又是药品的物品,但是不包括以治疗为目的的物品。具体的,本发明中的食品为可供人类食用或饮用的物质,包括加工食品,半成品和未加工食品,还包括保健食品,不包括烟草或只作药品用的物质。本发明中所述食品包括但不限于保健食品。凡是本领域的技术人员能够接受的食品形式,均在本发明的保护范围之内,本发明在此不做限定。在本发明中,保健食品是食品的一个种类,具有一般食品的共性,能调节人体的机能,适用于特定人群食用,但不以治疗疾病为目的。凡是本领域的技术人员能够接受的保健食品形式,均在本发明的保护范围之内,本发明在此不做限定。在本发明的一些具体实施方案中,所述应用中所述调节肠道菌群紊乱包括提高有益菌丰度和/或降低有害菌丰度。在本发明的一些具体实施方案中,所述应用中所述有益菌包括Bifidobacteriumbreve,Lactobacillusplantarum,Lactobacillusacidophilus,Lactobacillusreuteri,Acetitomaculumruminis,Lactobacillusrhamnosus;所述有害菌包括Clostridiumaceticum,Coriobacteriumglomerans,Clostridiumchauvoei,Clostridiumalcaliphilum,Porphyromonascircumdentaria,Sporobactertermitidis,Porphyromonascrevioricanis,Anaerotruncuscolihominis。在本发明的一些具体实施方案中,所述组合物的剂量为10mg/(kg·d)至200mg/(kg·d),优选为100mg/(kg·d)。本发明还提供了所述组合物在制备预防和/或治疗肠道菌群紊乱导致的疾病的药物或食品中的应用。在本发明中,所述食品指各种供人食用或者饮用的成品和原料以及按照传统既是食品又是药品的物品,但是不包括以治疗为目的的物品。具体的,本发明中的食品为可供人类食用或饮用的物质,包括加工食品,半成品和未加工食品,还包括保健食品,不包括烟草或只作药品用的物质。本发明中所述食品包括但不限于保健食品。凡是本领域的技术人员能够接受的食品形式,均在本发明的保护范围之内,本发明在此不做限定。在本发明中,保健食品是食品的一个种类,具有一般食品的共性,能调节人体的机能,适用于特定人群食用,但不以治疗疾病为目的。凡是本领域的技术人员能够接受的保健食品形式,均在本发明的保护范围之内,本发明在此不做限定。在本发明的一些具体实施方案中,所述应用中所述疾病为肥胖、胰岛素抵抗、结肠功能紊乱、肠炎或代谢综合征。本发明中所述代谢综合征是指人体的蛋白质、脂肪、碳水化合物等物质发生代谢紊乱的病理状态,是一组复杂的代谢紊乱症候群,是导致糖尿病心脑血管疾病的危险因素。其具有以下特点:①多种代谢紊乱集于一身,包括肥胖、高血糖、高血压、血脂异常、高血黏、高尿酸、高脂肪肝发生率和高胰岛素血症,这些代谢紊乱是心、脑血管病变以及糖尿病的病理基础。可见糖尿病不是一个孤立的病,而是代谢综合征的组成部分之一。②有共同的病理基础,目前多认为它们的共同原因就是肥胖尤其是中心性肥胖所造成的胰岛素抵抗和高胰岛素血症。③可造成多种疾病增加,如高血压、冠心病、脑卒中、甚至某些癌症,包括与性激素有关的乳腺癌、子宫内膜癌、前列腺癌,以及消化系统的胰腺癌、肝胆癌、结肠癌等。④有共同的预防及治疗措施,防治住一种代谢紊乱,也就有利于其他代谢紊乱的防治。临床表现为:1.腹部肥胖或超重;2.脂代谢异常;3.高血压;4.糖尿病、胰岛素抵抗及/或葡萄糖耐量异常。本发明还提供了所述应用中预防和/或治疗肠道菌群紊乱导致的疾病的食品,其选自固体制品、乳制品、溶液制品、粉末制品或悬浮液制品。在本发明的一些具体实施方案中,所述食品的剂型为软胶囊、硬胶囊、片剂、蜜膏、露剂、散剂、鲜汁、茶饮、酒剂、口服液、颗粒剂中的一种或多种。在本发明的一些具体实施方案中,所述食品的剂型选自胶囊剂、片剂、颗粒剂、口服液或散剂。在本发明中,所述食品指各种供人食用或者饮用的成品和原料以及按照传统既是食品又是药品的物品,但是不包括以治疗为目的的物品。具体的,本发明中的食品为可供人类食用或饮用的物质,包括加工食品,半成品和未加工食品,还包括保健食品,不包括烟草或只作药品用的物质。本发明中所述食品包括但不限于保健食品。凡是本领域的技术人员能够接受的食品形式,均在本发明的保护范围之内,本发明在此不做限定。在本发明中,保健食品是食品的一个种类,具有一般食品的共性,能调节人体的机能,适用于特定人群食用,但不以治疗疾病为目的。凡是本领域的技术人员能够接受的保健食品形式,均在本发明的保护范围之内,本发明在此不做限定。本发明还提供了所述应用中预防和/或治疗肠道菌群紊乱导致的疾病的药物,其剂型选自片剂、颗粒剂、胶囊剂、散剂、丸剂、口服液、糖浆剂、冲剂、滴丸剂或汤剂。在本发明的一些具体实施方案中,所述组合物的剂量为10mg/(kg·d)至200mg/(kg·d),优选为100mg/(kg·d)。本发明提供了一种菊粉山药多糖组合物在制备治疗或预防由肠道菌群紊乱导致的疾病的药物、保健食品及食品中的用途。本发明通过高脂饲料诱导小鼠肥胖二型糖尿病模型,观察菊粉山药多糖组合物通过肠道菌群对小鼠脂代谢的影响,本发明所述菊粉山药多糖组合物能够调节由饮食引起的肠道菌群紊乱,可明显改变肠道菌群的组成,使体内失衡的肠道菌群趋于正常,进而调节由饮食引起的肠道菌群紊乱所导致的肥胖的血脂和血糖指标,可明显降低血浆甘油三脂的含量,可以降低胆固醇、低密度脂蛋白和游离脂肪酸的含量。蛋白质芯片测定炎症因子的结果显示,与模型组比较,组合物组的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低57%、24%、23%、11%、77%、18%、21%、19%。组合物组能够显著的降低炎性反应,进而改善肠炎。这是因为高脂或高能量饮食诱导肠道菌群结构失调,增加了病菌的数量,减少了保护肠屏障细菌的数量,影响肠上皮细胞基因表达,导致肠道通透性增加,使得进入血液的内毒素增加,肌肉、肝脏和脂肪组织中多种炎性因子的表达量增加有关,如IL-1、TNF-α、MCP-1和IL-6等。而菊粉山药多糖调节菌群比例,显著地降低炎症因子水平,从而改善结肠功能紊乱,肠炎,代谢紊乱症等疾病。通过宏基因组学的研究,发现在肠道内菌群中哪些是有益菌,哪些是有害菌,其中富集在健康人里面的菌就是有益菌,富集在病人里面的就是有害菌,而菊粉山药多糖组合物能够提高富集在健康人肠道内菌群中有益菌的量,并能降低富集在肥胖和胰岛素抵抗的病人中有害菌的量。附图说明为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍。图1示本发明实施例4中不同分组样品的OTU数量boxplot图;图2示本发明实施例4中不同分组样品OTU数量的shannonindexboxplot图;图3示本发明实施例4中展示样品间物种多样性差异的JSD距离图;图4示本发明实施例4中展示样品间物种多样性差异的基于weightunifac的距离图;图5示本发明实施例4中所述菊粉山药多糖组合物的药理实验第12周不同组别小鼠粪便样品中菌群的基于effectsize的热图。具体实施方式本发明公开了菊粉山药多糖组合物在制备具有调节肠道内菌群功效的保健食品中的用途,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本
发明内容、精神和范围内对本文所述的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。本发明的目的在于提供一种菊粉山药多糖组合物的用途,具体来说是所述菊粉山药多糖组合物在调节肠道内菌群中具体的有益菌有害菌比例的用途。为实现上述目的,本发明的第一方面提供了一种菊粉山药多糖组合物在制备提高肠道内菌群中有益菌丰度,并且降低有害菌丰度的保健食品中的用途,所述菊粉山药多糖组合物包含菊粉和山药多糖,所述菊粉和山药多糖的重量比为1:3至3:1,优选1:1,所述组合物的剂量为10mg/(kg·d)至200mg/(kg·d),优选为100mg/(kg·d)。特别地,所述肠道内的有益菌为Bifidobacteriumbreve(短双歧杆菌),Lactobacillusplantarum(植物乳杆菌),Lactobacillusacidophilus(嗜酸乳杆菌),Lactobacillusreuteri(罗伊氏乳杆菌),Acetitomaculumruminis,Lactobacillusrhamnosus(鼠李糖乳杆菌),所述有害菌为Clostridiumaceticum(醋酸梭菌),Coriobacteriumglomerans(科里氏杆菌),Clostridiumchauvoei(肖氏梭菌),Clostridiumalcaliphilum(嗜碱梭菌),Porphyromonascircumdentaria(齿周卟啉单胞菌),Sporobactertermitidis,Porphyromonascrevioricanis(狗口腔卟啉单胞菌),Anaerotruncuscolihominis。本发明还提供了一种调节肠道内菌群中有益菌与有害菌比例的食品组合物,所述食品组合物包含菊粉山药多糖组合物,所述菊粉山药多糖组合物中,菊粉和山药多糖的重量比为1:3至3:1。优选地,所述食品组合物的剂型为固体、乳品、溶液制品、粉末制品和悬浮液制品中的一种。本发明还提供了一种调节肠道内菌群中有益菌与有害菌比例的保健食品组合物,所述保健食品组合物包含菊粉山药多糖组合物,所述菊粉山药多糖组合物中,菊粉和山药多糖的重量比为1:3至3:1。优选地,所述保健食品组合物的剂型为胶囊剂、片剂、颗粒剂、口服液和散剂中的一种。本发明的另一方面提供了菊粉山药多糖组合物在制备治疗或预防由肠道内菌群有益有害菌比例失调导致的疾病保健食品中的用途。特别地,所述疾病为由饮食引起的肠道菌群紊乱所导致的肥胖、胰岛素抵抗、结肠功 能紊乱、肠炎或代谢综合征。本发明的有益效果在于:本发明提供了一种菊粉山药多糖组合物在制备治疗或预防由肠道菌群紊乱导致的疾病的药物、保健食品及食品中的用途。本发明申请人通过高脂饲料诱导小鼠肥胖二型糖尿病模型,观察菊粉山药多糖组合物通过肠道菌群对小鼠脂代谢的影响,本发明所述菊粉山药多糖组合物能够调节由饮食引起的肠道菌群紊乱,可明显改变肠道菌群的组成,使体内失衡的肠道菌群趋于正常,进而调节由饮食引起的肠道菌群紊乱所导致的肥胖的血脂和血糖指标,可明显降低血浆甘油三脂的含量,可以降低胆固醇、低密度脂蛋白和游离脂肪酸的含量。通过宏基因组学的研究,发现在肠道内菌群中哪些是有益菌,哪些是有害菌,其中富集在健康人里面的菌就是有益菌,富集在病人里面的就是有害菌,而菊粉山药多糖组合物能够提高富集在健康人肠道内菌群中有益菌的量,并能降低富集在肥胖和胰岛素抵抗的病人中有害菌的量。本发明提供的组合物及其应用、含有该组合物的食品或药物中所用原料及试剂均可由市场购得。具体的,本发明所述菊粉和山药可以在市场上购得,其中菊粉购自上海亨代劳生物科技有限公司,产品型号为CAS号:9005-80-5。所述山药多糖通过以下制备方法制备获得:将山药粉碎后,按照山药∶水=1g∶5mL的比例加水,在75℃下加热搅拌提取3h,过滤获得的滤渣按照上述料液比、温度和时间继续提取两次,合并三次提取液,经过减压浓缩和离心获得澄清浓缩液,按照澄清浓缩液∶95%乙醇=1∶9的体积比将9倍体积95%乙醇加入到澄清浓缩液中,混匀后于4℃下过夜静置沉淀,离心收集沉淀,经过真空冷冻干燥即获得山药多糖。下面结合实施例,进一步阐述本发明:实施例1组合物的制备本实施中的菊粉山药多糖组合物包含菊粉和山药多糖,其中菊粉和山药多糖重量比为1:1,菊粉山药多糖组合物可以单独或与其他中草药或食品添加剂及保健食品或药品上可接受的辅料制成用于治疗或预防由肠道菌群紊乱导致的疾病的药物、保健食品或食品组合物;其中,药物和保健食品组合物的剂型为胶囊剂、片剂、颗粒剂、口服液和散剂等,食品组合物的剂型为固体、乳品、溶液制品、粉末制品和悬浮液制品等。本发明所述菊粉和山药可以在市场上购得,其中菊粉购自上海亨代劳生物科技有限公司,产品型号为CAS号:9005-80-5。所述山药多糖通过以下制备方法制备获得:将山药粉碎后,按照山药∶水=1g∶5mL的比例加水,在75℃下加热搅拌提取3h,过滤获得的滤渣按照上述料液比、温度和时间继续提取两次,合并三次提取液,经过减压浓缩和离心获得澄清浓缩液,按照澄清浓缩液∶95%乙醇=1∶9的体积比将9倍体积95%乙醇加入到澄清浓缩液中,混匀后于4℃下过夜静置沉淀,离心收集沉淀,经过真空冷冻干燥即获得山药多糖。实施例2同实施例1中的菊粉山药多糖组合物,其中菊粉山药多糖重量比为1:3。实施例3同实施例1中的菊粉山药多糖组合物,其中菊粉山药多糖重量比为3:1。实施例4本发明申请人使用上述实施例1所制得的菊粉山药多糖组合物进行了药理学实验,实验结果如下:1、实验材料1.1、实验仪器Thermo全波长酶标仪:赛默飞世尔科技中国,1510;JA1203N型分析天平:上海精密仪器有限公司产品;电子天平:常熟市双杰测试仪器厂,T1000。1.2、实验试剂葡萄糖测定试剂盒:上海荣盛生物药业有限公司,20131207147;总胆固醇测定试剂盒:上海荣盛生物药业有限公司,20131105146;甘油三酯测定试剂盒:上海荣盛生物药业有限公司,20131105121;低密度脂蛋白测定试剂盒:上海荣盛生物药业有限公司,20140302124;游离脂肪酸定量检测试剂盒:和光纯药工业株式会社,AME6194。1.3、实验动物与饲料C57BL/6小鼠30只,SPF级,18~22g,50~60天,雄性:广东省医学实验动物中心SCXK(粤)2013-0002;大小鼠维持饲料:广东省医学实验动物中心SCXK(粤)2013-0002;高脂纯化饲料MD45%:江苏美迪森生物医药有限公司。表1不同脂肪含量的饲料主要成分及能量构成1.4、实验药物表2动物实验原料清单2、实验方法受试动物进入广州中医药大学大学城实验动物中心后,3~4只/盒,20~25℃,RH40~70%,12h:12h昼夜间断照明;自由进食饮水,饮用水为实验动物中心制备的蒸馏水。适应性喂养一周后,不禁食眼底静脉丛麻醉采血,测量生化指标;根据体重(BW), 血糖(GLU),胆固醇(TC),甘油三酯(TG),随机均匀分组:正常组(n=8),模型组(n=12),菊粉山药多糖组合物组1(或简称组合物组1,n=9),菊粉山药多糖组合物组2(或简称组合物组2,n=9),菊粉山药多糖组合物组3(或简称组合物组3,n=9),菊粉组(n=10),山药多糖组(n=11),阳性对照组(n=10)。实验开始后,正常组给予维持饲料,其余各组均给予高脂纯化饲料,并同时开始灌胃给药,正常组与模型组给予蒸馏水,其余各组给予对应药物,灌胃体积为0.1ml/10g,持续14weeks。每日观察小鼠毛色,体重,精神状态,记录进食量,每周记录一次小鼠体重,第12周采集一次小鼠新鲜粪便。给药8周后,禁食14h,眼底静脉丛采血测量GLU、TC、TG、低密度脂蛋白(LDL-C)。给药11周后,禁食14h,进行口服糖耐量实验(OGTT):禁食后,按2g/kg灌胃给予葡萄糖溶液后,分别麻醉取灌胃后0min,20min,60min,120min时间点血测量血糖并绘制曲线求曲线下面积(AUC),同时测量TG,TC,LDL-C。给药13周后,禁食14h,眼底静脉丛采血测量TG,TC,LDL-C,游离脂肪酸(NEFA)。给药14周后,不禁食眼底静脉丛采血后,脱颈椎处死小鼠,解剖取组织脏器(肝、胰腺、肾、肌肉、小肠、小肠内容物、结肠、结肠内容物、盲肠、盲肠内容物、棕色脂肪、皮下脂肪、肾周脂肪、附睾周围脂肪)根据需要放置于中性甲醛固定或速冻于液氮后转移保存于-80℃冰箱。另外还利用蛋白质芯片技术测定了小鼠炎症因子,蛋白质芯片的检测原理主要是基于抗原抗体特异性非共价结合。本实验采用双抗体夹心法。夹心法抗体芯片是将捕获抗体预先固定在固相载体上,生物样品加入到芯片上一起孵育反应后,其特异性的抗原与捕获抗体结合,然后加入生物素标记的检测抗体一起孵育,最后通过HRP-链霉亲和素与化学发光底物、或者荧光染色剂-链霉亲和素结合作为信号检测。胶片显影、定影后用quantityone软件分析膜上斑点的灰度值。一张膜上附有39种细胞因子的抗体,一组样本在一张膜上检测。以模型组的灰度值为单位1作为对照,其余各组与模型组比较分析。3、统计学分析:本实验所有数据均采用均值±标准差(X±s)表示,组间差异性分析采用statview软件进行单因素方差分析和t检验,以P<0.05作为统计学差异参考标准。4、实验结果给药8周后,各组血糖无显著性差异;第八周禁食小鼠血液生化指标显示,模型组甘油三酯、胆固醇与低密度脂蛋白均高于正常组(P<0.05),而菊粉山药多糖组合物组低密度脂蛋白则低于模型组(P<0.05);可见小鼠在进食高脂饲料8周后,血脂含量明显增高。给药十三周后,第十三周禁食小鼠血液生化指标结果显示,模型组甘油三酯明显高于正常组(P<0.01),其余各组甘油三酯均低于模型组(P<0.05),模型组胆固醇与低密度脂蛋白也高于正常组(P<0.05);小鼠进食高脂饲料十三周后,各项血脂指标进一步升高,血糖也有升高的趋势,菊粉山药多糖组合物体现出了良好的降低甘油三酯的效果,但对胆固醇与低密度脂蛋白无显著影响。表3第十三周禁食小鼠血液生化指标从表3实验结果可以看出,本发明所述菊粉山药多糖组合物能显著(P<0.05)改善二型糖尿病肥胖的血脂和血糖指标,可显著(P<0.05)降低血浆甘油三脂的含量,可以降低胆固醇、低密度脂蛋白和游离脂肪酸的含量,对于治疗或预防由肠道菌群紊乱导致的肥胖或胰岛素抵抗有很好的有益效果。此外,从表3试验结果可以看出,相比于菊粉组和山药多糖组,本发明所述菊粉山药多糖组合物在剂量减少的情况下,能显著(P<0.05)改善二型糖尿病肥胖的血脂和血糖指标,可显著(P<0.05)降低血浆甘油三脂的含量,显著(P<0.05)降低胆固醇、低密度脂蛋白和游离脂肪酸的含量,对于治疗或预防由肠道菌群紊乱导致的肥胖或胰岛素抵抗有很好的有益效果,因此,本发明提供的组合物取得了增效作用。表4蛋白芯片测炎症因子结果蛋白质芯片测定炎症因子的结果(见表4)显示,与模型组比较,组合物组1的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低59%、29%、29%、19%、79%、20%、18%、22%。组合物组2的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低37%、13%、10%、7%、45%、9%、19%、10%。组合物组3的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低57%、24%、23%、11%、77%、18%、21%、19%。上述试验数据表明,组合物组能够显著的降低炎性反应,进而改善肠炎。这是因为高脂或高能量饮食诱导肠道菌群结构失调,增加了病菌的数量,减少了保护肠屏障细菌的数量,影响肠上皮细胞基因表达,导致肠道通透性增加,使得进入血液的内毒素增加,肌肉、肝脏和脂肪组织中多种炎性因子的表达量增加有关,如IL-1、TNF-α、MCP-1和IL-6等。而菊粉山药多糖调节菌群比例,显著地降低炎症因子水平,从而改善结肠功能紊乱,肠炎,代谢紊乱症等疾病。此外,与菊粉组比较,本发明提供的组合物组1的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低63%、34%、35%、25%、84%、25%、23%、27%,本发明提供的组合物组2的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低45%、17%、14%、13%、55%、13%、25%、15%,本发明提供的组合物组3的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低60%、26%、26%、17%、80%、20%、23%、21%。本发明提供的组合物组分别与菊粉组和山药多糖组比较,具有显著差异(P<0.05)。因此,本发明提供的组合物组能够显著(P<0.05)降低炎性反应,进而改善肠炎,相比于菊粉组和山药多糖组,本发明提供的组合物取得了增效作用。与山药多糖组比较,本发明提供的组合物组1的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低65%、37%、38%、29%、86%、27%、25%、29%,本发明提供的组合物组2的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低32%、10%、8%、5%、39%、7%、10%、9%,本发明提供的组合物组3的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低55%、19%、14%、 13%、56%、13%、25%、15%。本发明提供的组合物组分别与菊粉组和山药多糖组比较,具有显著差异(P<0.05)。因此,本发明提供的组合物组能够显著(P<0.05)降低炎性反应,进而改善肠炎,相比于菊粉组和山药多糖组,本发明提供的组合物取得了增效作用。采集应用实施例1中小鼠实验第12周的小鼠新鲜粪便,将不同组别之间的肠道菌落进行宏基因组学差异分析。本实验中采用的宏基因组学方法参见文献:KoyelMitra1etal.Integrativeapproachesforfindingmodularstructureinbiologicalnetworks.NatureGenetics2013.其中OTU(操作分类单位operationaltaxonomicunits)是指系统发生分析中的一个外部节点,是一个假定的分类单元;分类单位可能是菌株、种或属,统称每个分类单位为一个操作分类单位。很多场合下,OTU是指菌株。参见英文文献:DefiningoperationaltaxonomicunitsusingDNAbarcodedata.图1和表5中F1、正常组,F2、模型组,F4、菊粉山药多糖组合物组1,F5、菊粉山药多糖组合物组2,F6、菊粉山药多糖组合物组3,F7、菊粉组,F8、山药多糖组,F9、阳性对照组。图1和表5中“菊粉山药多糖组合物组”简写为“组合物”。1、样品Alpha多样性比较图1是不同分组样品的OTU数量boxplot图,从图1和表5中可以看出,模型组的OTU数量比正常组的要多,F4菊粉山药多糖组合物组1、F5菊粉山药多糖组合物组2、F6菊粉山药多糖组合物组3有提高OTU数量的作用。请补充本发明提供的组合物与阳性对照组、菊粉组、山药多糖组的比较分析内容。表5不同组别之间OTU数量差异比较图2是不同分组样品的shannonindexboxplot图,从图2和表6可以看出,模型组的多样性要高于正常组,组合物组的多样性跟模型组差不多。综上,本发明提供的组合物组与菊粉组、山药多糖组比较,具有显著差异(P<0.05);本发明提供的组合物组与阳性对照组相比,虽然效果不及阳性对照组,但是无显著差异(P>0.05)。表6不同组别shannonalpha多样性比较2、样品Beta多样性比较为了进一步展示样品间物种多样性差异,使用主坐标分析(Principalcoordinatesanalysis,PCoA)的方法展示各个样品间的差异大小。图中一共展示了2中距离,一种是基于样品OTUprofile计算的JSD距离,如图3;另一种距离是基于weightunifac距离的,见图4。图4中,如果两个样品距离较近,则表示这两个样品的物种组成较相似。3、样品组间显著性差异分析我们最关心的是F2模型组和F1正常组有差异的菌是否用药后得到调节,做出了图5。图5中挑选的OTU是在F1正常组和F2模型组有差异的OTU(effectsize>1.96),然后这些OTU同样在其他组和F2模型组之间检验,得出的effectsize画出上面的热图。OTU之间的差异还是很显著的,F1正常组的丰度要比F2模型组的低,而组合物组的丰度更低了,因为这些OTU是富集在F2模型组上的。表7展示了菊粉山药多糖组合物组对于肠道菌群中的各种有益菌与有害菌的调节作用,通过宏基因组学的手段分析比对各组第12周的小鼠新鲜粪便中的菌落,可知小鼠肠道中的有益菌为Bifidobacteriumbreve,Lactobacillusplantarum,Lactobacillusacidophilus,Lactobacillusreuteri,Acetitomaculumruminis,Lactobacillusrhamnosus,所述有害菌为Clostridiumaceticum,Coriobacteriumglomerans,Clostridiumchauvoei,Clostridiumalcaliphilum,Porphyromonascircumdentaria,Sporobactertermitidis,Porphyromonascrevioricanis,Anaerotruncuscolihominis。本发明实施例中的菊粉山药多糖组合物对上述有益菌的丰度有提高作用,对上述有害菌的丰度有降低作用。根据宏基因组学研究的方法和原理(参见Lietal.InnateimmunityandintestinalmicrobiotainthedevelopmentofType1diabetesNature455,1109-1113,23rd,October2008),将上述有益菌和有害菌在人肠道中的菊粉山药多糖组合物(100mg/(kg·d))调节结果进行测序鉴定,得到菊粉山药多糖组合物能够提高肠道内菌群中有益菌Bifidobacteriumbreve,Lactobacillusplantarum,Lactobacillusacidophilus,Lactobacillusreuteri,Acetitomaculumruminis,Lactobacillusrhamnosus的丰度,降低有害菌Clostridiumaceticum,Coriobacteriumglomerans,Clostridiumchauvoei,Clostridiumalcaliphilum,Porphyromonascircumdentaria,Sporobactertermitidis,Porphyromonascrevioricanis,Anaerotruncuscolihominis的丰度。可见菊粉山药多糖组合物能使有益菌的丰度增加,使有害菌的丰度明显降低,呈现出 明显地改善肠道菌群紊乱的作用(通过宏基因组学的研究,富集在健康人里面的菌就是有益菌,富集在病患者里面的就是有害菌)。表7相比病患组对于有益菌与有害菌的调节作用结果取所述菊粉山药组合物的剂量为10mg/(kg·d)至200mg/(kg·d)时的任意组合物配比,进行上述多项试验,试验结果相比模型组均具有良好的调节作用,显著差异(P<0.05),在实验组组合物1的100mg/(kg·d)的剂量时功效最优。实施例5本发明申请人使用上述实施例2所制得的菊粉山药多糖组合物按照同实施例4的试验方法进行检测,结果如下。表8动物实验原料清单表9第十三周禁食小鼠血液生化指标从表9实验结果可以看出,本发明所述菊粉山药多糖组合物能显著(P<0.05)改善二型糖尿病肥胖的血脂和血糖指标,可显著(P<0.05)降低血浆甘油三脂的含量,可以降低胆固醇、低密度脂蛋白和游离脂肪酸的含量,对于治疗或预防由肠道菌群紊乱导致的肥胖或胰岛素抵抗有很好的有益效果。此外,从表9试验结果可以看出,相比于菊粉组和山药多糖组,本发明所述菊粉山药多糖组合物在剂量减少的情况下,能显著(P<0.05)改善二型糖尿病肥胖的血脂和血糖指标,可显著(P<0.05)降低血浆甘油三脂的含量,显著(P<0.05)降低胆固醇、低密度脂蛋白和游离脂肪酸的含量,对于治疗或预防由肠道菌群紊乱导致的肥胖或胰岛素抵抗有很好的有益效果,因此,本发明提供的组合物取得了增效作用。表10蛋白芯片测炎症因子结果蛋白质芯片测定炎症因子的结果(见表10)显示,与模型组比较,组合物组1的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低60%、27%、24%、17%、67%、17%、25%、20%。组合物组2的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低32%、7%、8%、17%、37%、6%、6%、11%。组合物组3 的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低43%、15%、14%、9%、51%、9%、15%、20%。上述试验数据表明,组合物组能够显著的降低炎性反应,进而改善肠炎。这是因为高脂或高能量饮食诱导肠道菌群结构失调,增加了病菌的数量,减少了保护肠屏障细菌的数量,影响肠上皮细胞基因表达,导致肠道通透性增加,使得进入血液的内毒素增加,肌肉、肝脏和脂肪组织中多种炎性因子的表达量增加有关,如IL-1、TNF-α、MCP-1和IL-6等。而菊粉山药多糖调节菌群比例,显著地降低炎症因子水平,从而改善结肠功能紊乱,肠炎,代谢紊乱症等疾病。此外,与菊粉组比较,本发明提供的组合物组1的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低63%、31%、27%、21%、45%、21%、37%、26%,本发明提供的组合物组2的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低38%、15%、14%、25%、39%、7%、9%、13%,本发明提供的组合物组3的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低50%、27%、21%、17%、62%、13%、21%、25%。本发明提供的组合物组分别与菊粉组和山药多糖组比较,具有显著差异(P<0.05)。因此,本发明提供的组合物组能够显著(P<0.05)降低炎性反应,进而改善肠炎,相比于菊粉组和山药多糖组,本发明提供的组合物取得了增效作用。与山药多糖组比较,本发明提供的组合物组1的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低65%、38%、27%、123%、47%、21%、39%、28%,本发明提供的组合物组2的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低39%、19%、17%、25%、46%、13%、13%、16%,本发明提供的组合物组3的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低60%、29%、24%、19%、67%、17%、25%、29%。本发明提供的组合物组分别与菊粉组和山药多糖组比较,具有显著差异(P<0.05)。因此,本发明提供的组合物组能够显著(P<0.05)降低炎性反应,进而改善肠炎,相比于菊粉组和山药多糖组,本发明提供的组合物取得了增效作用。采集应用实施例1中小鼠实验第12周的小鼠新鲜粪便,将不同组别之间的肠道菌落进行宏基因组学差异分析。本实验中采用的宏基因组学方法参见文献:KoyelMitra1etal.Integrativeapproachesforfindingmodularstructureinbiologicalnetworks.NatureGenetics2013.其中OTU(操作分类单位operationaltaxonomicunits)是指系统发生分析中的一个外部节点,是一个假定的分类单元;分类单位可能是菌株、种或属,统称每个分类单位为一个操作分类单位。很多场合下,OTU是指菌株。参见英文文献:DefiningoperationaltaxonomicunitsusingDNAbarcodedata.表11中F1、正常组,F2、模型组,F4、菊粉山药多糖组合物组1,F5、菊粉山药多糖组合物组2,F6、菊粉山药多糖组合物组3,F7、菊粉组,F8、山药多糖组,F9、阳性对照组。表11中“菊粉山药多糖组合物组”简写为“组合物”。1、样品Alpha多样性比较从表11中可以看出,模型组的OTU数量比正常组的要多,F4菊粉山药多糖组合物组1、F5菊粉山药多糖组合物组2、F6菊粉山药多糖组合物组3有提高OTU数量的作用。综上,本发明提供的组合物组与菊粉组、山药多糖组比较,具有显著差异(P<0.05);本发明提供的组合物组与阳性对照组相比,虽然效果不及阳性对照组,但是无显著差异(P>0.05)。表11不同组别之间OTU数量差异比较图2是不同分组样品的shannonindexboxplot图,从图2和表12可以看出,模型组的多样性要高于正常组,组合物组的多样性跟模型组差不多。综上,本发明提供的组合物组与菊粉组、山药多糖组比较,具有显著差异(P<0.05);本发明提供的组合物组与阳性对照组相比,虽然效果不及阳性对照组,但是无显著差异(P>0.05)。表12不同组别shannonalpha多样性比较2、样品Beta多样性比较为了进一步展示样品间物种多样性差异,使用主坐标分析(Principalcoordinatesanalysis,PCoA)的方法展示各个样品间的差异大小。3、样品组间显著性差异分析我们最关心的是F2模型组和F1正常组有差异的菌是否用药后得到调节。挑选的OTU是在F1正常组和F2模型组有差异的OTU(effectsize>1.96),然后这些OTU同样在其他组和F2模型组之间做检验,得出的effectsize画出上面的热图。OTU之间的差异还是很显著的,F1正常组的丰度要比F2模型组的低,而组合物组的丰度更低了,因为这些OTU是富集在F2模型组上的。表13展示了菊粉山药多糖组合物组对于肠道菌群中的各种有益菌与有害菌的调节作用,通过宏基因组学的手段分析比对各组第12周的小鼠新鲜粪便中的菌落,可知小鼠肠道中的有益菌为Bifidobacteriumbreve,Lactobacillusplantarum,Lactobacillusacidophilus,Lactobacillusreuteri,Acetitomaculumruminis,Lactobacillusrhamnosus,所述有害菌为Clostridiumaceticum,Coriobacteriumglomerans,Clostridiumchauvoei,Clostridiumalcaliphilum,Porphyromonascircumdentaria,Sporobactertermitidis,Porphyromonascrevioricanis,Anaerotruncuscolihominis。本发明实施例中的菊粉山药多糖组合物对上述有益菌的丰度有提高作用,对上述有害菌的丰度有降低作用。表13相比病患组对于有益菌与有害菌的调节作用结果实验结果显示,实施例2制得的菊粉山药多糖组合物功效与实施例1制得的菌粉山药多糖组合物的效果相近,无显著差异(P>0.05),具有实施例1组合物产生效果的90%以上,能显著(P<0.05)改善二型糖尿病肥胖的血脂和血糖指标,可显著(P<0.05)降低血浆甘油三脂的含量,可以降低胆固醇、低密度脂蛋白和游离脂肪酸的含量,对于治疗或预防由肠道菌群紊乱导致的肥胖或胰岛素抵抗有很好的有益效果。并且所述菊粉山药多糖调节菌群比例,提高肠道内菌群中上述有益菌丰度,并且降低上述有害菌丰度,从而显著地降低炎症因子水平,从而改善结肠功能紊乱,肠炎,代谢紊乱症等疾病。取所述菊粉山药组合物的剂量为10mg/(kg·d)至200mg/(kg·d)时的任意组合物配比,进行上述多项试验,试验结果相比模型组均具有良好的调节作用,显著差异(P<0.05),在实验组组合物1的100mg/(kg·d)的剂量时功效最优。实施例6本发明申请人使用上述实施例3所制得的菊粉山药多糖组合物按照同实施例4的试验方法进行检测,结果如下。表14动物实验原料清单表15第十三周禁食小鼠血液生化指标从表15实验结果可以看出,本发明所述菊粉山药多糖组合物能显著(P<0.05)改善二型糖尿病肥胖的血脂和血糖指标,可显著(P<0.05)降低血浆甘油三脂的含量,可以降低胆固醇、低密度脂蛋白和游离脂肪酸的含量,对于治疗或预防由肠道菌群紊乱导致的肥胖或胰岛素抵抗有很好的有益效果。此外,从表15试验结果可以看出,相比于菊粉组和山药多糖组,本发明所述菊粉山药多糖组合物在剂量减少的情况下,能显著(P<0.05)改善二型糖尿病肥胖的血脂和血糖指标,可显著(P<0.05)降低血浆甘油三脂的含量,显著(P<0.05)降低胆固醇、低密度脂蛋白和游离脂肪酸的含量,对于治疗或预防由肠道菌群紊乱导致的肥胖或胰岛素抵抗有很好的有益效果,因此,本发明提供的组合物取得了增效作用。表16蛋白芯片测炎症因子结果蛋白质芯片测定炎症因子的结果(见表16)显示,与模型组比较,组合物组1的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低60%、27%、24%、17%、67%、17%、25%、20%。组合物组2的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低31%、9%、10%、5%、36%、5%、9%、11%。组合物组3的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低43%、15%、14%、9%、51%、9%、15%、20%。上述试验数据表明,组合物组能够显著的降低炎性反应,进而改善肠炎。这是因为高脂或高能量饮食诱导肠道菌群结构失调,增加了病菌的数量,减少了保护肠屏障细菌的数量,影响肠上皮细胞基因表达,导致肠道通透性增加,使得进入血液的内毒素增加,肌肉、肝脏和脂肪组织中多种炎性因子的表达量增加有关,如IL-1、TNF-α、MCP-1和IL-6等。而菊粉山药多糖调节菌群比例,显著地降低炎症因子水平,从而改善结肠功能紊乱,肠炎,代谢紊乱症等疾病。此外,与菊粉组比较,本发明提供的组合物组1的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低63%、35%、34%、19%、69%、19%、27%、25%。组合物组2的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低33%、12%、13%、11%、39%、15%、13%、15%。组合物组3的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低54%、25%、20%、14%、63%、14%、23%、21%。本发明提供的组合物组分别与菊粉组和山药多糖组比较,具有显著差异(P<0.05)。因此,本发明提供的组合物组能够显著(P<0.05)降低炎性反应,进而改善肠炎,相比于菊粉组和山药多糖组,本发明提供的组合物取得了增效作用。此外,与山药多糖组比较,本发明提供的组合物组1的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低65%、38%、37%、21%、70%、21%、27%、28%,本发明提供的组合物组2的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低36%、19%、16%、15%、42%、17%、19%、17%,本发明提供的组合物组3的IL-6、IL-1β、IL-2、MCP-1、IFN-γ、IL-10、TNF-α、Leptin分别表现为降低60%、27%、24%、17%、67%、17%、25%、20%。本发明提供的组合物组分别与菊粉组和山药多糖组比较,具有显著差异(P<0.05)。因此,本发明提供的组合物组能够显著(P<0.05)降低炎性反应,进而改善肠炎,相比于菊粉组和山药多糖组,本发明提供的组合物取得了增效作用。采集应用实施例3中小鼠实验第12周的小鼠新鲜粪便,将不同组别之间的肠道菌落进行宏基因组学差异分析。本实验中采用的宏基因组学方法参见文献:KoyelMitra1etal.Integrativeapproachesforfindingmodularstructureinbiologicalnetworks.NatureGenetics 2013.其中OTU(操作分类单位operationaltaxonomicunits)是指系统发生分析中的一个外部节点,是一个假定的分类单元;分类单位可能是菌株、种或属,统称每个分类单位为一个操作分类单位。很多场合下,OTU是指菌株。参见英文文献:DefiningoperationaltaxonomicunitsusingDNAbarcodedata.表17中F1、正常组,F2、模型组,F4、菊粉山药多糖组合物组1,F5、菊粉山药多糖组合物组2,F6、菊粉山药多糖组合物组3,F7、菊粉组,F8、山药多糖组,F9、阳性对照组。表17中“菊粉山药多糖组合物组”简写为“组合物”。1、样品Alpha多样性比较从表17中可以看出,模型组的OTU数量比正常组的要多,F4菊粉山药多糖组合物组1、F5菊粉山药多糖组合物组2、F6菊粉山药多糖组合物组3有提高OTU数量的作用。综上,本发明提供的组合物组与菊粉组、山药多糖组比较,具有显著差异(P<0.05);本发明提供的组合物组与阳性对照组相比,虽然效果不及阳性对照组,但是无显著差异(P>0.05)。表17不同组别之间OTU数量差异比较从表18可以看出,模型组的多样性要高于正常组,组合物组的多样性跟模型组差不多。综上,本发明提供的组合物组与菊粉组、山药多糖组比较,具有显著差异(P<0.05);本发明提供的组合物组与阳性对照组相比,虽然效果不及阳性对照组,但是无显著差异(P>0.05)。表18不同组别shannonalpha多样性比较2、样品Beta多样性比较为了进一步展示样品间物种多样性差异,使用主坐标分析(Principalcoordinates analysis,PCoA)的方法展示各个样品间的差异大小。3、样品组间显著性差异分析挑选的OTU是在F1正常组和F2模型组有差异的OTU(effectsize>1.96),然后这些OTU同样在其他组和F2模型组之间检验,得出的effectsize画出上面的热图。OTU之间的差异还是很显著的,F1正常组的丰度要比F2模型组的低,而组合物组的丰度更低了,因为这些OTU是富集在F2模型组上的。表19展示了菊粉山药多糖组合物组对于肠道菌群中的各种有益菌与有害菌的调节作用,通过宏基因组学的手段分析比对各组第12周的小鼠新鲜粪便中的菌落,可知小鼠肠道中的有益菌为Bifidobacteriumbreve,Lactobacillusplantarum,Lactobacillusacidophilus,Lactobacillusreuteri,Acetitomaculumruminis,Lactobacillusrhamnosus,所述有害菌为Clostridiumaceticum,Coriobacteriumglomerans,Clostridiumchauvoei,Clostridiumalcaliphilum,Porphyromonascircumdentaria,Sporobactertermitidis,Porphyromonascrevioricanis,Anaerotruncuscolihominis。本发明实施例中的菊粉山药多糖组合物对上述有益菌的丰度有提高作用,对上述有害菌的丰度有降低作用。表19相比病患组对于有益菌与有害菌的调节作用结果实验结果显示,实施例3制得的菊粉山药多糖组合物功效与实施例1制得的菌粉山药多糖组合物的效果相近,无显著差异(P>0.05),具有实施例1组合物产生效果的90%以上,能显著(P<0.05)改善二型糖尿病肥胖的血脂和血糖指标,可显著(P<0.05)降低血浆甘油三脂的含量,可以降低胆固醇、低密度脂蛋白和游离脂肪酸的含量,对于治疗或预防由肠道菌群紊乱导致的肥胖或胰岛素抵抗有很好的有益效果。并且所述菊粉山药多糖调节菌群比例,提高肠道内菌群中上述有益菌丰度,并且降低上述有害菌丰度,从而显著地降低炎症因子水平,从而改善结肠功能紊乱,肠炎,代谢紊乱症等疾病。取所述菊粉山药组合物的剂量为10mg/(kg·d)至200mg/(kg·d)时的任意组合物配比,进行上述多项试验,试验结果相比模型组均具有良好的调节作用,显著差异(P<0.05),在实验组组合物1的100mg/(kg·d)的剂量时功效最优。实施例7保健食品的制备取本发明实施例1至实施例3提供的组合物,添加食品中允许的辅料,按照常规方法制得食品。制得的食品可以为固体制品、乳制品、溶液制品、粉末制品或悬浮液制品。其中,保健食品的剂型可以为胶囊剂、片剂、颗粒剂、口服液或散剂。实施例8药物的制备取本发明实施例1至实施例3提供的组合物,添加药学上可接受的辅料,按照常规方法制得药物。制得的药物的剂型可以为片剂、颗粒剂、胶囊剂、散剂、丸剂、口服液、糖浆剂、冲剂、滴丸剂或汤剂。实施例9制得保健食品的检验取本发明实施例6制得的保健食品,按照中华人民共和国国家标准GB16740-2014《食品安全国家标准保健食品》进行检测,结果如下:3.1原料和辅料原料和辅料符合相应食品标准和有关规定。3.2感官要求感官要求符合表20的规定。表20感官要求3.3理化指标理化指标符合相应类属食品的食品安全国家标准的规定。3.4污染物限量污染物限量符合GB2762中相应类属食品的规定,无相应类属食品的符合表21的规定。表21污染物限量项目指标检验方法铅a(Pb)/(mg/kg)2.0GB5009.12总砷b(As)/(mg/kg)1.0GB/T5009.11总汞c(Hg)/(mg/kg)0.3GB/T5009.17a袋泡茶剂的铅≤5.0mg/kg;液态产品的铅≤0.5mg/kg;婴幼儿固态或半固态保健食品的铅≤0.3mg/kg;婴幼儿液态保健食品的铅≤0.02mg/kg。b液态产品的总砷≤0.3mg/kg;婴幼儿保健食品的总砷≤0.3mg/kg。c液态产品(婴幼儿保健食品除外)不测总汞;婴幼儿保健食品的总汞≤0.02mg/kg。3.5真菌毒素限量真菌毒素限量符合GB2761中相应类属食品的规定和(或)有关规定。3.6微生物限量微生物限量符合GB29921中相应类属食品和相应类属食品的食品安全国家标准的规定,无相应类属食品规定的符合表22的规定。表22微生物限量3.7食品添加剂和营养强化剂3.7.1食品添加剂的使用符合GB2760的规定。3.7.2营养强化剂的使用符合GB14880和(或)有关规定。综合上述检测结果,本发明制得的保健食品符合中华人民共和国国家标准GB16740-2014《食品安全国家标准保健食品》的规定。以上所述仅是本发明的优选实施方式,应当指出,对于本
技术领域:
的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1