自动移动检测的制作方法
本发明涉及用于对其中设备正在离开在解剖结构内且相对于解剖结构的稳定位置的事件进行自动检测的方法和系统。换句话说,本发明涉及一种用于自动检测设备在解剖结构内且相对于解剖结构的移动的方法和系统。此外,本发明涉及对应的计算机程序。
背景技术:
导丝和介入设备的导航和精确定位是冗长乏味且耗时的,并且要求额外的造影剂爆发以使设备相对于相关血管的位置变得清晰。由于散射,患者和医务人员在采集诊断性血管造影和介入性荧光透视期间都会暴露于x射线。期望导航支持以减少介入时间并提高定位准确度。
因此,3d路线图绘制(roadmapping)在许多x射线引导下的介入中是非常重要的。由于在没有注入造影剂的情况下血管解剖结构在荧光透视图像中几乎不可见,因此经(静态或动态)配准的3d路线图绘制为介入医师提供了用于各种任务(例如,导航、定位或部署设备和/或评估结果)的视觉参考。
静态运动补偿涉及配准3d路线图以找到针对整个荧光透视序列的单个几何变换,而动态运动补偿要求为序列中的每个帧找到正确的几何变换。
有两种实现动态运动补偿的方法。第一种方法包括跟踪连接到脉管解剖结构的解剖学界标,所述解剖学界标具有与血管相同的运动,例如在tavi流程期间的瓣膜定位和部署的背景中。
第二种方法包括跟踪连接到脉管解剖结构并因此具有相似运动的设备。设备清晰可见,是用于动态运动补偿算法的良好候选者。
这两种方法都有以下缺点:
·解剖学界标通常是非常模糊的且与不透明物体混杂,因此跟踪解剖学界标是一项艰巨的任务。额外地,检测和跟踪这样的界标要求来自用户的额外的输入。
·在血管内部锁定介入设备是方案的一部分,必须被最好地执行。如果要部署假体或支架,则该设备甚至可能被完全拉回。因此,设备解锁是常见的并且必须被检测到以评估运动补偿的有效性。
此外,导航系统能够通过提供接下来被显示或被叠加在实况荧光透视图片上的心脏路线图来帮助心脏病专家。在理想情况下,这种心脏路线图表示在血管造影期间采集的血管网络。
wo2011/039681a1描述了一种用于血管介入流程的准确定位的方法和医学成像系统。首先,利用注入的造影剂来采集感兴趣血管区域的至少一幅x射线图像。另外,在至少一幅采集到的图像内识别血管信息数据。然后,检测所述至少一幅采集到的图像中的所述感兴趣血管区域中的血管的第一钙化特征。另外,使用所述血管信息数据和检测到的钙化特征来生成血管表示。另外,采集所述感兴趣血管区域的至少一幅当前荧光透视图像。然后,检测在所述至少一幅当前荧光透视图像中的所述感兴趣血管区域中的所述血管的第二钙化特征,其中,所述第二钙化特征根据所述第一钙化特征。另外,将所述血管表示与所述荧光透视图像配准,其中,所述钙化特征用于所述配准。然后,通过将所述血管表示与所述至少一幅荧光透视图像进行组合来生成复合图像。最终显示所述复合图像。
在wo2004/034329a2中,描述了依赖于对心脏和呼吸周期的提取以及(处于填充状态的)血管造影图像与实况图像之间的这些循环的匹配来实现心脏路线图绘制的基本方法。
技术实现要素:
本发明提出了设备和解剖学界标两者的存在。尤其地,提出了一种使用解剖学界标进行自动设备解锁检测的方法,该方法结合基于设备的运动补偿,使得能够设计全自动的动态运动补偿方法。
能够看出,本发明的目的是提供一种消除或至少减少上述缺点的方法和设备。
本发明的另外的目的是提供器械在解剖部位中且相对于解剖部位的移动的指示。
这通过各自的独立权利要求中的每项的主题来实现。在各自的从属权利要求中描述了另外的实施例。
通常,一种用于对其中设备正在离开在解剖结构内且相对于所述解剖结构的稳定位置的事件进行自动检测的方法,所述方法包括以下步骤:接收荧光透视图像的序列,在荧光透视图像中的至少两幅荧光透视图像中检测设备,确定荧光透视图像的所述序列中的检测到的设备的运动场,通过考虑所述运动场而整个荧光透视图像的所述序列来生成经整合的图像的序列,基于所述经整合的图像来确定显著性度量,并且基于所述显著性度量来识别所述经整合的图像中的界标。另外,可以基于所述显著性度量的变化来确定所述界标是否相对于所述设备正在移动。
应当注意,可以以手动方式或借助于利用适当的图像处理计算机软件的自动程序在荧光透视图像中检测设备或设备的感兴趣部分。基于这种检测,也可以通过例如输入来手动定义器械的部分周围的区,或者可以根据先前确定的程序或软件算法来自动定义器械部分的周围的区。应当理解,在手动检测设备的部分之后,可以自动执行对区的定义,或者可以在系统在荧光透视图像中检测到包括设备的各方面之后手动定义区,并且通过例如对所述区进行突出显示来假定一部分。
在所描述的方法的背景中,设备可以是能够被引入到身体中的用于治疗或诊断目的的介入器械,例如,用于将支架插入脉管系统的导管。这种设备的感兴趣部分可以具体是设备的端部部分,即,设备的远端部分,例如,导管的远端部分,在该远端部分处容纳用于引入身体的支架。例如,该器械一方面可以是柔性的或刚性的导管或线端或电极,另一方面也可以是活检设备、套管或套管针。该器械也能够是内假体,例如,支架,封堵器(例如,专利卵圆孔封堵器),人造瓣膜等。
应当理解,运动场是一个数学函数,其给出了从给定图像到另一图像的像素的运动。例如,猪尾导管的运动场指示如何将猪尾从其当前帧中的位置移位且移位多少,以找到其在下一帧中的位置。换句话说,荧光透视图像的所述序列包括第一荧光透视图像和第二荧光透视图像,并且对运动场的所述确定包括例如对所述设备的在所述第一荧光透视图像中的检测到的位置与在所述第二荧光透视图像中的检测到的位置之间的位移的确定。因此,运动场可以包括与一个设备有关的多个像素的位移。在所描述的方法中,可以考虑与设备有关的至少一个像素的位移,以用于对多幅(即,至少两幅)荧光透视图像进行整合。
还应当注意,术语“显著性度量”指的是允许在图像中突出显示具有期望属性的区域的定量量度。显著性度量可以是根据经整合的图像计算出的地图,其中,像素值越高,该像素属于具有与该设备相同的运动的结构的可能性越高。给定属性的结构是“显著的”。这里,该属性“具有与设备相同的运动或位移”。换句话说,术语“显著性度量”指的是包括至少一个显著结构的地图,该显著结构可以被指代为界标。基于像素值的高度,在经整合的图像中确定界标,尤其是如钙化的解剖学界标。
本发明的目的是利用设备的运动场来增强这样的结构或界标,否则这些结构或界标将太模糊而无法检测到。
根据该方法的实施例,对荧光透视图像的所述序列的整合是时间整合。也就是说,根据已经生成这些荧光透视图像的时间序列来处理(即,整合)荧光透视图像的接收到的序列。
在多于两幅的经整合的图像的序列中,可以针对每幅新接收到的经整合的图像新确定显著性度量,使得生成显著性度量的序列。在这样的序列中,当将一个显著性度量中的界标的像素值与另一显著性度量进行比较时,显著性度量可能会变化。例如,当界标的像素值从一个显著性度量到下一显著性度量增加时,该设备相对于界标可能并不产生移位。另一方面,当界标的像素值从一个显著性度量到下一显著性度量降低时,能够假设该设备相对于界标正在移动。
根据一个实施例,该方法还可以包括以下步骤:将荧光透视图像的所述序列中的至少一幅荧光透视图像与路线图一起可视化为所述路线图在所述至少一幅荧光透视图像上的叠加。
当如上所述确定出所述界标相对于所述设备(或反之亦然)的运动时,可以掩蔽所述路线图。
应当注意,所述解剖学界标可以包括脉管系统中的钙化。要不然,所述界标还可以包括已经植入的元件,例如,已经植入被引入脉管系统的设备附近的支架或任何其它手术植入物或矫形植入物。
如果根据术前3dct体积对钙化进行预分割,则能够将钙化实时投影在2d序列上。因此,钙化的2d形状和外观是已知的,并且能够用于改善显著性度量。
如果根据术前3dct体积对钙化进行预分割,则钙化在2d序列上的投影可以用于细化执行时间整合的区域。
能够通过首先检测和掩蔽其他设备(例如,假体主动脉瓣)来缩小计算显著性度量的区域。
为了确保整个部署期间的动态运动补偿,检测解锁(并且因此故障)可以触发针对当前跟踪算法的替代方案,例如,钙化跟踪。
根据本发明的另一方面,一种用于对其中设备正在离开在解剖结构内且相对于所述解剖结构的稳定位置的事件进行自动检测的系统通常包括用于生成荧光透视图像的设备,以及用于根据上述方法处理所述荧光透视图像的处理设备。
所述系统还可以包括提供至少一幅路线图的数据库。
所述方法的结果(即,所实现的组合图像)可以被显示在合适的设备上,例如被显示在监视器上。
根据另外的方面,提供了一种用于对其中设备正在离开在解剖结构内且相对于所述解剖结构的稳定位置的事件进行自动检测的计算机程序,其中,所述计算机程序当在系统的处理设备上正被执行时令所述系统执行上述方法。
因此,可以基本上以自动方式执行根据本发明的方法,或至少主要以自动方式执行根据本发明的方法。因此,所述计算机程序可以包括用于收集和至少临时存储由适当系统生成的至少两幅荧光透视图像的指令集、用于识别荧光透视图像中示出的设备的指令集、用于确定荧光透视图像中的检测到的设备的运动场的指令集、用于基于运动场来整合荧光透视图像的指令集、用于基于经整合的图像来确定显著性度量的指令集、用于基于显著性度量来识别经整合的图像中的界标的指令集以及用于基于显著性度量的变化来确定界标是否相对于设备正在移动的指令集。
另外,所述计算机程序可以包括用于从包括先前记录的图像信息的数据库加载数据的指令集,或者可以包括用于从用户检索信息的指令集。
这样的计算机程序优选地被加载到数据处理器的工作存储器中。因此,数据处理器被配备为执行本发明的方法。另外,本发明涉及可以存储计算机程序的诸如cd-rom的计算机可读介质。然而,所述计算机程序也可以通过诸如万维网的网络来呈现,并且能够从这样的网络下载到数据处理器的工作存储器中。
必须指出,本发明的实施例是参考不同主题来描述的。尤其地,一些实施例是参考方法型权利要求来描述的,而其他实施例是参考装置型权利要求来描述的。然而,除非另有说明,本领域技术人员将从以上和以下的描述中推断出,除属于一种类型的主题的特征的任意组合之外,涉及不同主题的特征之间的任意组合也被认为在本申请中被公开。
以上定义的各方面以及本发明的另外的方面、特征和优点还能够从下文中将要描述的实施例的范例中导出,并且参考附图中还示出的实施例的范例进行解释,但是本发明不限于此。
附图说明
图1是图示根据本发明的方法的流程图。
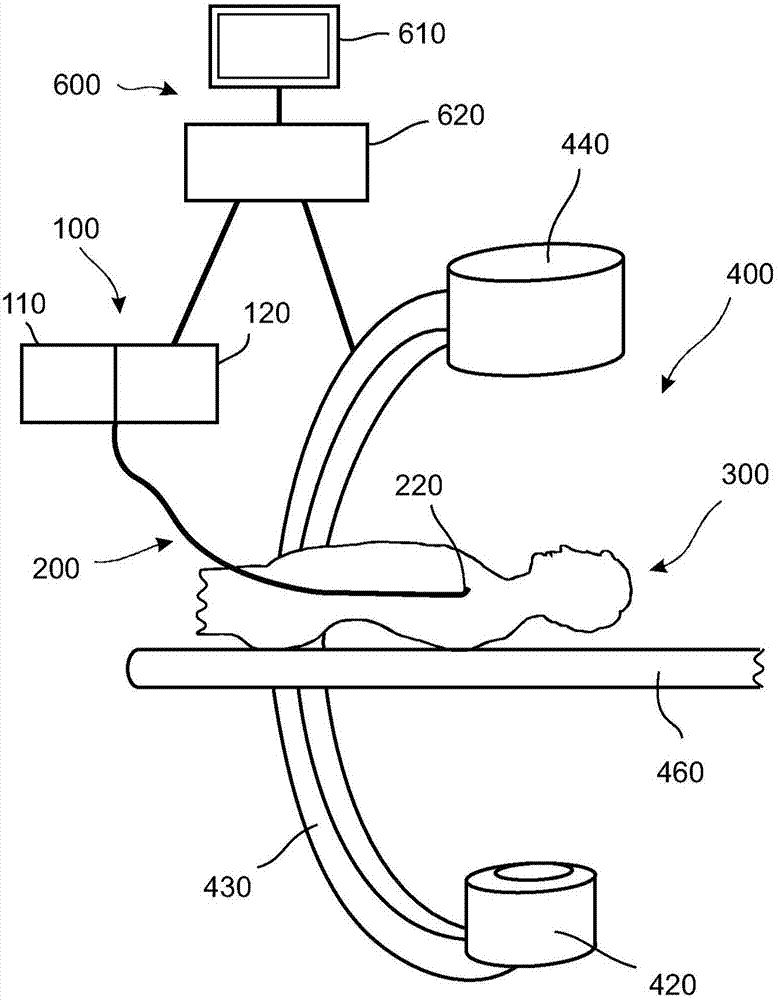
图2示出了根据本发明的系统的范例。
图3示出了具有突出显示的界标的荧光透视图像的范例。
图4示出了血管造影图像的范例。
图5示出了具有路线图的荧光透视图像的范例。
附图标记列表:
100控制台
110单元
120设备
200器械
220器械的端部部分
300患者
400x射线设备
420x射线源
430c型臂
440x射线探测器
460表
500界标
510变暗区
520路线图
600处理单元
610监视器
620控制设备
具体实施方式
图1中的流程图图示了根据本发明的方法的原理。应当理解,关于该方法描述的步骤是主要步骤,其中这些主要步骤可以被区分成或被分成若干子步骤。此外,这些主要步骤之间可能还有一些子步骤。因此,如果一个子步骤对于理解根据本发明的方法的原理很重要,则仅提及该子步骤。
作为范例的方式,在以下考虑tavi流程,其中动态运动补偿在瓣膜定位和瓣膜部署期间是特别有用的。
经受tavi介入的患者通常会具有钙化的主动脉和/或冠状动脉。如果这些钙化足够接近主动脉根部,则它们可以充当解剖学界标。
诊断和介入规划是基于诊断性血管造影的。导管在进入部位处插入脉管系统后,沿着大血管前进到要求处置的脉管结构。经由导管注入造影剂,并且cathlabx射线装备记录血管造影序列,所述血管造影序列示出填充有造影剂的血管。能够利用不同的成像器几何来重复诊断性血管造影采集。
在随后的介入中,将柔性的、部分或完全不透射线的导丝推进到受影响的脉管结构(例如,冠状动脉中的狭窄、神经血管动脉瘤或动静脉畸形)。荧光低剂量x射线监视可视化导丝,并允许介入医师在推进导丝时手眼协调。当被定位时,导丝充当轨道以递送介入设备(例如,用于扩张和支架递送的气囊、用于动脉瘤凝血的可拆卸线圈)。介入设备的递送和部署也是荧光透视控制的。
介入医师可以将导管锁定在主动脉的尖端。作为输入,可以假设已经在术前3dct体积中对主动脉根部进行分割(输入a到图1中的步骤s1)。另外,由x射线成像系统提供感兴趣区域的一幅或多幅血管造影图(输入b到图1中的步骤s1)。
在步骤s1中,可以将主动脉根部的3d路线图与先前的血管造影图静态地配准。然后,介入医师采集与血管造影图相同的几何参数的荧光透视序列,使得3d路线图的配准仍然有效(输入c到图1中的步骤s2)。
在步骤s2中,检测2dx射线序列中的注入导管的识别标志。也就是说,在x射线图像或帧中的至少两个中识别导管。
在步骤s3中,在x射线/荧光透视图像的序列中跟踪导管,使得获得针对当前帧的位移场或运动场。
在步骤s4中,在预期出现解剖学界标的区域中,运动场用于补偿各种运动(心跳、呼吸……)。在运动补偿区域中,执行对信号的时间整合。因此,具有与设备相同的运动的每个解剖结构将处于相同的位置处,因此它们的信号将通过时间整合而被增强。相反,时间整合将混合具有不同运动的目标或解剖结构,因此它们将显示为模糊区域。
然后在步骤s5中根据整合区域计算出显著性度量,其中,高值指示解剖结构已经被增强,而低值指示解剖结构已经被模糊化。
在步骤s6中,确定值是高还是低。在高值(图1中的路径h)的情况下,设备和解剖学界标遵循相同的位移/运动场,这意味着设备仍然被锁定到主动脉根部,并且该方法继续进行步骤s7。在低值(图1中的路径l)的情况下,至少一个解剖学界标具有与设备运动不相同的运动,使得能够断定该设备被解锁。在这种情况下,该方法将继续进行步骤s10。
在步骤s7中,由于血管结构本身不是不透射线的(即,在介入期间是不可见的),因此利用血管造影图到实况图像中的叠加技术(被称为路线图绘制)。可以在实况介入性荧光透视图旁边显示利用相似的成像器几何采集的静态诊断性血管造影图。对于血管内的导丝和设备的导航,静态血管造影图和实况荧光透视图的主观视觉融合是有利的。改进的背景丰富的可视化能够在导航中提供重要的支持。因此,将预处理的血管造影图的至少轮廓叠加在荧光透视图像流上,使得在一个屏幕上同步显示血管和介入设备。
在步骤s8中,可以显示显著性度量,即,可以显示其中指示设备附近的至少一个界标的地图。适当的显著性度量充当为对介入医师的视觉反馈,当设备被锁定时显示增强的解剖结构。应当注意,步骤s8也可以被省略。
在步骤s9中,检查当前处理的荧光透视帧是否是最后一帧。如果为是(y),则完成该流程,如果为否(n),则该流程通过在下一帧中跟踪设备来重复步骤s3。
如果在步骤s6中已经将值确定为低,即,已经检测到解锁,则在步骤s10中关闭3d路线图的显示,并且在步骤s11中能够发出视觉警告。
类似于步骤s9,在步骤s12中检查当前处理的荧光透视帧是否是最后一帧。如果为是(y),则完成该流程,如果为否(n),则该流程通过在下一帧中跟踪设备来重复步骤s3。
图2示出了根据本发明的示范性系统,该系统包括针对器械200的控制台100,该器械200可以被引入到患者300中。此外,x射线设备400相对于患者被布置为使得可以产生器械200的端部部分220所位于的区域的荧光透视图像。最后,提供处理单元600,所述处理单元600可以借助于x射线设备400以及控制台100来控制荧光透视图像的生成,以控制器械200的功能(如果适用)。
这里,控制器100还可以包括可以借以递送造影剂的单元110,使得可以生成例如血管造影图像或一系列血管造影图像。另一方面,借助于单元110,可以注入药物。另外,控制台100可以包括设备120,例如,借助于该设备120,可以控制器械200的端部部分220的取向,或者可以控制器械的特殊功能,如激光应用或对如支架的假体的放置,或引入气囊以及对气囊充气。应当注意,取决于想要的处置,控制台100还可以包括多于两个的单元或设备。
x射线设备400包括x射线源420以及用于x射线辐射的探测器440,其中,x射线源420以及x射线探测器440两者均被布置在c型臂430处,以确保两者相对于彼此的恰当取向。患者300可以被定位在诊察台460处。
处理单元600首先包括控制单元620,并且还包括监视器610,其中,可以在所述监视器上显示关于例如器械的端部的当前位置的信息的输出。
处理单元600还可以包括处理设备或工作存储器,在其上可以存储和/或执行根据本发明的执行解锁检测的计算机程序。
图3示出了荧光透视图像的一个范例,一方面示出了设备/导管200的远端部分,这里具体是导管上的基于塌缩的支架的心脏瓣膜,另一方面可以示出可以用作如图1所示的方法中的解剖学界标的钙化500。
图4示出了包括因升主动脉中具有造影剂的变暗区510的血管造影图像的范例。基于这样的血管造影图像,可以生成路线图520作为变暗区510的轮廓。
图5示出了荧光透视图像和在上述方法的步骤s1中生成的路线图的范例。
尽管已经在附图和前面的描述中详细图示和描述了本发明,但是这样的图示和描述应当被认为是图示性或示范性的,而非限制性的;本发明不限于所公开的实施例。
本领域技术人员通过研究附图、公开内容以及权利要求,在实践请求保护的发明时能够理解并实现对所公开的实施例的其他变型。在权利要求中,“包括”一词不排除其他元件或步骤,并且词语“一”或“一个”不排除多个。单个处理器或其他单元可以实现在权利要求中记载的若干项的功能。
尽管某些措施被记载在互不相同的从属权利要求中,但是这并不指示不能有利地使用这些措施的组合。计算机程序可以被存储/分布在合适的介质上,例如与其他硬件一起或作为其他硬件的部分供应的光学存储介质或固态介质,但是也可以被以其他形式分布,例如经由互联网或其他有线或无线的电信系统。权利要求中的任何附图标记都不应被解释为对范围的限制。
- 还没有人留言评论。精彩留言会获得点赞!