超声波手术系统的制作方法
本发明涉及一种超声波手术系统。
背景技术:
作为对生物体组织进行处置的处置器具之一,例如在日本特开2006-187617号公报中提出了一种能够对软骨进行处置的处置器具。该日本特开2006-187617号公报中提出的外科用切除装置具有轴(shaft)和组织作用前端部。在轴中形成有内腔。另外,组织作用前端部形成于轴的前端部,具有多个切除槽以及与轴的内腔连通的开口。这种结构的外科用切除装置使通过使轴旋转而进行旋转的组织作用前端部与软骨接触来进行软骨的切除。
技术实现要素:
日本特开2006-187617号公报中提出的外科用切除装置通过使组织作用前端部一边旋转一边接触软骨,来一边卷入软骨一边进行切除。因此,切削后的软骨表面容易成为粗糙的表面。
本发明的目的在于提供一种能够在适合于软骨的条件下进行处置的超声波手术系统。
本发明的第一方式的超声波手术系统是对软骨进行处置的超声波手术系统,具备:输出部,其生成驱动电力;振子,其与所述输出部连接,将所述驱动电力转换为超声波振动;探针,其与所述振子连接,用于传递所述超声波振动;切削部,其设置于所述探针,该切削部与所述软骨的规定部位接触并通过基于所述驱动电力所转换得到的超声波振动来使所述软骨的规定部位发热,并且在使该切削部与所述软骨接触的状态下由手术操作者推压该切削部来刮掉所述软骨;以及控制部,其对从所述输出部输出的所述驱动电力进行控制,使得所述软骨的规定部位的温度在2.2秒以内达到120℃以上。
根据本发明,能够提供一种能够在适合于软骨的条件下进行处置的超声波手术系统。
附图说明
图1是示出软骨、松质骨、皮质骨各自的成分的图。
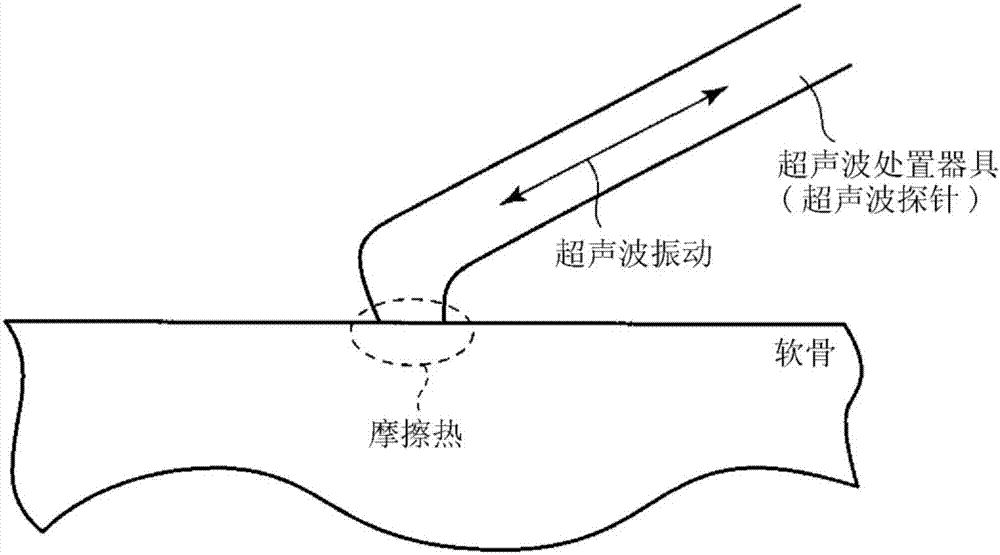
图2是示出利用超声波手术系统进行的软骨的切削的原理的图。
图3a是示出将烙铁以规定的按压负荷压紧于软骨时的切削温度与软骨切削量之间的关系的图。
图3b是示出将超声波切削器具以规定的按压负荷压紧于软骨时的切削温度与软骨切削量之间的关系的图。
图4是示出将烙铁压紧于软骨时的每个温度下的软骨表面和截面的状态的图。
图5a是示出将多个不同输出的超声波切削器具按压于软骨时的软骨的温度上升随时间变化的关系的图。
图5b是示出将图5a的输出a、b、c时的超声波切削器具按压于软骨时的软骨下骨的温度上升随时间变化的关系的图。
图6a是在输出a时将软骨的温度设为120℃的情况下的软骨与软骨下骨和松质骨的温度分布的示意图。
图6b是在输出b时将软骨的温度设为120℃的情况下的软骨与软骨下骨和松质骨的温度分布的示意图。
图6c是在输出c时将软骨的温度设为120℃的情况下的软骨与软骨下骨和松质骨的温度分布的示意图。
图7是示出本发明的各实施方式所涉及的手术系统的具体结构的一例的图。
图8是示出本发明的第一实施方式中的超声波手术系统的主要结构的框图。
图9是示出针对软骨测定改变了按压负荷或振幅时的切削量的变化的实验结果的图表。
图10是示出使用本发明的第一实施方式中的超声波手术系统进行的处置的流程的流程图。
图11是将使用高频手术系统(rf)切削软骨的切削处置结果、使用超声波手术系统(us)切削软骨的切削处置结果、以及使用利用电动机的手术系统(bur)切削软骨的切削处置结果进行比较所示出的图。
图12是示出使输出电流值过冲的变形例的图。
图13是示出本发明的第二实施方式的超声波手术系统的主要结构的框图。
图14是示出使用本发明的第三实施方式中的超声波手术系统进行的处置的流程的流程图。
图15是用于说明步骤s105中的切削部的推压的图。
具体实施方式
下面,参照附图来说明本发明的实施方式。
首先,对本实施方式的手术系统的工作方法的基本原理进行说明。本实施方式中的手术系统是软骨的切削处置系统。通过申请人的研究获知,以与对皮质骨、松质骨之类的其它骨的切削不同的机理进行软骨的切削。下面详细地进行说明。
图1是示出皮质骨、松质骨、软骨各自的成分的图。如图1所示,皮质骨和松质骨的主要成分是磷酸钙,与此相对,软骨的主要成分是蛋白质(胶原蛋白)。胶原蛋白不同于磷酸钙,具有弹性且柔软。因此,即使对胶原蛋白施加冲击,所施加的该冲击也会被吸收。因而,难以利用冲击来对以胶原蛋白为主要成分的软骨进行切削。
另一方面,通过申请人的研究获知,能够利用超声波手术系统来切削软骨。由于如上述的那样软骨吸收冲击,因此考虑利用超声波手术系统对软骨进行的切削是如图2所示那样通过利用使超声波切削器具与软骨接触时产生的摩擦热使软骨熔融来进行的。并且,图2是超声波手术系统的例子,使用超声波手术系统以外的加热设备也能够进行通过加热对软骨的切削。下面,进一步说明这种通过加热对软骨的切削。
图3a和图3b是示出软骨的温度与切削量之间的关系的图。在此,图3a是示出将烙铁以规定的按压负荷(2.94n)压紧于软骨时的软骨的温度与软骨的切削量之间的关系的图。另外,图3b是示出将超声波切削器具以规定的按压负荷(2.94n)压紧于软骨时的软骨的温度与软骨的切削量之间的关系的图。图3a和图3b的横轴表示生物体组织的温度(℃)。另外,图3a和图3b的纵轴表示软骨的切削量(切削深度)(mm3)。另外,图4是示出将烙铁压紧于软骨时的每个温度下的软骨表面和截面的状态的图。在图4中示出了40℃、80℃、120℃、160℃、200℃、240℃的状态。
在软骨的温度小于45℃时,如图3a和图3b所示,不进行软骨的切削。该温度范围内的软骨的表面和截面的状态被表示为图4的40℃的状态。
在软骨的温度为45℃~120℃时,如图3a和图3b所示,软骨的切削量与温度相应地变大。在该范围内,由于温度上升引起的切削量的增加小。该温度范围内的软骨的表面和截面的状态被表示为图4的80℃的状态。
在软骨的温度为120℃~160℃时,如图3a和图3b所示,软骨的切削量随着温度上升而急剧变大。该温度范围内的软骨的表面和截面的状态被表示为图4的120℃的状态。在该温度范围内,大幅地进行软骨的切削。
在软骨的温度为160℃~200℃时,如图3a和图3b所示,随着温度上升而产生的软骨的切削量的增加变小。该温度范围内的软骨的表面和截面的状态被表示为图4的160℃的状态。当软骨的温度达到160℃时,虽然进行软骨的切削,但软骨的表面开始烧焦。
当软骨的温度超过200℃时,如图3a和图3b所示,软骨的烧焦变大而软骨的切削量变得不规则。该温度范围内的软骨的表面和截面的状态被表示为图4的200℃的状态和240℃的状态。当软骨的温度超过200℃时,软骨表面的烧焦变大。
如图3a所示,仅通过利用烙铁施加热也能够进行软骨的切削。因而,可知,即使不是超声波切削器具,在对软骨施加了热的情况下,也能够切削软骨。但是,即使单纯地施加了热,在软骨的温度小于45℃时,软骨也不被切削,因此在对软骨进行切削处置时,需要使软骨的温度为45℃以上。另外,当软骨的温度超过200℃时,导致对软骨的热侵入变大,因此在对软骨进行切削处置时,期望使软骨的温度为220℃以下。并且,当考虑软骨的切削量与热侵入的大小之间的平衡时,在对软骨进行切削处置时,期望使软骨的温度为120℃-160℃。
另外,如根据图3a与图3b的比较也明确可知的那样,在烙铁与超声波切削器具比较时,在使用超声波切削器具的情况下,每个温度下的软骨的切削量(切削深度)更大。这是因为,在超声波切削器具的情况下,不只是单纯地对软骨施加热,还施加了通过超声波振动来刮掉熔融的软骨的作用。
在如上述的那样在软骨的切削中利用热的情况下,期望仅在需要进行处置的规定的区域施加热。例如,在作为处置对象的软骨为人体的软骨的情况下,存在发生了损伤的软骨、变性软骨之类的明确的处置对象。因而,期望仅在发生了损伤的软骨或变性软骨之类的需要的部位发生需要的温度上升,不在其周围的健康的软骨、软骨下的软骨下骨以及松质骨发生温度上升。一般地,已知松质骨/皮质骨之类的人体的细胞组织在40℃左右时可能发生损伤。另一方面,如上述的那样,期望在软骨的处置中使软骨的温度为120℃-160℃。当考虑到这些时,期望在尽可能短的时间内使作为处置部位的发生了损伤的软骨或变性软骨的温度为120℃附近,之后,在作为非处置部位的处置部位周围的松质骨等健康组织的温度上升之前结束处置。一般地,松质骨等开始发生损伤的温度为40℃左右,因此期望在软骨或变性软骨的温度达到了120℃时松质骨的温度没有达到40℃。
图5a是示出在将多个不同输出的超声波切削器具按压于软骨时的软骨的温度上升随时间变化的关系的图。在此,图5a的输出a是被调整为使软骨的温度在2.2秒内达到120℃的输出。另外,图5a的输出b是被调整为使软骨的温度在2.8秒内达到120℃的输出。另外,图5a的输出c是被调整为使软骨的温度在约20秒内达到120℃的输出。另一方面,图5b是示出在将图5a的输出a、b、c时的超声波切削器具按压于软骨时的软骨下骨的温度上升随时间变化的关系的图。在使软骨的温度在2.2秒内达到120℃的输出a的情况下,如图5b所示,在软骨的温度达到120℃的时间点,软骨下骨的温度没有超过40℃。另一方面,在使软骨的温度在2.8秒内达到120℃的输出b的情况下,如图5b所示,在软骨的温度达到120℃之前,软骨下骨的温度超过了40℃。同样地,在使软骨的温度在约20秒内达到120℃的输出c的情况下,如图5b所示,在软骨的温度达到120℃之前,软骨下骨的温度超过了40℃。
图6a是在输出a时将软骨的温度设为120℃的情况下的软骨与松质骨的温度分布的示意图。如图6a所示,在2.2秒的处置中,仅软骨的温度变为高温,软骨周边的软骨下骨和松质骨的温度上升被抑制。图6b是在输出b时将软骨的温度设为120℃的情况下的软骨与松质骨的温度分布的示意图。如图6b所示,在2.8秒的处置中,传递到软骨的热还被传递到软骨下骨和松质骨而导致松质骨的温度超过40℃。图6c是在输出c时将软骨的温度设为120℃的情况下的软骨与松质骨的温度分布的示意图。在图6c的例子中,也是在软骨的温度上升完成之前软骨下骨和松质骨的温度超过了40℃。
如以上那样,可知期望使利用超声波切削器具进行的处置为2.2秒以内。即,通过调整输出等使得软骨的温度能够在2.2秒以内达到120℃,能够实现适合于对人体的软骨进行处置的手术系统。
[第一实施方式]
对本发明的第一实施方式进行说明。图7是示出本发明的各实施方式所涉及的手术系统的具体结构的一例的图。如上述的那样,通过将软骨的温度设为适当的温度来进行软骨的切削处置。不对用于将软骨的温度设为适当的温度的方法进行限定。例如,可以将通过由超声波振动产生的摩擦热来使软骨的温度为45℃-220℃、优选为120℃-160℃的范围内的规定温度的系统用作本实施方式中的手术系统,也可以将通过由加热器进行的加热来使软骨的温度为45℃-220℃、优选为120℃-160℃的范围内的规定温度的系统用作本实施方式中的手术系统,还可以将通过施加高频电流来使软骨的温度为45℃-220℃、优选为120℃-160℃的范围内的规定温度的系统用作本实施方式中的手术系统。图7示出作为本实施方式所涉及的手术系统的一例的超声波手术系统1。
图7所示的超声波手术系统1具有用于利用超声波对生物体组织进行处置的切削器具10、向切削器具10供给驱动电力的电源装置80以及脚踏开关90。超声波手术系统1是适合于软骨的处置的系统。然而,在软骨以外的生物体组织的处置中也能够利用超声波手术系统1。
作为能量切削器具的切削器具10具有手持件20、从手持件20突出的探针180以及形成于探针180周围的细长形状的护套30。在以后的说明中,将切削器具10中的探针180侧称为切削器具10的前端侧,将手持件20侧称为基端侧。
手持件20在其内部具有超声波振子。超声波振子根据来自电源装置80的驱动电力进行超声波振动。手持件20将由该超声波振子产生的超声波振动传递至探针180。探针180通过护套30而与超声波振子连接,随着超声波振子的振动而进行振动。
护套30的前端形成为半圆筒状,设置于探针180的前端的切削部181从形成为该半圆筒状的部分露出。另外,在护套30的前端例如形成有冷刀182。冷刀182由耐腐蚀性的金属材料形成,用于容易地切除生物体组织。此外,也可以不设置冷刀182。
另外,手持件20具有输入部22。输入部22是用于输入用于驱动超声波振子的指示的部位。输入部22可以包括多个开关,以进行与多种超声波振子的驱动对应的多种输入。多个开关包含例如用于将超声波振子的驱动设为适合于软骨处置的驱动的开关。输入部22与电源装置80相连接。另外,手持件20内的超声波振子与电源装置80相连接。电源装置80检测向输入部22的输入,并将与该输入相应的驱动电力供给到超声波振子。
脚踏开关90具有与设置于手持件20的输入部22同样的功能。即,在脚踏开关90,与输入部22同样地设置有开关。脚踏开关90也可以与输入部22同样地包含多个开关。电源装置80当检测出向脚踏开关90的输入时,将与该输入相应的驱动电力供给到超声波振子。
在进行处置时,用户保持手持件20并使设置于进行超声波振动的探针180的切削部181与作为处置对象的生物体组织接触。此时,用户对输入部22或脚踏开关90进行操作来驱动超声波振子。由超声波振子产生的振动被传递至探针180。通过进行振动的探针180的切削部181与生物体组织接触,来进行生物体组织的切削或切除等处置。
图8是示出本发明的第一实施方式中的超声波手术系统1的主要结构的框图。在图8中,对于与图7中所说明的结构相同的结构,通过标注与图7相同的附图标记来省略说明。
如图8所示,电源装置80具有输出电路81和控制电路82。
输出电路81与超声波振子24电连接,是生成用于驱动设置于切削器具10的手持件20的内部的超声波振子24的驱动电力的输出部。基于该驱动电力从输出电路81向切削器具10输出输出电压和输出电流。
控制电路82例如由cpu、asic构成,是根据来自输入部22或脚踏开关90的输入来对输出电路81的驱动电力进行控制的控制部。例如,在根据来自输入部22或脚踏开关90的输入进行了设为软骨的切削处置模式的意思的指示的情况下,控制电路82对输出电路81进行控制,以由切削器具10产生使软骨的温度为上述的温度、即45℃-220℃、优选为120℃-160℃那样的超声波振动。在超声波手术系统的情况下,利用摩擦热来对软骨施加温度变化。如图9所示,已知由摩擦热产生的加热量是由超声波振动的振幅和切削器具10对软骨的按压负荷决定的。因而,例如,如果按压负荷的值被固定为由医生将切削器具10按压于生物体组织时的按压负荷的平均值,则摩擦热仅根据振幅而变化。在本实施方式中,在将按压负荷设为固定值的基础之上,通过实验来测定如使软骨的温度为45℃-220℃、优选为120℃-160℃的范围内的规定温度那样的振幅,并将测定出的振幅的值事先存储到控制电路82的存储器821中。控制电路82从存储器821读出该振幅的值,并对输出电路81的输出电流和输出电压进行控制,使得超声波振子24以所读出的振幅进行振动。
另外,如上述的那样,优选的是期望使处置部位的温度在2.2秒左右内上升到120℃。为了利用超声波手术系统使处置部位的温度快速地上升,只要单纯地使超声波振动的振幅增大即可。并且,通过使向切削部的按压负荷增大,能够使处置部位的温度更快地上升。
下面,说明本实施方式的超声波手术系统1的动作。图10是示出使用第一实施方式中的超声波手术系统1进行的处置的流程的流程图。图10示出膝关节处的变性软骨的切除处置的流程。图10的流程不限于膝关节,还能够应用于对肩关节等其它关节的处置。
在步骤s101中,医生使用套管针来形成用于能够将切削器具和关节镜插入至作为处置对象的生物体组织(在此,为膝关节内的变性软骨)的位置的孔。
在步骤s102中,医生将关节镜和超声波手术系统1的切削器具10经过关节镜用的孔插入到膝关节内。
在步骤s103中,医生一边观察通过关节镜显示于监视器上的膝关节内的图像一边使超声波手术系统1的切削部181与作为处置对象的变性软骨接触。
在步骤s104中,医生例如对输入部22进行操作来将超声波手术系统1设定为软骨模式,开始进行变性软骨的切除处置。当超声波手术系统1被设定为软骨模式时,控制电路82读出预先存储于存储器821中的振幅的值(例如使软骨的温度为120℃所需要的振幅的值),对输出电路81进行控制,使得超声波振子24以所读出的振幅进行振动。通过使正在以该振幅振动的切削部181以某固定的按压负荷接触变性软骨,变性软骨的温度上升。由此,变性软骨熔融来进行变性软骨的切除。在此,更优选的是,步骤s104中的振幅的值为使软骨的温度在规定的短时间内(2.2秒以内)达到120℃所需要的温度。由此,处置在短时间内结束,能够抑制非处置部位的不需要的温度上升。
如以上所说明的那样,根据本实施方式,着眼于通过使软骨的温度为45℃以上而使软骨熔融来进行软骨的切削,对由切削器具10产生的对软骨的加热量进行控制使得软骨的温度为45℃。由此,能够可靠地进行软骨的切削处置。
并且,根据本实施方式,还考虑软骨的热侵入的影响对由切削器具10产生的对软骨的加热量进行控制,使得软骨的温度为45℃-220℃、优选为120℃-160℃的范围内的规定温度。由此,能够以低侵入的方式进行软骨的切削处置。
并且,根据本实施方式,能够通过利用切削器具10对软骨的处置来使处置在短时间内结束。由此,能够抑制不需要进行处置的非处置部位的不需要的温度上升。
此外,在上述的实施方式中,作为手术系统,例示了超声波手术系统。在本实施方式中,只要能够使软骨的温度为45℃-220℃、优选为120℃-160℃的范围内的规定温度即可,还能够使用超声波手术系统以外的例如利用加热器的手术系统、利用高频电流的手术系统或者利用它们的组合之类的与超声波不同的能量的手术系统。然而,在使用超声波手术系统的情况下,与利用加热器的手术系统、利用高频的手术系统等相比,热侵入小。另外,与利用电动机的手术系统相比,处置后的软骨的表面光滑。
图11是将使用高频手术系统(rf)切削软骨的切削处置结果与使用超声波手术系统(us)切削软骨的切削处置结果进行比较所示出的图。此外,在图11中,为了进行比较,还示出使用利用电动机的手术系统(bur)切削软骨的切削处置结果(即,仅利用冲击的切削处置的结果)。如图11所示,在仅利用冲击的切削处置中,软骨几乎不被切削。不仅如此,软骨的表面不保留原型而呈现出绒毛状。另一方面,在利用高频的切削处置中,与利用电动机的处置相比,虽然进行软骨的切削,但是热侵入波及比较广的范围。与此相对,在利用超声波的切削处置中,进一步进行软骨的切削,并且热侵入比较小。
此外,已知的是,与高频手术系统相比,在超声波手术系统的情况下,升温速度慢。因此,在超声波手术系统中,为了使软骨的温度尽可能快速地达到目标温度,也可以如图12所示那样在超声波手术系统刚启动后的规定期间内使输出电流值相比于与本来的振幅值相当的输出电流值而言过冲。
[第二实施方式]
下面,对第二实施方式进行说明。在上述的实施方式中,在对切削器具10中的对软骨的加热量进行控制使得软骨为适合于切削的温度时,按照通过实测预先决定的设定(例如振幅)来进行控制。第二实施方式是对切削器具10中的对软骨的加热量进行反馈控制的例子。
图13是示出本发明的第二实施方式中的超声波手术系统1的主要结构的框图。在图13中,对于与图8中所说明的结构相同的结构,通过标注与图8相同的附图标记来省略说明。
第二实施方式中的超声波手术系统1的切削器具10具有温度传感器26。温度传感器26例如设置于切削器具10的前端内部,用于检测切削器具10的前端的温度、即软骨的温度,将与检测出的温度相应的信号输入到电源装置80的控制电路82。温度传感器26能够使用热电偶、热敏电阻等各种温度传感器。
第二实施方式中的控制电路82对输出电路81进行控制,以使由温度传感器26测定出的温度维持45℃-220℃、优选为120℃-160℃的范围内的规定温度。例如,在由温度传感器26测定出的温度小于规定温度的情况下,控制电路82以使来自输出电路81的输出电流增大的方式对输出电路81进行控制。另外,在由温度传感器26测定出的温度超过了规定温度的情况下,控制电路82以使来自输出电路81的输出电流减小的方式对输出电路81进行控制。
如以上所说明的那样,根据本实施方式,通过根据由温度传感器测定出的软骨的温度对来自输出电路81的输出电力进行反馈控制,相比于第一实施方式而言更可靠地进行软骨的切削处置。另外,能够省略如第一实施方式那样的存储器821。
在此,在第二实施方式中,利用温度传感器26测定软骨的温度。软骨的温度的测定方法不限于利用温度传感器的方法。
[第三实施方式]
下面,对第三实施方式进行说明。第三实施方式是处置的方法的变形例。如上述的那样,期望的是,在处置中,仅使处置部位的温度上升到120℃-160℃,使非处置部位的温度为40℃以下。作为实现该目的的方法,在超声波手术系统1的情况下考虑使振幅增大或使按压负荷增大。本实施方式通过处置的方法来进一步缩短处置的时间。
图14是示出利用第三实施方式中的超声波手术系统1进行的处置的流程的流程图。在此,与图10同样地,图14也示出膝关节处的变性软骨的切除处置的流程。图14的流程不限于膝关节,还能够应用于对肩关节等其它关节的处置。此外,在图14中,对于与图10相同的处理,适当地省略说明。即,省略对步骤s101-s103的处理的说明。
在步骤s204中,医生例如对输入部22进行操作来将超声波手术系统1设定为软骨模式,开始进行变性软骨的切除处置。当超声波手术系统1被设定为软骨模式时,控制电路82读出预先存储于存储器821中的振幅的值(例如,使软骨的温度在2.2秒以内达到120℃所需要的振幅的值),对输出电路81进行控制,使得超声波振子24以所读出的振幅进行振动。通过使正在以该振幅振动的切削部181以某固定的按压负荷接触变性软骨,变性软骨的温度上升。
在步骤s205中,医生利用探针180来如图15所示那样切削(切除)软骨(energyassistedtrimmingorremove,accurateshaving,excise:能量辅助修整或去除、精确的切削、切除)。“如图15所示那样”是指如剥皮那样一边产生具有连续性的连在一起的膜状的切削屑一边切削(切除)(paring)软骨,更具体地说,如以下那样。医生向作为与接触方向不同的方向的与软骨的表面大致平行的方向推压切削部181。由此,对软骨施加压缩力,软骨的温度进一步上升且变性软骨熔融,来进行变性软骨的切除。并且,通过对被加热后的软骨的表面向与软骨的表面平行的方向施加切削部181的推压,如图15所示那样呈膜状刮削软骨的表面。像这样,能够更高效地进行变性软骨的切除。
如以上所说明的那样,根据本实施方式,除了第一实施方式中所说明的效果以外,通过对被加热后的软骨的表面向与软骨的表面平行的方向施加切削部181的推压,能够更高效地进行变性软骨的切除。此外,在步骤s205中向与接触方向不同的方向进行推压,但是也可以通过向接触方向推压,来向软骨的厚度(深度)方向进行切削。
在此,第三实施方式的步骤s205的处理还能够应用于超声波处置系统以外的例如利用加热器的手术系统、利用高频电流的手术系统或者利用它们的组合之类的与超声波不同的能量的手术系统。
以上,基于实施方式说明了本发明,但是不言而喻的是,本发明并不限定于上述的实施方式,在本发明的主旨的范围内能够进行各种变形、应用。
- 还没有人留言评论。精彩留言会获得点赞!