作为促动力药的5-HT4受体激动剂的制作方法
技术领域
本发明涉及一种用于治疗人体的4-{[4-({[4-(2,2,2-三氟乙氧基)-1,2-苯并异噁唑-3-基]-氧基}甲基)哌啶-1-基]甲基}四氢化-2H-吡喃 -4-甲酸(下文称为“化合物A”)。具体而言,本发明涉及一种在治疗胃肠疾病或者预防或延缓胃肠疾病的发作或发展方面有用的具有选择性5-HT4受体激动性的化合物A。
本发明还涉及一种用于治疗胃肠疾病的药物组合物,所述药物组合物包含治疗有效量的化合物A或其药学上可接受的盐。本发明涉及一种用于治疗包括哺乳动物受治者在内的动物受治者中的胃肠疾病的方法,所述方法包括将化合物A或其药学上可接受的盐给药于包括哺乳动物受治者在内的动物受治者。本发明还涉及一种用于治疗包括哺乳动物受治者在内的动物受治者中的胃肠疾病的方法,所述方法包括将治疗有效量的化合物A或其药学上可接受的盐给药于有需要的包括哺乳动物受治者在内的动物受治者。
背景技术:
通常,人们发现5-HT4受体激动剂在治疗下列多种疾病方面有用,所述疾病例如胃食管反流疾病(GERD)、胃肠疾病、胃动力障碍、非溃疡性消化不良、机能性消化不良(FD)、肠易激综合症(IBS)、便秘、消化不良、食道炎、胃食管疾病、胃炎、恶心、中枢神经系统疾病、阿尔茨海默氏病(AD)、认知障碍、呕吐、偏头痛、神经疾病、疼痛、心血管疾病(例如,心力衰竭和心律失常)以及呼吸暂停综合症(参见,NPL1、NPL2、NPL3、NPL4、NPL5、NPL6和NPL7)。
显然,具有5-HT4受体激动活性的药物作为促动力药起作用。然而,5-HT4激动剂也已表现出在上胃肠道和下胃肠道中的组织特异性活性,所述5-HT4激动剂例如,西沙必利、莫沙必利、普卢卡必利和替加色罗。也就是说,莫沙必利和西沙必利选择性促进上胃肠(GI)的运动性而不是下GI运动性,因此,所述莫沙必利和西沙必利作为促动力药销售。
另一方面,普卢卡必利(NPL8)和替加色罗(NPL9)促进下GI 的运动性,因此,所述普卢卡必利(NPL8)和替加色罗(NPL9)在临床上用于治疗便秘和/或便秘型IBS(C-IBS)。此外,普卢卡必利(NPL8) 已表现出选择性刺激健康人体中的结肠运输而不改变胃排空或小肠运输(NPL10)。
此外,正在研制的velusetrag(TD-5108)(NPL11)和奈莫必利 (naronapride)(ATI-7505)(NPL12)落入治疗便秘的药物类别中。
在内侧靠前的位置中,大多数患有功能性肠病的患者通常具有影响上GI道和下GI道的重叠的症状。实际上,通常观察到IBS与GERD 有关。不幸的是,没有具有相同程度的上GI运动性和下GI运动性这两者的药物。因此,许多患有GI疾病的患者非常期望这样一种以单一给药的方式表现出对上GI运动性和下GI运动性均有刺激性影响的理想的药物。
为了解决上述问题,本发明的发明人已发现具有5-HT4激动性的化合物A在相同剂量条件下对窦(上)运动性和结肠(下)运动性均发挥刺激性影响。因此,本发明涉及明显地表现出以相同程度刺激性影响上GI运动性和下GI运动性这两者的化合物的第一实例。此外,化合物A对GI运动性的影响比本发明描述的实施例中所示的那些其他 5-HT4激动剂大得多(大于100倍)。这些特性表明对于患有功能性便秘和具有上GI症状的C-IBS(例如,消化不良或胃灼热)的患者而言,化合物A是有价值的且可行的其他促动力药的替代物。
引用文献列表
非专利文献
非专利文献1:Bockaert J.等人,TiPs 13;141-45,1992
非专利文献2:Ford A.P等人,Med.Res.Rev.13:633-62,1993
非专利文献3:Gullikson G.W.等人,Drug Dev.Res.26;405-17, 1992
非专利文献4:Richard M.Eglen等人,TiPs 16;391-98,1995
非专利文献5:Bockaert J.等人,CNS Drugs 1;6-15,1994
非专利文献6:Romanelli M.N.等人,Arzheim Forsch./Drug Res., 43;913-18,1993
非专利文献7:Kaumann A.J.等人,Naunyn-Schmiedebergs Arch Pharmacol.,344;150-59,1991
非专利文献8:Bouras E.P.等人,Gastroenterology.2001Feb;120 (2):354-60。
非专利文献9:Degen L.等人,Aliment Pharmacol Ther.2001Nov; 15(11):1745-51。
非专利文献10:Bauras E.P.等人,Gut,1999,44,682-686。
非专利文献11:Manini M.L.等人,Neurogastroenterol Motil.2010 Jan;22(1):42-9,e7-8.Epub 2009Aug 18。
非专利文献12:Camilleri M.等人,Neurogastroenterol Motil.2007 Jan;19(1):30-8。
技术实现要素:
本发明的目的在于提供一种用于治疗人体的化合物A。具体而言,本发明的目的在于提供一种在治疗胃肠疾病或者预防或延缓胃肠疾病的发作或发展方面有用的具有选择性5-HT4受体激动性的化合物A。
此外,本发明的目的在于提供一种用于治疗胃肠疾病的药物组合物,所述药物组合物包含治疗有效量的化合物A或其药学上可接受的盐,本发明的目的在于提供一种用于治疗包括哺乳动物受治者在内的动物受治者中的胃肠疾病的方法,所述方法包括将化合物A或其药学上可接受的盐给药于包括哺乳动物受治者在内的动物受治者,本发明的目的还在于提供一种用于治疗包括哺乳动物受治者在内的动物受治者中的胃肠疾病的方法,所述方法包括将治疗有效量的化合物A或其药学上可接受的盐给药于有需要的包括哺乳动物受治者在内的动物受治者。
本发明的要点如下:
[1]4-{[4-({[4-(2,2,2-三氟乙氧基)-1,2-苯并异噁唑-3-基]氧基}甲基)-哌啶-1-基]甲基}四氢化-2H-吡喃-4-甲酸或其药学上可接受的盐在制备用于治疗包括哺乳动物受治者在内的动物受治者中的胃肠疾病的药物中的用途;
[2]如[1]所述的用途,其中,4-{[4-({[4-(2,2,2-三氟乙氧基)-1,2-苯并异噁唑-3-基]氧基}甲基)哌啶-1-基]甲基}四氢化-2H-吡喃-4-甲酸或其药学上可接受的盐与已知在治疗或预防胃肠疾病或其症状中有用的一种或多种其他化合物联合使用;
[3]一种用于治疗胃肠疾病的药物组合物,所述药物组合物包含治疗有效量的4-{[4-({[4-(2,2,2-三氟乙氧基)-1,2-苯并异噁唑-3-基]氧基} 甲基)哌啶-1-基]甲基}四氢化-2H-吡喃-4-甲酸或其药学上可接受的盐;
[4]如[3]所述的药物组合物,其中,所述药物组合物还包含治疗有效量的已知在治疗或预防胃肠疾病或其症状中有用的一种或多种其他化合物;
[5]一种用于治疗包括哺乳动物受治者在内的动物受治者中的胃肠疾病的方法,所述方法包括将4-{[4-({[4-(2,2,2-三氟乙氧基)-1,2-苯并异噁唑-3-基]-氧基}甲基)哌啶-1-基]甲基}四氢化-2H-吡喃-4-甲酸或其药学上可接受的盐给药于包括哺乳动物受治者在内的动物受治者;
[6]如[5]所述的方法,其中,所述方法还包括给药治疗有效量的已知在治疗或预防胃肠疾病中有用的一种或多种其他化合物;
[7]一种用于治疗胃肠疾病的方法,所述方法包括将治疗有效量的 4-{[4-({[4-(2,2,2-三氟乙氧基)-1,2-苯并异噁唑-3-基]氧基}甲基)哌啶-1- 基]甲基}四氢化-2H-吡喃-4-甲酸或其药学上可接受的盐给药于有需要的包括哺乳动物受治者在内的动物受治者;
[8]如[7]所述的方法,其中,所述方法还包括给药治疗有效量的已知在治疗或预防胃肠疾病中有用的一种或多种其他化合物;以及
[9]用于治疗包括哺乳动物受治者在内的动物受治者中的胃肠疾病的4-{[4-({[4-(2,2,2-三氟乙氧基)-1,2-苯并异噁唑-3-基]氧基}甲基)-哌啶 -1-基]甲基}四氢化-2H-吡喃-4-甲酸或其药学上可接受的盐。
发明效果
目前意外地发现对上GI道和下GI道中的GI运动性均具有强烈影响的本发明的化合物A在治疗胃肠疾病中有用。
也就是说,本发明的发明人使用犬胃排空模型和犬胃肠运动性模型发现了本发明的化合物A在治疗胃肠疾病方面具有理想的性质。在上述模型中,已发现本发明的化合物A的效力比其他5-TH4激动剂(例如,西沙必利、莫沙必利和替加色罗)的效力强得多(效力大于100 倍)。
因此,本发明的化合物A在治疗胃肠疾病方面有用。
附图说明
图1为表示在禁食状态的清醒的犬中,口服给药化合物A之后,胃窦运动性以剂量依赖的方式增强的图。
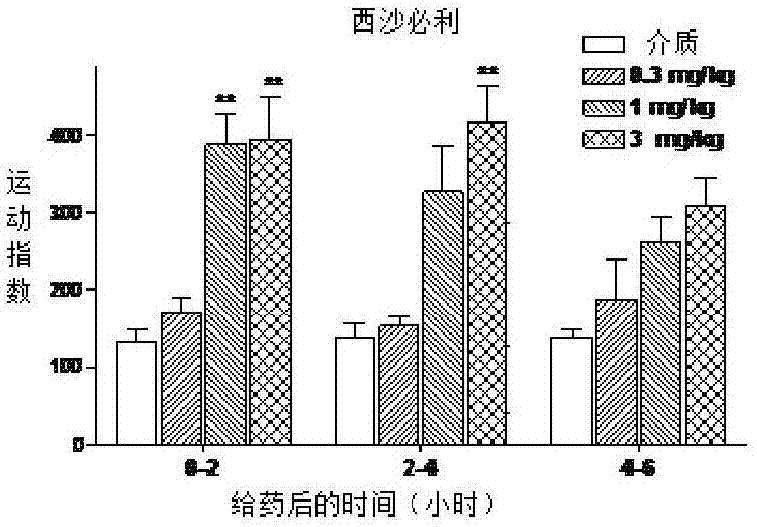
图2为表示在禁食状态的清醒的犬中,口服给药西沙必利之后,胃窦运动性以剂量依赖的方式增强的图。
图3为表示在禁食状态的清醒的犬中,莫沙必利对胃窦运动性的影响的图。
图4为表示在禁食状态的清醒的犬(典型跟踪)中,口服给药化合物A(1μg/kg)之后,胃窦和近侧结肠运动性增强的图。
图5为表示在禁食状态的清醒的犬(典型跟踪)中,普卢卡必利 (0.1mg/kg,0.3mg/kg)对胃窦、十二指肠和近侧结肠运动性的影响的图。
发明详述
用于治疗胃肠疾病的本发明的化合物A为4-{[4-({[4-(2,2,2-三氟乙氧基)-1,2-苯并异噁唑-3-基]氧基}甲基)哌啶-1-基]甲基}四氢化-2H- 吡喃-4-甲酸,其在WO2006/090224中公开。
本发明的化合物A包括溶剂化物、水合物、复合物、多晶型物、前体药物、异构体和同位素标记的化合物。
此外,本发明提供一种用于治疗包括哺乳动物受治者在内的动物受治者中的胃肠疾病的药物组合物,所述治疗包括将治疗有效量的化合物A或其药学上可接受的盐给药于上述受治者。
进一步而言,本发明还提供一种用于治疗胃肠疾病的药物组合物,所述药物组合物包含治疗有效量的化合物A或其药学上可接受的盐以及药学上可接受的载体。
此外,本发明提供一种用于治疗包括哺乳动物受治者在内的动物受治者中的胃肠疾病的方法,所述方法包括将治疗有效量的化合物A 或其药学上可接受的盐给药于有需要的上述受治者。进一步而言,本发明提供一种用于治疗包括哺乳动物受治者在内的动物受治者中的胃肠疾病的方法,所述方法包括将化合物A或其药学上可接受的盐给药于包括哺乳动物受治者在内的动物受治者。而且,本发明提供一种化合物A或其药学上可接受的盐在制备用于治疗包括哺乳动物受治者在内的动物受治者中的胃肠疾病的药物中的用途。
本文使用的术语“动物受治者”包括哺乳动物受治者或非哺乳动物受治者。合适的哺乳动物受治者的实例可包括但不限于:人类、啮齿类动物、宠物、家畜和灵长类动物。合适的啮齿类动物可包括但不限于:小鼠、大鼠、仓鼠、沙鼠以及豚鼠。合适的宠物可包括但不限于:猫、狗、兔以及白鼬。合适的家畜可包括但不限于:马、山羊、绵羊、猪、牛、美洲驼以及羊驼。合适的灵长类动物可包括但不限于:黑猩猩、狐猴、猕猴、狨、蜘蛛猿、松鼠猴和小猿。合适的非哺乳动物受治者的实例可包括但不限于:鸟类、爬行动物、两栖动物和鱼。鸟类的非限定性的实例包括鸡、火鸡、鸭和鹅。
术语“胃肠疾病”包括GERD、机能性消化不良、IBS、便秘和与 GI运动性降低有关的其他类型的胃肠疾病。术语“胃肠疾病”还包括诸如胃灼热、消化不良、恶心和腹痛之类的临床症状。
本文使用的术语“治疗(treating)”是指逆转、缓解、抑制或预防对其应用该术语的疾病或病症的发作或发展或者逆转、缓解、抑制或预防所述疾病或病症的一种或多种症状。如上治疗(treating)所定义的,本文使用的术语“治疗(treatment)”是指治疗(treating)的行为。
本发明还包括化合物A的同位素标记的化合物,但事实上,一个以上原子可被具有与通常在自然界中发现的原子量或质量数不同的原子量或质量数的原子替代。可掺入本发明的化合物中的同位素的实例包括氢、碳、氮、氧、磷、硫、氟和氯的同位素,分别例如,2H、3H、13C、14C、15N、18O、17O、31P、32P、35S、18F和36Cl。包含上述同位素和/或其它原子的其它同位素的本发明的化合物A、其前体药物、其药学上可接受的酯和所述化合物、所述酯或所述前体药物的药学上可接受的盐在本发明的范围之内。本发明的一些同位素标记的化合物(例如,掺入了诸如3H和14C之类的放射性同位素的那些化合物)在药物和/或基底组织分布分析中有用。含氚的氢(即,3H)同位素和碳-14(即,14C)同位素由于其易于呈现和检测而特别优选。进一步而言,用诸如氘(即,2H)之类的较重的同位素取代可提供由较大的代谢稳定性产生的治疗优势,例如,增加体内半衰期或降低剂量需求,因此,用诸如氘(即,2H)之类的较重的同位素取代在一些情况下可以是优选的。本发明的化合物A的同位素标记的化合物及其前体药物通常可通过实施专利公开WO2006/090224中公开的步骤以及通过用容易获得的同位素标记的试剂取代非同位素标记的试剂来制备。
本发明包括所获得的化合物A的盐的形式。
本发明的化合物A能够形成药学上可接受的无毒的阳离子。
用于制备化合物A的药学上可接受的碱加成盐的碱是那些形成无毒的碱加成盐的碱。所述碱加成盐可通过常规步骤来制备。
因为本发明的化合物A为碱性化合物,所以,它们能够由各种无机酸和有机酸形成各种不同的盐。
用于制备本发明的化合物A的碱性化合物的药学上可接受的酸加成盐的酸是那些形成无毒的酸加成盐的酸。所述酸加成盐可通过常规步骤来制备。
合适的盐的综述,请参见Berge S.M.等人在J.Pharm.Sci.,66,1-19, 1977中发表的文章。
还包括在本发明的范围内的是化合物A的生物前体(也称为“前体药物”)。化合物A的生物前体是其化学衍生物,该化学衍生物易于在生物体系中变回化合物A的母体化合物。具体而言,化合物A的生物前体在已将该生物前体给药于包括哺乳动物受治者在内的动物受治者(例如,人类受治者)并被所述受治者吸收之后变回母体化合物A。
使用前体药物的进一步的信息可在Pro-drugs as Novel Delivery Systems,Vol.14,ACS Symposium Series(T Higuchi和W Stella)以及 Bioreversible Carriers in Drug Design,Pergamon Press,1987(E B Roche 编辑,American Pharmaceutical Association)中找到。
当本发明的化合物A形成诸如水合物之类的溶剂化物时,这些溶剂化物包括在本发明的范围内。
对于治疗或预防胃肠疾病而言,本发明的化合物A对成人(60kg/ 体重)的合适剂量水平为约0.0001毫克/天至1000毫克/天,优选为约 0.001毫克/天至100毫克/天,以及更优选为约0.005毫克/天至50毫克 /天。化合物可以每天1至4次的方案给药。然而,在一些情况下,也可使用超出这些限制的剂量。
本发明的化合物A可通过先前说明的上述途径中的任一种单独给药或与药学上可接受的载体或稀释剂联合给药,并且这样的给药可以单一剂量或多剂量进行。更加具体而言,本发明的新治疗剂可以多种不同的剂型给药,即,本发明的新治疗剂可与各种药学上可接受的惰性载体联合以形成片剂、胶囊、锭剂、药片、硬糖、粉末、喷雾剂、霜剂、药膏、栓剂、胶状物、凝胶剂、糊剂、洗液、软膏、水性悬浮液、可注射溶液、酏剂、糖浆,等等。这些载体包括固体稀释剂或填充剂、无菌水性介质以及各种无毒有机溶剂,等等。而且,口服药物组合物可被适当地变甜和/或调味。总体而言,本发明的治疗上有效的化合物在这些剂型中的浓度水平为按重量计5%至70%,优选浓度水平为按重量计10%至50%。
对于口服给药而言,含有各种赋形剂的片剂可与各种崩解剂和造粒粘结剂一同使用,所述赋形剂例如,微晶纤维素、柠檬酸钠、碳酸钙、磷酸氢二钾和甘氨酸,所述崩解剂例如淀粉(优选为玉米淀粉、马铃薯淀粉或木薯淀粉)、海藻酸和一些硅酸盐复合物,所述造粒粘结剂例如,聚乙烯吡咯烷酮、蔗糖、明胶和阿拉伯胶。此外,为了压片的目的,诸如硬脂酸镁、月桂基硫酸钠和滑石之类的润滑剂通常非常有用。相似类型的固体组合物还可用作明胶胶囊中的填充剂,在这种关系中优选的物质还包括乳糖(lactose或milk sugar)以及高分子量聚乙二醇。当水性悬浮液和/或酏剂对于口服给药而言理想时,活性成分可与各种甜味剂或调味剂、着色剂或染料、乳化剂和/或悬浮剂(如果需要的话)和诸如水、乙醇、丙二醇、甘油之类的稀释剂以及它们的各种类似的组合联合。
对于肠胃外给药而言,可使用本发明的化合物A的芝麻油溶液或花生油溶液或者本发明的化合物A的水性丙二醇溶液。如果需要的话,水性溶液应当适当地缓冲(优选pH>8),并且液体稀释剂首先提供等渗。这些水性溶液适于静脉内注射的目的。油性溶液适于关节内、肌肉内以及皮下注射的目的。所有这些溶液在无菌条件下的制备易于通过本领域技术人员已知的标准制药技术来完成。此外,根据标准药物实践,当治疗皮肤炎症时,也可局部给药本发明的化合物A并且优选通过霜剂、胶状物、凝胶剂、糊剂、软膏等等的方式局部给药本发明的化合物A。
此外,本发明提供一种用于治疗包括哺乳动物受治者在内的动物受治者中的胃肠疾病的药物组合物,所述治疗包括将治疗有效量的化合物A或其药学上可接受的盐给药于上述受治者。
进一步而言,本发明还提供一种用于治疗胃肠疾病的药物组合物,所述药物组合物包含治疗有效量的化合物A或其药学上可接受的盐以及药学上可接受的载体。
本发明还提供一种通过将治疗有效量的本发明的化合物A或其药学上可接受的盐给药于有此需要的患者或者包括哺乳动物受治者在内的动物受治者来治疗胃肠疾病或者预防或延缓胃肠疾病的发作或发展的方法,其中,所述胃肠疾病与GI运动性降低有关。
在另一方面,本发明提供一种化合物A或其药学上可接受的盐在制备用于治疗胃肠疾病或者预防或延缓胃肠疾病的发作或发展的药物中的用途。
本发明的一种实施方式为化合物A与用于胃肠疾病的药物的组合。根据本发明的“组合”可表示为“固定组合”或“部分组合的试剂盒”。“固定组合”被界定为其中(i)至少一种用于胃肠疾病的药物和(ii)化合物A存在于一个单元中的组合。“部分组合的试剂盒”被界定为其中(i)至少一种用于胃肠疾病的药物和(ii)化合物A存在于多个单元中的组合。“部分组合的试剂盒”的成分可同时给药、顺序给药或者单独给药。根据本发明,用于胃肠疾病的药物与化合物A 的摩尔比为1:100至100:1,例如,1:50至50:1或1:20至20: 1或1:10至10:1。两种药物可以相同的比例单独给药。酸分泌抑制剂的实例为其他5-HT4激动剂、质子泵抑制剂、H2受体拮抗剂和用于 IBS或便秘的药物。这些实例为H2阻断剂和质子泵抑制剂,所述H2 阻断剂例如甲氰咪胺,甲胺呋硫,所述质子泵抑制剂例如,吡啶基甲基亚磺酰基苯并咪唑,所述吡啶基甲基亚磺酰基苯并咪唑例如,奥美拉唑、艾美拉唑、南索拉唑、泮托拉唑、雷贝拉唑或诸如来明拉唑之类的相关物质。
具体实施方式
化合物列表:
化合物A。
实施例1:
GI运动性通过对来自植入为研究运动性而准备的犬体内的力传感器的信号进行处理来评价。简言之,用异氟烷麻醉犬并且在无菌条件下打开腹腔。将腔外力传感器(F-12IS,Star Medical,Tokyo)缝合在胃窦、胃体、十二指肠和近侧结肠的浆肌层上。手术之后,将保护罩置于犬上并且将犬放在独立的笼内。实验之前,犬禁食过夜并且将犬放在屏蔽室内。运动性通过遥测系统(GTS-800,Star Medical,Tokyo) 和由采集软件(Eight Star,Star Medical,Tokyo)采集至个人电脑中的数据来测量。在确定了消化间期移行复合运动(IMC)之后,口服给药测试药物。然后记录内脏运动超过5小时(hrs)。为了定量地测量胃运动性,计算表示收缩面积的运动指数。在个人电脑上获得来自力传感器的信号并且通过处理软件(Analyze II;StarMedical)分析该信号。在禁食状态下,给药之后每2小时测定收缩曲线和基线围绕的面积。为了进行标准化,给药之前,计算的面积除以IMC峰高度,并且用作运动指数(MI)。结果表示为平均值±平均值的标准误差(S.E.M.,N=4-5)。统计学分析使用GraphPad Prism(GraphPad Software,Inc.),通过Dunnett多重比较检验执行。
结果:
在犬体内,化合物A以剂量依赖的方式(0.1μg/kg至10μg/kg) 使胃窦运动活性增强(图1)。在口服给药化合物A之后0至2小时期间,在1μg/kg条件下,测量的MI的变化达到了统计学显著性,1μ g/kg被确定为该模型中的最小有效剂量。剂量为1mg/kg的西沙必利使胃窦运动性显著增强(图2),但是莫沙必利在3mg/kg条件下趋于使窦运动性增强(图3)。GI运动性实验的这些数据与公开的文献(Mikami T.等人,J.Phrmacol.Exp.Ther.,325,190-199,2008;Mine Y.等人, J.Phrmacol.Exp.Ther.,283,100-1008,1997)中的那些数据一致。化合物A在增强胃窦运动性方面的效力比西沙必利强约1000倍。
在近侧结肠中,1μg/kg的化合物A使收缩的幅度和频率提高(图 4)。而且,治疗后,化合物A促进巨大移行性收缩的发生。另一方面,口服给药普卢卡必利(0.1mg/kg)刺激胃窦运动,但是在该剂量条件下不影响近侧结肠的收缩。只有高剂量(0.3mg/kg)的普卢卡必利治疗使结肠的运动活性提高,但是这诱导胃-十二指肠过度收缩(图5)。
结论:
患有功能性肠病的大部分患者通常具有影响上GI道和下GI道的重叠的症状。例如,通常发现IBS与GERD有关。化合物A是最有效的选择性的5-HT4激动剂之一,化合物A在相同剂量条件下对窦和结肠运动性发挥刺激性影响,在内脏中没有组织特异性活性。这些特性表明对于患有功能性便秘和具有诸如消化不良或胃灼热之类的上GI症状的C-IBS的患者而言,化合物A可以是有价值的且可行的其他促动力药的替代物。
目前,普卢卡必利已被欧洲药品管理局(European Medicines Agency)批准用于治疗慢性便秘。在犬的这种研究中,普卢卡必利在增强近侧结肠运动性的剂量条件下诱导胃-十二指肠过度收缩,这说明了组织特异性活性。通常,幽门环和十二指肠中的过度收缩并不导致胃排空。
产业上的可利用性
根据本发明,化合物A或其药学上可接受的盐在治疗胃肠疾病方面有用。
本申请引用的所有公开出版物(包括但不限于:授权的专利、专利申请和期刊论文)中的每一个的全部内容通过引用并入本文。虽然本发明已通过公开的实施方式进行了描述,但是本领域技术人员易于理解的是具体实验细节仅仅是对本发明的举例说明。应当理解,在不背离本发明的实质的前提下可进行各种改变。因此,本发明仅由权利要求来限定。
- 还没有人留言评论。精彩留言会获得点赞!