确定诱导尖端扭转型室性心动过速的可能性的方法与流程
本发明涉及心脏病学领域,更特别地涉及一种新的算法,该算法特别可用于确定药物是否能够诱导心室复极紊乱的方法,所述心室复极紊乱与尖端扭转型室性心动过速型的心室节律紊乱相关或不相关。
背景技术:
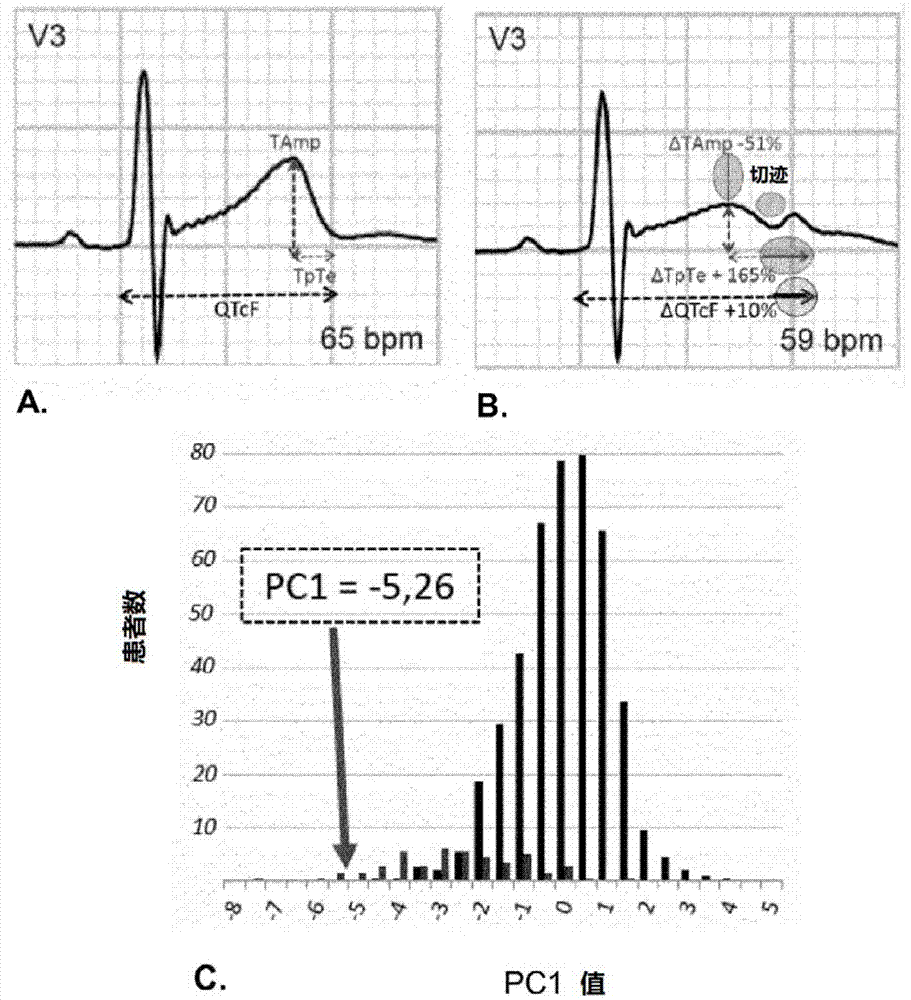
:尖端扭转型室性心动过速指特定类型的室性心动过速,即心室节律紊乱,导致心率加速,例如心动过速(但不同于心室颤动)。有两种类型的尖端扭转型室性心动过速:具有长qt间期的尖端扭转型室性心动过速和具有正常发作间期的qt和扭曲外观的多形性室性心动过速。药物诱导的尖端扭转型室性心动过速是个人规模和社会规模的公共卫生问题。在绝大多数情况下,这种不利影响的作用机制是抑制涉及心室复极的钾通道,称为ikr,其诱导复极期的延长,并且在心电图上特别导致qt间期的延长,所述qt间期是经心率校正过的(qtc)。如sekarski等人(《儿科学报(paediatrica)》,卷19,no.4,2008)所述,qt间期的延长可导致室性心律失常,其可恶化并导致猝死。因此,qt的延长目前构成了限制使用和从市场上撤出药物的最常见原因之一。在这样从市场上撤出的药物中,该出版物特别引用了西沙必利、特非那定、氟哌利多或舍吲哚。这些现象特别在iii类抗心律失常药物中观察到,该药物优先阻断钾通道,从而延长复极。目前市场上的iii类抗心律失常药物都具有包括甲磺酰苯胺基团(或其生物电子等排体)的基本结构。因此可以提及胺碘酮阿齐利特、溴苄胺、氯非铵、多非利特、依布利特司美利特、索他洛尔和决奈达隆上述出版物在表1和表2中列出了一定数量的已知延长qt的药物。该出版物还回顾:“亚利桑那大学治疗学教育和研究中心”建立并维护了这些药物的数据库,可在其网站www.torsades.org或https://crediblemeds.org/上找到。在申请新药上市许可文件的过程中,所有分子必须评估其致尖端扭转性室速潜能(诱导尖端扭转型室性心动过速的潜能)。该评估涉及对人类中由新药物诱导的心室复极,特别是qt间期延长或校正的qtc延长,的修饰的彻底研究。qtc间期的这种延长是目前推荐用于估计药物的ikr抑制程度的标志物,所述药物施用于具有基础状态下正常心室复极的受试者。因此,当qtc的增加大于20ms时,认为测试分子具有显著风险,证明在投放市场期间密切监测该节律风险是合理的。当qt/qtc延长为5至20ms时,这种情况处于“灰色区域”,必须进行额外的研究才能得出更可靠的结论。通常认为当观察到qt/qtc延长小于5ms时,分子在心脏复极方面是安全的。然而,该qtc间期的延长是非常不完美的参数,其对于心室ikr通道抑制不具有非常的特异性。因此,如果抑制ikr通道增加qt间期,后者可以在没有ikr抑制的情况下增加,药物诱导的尖端扭转型室性心动过速的风险则不那么大。随后,尽管有低估的致尖端扭转性室速风险,但其它分子仍然继续发展时,一些有用的分子会中断发展,因为这种风险被高估了。在个体规模上,药物诱导的尖端扭转型室性心动过速可能影响没有大的合并症的受试者并且可能导致死亡。对这种个体风险的决定因素仍然知之甚少,特别是在低钾血症和先天性长qt的情况下发现风险增加,但是没有可靠的诊断测试来评估这种个人风险,尤其是在基础状态下的正常qtc间期的情况下。因此,在上市前评估中,或针对特定患者,监管机构(例如食品和药品管理局)和临床医生都在寻求新的更相关的方法来预测药物的致尖端扭转性室速风险,这超出了药理学应激后qtc间期持续时间增加的简单分析的范围。索他洛尔是一种推荐的抗心律失常药物,并用于控制心房颤动患者的节律。索他洛尔具有很强的阻断ikr钾通道的能力,与诱导尖端扭转型室性心动过速的剂量依赖性风险相关,高达受治疗患者的7%。索他洛尔具有线性药代动力学,几乎完全吸收而没有很大的变异性,并且在口服摄入后3至5小时观察到最大浓度。couderc等人(《心脏节律(heartrhythm)》,2011年7月;8(7):1036-43)描述了在不同时间对描记和qtc、tamp或tpte值的分析,但是没有处理治疗后参数的动态变化;因此,该文献没有计算本申请中设想的δqtc、δtamp和δtpte值,也没有基于这些值计算主成分。us2008/188761描述了一种通过比较tamp和心率之间的相关性来检测钾通道延迟的方法,但是没有更大程度地描述本申请中设想的δqtc、δtamp和δtpte值,或者基于这些值计算主成分。recanatini等人(《医学研究报告(medresrev.)》2005年3月;25(2):133-66)在综述文章中描述了qt延长和尖端扭转型室性心动过速的关系,但未提及或暗示本申请中设想的策略。clark等人(《化学信息与建模杂志(jcheminfmodel.)》2009年11月;49(11):2617-26)描述了用于确定各种分子的长qt和尖端扭转型室性心动过速之间关系的方法,但未提及或暗示本申请中设想的策略。bottino等人(《生物物理学与分子生物学进展(progbiophysmolbiol.)》2006年1月至4月;90(1-3):414-43)描述了一种方法,可用于分析某些药物是否能够诱导尖端扭转型室性心动过速,但未提及或暗示本申请中设想的策略。suzuki等人(《生物物理学与分子生物学进展(progbiophysmolbiol.)》2008年9月;98(1):52-60)描述了用于确定分子是否能够诱导心律失常的计算机方法,但未提及或暗示本申请中设想的策略。因此,需要建立一种测试,该测试使得可以在施用于患者后预测药物可以诱导尖端扭转型室性心动过速的风险。或者,在施用具体药物后确定特定患者是否具有出现尖端扭转型室性心动过速的具体风险也是有利的。技术实现要素:本发明提供了一种方法,用于在简单的心电图测量之后容易地确定在施用药物后患者是否可能出现尖端扭转型室性心动过速事件。因此,本发明人证明了这样的事实:通过研究qtc以及研究两个附加值(t波的最大幅度(tamp)、和t波的峰值和末端之间的持续时间(tpte)),可以获得关于以下能力的可靠定量结果:物质抑制ikr钾通道的能力(物质的一般作用)、或在施用能够抑制ikr钾通道的物质之后患者出现这种对ikr钾通道抑制的能力(患者的个体反应效果)。通过组合在上述三个值之间观察到的变化,本发明人已经定义了一种算法,该算法使得可以提供关于由物质诱导的心脏复极紊乱的发生风险的精确信息。本发明人提出的算法是特别有利的,因为当在患者群组上进行测试时,它既可以获得关于特定物质或组合物的信息,也可以确定特定患者的个体风险,这使得它可以对有风险的患者进行适当的监测,同时降低监测先验上推理(priori)无风险患者的成本。在本发明的上下文中使用的测量因此使用以下测量:tamp:t波第一个峰值的最大幅度计算在施用期望测试的物质之前和之后t波的第一峰值的最大幅度之间的差异(表示为百分比)。事实上,在“切迹”的情况下,可以观察到t波的两个峰值。即使小于第二峰值,也应测量第一峰值的幅度。由此计算的数据为δtamp(%)=((施用前的tamp-施用后的tamp)/(施用前的tamp))×100在这种情况下,计算施用前和施用后t波的幅度之间的差异,使得δtamp为正。这是由于对ikr通道的抑制引起t波幅度减小。执行上述计算使得可以将该减少反映为百分比。以绝对值(mv)表达结果也使得可以计算操作算法。然而,可以计算施用后t波的幅度与施用前测量的幅度之间的差异,并且δtamp将是负的。在该公式中考虑的tamp值优选地是几个tamp测量值的平均值。测量可以在执行者将选择的导联上进行,但优选地在d2、v2、v3导联上进行。这些测量也可以在v4或v5导联上进行,特别是如果施用物质之前的tamp小于0.1mv。在一个特定实施方案中,并且为了减少由于ecg测量期间患者可能存在的变化引起的潜在误差,优选地测量平均波群上的tamp值(通常由从10秒内制成的记录中获得的标准中值波群(模板)生成),或者甚至在间隔几分钟生成的三个平均波群的平均值上测量tamp值。tpte:t波的最大第一峰值与t波末端之间的间期(tpte)计算施用期望测试的物质之前和之后t波的最大第一峰值与t波末端之间的差异(表示为百分比)。因此,计算的数据是δtpte(%)=((施用后的tpte-施用前的tpte)/(施用前的tpte))×100在该公式中考虑的tpte值优选地是几个tpte测量值的平均值。测量可以在执行者将选择的导联上进行,但优选在v2、v3、v4导联上进行。测量也可以在v5或v6导联上进行。在一个特定实施方案中,并且为了减少由于ecg测量期间患者可能存在的变化引起的潜在误差,优选地测量平均波群上的tpte值(通常由从10秒内制成的记录中获得的标准中值波群(模板)生成),或者甚至在间隔几分钟生成的三个平均波群的平均值上测量tpte值。tpte变化的绝对值(以毫秒为单位)也可以在算法的上下文中使用。qtcf:相对于心率校正的qt间期(qtc)使用合适的方法计算相对于心率校正的qt间期之间的差异(以百分比表示),该方法使心率对qtc值的影响最小化,也就是说在施用期望测试的物质之前和之后,在qtc作为心率函数的关系中建立等于零的斜率(通常,在成人中,通过fridericia的方法进行适当的校正,qtcf)。回顾:rr是qrs波群的开始与下一个qrs波群的开始之间的间期,以秒为单位表示。因此,使用qtcf计算的数据为δqtcf(%)=((施用后的qtcf-施用前的qtcf)/(施用前的qtcf))×100在该公式中考虑的qtcf值优选是几个qtcf测量值的平均值,特别是至少三个连续波群的平均值。与上面看到的其它值一样,可以使用在从几秒的记录获得的中值波群上获得的qtcf值,或平均波群的平均值上获得的qtcf值。可以在执行者将选择的导联上进行测量,但优选在d2导联上进行。然而,qtc也可以通过本领域已知的任何方法计算,特别是bazett的方法(qtcb):此处同样可以使用δqtc的绝对值,而不是百分比变化。通常,优选地计算δtamp、δqtc和δtpte,使得它们都具有相同的符号。要在本发明的上下文中实现的算法下面提出的算法使得可以获得称为pc1的定量值,其与确定ikr抑制的ecg符号的出现非常相关,并且推测与具有长qt的尖端扭转型室性心动过速事件的风险增加相关。pc1=a1xδtamp(%)+a2xδqtcf(%)+a3xδtpte(%)+b其中--0.05≤a1≤-0.030--0.2≤a2≤-0.1--0.04≤a3≤-0.02-1.5≤b≤2。优选地,--0.040≤a1≤-0.035--0.16≤a2≤-0.145--0.35≤a3≤-0.025-1.7≤b≤1.9。在一个优选实施方案中,-a1=-0.038±0.002-a2=-0.15±0.001-a3=-0.031±0.002-b=1.79±0.05。在一个优选实施方案中,-a1=-0.03814-a2=-0.15074-a3=-0.03059-b=1.79249。在一个特别的实施方案中,pc1=-0.038×δtamp(%)-0.151×δqtcf(%)-0.0306×δtpte(%)+1.792pc1值越负,所施用的物质抑制ikr通道的能力越强,并且推测患者出现尖端扭转型室性心动过速事件的风险越大。当如上所述计算的δtamp为正时,这些算法和值是有效的。如果计算的δtamp为负,则算法的值将改变,并且可以使用下面描述的方法定义新算法。同样,如果使用tamp、tpte和qtc之间的差的绝对值,则将获得具有其它值的算法。评价药物的致尖端扭转性室速潜能如上所述,重要的是能够在获得上市许可之前的临床试验期间评价化合物的致尖端扭转性室速潜能,以便能够草拟使用该药物的可能预防措施。物质的致尖端扭转性室速潜能是该物质在施用于患者后诱导尖端扭转型室性心动过速的潜能。fda(食品和药品管理局)和ema(欧洲药品管理局)已经发布了国际协调会议(ich)给出的关于如何开展这些试验的指南,标题为“e14clinicalevaluationofqt/qtcintervalprolongationandproarrhythmicpotentialfornon-antiarrhythmicdrugs”。这些指南可在该机构的网站上获取,并附有问题和答案。指南的地址是:http://www.fda.gov/downloads/drugs/guidancecomplianceregulatoryinformation/guidances/ucm073153.pdf非抗心律失常药物或延长心脏复极的物质的能力可以通过体表心电图(ecg)上qt间期的延长来测量。回想一下,该qt间期代表除极和随后的心室复极的持续时间,并且是从qrs波群的开始到t波末端测量的。心脏复极延迟为促进心律失常发展创造了环境,大多数明显是尖端扭转型室性心动过速(tdp),但也可能是其它室性快速性心律失常。如上所述,qt间期是致心律失常作用的风险的不完美的生物标志物,但是在一般人群中,qt间期与尖端扭转型室性心动过速的风险之间存在定性关系,尤其是对于引起qt间期大幅延长的药物而言。通常,校正所测量的qt间期的值(获得qtc)以便考虑心率,该qt间期与所述心率具有反比关系。然而,尚不清楚心律失常的发展是否与qt间期(绝对)或qtc的增加更密切相关。大多数具有诱导尖端扭转型室性心动过速风险的药物会增加绝对qt间期和qtc。通常,当测试分子使qtc增加小于5ms的时段时,认为所述分子在这方面是安全的。当它使qtc增加20ms的时段时,分子的作用必须成为上市后监测的主题。当分子使qtc增加5ms至20ms的时段时,这是一个“灰色区域”,也就是说,不可能先验地推断尖端扭转型室性心动过速的实际风险,并且需要进行额外的分析和研究。因此,需要严格地表征新药对延迟心脏复极的风险的作用。上面定义的算法使其成为可能,特别是如果用80mg的索他洛尔作为阳性对照进行研究,以qt/qtc增加在5ms至20ms的灰色区域中提供有价值的附加信息。在这个阶段,该研究是在患者群组上进行的。因此,对足够数量的患者进行这些研究,使得有可能获得呈现出期望测试的分子(感兴趣的药物)的统计现实的结果,从而消除患者间的变化。安慰剂和感兴趣的物质将优先进行比较,以确定该物质是否延长qt间期(可以在不使用安慰剂的情况下测量间期,但优选使用安慰剂以考虑到一天中qt的实际变化)。有利地,还将使用用于延长qt间期的阳性对照。因此,在fda指南中,前者建议使用阳性对照,其使qt/qtc增加约5ms,以证明清楚地检测到这种小幅度作用。可以使用两个阳性对照,一个通过诱导对ikr钾通道的明显抑制来增加qt间期(例如索他洛尔),另一个对照增加qt间期而没有显著抑制ikr通道,例如口服莫西沙星。已知延长qt的任何药物可用作对照,特别是如sekarski等人的表1或2中所引用的药物。然而,由于sekarski等人的表1和2的这些药物所带来的潜在风险,优选使用80mg的索他洛尔作为阳性对照。在这种浓度下,这种分子具有许多优点:-最大浓度是公知的(口服施用后约3小时),这使得可以容易地计划何时进行上述测量。-已知该分子抑制ikr通道。-在这种浓度下,该分子使qt/qtc增加约20ms。-在这种浓度下,该分子不会诱导尖端扭转型室性心动过速事件,并且因此对患者来说是安全的。然而,已知该分子在其临床使用剂量(使用高达320mg)下可诱导尖端扭转型室性心动过速。根据方案(可为下述方案),在群组患者上,对每个患者进行研究:-在施用期望研究致尖端扭转性室速潜能的物质之前,在患者上测量tamp、tpte和qtc。-在施用物质(因此可以是安慰剂、感兴趣的物质或阳性对照)之后,在患者上测量相同的参数tamp、tpte和qtc。可以对这些参数进行单次测量(如果对于该物质,患者血流中物质的药代动力学和浓度峰值是已知的),但是优选地,在几个时间间隔(例如,每1/4小时或每小时,取决于分子的半衰期)进行多次测量。定期揭示tamp、tpte和qtc,使得有可能增强检测物质的潜在致尖端扭转性室速作用的可能性,或甚至确定何时该作用最大。-根据上述公式计算δtamp、δtpte和δqtc值。-使用上述算法来计算每种测试物质的结果。通常,本领域技术人员将能够根据感兴趣的物质,特别考虑如上所述的fda指南,定义适当的方案(测量tamp、tpte和qtc的时间)。特别地,如果索他洛尔用作阳性对照(抑制ikr通道),则在施用后3小时测量上述值,这对应于该物质的最常见浓度峰值。如果使用另一种物质作为对照,则选择最合适时间(对应于对除极影响最大的时间)来测量上述值。由于这些对照是已知的,因此本领域技术人员知道如何确定这些时间。同样地,所用对照的最佳浓度将由本领域技术人员根据他们对将使用的对照分子的知识来确定。因此,出于上述节律风险的原因,他们可以使用80mg剂量的索他洛尔。可以任选地设想使用更大量的索他洛尔,但是由于其对患者的风险并且因为其与具有其适应症的患者中开始治疗的推荐不一致,因此不是优选的。在本领域技术人员对方案的定义中,在患者是女性时,优选在月经周期的同时进行各种测量。这是因为已知激素水平会影响女性复极紊乱(长qt)的风险。通常,如上所述,对于患者群组的每个患者执行上述步骤,并且因此对于每个患者(并且对于测量tamp、tpte和qtc参数的每个时间)和每种物质获得通过上述算法计算的值。对于测量tamp、tpte和qtc参数的每个时间,优选对每个患者和每种施用物质(感兴趣的物质和任选的安慰剂和阳性对照)获得的值取平均值。这使得可以省去“患者效应”,即两个患者能够对药物或给定物质作出不同反应的事实。然后,pc1值的平均值是更多地考虑感兴趣物质的实际假定的致尖端扭转性室速作用的值。优选地,患者群组(测试感兴趣的物质的患者数量)为至少10个患者,优选至少20个或甚至50或100个患者。本领域技术人员将能够确定患者群组中的最小受试者数量,以获得统计学上显著的结果。同样,在进行这些研究之前,本领域技术人员优选对感兴趣的物质进行药代动力学研究和剂量反应研究,以确定测量上述三种生理值的最佳时间。为了确定感兴趣物质的致尖端扭转性室速潜能,根据是否使用对照,分析将不同。如果索他洛尔用作抑制ikr通道的阳性对照根据测试分子的药代动力学特征,在由执行者确定的时间,针对每位患者,计算安慰剂,施用后3小时的索他洛尔和感兴趣的物质(测试分子)的pc1值。然后计算每种分子(测试、索他洛尔、安慰剂)的这些pc1值的平均值以及中值。如果测试分子组的pc1的平均值或中值显著低于索他洛尔组的平均值或中值,则该测试分子所诱导的ikr通道抑制,超出了判断为合理的风险,并且必须在投放市场后,经受额外测试和增加监测。如果测试分子组的pc1平均值与安慰剂的平均值没有显著差异,则可以认为该分子没有风险。如果测试分子组的pc1的平均值显著小于计算的安慰剂平均值,但与索他洛尔的pc1的平均值没有显著差异,则这是“灰色区域”。存在致尖端扭转性室速风险,因为它与索他洛尔一起存在,至少可能在较高剂量下存在致尖端扭转性室速风险。如果与安慰剂相比,观察到测试分子的qt/qtc增加超过5ms,则必须建立使用监测。如果使用除索他洛尔之外的阳性对照,则该分析是等效的,但是该阳性对照必须引起qt增加和ikr通道抑制,并且认为其致尖端扭转性室速风险差不多等于与80mg索他洛尔相关的致尖端扭转性室速风险。如果没有使用阳性对照上面定义的算法也可以在没有阳性对照的情况下使用,即使不建议不使用阳性对照。在这种情况下,根据fda指南,进行试验的群体优选包含约50%的女性和50%的男性,尽管有可能为60%的女性和40%的男性(或40%的女性和60%的男性)。患者一般为18至60岁。由于女性与男性相比发生复极紊乱的风险更大,因此使用具有上述分布的患者群组可以增加算法结果的相关性和可以从所得结果中得到的置信度,以及可以用所述结果进行的分析。根据测试分子的药代动力学特征,在由执行者确定的时间,针对每个患者,计算安慰剂和感兴趣的物质(测试分子)的pc1值。如果测试分子组的pc1平均值与安慰剂所得平均值没有显著差异,则可以认为该分子没有风险。如果测试分子组的pc1平均值显著大于安慰剂所得平均值,则可以认为该分子没有风险。如果测试分子组的pc1平均值为负,并且显著低于安慰剂组所得平均值,则该测试分子存在风险,并且必须在投放市场后,经受额外测试和增加监测。如果测试分子组的pc1的平均值为负,并且没有显著低于安慰剂计算的平均值,则这是“灰色区域”。如果与安慰剂相比,观察到测试分子的qt/qtc增加超过5ms,则必须建立使用监测。在通过上述方法确定的致尖端扭转性室速潜能或如果分子处于灰色区域的情况下,将进行更彻底的研究以确认这种潜能并最大程度地对其进行定性和定量。在没有阳性对照的情况下,优选对足以进行适当统计分析的一定数目患者进行研究。评价患者经历尖端扭转型室性心动过速事件的个体风险上述算法还可以在施用具有致尖端扭转性室速潜能的物质之后评价患者经历尖端扭转型室性心动过速事件的个体风险。为此,可以遵循下列方案:-在施用索他洛尔之前,在患者上测量tamp、tpte和qtcf。-在施用索他洛尔后3小时,在患者上测量相同的tamp、tpte和qtcf参数。如上所述,已知索他洛尔在口服后约3小时具有最大浓度,优选使用80mg单剂量。-根据上述公式计算δtamp、δtpte和δqtc值。-将上述算法应用于这些值,以获得最终的pc1结果。结果分析以下列方式进行:-如果pc1≤-3.2:经历尖端扭转型室性心动过速事件的风险非常高(这个值对应于风险高于男性的女性的5%,也就是说只有5%的女性的pc1低于这个值)。-如果-3.2<pc1≤-2.4:患者有高风险,但略低(女性的5%至10%)。-如果-2.4<pc1≤-1.25:患者有平均风险(对应于女性的10%-25%)。-如果-1.25<pc1≤-0.48:患者有低风险,对应于女性的25%-45%和男性的5%。-如果-0.48<pc1≤-0.22:患者的风险非常低,这个范围对应于女性的45%-53%和男性的5%至10%。-如果pc1>-0.22,可认为患者无风险。优选地,使用少量索他洛尔,即相当于临床治疗开始时通常施用的量。因此,优选施用患于者的索他洛尔剂量为80mg(单次口服摄入),这使得可以观察复极紊乱而不危及患者。这是因为已知索他洛尔可以抑制ikr钾通道。上述算法在接受单剂量80mg索他洛尔的患者群组中得到验证,测量在施用后3小时进行。获得的值是可靠的定量值,其与ikr钾通道的抑制相关。因此,该算法的结果使得可以指示患者是否可能对具有抑制ikr通道能力的药物起反应。因此,该测试比简单的qt/qtc测量更具信息性。根据获得的结果和由此确定的患者风险,本领域技术人员将能够调整患者的所需监测。因此,本发明涉及一种用于产生抑制ikr钾通道的定量变量的新型工具。因此,本发明涉及一种用于确定向患者施用组合物后诱导致尖端扭转性室速作用的风险的离体或体外方法,包括以下步骤:i.在算法中组合,通过以下方法获得的结果:a.汇集一个包含n个患者的群组,n大于或等于50、75或甚至100;b.向其施用抑制ikr通道的药物;c.在施用该药物之前和之后测量qtc、tamp和tpte,其中i.qtc=相对于心率校正的qt间期;ii.tamp=t波第一峰值的最大幅度;iii.tpte=t波的最大第一峰值与t波末端之间的间期;d.对于每个患者,与施用之前测量的那些相比,计算和施用药物后所得qtc、tamp和tpte值的变化相对应的δqtc、δtamp和δtpte,以百分比计;e.对δqtc、δtamp和δtpte值进行主成分分析,以产生三个新的定量变量pc1、pc2和pc3;f.所述算法是使得可以从δqtc、δtamp和δtpte获得pc1变量的公式;ii.获得这种组合的最终结果;iii.将该最终结果的值与参考值进行比较。在另一个实施方案中,i.d中使用的δqtc、δtamp和δtpte是差异的绝对值,而不是变化百分比。在该实施方案中,该方法是体外或离体的,也就是说它不应用于人体。它使用通过患者的心电图记录的数据,但不包括这些收集数据的步骤。因此,该方法不应用于人体。该申请还描述了一种用于确定向患者施用组合物后诱导致尖端扭转性室速作用的风险的方法,包括以下步骤:i.施用该组合物之前和之后,在患者中测量qtc(相对于心率校正的qt间期)、tamp(t波的第一峰值的最大幅度)和tpte(t波的最大第一峰值与t波末端之间的间期)值;ii.计算分别对应于在施用之前和之后获得的这些测量值的差异的δqtc、δtamp和δtpte值,以百分比计;iii.在算法中组合,通过以下方法获得的结果:a.汇集一个包含n个患者的群组,n大于或等于50、75或甚至100;b.向其施用抑制ikr通道的药物;c.在施用该药物之前和之后测量qtc、tamp和tpte;d.对于每个患者,与施用之前测量的那些相比,计算和施用药物后所得qtc、tamp和tpte值的变化相对应的δqtc、δtamp和δtpte,以百分比计;e.对δqtc、δtamp和δtpte值进行主成分分析,以产生三个新的定量变量pc1、pc2和pc3;f.所述算法是使得可以从δqtc、δtamp和δtpte获得pc1变量的公式;iv.获得算法中这种组合的最终结果;v.将该最终结果的值与参考值进行比较。该方法也可以是本发明的实施方案。在另一个实施方案中,ii和iii.d中使用的δqtc、δtamp和δtpte是差异的绝对值,而不是变化百分比。如此描述的方法还使得可以确定所用组合物是否抑制患者的ikr钾通道,在应用算法后获得的最终结果与ikr通道的抑制定量相关。上述方法中使用的算法如上所述。实施例1描述了如何获得特定算法。通常,为了获得可以在本申请中描述的方法的背景下使用的算法,遵循以下过程:a.汇集一个包含n个患者的群组。优选地,监测的患者数量n大于或等于50、75或甚至100,以获得具有实际统计值的结果;优选地,该群组包含相同数量的女性和男性,或者不超过60%的女性和40%的男性,反之亦然。这使得可以获得可用的算法,而不用考虑患者的性别如何。然而,这种用于获得算法的方法也可以使用仅为女性或仅为男性患者的群体来执行。然后获得的算法将是不同的,因为与男性相比,在女性中观察到的ikr通道的抑制更大。在根据本发明的方法的背景下,然后将根据期望进行研究的患者的性别使用一种或其它算法;b.向每个患者施用延长qt的药物,优选通过抑制ikr通道延长qt的药物。在该步骤施用的药物是如上所述的药物,特别是sekarski等人的表1或2的产品。本领域技术人员根据其药代动力学特征选择该药物,并且调整剂量以特别不危及该组群的患者,并同时允许在足够数目的患者中(足以进行统计分析)观察与该药物有关的qt延长。因此,出于上述原因,优选使用索他洛尔,特别是口服80mg索他洛尔。c.在施用该药物之前和之后测量qtc、tamp、tpte。在步骤b)中的施用药物之前,测量这些值(本次施用前的测量因此可能描述为步骤b0),并且在施用后测量这些值。因为步骤b中使用的药物是本领域技术人员已知的,所以在由本领域技术人员根据步骤b)的药物药代动力学特性确定的最佳时间进行施用后的测量,使得该药物诱导的qt延长最大。这通常对应于药物的血浆浓度最大的时间。如果在步骤b)中选择索他洛尔作为药物,则在施用后3小时进行测量;d.对于每个患者,与施用前测量的那些相比,计算和施用药物后所得qtc、tamp和tpte值之间的变化相对应的δqtc、δtamp和δtpte,以百分比计。因此,优选根据上述公式计算δqtc、δtamp和δtpte值。然而,δtamp可以根据公式δtamp=((施用后的tamp–施用前的tamp)/(施用前的tamp)×100计算。在另一个实施方案中,计算的δqtc、δtamp和δtpte是差异的绝对值,而不是变化百分比;e.对δqtc、δtamp和δtpte值进行主成分分析,以产生三个新的定量变量pc1、pc2和pc3。主成分分析(acp或pca分析)是一种将相关变量转换为彼此去相关的新变量的方法。在一个特定实施方案中,执行acp以便将三个变量δqtc、δtamp和δtpte转换为三个新的去相关变量pc1、pc2和pc3。acp分析是本领域已知的方法,其可以特别地使用本领域已知的任何软件来实施。可以在上述方法中使用的算法是使得可以从δqtc、δtamp和δtpte变量获得pc1变量的公式。在所获得的三个变量pc1、pc2和pc3中,所考虑的pc1变量是与δqtc、δtamp和δtpte中的每一个最佳相关的变量。这意味着用δqtc、δtamp和δtpte中的每一个计算的pc1的相关系数(绝对值)大于针对讨论中的δqtc、δtamp或δtpte对其它主成分pc2和pc3计算的相关系数。实例的表1清楚地表明,针对δqtc、δtamp和δtpte中的每一个进行计算,pc1的相关系数的绝对值大于pc2和pc3的相关系数的绝对值。如果根据上述公式计算δtamp使得δtamp为正,则pc1以相同的方式(具有相同符号的相关系数)与δqtc、δtamp和δtpte相关。如果δtamp为负,则pc1在相同意义上与δqtc和δtpte相关,在另一种意义上与δtamp相关。实例的表1显示了与δqtc、δtamp和δtpte负相关的pc1,而pc2与δqtc负相关并且与δtamp和δtpte正相关。pc3与δtamp负相关并且与δtpte和δqtc正相关。还应注意,pc1的每个“δ”值的相关系数高于其它两个新变量中的任何一个。本发明还涉及一种用于产生算法的方法,该算法使得可以产生与确定ikr抑制的ecg特征的外观相关联的定量值,即具有长qt的尖端扭转型室性心动过速事件的风险,所述方法包括上述步骤。本发明还涉及一种用于产生算法的(体外或离体)方法,该算法使得可以产生与确定ikr抑制的ecg特征的外观相关联的定量值,即具有长qt的尖端扭转型室性心动过速事件的风险,所述方法包括以下步骤:i)对于群组的每个患者,获得δqtc、δtamp和δtpte值,其对应于在施用药物之前和之后所得qtc、tamp和tpte值之间的差异,以百分比计,所述药物优选通过抑制ikr通道延长qt;ii)对这些δqtc、δtamp和δtpte值进行主成分分析,以产生三个新的定量变量pc1、pc2和pc3。由此产生的算法是使得可以从δqtc、δtamp和δtpte变量获得pc1变量的公式。pc1值如上所述。如上所述,所述方法可用于确定在施用已知具有致尖端扭转性室速作用的物质的情况下患者经历心室复极紊乱的个体风险,并且所述向患者施用的组合物是索他洛尔。因此,根据上述条件,设想一种用于确定在施用已知具有致尖端扭转性室速作用的物质的情况下患者经历心室复极紊乱的个体风险的方法,其特征在于将上述方法应用于所述患者,所述向患者施用的组合物是索他洛尔。根据上述要素进行个体风险分析。所描述的方法还可用于确定感兴趣的物质(测试分子或测试药物)是否具有致尖端扭转性室速性质。在该实施方案中,在包含大于或等于2的患者数的患者群组上重复根据本发明的方法。然后根据上面提供的信息分析针对每个患者获得的各种结果。如上所述,优选地,对于每个患者,使用感兴趣的物质和至少一种其它组合物重复该方法,所述其它组合物选自安慰剂和阳性对照,特别是对于选自索他洛尔和莫西沙星的阳性对照,优选至少一种阳性对照为索他洛尔。在这种情况下,优选在单次摄入中以80mg的剂量使用它。本发明还涉及一种用于实现上述方法的装置,或者包括用于实现上述方法的算法的微处理器。实际上,上述方法可以通过计算机实现。附图说明通过阅读下面的详细描述,并参考附图,本发明的其它特征和优点将显现出来,附图说明了:图1显示在一名患者中,服用索他洛尔之前(1.a)和服用索他洛尔之后3小时(1.b)的代表性心电图描记,以及该患者的pc1值,其代表相对于pc1值在群体中的分布(1.c)。观察到t波的双峰(切迹),以及pc1值距离0最远。图2显示在另一名患者中,服用索他洛尔之前(1.a)和服用索他洛尔之后3小时(1.b)的代表性心电图描记,以及该患者的pc1值,其代表相对于pc1值在群体中的分布(1.c)。该患者表现出弱的索他洛尔诱导的ikr抑制。因此计算的pc1值接近0。具体实施方式实施例实施例1–产生算法群体/患者群组患者群组是generepol研究的成员,由995名身体健康的来自欧洲或北非的18至60岁的志愿者组成。本研究的目的是确定与施用80mg索他洛尔后抑制ikr通道相关的遗传易感性,体重指数为19至29kg/m2,已收到知情同意书。使用了一些其它排除标准:妊娠、哮喘、心率低于50bpm,异常ecg(心电图)或qrs>100ms,收缩压<100mmhg,房室传导阻滞史或雷诺现象,已知慢性疾病如需要长期治疗的心脏或肾衰竭,qt延长药物或除避孕药、镇痛药和维生素之外的任何长期治疗,先天性长qt综合征、心律失常、猝死或qtc(fridericia方法,qtcf)>450ms的家族或个人史。测量ecg的方案在整夜未摄入食物后,志愿者在上午8点住院约6小时。插入静脉内导管以采集血液样品。然后使用连接到膝上型计算机的cardioplug装置(cardionics布鲁塞尔,比利时)记录患者的ecg。在患者仰卧休息10分钟后获得基础ecg记录(每个一式三份进行,持续10秒)。然后给患者单次口服剂量的80mg索他洛尔并继续进行ecg监测。服用索他洛尔后3小时(h10),在受试者持续仰卧10分钟后和午餐前再次记录ecg(一式三份)。在h3,采集血液样品以确定血浆索他洛尔浓度。在确认qtcf低于基础qtcf+40ms后,在服用索他洛尔后5至6小时参与者可以离开。分析ecg索他洛尔引起的qt增加,相当于代表了先天性医源性形式的长qt综合征(lqt2),在ecg上证明了基础描记和服用索他洛尔后3小时的描记之间出现的常规差异。量化了qtcf、tpte和tamp以及t波中存在的切迹(双峰)。根据ich指南e14,使用fridericia校正法(qtcf)相对于心率对qt进行校正。使用cardiabase软件(groupebanook,南锡,法国)进行ecg数据分析。qtcf、tpte和tamp的定量分析由两名训练有素的研究者进行,以限制评价者间的变异性。在v3、v4和v5导联上的代表性搏动(平均表示为10秒的ecg)上通过切线法一式三份地测量tpte。在t波双峰(切迹)的情况下,如果t波的幅度对于该峰值较小,则考虑的峰值是第一峰值。获得的平均值得以保留。如果无法在v3、v4或v5上测量tpte,则代替地在v2(代替v3)或v6(代替v4/v5)上进行测量。为了测量tamp,在dii、v2和v3导联上的代表性搏动(平均表示为10秒的ecg)上,在t波第一峰值最大幅度的位置上进行定位。计算并保留由这三个导联产生的tamp值的平均值,并且在10秒的三个不同ecg上测量(一式三份)。如果无法在这些导联之一上测量tamp(特别是因为低值(<0.1mv)),则使用v4导联。在dii导联上对连续三个搏动通过切线方法测量qtcf,并保留一式三份评价的平均值。有可能证明评价者之间的测量值保持一致且可重复。对于这些参数,测量在h3获得的值与基础值之间的差异。该差异表示为相对于基础值的百分比,并且进行计算使得计算的值为正。因此进行了以下计算:δqtcf(%)=(h3的qtcf–基础qtcf)/(基础qtcf)×100δtpte(%)=(h3的tpte–基础tpte)/(基础tpte)×100δtamp(%)=(基础tamp–h3的tamp)/(基础tamp)×100为了评价双峰(切迹),所有ecg由两名研究者独立评价。如果两名研究者达成协议,患者被描述为切迹者或非切迹者。如果评价中存在分歧,则受试者不包括在这些组中(评价群组中仅10名受试者,复制群组中的8名受试者因此不能被分类)。主成分分析对计算值δqtcf、δtpte和δtamp进行主成分分析,这使得可以产生三个非相关的替代标志物,从而更好地考虑三个初始相关值所携带的信息。使用r软件(https://www.r-project.org/)进行统计分析。结果索他洛尔诱导的心电图变化施用索他洛尔后3小时在心电图中观察到的变化表明抑制了ikr通道,其中,无论评价的定性或定量参数如何,在探索和复制群组中结果和观察所得是相似的。与先前的研究一致,索他洛尔还诱导qtcf持续时间的绝对和相对变化(分别为21.4±14ms和5.5±3.5%)。还观察到t波形状的典型变化,在探索和复制群组之间分别为tpte增加(14.2±15.6对15.9±20.5%,p=ns(不显著))和tamp减少(13.6±15.7对12.8±15.3%,p=ns)。然而,在观察到的所有变化中观察到大的受试者间的变异性。h3和基础水平之间的tpte、tamp和qtcf的变化在两个群组之间呈现相同比例的自相关。最后,40名(8%)或51名(10%)受试者在两个群组中表现出双峰(切迹)。他们几乎都是女性,并且这些患者的δtpte、δqtcf和δtamp高于在非切迹者(没有双峰(切迹)的患者)中观察到的那些。主成分分析主成分分析使得有可能产生三个新的定量值,与索他洛尔诱导的心室复极修饰有关。解释约65至67%表型方差的第一成分(pc1)反映了抑制ikr通道后的典型修饰,即tpte和qtcf的增加和tamp的减少(表1)。在一个或另一个探索(-2.5±1.5对0.3±1.1)或复制(-2.3±1.8对0.3±1.1)群组中,与未显示出这种双峰的患者(非切迹者)相比,在显示出双峰的患者(切迹者)中观察到pc1值显著降低(p<10-4)。因此,pc1值是ikr抑制的定量替代值。pc1值的分布如图1和图2所示,其例示了显示出极端的ikr抑制的患者,双峰(切迹)和极端负pc1值(图1),以及显示出弱ikr抑制的患者(图2)。其它主成分(pc2和pc3)分别解释了大约19-21%和14%的表型方差。表1.在探索群组(n=489,表格的上半部分)或复制群组(n=495,表格的下半部分)中δtamp、δtpte、δqtcf与主成分之间的相关性(r)相关性(r)δtampδtpteδqtcfpc1pc2pc3δtamp10.590.40-0.830.36-0.43δtpte0.5810.45-0.850.230.47δqtcf0.470.461-0.73-0.68-0.06pc1-0.84-0.84-0.78100pc20.280.3-.063010pc3-0.460.450.01001清楚地观察到,pc1在相同意义上与δtamp、δtpte和δqtcf相关(在该实施例中负相关),而pc2或pc3不是这种情况。还观察到pc1与δtamp、δtpte和δqtcf的相关系数的绝对值大于pc2或pc3与这些值的相关系数的绝对值。结论正如预期的那样,在基础水平和服用索他洛尔后3小时之间观察到tpte和qtcf的增加以及tamp的减少。通过δqtcf、δtpte和δtamp的主成分分析获得的新pc1值解释了“δ”数据(δqtcf、δtpte和δtamp)的总方差的大部分,因此与qtcf和tpte增加的共同机制相关,与tamp减少相关,并且是药物诱导的ikr抑制的定量和整合标志物。实施例2-应用算法来识别与ikr抑制风险增加相关的药物群体对615名身体健康的欧洲或北非型18至60岁女性进行了研究,所述女性qtcf<450ms,没有已知疾病或慢性疾病或长期治疗(但避孕除外),没有任何先天性长qt综合征、心律失常或猝死的家族史。测量和计算各种qtcf、tamp和tpte数据根据与实施例1相同的方案,在施用80mg单次口服剂量的索他洛尔之前和之后3小时测量qtcf、tamp和tpte。还计算δqtcf、δtpte和δtamp。主成分分析对δqtcf、δtpte和δtamp进行主成分分析(xlstat软件,),以产生三个新的去相关值。结果pc1变量以相同的方式与δqtcf、δtpte和δtamp相关(即在相同意义上与这些变量的每一个最大相关),这解释了63%的观察到的表型方差(特征为qtcf和tpte增加以及tamp减少)。还观察到,与没有避孕的女性组相比,服用屈螺酮作为避孕药的女性的pc1绝对值显著更高(分别为0.56[-0.13;1.5]和0.09[-0.58;1.1,p<0.05)。在该实施例中,由分析仅为女性的子组产生的pc1与δqtcf(r=0.71)、δtpte(r=0.85)和δtamp(r=0.83)正相关,而更大的pc1正值与更强的ikr抑制相关。同样,服用屈螺酮的女性在服用索他洛尔后3小时(25.8%)比未服用口服避孕药的女性(13.4%)有更多的双峰(切迹)。在这两组中,关于血浆索他洛尔浓度没有观察到差异。这些结果与屈螺酮的药理学性质一致,屈螺酮比其它避孕药具有更低的雄激素潜能,已知睾酮的保护性质。总结论实施例1清楚地表明,算法的应用使得有可能确定患者对索他洛尔的个体反应,以及该患者对药物诱导的ikr通道抑制的敏感性(并因此确定尖端扭转型室性心动过速的风险)。实施例2清楚地表明,本文所述的方法(使用基于δqtcf、δtpte和δtamp的主成分分析的算法)使得有可能鉴定给定物质(在这种情况下是屈螺酮)的qt-延长-诱导和ikr通道抑制性质。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1