假体心脏瓣膜及用于输送其的装置和方法与流程
本申请要求于2016年6月30日提交的题为“prostheticheartvalvesandapparatusandmethodsfordeliveryofsame(假体心脏瓣膜及用于输送其的装置和方法)”的美国临时申请号62/356,828的优先权和权益,其全部公开内容通过引用并入本文。
本文中描述了实施例,其涉及用于输送和部署假体瓣膜的装置和方法,具体涉及用于假体心脏瓣膜的装置和方法,用于将假体心脏瓣膜以反向配置输送到患者的心脏内。
背景技术:
假体心脏瓣膜可能对在心脏内的输送和部署提出了特别的挑战。心脏瓣膜病以及特别是主动脉瓣和二尖瓣疾病在美国(us)是重要的健康问题;在美国每年要实施接近90,000例瓣膜置换。涉及心脏瓣膜的原位置换的传统瓣膜置换手术被认为是“开心”外科手术。简而言之,手术需要外科手术打开胸腔,利用心肺机启动体外循环,使心脏停止并且打开心脏,切除并置换病变的瓣膜,以及重启心脏。虽然对于在其他方面健康的人而言,瓣膜置换手术的死亡风险通常为1-4%,但是由于需要进行体外循环,所以明显更高的发病率很大程度上与手术相关联。此外,对于老年患者,开心手术通常难以被忍受。因此,消除手术的体外部件可以导致发病率降低,并且可以显著地降低瓣膜置换疗法的成本。
虽然以经导管的方式置换主动脉瓣是深入研究的主题,但是对于二尖瓣的关注较少。这部分地反映了与自体(native)二尖瓣装置相关联的更高程度的复杂性,因此反映了在插入和锚固置换假体方面的更高程度的难度。存在用于经导管二尖瓣置换的输送设备和方法的需要。
一些已知的输送方法包括:将假体二尖瓣输送穿过心尖穿刺部位。在这样的手术中,瓣膜以压缩配置放置在例如34fr至36fr(即外径约11mm至12mm)的输送导管的内腔内。将假体瓣膜输送到心脏的心房可以例如经由经股动脉途径经心房(transatrially)直接进入心脏的左心房、经颈静脉途径或经心尖(transapically)来实现。在许多情况下,期望假体瓣膜具有小的外周长或轮廓,以允许通过例如28fr(即外径约9mm)的较小的输送导管插入。
因此,存在这样的假体心脏瓣膜的需要,该假体心脏瓣膜可以在输送期间具有小的轮廓,同时仍然维持在心脏内执行其期望功能所需的尺寸和特点。
还存在用于在心脏内输送和部署假体心脏瓣膜的设备和方法的需要,其中瓣膜设置在小直径的输送鞘内,然后在心脏内将瓣膜移动至膨胀配置。
技术实现要素:
在本文中描述了用于假体心脏瓣膜、输送装置和输送方法的各种实施例的装置和方法,用于经由经血管和经心尖输送途径将假体心脏瓣膜输送到患者的心脏。在一些实施例中,假体心脏瓣膜包括耦合到内框架的外框架,并且外框架能够在相对于内框架的第一配置和相对于内框架的第二反向配置之间移动。使用包括输送鞘的装置可以将瓣膜输送到心脏,该输送鞘限定内腔,当外框架处于反向配置时,该内腔可以在其中接收假体心脏瓣膜。致动线材可释放地耦合到外框架,并且可以用于在瓣膜部署在输送鞘外部和心脏内之后帮助恢复外框架。
附图说明
图1a和图1b分别为根据实施例的假体心脏瓣膜示为处于第一配置和第二配置的一部分的示意图。
图1c和图1d分别为图1a和图1b的假体心脏瓣膜示为设置在输送鞘内的一部分的示意图。
图2a和图2b分别为图1a和图1b的假体心脏瓣膜示为处于第一配置和第二配置的一部分的示意图。
图3至图5是根据实施例的假体心脏瓣膜的正视图、仰视图和俯视图。
图6是图3至图5的假体心脏瓣膜的内框架处于未膨胀配置的打开展平视图。
图7和图8分别是图6的内框架处于膨胀配置的侧视图和仰视图。
图9是图3至图5的瓣膜的外框架处于未膨胀配置的打开展平视图。
图10和图11分别是图9的外框架处于膨胀配置的侧视图和俯视图。
图12至图14是图6至图8的内框架和图9至图11的外框架的组件的侧视图、前视图和俯视图。
图15为根据实施例的内框架和外框架的组件示为处于偏置膨胀配置的侧视立体图。
图16为图15的组件的侧视立体图,所示的外框架被反向。
图17为图16的组件示为在输送鞘的内腔内处于收缩配置的侧视图。
图18为图17的组件示为处于第一部分部署配置的侧视图。
图19为图17的组件示为处于第二部分部署配置的侧视图。
图20为图17的组件的侧视图,示为处于第三部分部署配置,其中反向的外框架大体上部署在输送鞘外部。
图21为图17的组件的侧视图,示为处于第四部分部署配置,其中外框架已经恢复并呈现偏置膨胀配置。
图22至图24图示了将图15至图21的假体瓣膜输送到心脏的心房和天然二尖瓣瓣环内的方法的一部分的步骤。
图25是根据实施例的输送设备和假体心脏瓣膜的示意图。
图26a为图25的假体心脏瓣膜示为在在输送鞘内并耦合到瓣膜支座的一部分的侧视图。
图26b是图26a的假体瓣膜的附接构件的侧视图。
图26c是图26a的瓣膜支座的端视图。
图27是根据实施例的在输送鞘内部处于反向配置的假体瓣膜的横截面侧视图。
图28是根据实施例的在输送鞘内部处于反向配置的假体瓣膜的横截面侧视图的一部分,包括扩张器。
图29a是根据实施例的在输送鞘的内腔内部处于反向配置的假体心脏瓣膜的横截面侧视图。
图29b是图9a的假体心脏瓣膜处于反向配置并在输送鞘外部的侧视图。
图30a和图30b分别为根据实施例的假体心脏瓣膜示为处于第一配置和第二配置的一部分的示意图。
图30c和图30d分别为图30a和图30b的假体心脏瓣膜示为设置在输送鞘内的一部分的示意图。
图31a和图31b分别为图30a和图30b的假体心脏瓣膜示为处于第一配置和第二配置的一部分的示意图。
图32a是根据实施例的输送设备和假体心脏瓣膜的侧视图的示意图。
图32b是图32a的输送设备的长形构件的端视图的示意图。
图33a是根据实施例的输送鞘的横截面侧视图,其中假体瓣膜处于反向配置并且设置在输送鞘中。
图33b是图33a的假体心脏瓣膜处于反向配置并在输送鞘外部的侧视图的图示。
图33c是图33a的输送设备的长形构件的端视图的图示。
图33d是根据实施例的输送设备的长形构件的端视图的图示。
图34是根据实施例的输送系统和假体心脏瓣膜的部分横截面侧视图。
图35是沿着图34中的线35-35截取的剖视图,示出了耦合到输送系统的管构件的致动线材。
图36是图34的输送系统的管构件的近侧端视图。
图37a是图36的管构件的一部分的侧视图。
图37b是根据另一实施例的多内腔管构件和根据一实施例的远侧保持元件的一部分的侧视图。
图37c是根据另一实施例的图37b的多内腔管构件和远侧保持元件的一部分的视图。
图38a至图38d各自是致动线材的不同实施例的侧视图。
图39为图34的输送系统和假体心脏瓣膜示为处于第一部分部署配置的部分横截面侧视图。
图40为图34的输送系统和假体心脏瓣膜示为处于第二部分部署配置的部分横截面侧视图。
图41为图34的输送系统和假体心脏瓣膜示为处于第三部分部署配置的部分横截面侧视图。
图42是沿着图34中的线a-a截取的剖视图,示出了处于部分释放位置的致动线材。
图43图示了根据实施例的在心脏内输送和部署假体瓣膜的方法的流程图。
图44图示了根据实施例的在心脏内输送和部署假体瓣膜的方法的流程图。
具体实施方式
本文中描述了用于诸如假体二尖瓣之类的假体心脏瓣膜的装置和方法,该假体心脏瓣膜可以被配置成移动到反向配置,用于将假体瓣膜输送到患者的心脏内。如本文中所描述的,在一些实施例中,假体瓣膜包括外框架,当假体瓣膜处于偏置膨胀配置时,该外框架可以相对于内框架反向。假体二尖瓣可以由例如形状记忆材料形成。在使外框架反向之后,假体瓣膜可以插入输送鞘的内腔中,使得假体瓣膜移动到收缩配置。
输送鞘可以用于使用用于输送假体心脏瓣膜(例如,假体二尖瓣)的多种不同的输送途径将假体瓣膜输送到患者的心脏内,其中反向的假体瓣膜可能通过心脏的心房进入心脏。例如,本文中所描述的假体瓣膜可以使用如在pct国际申请号pct/us15/14572(“572号pct申请”)和/或pct国际申请号pct/us16/12305(“305号pct申请”)中所描述的经股动脉输送途径来输送,每个pct国际申请的公开内容通过引用整体并入本文;或经由经心房途径(诸如于2015年9月18日提交的题为“apparatusandmethodsfortransatrialdeliveryofprostheticmitralvalve(用于经心房输送假体二尖瓣的装置和方法)”的美国临时专利申请序列号62/220,704(“704号临时申请”)中所描述的,其整体通过引用并入本文)来输送。在另一示例中,如各自通过引用整体并入本文的题为“apparatusandmethodsfordeliveryofprostheticmitralvalve(用于输送假体二尖瓣的装置和方法)”的美国临时专利申请序列号62/305,678(“678号临时申请”)和题为“apparatusandmethodsfordeliveryofprostheticmitralvalve(用于输送假体二尖瓣的装置和方法)”的美国专利申请公开号2017/0079790(“790号公开”)所描述的,本文中所描述的假体瓣膜(例如如本文中所描述的反向瓣膜)可以经由经颈静脉途径输送,例如经由右心房并穿过房间隔并进入左心房。如果需要,则本文中所描述的假体瓣膜也可以向心尖输送。通过经心尖途径,在已经将输送鞘布置在心脏的左心房内之后,将假体二尖瓣向远侧移出输送鞘,使得反向的外框架恢复并且假体瓣膜呈现其偏置膨胀配置。然后,可以将假体二尖瓣定位在心脏的二尖瓣瓣环内。
在一些实施例中,装置包括输送鞘、长形构件,该输送鞘限定内腔,该长形构件限定第一内腔和第二内腔并且至少部分地设置在输送鞘的内腔内。该装置还包括假体心脏瓣膜,该假体心脏瓣膜至少部分地设置在处于收缩配置的输送鞘的内腔内并且周向地围绕长形构件的一部分。假体心脏瓣膜包括耦合到内框架的外框架。外框架能够在相对于内框架的第一配置和相对于内框架的第二配置之间移动,其中外框架相对于内框架反向。假体心脏瓣膜设置在输送鞘的内腔内,外框架处于第二配置并且轴向地设置在内框架的近侧。该装置还包括第一致动线材,该第一致动线材可释放地耦合到外框架的第一部分,并且从第一部分穿过长形构件的第一内腔并从输送鞘的近侧端部引出。该装置还包括第二致动线材,该第二致动线材可释放地耦合到外框架的第二部分,并且从第二部分穿过长形构件的第二内腔并从输送鞘的近侧端部引出。外框架的第一部分和第二部分被配置成,当植入心脏内时设置在心脏的心房内。
在一些实施例中,方法包括:将输送鞘的远侧端部插入穿过心脏的心尖区域并进入心脏的心房。输送鞘具有设置在输送鞘的内腔内的假体心脏瓣膜。假体心脏瓣膜包括外框架和耦合到外框架的内框架。外框架能够在相对于内框架的第一位置和相对于内框架的第二位置之间移动,其中外框架相对于内框架反向。假体心脏瓣膜设置在输送鞘的内腔内,在将输送鞘的远侧端部插入穿过心脏的心尖区域并进入心脏的心房期间,外框架处于相对于内框架的第二位置。该方法还包括:将假体心脏瓣膜向远侧移出输送鞘。该方法还包括:使假体心脏瓣膜的外框架过渡到相对于内框架的第一位置,使得假体心脏瓣膜至少部分地呈现偏置膨胀配置。该方法还包括:将假体心脏瓣膜定位在心脏的体环(annulus)内。
在一些实施例中,方法包括:将输送鞘的远侧端部插入心脏的心房中。输送鞘具有设置在输送鞘的内腔内的假体心脏瓣膜。假体心脏瓣膜包括外框架和耦合到外框架的内框架。外框架能够在相对于内框架的第一位置和相对于内框架的第二位置之间移动,其中外框架相对于内框架反向。假体心脏瓣膜设置在输送鞘的内腔内,在将输送鞘的远侧端部插入心脏的心房中期间,外框架处于相对于内框架的第二位置,并且至少部分地轴向地设置在内框架的近侧。该方法还包括:将假体心脏瓣膜向远侧移出输送鞘。该方法还包括:使假体心脏瓣膜的外框架过渡到相对于内框架的第一位置,使得假体心脏瓣膜至少部分地呈现偏置膨胀配置。该方法还包括:将假体心脏瓣膜定位在心脏的体环内。
在一些实施例中,装置包括外鞘、输送鞘以及假体心脏瓣膜,该外鞘限定内腔,该输送鞘限定内腔并且可移动地设置在由外鞘限定的内腔内,该假体心脏瓣膜设置在处于收缩配置的输送鞘的内腔内。假体心脏瓣膜包括耦合到内框架的外框架。内框架可移除地耦合到瓣膜支座的远侧端部。外框架能够在相对于内框架的第一配置和相对于内框架的第二配置之间移动,其中外框架相对于内框架反向。假体心脏瓣膜设置在输送鞘的内腔内,外框架处于第二配置。该装置还包括第一致动线材以及第二致动线材,该第一致动线材可释放地耦合到外框架的第一部分,该第二致动线材可释放地耦合到外框架的第二部分。第一致动线材和第二致动线材中的每个具有(1)第一部分以及(2)第二部分,该第一部分从外框架向近侧延伸、穿过外鞘的内腔、沿着输送鞘的外壁并且穿过由输送鞘限定的第一侧孔眼,该第二部分从外框架向近侧延伸、穿过外鞘的内腔、沿着所有输送鞘的外侧并且穿过由输送鞘限定的第二侧孔眼。第一致动线材和第二致动线材中的每个的第一部分和第二部分被配置成向近侧拉动,以将外框架从第二配置朝向相对于内框架的第一配置推动。
在一些实施例中,装置包括假体瓣膜,该假体瓣膜包括内框架和外框架,该外框架在多个耦合接头处耦合到内框架。多个耦合接头被配置成允许外框架相对于内框架移动,使得假体瓣膜可在第一配置和第二配置之间移动。当假体瓣膜处于第一配置时,外框架和内框架共同限定假体瓣膜的第一长度;当假体瓣膜处于第二配置时,外框架和内框架共同限定假体瓣膜的第二长度,并且第二长度大于第一长度。当假体瓣膜均处于第一配置和第二配置时,内框架具有相同的长度。
在一些实施例中,装置包括假体心脏瓣膜,该假体心脏瓣膜包括内框架和外框架,该外框架在多个耦合接头处耦合到内框架。假体瓣膜可在第一配置和第二配置之间移动。多个耦合接头被配置成允许外框架在相对于内框架的第一位置和相对于内框架的第二位置之间移动,其中外框架相对于内框架反向。当外框架处于第一位置时,假体瓣膜处于第一配置;当外框架处于第二位置时,假体瓣膜处于第二配置。
在一些实施例中,装置包括假体心脏瓣膜,该假体心脏瓣膜包括内框架和外框架,该外框架在多个耦合接头处耦合到内框架。多个耦合接头被配置成允许外框架相对于内框架移动,使得假体瓣膜可在第一配置和第二配置之间移动。外框架具有外框架耦合部以及外框架自由端部,该外框架耦合部在多个耦合接头处耦合到内框架。内框架具有内框架耦合部,该内框架耦合部在多个耦合接头处耦合到外框架。第一端部和内框架自由端部在内框架与第一端部相对的一端上。当假体瓣膜处于第一配置时,多个耦合接头设置在外框架自由端部和内框架的第一端部之间。当假体瓣膜处于第二配置时,多个耦合接头设置在内框架自由端部和外框架自由端部之间。
在一些实施例中,装置包括假体心脏瓣膜,该假体心脏瓣膜包括内框架,该内框架在多个耦合接头处耦合到外框架。多个耦合接头被配置成允许外框架相对于内框架移动,使得假体瓣膜可在第一配置和第二配置之间移动。外框架具有外框架耦合部以及外框架自由端部,该外框架耦合部在多个耦合接头处耦合到内框架。内框架具有内框架耦合部以及内框架自由端部,该内框架耦合部在多个耦合接头处耦合到外框架。当假体瓣膜处于第一配置时,外框架自由端部和内框架自由端部各自沿相同方向打开。当假体瓣膜处于第二配置时,外框架自由端部和内框架自由端部沿相反方向打开。
在一些实施例中,装置包括输送鞘、瓣膜支座以及假体心脏瓣膜,该输送鞘限定内腔,该瓣膜支座可移动地设置在输送鞘的内腔内,该假体心脏瓣膜至少部分地设置在处于收缩配置的输送鞘的内腔内。假体心脏瓣膜包括耦合到内框架的外框架,并且内框架可移除地耦合到瓣膜支座的远侧端部。外框架能够在相对于内框架的第一配置和相对于内框架的第二配置之间移动,其中外框架相对于内框架反向。假体心脏瓣膜设置在输送鞘的内腔内,外框架处于第二配置。第一致动线材可释放地耦合到外框架的开口自由端部的第一部分,第二致动线材可释放地耦合到外框架的开口自由端部的第二部分。第一致动线材和第二致动线材中的每个具有第一部分和第二部分,该第一部分从外框架向近侧延伸,该第二部分从外框架向近侧延伸。第一致动线材和第二致动线材中的每个的第一部分和第二部分被配置成向近侧拉动,以将外框架从第二配置朝向相对于内框架的第一配置推动。
在一些实施例中,装置包括外鞘、内鞘、管构件、瓣膜支座以及假体心脏瓣膜,该外鞘限定内腔,该内鞘可移动地设置在外鞘的内腔内并限定内腔,该管构件可移动地设置在外鞘的内腔内并限定内腔,该瓣膜支座可移动地设置在内鞘的内腔内以及由管构件限定的内腔内,该假体心脏瓣膜至少部分地设置在外鞘的内腔内并且至少部分地在内鞘的内腔内。假体心脏瓣膜包括耦合到内框架的外框架,并且内框架可移除地耦合到瓣膜支座的远侧端部。外框架能够在相对于内框架的第一配置和相对于内框架的第二配置之间移动,其中外框架相对于内框架反向。假体心脏瓣膜设置在外鞘的内腔和内鞘的内腔内,外框架处于第二配置。第一致动线材可释放地耦合到外框架的开口自由端部的第一部分,并且在管构件上的第一位置处可释放地耦合到管构件。第二致动线材可释放地耦合到外框架的开口自由端部的第二部分,并且在管构件上的第二位置处可释放地耦合到管构件。
在一些实施例中,方法包括:将输送鞘的远侧端部插入心脏的左心房中。输送鞘具有设置在输送鞘的内腔内的假体二尖瓣,并且假体二尖瓣具有耦合到内框架的外框架,使得外框架可在相对于内框架的第一位置和相对于内框架的第二位置之间移动,其中外框架相对于内框架反向。假体瓣膜设置在输送鞘的内腔内,外框架处于相对于内框架的第二位置。假体二尖瓣向远侧移出输送鞘,使假体二尖瓣的外框架恢复回到相对于内框架的第一位置,使得假体二尖瓣至少部分地呈现偏置膨胀配置。假体二尖瓣被定位在心脏的二尖瓣瓣环内。
图1a和图1b分别为根据实施例的假体心脏瓣膜100示为处于第一配置和第二配置的一部分的示意图,而图1c和图1d分别图示了图1a和图1b的假体心脏瓣膜100示为设置在输送鞘126的内腔内的各部分。图2a和图2b分别图示了图1a和图1b的假体心脏瓣膜100的一部分,并且示出了处于第一配置和第二配置中的每个的假体心脏瓣膜的长度尺寸。如上所述,在一些情形下,诸如当经由经股动脉、经心房或经颈静脉途径将假体瓣膜输送到心脏时,由于输送鞘的内腔的尺寸较小,所以假体瓣膜在输送期间的尺寸应当相应地构造尺寸。因此,期望具有一种假体瓣膜,其可以在用于植入心脏中(例如在天然二尖瓣瓣环内)的偏置膨胀配置和具有较小的外周长或轮廓的输送配置之间重新配置,以允许在输送鞘的内腔内输送。假体瓣膜100和本文所述的假体瓣膜的实施例可以被构造并且被形成,以实现这些期望的功能和特点。
假体心脏瓣膜100(在本文中也被称为“假体瓣膜”或“瓣膜”)可以例如是假体二尖瓣。瓣膜100包括外框架120和内框架150。如下文参照图3至图15更详细描述的,外框架120和内框架150各自形成为管状结构。如下文更详细描述的,外框架120和内框架150可以在多个耦合接头146处耦合在一起,多个耦合接头146围绕内框架150的周边和外框架120的周边而设置。瓣膜100还可以包括其他特征,诸如下文关于图3至图15所描述的那些特征。出于说明目的,仅关于图1a至图2b对内框架150和外框架120进行讨论。关于图1a至图2b所描述的瓣膜100的各种特点和特征可以适用于本文中所描述的任何假体瓣膜。
外框架120被配置成具有偏置膨胀或未变形的形状,并且可以被操纵和/或变形(例如压缩或约束),并且当释放时,返回到其原始(膨胀或未变形的)形状。例如,外框架120可以由诸如金属或塑料之类的材料形成,这些材料具有形状记忆特性。关于金属,镍钛诺(nitinol®)被发现特别有用,因为它可以被加工成奥氏体的、马氏体的或超弹性的。也可以使用其他形状记忆合金,诸如cu-zn-al-ni合金和cu-al-ni合金。内框架150可以由nitinol®的激光切割管形成。内框架150也可以具有偏置膨胀或未变形的形状,并且可以被操纵和/或变形(例如压缩和/或约束),并且当释放时,返回到其原始(膨胀或未变形)形状。下文关于瓣膜200和图3至图15对关于内框架150和外框架120的进一步细节进行描述。
使用各种不同的输送途径可以在心脏的左心房内输送和部署瓣膜100,这些输送途径包括例如如通过引用并入上文的572号pct申请中和/或305号pct申请中所述的经股输送途径,或如通过引用并入上文的704号临时申请、678号临时申请和790号公开中所述的经心房或经颈静脉途径。如上所述,在一些情形下,诸如当经由经股动脉或经心房途径将假体瓣膜输送到心脏时,由于输送鞘的内腔的尺寸较小,因此假体瓣膜在输送期间的尺寸应当相应地构造尺寸。因此,期望具有一种假体瓣膜,其可以在用于植入心脏中(例如在天然二尖瓣瓣环内)的偏置膨胀配置和具有较小的外周长或轮廓的输送配置之间重新配置,以允许在输送鞘的内腔内输送。假体瓣膜100和本文所述的假体瓣膜的实施例可以被构造并且被形成,以实现这些期望的功能和特点。
更具体地,瓣膜100可以具有偏置膨胀配置(如图1a和图2a所示)、反向配置(如图1b和图2b所示)以及压缩或收缩配置(如图1c和图1d所示)。膨胀配置允许瓣膜100在植入心脏内时起作用。瓣膜100可以移动至反向配置和压缩或收缩配置,用于将瓣膜100输送到患者的心脏。
为了使得瓣膜100能够移动到反向配置,外框架120可以以允许外框架120相对于内框架150移动的方式耦合到内框架150。更具体地,耦合接头146可以以允许外框架120相对于内框架150移动的方式将外框架120耦合到内框架150。例如,在一些实施例中,耦合接头146可以被配置成允许外框架120相对于内框架150、围绕耦合接头146旋转。在一些实施例中,耦合接头可在外框架120和内框架150之间提供枢转耦合。在一些实施例中,耦合接头可以在外框架120和内框架150之间提供柔性附接。如本文中参考假体瓣膜的各种实施例所述,耦合接头146可以是各种不同类型和配置。例如,耦合接头146可以包括活动铰链、柔性构件、缝合线、缠绕穿过开口的缝合线、插入穿过开口的销或突片或者其任何组合。
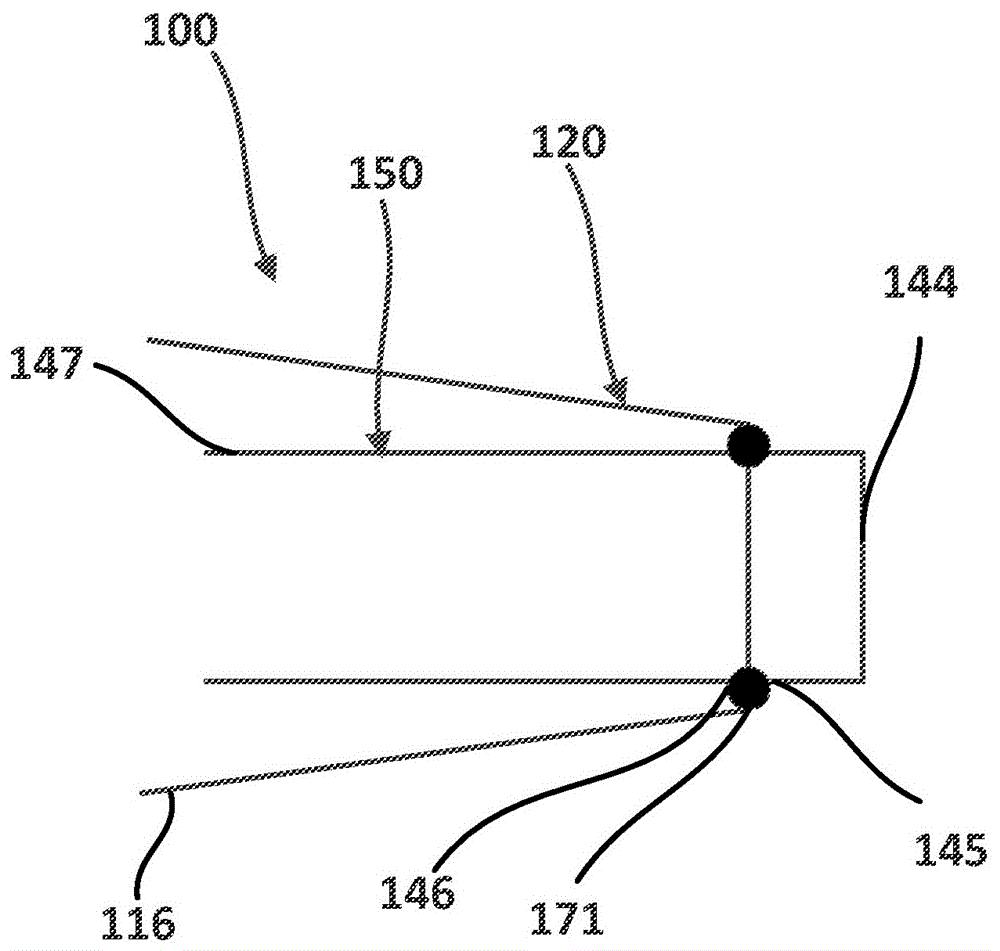
为了将瓣膜100从膨胀配置(图1a)移动到反向配置(图1b),通过将外框架120围绕耦合接头146移动(例如旋转、枢转、折曲),外框架120被移动到相对于内框架150的脱垂或反向配置,如图1b、图1d和图2b所示。瓣膜100的外框架120的弹性或超弹性结构也允许外框架120移动到并设置在相对于内框架150的脱垂或反向配置中。为了使外框架120移动到相对于内框架150的反向配置,外框架120经由耦合接头146相对于内框架150向远侧折叠或反向(至图1b中的右侧)。如图1a和图2a所示,外框架120在反向之前处于相对于内框架150的第一位置,其中开口或自由端部116(也称为外框架120的心房部分116)设置在耦合接头146的近侧或者左侧并且在与内框架150的自由端部147(也称为内框架的第二端部)相同的方向上。当外框架120移动到反向配置时(即相对于内框架150的第二位置),自由端部116设置在耦合接头146的远侧(或图1b和图2b中的右侧),并且在与内框架150的自由端部147相反的方向上。换句话说,当瓣膜100处于偏置膨胀配置(例如图1a)时,耦合接头146设置在内框架150的第一端部144(也称为系绳耦合部)与外框架120的自由端部116之间。当瓣膜100处于反向配置时(例如图1b)(即外框架120已经移动到反向配置或位置),耦合接头146设置在内框架150的自由端部或第二端部147与外框架120的自由端部116之间。
当处于反向配置时,瓣膜100的总长度增加,但是内框架150的长度和外框架120的长度保持相同(或大体上相同)。例如,如图2a和图2b所示,处于偏置膨胀配置(在如图2a所示反向之前)的瓣膜100的总长度l1小于当处于反向配置(图2b)时的瓣膜100的总长度l2。当瓣膜100都处于偏置膨胀配置和反向配置时,内框架150的长度li和外框架120的长度lo大体上相同(或相同)。另外,在一些实例中,依据外框架的特定配置,当瓣膜100处于反向配置时,瓣膜100的总外周长或外径可以更小。
在瓣膜100处于反向配置的情况下,瓣膜100可以放置在输送鞘126的内腔内,用于将瓣膜100输送到心脏的左心房,如图1d所示。当放置在输送鞘126的内腔内时,瓣膜100移动到收缩或压缩配置,其中瓣膜100的外径或外周长减小。因为瓣膜100处于反向配置,所以瓣膜100能够放置在比在其他情形下可能更小的输送鞘126内。例如,出于比较目的,图1c图示了放置在输送鞘126'的内腔内的瓣膜100,其中瓣膜100在被设置在输送鞘126'内之前尚未移动到反向配置。如图1c所示,当处于反向配置时,瓣膜100的外径减小,但是不会小到当放置在输送鞘126中时的瓣膜100的直径。因此,在图1c中,瓣膜100的整体外周长或外径为d1,并且在图1d中,瓣膜100的整体外周长或外径为d2,其小于d1。
因此,通过将外框架120设置成处于反向配置,瓣膜100可以收缩成更小的整体直径,即如果瓣膜100仅径向收缩时的话,放置在直径更小的输送鞘126中。这是因为当瓣膜处于偏置膨胀配置时,内框架150嵌套在外框架120的内部内,因此外框架120必须在内框架150周围收缩。在一些实施例中,内框架150和外框架同心设置。而在反向配置中,内框架150和外框架120相对于彼此轴向布置(即内框架没有嵌套在外框架150内),使得外框架120可以收缩而无需容纳其内部的内框架150的所有结构。换句话说,在内框架150大部分设置在外框架120内部或嵌套在外框架120内的情况下,框架结构的层或块不能被压缩到直径这么小。另外,如果框架是嵌套的,则结构的柔性较小,因此需要更大的力来弯曲瓣膜,例如以穿过曲折的脉管系统或在穿过房间隔后在左心房中进行紧转,以适当地定向用于插入二尖瓣瓣环中。
图3至图14图示了假体心脏瓣膜的另一实施例,该假体心脏瓣膜可以使用各种不同的输送途径在心脏的左心房内输送和部署,这些输送途径包括例如经股动脉输送途径或经心房输送途径。图3至图5分别是根据实施例的假体心脏瓣膜200的前视图、仰视图和俯视图。假体心脏瓣膜200(在本文中也称为“瓣膜”或“假体瓣膜”)被设计成置换受损或病变的自体心脏瓣膜,诸如二尖瓣。瓣膜200包括外框架组件210和耦合到外框架组件210的内瓣膜组件240。
如所示出的,外框架组件210包括外框架220,该外框架220在其外表面的全部或一部分上覆盖有外覆盖物230,并且由内覆盖物232覆盖在其内表面的全部或一部分上。外框架220可以为假体心脏瓣膜200提供几个功能,包括用作主要结构,作为将瓣膜锚固到自体心脏瓣膜装置上的锚固机构和/或用于单独锚固机构的附接点,承载内瓣膜组件240的支撑件和/或抑制假体心脏瓣膜200和自体心脏瓣膜装置之间的瓣周漏的密封件。
外框架220具有偏置膨胀配置,并且可以被操纵和/或变形(例如压缩和/或约束),并且当释放时,返回到其原始无约束形状。为实现这点,外框架220可以由诸如金属或塑料之类的材料形成,这些材料具有形状记忆特性。关于金属,nitinol®被发现特别有用,因为它可以加工成奥氏体的、马氏体的或超弹性的。还可以使用其他形状记忆合金,诸如cu-zn-al-ni合金和cu-al-ni合金。
如图3最佳所示,外框架组件210具有上端(例如心房部分216处)、下端(例如心室部分212处)以及其间的中间部分(例如体环部分214处)。上端或心房部分216(也被称为“外自由端部”)限定外框架组件210的开口端部。外框架组件210的中间或体环部分214具有周长,该周长被配置成(例如尺寸被设计成、形状被设计成)配合到自体房室瓣的体环中。外框架组件210的上端的周长大于中间部分的周长。在一些实施例中,外框架组件210的上端的周长大体上大于中间部分的周长。如图5最佳所示,外框架组件210的上端和中间部分具有d形横截面。这样,外框架组件210促使适当配合到自体房室瓣的体环中。
内瓣膜组件240包括内框架250、外覆盖物(未示出)和小叶(leaflet)270。如所示出的,内瓣膜组件240包括上部,该上部具有形成有多个拱的周边。内框架250包括六个轴向柱或框架构件,这六个轴向柱或框架构件支撑内瓣膜组件240的外覆盖物和小叶270。小叶270沿着被示为连合柱252的其中三个柱附接(在图4中最佳图示),并且内瓣膜组件240的外覆盖物附接到其他三个柱254(在图4中最佳图示),并且可选地附接到连合柱252。内瓣膜组件240和小叶270的每个外覆盖物由近似矩形的材料片形成,它们在其上端或心房端结合在一起。内瓣膜组件240的外覆盖物的下心室端可以结合到外框架组件210的内部覆盖物232,并且小叶270的下心室端可以形成自由边缘275,尽管耦合到连合柱252的下端。
尽管内瓣膜组件240被示为具有三个小叶,但是在其他实施例中,内瓣膜组件可以包括任何合适数目的小叶。小叶270能够在打开配置和闭合配置之间移动,其中小叶270在密封抵接面中接合(coapt)或接触。
外框架组件210的外覆盖物230和外框架组件210的内覆盖物232、内瓣膜组件240的外覆盖物260和内瓣膜组件240的小叶270可以由任何合适的材料或诸如上文所讨论的那些材料之类的材料的组合形成。在该实施例中,外框架组件210的内覆盖物232、内瓣膜组件240的外覆盖物和内瓣膜组件240的小叶270至少部分地由猪心包形成。而且,在该实施例中,外框架组件210的外覆盖物230至少部分地由聚酯形成。
内框架250在图6至图8中更详细地示出。具体地,图6至图8分别示出了根据实施例的处于未变形、初始状态下的内框架250(图6)、处于膨胀配置的内框架250的侧视图(图7)以及处于膨胀配置的内框架250的仰视图(图8)。
在该实施例中,内框架250由nitinol®的激光切割管形成。图6中图示了处于未变形、初始状态下的内框架250,即作为激光切割但为了便于说明而切割并部署成平板。内框架250可以分成四个部分,对应于最终形式的内框架250的功能上不同的部分:心房部分247、本体部分242、支柱部分243以及系绳夹或连接部分244。支柱部分243包括六个支柱,诸如支柱243a,其将本体部分242连接到系绳连接部分244。
系绳连接部分244(也称为内框架的第一端部)包括支柱的纵向延伸部,该纵向延伸部通过成对、相对的略呈v形的连接构件(或“微型v”)周向连接。系绳连接部分244被配置成通过施加压缩力而径向收缩,该压缩力使得微型v变为更加深入的v形,顶点纵向移动靠得更近并且v形的开口端周向移动靠得更近。因此,系绳连接部分244可以被配置成压缩地夹紧或紧握系绳的一端,要么直接连接到系绳线(例如编织的细丝线)上要么连接到诸如聚合物或金属片之类的中间结构上,该聚合物或金属片长期牢固地固定在系绳线上。
与系绳连接部分244形成对比,心房部分247(也称为“内框架自由端部”)和本体部分242被配置成径向膨胀。支柱部分243在膨胀的本体部分和压缩的系绳连接部分244之间形成纵向连接和径向过渡。本体部分242提供内框架耦合部245,内框架耦合部245包括六个纵向柱,诸如柱242a。内框架耦合部分245可以用于将小叶270附接到内框架240上,和/或可以用于诸如通过将内框架250连接到外框架220而将内部组件240附接到外部组件210上。在所图示的实施例中,柱包括开口,连接构件(诸如缝合细丝和/或线材)可以穿过该开口,以将柱耦合到其他结构。
图7和图8分别以侧视图和仰视图示出了处于完全变形的(即最终部署)配置的内框架250。
图9至图11更详细地示出了瓣膜200的外框架220。在该实施例中,外框架220也由nitinol®的激光切割管形成。图9图示了处于未变形的初始状态(即在激光切割时,但是为了便于说明而切割并展开成平板)的外框架220。外框架220可以分为外框架耦合部271、本体部分272和套箍部分273(其包括心房或自由端部216),如图9所示。外框架耦合部271包括多个开口或孔眼,诸如271a,外框架220可以通过该开口或孔眼耦合到内框架250,如下文更详细地讨论的。
图10和图11分别以侧视图和俯视图示出了处于完全变形的(即最终部署)配置的外框架220。如图11中最佳所示,外框架耦合部271的下端形成大致圆形的开口(在图11中用“o”表示)。该开口的直径优选地大致对应于内框架250的本体部分242的直径,以便于瓣膜200的两个部件的耦合。
图12至图14分别以前视图、侧视图和俯视图示出了耦合在一起的外框架220和内框架250。两个框架共同形成用于诸如瓣膜200之类的假体瓣膜的结构支撑。框架以与自体瓣膜体环的期望关系支撑瓣膜小叶结构(例如小叶270),支撑用于两个框架的覆盖物(例如外覆盖物230、内覆盖物232、内瓣膜组件240的外覆盖物)以为心房和心室之间的血液渗漏提供阻隔件,并且(通过内框架250)耦合到系绳(例如系绳组件290)以通过系绳连接到心室壁来帮助将假体瓣膜200保持在自体瓣膜体环中的适当位置。外框架220和内框架250在六个耦合点(代表点被标识为“c”)处连接。在该实施例中,耦合点用机械紧固件(诸如短长度的线材)实现、穿过外框架耦合部271中的孔眼(诸如孔眼271a)和内框架250的本体部分242中的内框架耦合部245中的对应开口(例如纵向柱,诸如柱242a)。因此,内框架250设置在外框架220内并牢固地耦合到外框架220。
图15至图21图示了在将假体心脏瓣膜300插入输送鞘326(参见例如图17至图21)用于输送到心脏的心房中之前重新配置假体心脏瓣膜300(例如假体二尖瓣)的方法。假体心脏瓣膜300(在本文中也称为“瓣膜”)可以被构造为与上述瓣膜100和200相同或相似,并且功能相同或相似。因此,下文不对关于瓣膜300的一些细节进行描述。应当理解,对于未具体讨论的特征和功能,那些特征和功能可以与瓣膜200相同或相似。
如图15所示,瓣膜300具有外框架320和内框架350。如上文针对瓣膜100和200所讨论的,瓣膜300的外框架320和内框架350可以各自用形状记忆材料形成并具有偏置膨胀配置。外框架320和内框架350可以移动到收缩配置,用于将瓣膜300输送到心脏。在制备用于输送到心脏的瓣膜300的示例方法中,瓣膜300的外框架320首先被设置成处于如图16所示的脱垂或反向配置。具体地,瓣膜300的外框架320的弹性或超弹性结构允许外框架320在瓣膜300插入输送鞘326的内腔之前设置在脱垂或反向配置中。如图16所示,为了将外框架320设置在反向配置中,外框架320向远侧折叠或反向(至图16的右侧),使得外框架320的开口自由端316朝向远离内框架350的开口自由端347。如上文针对瓣膜100所描述的,在这种反向配置中,瓣膜300的整个外周长或外径减小,并且整个长度增加。例如,图15所示的直径d1大于图16所示的直径d2,并且(图12所示,瓣膜200的)长度l1小于图16所示的瓣膜300的长度l2。在外框架320处于相对于内框架350的反向配置的情况下,瓣膜300可以放置在输送鞘326的内腔内,如图17所示,用于将瓣膜300输送到心脏的左心房。通过将外框架320设置在相对于内框架350的反向配置中,瓣膜300可以收缩成更小的总直径,即,当放置在比处于图15所示的配置的瓣膜300被径向塌缩而没有反向的直径更小的输送鞘中时。这是因为在图15所示的配置中,两个框架是同心的或嵌套的,因此外框架320必须在内框架350周围收缩,而在图16所示的配置中,两个框架大体上同轴但不是同心的或嵌套的。因此,在图16所示的配置中,外框架320可以收缩而不需要在其内部容纳内框架350。换句话说,在内框架350大部分设置在外框架320内部或嵌套在外框架320内的情况下,框架结构的层或块不能被压缩为直径这么小。另外,如果框架是嵌套的,则结构的柔性较小,因此需要更大的力来弯曲瓣膜,例如以穿过曲折的脉管系统或在穿过房间隔后在左心房中进行紧转,以适当地定向用于插入到二尖瓣瓣环中。
图22至图24图示了将瓣膜300输送到心脏的手术的一部分。在该实施例中,示出了瓣膜300经由例如在上文通过引用并入的572号pct申请和/或305号pct申请中所描述的经股动脉输送途径输送。在瓣膜300设置在输送鞘326的内腔内并且处于如图17所示的反向配置的情况下,输送鞘326可以插入股骨穿刺、穿过股静脉、穿过下腔静脉、进入右心房、穿过隔膜sp并进入心脏的左心房la。在输送鞘326的远侧端部设置在心脏的左心房内的情况下,瓣膜300可以部署在输送鞘326的远端的外部。例如,在一些实施例中,推进器设备338可以用于将瓣膜300移出或推出输送鞘326的远端。如图22至图24所示,系绳336可以附接到瓣膜300、并且延伸穿过二尖瓣瓣环、穿过左心室lv并且伸出顶点ap处的穿刺部位。在一些实施例中,通过在系绳336上向近侧拉动,可以从输送鞘326移出瓣膜300。在一些实施例中,可以通过用推进器设备推动并用系绳拉动来部署瓣膜300。
在瓣膜300离开输送鞘326的内腔时,外框架组件310首先以其如图18至图20的进程中所示的反向配置离开(也参见图22)。在外框架组件310完全在输送鞘326的内腔的外部之后,外框架320可以恢复到其如图21、图23和图24所示的膨胀或部署配置。在一些实施例中,由于其形状记忆特性,外框架320可以在完全离开输送鞘的内腔之后自动恢复。在一些实施例中,输送鞘或另一设备的部件可以用于辅助外框架组件310的恢复。在一些实施例中,推进器设备和/或系绳可以用于帮助恢复外框架组件310。瓣膜300可以继续部署,直到内框架350与左心房一起完全部署并且瓣膜300处于膨胀或部署配置(例如如图15和图24所示)为止。然后,可以使用心外膜垫设备339将瓣膜300和系绳336固定到心脏的顶点上,如图24所示并且如在572号pct申请和305号pct申请中更详细地描述的那样。
图25示意性地图示了输送系统的另一实施例,该输送系统可以用于通过例如经血管途径将假体心脏瓣膜输送和部署在患者心脏内。在该实施例中,输送系统405包括输送鞘426、瓣膜支座438(也称为“推动器”)、以及一根或多根致动线材474和476。在该示意图中,仅图示了两根致动线材,但是在其他实施例中,可以仅使用一根致动线材或多于两根致动线材。
输送鞘426可以用于输送瓣膜400,瓣膜400包括内瓣膜组件440以及外框架组件410,瓣膜组件440包括内框架(图25中未标示),外框架组件410包括外框架(图25中未标示)。瓣膜400可以被构造为与本文所述和/或305号pct申请中描述的任何假体瓣膜相同或相似,并且功能相同或相似,并且可以在部署或膨胀配置和输送配置之间移动,其中外框架被设置在相对于内框架的反向位置中,如本文所述和/或305号pct申请中所述。如图25所示,当瓣膜处于输送配置时(即外框架相对于内框架反向),瓣膜400可以设置在输送鞘426的内腔内。在该实施例中,当处于输送配置并且放置在输送鞘内时,外框架组件410设置在内瓣膜组件440的远侧。瓣膜支座438耦合到内瓣膜组件440并且致动线材耦合到外瓣膜组件410。瓣膜支座438可以经由耦合器406可释放地耦合到内瓣膜组件440,耦合器406附接到内瓣膜组件440,如图26a至图26c所示。在该实施例中,耦合器406呈t形杆或锤形。应当理解,可以使用具有其他配置和形状的耦合器。
如图26a所示,耦合器406被接收在凹陷404内,并且瓣膜400和瓣膜支座438可以设置在输送鞘426的内腔内。输送鞘426的内径的尺寸被设计,使得当瓣膜支座438和瓣膜400设置在其中时,耦合器406不能离开凹陷404。换句话说,输送鞘426的内壁将耦合器406维持在凹陷404内。当瓣膜400移动到输送鞘426的外部时,耦合器406将能够自由地离开凹陷404,使内框架450从瓣膜支座438释放。
在替代实施例中,瓣膜支座438可以经由线材或缝合线可移除地耦合到瓣膜400(例如瓣膜400的内框架450),这些线材或缝合线可以在将瓣膜400输送到心脏之后进行切割。在一些情况下,当瓣膜仍然设置在输送鞘426内时,瓣膜支座438可以与瓣膜400解耦合,而在其他实例中,在瓣膜400离开心脏内的输送鞘426之后,瓣膜支座438才可以与瓣膜400解耦合。
致动线材474和476可以利用各种不同的耦合方法耦合到外框架组件410的外框架。例如,外框架410可以包括环(如本文中关于外框架510、外框架1010和305号pct申请中所描述的),通过该环,致动线材474和476可以被接收或旋紧。外框架上的环的数目可以变化,并且每根致动线材连接穿过的环的数目可以变化。例如,在一些实施例中,外框架包括12个环,并且第一致动线材通过其中的6个环旋紧,并且第二致动线材通过其中的6个环旋紧。在其他实施例中,外框架可以包括12个环,并且可以存在4根致动线材,每根致动线材耦合到其中的3个环。在一些实施例中,单根致动线材通过外框架的所有环耦合。
在该实施例中,输送鞘426可以用于使用经血管途径(例如经股动脉、经心房、经颈静脉)将瓣膜400输送到心脏的左心房。当输送鞘426的远端设置在左心房内时,使用致动线材474、476将瓣膜400移出输送鞘426的内腔,以帮助将瓣膜400拉出输送鞘426。在一些情况下,瓣膜支座438还可以用于将瓣膜400推出输送鞘426。更具体地,致动线材474和476可以从外框架组件410延伸出输送鞘的远端,并且向近侧端延伸。在一些实施例中,致动线材474、476在输送鞘426外部向近侧延伸,然后通过侧孔眼或孔(未示出)返回到输送鞘426的内腔中,然后从输送鞘426的近侧端伸出。因此,用户(例如医生)可以拉动致动线材474和476的近侧端部,以转而将外框架组件410拉出输送鞘426的远端。在一些实施例中,致动线材474、476从外框架组件410向近侧延伸、返回穿过输送鞘426的远端(例如,而非穿过输送鞘的侧孔眼或孔)并且进入输送鞘的内腔内、然后从输送鞘426的近侧端伸出。下文对各种不同的实施例和配置进行更详细地描述。
在外框架组件410离开输送鞘426时,它仍将处于相对于内瓣膜组件440的反向配置。在外框架组件410至少部分地在输送鞘426的内腔外部时,外框架组件410可以开始恢复到其膨胀或部署配置(图25中未示出)。然而,在该实施例中,当瓣膜400被输送到心脏时,致动线材474和476可以用于选择性地(例如由操作者)辅助和/或控制瓣膜400的膨胀、部署和/或铰接。以这种方式,使用时,可以向远侧拉动致动线材474、476的近侧端部以操纵外框架组件410,以辅助和控制外框架组件410从其相对于内瓣膜组件440的反向配置过渡到其膨胀或部署配置(未示出)。在一些实施例中,致动线材474、476可以由用户手动抓握以向近侧拉动致动线材。在一些实施例中,致动线材474、476可以可操作地耦合到输送系统405,使得用户不必手动处置致动线材。例如,致动线材可以耦合到输送系统405的输送鞘和/或手柄组件(未示出)。在下文和305号pct申请中对输送系统的各种实施例进行更详细地描述。
图27图示了输送系统505的实施例,输送系统505可以用于在与关于本文描述的其他实施例(例如在图34至图42中示出和描述的实施例)和305号pct申请所描述的实施例的手术相似或相同的手术中在心脏内输送和部署假体心脏瓣膜500(在本文中也称为“瓣膜”)。因此,本文中没有对关于瓣膜500的一些细节和与其一起执行的手术进行描述。应当理解,对于未具体讨论的特征和功能,那些特征和功能可以与本文所述的瓣膜(例如瓣膜1000)和/或305号pct申请所述的瓣膜相同或相似。瓣膜500可以被构造成与本文和/或305号pct申请中描述的任何瓣膜相同或类似,并且功能相同或相似。例如,瓣膜500包括外框架组件,该外框架组件具有外框架520、内瓣膜组件540以及系绳536,内瓣膜组件540具有内框架550,系绳536耦合到内瓣膜组件。输送系统505包括外输送鞘526、内鞘508、瓣膜支座538(也称为“推动器”)和多内腔长形管构件503(也称为“管”或“管构件”或“多内腔长形构件”)。如图27所示,内鞘508可移动地设置在由外输送鞘526限定的内腔582内,并且管构件503可移动地设置在由内鞘508限定的内腔583内。瓣膜支座538可移动地设置在由内鞘508限定的内腔583内。
与本文所述的其他实施例和305号pct申请的实施例一样,瓣膜500可以从偏置膨胀配置移动到反向配置,用于将瓣膜500输送到心脏。更具体地,为了将瓣膜500置于反向配置,外框架520可以移动到相对于内框架550的反向配置。在该实施例中,当瓣膜500处于反向配置时,瓣膜500至少部分地放置在内鞘508的内腔内,并且设置在内鞘508的远侧端附近。瓣膜支座538也设置在内鞘508的内腔583内。内框架550可以利用与上文关于耦合器406、耦合器1006和/或305号pct申请所描述的耦合器中的任一耦合器相同或相似的方式的耦合器506可释放地耦合到瓣膜支座538。类似地,外框架520包括环562,通过环562,致动线材574-577可以以与本文中(例如关于瓣膜1000)和/或305号pct申请中所述相同或相似的方式被旋紧。内鞘508可移动地设置在外输送鞘526内。如图6所示,瓣膜500的一部分设置在内鞘508的外部并位于外输送鞘526的内腔582内。在一些情况下,在执行部署瓣膜的手术之前,整个瓣膜500可以设置在内鞘508的内腔583内。
在该实施例中,内鞘508限定侧孔眼509,致动线材574-577可以穿过侧孔眼509。更具体地,如图27所示,当瓣膜500设置在内鞘508的内腔583内时,致动线材574-577从外框架520向近侧延伸、沿着内鞘508的外侧并在外输送鞘526的内腔582内、返回通过由内鞘508限定的侧孔眼509、在内鞘508的内腔583内并由长形钉扎构件578-1、578-2、578-3、578-4(统称为钉扎构件578;钉扎构件578-3和578-4在图27中未示出;为了说明的目的,是指关于图35至图37a中所示和所述的钉扎构件1078-3和1078-4)钉扎到管构件503。如所示出的,致动线材574的第一端和致动线材575的第一端由钉扎构件578-2钉扎,并且致动线材576的第一端和致动线材577的第一端由钉扎构件578-1钉扎。致动线材574的第二端和致动线材576的第二端由钉扎构件578-4(未示出)钉扎,并且致动线材575的第二端和致动线材577的第二端由钉扎构件578-3(未示出)钉扎。
致动线材574-577可以以与下文关于输送系统1005所述相同或相似的方式由钉扎构件578-1、578-2、578-3、578-4钉扎到管构件503。因此,没有针对该实施例对关于例如管构件503、钉扎构件578-1、578-2、578-3、578-4和致动线材574-577的一些细节以及与其一起执行的手术进行描述。应当理解,对于未针对该实施例具体讨论的特征和功能,那些特征和功能可以与本文中描述的输送系统(例如输送系统1005)和/或305号pct申请中描述的输送系统相同或相似。
用户(例如医生)可以使用致动线材574-577所耦合的管构件503来控制和/或操纵例如针对输送系统1005所描述的瓣膜500的运动和/或部署。在该实施例中,如所示出的,致动线材574-577的至少一部分可以设置在输送鞘526的内部内,从而限制致动线材574-577暴露于输送鞘526外部的区域,用于输送和/或部署瓣膜500的至少一部分。尽管由内鞘508限定的侧孔眼509被示为设置在内鞘508的远侧端部处或附近,但是在其他实施例中,侧孔眼509可以设置在沿着内鞘508的长度(例如朝向管理鞘的中间部分或近侧部分)的任何合适位置。
在该实施例中,为了将瓣膜500输送到心脏,其中设置有瓣膜500、内鞘508、瓣膜支座538和管构件503的外输送鞘526的远侧端设置在心脏的左心房内。在输送鞘526的远侧端部设置在心脏的左心房内的情况下,瓣膜500可以部署在输送鞘526外部。例如,内鞘508、瓣膜支座538和管构件503可以相对于外鞘526向远侧移动,将瓣膜500移出或推出外鞘526的内腔582。另外或可替代地,可以向近侧移动或拉动外鞘526,留下瓣膜500的至少一部分设置在心脏内。在一些实例中,耦合到瓣膜500的系绳536可以用于帮助将瓣膜500拉出外鞘526的内腔582。
如本文的其他实施例和305号pct申请的实施例所述,当外框架520不受外鞘526约束时,外框架520可以开始恢复到其膨胀或未反向配置。致动线材575-577可以用于控制外框架520的恢复。更具体地,在外框架520至少部分地设置在外鞘526的远侧端外部之后,可以向近侧拉动管构件503,使得(钉扎到管构件503的)致动线材以受控方式向近侧(与图40中所示的相同或相似)拉动外框架520的远侧设置的部分,并且使得可以控制外框架520从其相对于内框架550的反向配置恢复。
另外,在一些实例中,致动线材574-577可以帮助将瓣膜500铰接和放置到其目的地(例如心脏的房室瓣的自体体环)中。例如,在瓣膜500离开外鞘526并且处于其恢复的膨胀或部分膨胀配置之后,致动线材574-577还可以用于约束、收缩或以其他方式移动瓣膜500(例如径向压缩瓣膜500的外框架520)。更具体地,在该实施例中,具有钉扎到其上的致动线材574-577的管构件503可以由用户操纵,以通过向近侧拉动或移动管件503来将外框架520移动或推动到更加压缩的配置(与图41所示的相似或者相同)。例如,可能期望在完全部署瓣膜500之前将瓣膜500重新定位在心脏内。
在瓣膜500的外框架520被设置成处于其非反向且至少部分膨胀的配置并且在心脏内的期望位置中的情况下,可以部署内框架550。如在305号pct申请中针对瓣膜2100所描述的,为了将内框架550与瓣膜支座538解耦合,可以向远侧移动瓣膜支座538和/或可以向近侧移动内鞘508,使得瓣膜支座538设置在内鞘508的内腔583外部。如此,耦合器506可以从凹陷504释放,将内框架550从瓣膜支座538释放或与其解耦合。在一些实施例中,可以拉动系绳536以帮助将内框架550移出内鞘508。当内框架550从瓣膜支座538释放并设置在内鞘508外部时,内框架550可以呈现其偏置膨胀配置。
在内框架550从瓣膜支座538释放之前或之后,致动线材574-577也可以从外框架520释放或与其解耦合。为了使致动线材574-577与外框架520解耦合,致动线材574-577中的每个的一端可以从管构件503上拔掉或解耦合。例如,钉扎构件578-3可以从管构件503的凹槽向近侧抽出(与如输送系统1005中所示的并且关于其所描述的凹槽相同或相似),使得致动线材577的第二端和致动线材575的第二端各自从管构件503释放或拔掉,但保持分别由钉扎构件578-2和578-1钉扎。类似地,钉扎构件578-4可以从凹槽向近侧抽出,使得致动线材574的第二端和致动线材576的第二端可以各自从管构件503释放或拔掉,但保持分别由钉扎构件578-2和578-1钉扎。在致动线材575-577中的每个的一端耦合到管构件503(在该示例中经由钉扎构件578-1和578-2)的情况下,可以向近侧拉动管构件503,其转而将致动线材574-577的相对端从外框架520的环562中拉出。因此,在致动线材574-577与外框架520分开的情况下,外框架可以呈现偏置膨胀或部分膨胀配置。
尽管在上文的示例中,描述了钉扎构件578-3和578-4被抽出以释放致动线材574-577的末端,但是可替代地,可以抽出钉扎构件578-1和578-2,而留下由钉扎构件578-3和578-4钉扎的致动线材574-577。进一步地,致动线材574-577可以在手术内以任何合适的顺序或时间周期与外框架520解耦合。例如,在一些实例中,在瓣膜500至少部分地离开输送鞘526之后但在瓣膜500安置在房室瓣的自体体环内之前,可以期望释放致动线材574-577。在其他实例中,例如,在瓣膜500至少部分地离开外输送鞘526之后并且在瓣膜500安置在房室瓣的自体体环内之后,可以释放致动线材574-577。
在一些实例中,例如如图28所示,输送系统505'可以包括扩张器设备或构件511'。扩张器511'可以例如是球囊扩张器,并且可以被配置成例如在输送假体瓣膜500'期间使开口或通道膨胀。扩张器设备511'可以与扩张器设备1711相同或类似,并且可以以与305号申请关于图43至图48所描述的方式和图72的输送方法相同或相似的方式使用。输送系统505'可以包括与例如本文所述的输送系统505和/或输送系统1005和/或305号pct申请所述的输送系统的相同或相似的特征,并且功能也与其相同或相似。
在一些实施例中,假体心脏瓣膜(例如本文所述的和/或305号pct申请所述的任何假体心脏瓣膜)可以包括外框架,该外框架具有多排环,任何合适数目的致动器线材可以通过这些环进行布线和/或可滑动地设置(例如以控制外框架在从输送鞘部署和输送时的恢复轮廓和定时)。图29a和图29b图示了假体心脏瓣膜600和输送系统605的这种实施例,该输送系统605可以用于在与本文中关于其他实施例和305号pct申请中描述的实施例所描述的手术相同或相似的手术中在心脏内输送和部署假体心脏瓣膜600(在本文中也称为“瓣膜”)。因此,本文中不对关于瓣膜600的一些细节和与其一起执行的手术进行描述。应当理解,对于未具体讨论的特征和功能,那些特征和功能可以与本文中和/或305号pct申请中描述的瓣膜和/或输送系统部件相同或相似。例如,瓣膜600可以被构造成与本文和/或305号pct申请中描述的任何瓣膜相同或类似,并且与其功能相同或相似。例如,瓣膜600包括外框架组件以及内瓣膜组件,该外框架组件具有外框架620,该内瓣膜组件具有内框架650。如图29a和图29b所示,输送系统605包括外输送鞘626。输送系统605还可以包括图29a和图29b中未示出的其他部件和特征,诸如例如与内鞘508相似的内鞘、与本文所述的瓣膜支座538相似的瓣膜支座和/或关于本文中和305号pct申请的其他实施例描述的任何其他合适的部件和/或特征。
与本文所述的其他实施例和305号pct申请的实施例一样,瓣膜600可以从偏置膨胀配置移动到反向配置,用于将瓣膜600输送到心脏,如图29a所示。在该实施例中,瓣膜600被定位成用于经血管输送,类似于上文针对瓣膜500所描述的。因此,当以反向配置设置在鞘626内时,外框架设置在内框架的远侧。在该实施例中,外框架620包括第一排环662和第二排环664,通过这些环,致动线材674-679可以以与本文中关于瓣膜400和/或瓣膜1000和/或305号pct申请中关于瓣膜2100所描述的相同或相似的方式被旋紧。
在该实施例中,致动线材674-679从外框架620向近侧延伸、进入外输送鞘626的内腔682内并从外输送鞘626的近侧端伸出。在替代实施例中,致动器线材674-679可以以与本文关于输送系统505和/或输送系统1005所描述的相同或相似的方式由钉扎构件(图29a和图29b中未示出)钉扎到管构件。
在该实施例中,为了将瓣膜600输送到心脏,其中设置有瓣膜600的外输送鞘626的远侧端设置在心脏的左心房内。在外输送鞘626的远侧端部设置在心脏的左心房内的情况下,瓣膜600可以部署在外鞘626的外部。例如,瓣膜600可以在外鞘626的内腔600外部相对于外鞘626向外侧移动。另外或可替代地,可以向近侧移动或拉动外鞘626,而留下瓣膜600的至少一部分设置在心脏内。在一些实施例中,耦合到瓣膜600的系绳(未示出)可以用于帮助将瓣膜600拉出外鞘626的内腔682。
如先前实施例和305号pct申请的实施例所述,当外框架620不受外鞘626约束时,外框架620可以开始恢复到其膨胀或未反向的配置。致动线材674-679可以用于控制外框架620的恢复。更具体地,在外框架620至少部分地设置在外鞘626的远端外部之后,可以向近侧拉动致动器线材674-679的近侧端,这反过来向远侧拉动外框架620的开口端(致动线材674-679耦合到开口端),以帮助恢复外框架620。例如,如关于本文中和305号pct申请中的其他实施例所描述的,用户(例如医生)可以拉动致动器线材674-679的端部以反过来将外框架620移动到其恢复配置,如图29b所示。同样说,(耦合到外框架620的)致动线材以受控方式向近侧(与图40中所示相同或相似)拉动外框架620的远侧设置的部分,并且使得可以控制外框架620从其相对于内框架650的反向配置的恢复。如关于该实施例所示和所述的,具有多排环(例如第一排环662和第二排环664)提供了对外框架620从其反向配置的恢复的加强控制。
在该实施例中,外框架620具有两排环,每排具有12个环。然而,在替代实施例中,外框架可以具有任何合适数目的环和/或排环,使得外框架620可以受控方式恢复。例如,在一些替代实施例中,外框架可以具有3排或更多排环。进一步地,在一些实施例中,环可以与外框一体地或整体地形成,而在其他实施例中,环中的一个或多个可以与外框架分开形成并且耦合到外框架(例如缝合到外框架)。
另外,在一些实例中,致动线材674-679可以帮助将瓣膜600接合和放置到其目的地(例如心脏的房室瓣的自体体环)中。例如,致动线材674-679还可以用于在瓣膜600离开外鞘626并且处于恢复膨胀或部分膨胀配置之后约束、收缩或以其他方式移动瓣膜600(例如径向压缩瓣膜600的外框架620)。
在瓣膜600的外框架620被设置成处于其非反向且至少部分膨胀配置(参见例如图29b)并且处于心脏内的期望位置中的情况下,内框架650可以被部署并且允许呈现其有偏置膨胀配置。在部署内框架650之前或之后,致动线材674-679也可以从外框架620释放或与外框架620解耦合。为了使致动线材674-679与外框架620解耦合,可以向近侧拉动致动线材674-679中的每个的一端,这反过来将致动线材674-679的相对端拉出外框架620的环674。在致动线材674-679与外框架620分开的情况下,外框架可以呈现偏置膨胀或部分膨胀配置。
在一些实例中,致动线材674-679可以在手术内以任何合适的顺序或时间周期与外框架620解耦合。例如,在一些实例中,在瓣膜600已经至少部分地离开输送鞘626之后但在瓣膜600安置在房室瓣的自体体环内之前,可以期望释放致动线材674-677。在其他实例中,例如,在瓣膜600已经至少部分地离开外输送鞘626之后并且在瓣膜600安置在房室瓣的自体体环内之后,可以释放致动线材674-679。
对上文和305号pct申请中所描述的实施例描述为用于经股动脉输送。在其他实施例中,类似的输送设备和方法可以用于假体心脏瓣膜的经心尖输送。本文描述了以下装置和方法,用于诸如假体二尖瓣之类的假体心脏瓣膜的经心尖输送和部署,该假体心脏瓣膜可以被配置成移动到反向配置,用于将假体瓣膜输送到患者的心脏内。如本文所述,在一些实施例中,假体瓣膜包括外框架,当假体瓣膜处于偏置膨胀配置时,该外框架可以相对于内框架反向。假体二尖瓣可以由例如形状记忆材料形成。在使外框架反向之后,假体瓣膜可以插入输送鞘的内腔中,使得假体瓣膜移动到收缩配置。
输送鞘可以用于使用各种不同的输送途径将假体瓣膜输送到患者的心脏内,用于输送假体心脏瓣膜(例如假体二尖瓣),其中反向的假体瓣膜将通过心脏的心室进入心脏并且进入心脏的心房。例如,如本文关于30a至图30d和图31a和图31b进一步详细描述的,反向的假体瓣膜可以使用心尖途径输送,即通过心脏的左心室的顶点输送。
在已经将输送鞘布置在心脏的左心房内(例如经由心尖途径)之后,将假体二尖瓣向远侧移出输送鞘,使得反向的外框架恢复并且假体瓣膜呈现其偏置膨胀配置。然后,假体二尖瓣可以被定位在心脏的二尖瓣瓣环内。
图30a和图30b分别为根据实施例的假体心脏瓣膜700示为处于第一配置和第二配置的一部分的示意图。图30c和图30d分别图示了图30a和图30b的假体心脏瓣膜700示为设置在输送鞘726'和726的内腔内的各部分。图31a和图31b分别图示了假体心脏瓣膜700处于图30a和图30b的第一配置和第二配置的一部分,并且示出了处于第一配置和第二配置中的每个的假体心脏瓣膜的长度尺寸。假体心脏瓣膜700(在本文中也称为“假体瓣膜”或“瓣膜”)可以例如是假体二尖瓣。瓣膜700包括外框架720和内框架750。外框架720和内框架750各自形成为管状结构,该管状结构类似于上文关于先前实施例和/或参考305号pct申请中的假体瓣膜更详细描述的结构。外框架720和内框架750可以在围绕内框架750的周长和外框架720的周长设置的多个耦合接头746处耦合在一起。瓣膜700还可以包括其他特征,诸如本文中和/或305号pct申请中描述的那些特征中的任何特征。出于说明目的,仅关于图30a至图31b对内框架750和外框架720进行讨论。关于图30a至图31b所描述的瓣膜700的各种特点和特征可以适用于本文所述的任何假体瓣膜。
外框架720被配置成具有偏置膨胀或未变形的形状,并且可以被操纵和/或变形(例如压缩或约束),并且当释放时,返回到其原始(膨胀或未变形)形状。例如,外框架720可以由具有形状记忆特性的材料形成,诸如金属或塑料。关于金属,nitinol®被发现特别有用,因为它可以加工成奥氏体的、马氏体的或超弹性的。还可以使用其他形状记忆合金,诸如cu-zn-al-ni合金和cu-al-ni合金。内框架750可以由nitinol®的激光切割管形成。内框架750还可以具有偏置膨胀或未变形的形状,并且可以被操纵和/或变形(例如压缩和/或约束),并且当释放时,返回到其原始(膨胀或未变形)形状。
可以使用各种不同的输送途径在心脏的左心房内输送和部署瓣膜700,这些输送途径包括例如如下文更详细描述的经心尖输送途径或者例如经心房、经颈静脉或经股动脉途径。如上所述,在一些情形中,诸如当经由经心尖途径将假体瓣膜输送到心脏时,可以期望使用内腔相对较小的输送鞘,因此,在输送期间假体瓣膜的尺寸应当相应地构造尺寸。因此,期望具有这样的假体瓣膜,该假体瓣膜可以在用于植入心脏中(例如天然二尖瓣瓣环内)的偏置膨胀配置和具有较小的外周长或轮廓的输送配置之间重新配置,以允许在输送鞘的内腔内输送。假体瓣膜700和本文所述的假体瓣膜的实施例可以被构造和形成,以实现这些期望的功能和特点。
更具体地,瓣膜700可以具有偏置膨胀配置(如图30a和图31a所示)、反向配置(如图30b和图31b所示)以及压缩或收缩配置(如图30c和图31d所示)。膨胀配置允许瓣膜700在植入心脏内时起作用。瓣膜700可以移动到反向配置和压缩或收缩配置,用于将瓣膜700输送到患者的心脏。
为了使得瓣膜700能够移动到反向配置,外框架720可以以允许外框架720相对于内框架750移动的方式耦合到内框架750。更具体地,耦合接头746可以以允许外框架720相对于内框架750移动的方式耦合到内框架750。例如,在一些实施例中,耦合接头746可以被配置成允许外框架720相对于内框架750围绕耦合接头746旋转。在一些实施例中,耦合接头可以在外框架720和内框架750之间提供枢转耦合。在一些实施例中,耦合接头可以在外框架720和内框架750之间提供柔性附接。耦合接头746可以是如本文中参考假体瓣膜的各种实施例并入的305号申请所描述的各种不同的类型和配置。例如,耦合接头746可以包括活动铰链、柔性构件、缝合线、穿过开口缠绕的缝合线、穿过开口插入的销或突片或者其任何组合。
为了将瓣膜700从膨胀配置(图30a)移动到反向配置(图30b),通过使外框架720围绕耦合接头746移动(例如旋转、枢转、折曲),外框架720被移动到相对于内框架750的脱垂或反向配置,如图30b、图30d和图31b所示。瓣膜700的外框架720的弹性或超弹性结构也允许外框架720移动到并且设置成处于相对于内框架750的反向配置。为了使外框架720移动到相对于内框架750的反向配置,外框架720经由耦合接头746相对于内框架750向近侧折叠或反向(至图30b中的右侧)。如图30a和图31a所示,外框架720在反向之前处于相对于内框架750的第一位置,其中开口或自由端部716(也称为外框架720的心房部分716)设置在耦合接头746的远侧或者左侧并且在与内框架750的自由端部747(也称为内框架的第二端部)相同的方向上。当外框架720移动到反向配置时(即相对于内框架750的第二位置),自由端部716设置在耦合接头746的近侧(或图30b和图31b中的右侧)并且在与内框架750的自由端部747相反的方向上。换句话说,当瓣膜700处于偏置膨胀配置(例如图30a)时,耦合接头746设置在内框架750的第一端部744(也称为系绳耦合部)与内框架720的自由端部716之间。当瓣膜700处于反向配置时(例如图30b)(即外框架720已经移动到反向配置或位置),耦合接头746设置在内框架750的自由端部或第二端部747与外框架720的自由端部716之间。
当处于反向配置时,瓣膜700的整个长度增加,但内框架750的长度和外框架720的长度保持相同(或大体上相同)。例如,如图31a和图31b所示,处于偏置膨胀配置(在如图31a所示反向之前)的瓣膜700的整个长度l1小于处于反向配置(图31b)时的瓣膜700的整个长度l2。当瓣膜700处于偏置膨胀配置和反向配置时,内框架750的长度li和外框架720的长度lo大体上相同(或相同)。另外,在一些实例中,依据外框架的特定配置,当瓣膜700处于反向配置时,瓣膜700的整个外周长或外径可以更小。
在瓣膜700处于反向配置的情况下,瓣膜700可以放置在输送鞘726的内腔内,用于将瓣膜700输送到心脏的左心室和左心房,如图30d所示。当放置在输送鞘726的内腔内时,瓣膜700移动到收缩或压缩配置,其中瓣膜700的外径或外周长减小。因为瓣膜700处于反向配置,所以瓣膜700能够放置在比其他情形可能更小的输送鞘726内。例如,出于比较目的,图30c图示了放置在输送鞘726'的内腔内的瓣膜700,其中在设置在输送鞘726'内之前,瓣膜700尚未移动到反向配置。如图30c所示,当处于反向配置时,瓣膜700的外径减小,但是当放置在输送鞘726中时,不会小至瓣膜700的直径。因此,在图30c中,瓣膜700的整个外周长或外径为d1,并且在图30d中,瓣膜700的整个外周长或外径为d2,其小于d1。
因此,通过将外框架720设置成处于反向配置,瓣膜700可以收缩成更小的整个直径,即如果瓣膜700仅仅径向收缩的的话,放置在直径更小的输送鞘726中。这是因为当瓣膜处于偏置膨胀配置时,内框架750嵌套在外框架720的内部内,因此外框架720必须在内框架750周围收缩。在一些实施例中,内框架750和外框架同心设置。而在反向配置中,内框架750和外框架720相对于彼此轴向布置(即内框架没有嵌套在外框架750内),使得外框架720可以收缩,而不需要容纳其内部的内框架750的所有结构。换句话说,在内框架750大部分设置在外框架720内部或嵌套在外框架720内的情况下,框架结构的层或块不能被压缩到直径这么小。另外,如果框架是嵌套的,则结构的柔性较小,因此,需要更大的力来弯曲瓣膜,例如,以穿过曲折的解剖结构或进行转弯通过患者,以适当地定向用于插入二尖瓣瓣环中。
图32a是输送系统的侧视图的示意图,该输送系统可以用于例如使用经心尖途径在患者心脏内输送和部署假体心脏瓣膜。在该实施例中,输送系统805包括输送鞘826、扩张器870、长形构件880以及两根致动线材874和876。图32b是长形构件880的前视图的示意图。在该示意图中,仅示出了两根致动线材,但是在其他实施例中,可以仅使用一根致动线材或多于两根致动线材。
输送鞘826可以用于输送瓣膜800,瓣膜800包括内瓣膜组件840以及外框架组件810,内瓣膜组件840包括内框架(图32a和图32b中未标示),外框架组件810包括外框架(图32a和图32b未标示)。瓣膜800可以构造成与本文所述和/或305号pct申请中描述的假体瓣膜相同或类似,并且功能与其相同或类似,并且可以在部署或膨胀配置和其中如上所述外框架被设置成处于相对于内框架的反向位置的输送配置之间移动。如图32a所示,当瓣膜处于输送配置时,瓣膜800可以设置在输送鞘826的内腔内(即外框架相对于内框架反向并且当在输送鞘中时定位在内框架的近侧)。致动线材874、876可释放地耦合到外框架组件810。这样,在输送到并安置在患者心脏的自体体环内之后,致动线材874、876可以从外框架组件810释放并且从患者移除,留下假体心脏瓣膜植入患者的心脏内,如本文中更详细描述的。
扩张器870具有流体输送部分872和可收缩的扩张部分873(在本文中也称为“扩张部分”)。流体输送部分872被配置成接收流体并将流体输送到扩张部分873,以对扩张部分873充气。扩张部分873被配置成被充气,使得当被充气时,它可以随着输送系统805被引入患者的心脏而扩张(例如膨胀开口或通道)到心脏的一个或多个部分。例如,在经心尖输送途径期间使用时,扩张部分873当被充气时可以延伸到输送鞘826的远侧端外部并且为输送鞘826提供引入件并且帮助打开或扩大心外膜表面处的进入开口,并且很容易通过二尖瓣瓣环进入而不会使瓣膜的腱索缠绕。在将输送鞘826放置在心脏内的期望位置的情况下,可以对扩张器部分873放气并移除,留下输送鞘826在心脏内。
扩张部分873可以具有任何合适的形状或尺寸以扩张心脏的一部分(例如心脏的心尖部分中的切口),从而帮助将瓣膜800输送到心脏的心房。例如,在一些实施例中,扩张部分可以具有锥形和/或逐渐变尖的形状,其具有圆形或钝的远侧尖端。在其他实施例中,扩张部分可以具有圆形、椭圆形、三角形或其他合适的形状。尽管未示出,但是在一些实施例中,扩张器可以限定穿过其中的引导线材内腔。例如,在输送假体瓣膜期间,引导线材可以延伸通过心脏的心尖部分、穿过心脏的左心室并进入左心房。在这样的实施例中,扩张器可以在该引导线材之上旋紧以插入心脏中。引导线材可以是任何合适的尺寸。例如,在一些实施例中,引导线材的范围可以从大约0.03''引导线材到0.04''引导线材(例如0.035''引导线材)。于2014年10月29日提交的美国专利申请号14,527,382(“382号申请”)中描述了示例性扩张器设备,其全部公开内容通过引用并入本文。如本文更详细描述的,在将输送鞘826放置在心脏内的期望位置的情况下,可以对扩张器部分873进行放气(通过从其中移除流体)并沿着引导线材移除,留下输送鞘826在心脏内。
长形构件880可以用于翻转(flip)外框架组件810并且向心脏输送扩张器870的至少一部分并且从心脏缩回扩张器870的至少一部分。长形构件880限定扩张器内腔882,扩张器内腔882被配置成可滑动地接收扩张器870。更具体地,扩张器内腔882被配置成在放气时可滑动地接收输送部分872和扩张部分873,如本文中更详细描述的。长形构件880还限定了四个致动器线材内腔884(如图32b所示),这四个致动器线材内腔884与扩张器内腔882径向间隔开并且被配置成可滑动地接收致动器线材874、876。长形构件880可滑动地设置在输送导管826内并且通过内瓣膜组件840和外瓣膜组件810两者的中心部分。尽管未示出,但是在一些实施例中,长形构件880的尺寸可以变化,例如,其外径或周长可以在长形构件880的各个部分处增加和/或减小。例如,在一些实施例中,当长形构件880设置在输送鞘826内并延伸穿过瓣膜800的中心部分时,长形构件880在瓣膜800的近侧的一部分可以具有第一直径;并且长形构件880延伸穿过瓣膜800的中心部分(例如,内瓣膜组件840的小叶之间)的一部分可以具有小于第一直径的第二直径。这样,长形构件880被配置成穿过瓣膜800的一部分设置的部分的直径减小可以防止或减少长形构件880对瓣膜800的不期望的潜在干扰。类似地,扩张器870的部分(例如流体输送部分872)可以在尺寸(例如直径)上变化,其与长形构件880的尺寸变化相对应。
致动线材874、876可以使用各种不同的耦合方法耦合到外框架组件810的外框架。例如,外框架组件810的外框架可以包括环(图32a和图32b中未示出),通过该环,致动线材874、876可以被接收或旋紧。在并入本文的305号pct申请中(参见例如图57)并且关于图27描述了这种外框架。外框架上的环的数目可以变化,并且每根致动线材连接的环的数目可以变化。例如,在一些实施例中,外框架包括12个环,并且第一致动线材(例如致动线材874)通过其中的6个环旋紧,并且第二致动线材(例如致动线材876)通过其中的6个环旋紧。在其他实施例中,外框架可以包括12个环,并且可以存在4根致动线材,每根致动线材耦合到其中的3个环。在一些实施例中,单根致动线材通过外框架的所有环耦合。
为了在心脏内输送和部署假体瓣膜800,输送鞘826可以插入穿过患者心脏的心外膜表面(例如在心脏的顶点区域处或附近)并且延伸穿过心脏的左心室并且到达左心房。在将输送鞘826插入心脏之前,扩张器870的扩张部分873延伸到输送鞘826的远侧端的外部,可以将流体注射到流体输送部分872,从而对扩张器870的扩张部分873充气。扩张部分873的远侧端部(例如逐渐变尖的远侧端)可以为输送鞘826提供引入件并帮助打开或扩大心外膜表面处的进入开口并且通过二尖瓣瓣环。当输送鞘826放置在心脏内的期望位置时,流体可以至少部分地从扩张部分873抽出或移除,从而使扩张部分873放气,并且可以通过输送导管移除放气后的扩张部分873,留下输送鞘826、内瓣膜组件840和外框架组件810在心脏内。
在输送鞘826的远侧端设置在左心房内的情况下,通过向近侧抽出输送鞘826和/或使用推进器设备将瓣膜800推出输送鞘826的远侧端和/或使用长形构件880和致动线材874、876来帮助将瓣膜800拉出输送鞘826的远侧端,可以将瓣膜800移出输送鞘826的内腔。更具体地,在致动线材874、876耦合到外框架组件810的情况下,致动线材874、876的末端可以从外框架组件810向远侧延伸出输送鞘826的远侧端,然后经由由长形构件880限定的侧孔眼或孔886(在图32a中标示)进入长形构件880的致动线材内腔884。在一些实施例中,致动线材内腔延伸出长形构件880的远侧端中的开口,而非侧开口。换句话说,内腔884可以延伸到长形构件880的远侧端。致动线材874、876的末端然后可以向近侧延伸穿过长形构件880的致动线材内腔884并且延伸出长形构件880的近侧端和输送鞘826的近侧端。更具体地,每根线材874、876具有两个末端。第一末端保持在长形构件880的近侧端,而第二末端通过第一致动线材内腔884向远侧延伸、穿过外框架组件810的环(未示出)、返回通过第二致动线材内腔并且向近侧延伸出长形构件880的近侧端。因此,对于具有两根致动线材和四根致动线材内腔的实施例,致动线材的四个末端将在输送系统305的远侧端的近侧延伸或者耦合到输送系统的一部分(例如导管或手柄)。因此,用户(例如医生)可以拉动致动线材874、876的端部以反过来将外框架组件810拉出输送鞘826的远侧端,如下文更详细描述的。
在一些实施例中,致动线材874、876的端部从长形构件880的近侧端向近侧延伸并且可操作地耦合到手柄(未示出)。手柄可以由用户操纵以选择性地拉动和/或释放致动线材874、876。在一些实施例中,手柄可以包括一个或多个拨动开关或类似机构以帮助控制瓣膜800的过渡。这样,用户可以使用手柄选择性地将瓣膜800向远侧拉动并从输送鞘826中拉出,并选择性地控制外框架组件810的配置之间的翻转或过渡。在一些实施例中,致动线材的端部向近侧延伸穿过输送鞘的致动线材内腔并从长形构件的近侧端伸出,但仍然在输送鞘内。在这样的实施例中,手柄或功能类似的致动线材操纵器可操作地耦合到致动线材,并且可以被致动和/或操纵以选择性地拉动或释放致动线材,用于输送和/或部署瓣膜800,如上所述。
在瓣膜800的输送期间,当内瓣膜组件840离开输送鞘826的远侧端时,外框架组件810将处于相对于内瓣膜组件840的反向配置(类似于关于图30b所示和所述)。在内瓣膜组件840在输送鞘826的内腔外部之后,外框架组件810可以开始离开输送鞘826的内腔并且恢复到其膨胀或部署配置(类似于例如关于图30a所示)。在该实施例中,在瓣膜800被输送到心脏时,致动线材874、876可以用于选择性地(例如由操作者)辅助和/或控制瓣膜800的膨胀和恢复轮廓。例如,长形构件880的远侧端可以向远侧移出输送鞘826,并且可以向近侧拉动(或者可以操纵与其耦合的手柄)致动线材874、876的端部(向近侧伸出输送鞘826),其反过来相对于内框架向远侧拉动外框架的开口端,以帮助将外框架移动到其恢复的膨胀配置。因此,致动线材和长形构件880可以用于帮助操纵外框架组件810,以辅助和控制外框架组件810从其相对于内瓣膜组件840的反向配置到其膨胀或部署配置的过渡。这样,作为外框架组件810的瓣膜800的轮廓从其反向配置过渡到其恢复的膨胀或部署配置可以根据用户的需要选择性地最小化和/或以其他方式操纵。在瓣膜800在其配置之间的整个这种过渡过程中以及在输送和部署瓣膜800期间对其轮廓的这种控制可以促进更安全、更可重复且高效的瓣膜输送和部署手术。在一些实施例中,致动线材874、876可以由用户手动抓握以向近侧拉动致动线材。在一些实施例中,致动线材874、876可以可操作地耦合到输送系统805,使得用户不必手动处置致动线材。例如,致动线材可以耦合到输送系统805的输送鞘和/或手柄组件(未示出)。
在外框架组件810相对于内瓣膜组件840恢复使得瓣膜800以其部署配置设置在心脏的体环内的情况下,可以从心脏移除输送系统805。例如,致动线材874、876可以与外框架组件810解耦合并且经由长形构件880从心脏移除,并且可以从心脏抽出长形构件880和输送鞘826,留下瓣膜800植入心脏的体环内。更具体地,为了将致动线材874、876与外框架组件810解耦合并从患者移除致动线材874、876,可以向近侧拉动致动线材874、876的单个近侧端,使得向远侧拉动致动线材874、876的另一近侧端通过致动器线材内腔884、拉出长形构件880中的孔眼或孔886、穿过外框架820的环并向后拉出通过致动器线材内腔884。因此,在致动线材874、876用于促进心脏内的瓣膜800的输送和部署之后,致动线材874、876可以从长形构件880、输送鞘826和患者移除。
图33a是输送系统905的侧视图的图示,输送系统905可以用于利用例如经心尖途径将假体心脏瓣膜900输送和部署在患者的心脏内。输送系统905可以被构造成与例如输送系统805相同或相似,并且功能与其相同或相似。进一步地,瓣膜900可以被构造成与本文所述的任何假体瓣膜或305号pct申请中描述的任何假体瓣膜相同或相似,并且功能与其相同或相似,并且如本文中关于瓣膜800所描述的,可以在部署或膨胀配置与其中外框架处于相对于内框架的反向位置的输送配置之间移动。如图33a所示,瓣膜900被设置成处于其反向配置,并且在部署并植入心脏内之前径向约束在输送鞘内,如下文更详细描述的。进一步地,如图33b所示,瓣膜900在被输送到心脏之后并且在移除了致动线材和输送鞘之前被设置成处于恢复的部署配置。应当理解,对于未关于输送系统905具体讨论的特征和功能,那些特征和功能可以与输送系统805或本文中所描述的任何输送系统相同或相似。类似地,应当理解,对于未关于假体瓣膜900具体讨论的特征和功能,那些特征和功能可以与瓣膜800或305号pct申请中描述的任何瓣膜相同或相似。
输送系统905包括输送鞘926、扩张器970、长形构件980和两根致动线材974和976。图33c是长形构件980的远侧端视图。输送鞘926可以用于输送瓣膜900,瓣膜900包括内瓣膜组件940以及外框架组件910,内瓣膜组件940包括内框架(图33a中未标示),外框架组件910包括外框架(图33a中未标示)。
长形构件980可以用于帮助外框架组件910的翻转,并且向心脏输送扩张器的至少一部分并从心脏缩回该部分。如图33c所示,长形构件980限定扩张器内腔982,扩张器内腔982被配置成可滑动地接收扩张器970。更具体地,当对扩张器部分973放气时,扩张器内腔982被配置成可滑动地接收扩张器970。长形构件980还限定了四个致动器线材内腔984(如图33c所示),这四个致动器线材内腔984与扩张器内腔982径向间隔开并且被配置成接收致动线材974、976。长形构件980可滑动地设置在输送导管926内,并且通过内瓣膜组件940和外框架组件910两者的中心部分。在替代实施例中,长形构件可以限定任何合适数目的致动器线材内腔。例如,如图33d所示,长形构件980'可以限定与扩张器内腔982'径向间隔开的六个致动器线材内腔984'。类似于上文讨论的致动器线材内腔984,六个致动器线材内腔984'可以被配置成接收致动器线材(例如致动器线材974和976)。在又一些替代实施例中,致动器线材内腔可以被配置成接收任何合适数目的致动器线材。例如,在输送系统包括限定六个致动器线材内腔(例如致动器线材内腔984')的长形构件的一些实施例中,输送系统可以包括三根致动器线材。在这样的实施例中,在一些实例中,每根致动器线材可以通过两个致动器线材内腔进行布线。换句话说,第一致动器线材可以通过第一组两个致动器线材内腔进行布线;第二致动器线材可以通过第二组两个致动器线材内腔进行布线;第三致动器线材可以通过第三组两个致动器线材内腔进行布线。进一步地,长形构件可以具有任何合适的形状(例如圆形、椭圆形、三角形等)。例如,如图33d所示,长形构件980'是圆形的。
在该实施例中,如所示出的,致动线材974、976可以可释放地耦合到外框架组件910的外框架。例如,如图33a和图33b所示,致动线材974、976可以穿过环962,环962围绕外框架组件910的开口端部设置。更具体地,如上所述,每根致动线材974、976的第一端保持在长形构件980的近侧端,而第二端向远侧延伸通过第一致动线材内腔984、穿过外框架组件910的环962、返回通过第二致动线材内腔984并向近侧端延伸出长形构件980的近侧端(参见例如图33b)。
为了在心脏内输送和部署假体瓣膜900,输送鞘926可以插入穿过患者心脏的心外膜表面(例如在心脏的顶点区域处或附近)并且延伸通过心脏的左心室并且到达左心房。在将输送鞘926插入心脏之前,随着扩张器的扩张部分延伸到输送鞘926的远侧端的外部,可以将流体注射到流体输送部分972,从而对扩张器970的扩张部分973充气。扩张部分973的远侧端部(例如逐渐变尖的远侧端)可以为输送鞘926提供引入件并帮助打开或扩大心外膜表面处的进入开口并且通过二尖瓣瓣环。当输送鞘926放置在心脏内的期望位置时,流体可以至少部分地从扩张部分973抽出或移除,从而对扩张部分973放气,并且可以通过输送导管926移除放气后的扩张部分973,留下输送鞘926、内瓣膜组件940和外框架组件910在心脏内。
在输送鞘926的远侧端设置在左心房内的情况下,通过例如向近侧抽出输送鞘926和/或向远侧移动长形构件980并且使用致动线材974、976来帮助将瓣膜900拉出输送鞘926的远侧端,瓣膜900可以移出输送鞘926的内腔。如上文针对先前实施例所述,内瓣膜组件940将首先离开输送鞘926,然后离开外框架组件910。在不受输送鞘926的约束情况下,内瓣膜组件940和外框架组件910可以呈现其偏置膨胀配置。
为了翻转或恢复外框架组件910,长形构件980可以向远侧移出输送鞘926,如图33b所示。随着向远侧移动长形构件980,可以向近侧拉动致动线材974、976的近侧端,这将反过来向远侧拉动外框架组件910的开口端(致动线材974、976耦合到其上),以帮助恢复外框架。例如,如上所述,用户(例如医生)可以拉动致动线材974、976的端部,以反过来将外框架组件910移动到其恢复配置。在一些实施例中,致动线材974、976的端部从长形构件980的近侧端向近侧延伸并且可操作地耦合到手柄(未示出)。手柄可以由用户操纵以选择性地拉动和/或释放致动线材974、976。在一些实施例中,手柄可以包括一个或多个拨动开关或类似机构,以帮助控制瓣膜900的过渡。这样,用户可以使用手柄选择性地向远侧拉出瓣膜900并从输送鞘926中拉出,并选择性地控制外框架组件910的配置之间的翻转或过渡。在一些实施例中,致动线材的端部向近侧延伸通过输送鞘的致动线材内腔并从长形构件的近侧端伸出,但仍然在输送鞘内。在这样的实施例中,手柄或功能类似的致动线材操纵器可操作地耦合到致动线材,并且可以被致动和/或操纵以选择性地拉动或释放致动线材以用于输送和/或部署瓣膜900,如上所述。
如上所述,当瓣膜900离开输送鞘926的远侧端时,外框架组件910将处于相对于内瓣膜组件940的反向配置(类似于关于图30b示出和描述的)。在内瓣膜组件940在输送鞘926的内腔的外部之后,外框架组件910可以开始离开输送鞘926的内腔并且恢复到其膨胀或部署配置(如图33b所示)。在该实施例中,当瓣膜900被输送到心脏时,致动线材974、976可以用于选择性地(例如由操作者)辅助和/或控制瓣膜900的膨胀和恢复轮廓。例如,长形构件980的远侧端可以向远侧移出输送鞘926,并且可以向近侧拉动(或者可以操纵与其耦合的手柄)致动线材974、976的端部(向近侧伸出输送鞘926),这反过来相对于内框架向远侧拉动外框架的开口端,以帮助将外框架移动到其恢复的膨胀配置。因此,致动线材974、976和长形构件980可以用于帮助操纵外框架组件910,以辅助和控制外框架组件910从其相对于内瓣膜组件940的反向配置过渡到其膨胀或部署配置。这样,作为外框架组件910从其反向配置过渡到其恢复的膨胀或部署配置的瓣膜900的轮廓可以根据用户的需要选择性地最小化和/或以其他方式操纵。在瓣膜900在其配置之间的整个过渡期间以及在输送和部署瓣膜900期间对其轮廓的这种控制可以促进更安全、更可重复且高效的瓣膜输送和部署手术。在一些实施例中,致动线材974、976可以由用户手动抓握以向近侧拉动致动线材。在一些实施例中,致动线材974、976可以可操作地耦合到输送系统905,使得用户不必手动处置致动线材。例如,致动线材可以耦合到输送系统905的输送鞘和/或手柄组件(未示出)。
在外框架组件910相对于内瓣膜组件940恢复使得瓣膜900以其部署配置(如图33b所示)设置在心脏的体环内的情况下,可以从心脏移除输送系统905。例如,致动线材974、976可以与外框架组件910解耦合并且经由长形构件980从心脏移除,并且长形构件980和输送鞘926可以从心脏抽出,留下瓣膜900植入心脏的体环内。更具体地,为了使致动线材974、976与外框架组件910解耦合并从患者移除致动线材974、976,可以向近侧拉动致动线材974、976的单个近侧端,使得向远侧拉出致动线材974、976的另一近侧端通过致动器线材内腔984、穿过长形构件980中的侧孔眼或孔986(与对应的致动器线材内腔984连通的每个侧孔眼或孔986)、穿过外框架920的环962并且向后伸出通过致动器线材内腔984。这样,致动线材974、976可以在致动线材974用于促进瓣膜900在心脏内的输送和部署之后从长形构件980、输送鞘926和患者移除。
在一些实施例中,在瓣膜900已经输送和部署在心脏内之后,可以向远侧移动输送鞘926(在已经从长形构件980、输送鞘926和/或患者移除致动线材974、976之前和/或之后),以至少捕获瓣膜900的近侧部分或以其他方式至少与其啮合并且至少部分地收缩瓣膜的近侧部分。然后,输送鞘926可以用于在心脏内移动和/或重新定向(例如旋转、计时、使其成一角度)瓣膜900。例如,用户可以使输送鞘926绕其纵向轴线旋转,以反过来使瓣膜900绕其纵向轴线旋转。这样,例如当瓣膜900最初没有以适当方式植入时,用户可以确保瓣膜900适当地植入心脏内,而不必从心脏移除瓣膜900。
图34至图42图示了根据另一实施例的用于在心脏内输送和部署假体心脏瓣膜(诸如假体心脏瓣膜1000)的输送系统1005。假体心脏瓣膜1000(在本文中也称为“瓣膜”)可以被构造成与本文所述的任何瓣膜相同或相似,并且功能也与其相同或相似。因此,本文中没有对关于瓣膜1000的一些细节进行描述。如图34所示,瓣膜1000具有外框架组件1010、内瓣膜组件1040以及系绳1036,外框架组件1010具有外框架1020,内瓣膜组件1040具有内框架1050,系绳1036耦合到内框架1050。如上文针对先前实施例(例如瓣膜100、200、300等)所述,瓣膜1000的外框架1020和内框架1050可以各自用形状记忆材料形成并且具有偏置膨胀或部署配置。外框架1020和内框架1050可以移动到收缩或未部署的配置,用于将瓣膜1000输送到心脏,其中外框架1020相对于内框架1050反向。为了准备用于输送到心脏的瓣膜1000,瓣膜1000的外框架1020首先被设置成处于如图34所示的脱垂或反向配置。具体地,瓣膜1000的外框架1020的弹性或超弹性结构允许外框架1020被设置成处于如上文例如对于瓣膜100所述的相对于内框架1050的脱垂或反向配置。
例如,为了将外框架1020设置成相对于内框架1050处于其反向配置,外框架1020向远侧折叠或反向,使得外框架1020指向远离内框架1050。在外框架1020处于反向配置的情况下,瓣膜1000可以放置在输送系统1005的内腔内,如图34所示,用于将瓣膜1000输送到心脏的左心房。如上文所讨论的,通过将瓣膜1000的外框架1020设置成处于反向配置,瓣膜1000可以收缩成较小的整个直径,即,放置在比瓣膜1000当内框架1050和外框架1020彼此同心设置时径向塌缩的直径较小的输送鞘中。
在该实施例中,输送系统1005包括外输送鞘1026、内鞘1008、瓣膜支座1038(也称为“推动器”)和多内腔长形管构件1003(也称为作为“管”或“管构件”或“多内腔长形构件”)。如图34和图39至图41所示,管构件1003可移动地设置在由外输送鞘1026限定的内腔1082内。内鞘1008可移动地设置在内腔1082内和由管构件1003限定的内腔1080内。瓣膜支座1038可移动地设置在由内鞘1008限定的第一内腔1083和第二内腔1085内,第一内腔1083和第二内腔1085彼此流体连通。
为了将瓣膜1000部署在心脏内,首先移动瓣膜1000的外框架1020或使其置于其相对于内框架1050的反向配置。如图34所示,瓣膜1000的一部分放置在外鞘的内腔1082内,并且瓣膜1000的一部分放置在内鞘1008的内腔1083内。如上文针对先前实施例所描述的,当瓣膜1000放置在输送系统(例如外鞘1026和内鞘1008)内时,瓣膜1000可以被压缩或收缩成较小的配置(例如较小的外周长)。
内框架1050可以经由耦合器1006可释放地耦合到瓣膜支座1038,这些耦合器1006以与上文针对输送系统405所描述的方式相同的方式(参见例如图26a至图26c)接收在由瓣膜支座1038限定的对应凹陷1004内。这样,瓣膜支座1038可以用于保持瓣膜1000,以在瓣膜1000部署在心脏内时帮助控制和操纵它。另外,当瓣膜1000在输送鞘1026的内腔内移动时以及在部署在输送鞘1026的外部期间,瓣膜支座1038可以限制内框架1050的径向膨胀。如上文针对瓣膜400所描述的,内鞘1008的内径1082的可以被构造尺寸,使得当瓣膜支座1038和瓣膜1000设置在其中时,耦合器1006不能离开凹陷1004。换句话说,内鞘1008的内壁将耦合器1006维持在凹陷1004内。当瓣膜1000移动到内鞘1008的外部时,耦合器1006将能够自由地离开凹陷1004,使内框架1050从瓣膜支座1038释放。
在替代实施例中,瓣膜支座1038可以经由线材或缝合线可移除地耦合到瓣膜1000(例如瓣膜1000的内框架1050),该线材或缝合线可以在将瓣膜1000输送到心脏之后进行切割。在一些情况下,当瓣膜仍然设置在外输送鞘1026内时,瓣膜支座1038可以与瓣膜1000解耦合,而在其他实例中,瓣膜支座1038可以在瓣膜1000离开心脏内的输送鞘1026之后,与瓣膜1000解耦合。
尽管未示出,但是在其他实施例中,如针对先前实施例所描述的,瓣膜支座1038可以仅在部署期间接触并推动瓣膜1000,而无需将内框架1050固定到瓣膜支座1038上。在这样的实施例中,在一些实例中,当内框架1050设置在内鞘1008中时,内框架1050的径向膨胀可以受到内鞘1008的约束。
在该实施例中,第一致动线材1076、第二致动线材1074、第三致动线材1076和第四致动线材1077各自耦合到外框架组件1010。更具体地,外框架组件1010的外框架1020包括环1062,通过该环1062,致动线材1074-1077可以被旋紧或接收。在该实施例中,外框架1020包括12个环1062,并且每根致动线材1074-1077通过其中的三个环1062旋紧。在其他实施例中,外框架1020上可以设置不同数目的环,并且可以存在不同数目的致动器。进一步地,每根致动线材可以通过与针对该实施例所示出的数目不同的环被旋紧或接收。
当瓣膜1000设置在例如如图34所示的输送系统1005内时,致动线材1074-1077各自从外框架1020、在外鞘的内腔1082内并且沿着内鞘1008的外壁向近侧延伸,被收拢或放置在一个或多个密封件1081或其他保持设备后面,并且由长形钉扎构件1078-1、1078-2、1078-3、1078-4(统称为钉扎构件1078)钉扎到管构件1003。如下文更详细描述的,密封件1081可以被配置成使得致动线材1074-1077在致动和部署瓣膜1000期间可以相对于密封件1081滑动。
如图34和图39至图41所示,致动线材1074的第一端和致动线材1075的第一端由钉扎构件1078-2钉扎,而致动线材1076的第一端和致动线材1077的第一端由钉扎构件1078-1钉扎。致动线材1074的第二端和致动线材1076的第二端由钉扎构件1078-4(图34和图39至图41的部分剖视图中未示出)钉扎,而致动线材1075的第二端和致动线材1077的第二端由钉扎构件1078-3(图34和图39至图41的部分剖视图中未示出)钉扎。为了便于说明,致动线材的第二端在图34和图39至图41中被示为分开的。
图35是沿着图34中的线35-35截取的剖视图,并且图示了致动线材1074-1077的钉扎。为了说明的目的,致动线材1074-1077被示为没有附接到外框架上。图38a图示了致动线材1074并且代表其他致动线材1075-1077。图38b、图67b和图67c图示了被标示为1074'、1074''和1074'''的致动线材的替代实施例。如图38a所示,致动线材1074-1077各自包括致动线材的两端上的环,其由钉扎构件1078钉扎。在图38b中,钉扎构件可以在致动线材1074'的一端上钉扎较小的环,并且在致动线材1074'的相对端上钉扎较大的环的末端。在图38c中,致动线材2475''处于闭环形式,并且环的每端可以由钉扎构件钉扎。在图38d中,致动线材1074'''包括两个长形环和较小的中心环。在该实施例中,致动线材1074'''可以由三个钉扎构件钉扎,第一钉扎构件可以钉扎其中一个较大的环的末端,第二钉扎构件可以钉扎另一较大的环的末端,并且小环可以由第三钉扎构件钉扎。在图38b至图38d的每个实施例中,致动线材的两层将通过瓣膜的外框架的环或通过其旋紧。还可以使用其他替代配置。
如图36和图37a所示,多内腔管构件1003限定了四个钉扎构件内腔1079-1、1079-2、1079-3、1079-4(统称为钉扎构件内腔1079)。致动线材1074-1077的端部放置在由管构件1003限定的周向凹陷或凹槽1084内,其中钉扎构件1078通过致动线材1074-1077的末端上的环接收,将致动线材1074-1077钉扎到管构件1003。因此,在心脏内部署瓣膜1000期间,用户(例如医生)可以使用致动线材1074-1077所耦合的管构件1003来控制和/或操纵瓣膜1000的移动,如下文更详细描述的。
图37b和图37c图示了多内腔管构件1103的替代实施例,多内腔管构件1103可以与如图37b所示的远侧保持元件1186或如图37c所示的远侧保持元件1286一起使用。远侧保持元件1186和1286可以被设置成邻接多内腔管构件1103的远侧端并且可以至少部分地限定凹陷区域以接收致动线材的环端,并且在输送和部署假体瓣膜期间,可以为多内腔管构件1103提供增强的整体强度和耐用度。远侧保持元件1186、1286可以由与多内腔管构件1103相同或不同的材料形成。在一些实施例中,期望远侧保持元件1186、1286可以由强度特性大于多内腔管构件1103的材料形成。例如,远侧保持元件1186、1286可以由金属或刚性塑料形成。
如图37b和图37c所示,多内腔管构件1103(本文中也称为“管构件”)可以限定中心内腔1180和多个钉扎构件内腔,其包括如图37b和图37c所示的钉扎构件内腔1179-3和1179-4(统称为1179),其可以分别在其中接收钉扎构件,诸如钉扎构件1078-3和1078-4。尽管未示出,但是管构件1103还可以限定钉扎构件内腔,其可以接收如针对图36中的管构件1003所示的钉扎构件1078-1和1078-2。
如图37b所示,远侧保持元件1186可以接收在内腔1180内并且可以限定内腔1187,通过该内腔1187,可以可滑动地接收瓣膜支座1038。尽管未示出,但是远侧保持元件1186可以使用各种不同的耦合方法耦合到管构件1103。例如,在一些实施例中,远侧保持元件1186可以粘结到管构件1103。在一些实施例中,远侧保持元件1186可以包括一个或多个特征,诸如倒钩,其允许它被插入到管构件1103中但不会被移除。在一些实施例中,远侧保持元件1186可以包括与管构件1103的对应特征互锁的凹口和/或管构件1103可以在保持元件1186上回流或模制。各种其他耦合方法和/或稳固策略组合可以用于将远侧保持元件1186耦合到管构件1103。在一些实施例中,远侧保持元件1186可以在管构件1103的内腔1180内向近侧延伸并且在管构件1103的近侧端部处耦合。
远侧保持元件1186还限定钉扎构件内腔1169,钉扎构件内腔1169与多内腔管构件1103的钉扎构件内腔1179对齐,使得钉扎构件1078可以接收在其中。近侧肩部1188可以被设置成邻接多内腔管构件1103的远侧端。远侧保持元件1186还限定了周向凹陷区域1184,周向凹陷区域1184在近侧肩部1188和远侧保持元件1186的远侧端部之间限定。如图37b所示,致动线材1074-1077的环端可以被接收在凹陷区域1184内并且由如上文针对多内腔管构件1003所描述的钉扎构件1078钉扎。
图37c图示了被设置成邻接多内腔管构件1103的远侧端的远侧保持元件1286。与先前实施例一样,远侧保持元件1286可以被接收在内腔1180内并且可以限定内腔1287,通过该内腔1287,可以滑动地接收瓣膜支座1038。远侧保持元件1286可以以与上文针对远端保持元件1186所描述的方式相同的方式耦合到管构件1103。远侧保持元件1286还包括近侧肩部1288,近侧肩部1288被配置成邻接多内腔管构件1103的远侧端。远侧保持元件1286还限定了周向凹陷区域1284,周向凹陷区域1284可以接收致动线材1074''-1077''的环端,这些环端可以由钉扎构件1078(图37中所示的1078-3和1078-4)钉扎。在该示例中,致动线材被配置为闭环,如针对图38c中的致动线材1074''所示。
将瓣膜1000输送到心脏的手术可以与本文中、上文通过引用并入的572号pct申请和/或305号pct申请中所描述的任何手术相同或相似。例如,以反向配置设置在输送系统1005内的瓣膜1000可以以与本文中关于其他实施例和/或参考305号pct申请的图43至图48所描述的相同或相似的方式输送到心脏的左心房。在输送鞘1026的远侧端部设置在心脏的左心房内的情况下,瓣膜1000可以部署在输送鞘1026的外部。例如,如图39所示,内鞘1008、瓣膜支座1038和管构件1003可以相对于外鞘1026向远侧移动,将瓣膜1000移出或推出外鞘1026的内腔1082。另外或可替代地,可以向近侧移动或拉动外鞘1026,留下瓣膜1000的至少一部分设置在心脏内。在一些情况下,耦合到瓣膜1000的系绳1036可以用于帮助将瓣膜1000拉出外鞘1026的内腔。
如上文针对先前实施例所述,当外框架1020变得不受外鞘1026约束时,外框架1020可以开始恢复到其膨胀或未反向配置。致动线材1075-1077可以用于控制外框架1020的恢复。更具体地,可以向近侧拉动管构件1003,使得(钉扎在管构件1003的)致动线材以受控方式向近侧(如图40所示)拉动外框架1020的远侧设置的部分,并且使得可以控制外框架1020从其相对于内框架1050的反向配置的恢复。
另外,在一些实例中,致动线材1074-1077可以协助将瓣膜1000接合和放置到其目的地(例如心脏的房室瓣膜的自体体环)中。例如,如图41所示,在瓣膜1000离开外鞘1026并且处于其恢复的膨胀或部分膨胀配置之后,致动线材1074-1077还可以用于约束、收缩或以其他方式移动瓣膜1000(例如径向压缩瓣膜1000的外框架1020)。更具体地,在该实施例中,其上钉扎有致动线材1074-1077的管构件1003可以由用户操纵以通过向近侧拉动或推动管构件1003来将外框架移动或推动到更加压缩的配置(如图41所示)。例如,这可能期望在完全部署瓣膜1000之前将瓣膜1000重新定位在心脏内。
回到图40,当瓣膜1000的外框架1020被设置成处于其非反向且至少部分膨胀配置并且处于心脏内的期望位置时,可以部署内框架1050。如上文针对瓣膜400所描述的,为了使内框架1050与瓣膜支座1038解耦合,可以向远侧移动瓣膜支座1038和/或可以向近侧移动内鞘1008,使得瓣膜支座1038设置在内鞘1008的内腔1083外部。如此,耦合器1006可以从凹陷1004释放,从而使内框架1050从瓣膜支座1038释放或与其解耦合。在一些实施例中,可以拉动系绳1036以帮助将内框架1050移出内鞘1008外。当内框架1050从瓣膜支座1038释放并设置在内鞘1008外部时,内框架1050可以呈现其偏置膨胀配置。
在内框架1050从瓣膜支座1038释放之前或之后,致动线材1074-1077也可以从外框架1020释放或解耦合。为了使致动线材1074-1077与外框架1020解耦合,每根致动线材1074-1077的一端可以从管状构件1003拔掉或与管状构件1003解耦合。例如,如图42所示,可以从凹槽1084向近侧抽出钉扎构件1078-3(参见图35),使得致动线材1077的第二端和致动线材1075的第二端各自从管构件1003释放或拔掉,但仍然分别由钉扎构件1078-2和1078-1钉扎。类似地,可以从凹槽1084向近侧抽出钉扎构件1078-4(参见图35),使得致动线材1074的第二端和致动线材1076的第二端可以各自从管构件1003释放或拔掉,但仍然分别由钉扎构件1078-2和1078-1钉扎。在每根致动线材1075-1077的一端耦合到管构件1003(在该示例中,经由钉扎构件1078-1和1078-2)的情况下,可以向近侧拉动管构件1003,这反过来将致动线材1074-1077的相对端拉出外框架1020的环1062。因此,在致动线材1074-1077与外框架1020分开的情况下,外框架可以呈现偏置膨胀或部分膨胀配置。
尽管在上文的示例中,示出了钉扎构件1078-3和1078-4被抽出以释放致动线材1074-1077的末端,但是可替代地,钉扎构件1078-1和1078-2可以被抽出,从而使致动线材1074-1077由钉扎构件1078-3和1078-4钉扎。进一步地,致动线材1074-1077可以在手术内以任何合适的顺序或时间周期与外框架1020解耦合。例如,在一些实例中,期望在瓣膜1000至少部分地离开输送鞘1026之后但在瓣膜1000安置在房室瓣膜的自体体环内之前,可以释放致动线材1074-1077。在其他实例中,例如,在瓣膜1000至少部分地离开外输送鞘1026之后并且在瓣膜1000安置在房室瓣膜的自体体环内之后,可以释放致动线材1074-1077。
图43是图示了在心脏内输送和部署假体瓣膜的方法的流程图。该方法包括:在1300处,插入输送鞘的远端通过心脏的心尖区域并进入心脏的心房。输送鞘具有假体心脏瓣膜,该假体心脏瓣膜设置在输送鞘的内腔内。假体心脏瓣膜包括外框架和耦合到外框架的内框架。外框架可在相对于内框架的第一位置和相对于内框架的第二位置之间移动,外框架相对于内框架反向。假体瓣膜设置在输送鞘的内腔内,其中外框架在插入期间处于相对于内框架的第二位置。在1302处,假体心脏瓣膜向远侧移出输送鞘。在1304处,假体心脏瓣膜的外框架过渡到相对于内框架的第一位置,使得假体心脏瓣膜至少部分地呈现偏置膨胀配置。在1306处,假体心脏瓣膜定位在心脏的体环内。
图44是图示了在心脏内输送和部署假体瓣膜的方法的流程图。在1400处,将输送鞘的远侧端部插入心脏的心房。输送鞘具有假体心脏瓣膜,该假体心脏瓣膜设置在输送鞘的内腔内。假体心脏瓣膜包括外框架和耦合到外框架的内框架。外框架可在相对于内框架的第一位置和相对于内框架的第二位置之间移动,外框架相对于内框架反向。假体心脏瓣膜设置在输送鞘的内腔内,其中外框架在插入期间处于相对于内框架的第二位置,并且至少部分地轴向地设置在内框架的近侧。在1402处,假体心脏瓣膜向远侧移出输送鞘。在1404处,假体心脏瓣膜的外框架过渡到相对于内框架的第一位置,使得假体心脏瓣膜至少部分地呈现偏置膨胀配置。在1406处,假体心脏瓣膜定位在心脏的体环内。
虽然上文已经描述了各种实施例,但是应当理解,它们通过仅示例但不限制的方式进行呈现。尽管上文所描述的方法表明了以一特定次序发生某些事件,但是可以修改某些事件的排序。附加地,当可能时,某些事件可以在并行过程中同时执行,以及如上所述依序执行。
尽管上文所描述的示意图和/或实施例表明了以某些方位或位置布置的某些部件,但是可以修改部件的布置。虽然已经具体示出和描述了实施例,但是应当理解,可以在形式和细节上进行各种改变。除了互斥组合之外,本文中所描述的装置和/或方法的任何部分还可以以任何组合进行组合。本文中所描述的实施例可以包括所描述的不同实施例的功能、部件和/或特征的各种组合和/或子组合。
例如,尽管没有针对每个实施例进行具体描述,但是输送系统的任何实施例可以包括诸如球囊扩张器构件之类的扩张器设备或构件。进一步地,本文中所描述的假体心脏瓣膜可以使用如关于305号pct申请的图43至图48和图72所述的心外膜垫设备固定到心脏。而且,尽管未针对每个实施例进行示出,但是输送设备或系统的任何实施例可以包括瓣膜支座或瓣膜推动器,该瓣膜支座或瓣膜推动器被配置成在输送瓣膜期间将瓣膜推动出输送鞘的远侧端。
进一步地,尽管未示出,但是输送设备或系统的任何实施例可以包括手柄或手柄组件,各种输送鞘和组件可操作地耦合到该手柄或手柄组件,并且用户(例如医生)可以抓握并使用该手柄或手柄组件来操纵输送设备或系统。
另外,本文中所描述的系统和方法还可以适用于假体三尖瓣。例如,在这种情况下,可以将手术导管插入心脏的右心室,并且将输送鞘直接(经心房)或经由颈静脉或股静脉输送到心脏的右心房。
另外,本文中所描述的系统和方法还可以适用于与假体三尖瓣一起使用。例如,在这种情况下,输送鞘可以经心尖输送到心脏。
- 还没有人留言评论。精彩留言会获得点赞!