用于增强组合物递送的方法和装置与流程
本申请要求2016年10月20日提交的美国临时专利申请序列号62/410,685的权益,该临时专利申请据此全文以引用方式并入本文。
本发明涉及一种用于增强组合物递送的方法和装置。
背景技术:
目前用于治疗体内(血管或移植物)闭塞的方法和装置采用球囊导管或支架将药物递送到血管内部。药物洗脱支架提供的优点是,该装置可以被设计成通过改变药物洗脱曲线而将药物的递送延长数周或数月,但在大多数情况下却留下了金属支架。涂覆药物的球囊提供了不留下任何东西的优点,然而,由于在递送药物时血管被球囊闭塞这一事实,药物被递送较短的时间段。
在这两种装置中,递送的主要机制是药物简单地扩散到血管壁中,并且在流动状态下经受药物洗出。此外,由于简单扩散是递送的主要机制,所以在这两种装置中,药物经表面递送到血管壁上。
技术实现要素:
一种利用射频能量来增强组合物向患者身体区域递送的方法包括将耦合到射频能量源的第一电极和第二电极引导到该身体区域附近的位置。从第一电极和第二电极中的至少一者提供从射频能量源到该身体区域的经调制脉冲形式的射频能量,以提供被配置成增强该组合物的递送的递送条件。使用组合物递送元件将该组合物递送到该身体区域附近。
一种利用射频能量来增强组合物向患者身体区域递送的装置包括具有近侧端部和远侧端部的第一纵向构件,该第一纵向构件的至少一个内腔在该近侧端部与该远侧端部之间延伸。组合物递送元件位于该纵向构件的远侧端部处。该组合物递送元件具有涂覆在其外表面上的组合物。至少两个电极耦合到射频源并位于该组合物递送元件内。这些电极是绝缘的,使得至少两个电极能够产生电场以增强组合物向身体区域的递送。
此技术提供了许多优点,包括提供用于将组合物递送到身体区域的更有效果且更有效率的装置和方法。此技术的装置和方法允许组合物在身体区域部位内保持延长的时间段,以提供增强的治疗。特别地,使用由射频能量或其他能量源产生的空化、冲击波、电穿孔等有助于递送组合物。本发明的技术有利地提供了一种用于将药物递送到血管壁或闭塞中以使得药物在目标部位内保持较长的时间段而不留下任何东西的增强方法。药物在目标部位内长效作用可以改善结局(例如降低再闭塞率、再狭窄率或血运重建率)。
附图说明
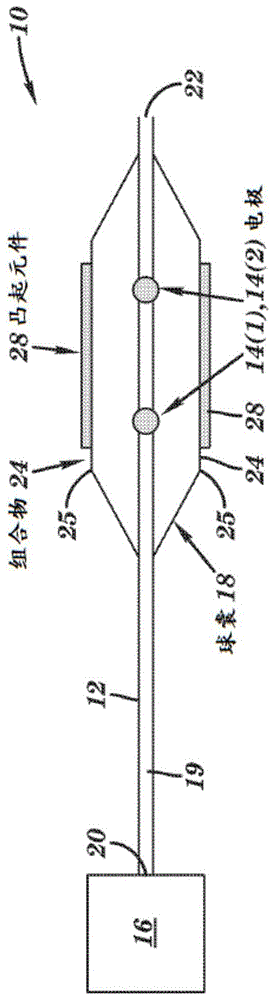
图1是本发明技术的使用射频能量进行组合物递送的示例性装置的示意图。
图2是位于具有闭塞的身体区域中的本发明技术的使用射频能量进行组合物递送的另一示例性装置的示意图。
图3是位于具有闭塞的身体区域中的本发明技术的使用射频能量进行组合物递送的另一示例性装置的示意图。
图4是图3中所示的用于组合物递送的装置的替代性实例的示意图。
图5是图1中所示的使用射频能量进行组合物递送的示例性装置的示意图,展示了电极与射频能量源之间的示例性耦合。
图6是图5的纵向构件的示意性端视图,该纵向构件具有两个耦合的绝缘电极。
图7是用另一示例性组合物递送元件进行组合物递送的示例性装置的示意图。
图8是用于将示例性凸起元件固定到可以与本发明技术的组合物递送装置一起使用的示例性组合物递送元件的配置的示意图。
图9a至图9c展示了使用射频能量来增强组合物递送的示例性方法。
图10展示了具有带多孔表面的组合物递送元件的另一示例性组合物递送装置的示意图。
图11展示了在非闭塞血管内使用射频能量进行等离子体介导消融的效果。
具体实施方式
图1和图5展示了利用射频能量来增强组合物向患者身体区域的递送的示例性组合物递送装置10。尽管描述了射频能量,但也可以利用其他能量形态,举例而言,诸如超声能量或激光能量。组合物递送装置10包括:第一纵向构件12,该第一纵向构件包括电极14(1)和14(2);射频能量源16;以及组合物递送元件18,但该组合物递送装置10可以在其他配置中包括其他类型和/或数目的元件、部件和/或装置,诸如附加电极和/或纵向构件。该示例性技术提供了许多优点,包括向患者身体内的区域更有效果且更有效率地递送组合物。
更具体地参照图1,组合物递送装置10包括第一纵向构件12,该第一纵向构件被配置成推进到患者身体中并且位于患者的身体区域附近。该身体区域可以是身体中的各种区域,包括器官、身体内腔或体腔,诸如各种导管或脉管、血管、移植物、腺体。在一个实例中,该身体区域可以是包括需要治疗的闭塞或肿瘤的体内区域。在该实例中,第一纵向构件12包括在该第一纵向构件12的近侧端部20与远侧端部22之间延伸的内腔19,但该纵向构件12可以包括附加的内腔。内腔19被配置成在其中接纳附加的纵向构件,仅举例而言,诸如导丝、导管、微导管或探针。
在该实例中,纵向构件12具有位于其上的电极14(1)和14(2),以提供电极14(1)和14(2)的双极性布置,但电极14(1)和14(2)在其他配置中可以位于其他元件上以提供双极性布置。
在另一个实例中,如图2所示,组合物递送装置10还包括第二纵向构件13,该第二纵向构件被配置成插入到第一纵向构件12的内腔19中,以便在患者的身体区域附近递送。在该实例中,第二纵向构件13是导丝或导管,电极14(1)和14(2)位于其上以提供双极性布置。
在又一个实例中,如图3所示,组合物递送装置10还包括第三纵向构件23,该第三纵向构件被配置成插入到第一纵向构件的内腔19中。仅举例而言,第三纵向构件23可以是导丝或导管。第二纵向构件13和第三纵向构件23是独立的、不重叠的导丝或导管,可以如下所述沿相同方向或相反方向递送到身体区域。
在另一个实例中,电极14(1)或14(2)中的一个位于贴片上,该贴片可以靠近患者的待治疗的身体区域放置在该患者的皮肤上。将贴片紧靠该身体区域放置,以允许实现电极14(1)与14(2)之间的双极性布置。
现在参照图4,在一个实例中,第一纵向构件12的内腔19包括多个内腔区段,以将第二纵向构件13和第三纵向构件23分开递送到身体区域。在又一个实例中,第二纵向构件13可以被配置成接纳第三纵向构件23,使得第三纵向构件23位于第二纵向构件13内。再次参照图3,在该实例中,电极14(1)和14(2)分别位于第二纵向构件13和第三纵向构件23上,以便提供双极性布置。
在一个实例中,电极14(1)和14(2)可以是球囊标记,但也可以利用其他类型的电极。参照图5,电极14(1)和14(2)经由导线17(1)和17(2)耦合到射频能量源16。导线17(1)和17(2)以螺旋构型围绕第一纵向构件12缠绕。导线17(1)和17(2)从射频能量源16递送射频能量,以向身体区域提供射频能量,但也可以采用被配置成供应其他能量形态的其他能量源。
现在参照图6,电极14(1)和14(2)是绝缘的,诸如具有介质阻挡层,使得这两个电极14(1)和14(2)能够在身体区域中产生电场。另外,选择绝缘以允许电极14(1)和14(2)能够承受在电极14(1)和14(2)周围产生等离子体放电。电极14(1)和14(2)还可以具有位于电极14(1)和14(2)的暴露部分处的介质阻挡层,以进一步有助于承受等离子体产生。
再次更具体地参照图1和图5,射频能量源16提供通过电极14(1)和14(2)递送到身体区域的射频能量源,但也可以采用其他能量形态。在一个实例中,射频能量源16向电极14(1)和14(2)提供经调制的射频能量脉冲。在一个实例中,射频能量源16被配置成提供脉冲宽度介于约0.05微秒至约500微秒之间的经调制脉冲,但也可以采用脉冲宽度小于0.05微秒或介于500微秒与1秒之间的经调制脉冲。射频能量源16还可以被配置成以脉冲群的形式提供经调制脉冲。仅举例而言,每个经调制脉冲群都可以具有介于2个与10个之间的脉冲。在另一个实例中,经调制脉冲被分组成脉冲串,仅举例而言,这些脉冲串的脉冲串宽度介于100ms至1s之间,并且每个脉冲串之间的间隔介于1ms至100ms之间。
射频能量源16在介于400v至4000v之间的电压下提供射频能量,但在一些实例中可以利用小于400v的电压。射频能量源16能够以在身体区域中产生递送条件的水平提供射频能量,该递送条件增强组合物的递送,诸如空化、微射流、冲击波、电刺激或化学反应。在一个实例中,射频能量源16提供能量以产生瞬时大小介于0.1mpa至20mpa之间的冲击波。在另一个实例中,射频能量源16提供能量以便在身体区域中产生直径介于1μm与10mm之间的一个或多个空化囊泡区域。可以使用组合物递送装置10由递送至身体区域的组合物形成这些空化囊泡。
再次更具体地参照图1和图5,组合物递送装置10还包括位于第一纵向构件12的远侧端部22处的组合物递送元件18。组合物递送元件18包括待递送至身体区域的组合物的组合物层24,该组合物层位于该组合物递送元件18的表面25上。组合物层24涂覆在组合物递送元件18的表面25上并且/或者嵌入该表面内。仅举例而言,施加组合物层24的方法可以包括喷涂、浸涂、气相沉积、等离子体沉积、使用化学键合或使用电学键合。
在另一个实例中,组合物并非被放置在组合物递送元件的外部上,而是被注射到组合物递送元件18的内部。组合物递送元件18包括孔50,这些孔允许组合物通过孔50逸出并被递送到身体区域(诸如闭塞或血管壁)中,如图10所示。如下面进一步描述的,通过激活射频能量来增强这种对组合物的递送。在另一个实例中,组合物作为带电化合物位于组合物递送元件上。然后以相似的电荷递送射频能量,使组合物从组合物递送元件18被排斥到组织中。除此之外或作为替代,可以通过添加带电部分来修饰电中性治疗剂,使得包含带电部分的经修饰治疗剂可以更容易受到能量场的影响。除此之外,治疗剂可以浸没或溶解在导电流体中,由此如上所述在能量场影响下的导电流体路径用作促进治疗剂向治疗区域递送的载体。举例而言,可以使用治疗贫血的药物。
该组合物是治疗剂或药物化合物。可以与组合物递送装置一起使用的组合物的非限制性实例包括血栓溶解剂、纤维蛋白溶解酶、凝血酶抑制剂、抗血小板剂、抗凝血剂、抗再狭窄剂或抗癌剂,但也可以使用组合物递送装置10来递送其他治疗剂或药物化合物。该组合物可以是药物、气体或液体,这些物质可以对目标身体区域产生影响。作为一个实例,该组合物可以是紫杉醇或取自limus家族药物的药物,并且可以用于递送到闭塞的血管体,以减小这种血管再闭塞或再狭窄的可能性。
预期本发明的实施方案可以用于递送其他治疗剂或其他生物活性物质,包括但不限于:氨基酸、合成代谢物、镇痛剂和拮抗剂、麻醉剂、驱虫剂、抗肾上腺素剂、抗哮喘剂、抗动脉粥样硬化剂、抗菌剂、抗胆固醇剂、抗凝血剂、抗抑郁剂、解毒剂、止吐剂、抗癫痫药、抗纤维蛋白溶解剂、抗炎剂、抗高血压剂、抗代谢剂、抗偏头痛剂、抗真菌剂、止恶心剂、抗肿瘤剂、抗肥胖剂、抗帕金森病剂、抗原生动物剂、抗精神病剂、抗风湿剂、防腐剂、抗癫痫剂、抗病毒剂、细菌疫苗、生物类黄酮、钙通道阻滞剂、毛细管稳定剂、凝血剂、皮质类固醇、用于抑制细胞生长治疗的解毒剂、造影剂(如造影剂、放射性同位素和其他诊断剂)、电解质、酶、酶抑制剂、神经节苷脂和神经节苷脂衍生物、止血剂、激素、激素拮抗剂、安眠剂、免疫调节剂、免疫刺激剂、免疫抑制剂、矿物质、肌肉松弛剂、神经调节剂、神经递质和促智药、渗透性利尿剂、副交感神经阻断剂、副交感神经拟似剂、肽、蛋白质、呼吸兴奋剂、平滑肌松弛剂、交感神经阻断剂、交感神经拟似剂、血管扩张剂、血管保护剂、用于基因疗法的载体、病毒疫苗、病毒、维生素等。
在该实例中,组合物递送元件18是具有多孔表面25的可扩张球囊,组合物层24施加到该多孔表面上,但也可以利用其他组合物递送元件,诸如可扩张导管、或支架。在另一个实例中,举例而言,组合物递送元件18可以是由该组合物填充的微泡,这些微泡通过第一纵向构件12的内腔19被递送到身体区域。在另一个实例中,如图7所示,组合物递送元件18包括组合物位于其上的多个可扩张肋件。
现在再次更具体地参照图1和图5,组合物递送元件18(诸如球囊)包括位于其表面25上的一个或多个凸起元件28。凸起元件28被配置成同时刻划或切割身体区域,诸如闭塞,使得组合物可以更容易地扩散到组合物递送元件18插入其中的区域中。凸起元件28可以包括位于组合物递送元件18上的纵向元件或周向元件。在一个实例中,凸起元件28具有三角形横截面,但也可以利用其他配置。举例而言,凸起元件28由金属或聚合物构成,但也可以利用其他材料。组合物层24可以直接施加到组合物递送元件18的凸起元件28上。在该实例中,凸起元件28直接联接到组合物递送元件12。作为替代,现在参照图8,凸起元件28可以直接联接到第一纵向构件12,但也可以利用其他配置。
现在将参考图1至图8来描述利用射频能量来增强组合物向患者身体区域的递送的方法的实例。首先,将包括组合物递送元件18的纵向构件12递送到待治疗患者的身体区域,该组合物递送元件具有位于表面25上的组合物层24。该身体区域可以是身体中的各种区域,诸如器官、身体内腔或体腔,诸如各种导管或脉管、血管、移植物、腺体。在一个实例中,该身体区域可以是包括需要治疗的闭塞或肿瘤的体内区域。组合物层24可以涂覆或嵌入在组合物递送元件18的表面25上,但在其他实例中,组合物层24可以位于从组合物递送元件18的表面25突伸出的凸起元件(诸如可扩张球囊)上。
一旦位于身体区域中,组合物递送元件18就可以扩张,以将组合物层24施加到身体区域。该组合物是治疗剂或药物化合物。可以与组合物递送装置一起使用的组合物的非限制性实例包括血栓溶解剂、纤维蛋白溶解酶、凝血酶抑制剂、抗血小板剂、抗凝血剂、抗再狭窄剂或抗癌剂,但也可以使用组合物递送装置10来递送其他治疗剂或药物化合物。
接下来,将耦合到射频能量源16的第一电极14(1)和第二电极14(2)引导到身体区域附近的位置。在一个实例中,纵向构件12具有位于其上的电极14(1)和14(2),如图1和图5所示,使得电极14(1)和14(2)与纵向构件12同时递送。
在另一个实例中,如图2所示,电极14(1)和14(2)在第二纵向构件13上递送,该第二纵向构件被配置成插入到第一纵向构件12的内腔19中,以便在患者的身体区域附近递送。在该实例中,电极14(1)和14(2)在递送组合物递送元件18之后被引导到身体区域。
在又一个实例中,如图3所示,电极14(1)和14(2)分别在第二纵向构件13和第三纵向构件23上通过第一纵向构件12的内腔19被引导到身体区域,其中第二纵向构件和第三纵向构件是独立的、不重叠的导丝或导管。在该实例中,第二纵向构件13和第三纵向构件23可以使用如美国专利号9,561,073中所述的顺行/逆行方法沿相同方向或相反方向递送到身体,该美国专利的公开内容全文通过引用并入本文。
如在相同发明人的美国专利号7,918,859(该专利全文并入本文)中所公开的,在受控的顺行和逆行跟踪(cart)技术中,逆行方法利用了冠状动脉间通道。这种通道可以是心外膜通道、心房间通道、隔膜内通道(也称为隔膜侧支)或旁路移植物。cart技术的基本概念是通过在顺行和逆行这两种方向上接近闭塞,优选地使用有限的剥离,来形成通过该闭塞的通道。
在另一个实例中,包括电极14(1)或14(2)中的一个电极的贴片在患者待治疗的身体区域附近放置在该患者的皮肤上。将贴片紧靠该身体区域放置,以允许实现电极14(1)与14(2)之间的双极性布置。
接下来,射频能量以经调制脉冲的形式从射频能量源16递送到电极14(1)和14(2)。在一个实例中,射频能量源16提供脉冲宽度介于约0.05微秒至约500微秒之间的经调制脉冲,但也可以采用脉冲宽度小于0.05微秒或介于500微秒与1秒之间的经调制脉冲。仅举例而言,射频能量源16还可以以具有介于2个与10个之间的脉冲的脉冲群的形式提供经调制脉冲。在另一个实例中,经调制脉冲被分组成脉冲串,仅举例而言,这些脉冲串的脉冲串宽度介于100ms至1s之间,并且每个脉冲串之间的间隔介于1ms至100ms之间。
可以使用心电图(ecg)或从患者身体获得的另一种波形信号来对经调制脉冲的递送进行门控。在一个实例中,包含电极的第三贴片可以放置在身体区域外部,并且电耦合到电极14(1)和14(2)。在又一个实例中,第三电极可以位于身体区域附近,以便基于射频能量的递送来测量阻抗。然后可以利用阻抗测量结果来优化射频能量的递送。
射频能量源16在介于400v至4000v之间的电压下提供射频能量,但在一些实例中可以利用小于400v的电压。在一个实例中,射频能量在身体区域中的入射强度介于约0.1焦耳/平方毫米至5焦耳/平方毫米之间。在一个实例中,射频能量被递送直到满足电气限值,诸如100欧姆,但也可以采用其他电气限值。
射频能量源16以在身体区域中产生递送条件的水平提供射频能量,该递送条件增强组合物的递送,诸如空化、微射流、冲击波、电刺激或化学反应。在一个实例中,射频能量源16提供能量以产生瞬时大小介于0.1mpa至20mpa之间的冲击波。在另一个实例中,射频能量源16提供能量以便在身体区域中产生直径介于1μm与10mm之间的一个或多个空化囊泡区域。可以使用组合物递送装置10由递送至身体区域的组合物形成这些空化囊泡。
递送射频能量不仅延长了对组合物的递送,还将组合物嵌入身体区域内,从而提供增强的治疗。可以使用对脉冲的多种修改来调整射频信号,诸如通过缩短或延长脉冲持续时间或调整脉冲周期。作为一个实例,通过将脉冲持续时间缩短到微秒或纳秒范围,可以获得更强的机械效果,从而产生让组合物进入身体区域的更强机械效应(即,让组合物更深地注射或嵌入到身体区域中)。组合物嵌入更深有可能导致该组合物在身体区域内的持续时间更长,从而使该组合物能够具有更持久的效果。
举例而言,可以利用射频能量的递送来提供增强该组合物扩散到身体区域中的机械力。作为替代,可以采用射频能量来对身体区域本身产生影响,诸如血管舒张、细胞渗透性增加或可逆电穿孔,这增加了组合物向身体区域递送的有效性。
举例而言,该方法可以用于治疗闭塞。射频能量施加在两个电极14(1)与14(2)之间,从而产生等离子体并利用等离子体产生的效应(诸如空化或冲击波)改变周围的斑块或闭塞或血管壁。组合物被递送到闭塞,由于等离子体产生的效应,该闭塞现在已变得更易于扩散或递送该组合物,从而增强了该组合物向血管壁中的递送。将射频能量递送到血管壁或闭塞可以引起血管舒张、改变细胞渗透性或电穿孔等,以增强组合物的递送。通过调节射频信号,组合物可以更深地递送到血管壁中,从而允许该组合物在血管壁内保留延长的时间段并改善组合物在脉管系统内的耐久性。
在另一个实例中,电极14(1)和14(2)与组合物被放置在同一个装置上,这允许同时修改周围组织并递送射频能量,从而增强组合物的递送。在该实例中,组合物递送元件18(诸如球囊导管)具有被放置在球囊的外表面25上的组合物层24。电极14(1)和14(2)位于组合物递送元件18的内部,要么如图1所示作为第一纵向构件12的附件,要么如图2和图3所示通过第一纵向构件12的内腔19递送。然后递送射频能量,射频能量的效应通过组合物递送元件18(诸如球囊)传递到组合物层24和血管壁,从而增强该组合物向血管壁的递送。
现在将参考图9a至图9c来描述利用射频能量来增强组合物向患者身体区域(诸如闭塞)的递送的另一种示例性方法。在该实例中,在将组合物递送到身体区域之前,在第二纵向构件13和第三纵向构件23上将电极14(1)和14(2)引导到血管中的闭塞区域,如图9a所示。
然后如上所述施加射频能量。施加射频能量产生了等离子体并利用等离子体产生的效应(诸如空化或冲击波)改变周围的斑块或闭塞或血管壁,如图9b所示。然后从该身体区域移除电极14(1)和14(2)。
接下来,使用组合物递送元件18将组合物递送到闭塞,如图9c所示。由于等离子体产生的效应,该闭塞已变得更易于扩散或递送该组合物,从而增强了该组合物向血管壁中的递送。将射频能量递送到血管壁或闭塞可以引起血管舒张、改变细胞渗透性或电穿孔等,以增强组合物的递送。通过调节射频信号,组合物可以更深地递送到血管壁中,从而允许该组合物在血管壁内保留延长的时间段并改善组合物在脉管系统内的耐久性。
实施例
临床前工作(图11)已经证实,在非常高的电压下,在非闭塞血管内使用射频能量进行等离子体介导的消融的效果可以导致传播到血管壁中的效应。特别地,内侧剥离和/或血管周围出血可能发生在外血管壁中。然而,通过改变射频递送设置,可以控制这些效果,使得它们增强组合物向血管壁或闭塞中的递送,而不会产生有害效应。改变的实例可以包括降低电压水平或电流水平、修改脉冲周期、修改脉冲持续时间,或修改在射频递送期间递送的脉冲数。
作为一个实例,就血管壁中的闭塞而言,已经证实使用在1200v至2000v范围内的电压可以在非常短的时间段内消融组织并且产生通过闭塞的通道。递送药物或其他组合物可能需要较少的能量或较低的电压,因为目的不是产生通道,而是增强药物向血管壁中的递送。类似地,已经证实,非常短的脉冲(大约数纳秒)相比较长的脉冲,通常产生较大的机械力(例如冲击波)。优选的是递送足够大的机械力,以增强药物或组合物向血管壁中的递送,而不会对血管壁本身造成损害。
因此,如通过本文的实施例展示和描述的,此技术提供了用于将组合物递送到身体区域的更有效果且更有效率的装置和方法。此技术的装置和方法允许组合物在身体区域部位内保持延长的时间段,以提供增强的治疗。特别地,使用由射频能量或其他能量源产生的空化、冲击波、电穿孔等有助于递送组合物。此技术还有利地提供了一种用于将药物递送到脉管壁或闭塞中以使得药物在目标部位内保持较长的时间段而不留下任何东西的增强方法。药物在目标部位内长效作用可以改善结局(例如降低再闭塞率、再狭窄率或血运重建率)
已如此描述本发明的基础概念,本领域的技术人员应相当清楚,前述详细公开内容意图作仅为实例呈现,而非限制性的。尽管本文中未明确陈述,但本领域的技术人员应想到并期望各种更改、改进以及修改。这些更改、改进以及修改意图据此提出,并且在本发明的实质和范围之内。因此,本发明仅受以下权利要求及其等同物限制。
- 还没有人留言评论。精彩留言会获得点赞!