治疗脂蛋白代谢障碍的化合物的制作方法
本公开文本涉及肝素类似物作为前蛋白转化酶枯草杆菌蛋白酶样/克新(kexin)9型(pcsk9)的抑制剂用于治疗脂蛋白代谢障碍的用途。
背景技术:
由动脉粥样硬化引起的冠状动脉疾病是欧洲和美国的主要死因。发生动脉粥样硬化的主要风险因素是高胆固醇血症,其中循环中携带胆固醇的低密度脂蛋白(ldl胆固醇或ldl-c)颗粒的水平升高。ldl胆固醇颗粒的代谢高度受调节以平衡胆固醇的合成与饮食摄入,以服务于体内对胆固醇的需求。ldl胆固醇周转中的关键调节剂是ldl受体(ldlr),其介导ldl颗粒的细胞摄取并降低循环中的ldl胆固醇水平,如通过由ldlr缺乏或功能受损引起的家族性高胆固醇血症的患者所说明。
成功的降低ldl胆固醇血浆水平的策略是增加细胞ldlr水平,并且目前用于降低ldl胆固醇的最广泛使用的药物是他汀类(statin)。他汀类抑制胆固醇合成并上调ldlr的表达,由此总体上导致减少循环ldl胆固醇的量。然而,大量患者由于各种副作用而对他汀类无反应或不耐受他汀类。此外,他汀类还增加前蛋白转化酶枯草杆菌蛋白酶样/克新9型(pcsk9)的表达,pcsk9最近被鉴别为ldlr的有效负调节剂(seidah等人,2014),由此抵消了对ldl胆固醇的有益效果。
靶向pcsk9是最近用于降低血浆ldl-c的策略(lagace等人,2006)。由于pcsk9结合ldlr,由此削弱受体的再循环并增强受体的溶酶体降解,ldlr的细胞水平因而下降。pcsk9功能获得型突变导致循环ldl-c由于ldlr的降解增加而显著增加。与之相比,具有pcsk9功能丧失型突变的个体显示ldl-c的水平下降,并且展现较少冠状动脉心脏病事件。若干个主要医药公司的用于减轻高胆固醇血症的靶向pcsk9的治疗策略已获得批准。据报道,在iii期临床试验中,给予针对pcsk9的ldlr结合位点的pcsk9特异性抗体可降低ldl-c血浆水平(mullard(2015)natrevdrugdiscov;sheridan(2015)naturebiotechnology)。然而,pcsk9:ldlr结合常数在120-620nm范围内(cunningham等人,2007;fisher等人,2007),而pcsk9血浆浓度为约6nm(lakoski等人,2009),使得pcsk9非常不可能以生理相关浓度直接结合ldlr。另外,pcsk9仅靶向肝中的ldlr,而不靶向例如也表达高水平ldlr的产生类固醇激素的组织中的ldlr,说明需要肝特异性共受体(seidah等人,2014)。因此,ldlr很可能不是主要pcsk9受体。而是,未知受体(受体x)可捕获循环pcsk9并随后将其递送到ldlr。因此,对pcsk9结合到此受体的抑制是与抑制pcsk9:ldlr相互作用相比更优的策略。
技术实现要素:
本发明者已发现,pcsk9具有针对类肝素硫酸蛋白聚糖(hspg)的结合基序。引入此基序中的突变以及肝素对hspg的结合的抑制保护ldlr免受pcsk9诱导的降解。与pcsk9抑制性抗体的临床试验相比,对pcsk9与hspg之间的相互作用的抑制具有更优的治疗潜力(chan等人,2009)。重要的是,pcsk9中的hspg结合基序与ldlr结合表面的hspg结合基序不同。hspg由经一条或多条类肝素硫酸糖胺聚糖链取代的核心蛋白组成。肝素是一类在结构上与类肝素硫酸(hs)密切相关的糖胺聚糖。肝素和hs都是由重复二糖单元构成,所述二糖单元由糖醛酸(葡糖醛酸(glca)或艾杜糖醛酸(idoa))和n-乙酰葡糖胺(glcn)组成,其可经o-硫酸化和/或n-硫酸化。肝素是类肝素硫酸的高度硫酸化变体。hspg是高糖基化蛋白,其结合具有hspg结合基序的蛋白质配体,产生例如生长因子的局部储积(xu和esko,2014)。数据显示,pcsk9结合hspg,并且所述相互作用通过pcsk9中hspg结合基序的定点诱变而被消除,导致不能结合肝素并展现受损的降解ldlr的能力的pcsk9突变体。另外,细胞与肝素或肝素类似物孵育导致ldlr的水平升高,伴随培养基中pcsk9的浓度增加。综上所述,本发明的例子中概述的结果显示,pcsk9功能依赖于hspg的结合,并且ldlr的细胞水平在pcsk9与hspg之间的相互作用消除时增加。
因此,hspg在pcsk9介导的细胞表面ldlr的降解中具有关键作用。本发明的发现显示,hspg在pcsk9诱导的ldlr的下调中具有决定性作用。
可在阻断pcsk9功能中,特别是在抑制pcsk9对ldlr水平的效应中,靶向pcsk9与hspg之间的相互作用位点。由此公开治疗脂蛋白代谢障碍的新策略。
在第一方面中,本发明涉及组合物,所述组合物包含具有式(i)的通式结构的化合物:
或其医药上可接受的盐、溶剂合物、多晶型或互变异构体,
其中:
-r1选自:烷基、经取代的烷基、杂烷基、经取代的杂烷基、烷基磺酰基、经取代的烷基磺酰基、烯基、经取代的烯基、炔基、经取代的炔基、烷氧基、经取代的烷氧基、酯、酰胺、酰基、经取代的酰基、氨基、经取代的氨基、硫代烷基、经取代的硫代烷基、芳基、杂芳基、经取代的芳基、氢和卤素;
-各r2独立地选自:-oso3-、-oh、-nh2、-nhso3-、-nhoch3和-opo32-;
-各r3独立地选自:-oso3-、-oh和-opo32-;
-各r4独立地选自:-oso3-、-oh、-opo32-和-h;
-各r5独立地选自:-ch2oso3-、-ch2oh、-coo-和-ch2opo32-;
-n是等于或大于1的整数;
所述组合物用于治疗受试者的脂蛋白代谢障碍。
在一个方面中,本发明涉及抑制ldlr降解的方法,所述方法包括给予包含如本文所定义的化合物的组合物。
在另一方面中,本发明涉及降低有需要的受试者的血浆脂蛋白水平的方法,所述方法包括向所述受试者给予如本文所定义的化合物或药物组合物的步骤。在一个实施方案中,脂蛋白是ldl-c。
附图说明
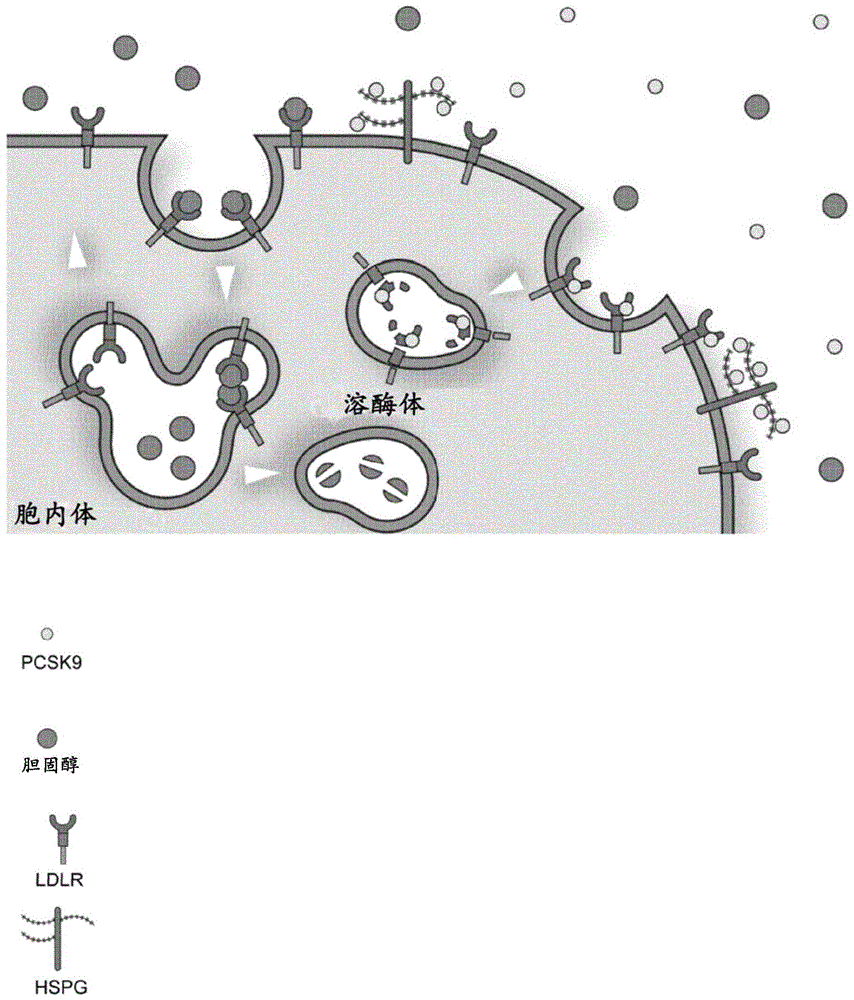
图1:所提出的描绘hspg捕获pcsk9并随后将其呈递到肝细胞表面处的ldlr的模型的图。ldlr吸收来自循环的ldl-c颗粒并将其递送到溶酶体以供降解,同时受体(ldlr)在胞内体中释放负荷后再循环到细胞表面。在结合到pcsk9后,ldlr自身在溶酶体中降解。有人提出,肝细胞表面上的hspg捕获pcsk9并将其呈递到ldlr,由此确保pcsk9:ldlr复合物形成的最佳条件。因此,pcsk9的高活性导致细胞表面处的ldlr的水平降低以及血浆胆固醇增加,而抑制pcsk9活性降低血浆胆固醇水平并减慢冠状动脉疾病的进展。
图2:(a)显示pcsk9的空间填充模型,其中ldlr结合位点和hspg结合位点分别由左箭头和右箭头指示。(b)pcsk9(pdbid:2pmw)中带正电荷的氨基酸(r:精氨酸,h:组氨酸)的所预测hspg结合位点的静电表面(红色负电;蓝色正电)处的肝素五糖(sanorg,小棍)(piper等人,2007)。(c)sanorg叠加到pcsk9中的hspg结合位点(带状物)上。(d)在用或不用肝素酶i处理后,表达pcsk9的非透化hepg2细胞(白色)。将细胞核用hoechst染色(深灰色)。(e)通过肝素亲和色谱法分析结合到肝素的pcsk9。将pcsk9在500mm的nacl浓度下从柱洗脱。
图3:在cho细胞中瞬时表达pcsk9变体,其中所指示氨基酸残基突变为丙氨酸。(a)细胞裂解产物和培养基的抗pcsk9蛋白质印迹显示所有pcsk9变体的表达,以及在细胞裂解产物中从前蛋白(前pcsk9)正确加工为成熟pcsk9,以及成熟pcsk9分泌到细胞的培养基中。在模拟经转染细胞中未检测到pcsk9的表达。(b)通过亲和色谱法和之后具有抗pcsk9的级分的蛋白质印迹,针对与肝素的结合,分析分泌到瞬时转染的cho细胞的培养基中的pcsk9突变体。所有突变体都具有在所指示位置的丙氨酸取代。野生型(wt)pcsk9和突变体r165r167是在对应于0.3-0.4mnacl的级分中洗脱,而pcsk9突变体r96r97和r104r105显示降低的对肝素的亲和性,并且是在穿流液中或在第一级分中发现。pcsk9突变体r93r104r105h139和r93r96r97r104r105h139仅在穿流液中发现并且未结合到肝素。(c)hspg结合结构域是与ldlr结合位点相对定位,如与ldlr片段复合的pcsk9(pdb:3p5b)的表面表示中pcsk9的空间填充模型中所示。ldlr片段含有β螺旋桨结构域和egf结构域a和b以及l7,同时显示pcsk9c末端催化结构域和前结构域具有碱性螺旋。所建模的肝素片段显示为小棍。(d)在通过亲和色谱法和蛋白质印迹分析时,来自hepg2细胞的培养基的内源性pcsk9和apoe显示类似的与肝素的结合。
图4:与wtpcsk9(10nm)一起孵育18小时的hepg2细胞显示比与突变体(r93r96r97r104r105h139)pcsk9(mut4)一起孵育的细胞显著更低的ldlr水平。通过蛋白质印迹评估ldl受体水平(a),显示gapdh的水平作为对照。棒图(b)显示通过光密度测定法(n=3)定量的ldlr的平均值和平均值的标准偏差(sem)。使用student'st测试评估结果。**p<0.01,****p<0.0001。
图5:与肝素(50u/ml)一起孵育24h的hepg2细胞通过蛋白质印迹评估显示提高的ldlr水平(a)。显示gapdh水平作为对照。棒图(b)显示通过光密度测定法(n=4)定量的ldlr的平均值和平均值标准偏差(sem)。如通过elisa所测量,与肝素一起孵育也导致培养基中的pcsk9水平升高(c)。棒图显示平均pcsk9浓度和sem(n=4)。使用student’st测试评估结果。***p<0.001,****p<0.0001。(d)=非透化hepg2细胞的pla分析显示,ldlr与pcsk9之间的共定位在将细胞与肝素(50u/ml)一起孵育后显著减少。
图6:(a)使用无细胞pcsk9/ldlr结合分析(bpsbioscience)发现,肝素(5和50u/ml)不抑制pcsk9与ldlr的直接相互作用,与靶向pcsk9的ldlr结合区的对照抑制剂抗pcsk9抗体(5nm)(bpsbioscience71207)相反。在结合分析中,对来自结合到固定ldlr的生物素化pcsk9的化学发光信号进行定量,并且此处显示相对于来自无抑制剂样品的信号标准化的结果。棒图显示平均值(n=3)和标准偏差误差棒。使用student’st测试评估结果。*****p<0.00001。y轴:如果无抑制剂的%。(b)如通过elisa所测量(n=3),肝素对培养基中的pcsk9的剂量依赖性效应。y轴:培养基中的pcsk9(%);(c)通过rt-pcr对细胞裂解产物中的mrna水平的定量分析。
图7:与增加浓度(0-250μg/ml)的肝素类似物arixtra(磺达肝素(fondaparinux),glaxosmithklinepharma)一起孵育24小时的hepg2细胞具有升高的ldlr水平。显示gapdh蛋白质印迹作为上样对照。
图8:(a)在与法安明(fragmin)(100u/ml)和亭扎肝素钠(innohep)(100u/ml)一起孵育18小时后hepg2细胞中的ldlr的蛋白质印迹,其显示低分子量肝素的这两种治疗制剂可增加ldlr的细胞水平,与肝素(50u/ml)的效应相当。显示gapdh的蛋白质印迹作为上样对照。(b)蛋白质印迹,其显示在静脉内给予单独的或与50u肝素组合的10μgpcsk9之后1小时,小鼠肝中的ldlr水平。加载50μg膜制剂。作为对照显示分拣蛋白(sortilin)的蛋白质印迹,所述分拣蛋白是先前显示并非pcsk9诱导的降解靶标的pcsk9受体。(c)b)的定量。通过光密度测定法对区带进行定量,并且点图以注射媒剂(0.9%nacl)的对照的百分比显示每一样品的单独水平以及平均值和sem。共注射pcsk9和肝素的小鼠显示显著较高的ldlr水平(60.3±12.3%ldlr相对于24.0±4.04%,n=7只小鼠/组,p=0.0157,双尾student’st测试)。
图9:(a)在与肝素模拟物硫酸葡聚糖(200μg/ml)一起孵育24小时后hepg2细胞中的ldlr的蛋白质印迹,其显示这种化合物可有效提高ldlr的细胞水平。显示肝素(50u/ml)用于比较。显示gapdh作为上样对照。(b)ldlr水平的光密度测定法定量显示在与硫酸葡聚糖(0-200μg/ml)一起孵育后,hepg2细胞中的ldlr的浓度依赖性增加。棒图以未处理细胞的%显示ldlr平均值和sem误差棒。(c)pcsk9和硫酸葡聚糖的微量热泳动(mst)结合曲线。y轴:荧光信号。x轴:硫酸葡聚糖或葡聚糖浓度,kd=180μm。圆形:硫酸葡聚糖。正方形:葡聚糖。(d)在与硫酸戊聚糖(0-200μg/ml)一起孵育24小时后,hepg2细胞中的ldlr的蛋白质印迹、光密度测定法定量(e),显示来自经50-200μg/ml硫酸戊聚糖处理的细胞的裂解产物中的ldlr增加4倍。棒图以未处理细胞的%显示ldlr平均值和sem误差棒。(f),pcsk9和硫酸戊聚糖的mst结合曲线。y轴:荧光信号。x轴:硫酸戊聚糖浓度。圆形:硫酸戊聚糖,kd=381μm。正方形:对照。(g),在与舒拉明(suramin)(0-200μg/ml)一起孵育24小时后,hepg2细胞中的ldlr的定量。棒图以未处理细胞的%显示ldlr平均值和sem误差棒。与舒拉明一起孵育的hepg2细胞中的ldlr的代表性蛋白质印迹显示于(a)中。(h):pcsk9和舒拉明的mst结合曲线。y轴:荧光信号。x轴:舒拉明浓度。圆形:舒拉明,kd=190μm。正方形:对照。(i)在与硫代磷酸寡核苷酸s-dc-36(0-5.0μm)一起孵育24小时后,hepg2细胞中的ldlr的蛋白质印迹,和光密度测定法定量(j),其显示细胞受体水平的浓度依赖性升高。棒图以未处理细胞的%显示ldlr平均值和sem误差棒。使用student’st测试评估结果。*p<0.05,**p<0.01,***p<0.001,****p<0.0001。(k)pcsk9和s-dc-36的mst结合曲线。y轴:荧光信号。x轴:s-dc-36浓度。圆形:s-dc-36,kd=4.8μm。正方形:对照。
图10:在注射pcsk9(10μg)之前输注肝素酶i完全抑制pcsk9诱导的ldlr降解。显示代表性样品的蛋白质印迹(a)和ldlr的棒图定量(b)。对于蛋白质印迹,使用gapdh作为上样对照。e:空泳道。对照n=7,pcsk9n=6,肝素酶n=5,肝素酶/pcsk9n=5。与仅注射pcsk9的小鼠相比,共注射pcsk9(10μg)和肝素(50u)或舒拉明(300μg)的小鼠显示显著更高的ldlr水平(c)。对照n=15,pcsk9n=10,pcsk9/肝素n=7,pcsk9/舒拉明n=3。(d)在静脉内注射肝素(50u)后pcsk9的血浆水平,如通过鼠类pcsk9特异性elisa所评价。
图11:在静脉内给予单独的或与50μgpcsk9抑制性抗体5e11组合的10μgpcsk9后1小时,小鼠肝中的ldlr水平。
图12:棒图,其显示在与10ng/ml经荧光染料bodipy标记的ldl颗粒一起孵育4小时后,在与舒拉明(200μg/ml)一起孵育过夜后,hepg2细胞中的相对荧光信号。舒拉明对pcsk9的抑制将ldl摄取增加两倍。
图13:(a)和(b)棒图,显示如通过蛋白质印迹所评价,在与100μm舒拉明或hmgcoa还原酶抑制剂美伐他汀(mevastatin)和斯伐他汀(simvastatin)一起孵育24小时和48小时后,hepg2细胞中的ldlr水平。与舒拉明一起孵育的细胞显示高于与他汀一起孵育的细胞的ldlr水平。
图14:(a)使用合成聚糖微阵列对pcsk9与细胞外基质聚糖之间的相互作用的剖析。仅显示与不同肝素片段的结合。包括天然肝素作为阳性对照。(b)显示聚糖微阵列中使用的肝素子结构。与pcsk9相互作用的结构含有[4)-α-glcn-6,n-二硫酸(1→4)-α-idoa-2-硫酸-(1→]的重复。
图15:(a)在小鼠中注射后,具有突变的hspg结合位点的pcsk9(r93r96r97r104r105h139,mut4)(10μg)在诱导肝ldlr降解(每一者的n=3)中无效。蛋白质印迹的定量显示于(b)中。(c)pcsk9而不是pcsk9mut4显著增加饲喂西餐饮食的小鼠中的总胆固醇(对照n=25,pcsk9n=12,pcsk9mut4n=9)。(d)所注射的pcsk9mut4以高于pcsk9wt的浓度保持在循环中,与减少的hspg捕获和ldlr清除一致。
图16:(a)在分析中测试化合物(x)抑制pcsk9-肝素相互作用的能力,其中在抑制剂存在下用肝素-琼脂糖珠粒使pcsk9(1μg/ml)沉淀。在过夜孵育后,使珠粒沉淀,并且通过elisa评估上清液中的未沉淀pcsk9(=游离pcsk9)。棒图显示如所指示的具有增加浓度的化合物(x)的样品中的游离pcsk9(%),将其针对不含肝素-琼脂糖珠粒的样品(输入对照)中的pcsk9浓度标准化。阴性对照样品是在无抑制剂的情况下孵育,并且阳性对照样品是与可溶肝素(5mg/ml)一起孵育。显示平均值和sem(n=2)。(b)与如所指示的化合物(x)浓度一起孵育过夜的hepg2细胞中ldlr水平的代表性蛋白质印迹。棒图显示对wb的定量(平均值和sem,n=2)。将对照细胞在无抑制剂的情况下孵育(阴性对照)或与500μg肝素/ml一起孵育(阳性对照)。(c)在注射pcsk9(0.4mg/kg)前1小时注射pcsk9抑制剂化合物(x)(0,13mg/kg)或依洛尤单抗(evolocumab)(8mg/kg)的小鼠(balb6/cjrj,雄性,10周)肝样品中的ldlr水平。肝样品是在pcsk9注射后1小时收集。向对照组注射nacl(0.9%),之后注射pcsk9或nacl。棒图显示平均值和sem。nacl/nacl组n=3,nacl/pcsk9组n=5,依洛尤单抗/pcsk9组n=5,化合物(x)/pcsk9组n=8。
图17:(a)与肝素六聚体或18聚体以如所指示的浓度一起孵育过夜的hepg2细胞中的ldlr水平的蛋白质印迹。(b)棒图显示对wb的定量(平均值和sem,n=2)。
图18:(a)通过亭扎肝素钠的尺寸排阻色谱获得的洗脱图。随后在hepg2细胞中测试所指示级分的pcsk9抑制性活性。(b)蛋白质印迹,其显示与尺寸排阻级分(20μm)一起孵育的hepg2细胞中的ldlr水平。与级分h6一起孵育过夜将细胞ldlr增加5倍,并使用强阴离子交换(sax)色谱将此级分进一步分级分离(图19)。
图19:(a)亭扎肝素钠级分h6的通过强阴离子交换(sax)色谱获得的洗脱图。(b)与所选sax级分一起孵育过夜的hepg2中的ldlr的蛋白质印迹。sax级分i1、i8和i9含有具有pcsk9抑制性活性的肝素片段,并且在所测试浓度(500nm)下将ldlr水平增加多达2倍。
图20:pcsk9与肝素-白蛋白的结合的biacore分析。该分析使用与肝素-白蛋白(sigmah0403)或白蛋白(sigmaa4503)偶联的传感器芯片。(a)pcsk9与肝素-白蛋白的结合。(b)pcsk9与白蛋白的结合。pcsk9以700pm的亲和常数与肝素-白蛋白结合,未观察到与偶联有白蛋白的传感器芯片的结合。实施干扰分析来评价pcsk9与化合物(x)之间的结合。(c)将与增加浓度的化合物(x)一起预孵育的pcsk9输注在与肝素-白蛋白偶联的传感器芯片上。结合曲线揭示,化合物(x)抑制pcsk9与肝素-白蛋白传感器芯片的结合,估计ic50为50nm。
图21:(a)蔗糖八硫酸酯的结构。(b)棒图显示通过肝素-琼脂糖珠粒在如所指示的蔗糖八硫酸酯浓度存在下的pcsk9沉淀。相对于无肝素-琼脂糖珠粒的样品(输入对照)中的pcsk9浓度计算未沉淀的pcsk9(游离pcsk9)的百分比。将阳性对照样品与可溶肝素(5mg/ml)一起孵育。显示平均值和sem(n=3-2)。
定义
如本文所用,术语“酰基”意指如下文所定义含有至少一个氧代部分(-c=o)的烷基。
术语“烷烃”是指饱和直链、支链和/或环状碳氢化合物。所述烷烃可具有通式cnh2n+2。在一些实施方案中,所述烷烃包含环结构。
如本文所用术语“烯基”是指通过移除一个-h衍生自烯烃的取代基。烯烃可为包含至少一个双键的非环状碳氢化合物。通常,烯基将具有通式-cnh2n-1。
术语“烷基”是指通过移除一个-h衍生自烷烃的取代基。
如本文所用术语“炔基”是指通过移除一个-h衍生自炔烃的取代基。炔烃可为包含至少一个三键的任何非环状碳氢化合物。通常,炔基将具有通式-cnh2n-3。
术语“烷基磺酰基”是指-s(o)2-烷基,其可为末端基团或桥接基团。
术语“酰胺”是指官能团rc(o)nr'r"。
如本文所用术语“氨基”是指通式
波形线指示该取代基的连接点。氨基因此可为例如-nh2或-nh-。
如本文所用术语“芳烃”是指芳香族单环或多环碳氢化合物。
如本文所用术语“芳基”是指从芳烃通过从环中的c移除一个-h衍生的取代基。待用于本发明的有用芳基的例子包含苯基、萘基、蒽基、菲基和芘基。
术语“酯”是指官能团rcoor′。
如本文所用术语“卤素”是指选自-f、-cl、-br和-i的取代基。
术语“肝素类似物”是指结构上与肝素类似的化合物。
术语“肝素模拟物”是指功能表现类似于(即模拟)肝素的化合物。因此,在本公开文本的背景中,这个术语包括结构上类似于肝素的化合物,以及与肝素具有不同结构但具有相同功能的化合物。
如本文所用术语“杂烷基”是指其中一个或多个碳已被选自s、o、p和n的杂原子更换的烷基。
如本文所用术语“杂芳基”是指通过从杂芳烃的环结构中的原子移除一个-h衍生自所述杂芳烃的取代基。杂芳烃是环结构中包含一个或多个杂原子的单环或多环芳香族化合物。所述杂原子优选地选自s、n和o。待用于本发明的有用杂芳基的非限制性例子包含唑基、吡啶基、嘧啶基、呋喃基和苯硫基。
ldl-胆固醇(ldl-c)水平:给定个体的最佳ldl-c水平根据其潜在心脏病风险而不同。对于健康个体,ldl-c水平应理想地小于2.6-3.3mmol/l(或100-129mg/dl)。介于3.4与4.1mmol/l之间或130与159mg/dl之间的水平是临界性高水平,介于4.1与4.9mmol/l之间或160与189mg/dl之间的水平是高水平,并且高于4.9mmol/l或189mg/dl的水平是极高水平。对于具有心脏病风险的个体,低于2.6mmol/l或100mg/dl的水平是推荐的,而对于具有极高心脏病风险的个体,需要低于1.8mmol/l或70mg/dl的水平。
低密度脂蛋白受体(ldlr)水平:细胞中ldlr的合成受游离细胞内胆固醇水平的调节;如果胆固醇对于细胞的需要过多,那么将抑制ldlr的转录。ldlr水平可通过本领域已知的方法来估计,例如但不限于蛋白质印迹、rt-pcr和流式细胞术。
术语“低分子量肝素”是指一类大小有限的肝素。天然肝素由不同长度或分子量的分子链组成。例如,从5000到超过40,000道尔顿的不同分子量的链构成多分散性医药级肝素。相反,低分子量肝素仅由短链多糖组成。低分子量肝素定义为平均分子量小于8000da并且所有链中至少60%的分子量小于8000da的肝素盐。这些肝素是通过本领域技术人员已知的多种方法来获得,例如聚合肝素的分级分离或解聚。
术语“脂蛋白代谢障碍”是指脂质体内平衡的障碍和与其相关的障碍,包括例如糖尿病、肥胖症、代谢综合征、黄瘤、高胆固醇血症、家族性高胆固醇血症、血脂异常、高甘油三酯血症、高脂血症、谷固醇血症、高血压、心绞痛、急性冠脉综合征、冠状动脉心脏病、动脉粥样硬化、动脉硬化、血管炎症和脓毒症。
pcsk9水平:在一般群体中,pcsk9的血浆水平从30到3000ng/ml变化,并且女性的中值水平一般高于男性。pcsk9水平与ldl-c水平相关联。
如本文所用术语“单糖单元”是指碳水化合物的最基础单元,并包括醛糖、酮糖和众多种衍生物。如果多于一个单糖单元相连,连接可个别地为α或β(1→2)、α或β(1→3)或者α或β(1→4)。优选地,连接为α或β(1→4)。单糖单元可为醛糖或酮糖。
如本文所用术语“经取代的”在关于化学化合物时是指一个或多个氢基经另一部分取代。因此,如本文所用的“经x取代”在关于化学化合物时是指一个或多个氢基经x取代。类似地,“经取代的x”是指x,其中一个氢基已经另一部分取代。例如,“经取代的烷基”是指烷基-r,其中r是除了-h以外的任何部分。
如本文所用术语“取代基”在关于化学化合物时是指代替氢原子取代的原子或原子团。
如本文所用术语“硫代烷基”是指通式-s-烷基的取代基。
如本文所用术语“硫代芳基”是指通式-s-芳基的取代基。
具体实施方式
本发明是如权利要求书中所界定。
肝素类似物
本发明在第一方面中涉及组合物,所述组合物包含用于治疗受试者的脂蛋白代谢障碍的化合物。该化合物通常为肝素类似物。肝素类似物的例子描述于r.lever等人(编辑),heparin-acenturyofprogress,handbookofexperimentalpharmacology207,springer-verlagberlinheidelberg2012中,该文献是通过引用结合于此。
在一个方面中,本发明的肝素类似物式(i)的通式结构:
或其医药上可接受的盐、溶剂合物、多晶型或互变异构体,
其中:
-r1选自:烷基、经取代的烷基、杂烷基、经取代的杂烷基、烷基磺酰基、经取代的烷基磺酰基、烯基、经取代的烯基、炔基、经取代的炔基、烷氧基、经取代的烷氧基、酯、酰胺、酰基、经取代的酰基、氨基、经取代的氨基、硫代烷基、经取代的硫代烷基、芳基、杂芳基、经取代的芳基、氢和卤素;
-各r2独立地选自:-oso3-、-oh、-nh2、-nhso3-、-nhoch3和-opo32-;
-各r3独立地选自:-oso3-、-oh和-opo32-;
-各r4独立地选自:-oso3-、-oh、-opo32-和-h;
-各r5独立地选自:-ch2oso3-、-ch2oh、-coo-和-ch2opo32-;
-n是等于或大于1的整数;
所述组合物用于治疗受试者的脂蛋白代谢障碍。
在一个实施方案中,n为1、2、3或4。
在一些实施方案中,式(i)的化合物中的r1包含式(ii)的基团:
其中:
-x为ch2或so2
-m独立地是等于或大于1的整数。
在一个实施方案中,m为1、2、3、4、5或6。在一个实施方案中,r1包含式(xi)的基团。
在一些实施方案中,r1是经取代的杂烷基。所述经取代的杂烷基可包含一个或多个单糖单元。在一些实施方案中,r1包含至少一个单糖单元,例如至少两个单糖单元,例如至少三个单糖单元,例如至少四个单糖单元。在优选实施方案中,在r1包含至少一个单糖单元时,式(i)中的n为1。
在一个实施方案中,r1进一步包含选自以下部分:烷基、经取代的烷基、杂烷基、经取代的杂烷基、烷基磺酰基、经取代的烷基磺酰基、烯基、经取代的烯基、炔基、经取代的炔基、烷氧基、经取代的烷氧基、酯、酰胺、酰基、经取代的酰基、氨基、经取代的氨基、硫代烷基、经取代的硫代烷基、芳基、杂芳基、经取代的芳基、氢和卤素。
在一个实施方案中,r1包含选自以下的基团:式(xvi)、式(xvii)、式(xviii)、式(xix)、式(xx)、式(xxix)、式(xxx)、式(xxxi)、-peg2000-ome和-peg5000-ome:
在另一实施方案中,r1选自以下基团:式(xvi)、式(xvii)、式(xviii)、式(xix)、式(xx)、式(xxix)、式(xxx)、式(xxxi)、-peg2000-ome和-peg5000-ome。
在一些实施方案中,化合物是肝素模拟物。所述肝素模拟物可为基于pi-88的衍生物。pi-88(式(xxiii),其中r8是-po32-,并且r9各个为-so3-或-h,见下文)是高硫酸化、单磷酸化甘露糖寡糖的混合物,并且已知其为乙酰肝素酶抑制剂。
因此,在一些实施方案中,式(i)中的n为1并且r1包含式(xv)的基团,其中s为等于或大于1的整数。在一个实施方案中,s为1、2或3。
在一个实施方案中,式(i)的化合物是式(xxiv)的化合物,其中p为等于或大于1的整数。
在优选实施方案中,其中该化合物为:
a.式(xxiv)的化合物,其中p为2并且r1为式(xx);
b.式(xxiv)的化合物,其中p为2并且r1为式(xvii);
c.式(xxiv)的化合物,其中p为2并且r1为式(xviii);
d.式(xxiv)的化合物,其中p为3并且r1为式(xvii);
e.式(xxiv)的化合物,其中p为0并且r1为式(xvii);
f.式(xxiv)的化合物,其中p为1并且r1为式(xvii);
g.式(xxiv)的化合物,其中p为1并且r1为式(xix);
h.式(xxiv)的化合物,其中p为3并且r1为式(xx);或
i.式(xxiv)的化合物,其中p为3并且r1为式(xxix)。
在一个实施方案中,p为1并且式(i)的化合物是式(xxv)的化合物。
在优选实施方案中,化合物为:
j.式(xxv)的化合物,其中r1为式(xvii);或
k.式(xxv)的化合物,其中r1为式(xix)。
在一个实施方案中,式(i)的化合物具有结构(ix)。
在一个实施方案中,式(i)的化合物是式(xxvi)的化合物,其中q为等于或大于1的整数。在一个实施方案中,q为1、2或3。
在一个实施方案中,r10为-o-r1。在另一实施方案中,r10包含选自以下的基团:式(xxi)、式(xxii)、-o-式(xvi)、-o-式(xvii)、-o-式(xviii)、-o-式(xix)和-o-式(xx)。在另一实施方案中,r10选自以下基团:式(xxi)、式(xxii)、-o-式(xvi)、-o-式(xvii)、-o-式(xviii)、-o-式(xix)、-o-式(xx)和-o-式(xxix)。
在优选实施方案中,化合物为:
l.式(xxvi)的化合物,其中q为2并且r10为-o-式(xvii);
m.式(xxvi)的化合物,其中q为2并且r10为式(xxi);
n.式(xxvi)的化合物,其中q为1并且r10为式(xvii);
o.式(xxvi)的化合物,其中q为2并且r10为-o-式(xxii);
p.式(xxvi)的化合物,其中q为1并且r10为-o-式(xvii);
q.式(xxvi)的化合物,其中q为2并且r10为-o-式(xviii);
r.式(xxvi)的化合物,其中q为1并且r10为-o-式(xviii);
s.式(xxvi)的化合物,其中q为0并且r10为-o-式(xvii);或
t.式(xxvi)的化合物,其中q为0并且r10为-o-式(xxi)。
在一个实施方案中,式(i)的化合物是式(xxvii)的化合物。
在优选实施方案中,化合物是式(xxvii)并且r10为式(xvii)。
在一个实施方案中,式(i)的化合物是式(xxviii)的化合物。
在优选实施方案中,化合物为:
u.式(xxviii)的化合物,其中r10为-o-式(xvii),r11为h,并且r12为or9;或
v.式(xxviii)的化合物,其中r10为式(xxi),r11为or9,并且r12为h。
在一个实施方案中,化合物具有通式结构(xii)。
在一个实施方案中,r2为-oso3-。在另一实施方案中,r3为-oso3-。在另一实施方案中,r4为-oso3-。在另一实施方案中,r5为-ch2oso3-。在优选实施方案中,r2、r3和r4为-oso3-并且r5为-ch2oso3-。在一个实施方案中,r9为-oso3-。
在一个实施方案中,医药上可接受的盐为钠盐。
在一个实施方案中,化合物具有通式结构(xiii)。
在优选实施方案中,n为2、3或4。
在一个实施方案中,化合物具有通式结构(xiv)。
在优选实施方案中,式(i)的化合物为化合物(x):
在优选实施方案中,式(i)的化合物为3β-胆甾烷基2,3,4,6-四-o-磺基-α-d-吡喃葡萄糖基-(1→4)-2,3,6-三-o-磺基-α-d-吡喃葡萄糖基-(1→4)-2,3,6-三-o-磺基-α-d吡喃葡萄糖基-(1→4)-2,3,6-三-o-磺基-β-d-吡喃葡萄糖苷十三钠盐。
在一个实施方案中,式(i)的化合物具有通式结构(iii):
其中:
-r1选自:烷基、经取代的烷基、杂烷基、经取代的杂烷基、烷基磺酰基、经取代的烷基磺酰基、烯基、经取代的烯基、炔基、经取代的炔基、烷氧基、经取代的烷氧基、酯、酰胺、酰基、经取代的酰基、氨基、经取代的氨基、硫代烷基、经取代的硫代烷基、芳基、杂芳基、经取代的芳基、氢和卤素;
-r2和r6各自独立地选自:-oso3-、-oh、-nh2、-nhso3-、-nhoch3和-opo32-;
-r3和r7各自独立地选自:-oso3-、-oh和-opo32-;
-r5和r8各自独立地选自:-ch2oso3-、-ch2oh、-coo-和-ch2opo32-;
-各r4独立地选自:-oso3-、-oh、-opo32-和-h;
-n为等于或大于1的整数。
在一个实施方案中,式(i)的化合物具有通式结构(iv):
在一个实施方案中,式(i)的化合物具有通式结构(v):
在一个实施方案中,式(i)的化合物具有通式结构(vi):
肝素和类肝素硫酸由重复二糖单元组成。在一个实施方案中,式(iii)-(vi)的化合物中的重复单元数为1。在另一实施方案中,式(iii)-(vi)的化合物中的重复单元数为2。在另一实施方案中,式(iii)-(vi)的化合物中的重复单元数为3。在另一实施方案中,式(iii)-(vi)的化合物中的重复单元数为4。在另一实施方案中,式(iii)-(vi)的化合物中的重复单元数为5。在另一实施方案中,式(iii)-(vi)的化合物中的重复单元数为6。在另一实施方案中,式(iii)-(vi)的化合物中的重复单元数为7。在另一实施方案中,式(iii)-(vi)的化合物中的重复单元数为8。在另一实施方案中,式(iii)-(vi)的化合物中的重复单元数为9。在另一实施方案中,式(iii)-(vi)的化合物中的重复单元数为10。
在一个实施方案中,式(i)的化合物具有通式结构(vii):
在一个实施方案中,化合物具有通式结构(viii):
在具体实施方案中,式(i)的化合物为肝素i并具有以下结构:
在具体实施方案中,式(i)的化合物为肝素vii并具有以下结构:
在一些实施方案中,化合物进一步包含缀合到所述化合物的白蛋白结合部分。在一个实施方案中,白蛋白结合部分是脂肪酸,其可选自:辛酸、癸酸、月桂酸、肉豆蔻酸、棕榈酸、硬脂酸、花生酸、山嵛酸、木蜡酸、蜡酸、肉豆蔻脑酸、棕榈油酸、衫皮酸(sapienicacid)、油酸、反油酸、异油酸、亚油酸、反亚油酸(linoelaidicacid)、α-亚麻酸、花生四烯酸、二十碳五烯酸、芥酸和二十二碳六烯酸。
在一些实施方案中,胆汁酸缀合到式(i)的化合物。在一个实施方案中,缀合的胆汁酸选自:胆酸、牛磺胆酸、甘胆酸、牛磺鹅脱氧胆酸、甘氨鹅脱氧胆酸、鹅脱氧胆酸、脱氧胆酸和石胆酸。在一个实施方案中,式(i)的化合物通过末端氨基(作为r)共价连接到下式的树枝状结构:
肝素类似物与pcsk9的结合
在一些实施方案中,肝素类似物能抑制hspg与pcsk9的结合。在一些实施方案中,肝素类似物结合到pcsk9的任何氨基酸残基,如下文所述。在本公开文本通篇中应理解,能抑制hspg与pcsk9变体结合的化合物也在本发明的范围内。pcsk9变体应理解为具有与seqidno:1基本上相同的序列的多肽,例如具有seqidno:1中一些残基的保守取代的变体。
在一些实施方案中,所述化合物特异性识别并结合pcsk9的hspg结合位点内的区域(seqidno:1),所述区域包含pcsk9(seqidno:1)的氨基酸残基78到167中的至少一个,例如氨基酸残基78到92中的至少一个,例如氨基酸残基93到97中的至少一个,例如氨基酸残基98到103中的至少一个,例如氨基酸残基104到105中的至少一个,例如氨基酸残基106到135中的至少一个,例如氨基酸残基136到139中的至少一个,例如氨基酸残基140到164中的至少一个,例如pcsk9(seqidno:1)的氨基酸残基165到167中的至少一个。
本文提供特异性识别并结合pcsk9(seqidno:1)的hspg结合位点内的区域的化合物,所述区域包含pcsk9(seqidno:1)的氨基酸残基78到167中的至少一个,例如pcsk9(seqidno:1)的氨基酸残基78到167中的至少2个,例如至少5个,例如至少10个,例如至少15个,例如至少20个,例如至少25个,例如至少30个,例如至少35个,例如至少40个,例如至少45个,例如至少50个,例如至少55个,例如至少60个,例如至少65个,例如至少70个,例如至少75个,例如至少80个,例如至少85个,例如所有氨基酸残基。
在一些实施方案中,所述化合物特异性识别并结合一区域,所述区域包含pcsk9(seqidno:1)的氨基酸残基78到92中的至少一个,例如氨基酸残基93到97中的至少一个,例如氨基酸残基98到103中的至少一个,例如氨基酸残基104到105中的至少一个,例如氨基酸残基106到135中的至少一个,例如氨基酸残基136到139中的至少一个,例如氨基酸残基140到164中的至少一个,例如氨基酸残基165到167中的至少一个。
在一些实施方案中,所述化合物特异性识别并结合一区域,所述区域包含pcsk9(seqidno:1)的氨基酸残基78到92,例如氨基酸残基93到97,例如氨基酸残基98到103,例如氨基酸残基104到105,例如氨基酸残基106到135,例如氨基酸残基136到139,例如氨基酸残基140到164,例如氨基酸残基165到167中的至少一个。
因此,在一个实施方案中,所述化合物特异性识别并结合pcsk9的hspg结合位点内的区域,所述区域包含氨基酸残基78到167。在另一实施方案中,所述化合物特异性识别并结合pcsk9的hspg结合位点内的区域,所述区域包含氨基酸残基78到95。在另一实施方案中,所述化合物特异性识别并结合pcsk9的hspg结合位点内的区域,所述区域包含氨基酸残基96到100。在另一实施方案中,所述化合物特异性识别并结合pcsk9的hspg结合位点内的区域,所述区域包含氨基酸残基101到105。在另一实施方案中,所述化合物特异性识别并结合pcsk9的hspg结合位点内的区域,所述区域包含氨基酸残基106到110。在另一实施方案中,所述化合物特异性识别并结合pcsk9的hspg结合位点内的区域,所述区域包含氨基酸残基111到115。在另一实施方案中,所述化合物特异性识别并结合pcsk9的hspg结合位点内的区域,所述区域包含氨基酸残基116到120。在另一实施方案中,所述化合物特异性识别并结合pcsk9的hspg结合位点内的区域,所述区域包含氨基酸残基121到125。在另一实施方案中,所述化合物特异性识别并结合pcsk9的hspg结合位点内的区域,所述区域包含氨基酸残基126到130。在另一实施方案中,所述化合物特异性识别并结合pcsk9的hspg结合位点内的区域,所述区域包含氨基酸残基131到135。在另一实施方案中,所述化合物特异性识别并结合pcsk9的hspg结合位点内的区域,所述区域包含氨基酸残基136到140。在另一实施方案中,所述化合物特异性识别并结合pcsk9的hspg结合位点内的区域,所述区域包含氨基酸残基141到145。在另一实施方案中,所述化合物特异性识别并结合pcsk9的hspg结合位点内的区域,所述区域包含氨基酸残基146到150。在另一实施方案中,所述化合物特异性识别并结合pcsk9的hspg结合位点内的区域,所述区域包含氨基酸残基151到155。在另一实施方案中,所述化合物特异性识别并结合pcsk9的hspg结合位点内的区域,所述区域包含氨基酸残基156到160。在另一实施方案中,所述化合物特异性识别并结合pcsk9的hspg结合位点内的区域,所述区域包含氨基酸残基161到167。
因此,提供结合一个或多个氨基酸的化合物,所述氨基酸选自pcsk9(seqidno:1)的r93、r96、r97、r104、r105、k136、h139、r165和r167,例如选自pcsk9的r93、r96、r97、r104、r105、k136、h139、r165和r167的1个氨基酸,例如2个氨基酸,例如3个氨基酸,例如4个氨基酸,例如5个氨基酸,例如6个氨基酸,例如7个氨基酸,例如8个氨基酸,例如所有氨基酸。
因此,在一个实施方案中,化合物结合到pcsk9的r93。在另一实施方案中,化合物结合到pcsk9的r96。在另一实施方案中,化合物结合到pcsk9的r97。在另一实施方案中,化合物结合到pcsk9的r104。在另一实施方案中,化合物结合到pcsk9的r105。在另一实施方案中,化合物结合到pcsk9的k136。在另一实施方案中,化合物结合到pcsk9的h139。在另一实施方案中,化合物结合到pcsk9的r165。在另一实施方案中,化合物结合到pcsk9的r167。
在一个实施方案中,化合物结合到pcsk9的r96和r97。在另一实施方案中,化合物结合到pcsk9的r104和r105。在另一实施方案中,化合物结合到pcsk9的k136和h139。在另一实施方案中,化合物结合到pcsk9的r93和h139。在另一实施方案中,化合物结合到pcsk9的r93、r104、r105和h139。在另一实施方案中,化合物结合到pcsk9的r165和r167。在另一实施方案中,化合物结合到pcsk9的r93、r96、r97、r104、r105和h139。
ldlr和ldl-c水平
与在本文所公开化合物不存在下的结合相比,所述化合物与pcsk9的结合导致降低pcsk9与ldlr的结合。这继而导致,与在所述化合物不存在下的水平相比,衍生自表达的ldlr细胞系的细胞的ldlr的水平升高,所述细胞系例如肝细胞衍生的细胞系,例如其表面上的ldlr的水平升高。
在一些实施方案中,化合物是如上文所定义的肝素类似物,并且与在所述肝素类似物不存在下的结合相比,其与pcsk9的结合导致pcsk9与ldlr的结合降低。此继而导致,与在所述肝素类似物不存在下的水平相比,衍生自表达的ldlr细胞系的细胞的ldlr的水平升高,所述细胞系例如肝细胞衍生的细胞系。
在一些实施方案中,与在所述化合物不存在下的降解相比,该化合物与pcsk9的结合导致ldlr的溶酶体降解减少。在具体实施方案中,化合物是如上文所定义的肝素类似物,并且与在所述肝素类似物不存在下的降解相比,该肝素类似物与pcsk9的结合导致ldlr的溶酶体降解减少。
在一些实施方案中,与在所述化合物不存在下的水平相比,该化合物与pcsk9的结合导致ldl-c的血浆水平降低。术语‘血浆ldl-c水平’应理解为是指血浆中的ldl-c水平,即ldl-c蛋白的量。在具体实施方案中,化合物是如上文所定义的肝素类似物,并且与在所述肝素类似物不存在下的水平相比,该肝素类似物与pcsk9的结合导致ldl-c的血浆水平降低。
ldl-c的血浆水平可在体内或体外测定。测定ldl-c的血浆水平的方法为本领域已知,并且包括但不限于蛋白质印迹、免疫染色、elisa、超速离心、快速蛋白液相色谱(fplc)和酶热量测定。
脂蛋白代谢障碍
本文提供组合物,其包含用于治疗脂蛋白代谢障碍的化合物。因此,本文提供如本文所定义的化合物用于制备治疗脂蛋白代谢障碍的药物的用途。还公开如本文所定义的化合物,其用于治疗有需要的受试者的脂蛋白代谢障碍的方法中。pcsk9的序列可在受试者之间不同,例如可在一些个体中发现可导致保守取代的个体特异性snp。应理解,抑制hspg与这类pcsk9变体结合的化合物也在本发明的范围内。
在一些实施方案中,脂蛋白代谢障碍与异常pcsk9血浆水平相关。在其他实施方案中,脂蛋白代谢障碍与表达ldlr的细胞例如肝细胞的表面的异常ldlr水平有联系。脂蛋白代谢障碍还可与异常pcsk9血浆水平和表达的ldlr的细胞例如肝细胞的表面的异常ldlr水平有联系。pcsk9血浆水平在人类中从30到3000ng/ml变化。异常pcsk9血浆水平是指与健康个体的平均水平显著不同的pcsk9的血浆水平。在一些实施方案中,异常pcsk9血浆水平显著高于健康个体的平均水平。同样,例如肝细胞表面的异常ldlr水平是指与健康个体的平均水平显著不同的ldlr水平。在一些实施方案中,表达ldlr的细胞例如肝细胞的表面的异常ldlr水平显著低于健康个体的平均水平。
在一些实施方案中,障碍的特征在于异常ldl-c水平,特别是升高的ldl-c水平。
脂蛋白代谢障碍是脂质体内平衡的障碍和与其相关的障碍,并且包括例如高胆固醇血症、家族性高胆固醇血症、血脂异常、高脂血症、高甘油三酯血症、谷固醇血症、动脉粥样硬化、动脉硬化、冠状动脉心脏病、代谢综合征、急性冠脉综合征、黄瘤、高血压、心绞痛、肥胖症、糖尿病,血管炎症和脓毒症。所述障碍可例如由脂蛋白颗粒的结构蛋白中的缺陷、识别各种类型脂蛋白的细胞受体中的缺陷或裂解脂肪的酶中的缺陷而引起。由于所述缺陷,脂质可变得沉积于血管壁中。
高胆固醇血症(或血脂异常)是血液中存在高水平的胆固醇。其为一种形式的高脂血症(血液中的脂质水平升高)和高脂蛋白血症(血液中的脂蛋白水平升高)。混合血脂异常是ldl胆固醇和甘油三酯水平升高,其通常伴随低水平的hdl胆固醇。家族性高胆固醇血症是由ldlr基因中的突变引起的遗传障碍,并且特征为血液中的高胆固醇水平,尤其是ldl胆固醇。
高甘油三酯血症表示甘油三酯的高血液水平。即使在高胆固醇血症不存在下,甘油三酯的升高水平与动脉粥样硬化相关,并且使得易患心血管疾病。极高甘油三酯水平也增加急性胰腺炎的风险。
谷固醇血症或植物固醇血症是罕见的常染色体隐性遗传性脂质代谢障碍,其特征为饮食性固醇的吸收过多和胆汁分泌减少,导致例如高胆固醇血症、腱黄瘤和结节性黄瘤、动脉粥样硬化的过早发展。
动脉粥样硬化(也称为动脉硬化性血管疾病或asvd)是动脉硬化的具体形式,其中动脉壁由于白细胞的侵袭和积累而增厚,含有活的活性白细胞(产生炎症)和死细胞残余(包括胆固醇和甘油三酯)二者。因此,动脉粥样硬化是由于动脉壁中白细胞的慢性炎症反应所致的影响动脉血管的综合征。
动脉硬化是涉及动脉壁的增厚、硬化和弹性丧失的病症。
冠状动脉心脏病也称为动脉粥样硬化性动脉疾病、动脉粥样硬化性心血管疾病、冠状动脉心脏病或缺血性心脏病,是心脏病的最常见类型和心脏病发作的病因。该疾病是由于沿心脏动脉内壁积累斑块所致,其使动脉管腔变窄并减小到达心脏的血流。
代谢综合征是能量利用和储存的障碍,通过以下五种医学病症中三种的共同出现来诊断:腹部(中心)肥胖症、血压升高、空腹血糖升高、高血清甘油三酯和高密度胆固醇水平低。代谢综合征增加发展心血管疾病(特别是心力衰竭)和糖尿病的风险。代谢综合征也称为代谢综合征x、心脏代谢综合征、综合征x、胰岛素抵抗综合征、reaven氏综合征和chaos(在澳大利亚)。代谢综合征和前驱糖尿病似乎是相同障碍,仅通过不同生物标记物集来诊断。
急性冠脉综合征是指由于冠状动脉中的血流减小,使得部分心肌无法正常发挥功能或死亡所致的一组病症。
黄瘤是脂肪沉积的皮肤表现,其中脂质在皮肤内的大型泡沫细胞中积累。黄瘤与高脂血症相关。
高血压或高血液压力有时称为动脉高血压,是其中动脉血压升高的慢性医学病症。
心绞痛(或绞痛)是指胸部疼痛、压迫或挤压感,通常是由于冠状动脉阻塞或痉挛引起心肌缺血所致。虽然心绞痛可源自贫血、心律不齐和心力衰竭,但其主要病因是冠状动脉疾病。
肥胖症是一种医学病症,其中过多身体脂肪积累到可对健康产生负面影响的程度,导致预期寿命缩短和/或健康问题增加,例如心脏病风险增加、2型糖尿病、阻塞性睡眠呼吸暂停、某些类型的癌症和骨关节炎。
糖尿病(diabetesmellitus)一般称为糖尿病(diabetes),是一组代谢疾病,其中在延长时间段期间存在高血糖水平。存在若干种类型的糖尿病,包括i型糖尿病、ii型糖尿病和妊娠糖尿病。1型糖尿病的特征为胰腺的胰岛中产生胰岛素的β细胞损失,导致胰岛素缺乏。2型糖尿病的特征为胰岛素抵抗,其可与相对减少的胰岛素分泌组合。人们认为身体组织对胰岛素的缺陷性反应性涉及胰岛素受体。妊娠糖尿病与2型糖尿病类似,发生于所有妊娠的2-10%中。
脓毒症是感染的可能危及生命的并发症,其在身体对感染的反应损伤自身组织和器官时发生。在感染期间,ldl受体也参与从循环移除细菌脂质,例如脂多糖。pcsk9抑制可为在脓毒症患者的治疗中促进病原体脂质清除的有用策略(walley等人,2016)。
脂蛋白代谢障碍的治疗
需要治疗脂蛋白代谢障碍的个体或受试者是患有、怀疑患有脂蛋白代谢障碍或具有患脂蛋白代谢障碍的风险的个体。在一些实施方案中,需要治疗的个体是哺乳动物,优选地人类。
在优选实施方案中,脂蛋白代谢障碍选自:血脂异常、高胆固醇血症和冠状动脉心脏病。在优选实施方案中,脂蛋白代谢障碍是冠状动脉心脏病。
在一些实施方案中,治疗是预防性的。
在一些实施方案中,治疗包含向所述受试者给予如本文所公开的化合物的步骤。该化合物可以介于0.1mg/kg体重与1000mg/kg体重之间的日剂量来给予。因此,在一些实施方案中,化合物是以介于0.1mg/kg体重与1000mg/kg体重之间的日剂量来给予,例如介于0.2mg/kg体重与900mg/kg体重之间,例如介于0.3mg/kg体重与800mg/kg体重之间,例如介于0.5mg/kg体重与700mg/kg体重之间,例如介于1.0mg/kg体重与500mg/kg体重之间,例如介于5mg/kg体重与400mg/kg体重之间,例如介于10mg/kg体重与300mg/kg体重之间,例如介于25mg/kg体重与250mg/kg体重之间,例如介于50mg/kg体重与200mg/kg体重之间,例如介于75mg/kg体重与150mg/kg体重之间,例如介于100mg/kg体重与125mg/kg体重之间。在一些实施方案中,化合物是以介于0.1mg/kg体重与1000mg/kg体重之间的日剂量来给予,例如介于0.1mg/kg体重与10mg/kg体重之间,例如介于10mg/kg体重与25mg/kg体重之间,例如介于25mg/kg体重与50mg/kg体重之间,例如介于50mg/kg体重与100mg/kg体重之间,例如介于100mg/kg体重与250mg/kg体重之间,例如介于250mg/kg体重与500mg/kg体重之间,例如介于500mg/kg体重与750mg/kg体重之间,例如介于750mg/kg体重与1000mg/kg体重之间。
要根据本发明治疗的适应症的潜在病因是患者血液中的ldl-c水平升高。因此,在一个方面中,本发明涉及抑制ldlr降解的方法,其导致ldl-c与所述ldlr的结合增加。由此通过给予如通式(i)中所定义的化合物来治疗该患者。
因此,本文提供降低有需要的受试者的血浆ldl-c水平的方法,所述方法包括向所述受试者给予如本文所定义的化合物或药物组合物的步骤。血浆ldl-c水平可在体内或体外通过本领域中已知的任何方法来测定,如上文所述。
在一个方面中,本发明涉及降低有需要的受试者的血浆脂蛋白水平的方法,所述方法包括向所述受试者给予如本文所定义的化合物或药物组合物的步骤。
药物组合物
本文还公开药物组合物,其包含至少一种如本文所定义的化合物。在一些实施方案中,组合物包含一种如本文所公开的化合物。在其他实施方案中,组合物包含两种或更多种化合物,例如三种或更多种化合物,例如四种或更多种化合物,例如五种或更多种化合物。
在一些实施方案中,组合物进一步包含以下中的至少一项:
-抑制pcsk9与ldlr结合的抗体;
-他汀;
-消胆胺(cholestyramine);
-胆固醇吸收抑制剂,例如依折麦布(ezetimibe)。
在一些实施方案中,化合物是与另一化合物组合给予,所述另一化合物例如抗pcsk9抗体,例如结合到pcsk9的ldlr结合位点的抗体,或他汀。在一些实施方案中,化合物是与选自以下的抗体一起给予:罗德希珠单抗(lodelcizumab)、劳潘希珠单抗(ralpancizumab)、阿里诺单抗(alirocumab)、依洛尤单抗和柏可珠单抗(bococizumab)。
因此,在一些实施方案中,药物组合物包含至少一种如本文所定义的化合物和至少一种选自以下的额外化合物:抑制pcsk9与ldlr的结合的抗体、他汀或消胆胺。在一个实施方案中,药物组合物包含一种如本文所定义的化合物和抑制pcsk9与ldlr结合的抗体。在一个实施方案中,药物组合物包含一种如本文所定义的化合物和他汀。在一个实施方案中,药物组合物包含一种如本文所定义的化合物和消胆胺。在一个实施方案中,药物组合物包含一种如本文所定义的化合物、抑制pcsk9与ldlr的结合的抗体和他汀。在一个实施方案中,药物组合物包含一种如本文所定义的化合物、抑制pcsk9与ldlr的结合的抗体和消胆胺。在一个实施方案中,药物组合物包含一种如本文所定义的化合物、消胆胺和他汀。在一个实施方案中,药物组合物包含一种如本文所定义的化合物、抑制pcsk9与ldlr的结合的抗体、他汀和消胆胺。
药物组合物任选地包含一种或多种医药上可接受的载剂赋形剂,并且是通过常规技术来制备,例如如以下文献中所述:remington:thescienceandpracticeofpharmacy1995,e.w.martin编辑,mackpublishingcompany,第19版,easton,pa。组合物可显现为常规形式,例如胶囊、片剂、气溶胶、溶液、悬浮液或局部应用。通常,本发明的药物组合物经配制用于非经肠给予,例如通过静脉内或皮下注射给予,并且可以单位剂型存在于安瓿、预填充注射器、小体积输注中,或与所添加防腐剂一起存在于多剂量容器中。组合物可采取诸如以下等形式:油性或水性媒剂中的悬浮液、溶液或乳液,例如在水性聚乙二醇中的溶液。组合物可适于口服。这对于小分子组合物特别合适。油性或非水性载剂、稀释剂、溶剂或媒剂的例子包括丙二醇、聚乙二醇、植物油(例如,橄榄油)和可注射有机酯(例如,油酸乙酯),并且可含有配制剂,例如防腐剂、润湿剂、乳化或悬浮剂、稳定剂和/或分散剂。或者,活性成分可呈粉末形式(通过无菌固体的无菌分离或通过从溶液冻干来获得)用于在使用前用适宜媒剂(例如,无菌、无致热原水)构造。可用于非经肠配制物的油包括石油、动物油、植物油或合成油。可用于所述配制物中的油的具体例子包括花生油、大豆油、芝麻油、棉籽油、玉米油、橄榄油、矿脂油和矿物油。用于非经肠配制物中的适宜脂肪酸包括油酸、硬脂酸和异硬脂酸。油酸乙酯和肉豆蔻酸异丙酯是适宜脂肪酸酯的例子。非经肠配制物通常将在溶液中含有以重量计约0.0001%到约25%,例如约0.5%到约25%的活性成分。可使用防腐剂和缓冲液。为了使对注射部位的刺激降到最低或消除该刺激,所述组合物可含有一种或多种非离子型表面活性剂,其具有约12到约17的亲水性-亲脂性平衡(hlb)。所述配制物中的表面活性剂的量通常将在以重量计约0.000001%到约15%范围内,例如以重量计0.000001%到约5%,或以重量计约5%到约15%。适宜表面活性剂包括聚乙烯山梨聚糖脂肪酸酯,例如山梨聚糖单油酸酯,以及通过环氧丙烷与丙二醇的缩合形成的环氧乙烷与疏水性碱的高分子量加合物。非经肠配制物可存在于单位剂量或多剂量密封容器中,例如安瓿和小瓶,并且可储存于冷冻干燥(冻干)条件下,在即将使用前仅需要添加注射用无菌液体赋形剂,例如水。
然而,根据本发明的主要药物递送途径是非经肠途径,以将药剂引入血流中,以最终靶向相关组织。
在一个实施方案中,给予药剂以穿过要给予其生物活性物质的动物的任何粘膜,例如在鼻、阴道、眼、口、生殖道、肺、胃肠道或直肠中的粘膜,优选地鼻粘膜或口腔粘膜。
在优选实施方案中,本发明药剂是非经肠给予,也就是通过静脉内、肌内、脊柱内、皮下、鼻内、直肠内、阴道内或腹膜内给予来进行。非经肠给予的皮下和肌内形式通常是优选的。所述给予的适当剂型可通过常规技术来制备。化合物还可通过吸入给予,其为通过鼻内和经口吸入给予。所述给予的适当剂型,例如气溶胶配制物或计量剂量吸入剂,可通过常规技术来制备。
在一个实施方案中,本发明的药物组合物经配制用于非经肠给予,例如通过注射给予。
在另一实施方案中,本发明的药物组合物经配制用于静脉内、肌内、脊柱内、腹膜内、皮下、推注或连续给予。
给予的速率和频率可由医师根据不同病例来决定。在一个实施方案中,给予是以30分钟到24小时的间隔进行,例如以1到6小时的间隔进行,例如每天一次。
治疗持续时间可根据障碍的严重度而变。在一个实施方案中,治疗持续时间为1天到28天,例如2天到25天,例如5天到20天,例如7天到15天。在慢性病例中,治疗持续时间可为终生。
剂量可由负责医师基于患者的特征以及给予手段和模式来决定。在本发明的一个实施方案中,如上文所定义的药物组合物的活性化合物的剂量介于0.1mg/kg体重与1000mg/kg体重之间。
剂量可作为推注给予或作为连续给予来给予。关于推注给予,药物组合物可以30分钟到24小时的间隔来给予,例如每天一次。
在一些实施方案中,组合物的ph介于ph4与ph10之间。
在一些实施方案中,组合物经配制用于经口给予。
在一些实施方案中,组合物经配制用于非经肠给予。在具体实施方案中,非经肠给予是通过注射进行。所述非经肠给予可为静脉内、肌内、脊柱内、腹膜内、皮下、推注或连续给予。
在一个实施方案中,本文所公开的化合物是在血清中稳定的肝素类似物。
本文还提供如上文所定义的化合物,其是无毒性的,特别是在给予后无毒。在一些实施方案中,化合物是在给予后无毒的肝素类似物。
实施例
实施例1:pcsk9中hspg结合位点的定位。
检查pcsk9(pdb:2pmw)的静电表面(图2b),并鉴别由位于pcsk9前结构域中的6个表面暴露的碱性残基构成的假定肝素结合位点。结合位点是由在位置93、96、97、104和105的精氨酸(r)残基和在位置139的组氨酸(h)形成,其显示与肝素五糖(sanorg)的硫酸基的完美配对(herbert等人,1996)(herbert等人,1996)(图2b和2c)。发现该位点与位于pcsk9的无活性催化结构域中的ldlr结合表面相对(图2a)。将肝素片段对接到与ldlr复合的pcsk9的共晶体结构上(pdb:3p5b)表明,类肝素硫酸结合容许随后的pcsk9:ldlr复合物形成(图3c)。
实施例2:肝素酶处理在体外抑制pcsk9细胞表面结合并在体内保护ldl受体免受pcsk9诱导的降解
我们推测,hspg可能参与pcsk9的捕获。因此,用肝素酶i处理人类肝细胞衍生的稳定表达pcsk9的hepg2细胞。酶肝素酶i在糖醛酸与n-乙酰基-d-葡糖胺之间的1,4o-连接处裂解类肝素硫酸gag链,由此移除细胞表面类肝素硫酸链。
将用pcsk9稳定转染的hepg2细胞以50.000个细胞/盖玻片接种并孵育过夜,之后添加于pbs(0,0002un/ml)中的肝素酶i(sigmaaldrich/h2519)或仅添加pbs。将细胞在37℃下孵育1h,之后在4%多聚甲醛中固定,并用一抗和二抗对非透化细胞进行免疫染色。用hoechst染料(sigmaaldrich)使细胞核可视化。在zeisslsm780上获取图像。
实际上,处理导致表面pcsk9染色的强度显著降低,表明hspg对pcsk9细胞结合具有关键作用(图2d)。
为了在体内测试酶移除类肝素硫酸gag对pcsk9活性的效应,在注射pcsk9(10μg)前5min向10-12周龄雄性balb6/cjrj小鼠输注通过尾静脉导管给予的肝素酶i(30u)。在对照小鼠中,用0.9%盐水注射替代肝素酶注射和/或pcsk9注射。在肝素酶输注期间,将小鼠用通过面罩连续给予的异氟醚轻度麻醉。注射后1小时,处死小鼠并采集肝组织样品并速冻,之后提取蛋白质并评估通过蛋白质印迹ldlr水平(图10a)。
注射肝素酶i完全保护ldlr免受pcsk9诱导的降解,表明在体内,hspg在pcsk9诱导的ldlr降解中起作用(图10a和b)。
为了验证pcsk9与类肝素硫酸gag链之间的直接相互作用,采用亲和色谱法使用与肝素共价偶合的琼脂糖珠粒。
将纯化的pcsk9加载到pbs中的5mlhitrap肝素hp柱(gehealthcare)上。将该柱与
在不同实验中,将来自经目标pcsk9变体转染的hepg2细胞或cho细胞的条件培养基与肝素琼脂糖cl-6b珠粒(gehealthcare)在10mmnah2po4(结合缓冲液)中一起孵育。在旋转器上在4℃下孵育过夜后,在结合缓冲液中洗涤珠粒,之后在增加浓度的nacl中分批洗脱肝素结合蛋白。通过蛋白质印迹评估输入、穿流液和洗脱级分中的pcsk9。
我们发现,来自hepg2细胞的条件培养基的内源性pcsk9也
结合肝素并显示与apoe类似的洗脱图,apoe是一种已充分确立的hspg结合蛋白(图3d)。
实施例3:对pcsk9/hspg相互作用重要的残基的鉴别
为了使pcsk9/hspg相互作用中所涉及的关键残基的范围进一步变窄,克隆并表达hspg结合基序中具有点突变的pcsk9变体。通过pcr引入突变以用例如丙氨酸(ala/a)的中性残基替代通过3d结构模型对接鉴别的带电荷的氨基酸精氨酸(arg/r)、赖氨酸(lys/k)和组氨酸(his/h)。
分析人类野生型和以下丙氨酸取代变体:
野生型pcsk9(seqidno:1)
突变体r93
突变体r96r97
突变体r104r105
突变体r165r167
突变体r93r104r105h139a
突变体r93r96r97r104r105h139
由于不适当折叠的pcsk9通常在前肽中不裂解并因此保留在内质网中,可通过监测其加工和分泌来评估pcsk9突变体变体的正确折叠。通过对中国仓鼠卵巢(cho)细胞的瞬时转染以及之后对细胞溶解产物中和周围培养基中pcsk9的蛋白质印迹分析来评价将前pcsk9加工为成熟蛋白质和成熟pcsk9变体的分泌(图3a)。
通过亲和色谱法和之后使用抗pcsk9抗体的蛋白质印迹来评价pcsk9突变体蛋白质结合到肝素的能力。
将来自经目标pcsk9变体转染的cho细胞的条件培养基与肝素琼脂糖cl-6b珠粒(gehealthcare)在10mmnah2po4(结合缓冲液)中一起孵育。在旋转器上在4℃下孵育过夜后,在结合缓冲液中洗涤珠粒,之后在增加浓度的nacl中分批洗脱肝素结合蛋白。通过蛋白质印迹评估输入、穿流液和洗脱级分中的pcsk9。
突变体r93、r96r97和r104r105显示与野生型pcsk9或突变体r165r167相比较低的肝素亲和性,并且突变体r93r104r105h139和r93r96r97r104r105h139不结合肝素并且仅发现于穿流液中(图3b)。
实施例4:具有突变的hspg结合结构域的pcsk9变体无法诱导ldl受体降解
在细胞分析中测试纯化的pcsk9变体,以测试其与野生型pcsk9相比诱导ldlr降解的能力。通过将hepg2细胞与野生型pcsk9(wt)或上文pcsk9突变体一起孵育来分析对ldlr降解的诱导,并通过蛋白质印迹评价ldlr水平。将hepg2细胞以250.000个细胞/孔的密度接种于12孔板中。在过夜孵育后,将培养基用含有pcsk9wt或突变体r93r96r97r104r105h139的新鲜培养基更换。在孵育18小时后采集细胞并裂解,并通过蛋白质印迹评价ldlr水平并且通过光密度测定法定量。
与突变体r93r96r97r104r105h139一起孵育的细胞中的ldlr水平显著(约两倍)高于在与wtpcsk9一起孵育的细胞中测量的水平(图4a和b),显示hspg结合结构域内的突变导致pcsk9诱导的ldlr降解减少。
实施例5:肝素和肝素类似物防止pcsk9:ldlr复合物形成。
使用邻近连接分析(pla)测试外源添加的肝素是否与细胞表面hspg竞争结合内源性pcsk9,并由此防止pcsk9:ldlr复合物形成(soderberg等人,2006)。
pla(
使用对非透化hepg2细胞中的内源性细胞表面pcsk9和ldlr进行的此分析来观察pcsk9:ldlr复合物的高丰度簇(图5d)。
在与肝素一起孵育后,这些簇的数目和强度都显著降低,表明结合到hspg的pcsk9在随后与细胞表面ldlr的复合物形成中起作用。
我们发现,将hepg2细胞与肝素一起孵育(50u/ml,18hr)导致两倍到三倍高的ldlr蛋白水平(图5a-5b),并且观察到与低分子量肝素的两种其他治疗性制剂相似的效应(图8a)。
经肝素处理的hepg2细胞中的细胞ldlr的增加为剂量依赖性,并且伴随培养基中pcsk9的显著增加(图6b)。pcsk9浓度是使用来自r&dsystems的human(dpc900)quantikineelisa试剂盒根据制造商方案来测量。
由肝素诱导的细胞ldlr和细胞外pcsk9的增加是在翻译后水平发生,因为除了在最高肝素浓度下的pcsk9以外,未观察到mrna变化(图6c)。
在通过iscripttmcdna合成试剂盒(biorad)从0.5μgrna模板进行cdna合成后,使用nucleospinrna制备试剂盒(macherey-nagel)进行从hepg2细胞提取rna。用iq
我们发现,25u/ml肝素有效对抗pcsk9活性,如从虽然pcsk9mrna增加两倍,但ldlr增加约2.5倍可显而易见(图8b)。
与肝素(50u/ml)一起孵育24h的hepg2细胞显示如通过蛋白质印迹所评估的增加的ldlr水平(图5a)。ldlr水平也通过光密度测定法(n=4)来定量(图5b)。与肝素一起孵育还导致培养基中的pcsk9水平增加,如通过elisa所测量(图5c)。
肝素不干扰pcsk9与ldlr之间的直接相互作用,如根据制造商方案通过pcsk9/ldlr结合分析所分析(图6a)(bpsbioscience)。简单来说,在肝素(5或50u/ml)或针对pcsk9的ldlr结合结构域(bpsbioscience71207号)产生的抗pcsk9抗体存在下,将微孔滴定板中涂布有ldlr细胞外结构域的孔与生物素化pcsk9一起孵育。在洗涤后,将孔与辣根过氧化物酶(hrp)标记的抗生蛋白链菌素一起孵育,并通过添加hrp底物来评价pcsk9与ldlr细胞外结构域的结合,并使用化学发光微板读取器来评估信号。
pcsk9与ldlr之间的相互作用不受肝素添加的影响,指示肝素与pcsk9的结合通过防止pcsk9与细胞表面hspg的相互作用而导致ldlr降解减少。
与磺达肝素(arixtra)(25、100或250μg/ml)一起孵育24h的hepg2细胞显示增加的ldlr水平,如通过蛋白质印迹所评估(图7)。这些结果指示,例如磺达肝素的肝素类似物与pcsk9的结合通过防止pcsk9与细胞表面hspg相互作用而导致ldlr降解减少。
实施例6:肝素模拟物防止pcsk9:ldlr相互作用。
过去100年间已研发出若干种模拟肝素结构的分子用于多种治疗应用,其中7种目前用于临床。这7种分子称为肝素模拟物并属于不同化学类别,包括多种寡糖、寡核苷酸和萘衍生物。测试肝素模拟物子集的结合pcsk9并增加hepg2细胞中的ldlr的能力(图9)。
使用微量热泳动(mst)来评价pcsk9与配体(舒拉明、硫酸葡聚糖5000、葡聚糖5000、硫酸戊聚糖和s-dc-36)之间的平衡结合亲和性(jerabek-willemsen等人,2011)。使用mo-l003monolithblue-nhs标记试剂盒(nanotempertechnologies)来标记pcsk9,并实现蛋白质对染料的1:1摩尔比的标记效率。pcsk9是以100nm的终浓度来应用。在1:1稀释液(在pbs+0.05%tween-20中)中滴定未标记的结合配偶体,其中最高浓度如下:舒拉明为15.4mm,硫酸葡聚糖5000为2.3mm,葡聚糖5000为2.3mm,硫酸戊聚糖为16.3mm并且s-dc-36为250μm。在标准品处理的毛细管(nanotempertechnologies)中在monolithnt.115仪器(nanotempertechnologies)上使用20%led和80%mst功率进行mst测量。激光的接通和断开时间分别为5s和35s。使用所有16个毛细管中的mst缓冲液中的100nm经标记pcsk9在与上文所提到相同的条件下进行阴性对照。对于舒拉明、硫酸葡聚糖5000和s-dc-36,在80%mst功率下从温度跃迁期获得结合曲线;并且对于硫酸戊聚糖,在80%mst功率下从热泳动+温度跃迁期获得结合曲线。对于每种结合配偶体,用graphpadprism6拟合s形剂量反应曲线以得到平均kd值。因为在高浓度舒拉明存在下观察到pcsk9的荧光猝灭,在mst装置上分析之前,通过用10%sds预处理pcsk9并随后将样品在90℃下加热15min来进行变性分析。这消除了猝灭效应,指示在非变性条件下pcsk9的荧光猝灭是由于实际配体结合事件所致。
如使用mst所测定,硫酸化寡糖硫酸葡聚糖(图9c)和硫酸戊聚糖(图9f)都直接结合到pcsk9,亲和性分别为179.5μm和381.3μm,并导致细胞ldlr的剂量依赖性增加(图9a-b和图9d-e),达到与对照相比约400%的平稳态,并且在此分析中显著优于他汀的最大效应。该相互作用依赖于硫酸基的存在,因为非硫酸化葡聚糖不显示对pcsk9的亲和性。硫酸化萘衍生物舒拉明(非洲昏睡病的抗寄生虫药物)以190μm亲和性结合pcsk9(图9h),导致高达15倍的ldlr增加(图9a、9g),伴随荧光标记的ldl颗粒的细胞摄取增加(图12)。进一步测试36聚体单链dna分子(硫代磷酸寡脱氧胞苷,s-dc-36)并发现,其以4.8μm的kd结合pcsk9(图9k)并在此浓度范围下显示有效抑制性效应(图9i-j)。
实施例7:pcsk9显示对具体糖组成和硫酸化模式的选择性。
为了剖析pcsk9与带负电的糖的相互作用的特异性和选择性,分析pcsk9与由固定的合成细胞外基质聚糖(包括肝素的确定链长度和硫酸化模式(图14a)以及相关糖胺聚糖硫酸角质素和硫酸皮肤素)组成的聚糖微阵列的结合。
包括类肝素硫酸/肝素、硫酸角质素、硫酸皮肤素和5kda天然肝素(santacruz)的合成寡糖的细胞外基质聚糖微阵列是如先前所述使用250μm点样溶液来制备(hecht等人,2009;depaz等人,2006)。在点样后,将微阵列载玻片在潮湿室中孵育过夜,之后进行三个水洗步骤并用50mm乙醇胺溶液(ph9)在50℃下猝灭1h,以移除剩余的反应基团。用水将载玻片洗涤三次,在室温下用pbs中的1%(w/v)bsa(ph7.4)封闭1h并通过离心(5min,300xg)干燥。将稀释于1%(w/v)bsa-pbs中的pcsk9(25μg/ml)在4℃下在潮湿室中孵育过夜。在使用0.1%(v/v)tween-pbs的三个洗涤步骤后,与稀释于1%bsa-pbs中的预孵育的0.1μg/ml人源化抗pcsk9mab和5μg/ml山羊抗人iggalexafluor647(lifetechnologies)在室温下一起孵育1h。用0.1%(v/v)tween-pbs将载玻片洗涤三次,用水冲洗一次并通过离心干燥。对于数据采集,用genepix4300微阵列扫描仪(moleculardevices,sunnyvale,ca,usa)通过在635nm下激发alexafluor647来扫描载玻片。光电倍增管值(pmt)经设定以揭示无饱和扫描。用genepixpro7软件(moleculardevices)确定中值荧光值。
pcsk9显示对由[4)-α-glcn-6,n-二硫酸(1→4)-α-idoa-2-硫酸-(1→]组成的肝素二糖重复的选择性,如从分别涵盖三个和两个重复的类肝素硫酸/肝素子结构i和vii的结合显而易见(图14b)。有效结合需要最少两个重复,因为对于仅由一个重复组成的类肝素硫酸/肝素子结构,未观察到结合。对glcn的氨基处的硫酸基以及glcn的碳6和idoa的碳2处的酯连接硫酸基的需求也通过比较与类肝素硫酸/肝素子结构肝素i、肝素ii和肝素iii的结合而显而易见。
这些结果证实了pcsk9对具体糖组成和硫酸化模式的偏好(图14b)。
实施例8:低分子量肝素的治疗性制剂保护ldlr免受pcsk9诱导的降解。
与低分子量肝素制剂法安明(1-100u/ml)或亭扎肝素钠(1-100u/ml)一起孵育过夜的hepg2细胞显示增加的ldlr水平,如通过蛋白质印迹所评估(图8a)。法安明和亭扎肝素钠的效应与肝素(图5a)和五糖arixtra(图7)的效应相当。
这些结果显示,在小分子pcsk9抑制剂研发中,使用肝素:pcks9复合物作为模板的基于结构的药物设计是可行的方法。
实施例9:在体内肝素保护ldlr免受pcsk9诱导的降解。
使小鼠(balb6/cjrj)经历单独的或与肝素(50u)组合的10μg人类重组pcsk9的单一静脉内给予(尾静脉)。注射后1小时,处死小鼠并收集肝组织。膜蛋白制剂中ldlr的蛋白质印迹分析显示,共注射肝素的小鼠的肝ldlr水平显著高于仅注射pcsk9的小鼠(图8b,在图8c中定量)。
这些结果显示,pcsk9:肝素相互作用可提供研发小分子pcsk9抑制剂的框架。
实施例10:降低不响应他汀治疗的患者的ldl胆固醇。
给具有升高ldl胆固醇的患者开具他汀治疗。该患者不响应他汀治疗。随后给该患者开具皮下注射25-500mg组合物的治疗,所述组合物包含经设计以阻断人类pcsk9中的hspg结合位点的肝素类似物。该注射是以1-28天的间隔进行。观察到ldl-c水平显著下降,显示非经肠给予肝素类似物可导致不响应他汀治疗的患者的ldl-c水平降低。
实施例11:使用针对pcsk9的hspg结合位点的肝素类似物降低ldl胆固醇。
给具有升高的ldl胆固醇水平的患者开具给予肝素类似物,所述肝素类似物经设计以阻断人类pcsk9的hspg结合位点。该化合物是以0.1-30mg/kg的剂量经口给予。观察到ldl-c水平显著降低,显示经口给予经设计以阻断人类pcsk9中的hspg结合位点的肝素类似物可导致患者的ldl-c水平下降。
实施例12:降低不响应他汀治疗的患者的ldl胆固醇。
患者接受针对升高的ldl-c水平的他汀治疗。然而,在ldl-c水平首先下降后,并且由于他汀诱导的pcsk9的表达增加,该治疗未成功地显著降低ldl-c水平。
除了他汀以外,向该患者给予抑制hspg与pcsk9的结合的化合物。该给予是每周并且以低剂量(25-150mg)的化合物与他汀的组合来进行。观察到ldl-c水平显著降低,并且达到ldl-c的所需水平。
这个实施例显示,向基于他汀的治疗补充给予肝素类似物可成功地降低ldl-c水平。
实施例13:具有突变的hspg结合位点的pcsk9无法升高ldl胆固醇水平。
通过不含cg二核苷酸的表达质粒(invivogen)的尾部高压注射使野生型pcsk9和pcsk9的hspg结合突变体在小鼠肝中过表达;与易被cg碱基对的甲基化所灭活的常规质粒相比,这些质粒展现长期表达。野生型pcsk9的过表达诱导增强的ldlr降解,导致升高的血清ldl胆固醇,并由此表现为“功能获得型”变体。pcsk9的hspg突变体表现为“功能丧失型”变体,由于ldl受体降解减少而产生较少升高的血清ldl胆固醇水平。
结果证实pcsk9hspg结合结构域对于动物中的ldl受体降解的关键作用。
实施例14:基于pcsk9与肝素和肝素模拟物的相互作用的小分子pcsk9抑制剂的基于结构的药物设计。
在hepg2细胞培养分析中测试选自低分子量肝素和肝素类似物的候选化合物的抑制pcsk9功能并提高ldlr水平的能力。使用肝素类似物磺达肝素(商品名arixtra)作为参考化合物。使用所获得的结构信息导出3-5个药效团模型,使用其筛选3百万种可购买化合物的现有数据库。选择50种化合物的基于多样性的集合在hepg2细胞中进行功能测试。成功的抑制剂有助于校准分子对接模型和可购买化合物的第二筛选。选择50种化合物用于购买和体外测试。随后在小鼠模型中测试三种最有前景的候选物,以评估对肝中ldlr水平和血浆中的胆固醇的体内效应。
实施例15:对候选pcsk9抑制剂的测试
使用具有在内源性鼠类pcsk9启动子控制下的人类pcsk9表达的ldlr杂合(ldlr+/-)型冠状动脉疾病小鼠模型进行候选pcsk9抑制剂的临床前测试。用pcsk9抑制剂将饲喂西餐饮食的动物治疗6-8个月的时间,之后在经解剖主动脉中脂肪沉积物的油红o染色后,通过显微镜检查评估动脉粥样硬化性斑块面积。在实验期间每隔一个月通过elisa评价胆固醇的血浆浓度。
这些研究将容许评估候选pcsk9抑制剂降低血清胆固醇的能力。
实施例16:硫酸葡聚糖和戊聚糖保护ldlr免受pcsk9诱导的降解
在经修饰多糖化合物的肝素模拟物类别中,在基于hepg2的体外细胞分析中测试硫酸葡聚糖(图9a-b)和戊聚糖(图9d-e)。过夜孵育后,通过蛋白质印迹评估ldlr水平,显示在用硫酸葡聚糖(0-200μg/ml)处理后,ldlr的浓度依赖性增加,其中ldlr上调多达3倍。戊聚糖(0-200μg/ml)孵育导致ldlr在从50μg/ml的浓度的4倍增加。
实施例17:戊聚糖对肝ldlr水平的效应
将戊聚糖-多硫酸酯注射到表达人类pcsk9的小鼠中以评估该物质保护ldlr免受pcsk9诱导的降解的能力。
这些研究将确认,给予戊聚糖在体内导致ldlr水平升高。
实施例18:戊聚糖对血清胆固醇水平的效应
通过经口或皮下注射戊聚糖-多硫酸酯治疗具有升高血清胆固醇的患者以评估该物质降低血清胆固醇的能力。根据制造商,戊聚糖-多硫酸酯是从消化道吸收,中值为摄入经口剂量后2小时。随后测量胆固醇水平。
这些研究将确认,戊聚糖导致降低的血清胆固醇水平。
实施例19:亭扎肝素钠级分的pcsk9抑制性效应
亭扎肝素钠(低分子量肝素)含有大小在5000到8000da范围内的肝素片段,并且是pcsk9活性的有效抑制剂。为了进一步鉴别pcsk9抑制性片段,通过尺寸排阻色谱对亭扎肝素钠进行分级分离(图18a)。在基于hepg2细胞的分析中测试所获得的级分抑制pcsk9和升高ldlr的细胞水平的能力(图18b)。在这个分析中,发现在与糖浓度20μm一起孵育过夜后,多个级分可升高ldlr水平(2-5倍)。最高ldlr水平是用尺寸排阻级分h6获得,其随后经历强阴离子交换(sax)色谱(图19a)。将hepg2细胞与所获得的sax级分(500nm)一起孵育,并评估ldlr水平(图19b)。sax级分i1、i8和i9含有具有pcsk9抑制性活性的肝素片段,并且在所测试浓度(500nm)下将ldlr水平增加多达2倍。
实施例20:在biacore分析中化合物(x)抑制pcsk9与肝素的结合。
使用与白蛋白(sigmaa4503)或肝素-白蛋白(sigmah0403)偶联的传感器芯片的biacore分析用于评估pcsk9与肝素之间的相互作用。该分析揭示,pcsk9以700pm的亲和常数结合到白蛋白-肝素(图20a),未观察到与偶联有白蛋白的对照传感器芯片的结合(图20b)。实施使用biacore分析的干扰分析以评价化合物(x)与pcsk9之间的结合。将100nmpcsk9的溶液与增加浓度的化合物(x)(0nm、10nm、100nm、1μm和10μm)一起孵育,随后将溶液输注在与肝素-白蛋白偶联的传感器芯片上。结合曲线揭示,化合物(x)抑制pcsk9与肝素-白蛋白传感器芯片的结合,估计ic50为50nm(图20c)。
实施例21:化合物(x)抑制pcsk9与肝素-琼脂糖珠粒的结合
在肝素-琼脂糖结合分析中测试化合物(x)对pcsk9与肝素/类肝素硫酸的结合的抑制。将肝素-琼脂糖珠粒(2μl)与pcsk9(1μg/ml)和增加浓度的化合物(x)(0-500μg/ml)在总体积150μl的10mmnah2po4中一起孵育。在4℃下旋转过夜后,珠粒沉淀,并通过elisa评估上清液中未沉淀pcsk9(游离pcsk9)的浓度。将每个样品中的游离pcsk9浓度针对不含肝素-琼脂糖珠粒的样品(输入对照)中的pcsk9水平标准化。包括含有可溶肝素(5mg/ml)的样品作为阳性对照(图16a)。在此分析中,化合物(x)(500-200μg/ml)完全抑制pcsk9与肝素-琼脂糖的相互作用。对于比较,添加可溶肝素导致50%抑制。这些结果显示,化合物(x)在体外有效抑制pcsk9与肝素的结合。
实施例22:化合物(x)在体外保护ldlr抵抗pcsk9。
与化合物(x)(0-200μg/ml)一起孵育24h的hepg2细胞显示浓度依赖性增加的ldlr水平,如通过细胞溶解产物的蛋白质印迹所评估和通过光密度测定法所定量(图16b)。将对照细胞在无添加剂的情况下(阴性对照)或与500μg/ml肝素一起(阳性对照)孵育。相对于在没有添加剂的情况下孵育的hepg2细胞的溶解产物中发现的水平来计算ldlr水平。化合物(x)孵育导致多达12倍高的ldlr水平。对于比较,与肝素(500μg/ml)一起孵育的细胞显示约3倍升高的ldlr。
这些实验显示,在hepg2细胞中,化合物(x)保护ldlr免受pcsk9诱导的降解。
实施例23:化合物(x)在体内抑制pcsk9诱导的ldlr降解
在注射pcsk9(10μg)之前60分钟使小鼠(balb6/cjrj)经历3.2μg化合物(x)的单一静脉内(尾静脉)给予。在pcsk9注射后60min通过蛋白质印迹评价pcsk9诱导的肝ldlr降解并通过光密度测定法定量(图16c)。向对照小鼠注射nacl或对照抑制剂依洛尤单抗(200μg),所述依洛尤单抗为市售pcsk9抑制性单克隆抗体(amgen)。相对于仅注射nacl的小鼠中的ldlr水平来计算ldlr水平。在未预先注射抑制剂并注射pcsk9的小鼠中,ldlr水平下降50%,而在注射化合物(x)(0.13mg/kg)或依洛尤单抗(8mg/kg)的小鼠中未观察到下降。
这些研究显示,在pcsk9注射前给予化合物(x)以显著较低的剂量与依洛尤单抗同样有效地保护ldlr。
实施例24:在hepg2细胞中化合物(x)对ldl-胆固醇清除的效应
将接种于96孔中的hepg2细胞与化合物(x)(200μg/ml)一起孵育过夜。第二天添加经dii荧光染料(thermofisherscientific)标记的ldl颗粒(5μg/ml)并在37℃下孵育4h。在用pbs洗涤细胞后,在激发/发射552/573nm下评估ldl颗粒的细胞摄取。在-80℃下孵育过夜后,使用cyquant细胞增殖分析(thermofisherscientific)对每孔细胞数进行定量。
这些研究将确认,pcsk9活性的化合物(x)抑制在体外增加ldl-胆固醇的摄取。
实施例25:在人类中化合物(x)对血清ldl-胆固醇水平的效应
用每周静脉内注射的化合物(x)(剂量)治疗具有升高血清ldl-胆固醇水平的患者6周,以评估化合物(x)作为ldl-胆固醇降低治疗的能力。ldl-胆固醇(hplc)是在治疗前以及在治疗期间一周一次取样的血液中测量。
这些研究将确认,在患有高胆固醇血症的人类中,化合物(x)降低血清ldl-胆固醇。
实施例26:硫酸化六聚体和18聚体肝素在体外抑制pcsk9功能
将hepg2细胞与0-200μg/ml含有平均1,3个硫酸基/二糖的异质性硫酸化六聚体或18聚体寡糖一起孵育。在过夜孵育后,收获细胞并通过蛋白质印迹分析ldlr的细胞水平(图17a)并通过光密度测定法进行定量(图17b)。在所测试最高浓度下(200μg/ml),与对照细胞相比,与这些肝素中的任一种一起孵育的细胞显示6-8倍增加的细胞ldlr水平。此外,在低到10μg/ml的浓度下,六聚体具有有效pcsk9抑制性效应。
实施例27:蔗糖八硫酸酯抑制pcsk9与肝素-琼脂糖珠粒的结合
在肝素-琼脂糖结合分析中测试对pcsk9与肝素/类肝素硫酸的结合的蔗糖八硫酸酯(图21a)抑制。将肝素-琼脂糖珠粒(2μl)与pcsk9(1μg/ml)和增加浓度的蔗糖八硫酸酯(0-500μg/ml)在总体积150μl的10mmnah2po4中一起孵育。在4℃下过夜孵育后,珠粒沉淀,并通过elisa评估上清液中未沉淀pcsk9(游离pcsk9)的浓度。相对于无肝素-琼脂糖珠粒的样品(输入对照)中的pcsk9浓度来计算游离pcsk9的百分比(图21b)。在此分析中,蔗糖八硫酸酯在500-250μg/ml浓度下抑制pcsk9与肝素-琼脂糖以及5mg/ml可溶肝素(阳性对照)的沉淀。这些结果显示,蔗糖八硫酸酯在体外有效抑制pcsk9与肝素的结合。
序列
seqidno:1:pcsk9蛋白-ncbi登录号:ng_009061.1
mgtvssrrswwplplllllllllgpagaraqededgdyeelvlalrseedglaeapehgttatfhrcakdpwrlpgtyvvvlkeethlsqsertarrlqaqaarrgyltkilhvfhgllpgflvkmsgdllelalklphvdyieedssvfaqsipwnleritppryradeyqppdggslvevylldtsiqsdhreiegrvmvtdfenvpeedgtrfhrqaskcdshgthlagvvsgrdagvakgasmrslrvlncqgkgtvsgtliglefirksqlvqpvgplvvllplaggysrvlnaacqrlaragvvlvtaagnfrddaclyspasapevitvgatnaqdqpvtlgtlgtnfgrcvdlfapgediigassdcstcfvsqsgtsqaaahvagiaammlsaepeltlaelrqrlihfsakdvineawfpedqrvltpnlvaalppsthgagwqlfcrtvwsahsgptrmatavarcapdeellscssfsrsgkrrgermeaqggklvcrahnafggegvyaiarccllpqancsvhtappaeasmgtrvhchqqghvltgcsshwevedlgthkppvlrprgqpnqcvghreasihascchapgleckvkehgipapqeqvtvaceegwtltgcsalpgtshvlgayavdntcvvrsrdvsttgstsegavtavaiccrsrhlaqasqelq*
参考文献
benimetskayaetal.(1995)nucleicacidsres23:4239-4245
birdetal.(1988)science242:423-426.
chanetal.(2009)procnatlacadsciusa.2009jun16;106(24):9820-5.doi:10.1073/pnas.0903849106
cunninghametal.(2007)natstructmolbiol.14(5):p.413-9.
depaz,j.l.,spillmann,d.&seeberger,p.h.,(2006)chemcommun(camb),3116-8
fisheretal.(2007)jbiolchem.282(28):p.20502-12.
greenbergas,avilad,hughesm,hughesa,mckinneyec,flajnik.(1995)nature.374,168-173.
gunsetal.,2009.britishjournalofpharmacology(2010),159,326-336
gustafsenetal.(2014)cellmetab19(2):p.310-8
hamers-castermanc,atarhoucht,muyldermanss,etal.(1993)nature.363(6428):446-8.
hecht,m.l.etal.(2009)jproteomeres8,712-20
herbertetal.,circres79,590-600(1996).
hollingeretal.(1993)proc.natl.acadsci.usa90:6444-6448.
hustonetal.(1988)proc.natl.acad.sci.usa85:5879-5883.
jerabek-willemsenetal.(2011)assaydrugdevtechnol.9(4):p.342-53.
kohlerandmilstein(1975)nature256:495.
lagaceetal.(2006)jclininvest.2006nov;116(11):2995-3005
lakoskietal.(2009)jclinendocrinolmetab.94(7):p.2537-43.
limaetal.,biochimbiophysacta.2009jun;1794(6):873-81.
lonberg,n.etal.(1994)nature368(6474):856-859.
munckpetersenetal(1999)emboj18(3):595-604.
mccoy,a.j.,etal.,structureofbeta-antithrombinandtheeffectofglycosylationonantithrombin'sheparinaffinityandactivity.jmolbiol,2003.326(3):p.823-33.
nour-eldinhh,hansenbgetal.(2006)nucleicacidsres.34(18):e122.
piperetal.(2007).structure,2007.15(5):p.545-52.
reitery,brinkmannu,etal.(1994)j.biol.chem.269(15):18327-31.
seidahetal.(2014)circres.2014mar14;114(6):1022-36.doi:10.1161/circresaha.114.301621
sheridan(2013).natbiotechnol.2013dec;31(12):1057-8.doi:10.1038/nbt1213-1057.
soderbergetal.,natmethods3,995-1000(2006).
steinetal.(1995)natmed1:1119-1121.
villiersbr,steinv,hollfelderf.(2010)proteinengdessel.23(1):1-8.
walleyk.r.etal.,curropincritcare.2016oct;22(5):464-9
wardes,güssowd,griffithsad,jonespt,winterg.(1989)nature341:544-546.
wozniak-knoppg,stadlmannj,rükerf(2012)plosone7(1):e30083.
yabukovetal.(1993)jbiolchem.268(25):18818-23.
xuandesko(2014)annurevbiochem.2014;83:129-57
序列表
<110>aarhusuniversitet
<120>治疗脂蛋白代谢障碍的化合物
<130>p4324pc00
<160>21
<170>patentinversion3.5
<210>1
<211>692
<212>prt
<213>智人
<220>
<221>结合
<222>(78)..(167)
<223>hspg结合位点
<220>
<221>misc_特征
<222>(93)..(93)
<223>r93
<220>
<221>misc_特征
<222>(96)..(96)
<223>r96
<220>
<221>misc_特征
<222>(97)..(97)
<223>r97
<220>
<221>misc_特征
<222>(104)..(104)
<223>r104
<220>
<221>misc_特征
<222>(105)..(105)
<223>r105
<220>
<221>misc_特征
<222>(136)..(136)
<223>k136
<220>
<221>misc_特征
<222>(139)..(139)
<223>h139
<220>
<221>misc_特征
<222>(165)..(165)
<223>r165
<220>
<221>misc_特征
<222>(167)..(167)
<223>r167
<400>1
metglythrvalserserargargsertrptrpproleuproleuleu
151015
leuleuleuleuleuleuleuglyproalaglyalaargalaglnglu
202530
aspgluaspglyasptyrglugluleuvalleualaleuargserglu
354045
gluaspglyleualaglualaprogluhisglythrthralathrphe
505560
hisargcysalalysaspprotrpargleuproglythrtyrvalval
65707580
valleulysglugluthrhisleuserglnsergluargthralaarg
859095
argleuglnalaglnalaalaargargglytyrleuthrlysileleu
100105110
hisvalphehisglyleuleuproglypheleuvallysmetsergly
115120125
aspleuleugluleualaleulysleuprohisvalasptyrileglu
130135140
gluaspserservalphealaglnserileprotrpasnleugluarg
145150155160
ilethrproproargtyrargalaaspglutyrglnproproaspgly
165170175
glyserleuvalgluvaltyrleuleuaspthrserileglnserasp
180185190
hisarggluilegluglyargvalmetvalthraspphegluasnval
195200205
proglugluaspglythrargphehisargglnalaserlyscysasp
210215220
serhisglythrhisleualaglyvalvalserglyargaspalagly
225230235240
valalalysglyalasermetargserleuargvalleuasncysgln
245250255
glylysglythrvalserglythrleuileglyleuglupheilearg
260265270
lysserglnleuvalglnprovalglyproleuvalvalleuleupro
275280285
leualaglyglytyrserargvalleuasnalaalacysglnargleu
290295300
alaargalaglyvalvalleuvalthralaalaglyasnpheargasp
305310315320
aspalacysleutyrserproalaseralaprogluvalilethrval
325330335
glyalathrasnalaglnaspglnprovalthrleuglythrleugly
340345350
thrasnpheglyargcysvalaspleuphealaproglygluaspile
355360365
ileglyalaserseraspcysserthrcysphevalserglnsergly
370375380
thrserglnalaalaalahisvalalaglyilealaalametmetleu
385390395400
seralagluprogluleuthrleualagluleuargglnargleuile
405410415
hispheseralalysaspvalileasnglualatrppheprogluasp
420425430
glnargvalleuthrproasnleuvalalaalaleuproproserthr
435440445
hisglyalaglytrpglnleuphecysargthrvaltrpseralahis
450455460
serglyprothrargmetalathralavalalaargcysalaproasp
465470475480
glugluleuleusercysserserpheserargserglylysargarg
485490495
glygluargmetglualaglnglyglylysleuvalcysargalahis
500505510
asnalapheglyglygluglyvaltyralailealaargcyscysleu
515520525
leuproglnalaasncysservalhisthralaproproalagluala
530535540
sermetglythrargvalhiscyshisglnglnglyhisvalleuthr
545550555560
glycysserserhistrpgluvalgluaspleuglythrhislyspro
565570575
provalleuargproargglyglnproasnglncysvalglyhisarg
580585590
glualaserilehisalasercyscyshisalaproglyleuglucys
595600605
lysvallysgluhisglyileproalaproglngluglnvalthrval
610615620
alacysglugluglytrpthrleuthrglycysseralaleuprogly
625630635640
thrserhisvalleuglyalatyralavalaspasnthrcysvalval
645650655
argserargaspvalserthrthrglyserthrsergluglyalaval
660665670
thralavalalailecyscysargserarghisleualaglnalaser
675680685
glngluleugln
690
<210>2
<211>318
<212>dna
<213>人工序列
<220>
<223>通过对大鼠杂交瘤bnt-8h4-b8/c7-e11、bnt-5e11-d4/g1-e4表达的免疫球蛋白基因的可变区进行测序获得的序列
<220>
<221>cds
<222>(1)..(318)
<223>bnt-8h4-b8/c7-e11_vk
<220>
<221>v_区
<222>(1)..(69)
<220>
<221>v_区段
<222>(70)..(102)
<223>cdr1
<220>
<221>v_区
<222>(103)..(147)
<220>
<221>v_区段
<222>(148)..(168)
<223>cdr2
<220>
<221>v_区
<222>(169)..(264)
<220>
<221>v_区段
<222>(265)..(288)
<223>cdr3
<220>
<221>j_区段
<222>(289)..(318)
<400>2
gatattgtgatgacccagtctccctcactcctgtctgcatctgtggga48
aspilevalmetthrglnserproserleuleuseralaservalgly
151015
gacagagtcactcttagctgcaaaggaagtcagaatattaacaattac96
aspargvalthrleusercyslysglyserglnasnileasnasntyr
202530
ttagcctggtaccaacaaaagctcggagaagctcccaaactcctgatc144
leualatrptyrglnglnlysleuglyglualaprolysleuleuile
354045
tataatacaaacagtttacaaacgggcatcccatcaaggttcagtggc192
tyrasnthrasnserleuglnthrglyileproserargphesergly
505560
agtggatctggtacagattgcacactcaccatcagaagcctgcagcct240
serglyserglythraspcysthrleuthrileargserleuglnpro
65707580
gaagatgttgccacatatttctgctatcagtataacaacgggaacacg288
gluaspvalalathrtyrphecystyrglntyrasnasnglyasnthr
859095
tttggaggtgggaccaagctggagctgaaa318
pheglyglyglythrlysleugluleulys
100105
<210>3
<211>106
<212>prt
<213>人工序列
<220>
<223>合成构建体
<400>3
aspilevalmetthrglnserproserleuleuseralaservalgly
151015
aspargvalthrleusercyslysglyserglnasnileasnasntyr
202530
leualatrptyrglnglnlysleuglyglualaprolysleuleuile
354045
tyrasnthrasnserleuglnthrglyileproserargphesergly
505560
serglyserglythraspcysthrleuthrileargserleuglnpro
65707580
gluaspvalalathrtyrphecystyrglntyrasnasnglyasnthr
859095
pheglyglyglythrlysleugluleulys
100105
<210>4
<211>336
<212>dna
<213>人工序列
<220>
<223>通过对大鼠杂交瘤bnt-8h4-b8/c7-e11、bnt-5e11-d4/g1-e4表达的免疫球蛋白基因的可变区进行测序获得的序列
<220>
<221>cds
<222>(1)..(336)
<223>bnt-5e11-d4/g1-e4_vk
<220>
<221>v_区
<222>(1)..(69)
<223>fwr1
<220>
<221>v_区段
<222>(70)..(117)
<223>cdr1
<220>
<221>v_区
<222>(118)..(162)
<223>fwr2
<220>
<221>v_区段
<222>(163)..(183)
<223>cdr2
<220>
<221>v_区
<222>(184)..(279)
<223>fwr3
<220>
<221>v_区段
<222>(280)..(306)
<223>cdr3
<220>
<221>j_区段
<222>(307)..(336)
<223>jk
<400>4
gatgttgtgttgacacaaactccagttttcctgtctgtcacacttgga48
aspvalvalleuthrglnthrprovalpheleuservalthrleugly
151015
gatcagacttctatatcttgtaggtctagtcagagtctggaatatagt96
aspglnthrserilesercysargserserglnserleuglutyrser
202530
gatggatacacttatttggaatggtacctacagaaaccgggccagtct144
aspglytyrthrtyrleuglutrptyrleuglnlysproglyglnser
354045
ccacagctcctcatctatgaagtttccaaccgattttctggggtccca192
proglnleuleuiletyrgluvalserasnargpheserglyvalpro
505560
gacaggttcattggcagtgggtcagggacagatttcaccctcaagatc240
aspargpheileglyserglyserglythraspphethrleulysile
65707580
agcagagtagagcctgaggacttgggagtttattactgcttccaaggt288
serargvalgluprogluaspleuglyvaltyrtyrcyspheglngly
859095
acacatgatcctctcacgttcggttctgggaccaagctggagatcaaa336
thrhisaspproleuthrpheglyserglythrlysleugluilelys
100105110
<210>5
<211>112
<212>prt
<213>人工序列
<220>
<223>合成构建体
<400>5
aspvalvalleuthrglnthrprovalpheleuservalthrleugly
151015
aspglnthrserilesercysargserserglnserleuglutyrser
202530
aspglytyrthrtyrleuglutrptyrleuglnlysproglyglnser
354045
proglnleuleuiletyrgluvalserasnargpheserglyvalpro
505560
aspargpheileglyserglyserglythraspphethrleulysile
65707580
serargvalgluprogluaspleuglyvaltyrtyrcyspheglngly
859095
thrhisaspproleuthrpheglyserglythrlysleugluilelys
100105110
<210>6
<211>336
<212>dna
<213>人工序列
<220>
<223>通过对大鼠杂交瘤bnt-8h4-b8/c7-e11、bnt-5e11-d4/g1-e4表达的免疫球蛋白基因的可变区进行测序获得的序列
<220>
<221>cds
<222>(1)..(336)
<223>bnt-5e11-d4/g1-e4_vh
<220>
<221>v_区
<222>(1)..(90)
<223>fwr1
<220>
<221>v_区段
<222>(91)..(108)
<223>cdr1
<220>
<221>v_区
<222>(109)..(150)
<223>fwr2
<220>
<221>v_区段
<222>(151)..(198)
<223>cdr2
<220>
<221>v_区
<222>(199)..(294)
<223>fwr3
<220>
<221>v_区段
<222>(295)..(303)
<223>cdr3
<220>
<221>j_区段
<222>(304)..(336)
<223>jh
<400>6
gaggtgcagctgcaggagtcaggacctggccttgtgaaaccttcacag48
gluvalglnleuglngluserglyproglyleuvallysprosergln
151015
tcactctccctcacctgttctgtcactggttacaccattaccagtggt96
serleuserleuthrcysservalthrglytyrthrilethrsergly
202530
tatgattggagctggatccggaggttcccaggaaatacaatggagtgg144
tyrasptrpsertrpileargargpheproglyasnthrmetglutrp
354045
atgggagacataagttacagtggtagcactaactacaacccatcgctc192
metglyaspilesertyrserglyserthrasntyrasnproserleu
505560
aaaagtcgagtctccattacaagagacacatccaagaatcagttcttc240
lysserargvalserilethrargaspthrserlysasnglnphephe
65707580
ctgcagttgaactctgtaactactggggatacagccacatattactgt288
leuglnleuasnservalthrthrglyaspthralathrtyrtyrcys
859095
gcaaaactacccggctggggccaaggcactctggtcactgtctcttca336
alalysleuproglytrpglyglnglythrleuvalthrvalserser
100105110
<210>7
<211>112
<212>prt
<213>人工序列
<220>
<223>合成构建体
<400>7
gluvalglnleuglngluserglyproglyleuvallysprosergln
151015
serleuserleuthrcysservalthrglytyrthrilethrsergly
202530
tyrasptrpsertrpileargargpheproglyasnthrmetglutrp
354045
metglyaspilesertyrserglyserthrasntyrasnproserleu
505560
lysserargvalserilethrargaspthrserlysasnglnphephe
65707580
leuglnleuasnservalthrthrglyaspthralathrtyrtyrcys
859095
alalysleuproglytrpglyglnglythrleuvalthrvalserser
100105110
<210>8
<211>354
<212>dna
<213>人工序列
<220>
<223>通过对大鼠杂交瘤bnt-8h4-b8/c7-e11、bnt-5e11-d4/g1-e4表达的免疫球蛋白基因的可变区进行测序获得的序列
<220>
<221>cds
<222>(1)..(354)
<223>bnt-8h4-b8/c7-e11_vh
<220>
<221>v_区
<222>(1)..(90)
<223>fwr1
<220>
<221>v_区段
<222>(91)..(111)
<223>cdr1
<220>
<221>v_区
<222>(112)..(153)
<223>fwr2
<220>
<221>v_区段
<222>(154)..(201)
<223>cdr2
<220>
<221>v_区
<222>(202)..(297)
<223>fwr3
<220>
<221>v_区段
<222>(298)..(321)
<223>cdr3
<220>
<221>j_区段
<222>(322)..(354)
<223>jh
<400>8
caggttactctgaaagagtctggccctgggatattgcagccttcccag48
glnvalthrleulysgluserglyproglyileleuglnprosergln
151015
accctcagtctgacttgctctttctctgggttttcactgagcagttca96
thrleuserleuthrcysserpheserglypheserleuserserser
202530
ggtatatgtgtgagctggattcgtcagccttcagggaagggtctggag144
glyilecysvalsertrpileargglnproserglylysglyleuglu
354045
tggctggcaactatttgttgggaggatagtaagggctacaacccttct192
trpleualathrilecystrpgluaspserlysglytyrasnproser
505560
ctgaagaaccggctcacgatctccaaggacacctccaacaaccaagca240
leulysasnargleuthrileserlysaspthrserasnasnglnala
65707580
ctcctcaggatcaccagtgtggacactgcagataccgccatttactac288
leuleuargilethrservalaspthralaaspthralailetyrtyr
859095
tgtgctcgggtttattactggtactttgacttctggggcccaggaacc336
cysalaargvaltyrtyrtrptyrpheaspphetrpglyproglythr
100105110
atggtcaccgtgtcctca354
metvalthrvalserser
115
<210>9
<211>118
<212>prt
<213>人工序列
<220>
<223>合成构建体
<400>9
glnvalthrleulysgluserglyproglyileleuglnprosergln
151015
thrleuserleuthrcysserpheserglypheserleuserserser
202530
glyilecysvalsertrpileargglnproserglylysglyleuglu
354045
trpleualathrilecystrpgluaspserlysglytyrasnproser
505560
leulysasnargleuthrileserlysaspthrserasnasnglnala
65707580
leuleuargilethrservalaspthralaaspthralailetyrtyr
859095
cysalaargvaltyrtyrtrptyrpheaspphetrpglyproglythr
100105110
metvalthrvalserser
115
<210>10
<211>6
<212>prt
<213>人工序列
<220>
<223>seqidno:7的cdr1
<400>10
serglytyrasptrpser
15
<210>11
<211>16
<212>prt
<213>人工序列
<220>
<223>seqidno:7的cdr2
<400>11
aspilesertyrserglyserthrasntyrasnproserleulysser
151015
<210>12
<211>3
<212>prt
<213>人工序列
<220>
<223>seqidno:7的cdr3
<400>12
leuprogly
1
<210>13
<211>16
<212>prt
<213>人工序列
<220>
<223>seqidno:5的cdr1
<400>13
argserserglnserleuglutyrseraspglytyrthrtyrleuglu
151015
<210>14
<211>7
<212>prt
<213>人工序列
<220>
<223>seqidno:5的cdr2
<400>14
gluvalserasnargpheser
15
<210>15
<211>9
<212>prt
<213>人工序列
<220>
<223>seqidno:5的cdr3
<400>15
pheglnglythrhisaspproleuthr
15
<210>16
<211>7
<212>prt
<213>人工序列
<220>
<223>seqidno:9的cdr1
<400>16
serserglyilecysvalser
15
<210>17
<211>16
<212>prt
<213>人工序列
<220>
<223>seqidno:9的cdr2
<400>17
thrilecystrpgluaspserlysglytyrasnproserleulysasn
151015
<210>18
<211>8
<212>prt
<213>人工序列
<220>
<223>seqidno:9的cdr3
<400>18
valtyrtyrtrptyrpheaspphe
15
<210>19
<211>11
<212>prt
<213>人工序列
<220>
<223>seqidno:3的cdr1
<400>19
lysglyserglnasnileasnasntyrleuala
1510
<210>20
<211>7
<212>prt
<213>人工序列
<220>
<223>seqidno:3的cdr2
<400>20
asnthrasnserleuglnthr
15
<210>21
<211>8
<212>prt
<213>人工序列
<220>
<223>seqidno:3的cdr3
<400>21
tyrglntyrasnasnglyasnthr
15
- 还没有人留言评论。精彩留言会获得点赞!