利用碱化剂的血液净化的制作方法
本发明涉及一种利用碱化剂的血液净化。
本申请基于2017年4月18日在日本提出申请的日本特愿2017-82423号、2017年4月24日在日本提出申请的日本特愿2017-85741号、2017年5月25日在日本提出申请的日本特愿2017-103935号以及2017年9月12日提出国际申请的申请pct/jp2017/032931而主张优先权,将其内容援引于本说明书中。
背景技术:
需要透析、移植的终末期肾衰竭(end-stagekidneydisease:eskd)患者在世界上日益增加。在日本也有增加趋势,2014年末的透析患者数达到32万人。
被认为是该eskd的候补的是慢性肾病(ckd)。ckd是不论原疾病如何,是包括慢性发展的肾病的概念,是包括由肾小球滤过量(gfr)表示的肾功能降低或者提示发现肾脏损伤的表现慢性地(3个月以上)持续的所有病态的概念。ckd不仅有发展成eskd的风险,而且有心血管疾病(cvd)等的高发病风险,因此,早期发现ckd并进行适当的治疗非常重要。迄今为止虽然确立了许多ckd治疗法,但尚不充分,进一步寻求肾保护剂的开发。
对于ckd,伴随肾清除率的降低,各种尿毒症物质在生物体内蓄积。其中,作为色氨酸的最终代谢产物的硫酸吲哚酚伴随ckd的发展而血中浓度增加,高浓度(100μm~1mm)的硫酸吲哚酚在血中蓄积。已知硫酸吲哚酚也与由肾脏的纤维化引起的肾损伤的发展、由血管钙化引起的cvd等ckd并发症密切相关,并有血清中的硫酸吲哚酚浓度与透析患者的死亡率、心血管事件发病率相关这样的报告(非专利文献1)。而且,认为通过使ckd患者的血中硫酸吲哚酚的浓度降低,能够抑制发展为eskd,能够抑制与肾衰竭相关的cvd的发病。实际上,在肠道内吸附作为硫酸吲哚酚的前体的吲哚而使血中硫酸吲哚酚浓度降低的球形吸附碳制剂(kremezin(注册商标))使ckd患者的透析导入延迟,改善动脉硬化(非专利文献2)。
另一方面,对于已发展的ckd患者,血中的碳酸氢根离子(hco3-)浓度变低,发病为代谢性酸中毒,因此,给予碳酸氢钠、柠檬酸制剂等碱化剂。而且,报告了通过给予作为碱化剂的碳酸氢钠,ckd的发展得到抑制(非专利文献3)。另外,报告了在由蛋白质过负荷引起的肾病动物模型中,碳酸氢钠的口服给予抑制由酸性尿引起的肾小管细胞损伤(非专利文献4)。
然而,对于通过对早期的ckd患者给予碱化剂而抑制肾损伤的发展并没有报告,对于尿毒症物质的血中浓度降低也没有报告。
现有技术文献
非专利文献
非专利文献1:barreto,f.c.,etal.:serumindoxylsulfateisassociatedwithvasculardiseaseandmortalityinchronickidneydiseasepatients.clin.j.am.soc.nephrol.,4:1551-1558,2009.
非专利文献2:nakamurat.,etal.:oraladsorbentast-120decreasescarotidintima-mediathicknessandarterialstiffnessinpatientswithchronicrenalfailure.kidneybloodpressres,27:121-6,2004.
非专利文献3:brito-ashurst,i.d.,etal.:bicarbonatesupplementationslowsprogressionofckdandimprovesnutritionalstatus.j.am.soc.nephrol.,20:2075-2084,2009.
非专利文献4:soumat.,etal.:luminalalkalinizationattenuatesproteinuria-inducedoxidativedamageinproximaltubularcells.j.am.soc.nephrol.,22:635-648,2011.
技术实现要素:
本发明的课题之一在于提供对肾病患者的血液净化有用的药物。本发明的另一个课题在于提供对慢性肾病的发展(慢性肾病的重症化)的抑制、尿毒症症状的治疗和预防以及透析导入的延迟有用的药物。本发明的另一个课题在于提供对抑制从急性肾病向慢性肾病的发展有用的药物。本发明的另一个课题在于提供用于促进尿毒症物质排出体外的食品。本发明的另一个课题在于提供肾功能维持用(例如,肾小管损伤抑制用、肾小管细胞保护用或肾小管功能维持用)的食品。本发明的另一个课题在于提供判定慢性肾病的发展抑制的方法、判定血中的尿毒症物质的浓度降低和/或尿毒症物质向尿中的排出促进的方法。
本发明人等为了实现上述课题进行了深入研究,结果发现使体液碱化的药剂对促进从肾病患者体内排泄尿毒症物质(例如,促进尿毒症物质向尿中排泄)有用,完成了本发明。
本发明在一个方面中,提供一种尿毒症物质向体外的排泄促进用药物组合物,包含碱化剂。
本发明在一个方面中,提供一种尿毒症物质的血中浓度降低用药物组合物,包含碱化剂。
本发明在一个方面中,提供一种慢性肾病的尿中排泄促进用药物组合物,包含碱化剂。
本发明在一个方面中,提供一种慢性肾病的尿毒症症状的改善用药物组合物,包含碱化剂。
本发明在一个方面中,提供一种慢性肾病的透析导入的延迟用药物组合物,包含碱化剂。
本发明在一个方面中,提供一种伴随慢性肾病的心血管系统疾病的治疗或预防用药物组合物,包含碱化剂。
本发明在一个方面中,提供一种从急性肾病向慢性肾病的发展抑制用药物组合物,包含碱化剂。
本发明在一个方面中,提供一种尿毒症物质的体外排泄促进用食品组合物,包含碱化剂。
本发明在一个方面中,提供一种判定慢性肾病的发展抑制的方法。
本发明在一个方面中,提供一种判定人血中的尿毒素的浓度降低和/或尿毒素向尿中的排出促进的方法。
即,本发明具有以下的方面。
(1)一种尿毒症物质的血中浓度降低用药物组合物,包含碱化剂。
(2)一种尿毒症物质的尿中排泄促进用药物组合物,包含碱化剂。
(3)一种尿毒症物质的体外排泄促进用药物组合物,包含碱化剂。
(4)根据(2)或(3)所述的药物组合物,其中,尿中排泄或体外排泄依赖于尿毒症物质的血中浓度。
(5)根据(1)~(4)中任一项所述的药物组合物,其中,对慢性肾病或急性肾病的患者进行给予。
(6)根据(1)~(5)中任一项所述的药物组合物,其中,尿毒症物质为选自硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和精氨基琥珀酸中的至少1种。
(7)根据(1)~(6)中任一项所述的药物组合物,其中,尿毒症物质为硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和精氨基琥珀酸。
(8)根据(1)~(6)中任一项所述的药物组合物,其中,尿毒症物质为硫酸吲哚酚、硫酸对甲酚和苯基乙酰基l谷氨酰胺。
(9)根据(1)~(6)中任一项所述的药物组合物,其中,尿毒症物质为硫酸吲哚酚和苯基乙酰基l谷氨酰胺。
(10)根据(1)~(6)中任一项所述的药物组合物,其中,尿毒症物质为硫酸吲哚酚和马尿酸。
(11)根据(1)~(6)中任一项所述的药物组合物,其中,尿毒症物质为苯基乙酰基l谷氨酰胺和硫酸对甲酚。
(12)根据(1)~(6)中任一项所述的药物组合物,其中,尿毒症物质为硫酸吲哚酚。
(13)一种慢性肾病的尿毒症症状的改善用药物组合物,包含碱化剂。
(14)一种慢性肾病的透析导入的延迟用药物组合物,包含碱化剂。
(15)一种伴随慢性肾病的心血管系统疾病的治疗或预防用药物组合物,包含碱化剂。
(16)根据(15)所述的药物组合物,其中,改善动脉硬化。
(17)一种慢性肾病的发展抑制用药物组合物,包含碱化剂。
(18)一种肾小管损伤的治疗或预防用药物组合物,包含碱化剂。
(19)根据(1)~(18)中任一项所述的药物组合物,其中,对早期的慢性肾病患者进行给予。
(20)根据(1)~(18)中任一项所述的药物组合物,其中,对阶段g3b以下的慢性肾病患者进行给予。
(21)根据(1)~(18)中任一项所述的药物组合物,其中,对阶段g2以上且g3b以下的慢性肾病患者进行给予。
(22)根据(1)~(18)中任一项所述的药物组合物,其中,对阶段g2和g3a的慢性肾病患者进行给予。
(23)根据(1)~(18)中任一项所述的药物组合物,其中,对阶段g2的慢性肾病患者进行给予。
(24)根据(1)~(18)中任一项所述的药物组合物,其中,对尿中的β2-微球蛋白浓度为290μg/l以下的患者进行给予。
(25)根据(1)~(18)中任一项所述的药物组合物,其中,对尿中的β2-微球蛋白浓度为50~150μg/l以下的患者进行给予。
(26)根据(1)~(18)中任一项所述的药物组合物,其中,对血中的半胱氨酸蛋白酶抑制剂c浓度为0.5~2.2mg/l以下的患者进行给予。
(27)根据(1)~(18)中任一项所述的药物组合物,其中,对血中的半胱氨酸蛋白酶抑制剂c浓度为1.0~1.3mg/l以下的患者进行给予。
(28)一种从急性肾病向慢性肾病的发展抑制用药物组合物,包含碱化剂。
(29)根据(1)~(28)中任一项所述的药物组合物,其中,碱化剂为柠檬酸的医药上可允许的盐、或其水合物或者它们的混合物。
(30)根据(1)~(29)中任一项所述的药物组合物,其中,碱化剂为柠檬酸钠、柠檬酸钾或其水合物或者它们的混合物。
(31)根据(1)~(30)中任一项所述的药物组合物,其中,碱化剂包含柠檬酸钠或其水合物与柠檬酸钾或其水合物的混合物。
(32)根据(1)~(31)中任一项所述的药物组合物,其中,碱化剂为柠檬酸钠或其水合物。
(33)根据(1)~(32)中任一项所述的药物组合物,其中,药物组合物为片剂。
(34)根据(1)~(33)中任一项所述的药物组合物,其中,在碱化剂的给予12周后检测到与碱化剂给予开始前相比尿毒症物质的血中浓度降低。
(35)根据(1)~(34)中任一项所述的药物组合物,其中,在碱化剂的给予12周后检测到与碱化剂给予开始前相比尿毒症物质的尿中浓度增加。
(36)根据(1)~(35)中任一项所述的药物组合物,其中,在碱化剂的给予12周后检测到与碱化剂给予开始前相比尿毒症物质的体外排泄增加。
(37)根据(1)~(36)中任一项所述的药物组合物,其中,通过碱化剂的给予,尿中的β2-微球蛋白浓度的增加得到抑制。
(38)根据(1)~(37)中任一项所述的药物组合物,其中,通过碱化剂的给予,在给予12周后,尿中的β2-微球蛋白浓度的增加得到抑制。
(39)根据(1)~(38)中任一项所述的药物组合物,其中,通过碱化剂的给予,与给予开始前相比,尿中的β2-微球蛋白浓度实质上没有降低。
(40)根据(1)~(39)中任一项所述的药物组合物,其中,通过碱化剂的给予,在给予12周后,与给予开始前相比,尿中的β2-微球蛋白浓度实质上没有降低。
(41)根据(1)~(40)中任一项所述的药物组合物,其中,通过碱化剂的给予,与给予开始前相比,血中的半胱氨酸蛋白酶抑制剂c实质上没有增加。
(42)根据(1)~(41)中任一项所述的药物组合物,其中,通过碱化剂的给予,与给予开始前相比,在给予12周后,血中的半胱氨酸蛋白酶抑制剂c实质上没有增加。
(43)根据(1)~(42)中任一项所述的药物组合物,其中,通过碱化剂的给予,与给予开始前相比,没有确认到近端肾小管损伤的改善和/或肾小球损伤改善,与给予开始前相比,确认到尿毒症物质的血中浓度降低、尿毒症物质的尿中排泄促进和/或尿毒症物质的体外排泄促进。
(44)根据(1)~(43)中任一项所述的药物组合物,其中,在碱化剂给予12周后,通过碱化剂的给予,与给予开始前相比,没有确认到近端肾小管损伤的改善和/或肾小球损伤改善,与给予开始前相比,确认到尿毒症物质的血中浓度降低、尿毒症物质的尿中排泄促进和/或尿毒症物质的体外排泄促进。
(45)根据(1)~(44)中任一项所述的药物组合物,其中,以1~3g/天给予碱化剂。
(46)根据(1)~(45)中任一项所述的药物组合物,其中,以1~1.5g/天给予碱化剂。
(47)根据(1)~(46)中任一项所述的药物组合物,其中,以晨尿的ph成为ph5.2~ph6.8的方式给予碱化剂。
(48)根据(1)~(47)中任一项所述的药物组合物,其中,以晨尿的ph成为ph6.0以上且小于ph6.2的方式给予碱化剂。
(49)根据(1)~(48)中任一项所述的药物组合物,其中,给予12周以上的碱化剂。
(50)根据(1)~(49)中任一项所述的药物组合物,其中,给予12周碱化剂。
(50-1)根据(1)~(50)中任一项所述的药物组合物,其中,通过碱化剂的给予,尿中的尿毒症物质的量增加。
(50-2)根据(1)~(50)和(50-1)中任一项所述的药物组合物,其中,通过碱化剂的给予,尿中的尿毒症物质的浓度增加。
(50-3)根据(1)~(50)、(50-1)和(50-2)中任一项所述的药物组合物,其中,通过碱化剂的给予,确认到尿毒症物质的血中浓度降低效果、尿中排泄促进效果和/或体外排泄促进效果,相对于给予安慰剂确认到该效果。
(50-4)根据(1)~(50)和(50-1)~(50-3)中任一项所述的药物组合物,其中,通过碱化剂的给予,发挥尿毒症物质的血中浓度降低效果、尿中排泄促进效果和/或体外排泄促进效果,相对于碱化剂给予前确认到该效果。
(50-5)根据(1)~(50)、和(50-1)~(50-4)中任一项所述的药物组合物,其中,药物组合物为片剂。
(50-6)根据(1)~(50)、和(50-1)~(50-5)中任一项所述的药物组合物,其中,尿为晨尿。
(51)一种尿毒症物质的血中浓度降低用、尿中排泄促进用和/或体外排泄促进用食品组合物,包含碱化剂。
(52)根据(51)所述的食品组合物,其中,碱化剂为柠檬酸碱金属盐或其水合物或者它们的混合物。
(52-1)根据(51)或(52)所述的食品组合物,其中,维持肾功能(抑制肾小管损伤、保护肾小管细胞或维持肾小管功能)。
(52-2)根据(51)、(52)和(52-1)中任一项所述的食品组合物,其中,以1~3g/天摄取碱化剂。
(52-3)根据(51)、(52)、(52-1)和(52-2)中任一项所述的食品组合物,其中,以1~1.5g/天摄取碱化剂。
(52-4)根据(51)、(52)和(52-1)~(52-3)中任一项所述的食品组合物,其中,与碱化剂摄取开始前相比或者与安慰剂摄取相比,尿毒症物质的血中浓度降低。
(52-5)根据(51)、(52)和(52-1)~(52-4)中任一项所述的食品组合物,其中,与碱化剂摄取开始前相比或者与安慰剂摄取相比,尿毒症物质的尿中浓度增加。
(52-6)根据(51)、(52)和(52-1)~(52-5)中任一项所述的食品组合物,其中,与碱化剂摄取开始前相比或者与安慰剂摄取相比,尿毒症物质的尿中量增加。
(52-7)根据(51)、(52)和(52-1)~(52-6)中任一项所述的食品组合物,其中,与碱化剂摄取开始前相比或者与安慰剂摄取相比,尿毒症物质的体外排泄增加。
(52-8)根据(51)、(52)和(52-1)~(52-7)中任一项所述的食品组合物,其中,通过碱化剂的摄取,尿中的β2-微球蛋白浓度的增加得到抑制。
(52-9)根据(51)、(52)和(52-1)~(52-8)中任一项所述的食品组合物,其中,通过碱化剂的摄取,与摄取前或安慰剂摄取相比,尿中的β2-微球蛋白浓度实质上没有降低。
(52-10)根据(51)、(52)和(52-1)~(52-9)中任一项所述的食品组合物,其中,通过碱化剂的摄取,血中的半胱氨酸蛋白酶抑制剂c实质上没有增加。
(52-11)根据(51)、(52)和(52-1)~(52-10)中任一项所述的食品组合物,其中,摄取12周以上的碱化剂。
(52-12)根据(51)、(52)和(52-1)~(52-11)中任一项所述的食品组合物,其中,摄取12周碱化剂。
(53)一种判定慢性肾病的发展抑制的方法,包括对尿的ph进行测定。
(54)一种判定慢性肾病患者的血中的尿毒症物质的浓度降低的方法,包括对尿的ph进行测定。
(55)一种判定慢性肾病患者的尿毒症物质向尿中的排出促进的方法,包括对尿的ph进行测定。
进而,本发明具有以下的方面。
(56)一种药物组合物,是包含碱化剂的尿毒症物质的血中浓度降低用药物组合物,其为片剂。
(57)一种药物组合物,是包含碱化剂的尿毒症物质的尿中排泄促进用药物组合物,其为片剂。
(58)根据(56)或(57)所述的药物组合物,其中,对慢性肾病或急性肾病的患者进行给予。
(59)根据(56)~(58)中任一项所述的药物组合物,其中,尿毒症物质为选自硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和精氨基琥珀酸中的至少1种。
(60)根据(56)~(59)中任一项所述的药物组合物,其中,尿毒症物质为硫酸吲哚酚。
(61)一种药物组合物,是包含碱化剂的慢性肾病的发展抑制用药物组合物,其为片剂。
(62)一种药物组合物,是包含碱化剂的肾小管损伤的治疗或预防用药物组合物,其为片剂。
(63)根据(56)~(62)中任一项所述的药物组合物,其中,碱化剂为柠檬酸的医药上可允许的盐、或其水合物或者它们的混合物。
(64)根据(56)~(63)中任一项所述的药物组合物,其中,碱化剂包含柠檬酸钠或其水合物与柠檬酸钾或其水合物的混合物。
进而,本发明具有以下的方面。
(65)一种食品组合物,包含碱化剂,用于维持肾功能。
(66)根据(65)所述的食品组合物,肾功能维持是肾小管损伤抑制、肾小管细胞保护或肾小管功能维持。
(67)根据(66)所述的食品组合物,其中,肾小管为近端肾小管。
(68)根据(65)~(67)中任一项所述的食品组合物,其中,碱化剂为柠檬酸的可允许作为食品的盐、或其水合物或者它们的混合物。
(69)根据(65)~(68)中任一项所述的食品组合物,其中,碱化剂包含柠檬酸钠或其水合物与柠檬酸钾或其水合物的混合物。
(70)根据(65)~(69)中任一项所述的食品组合物,其中,碱化剂为柠檬酸钠或其水合物。
(71)根据(65)~(70)中任一项所述的食品组合物,其中,食品组合物为片剂。
(72)根据(65)~(71)中任一项所述的食品组合物,其中,在食品组合物的包装、容器或说明书标示肾功能维持的效果。
(73)根据(65)~(71)中任一项所述的食品组合物,其中,在食品组合物的包装、容器或说明书标示肾小管损伤抑制、肾小管细胞保护或肾小管功能维持的效果。
(74)根据(65)~(72)中任一项所述的食品组合物,其中,被在意肾脏健康的健康人摄取。
(75)根据(65)~(71)和(73)中任一项所述的食品组合物,其中,被在意肾小管健康的健康人摄取。
(76)根据(65)~(75)中任一项所述的食品组合物,其中,被尿中的β2-微球蛋白浓度为290μg/l以下的对象摄取。
(77)根据(65)~(76)中任一项所述的食品组合物,其中,被尿中的β2-微球蛋白浓度为50~150μg/l的对象摄取。
(78)根据(65)~(77)中任一项所述的食品组合物,其中,被血中的半胱氨酸蛋白酶抑制剂c浓度为0.5~2.2mg/l的对象摄取。
(79)根据(65)~(78)中任一项所述的食品组合物,其中,被血中的半胱氨酸蛋白酶抑制剂c浓度为1.0~1.3mg/l的对象摄取。
(80)根据(65)~(79)中任一项所述的食品组合物,其中,通过食品组合物的摄取,尿中的β2-微球蛋白浓度的增加得到抑制。
(81)根据(65)~(80)中任一项所述的食品组合物,其中,通过食品组合物的摄取,在摄取12周后,尿中的β2-微球蛋白浓度的增加得到抑制。
(82)根据(65)~(81)中任一项所述的食品组合物,其中,通过食品组合物的摄取,与摄取开始前或安慰剂相比,尿中的β2-微球蛋白浓度实质上没有降低。
(83)根据(65)~(82)中任一项所述的食品组合物,其中,通过食品组合物的摄取,在摄取12周后,与摄取开始前或安慰剂相比,尿中的β2-微球蛋白浓度实质上没有降低。
(84)根据(65)~(83)中任一项所述的食品组合物,其中,通过食品组合物的摄取,与摄取开始前相比,血中的半胱氨酸蛋白酶抑制剂c实质上没有增加。
(85)根据(65)~(84)中任一项所述的食品组合物,其中,通过食品组合物的摄取,与安慰剂相比,血中的半胱氨酸蛋白酶抑制剂c实质上没有增加。
(86)根据(65)~(85)中任一项所述的食品组合物,其中,通过食品组合物的摄取,抑制与慢性肾病的病期发展相伴的晨尿中的β2-微球蛋白的量的增加。
(87)根据(65)~(86)中任一项所述的食品组合物,其中,通过食品组合物的摄取,不对慢性肾病患者的肾小球功能造成影响,另一方面,抑制与慢性肾病的病期发展相伴的近端肾小管细胞损伤,保护近端肾小管细胞。
通过本发明所提供的药物组合物等,哺乳动物中的尿毒症物质被排出到体外。通过本发明所提供的方法,能够初步判断尿毒症物质是否被排出到体外、和/或能否抑制慢性肾病的发展。通过本发明所提供的食品组合物等,能够维持哺乳动物的肾功能,更具体而言,能够抑制肾小管损伤、保护肾小管细胞或维持肾小管功能。
附图说明
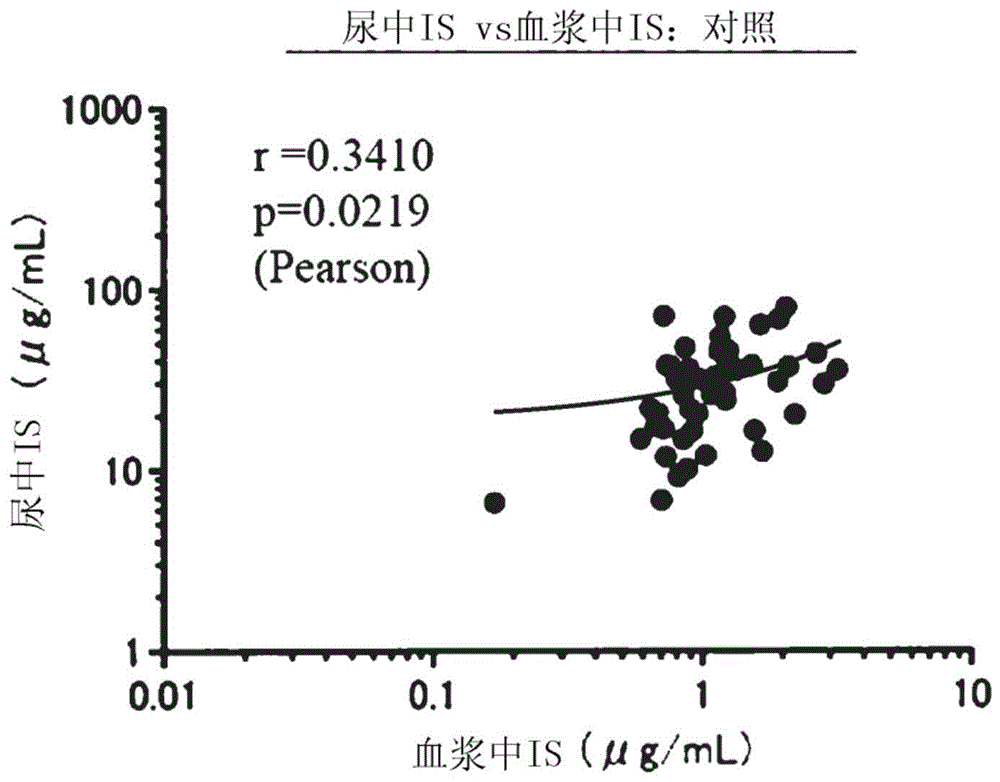
图1是表示试验开始6、12和24周后的对照组的患者中的尿中硫酸吲哚酚浓度与血浆中硫酸吲哚酚浓度的相关的图。
图2是表示试验开始6、12和24周后的柠檬酸钾·柠檬酸钠水合物配合制剂给予组的患者中的尿中硫酸吲哚酚浓度与血浆中硫酸吲哚酚浓度的相关的图。
图3是表示试验开始6、12和24周后的碳酸氢钠制剂给予组的患者中的尿中硫酸吲哚酚浓度与血浆中硫酸吲哚酚浓度的相关的图。
图4是表示试验开始6、12和24周后的全部患者中的尿中硫酸吲哚酚浓度与血浆中硫酸吲哚酚浓度的相关的图。
图5是表示试验开始6、12和24周后的对照组的患者中的尿中硫酸对甲酚浓度与血浆中硫酸对甲酚浓度的相关的图。
图6是表示试验开始6、12和24周后的柠檬酸钾·柠檬酸钠水合物配合制剂给予组的患者中的尿中硫酸对甲酚浓度与血浆中硫酸对甲酚浓度的相关的图。
图7是表示试验开始6、12和24周后的碳酸氢钠制剂给予组的患者中的尿中硫酸对甲酚浓度与血浆中硫酸对甲酚浓度的相关的图。
图8是表示试验开始6、12和24周后的全部患者中的尿中硫酸对甲酚浓度与血浆中硫酸对甲酚浓度的相关的图。
图9是表示试验开始6、12和24周后的对照组的患者中的尿中马尿酸浓度与血浆中马尿酸浓度的相关的图。
图10是表示试验开始6、12和24周后的柠檬酸钾·柠檬酸钠水合物配合制剂给予组的患者中的尿中马尿酸浓度与血浆中马尿酸浓度的相关的图。
图11是表示试验开始6、12和24周后的碳酸氢钠制剂给予组的患者中的尿中马尿酸浓度与血浆中马尿酸浓度的相关的图。
图12是表示试验开始6、12和24周后的全部患者中的尿中马尿酸浓度与血浆中马尿酸浓度的相关的图。
图13是表示试验开始6、12和24周后的对照组的患者中的尿中精氨基琥珀酸浓度与血浆中精氨基琥珀酸浓度的相关的图。
图14是表示试验开始6、12和24周后的柠檬酸钾·柠檬酸钠水合物配合制剂给予组的患者中的尿中精氨基琥珀酸浓度与血浆中精氨基琥珀酸浓度的相关的图。
图15是表示试验开始6、12和24周后的碳酸氢钠制剂给予组的患者中的尿中精氨基琥珀酸浓度与血浆中精氨基琥珀酸浓度的相关的图。
图16是表示试验开始6、12和24周后的全部患者中的尿中精氨基琥珀酸浓度与血浆中精氨基琥珀酸浓度的相关的图。
图17是表示试验开始6、12和24周后的对照组的患者中的尿中苯基乙酰基l谷氨酰胺浓度与血浆中苯基乙酰基l谷氨酰胺浓度的相关的图。
图18是表示试验开始6、12和24周后的柠檬酸钾·柠檬酸钠水合物配合制剂给予组的患者中的尿中苯基乙酰基l谷氨酰胺浓度与血浆中苯基乙酰基l谷氨酰胺浓度的相关的图。
图19是表示试验开始6、12和24周后的碳酸氢钠制剂给予组的患者中的尿中苯基乙酰基l谷氨酰胺浓度与血浆中苯基乙酰基l谷氨酰胺浓度的相关的图。
图20是表示试验开始6、12和24周后的全部患者的尿中苯基乙酰基l谷氨酰胺浓度与血浆中苯基乙酰基l谷氨酰胺浓度的相关的图。
具体实施方式
1.药物组合物
本发明所提供的药物组合物可以包含碱化剂作为有效成分。
碱化剂是指具有提高哺乳动物(特别是人)的体液、例如血液或尿的hco3-浓度、ph的能力的药剂。作为碱化剂的例子,可举出柠檬酸的医药上可允许的盐、或其水合物或者它们的混合物以及碳酸氢钠(小苏打)。作为柠檬酸的医药上可允许的盐的例子,可举出柠檬酸碱金属盐。作为柠檬酸碱金属盐的例子,可举出柠檬酸钾和柠檬酸钠,也可以分别为稳定的柠檬酸钾的一水合物(c6h5k3o7·h2o)和柠檬酸钠的二水合物(c6h5na3o7·2h2o)等水合物。
作为优选的碱化剂的例子,可举出柠檬酸钠、柠檬酸钾或其水合物或者它们的混合物,例如可以为柠檬酸钾的一水合物(c6h5k3o7·h2o)和柠檬酸钠的二水合物(c6h5na3o7·2h2o)的混合物。柠檬酸钾的一水合物(c6h5k3o7·h2o)和柠檬酸钠的二水合物(c6h5na3o7·2h2o)的混合比可以由本领域技术人员适当设定,例如,可以将柠檬酸钾的一水合物与柠檬酸钠的二水合物的摩尔比设定成相对于柠檬酸钾的一水合物1,柠檬酸钠的二水合物为0.01~100。也可以使混合比以摩尔比计约为1:1。
另外,优选的碱化剂的其它例子可举出柠檬酸钠或其水合物,例如可以为柠檬酸钠的二水合物(c6h5na3o7·2h2o)。
另外,优选的碱化剂的其它例子可举出柠檬酸钾或其水合物,例如可以为柠檬酸钾的一水合物(c6h5k3o7·h2o)。
在一个实施方式中,本发明的药物组合物中所含的碱化剂可以包含柠檬酸钠或其水合物与柠檬酸钾或其水合物的混合物。
在其它实施方式中,本发明的药物组合物中所含的碱化剂可以仅由柠檬酸钠或其水合物与柠檬酸钾或其水合物的混合物构成。
本说明书中,提及碱化剂(例如,柠檬酸钾的一水合物(c6h5k3o7·h2o)和柠檬酸钠的二水合物(c6h5na3o7·2h2o))的重量时,其重量可以为干燥重量。
本说明书中,尿毒症物质是指通过正常的肾来排泄的物质(废物、毒素等),因肾功能降低等某些原因而排泄功能降低时,在血中增加(蓄积)而引起尿毒症的症状或疾病的物质。尿毒症物质的例子可举出硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和精氨基琥珀酸。
其中,硫酸吲哚酚是通过肠内细菌由来自食物蛋白质的色氨酸生成的吲哚在肝脏中被氧化和硫酸轭合而生成的。硫酸吲哚酚在血中其大部分与白蛋白结合而存在,不会被代谢,对于健康人,可从肾脏排泄到尿中,但在肾病患者的情况下,由于肾脏功能降低而成为在血中以高浓度蓄积的状态。
作为尿毒症物质的硫酸吲哚酚不仅在肾病患者中引起尿毒症,而且成为使慢性肾病患者发展到透析导入的原因。
因此,通过使血中的硫酸吲哚酚浓度降低,肾病患者的尿毒症症状得到改善,能够治疗和/或预防尿毒症。另外,通过使血中的硫酸吲哚酚浓度降低,能够使慢性肾病患者的透析导入延迟。在一个实施方式中,慢性肾病患者为进行性的慢性肾病。
本说明书中,[a、b和/或c]这样的表达表示“选自a、b和c中的至少1种”。因此,例如,“硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和/或精氨基琥珀酸”表示“选自硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和精氨基琥珀酸中的至少1种”。
另外,作为尿毒症物质的硫酸吲哚酚引起心肌的纤维化、动脉硬化、血管平滑肌细胞的增殖、血管内皮细胞损伤、动脉壁的肥厚、大动脉的钙化等,并发作为慢性肾病患者的并发症之一的心血管系统疾病(例如,心衰竭、心肌梗塞)和/或作为脑血管系统疾病的中风等。
因此,通过使血中的硫酸吲哚酚浓度降低,能够抑制心肌的纤维化、动脉硬化、血管平滑肌细胞的增殖、血管内皮细胞损伤、动脉壁的肥厚、大动脉的钙化等,治疗和/或预防作为慢性肾病患者的并发症之一的心血管系统疾病和/或脑血管系统疾病。
在一个方面中,本发明所提供的药物组合物能够使血中的尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸、精氨基琥珀酸和其组合)的浓度降低。硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸、精氨基琥珀酸和其组合的例子可举出硫酸吲哚酚、硫酸对甲酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和硫酸对甲酚;硫酸吲哚酚和马尿酸;硫酸吲哚酚和苯基乙酰基l谷氨酰胺;硫酸对甲酚和苯基乙酰基l谷氨酰胺;马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚;硫酸对甲酚;马尿酸;和苯基乙酰基l谷氨酰胺。
本说明书中,“血中的尿毒症物质的浓度的降低”是指与本发明所提供的药物组合物的给予前的血中的尿毒症物质的浓度相比,给予后的血中的尿毒症物质的浓度降低,或者是指通过给予本发明所提供的药物组合物,与给予安慰剂相比,血中的尿毒症物质的浓度降低。
在一个实施方式中,通过给予本发明所提供的药物组合物,与给予前相比,血中的尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸、精氨基琥珀酸和其组合(例如,硫酸吲哚酚、硫酸对甲酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和硫酸对甲酚;硫酸吲哚酚和马尿酸;硫酸吲哚酚和苯基乙酰基l谷氨酰胺;硫酸对甲酚和苯基乙酰基l谷氨酰胺;马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚;硫酸对甲酚;马尿酸;或苯基乙酰基l谷氨酰胺))的浓度降低,其降低量为给予前的尿毒症物质的血中浓度的1~5%、3~5%、1~10%、3~10%、5~10%、1~15%、3~15%、5~15%、1~30%、1~40%、3~40%、5~40%、1~50%、3~50%、5~50%、30~50%、1~60%、5%以上、10%以上或30%以上。
在一个实施方式中,尿毒症物质的血中浓度的降低量由以下的计算式(1)计算。
尿毒症物质的血中浓度的降低量(%)=[(药物组合物给予前的尿毒症物质的血中浓度(ng/ml)-药物组合物给予后的尿毒症物质的血中浓度(ng/ml))/药物组合物给予前的尿毒症物质的血中浓度(ng/ml)]×100(1)
在一个实施方式中,通过本发明所提供的药物组合物的6、12或24周的连续给予,与给予前相比,血中的尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸、精氨基琥珀酸和其组合(例如,硫酸吲哚酚、硫酸对甲酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和硫酸对甲酚;硫酸吲哚酚和马尿酸;硫酸吲哚酚和苯基乙酰基l谷氨酰胺;硫酸对甲酚和苯基乙酰基l谷氨酰胺;马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚;硫酸对甲酚;马尿酸;或苯基乙酰基l谷氨酰胺))的浓度降低,其降低量为给予前的尿毒症物质的血中浓度的1~5%、3~5%、1~10%、3~10%、5~10%、1~15%、3~15%、5~15%、1~30%、1~40%、3~40%、5~40%、1~50%、3~50%、5~50%、30~50%、1~60%、5%以上、10%以上或30%以上。
在一个方面中,本发明所提供的药物组合物能够促进尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸、精氨基琥珀酸和其组合)向尿中的排泄。硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸、精氨基琥珀酸和其组合的例子可举出硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和精氨基琥珀酸;硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚、硫酸对甲酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和马尿酸;硫酸吲哚酚和苯基乙酰基l谷氨酰胺;马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和硫酸对甲酚;硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸对甲酚和马尿酸;硫酸吲哚酚和精氨基琥珀酸;硫酸对甲酚和精氨基琥珀酸;马尿酸和精氨基琥珀酸;苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚;硫酸对甲酚;马尿酸;精氨基琥珀酸;和苯基乙酰基l谷氨酰胺。
本说明书中,“尿毒症物质向尿中的排泄的促进”是指与本发明所提供的药物组合物的给予前的尿中的尿毒症物质的浓度相比,给予后的尿中的尿毒症物质的浓度增加,是指通过本发明所提供的药物组合物的给予,与安慰剂给予相比,尿中的尿毒症物质的浓度增加,是指与本发明所提供的药物组合物的给予前的尿中的尿毒症物质的量相比,给予后的尿中的尿毒症物质的量增加,或者是指通过本发明所提供的药物组合物的给予,与安慰剂给予相比,尿中的尿毒症物质的量增加。
本说明书中,“尿中”例如是指“晨尿中”。
在一个实施方式中,通过本发明所提供的药物组合物的给予,与给予前相比,尿中的尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸、精氨基琥珀酸和其组合(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和精氨基琥珀酸;硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚、硫酸对甲酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和马尿酸;硫酸吲哚酚和苯基乙酰基l谷氨酰胺;马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和硫酸对甲酚;硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸对甲酚和马尿酸;硫酸吲哚酚和精氨基琥珀酸;硫酸对甲酚和精氨基琥珀酸;马尿酸和精氨基琥珀酸;苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚;硫酸对甲酚;马尿酸;精氨基琥珀酸;或苯基乙酰基l谷氨酰胺))的浓度增加1~100%、1~50%、3~50%、5~50%、10~50%、15~50%、1~40%、5~40%、10~40%、1~30%、5~30%、10~30%、15~30%、10%以上、20%以上、30%以上或40%以上。
在一个实施方式中,尿毒症物质的尿中浓度的增加量由以下的计算式(2)计算。
尿毒症物质的尿中浓度的增加量(%)=[(药物组合物给予后的尿毒症物质的尿中浓度(ng/ml)-药物组合物给予前的尿毒症物质的尿中浓度(ng/ml))/药物组合物给予前的尿毒症物质的尿中浓度(ng/ml)]×100(2)
在一个实施方式中,通过本发明所提供的药物组合物的6、12或24周的连续给予,与给予前相比,尿中的尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸、精氨基琥珀酸和其组合(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和精氨基琥珀酸;硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚、硫酸对甲酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和马尿酸;硫酸吲哚酚和苯基乙酰基l谷氨酰胺;马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和硫酸对甲酚;硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸对甲酚和马尿酸;硫酸吲哚酚和精氨基琥珀酸;硫酸对甲酚和精氨基琥珀酸;马尿酸和精氨基琥珀酸;苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚;硫酸对甲酚;马尿酸;精氨基琥珀酸;或苯基乙酰基l谷氨酰胺))的浓度增加1~100%、1~50%、3~50%、5~50%、10~50%、15~50%、1~40%、5~40%、10~40%、1~30%、5~30%、10~30%、15~30%、10%以上、20%以上、30%以上或40%以上。
在一个方面中,本发明所提供的药物组合物能够促进尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸、精氨基琥珀酸和其组合)从血中向尿中排泄,促进向体外排泄。硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸、精氨基琥珀酸和其组合的例子可举出硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和精氨基琥珀酸;硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚、硫酸对甲酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和马尿酸;硫酸吲哚酚和苯基乙酰基l谷氨酰胺;马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和硫酸对甲酚;硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸对甲酚和马尿酸;硫酸吲哚酚和精氨基琥珀酸;硫酸对甲酚和精氨基琥珀酸;马尿酸和精氨基琥珀酸;苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚;硫酸对甲酚;马尿酸;精氨基琥珀酸;和苯基乙酰基l谷氨酰胺。
在一个实施方式中,通过本发明所提供的药物组合物的给予,与尿中的尿毒症物质的浓度相对于本发明所提供的药物组合物的给予前的血中尿毒症物质浓度之比相比,尿中的尿毒症物质的浓度相对于给予后的血中尿毒症物质浓度之比增加。在一个实施方式中,通过本发明所提供的药物组合物的给予,与安慰剂给予相比,尿中的尿毒症物质的浓度相对于血中尿毒症物质浓度之比增加。
在一个实施方式中,通过本发明所提供的药物组合物的给予,与给予前相比,尿中的尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸、精氨基琥珀酸和其组合(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和精氨基琥珀酸;硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚、硫酸对甲酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和马尿酸;硫酸吲哚酚和苯基乙酰基l谷氨酰胺;马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和硫酸对甲酚;硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸对甲酚和马尿酸;硫酸吲哚酚和精氨基琥珀酸;硫酸对甲酚和精氨基琥珀酸;马尿酸和精氨基琥珀酸;苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚;硫酸对甲酚;马尿酸;精氨基琥珀酸;或苯基乙酰基l谷氨酰胺))的浓度相对于血中浓度之比(尿中浓度(ng/ml)/血中浓度(ng/ml))增加1~100%、1~50%、3~50%、5~50%、10~50%、15~50%、1~40%、5~40%、10~40%、1~30%、5~30%、10~30%、15~30%、10%以上、20%以上、30%以上或40%以上。
在一个实施方式中,尿毒症物质的尿中浓度相对于血中浓度之比(尿中浓度(ng/ml)/血中浓度(ng/ml))的增加量由以下的计算式(3)计算。
尿毒症物质的尿中浓度相对于血中浓度之比的增加量(%)=[(药物组合物给予后的尿毒症物质的尿中浓度相对于血中浓度之比-药物组合物给予前的尿毒症物质的尿中浓度相对于血中浓度之比)/药物组合物给予前的尿毒症物质的尿中浓度相对于血中浓度之比]×100(3)
在一个实施方式中,通过本发明所提供的药物组合物的6、12或24周的连续给予,与给予前相比,尿中的尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸、精氨基琥珀酸和其组合(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和精氨基琥珀酸;硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚、硫酸对甲酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸吲哚酚、苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚、马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和马尿酸;硫酸吲哚酚和苯基乙酰基l谷氨酰胺;马尿酸和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和硫酸对甲酚;硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸对甲酚和马尿酸;硫酸吲哚酚和精氨基琥珀酸;硫酸对甲酚和精氨基琥珀酸;马尿酸和精氨基琥珀酸;苯基乙酰基l谷氨酰胺和精氨基琥珀酸;硫酸吲哚酚;硫酸对甲酚;马尿酸;精氨基琥珀酸;或苯基乙酰基l谷氨酰胺))的浓度相对于血中浓度之比(尿中浓度(ng/ml)/血中浓度(ng/ml))增加1~100%、1~50%、3~50%、5~50%、10~50%、15~50%、1~40%、5~40%、10~40%、1~30%、5~30%、10~30%、15~30%、10%以上、20%以上、30%以上或40%以上。
在一个实施方式中,通过本发明所提供的药物组合物的给予,依赖于尿毒症物质的血中浓度而促进尿毒症物质向体外的排泄。
在一个实施方式中,通过本发明所提供的药物组合物的给予,依赖于尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸、精氨基琥珀酸和其组合)的血中浓度而促进尿毒症物质向尿中的排泄。例如,在尿毒症物质的血中浓度为高值的情况下,与其相应地,该尿毒症物质向尿中的排泄量成为高值。在尿毒症物质的血中浓度为低值的情况下,尿毒症物质向尿中的排泄量成为低值。这样的依赖于血中浓度的尿毒症物质的尿中排泄表明本发明所提供的药物组合物的副作用的风险低、安全性优异。硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸、精氨基琥珀酸和其组合的例子可举出硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和精氨基琥珀酸;硫酸吲哚酚、硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和硫酸对甲酚;硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸吲哚酚;硫酸对甲酚;和苯基乙酰基l谷氨酰胺。
在一个实施方式中,通过本发明所提供的药物组合物的给予,依赖于尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸、精氨基琥珀酸和其组合)的血中浓度而促进尿毒症物质向尿中的排泄,由此尿毒症物质的血中浓度降低。硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸、精氨基琥珀酸和其组合的例子可举出硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和精氨基琥珀酸;硫酸吲哚酚、硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和苯基乙酰基l谷氨酰胺;硫酸吲哚酚和硫酸对甲酚;硫酸对甲酚和苯基乙酰基l谷氨酰胺;硫酸吲哚酚;硫酸对甲酚;和苯基乙酰基l谷氨酰胺。
在一个实施方式中,通过本发明所提供的药物组合物的给予,依赖于硫酸吲哚酚的血中浓度而将硫酸吲哚酚排泄到尿中,结果硫酸吲哚酚的尿中浓度相对于血中浓度之比(尿中浓度/血中浓度)可成为1~1000,优选可成为1~200,更优选可成为1~100,进一步更优选可成为10~100。该实施方式中,本发明所提供的药物组合物可以对硫酸吲哚酚的血中浓度为0.01~100μg/ml(例如,0.1~30μg/ml)的人(例如,慢性肾病患者)进行给予。另外,进行给予的结果,硫酸吲哚酚的血中浓度可成为0.01~10μg/ml(例如,0.03~10μg/ml)。
在一个实施方式中,通过本发明所提供的药物组合物的给予,依赖于硫酸对甲酚的血中浓度而将硫酸对甲酚排泄到尿中,结果硫酸对甲酚的尿中浓度相对于血中浓度之比(尿中浓度/血中浓度)可成为0.1~1000,优选可成为1~300,更优选可成为1~150,进一步更优选可成为1~100。该实施方式中,本发明所提供的药物组合物可以对硫酸对甲酚的血中浓度为0.003~300μg/ml(例如,0.01~30μg/ml)的人(例如,慢性肾病患者)进行给予。另外,进行给予的结果,硫酸对甲酚的血中浓度可成为0.001~100μg/ml(例如,0.001~30μg/ml)。
在一个实施方式中,通过本发明所提供的药物组合物的给予,依赖于苯基乙酰基l谷氨酰胺的血中浓度而将苯基乙酰基l谷氨酰胺排泄到尿中,结果苯基乙酰基l谷氨酰胺的尿中浓度相对于血中浓度之比(尿中浓度/血中浓度)可成为1~1500,优选可成为1~1000,更优选可成为10~800,进一步更优选可成为可成为10~600。该实施方式中,本发明所提供的药物组合物可以对苯基乙酰基l谷氨酰胺的血中浓度为0.03~30μg/ml(例如,0.1~10μg/ml)的人(例如,慢性肾病患者)进行给予。另外,进行给予的结果,苯基乙酰基l谷氨酰胺的血中浓度可成为0.01~10μg/ml(例如,0.03~10μg/ml)。
在一个实施方式中,通过将本发明所提供的药物组合物对多个人(例如,慢性肾病患者)进行给予,各个体的硫酸吲哚酚的尿中浓度相对于血中浓度之比(尿中浓度/血中浓度)显示高相关性。该实施方式中,高相关性可以通过利用pearson检验得到的r值为0.4以上且1以下、0.5以上且1以下、0.6以上且1以下或0.7以上且1以下(优选为0.7以上且1以下)来表示。另外,本发明所提供的药物组合物可以对硫酸吲哚酚的血中浓度为0.01~10μg/ml(例如,0.1~10μg/ml)的人(例如,慢性肾病患者)进行给予,进行给予的结果,硫酸吲哚酚的血中浓度可成为0.01~10μg/ml(例如,0.1~10μg/ml)。
在一个实施方式中,通过将本发明所提供的药物组合物对多个人(例如,慢性肾病患者)进行给予,各个体的硫酸对甲酚的尿中浓度相对于血中浓度之比(尿中浓度/血中浓度)显示高相关性。该实施方式中,高相关性可以通过利用pearson检验得到的r值为0.4以上且1以下、0.5以上且1以下、0.6以上且1以下或0.7以上且1以下(优选为0.7以上且1以下)来表示。另外,本发明所提供的药物组合物可以对硫酸对甲酚的血中浓度为0.001~100μg/ml(例如,0.01~50μg/ml)的人(例如,慢性肾病患者)进行给予,进行给予的结果,硫酸对甲酚的血中浓度可成为0.001~100μg/ml(例如,0.01~50μg/ml)。
在一个实施方式中,通过将本发明所提供的药物组合物对多个人(例如,慢性肾病患者)进行给予,各个体的苯基乙酰基l谷氨酰胺的尿中浓度相对于血中浓度之比(尿中浓度/血中浓度)显示高相关性。该实施方式中,高相关性可以通过利用pearson检验得到的r值为0.4以上且1以下、0.5以上且1以下、0.6以上且1以下或0.7以上且1以下(优选为0.7以上且1以下)来表示。另外,本发明所提供的药物组合物可以对苯基乙酰基l谷氨酰胺的血中浓度为0.01~10μg/ml(例如,0.05~10μg/ml)的人(例如,慢性肾病患者)进行给予,进行给予的结果,苯基乙酰基l谷氨酰胺的血中浓度可成为0.01~10μg/ml(例如,0.05~10μg/ml)。
通过这样的本发明所提供的药物组合物的特征,本发明所提供的药物组合物在一个方面中不仅可作为尿毒症物质的血中浓度降低用药物组合物和/或尿毒症物质的尿中排泄促进用药物组合物使用,而且也可作为肾病患者的尿毒症症状的改善用药物组合物、肾病患者的尿毒症的治疗和/或预防用药物组合物、慢性肾病的发展抑制用药物组合物和慢性肾病患者的透析导入的延迟用药物组合物中的任一者来使用。
本说明书中,“改善”是包括使“病态的”或“异常的”症状、状态或疾病接近“健康的”或“正常的”状态或以其为目的,以及成为“健康的”或“正常的”状态或以其为目的的概念。因此,在1个实施方式中,“改善”包括作为“病态的”或“异常的”症状或状态的指标的数值随着上述“改善”而变小或变大而接近正常的值或成为正常的值。在其它实施方式中,“改善”包括随着上述“改善”,血中的尿毒症物质的浓度变小,并包括尿中的尿毒症物质的浓度变大,进而,在血中的尿毒症物质的浓度变得充分小时,尿中的尿毒症物质的浓度也可以转为减少。
本说明书中,“健康”表示没有急性或慢性的疾病或损伤的状态,“正常”表示健康的对象处于通常所表现的状态。
本说明书中,“治疗”是包括使“病态的”或“异常的”症状、状态或疾病消失、完全治愈、治愈或缓解和以其为目的,包括抑制“病态的”或“异常的”症状、状态或疾病的恶化和以为目的,并且包括上述“改善”的概念。在此,抑制具有后述的含义。在一个实施方式中,“治疗”是指使“病态的”或“异常的”症状、状态或疾病消失、完全治愈、治愈或缓解和以其为目的。在其它实施方式中,“治疗”是指使“病态的”或“异常的”症状、状态或疾病消失、完全治愈、治愈或缓解。
本说明书中,“预防”是包括将“病态的”或“异常的”症状、状态或疾病的发病防止于未然和以其为目的的概念。
本说明书中,“延迟”是包括将至成为对象的事件的时间延长和以其为目的,并且包括延长时间以便不会表现出成为上述对象的事件的概念。
本说明书中,“抑制”是包括使症状、状态或疾病的恶化或发展停止或减速和以其为目的,并且包括改善上述症状、状态或疾病或为其为目的的概念。在此,改善具有上述的含义。上述“症状、状态或疾病的恶化或发展”包括“病态的”或“异常的”症状、状态或疾病的恶化或发展以及从“健康的”或“正常的”状态向“病态的”或“异常的”症状、状态或疾病的恶化或发展。在一个实施方式中,“抑制”是指使症状、状态或疾病的恶化或发展停止或减速或以此为目的。在其它实施方式中,“抑制”是指使症状、状态或疾病的恶化或发展停止或减速。
在此,上述症状、状态或疾病在本发明所提供的药物组合物的给予前和给予后进行比较。
另外,通过如上所述的本发明所提供的药物组合物的特征,本发明所提供的药物组合物在一个方面中,也可以作为肾病患者的心肌的纤维化抑制用药物组合物、肾病患者的动脉硬化抑制用药物组合物、肾病患者的血管平滑肌细胞的增殖抑制用药物组合物、肾病患者的血管内皮细胞损伤抑制用药物组合物、肾病患者的动脉壁的肥厚抑制用药物组合物、肾病患者的大动脉的钙化抑制用药物组合物和伴随慢性肾病的心血管系统疾病的治疗和/或预防用药物组合物中的任一种使用。
进而,由于报告了对非糖尿病性慢性肾病患者给予使硫酸吲哚酚的血中浓度降低的药剂时,作为动脉硬化的指标的脉搏波传播速度和颈动脉内膜中膜复合体厚度与给予前相比显著地改善(nakamurat.,etal.:oraladsorbentast-120decreasescarotidintima-mediathicknessandarterialstiffnessinpatientswithchronicrenalfailure.kidneybloodpressres,27:121-6,2004.),因此,使硫酸吲哚酚的血中浓度降低的本发明所提供的药物组合物在一个方面中,可以作为肾病患者(优选为慢性肾病患者,更优选为非糖尿病性慢性肾病患者)的动脉硬化的改善用药物组合物或动脉(例如,颈动脉)壁的肥厚改善用药物组合物使用。
另外,报告了使硫酸吲哚酚的血中浓度降低的药剂抑制由顺铂引起的急性肾损伤(morisakit.,et.al.,:regulationofrenalorganiciontransportersincisplatin-inducedacutekidneyinjuryanduremiainrats.pharm.res.,25(11):2526-33,2008)。因此,使硫酸吲哚酚的血中浓度降低的本发明所提供的药物组合物在一个方面中,可以作为急性肾病的治疗用药物组合物或从急性肾病向慢性肾病的发展抑制用药物组合物使用。
另外,报告了作为尿毒症物质的硫酸对甲酚是血管内皮损伤的原因物质(meijersb.k.,et.al.,:theuremicretentionsolutep-cresylsulfateandmarkersofendothelialdamage.,am.j.kidneydis.,54:891-901,2009)。
促进硫酸对甲酚的尿中排泄的本发明所提供的药物组合物在一个方面中,可以作为肾病患者(优选为慢性肾病患者)的血管内皮损伤抑制用药物组合物使用。
另外,报告了作为尿毒症物质的苯基乙酰基l谷氨酰胺增加慢性肾病患者的心血管系统疾病的发病风险。
促进苯基乙酰基l谷氨酰胺的尿中排泄的本发明所提供的药物组合物在一个方面中,可以作为慢性肾病患者的心血管系统疾病的治疗和/或预防用药物组合物使用。
在一个实施方式中,本发明所提供的药物组合物促进硫酸吲哚酚、硫酸对甲酚、马尿酸、精氨基琥珀酸、苯基乙酰基l谷氨酰胺等尿毒症物质的尿中排泄,因此,本发明所提供的药物组合物可以作为肾病患者(优选为慢性肾病患者)的硫酸吲哚酚、硫酸对甲酚、马尿酸、精氨基琥珀酸和/或苯基乙酰基l谷氨酰胺的尿中排泄促进用药物组合物使用。
在一个实施方式中,为了使血中的硫酸吲哚酚浓度、血中的硫酸对甲酚浓度、血中的马尿酸浓度和/或血中的苯基乙酰基l谷氨酰胺浓度降低,对肾病患者(优选为慢性肾病患者)给予柠檬酸的医药上可允许的盐、或其水合物或者它们它们的混合物(例如,柠檬酸钾一水合物和柠檬酸钠二水合物的混合物)。
在一个实施方式中,为了使尿中的硫酸吲哚酚浓度、尿中的硫酸对甲酚浓度、尿中的马尿酸浓度、尿中的精氨基琥珀酸浓度和/或尿中的苯基乙酰基l谷氨酰胺浓度增加(优选为了使尿中的硫酸吲哚酚浓度、尿中的硫酸对甲酚浓度和尿中的苯基乙酰基l谷氨酰胺浓度增加),对肾病患者(优选为慢性肾病患者)给予柠檬酸的医药上可允许的盐、或其水合物或者它们的混合物(例如,柠檬酸钾一水合物和柠檬酸钠二水合物的混合物)。
在一个实施方式中,为了使血中的硫酸对甲酚浓度和/或血中的苯基乙酰基l谷氨酰胺浓度降低,对肾病患者(优选为慢性肾病患者)给予碳酸氢钠。
在一个实施方式中,为了使尿中的精氨基琥珀酸浓度增加,对肾病患者(优选为慢性肾病患者)给予碳酸氢钠。
本发明所提供的药物组合物在一个方面中,可以作为肾小管损伤的治疗用药物组合物、肾小管损伤的预防用药物组合物或肾小管损伤抑制用药物组合物使用。肾小管可以为例如近端肾小管。
本发明所提供的药物组合物在其它方面中,可以作为肾功能维持用药物组合物使用。
作为一个实施方式,本发明所提供的药物组合物为肾小管细胞损伤抑制用药物组合物、肾小管细胞保护用药物组合物或肾小管细胞功能(例如,水、钠离子、钾离子、钙离子、磷酸根离子、碳酸氢根离子、氯离子、葡萄糖、氨基酸、维生素等的再吸收)维持用药物组合物。
作为一个实施方式,本发明所提供的药物组合物为近端肾小管细胞损伤抑制用药物组合物、近端肾小管细胞保护用药物组合物或近端肾小管细胞功能(例如,葡萄糖、氨基酸、维生素等的再吸收)维持用药物组合物。
作为一个实施方式,本发明所提供的药物组合物抑制伴随慢性肾病的病期发展的尿中(例如,晨尿)的β2-微球蛋白的量(浓度)的增加。
在一个实施方式中,本发明所提供的药物组合物不对慢性肾病患者的肾小球功能造成影响,另一方面,抑制伴随慢性肾病的病期发展的近端肾小管细胞损伤,保护近端肾小管细胞。
本说明书中,“肾功能维持”是指例如肾小管损伤抑制、肾小管细胞保护或肾小管功能维持。肾小管也可以为例如近端肾小管,肾小管功能维持或近端肾小管功能维持的1个方面为肾小管细胞的功能维持或近端肾小管细胞的功能维持。
本说明书中,“细胞的保护”是指细胞状态的维持或保全或者细胞损伤的抑制。在此,抑制具有上述的含义。
本说明书中,“细胞功能的维持”是指细胞功能的保全或细胞功能恶化的抑制。在此,抑制具有上述的含义。
在此,细胞的状态或功能在本发明所提供的药物组合物的给予前和给予后进行比较。
本说明书中,“晨尿”表示起床后最初的尿。
作为一个实施方式,本发明所提供的药物组合物与给予开始前相比,在给予6周后、12周后和/或24周后抑制尿中(例如,晨尿)的β2-微球蛋白的量(浓度)的增加。
作为一个实施方式,本发明所提供的药物组合物抑制伴随慢性肾病的病期发展的尿中(例如,晨尿)的β2-微球蛋白的量(浓度)的增加,但与本发明所提供的药物组合物给予开始前相比,不使尿中(例如,晨尿)的β2-微球蛋白的量(浓度)实质上降低。在该实施方式中,例如,将本发明所提供的药物组合物给予开始前的尿中(例如,晨尿)的β2-微球蛋白的量(浓度)设为1时,给予后的尿中(例如,晨尿)中的β2-微球蛋白的量(浓度)可以为0.7~1.0或者1.0以上、0.8~1.0或者1.0以上、0.85~1.0或者1.0以上、0.9~1.0或者1.0以上、0.7~2.0、0.8~2.0、0.85~2.0、0.9~2.0、0.7~1.6、0.8~1.6、0.85~1.6或0.9~1.6。
作为一个实施方式,本发明所提供的药物组合物抑制伴随慢性肾病的病期发展的尿中(例如,晨尿)的β2-微球蛋白的量(浓度)的增加,但与本发明所提供的药物组合物给予开始前相比,在给予6周后、给予12周后和/或给予24周后,不使尿中(例如,晨尿)的β2-微球蛋白的量(浓度)实质上降低。该实施方式中,例如,将本发明所提供的药物组合物给予开始前的尿中(例如,晨尿)的β2-微球蛋白的量(浓度)设为1时,给予6周后、给予12周后或给予24周后的尿中(例如,晨尿)的β2-微球蛋白的量(浓度)可以为0.7~1.0或者1.0以上、0.8~1.0或者1.0以上、0.85~1.0或者1.0以上、0.9~1.0或者1.0以上、0.7~2.0、0.8~2.0、0.85~2.0、0.9~2.0、0.7~1.6、0.8~1.6、0.85~1.6或0.9~1.6。
作为一个实施方式,本发明所提供的药物组合物与给予开始前相比,不使血中(例如,血浆中)的半胱氨酸蛋白酶抑制剂c的量(浓度)实质上增加。该实施方式中,例如,将本发明所提供的药物组合物给予开始前的血中(例如,血浆中)的半胱氨酸蛋白酶抑制剂c的量(浓度)设为1时,给予后的血中(例如,血浆中)的半胱氨酸蛋白酶抑制剂c的量(浓度)可以为1.0以下或者1.0~1.2、1.0以下或者1.0~1.15、1.0以下或者1.0~1.1、1.0以下或者1.0~1.05、0.9~1.2、0.9~1.15、0.9~1.1、0.9~1.05、0.95~1.2、0.95~1.15、0.95~1.1或0.95~1.05。
作为一个实施方式,本发明所提供的药物组合物与给予开始前相比,在给予6周后、给予12周后和/或给予24周后,不使血中(例如,血浆中)的半胱氨酸蛋白酶抑制剂c的量(浓度)实质上增加。该实施方式中,例如,将本发明所提供的药物组合物给予开始前的血中(例如,血浆中)的半胱氨酸蛋白酶抑制剂c的量(浓度)设为1时,在给予6周后、给予12周后或给予24周后,血中(例如,血浆中)的半胱氨酸蛋白酶抑制剂c的量(浓度)可以为1.0以下或者1.0~1.2、1.0以下或者1.0~1.15、1.0以下或者1.0~1.1、1.0以下或者1.0~1.05、0.9~1.2、0.9~1.15、0.9~1.1、0.9~1.05、0.95~1.2、0.95~1.15、0.95~1.1或0.95~1.05。
作为一个实施方式,通过本发明所提供的药物组合物的给予,与给予开始前相比,在给予6周后、给予12周后和/或给予24周后,尽管未确认到近端肾小管损伤的改善和/或肾小球损伤改善,但与给予开始前相比,在给予6周后、给予12周后和/或给予24周后,确认到尿毒症物质的血中浓度降低、尿毒症物质的尿中排泄促进和/或尿毒症物质的体外排泄促进。
作为一个实施方式,通过本发明所提供的药物组合物的给予,与给予开始前相比,在给予6周后、给予12周后和/或给予24周后,尽管未确认到近端肾小管损伤的改善和/或肾小球损伤改善,但与给予开始前相比,在给予6周后、给予12周后和/或给予24周后,确认到尿毒症物质的血中浓度降低、尿毒症物质的尿中排泄促进和/或尿毒症物质的体外排泄促进。
本发明所提供的药物组合物对人或其它哺乳动物以口服或非口服进行给予,非口服给予的例子可举出静脉内给予、皮下给予、肌肉内给予、关节内给予、经粘膜给予、经皮给予、经鼻给予、直肠给予、髄腔内给予、腹腔内给予、局部给予。
本发明所提供的药物组合物可以将碱化剂直接使用或者与药学上可允许的载体例如赋形剂(例如,乳糖、d-甘露醇、结晶纤维素、葡萄糖)、粘合剂(例如,羟丙基纤维素(hpc)、明胶、聚乙烯基吡咯烷酮(pvp))、润滑剂(例如,硬脂酸镁、滑石)、崩解剂(例如,淀粉、羧甲基纤维素钙(cmc-ca))、稀释剂(例如,注射用水、生理盐水)和需要时的其它添加剂(例如,ph调节剂、表面活性剂、增溶剂、防腐剂、乳化剂、等张剂、稳定剂)混合而制备,可以为片剂、胶囊剂、悬浮剂、注射剂、栓剂等制剂。例如,制成片剂时,可以将碱化剂与赋形剂(例如,乳糖、d-甘露醇、结晶纤维素、葡萄糖)、崩解剂(例如,淀粉、羧甲基纤维素钙(cmc-ca))、粘合剂(例如,羟丙基纤维素(hpc)、明胶、聚乙烯基吡咯烷酮(pvp))、润滑剂(例如,硬脂酸镁、滑石)等混合而制成制剂。
以下对本发明的片剂更详细地进行说明。
在一个实施方式中,本发明所提供的药物组合物为片剂。本发明所提供的片剂除碱化剂(例如,柠檬酸钾或其水合物;柠檬酸钠或其水合物;柠檬酸钾的一水合物和柠檬酸钠的二水合物的混合物;或碳酸氢钠)以外还可以包含在制剂领域中惯用的药学上可允许的添加剂。作为这样的添加剂的例子,可举出赋形剂、粘合剂、崩解剂、流动化剂、矫味剂、润滑剂、ph调节剂、表面活性剂、稳定剂和香料。
本发明所提供的片剂中的碱化剂的含量相对于片剂可以为10~95重量%,优选可以为30~90重量%,更优选可以为60~85重量%。
本发明所提供的片剂中可使用的赋形剂的例子可举出乳糖(例如,乳糖水合物、无水乳糖)、葡萄糖、蔗糖、果糖、麦芽糖等糖类、赤藓糖醇、山梨糖醇、麦芽糖醇、木糖醇、d-甘露醇等糖醇类、淀粉(例如,玉米淀粉、马铃薯淀粉、米淀粉、小麦淀粉)、结晶纤维素、偏硅酸铝酸镁、无水磷酸钙、沉降碳酸钙、硅酸钙、乳酸钙和乙基纤维素,特别优选结晶纤维素。
本发明所提供的片剂中的赋形剂的含量相对于片剂可以为1~95重量%,优选可以为1~80重量%,更优选可以为3~80重量%,进一步优选可以为3~20重量%。
本发明所提供的片剂中可使用的粘合剂的例子可举出羟丙基纤维素、羟丙基甲基纤维素、聚乙烯基吡咯烷酮、糊精、甲基纤维素、聚乙烯醇、海藻酸钠、甲基丙烯酸氨基烷基酯共聚物、聚乙二醇、α-化淀粉(例如,部分α-化淀粉)、琼脂和明胶,特别优选羟丙基纤维素。
本发明所提供的片剂中的粘合剂的含量相对于片剂可以为0.1~30重量%,优选可以为0.1~10重量%,更优选可以为0.3~3重量%。
本发明所提供的片剂中可使用的崩解剂的例子可举出交联羧甲基纤维素钠、羧甲基纤维素钙、羧甲基淀粉钠、低取代度羟丙基纤维素、交联聚维酮、淀粉(例如,小麦淀粉、玉米淀粉、部分α-化淀粉)和羧甲基纤维素,特别优选部分α-化淀粉。
本发明所提供的片剂中的崩解剂的含量相对于片剂可以为0.3~20重量%,优选可以为1~10重量%,更优选可以为3~10重量%。
本发明所提供的片剂中可使用的流动化剂的例子可举出轻质无水硅酸、滑石和偏硅酸铝酸镁。
本发明所提供的片剂中的流动化剂的含量相对于片剂可以为0.03~3重量%,优选可以为0.1~3重量%,更优选可以为0.3~3重量%。
本发明所提供的片剂中可使用的矫味剂的例子可举出柠檬酸(例如,柠檬酸酐)、苹果酸、乙酸、酒石酸、富马酸、抗坏血酸等酸味剂(但是,上述矫味剂不包括本发明的碱化剂)、糖精钠、甘草酸二钾、阿斯巴甜(注册商标)、甜菊糖、索马甜和三氯蔗糖等甜味剂。
本发明所提供的片剂中的矫味剂的含量相对于片剂可以为0.03~3重量%,优选可以为0.1~3重量%,更优选可以为0.3~3重量%。
本发明所提供的片剂中可使用的润滑剂的例子可举出硬脂酸镁、硬脂酸钙、滑石、轻质无水硅酸、蔗糖脂肪酸酯、巴西棕榈蜡、聚乙二醇和硬脂富马酸钠,特别优选硬脂酸镁。
本发明所提供的片剂中的润滑剂的含量相对于片剂可以为0.1~30重量%,优选可以为0.3~10重量%,更优选可以为1~3重量%。
本发明所提供的片剂中可使用的ph调节剂的例子可举出柠檬酸、磷酸盐(例如,磷酸二氢钠、磷酸二氢钾)、碳酸盐(例如,碳酸镁、碳酸钠)、酒石酸盐、富马酸盐、乙酸盐和氨基酸盐(但是,上述ph调节剂不包括本发明的碱化剂)。
本发明所提供的片剂中的ph调节剂的含量相对于片剂可以为0.1~30重量%,优选可以为0.3~10重量%,更优选可以为1~5重量%。
本发明所提供的片剂中可使用的表面活性剂的例子可举出月桂基硫酸钠、聚山梨酸酯、蔗糖脂肪酸酯、聚氧乙烯氢化蓖麻油、硬脂酸聚乙二醇酯、聚乙二醇和泊洛沙姆。
本发明所提供的片剂中的表面活性剂的含量相对于片剂可以为0.01~3重量%,优选可以为0.03~1重量%,更优选可以为0.03~0.5重量%。
本发明所提供的片剂中可使用的稳定剂的例子可举出柠檬酸(例如,柠檬酸酐)、苹果酸、乙酸、酒石酸、马来酸、抗坏血酸、乙二胺四乙酸钠、生育酚(但是,上述稳定剂不包括本发明的碱化剂),特别优选柠檬酸酐。
本发明所提供的片剂中的稳定剂的含量相对于片剂可以为0.01~30重量%,优选可以为0.1~30重量%,更优选可以为1~20重量%。
本发明所提供的片剂中可使用的香料的例子可举出柠檬、橙子、葡萄柚等的柑橘系香料、薄荷、留兰香和薄荷醇,可以在片剂中含有适量(例如,相对于片剂为0.01~1重量%,更优选为0.01~0.1重量%)
本发明所提供的片剂中的碱化剂和药学上可允许的添加剂的合计含量相对于片剂不超过100重量%。
本发明所提供的片剂含有上述的成分,既可以制成未实施包衣层的素片,也可以制成实施了包衣层的薄膜包衣片。包衣层的含量可以由本领域技术人员适当设定,例如相对于素片可以为0.1~10重量%。包衣层中,除包衣基剂以外,还可以适当含有增塑剂、着色剂、光泽剂等。
本发明所提供的片剂中可使用的包衣基剂的例子可举出羟丙基纤维素、羟丙基甲基纤维素、乙基纤维素、乙酸邻苯二甲酸纤维素、甲基丙烯酸共聚物和聚乙烯基吡咯烷酮,特别优选羟丙基甲基纤维素。本发明所提供的片剂中的包衣基剂的含量相对于片剂可以为0.01~10重量%,优选可以为0.3~3重量%。
本发明所提供的片剂中可使用的包衣增塑剂的例子可举出柠檬酸三乙酯、中链脂肪酸三甘油酯、三乙酸甘油酯、甘油、丙二醇和聚乙二醇(例如,聚乙二醇6000),特别优选聚乙二醇6000。本发明所提供的片剂中的包衣增塑剂的含量相对于片剂可以为0.01~1重量%,优选可以为0.03~3重量%。
本发明所提供的片剂中可使用的包衣着色剂的例子可举出氧化钛、黄色三氧化二铁、三氧化二铁、黑色氧化铁、食用蓝色2号和食用蓝色2号铝色淀。本发明所提供的片剂中的包衣着色剂的含量相对于片剂可以为0.01~1重量%,优选可以为0.03~3重量%。
本发明所提供的片剂中可使用的包衣光泽剂的例子可举出巴西棕榈蜡。本发明所提供的片剂中的包衣光泽剂的含量相对于片剂可以为0.0001~0.1重量%,优选可以为0.001~0.01重量%。
本发明所提供的药物组合物可以通过制药领域中公知的方法来制造。例如,制成片剂时,制造方法中可包括:将碱化剂(例如,柠檬酸钾或其水合物;柠檬酸钠或其水合物;柠檬酸钾的一水合物和柠檬酸钠的二水合物的混合物;或碳酸氢钠)与添加物混合的混合工序,造粒工序,压片工序和/或包衣工序。
混合工序可包括将碱化剂与赋形剂、稳定剂、崩解剂和/或粘合剂等添加物混合的工序。另外,在压片工序之前,可进一步包括将包含碱化剂和添加剂的混合物与润滑剂、矫味剂和/或香料混合的工序。混合可以使用v型混合机、w型混合机、容器式混合机、转鼓式混合机、搅拌混合机等进行。
造粒工序可以通过制药领域中公知的造粒方法来进行。造粒方法的例子可举出干式造粒法、湿式造粒法、流动层造粒法。
作为一个实施方式,混合工序中得到的混合物、造粒工序中得到的造粒物可通过适当粉碎和/或筛分而制成具有期望粒径的混合物、造粒物。粉碎可以利用例如球磨机、喷射磨机、锤磨机等制药领域中公知的粉碎机来进行。筛分可以使用16目筛(网眼1000μm)~32目筛(网眼500μm)等来进行。
压片工序可以通过制药领域中公知的压片方法来进行。压片方法的例子可举出直接压片法、干式压片法、湿式压片法、外部润滑压片法。例如,可以使用单发式压片机、旋转式压片机等制药领域中公知的压片机将上述的工序中得到的混合物、造粒物压片。使用单发式压片机、旋转式压片机等时,可以采用1kn~30kn的压片压力。
包衣工序可以通过制药领域中公知的方法来进行。例如,可以通过将包含包衣基剂和增塑剂、着色剂、光泽剂等的包衣液喷涂于素片的外侧来进行。
在一个实施方式中,本发明所提供的片剂可以通过将碱化剂、赋形剂(例如,乳糖、d-甘露醇、结晶纤维素和/或葡萄糖)、粘合剂(例如,羟基丙基纤维素(hpc)、明胶和/或聚乙烯基吡咯烷酮(pvp))、稳定剂(例如,柠檬酸酐)、崩解剂(例如,淀粉(例如,部分α-化淀粉)和/或羧甲基纤维素钙(cmc-ca))和润滑剂(例如,硬脂酸镁)混合并进行压片而得到素片;在该素片的外侧形成包含包衣基剂(例如,羟丙基纤维素、羟丙基甲基纤维素和/或pvp)和增塑剂(例如,柠檬酸三乙酯和/或聚乙二醇6000)、着色剂(例如,三氧化二铁和/或氧化钛)、光泽剂(例如,巴西棕榈蜡)的包衣层来制造。
在一个实施方式中,得到的片剂的硬度可以为10~200n,优选可以为30~150n。
本发明所提供的药物组合物中的碱化剂的量可适当设定。
在一个实施方式中,本发明所提供的药物组合物中的碱化剂的量可以以碱化剂的给予量成为通过对人进行给予而痛风或高尿酸血症的酸性尿得到改善的量、或比其少的量的方式进行设定,例如,对于痛风或高尿酸血症的酸性尿的改善,可以以成为在日本被许可的1天用量(例如,碱化剂为柠檬酸制剂时:将1片中含有柠檬酸钾(c6h5k3o7·h2o)231.5mg和柠檬酸钠水合物(c6h5na3o7·2h2o)195.0mg的片剂口服给予1次2片、1天3次,碱化剂为碳酸氢钠时:口服给予1天3~5g)的1~50%或10~20%的方式进行设定。
在一个实施方式中,本发明所提供的药物组合物为片剂,在1片剂中,可以含有10mg~1g、优选100mg~500mg、更优选400mg~500mg的作为碱化剂的柠檬酸钾一水合物或柠檬酸钠二水合物。
在一个实施方式中,本发明所提供的药物组合物为片剂,在1片剂中,可以分别含有10mg~300mg、合计含有20mg~600mg的柠檬酸钾一水合物和柠檬酸钠二水合物,优选分别含有150~250mg、合计含有400~500mg的柠檬酸钾一水合物和柠檬酸钠二水合物,更优选分别含有190~240mg、合计含有400~450mg的柠檬酸钾一水合物和柠檬酸钠二水合物。
在一个实施方式中,本发明所提供的药物组合物为片剂,在1片剂中,可以含有10mg~1g、优选100mg~500mg的作为碱化剂的碳酸氢钠。
作为一个实施方式,本发明所提供的药物组合物为片剂,作为碱化剂,可以含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,作为添加剂,可以含有柠檬酸酐、结晶纤维素、部分α-化淀粉、羟丙基纤维素、硬脂酸镁、羟丙基甲基纤维素、聚乙二醇6000、氧化钛和巴西棕榈蜡。
作为一个实施方式,可以将含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg的片剂作为1给予单位。
本说明书中,“给予单位”表示制剂的单位,“1给予单位”表示制剂的最小单位。因此,例如,如果为片剂,则给予单位为各片剂,1给予单位表示1个片剂。如果为注射剂,则给予单位为加入到安瓿或药瓶等密封容器中的注射剂,1给予单位表示加入到1个安瓿或药瓶等密封容器中的注射剂。
本发明所提供的药物组合物对人或其它哺乳动物进行给予时,可以每1次给予1个或2个以上的上述给予单位,也可以将上述1给予单位分割而给予。
碱化剂的给予量可根据碱化剂的种类、给予方法、给予对象的年龄、体重、性别、症状、对药剂的敏感性等而适当决定,也可以根据症状的改善状况而调节给予量。
在一个实施方式中,对人口服给予作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物的混合物或碳酸氢钠时,可以将为了改善痛风以及高尿酸血症的酸性尿而在日本被许可的1天的给予量(例如,碱化剂为柠檬酸制剂时:将1片中含有柠檬酸钾(c6h5k3o7·h2o)231.5mg和柠檬酸钠水合物(c6h5na3o7·2h2o)195.0mg的片剂口服给予1次2片、1天3次,碱化剂为碳酸氢钠时:口服给予1天3~5g)的一半量作为1天的给予量。
在一个实施方式中,对人口服给予作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物的混合物或碳酸氢钠时,可以将为了改善痛风以及高尿酸血症的酸性尿而在日本被许可的1天的给予量(例如,碱化剂为柠檬酸制剂时:将在1片中含有柠檬酸钾(c6h5k3o7·h2o)231.5mg和柠檬酸钠水合物(c6h5na3o7·2h2o)195.0mg的片剂口服给予1次2片、1天3次,碱化剂为碳酸氢钠时:口服给予1天3~5g)作为1天的给予量。
在一个实施方式中,对人口服给予作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物的混合物或碳酸氢钠时,可以将为了改善痛风以及高尿酸血症的酸性尿而在日本被许可的1天的给予量(例如,碱化剂为柠檬酸制剂时:将1片中含有柠檬酸钾(c6h5k3o7·h2o)231.5mg和柠檬酸钠水合物(c6h5na3o7·2h2o)195.0mg的片剂口服给予1次2片、1天3次,碱化剂为碳酸氢钠时:口服给予1天3~5g)的一般量作为1日的给予量开始给予,然后,将给予量增量至为了改善痛风以及高尿酸血症的酸性尿而在日本被许可的1天的给予量。
在一个实施方式中,碱化剂的给予量可以为通过口服给予碱化剂而使人的尿(例如,晨尿)的ph成为ph5.2~ph6.8、ph5.5~ph6.8、ph5.8~ph6.8、ph5.8~ph6.5、ph5.8~ph6.2、ph5.8以上且小于ph6.2、ph6.0~ph6.5、ph6.0~ph6.4、ph6.0~ph6.3、ph6.0~ph6.2、ph6.0以上且小于ph6.2、ph6.1~ph6.3、ph6.2~6.8、ph6.2~ph6.5或ph6.5~6.8这样的给予量。
在一个实施方式中,碱化剂的给予量可以为通过给予碱化剂而使人的尿(例如,晨尿)的ph在给予6周、12周或24周后成为ph5.2~ph6.8、ph5.5~ph6.8、ph5.8~ph6.8、ph5.8~ph6.5、ph5.8~ph6.2、ph5.8以上且小于ph6.2、ph6.0~ph6.5、ph6.0~ph6.4、ph6.0~ph6.3、ph6.0~ph6.2、ph6.0以上且小于ph6.2、ph6.1~ph6.3、ph6.2~6.8、ph6.2~ph6.5或ph6.5~6.8这样的给予量。
在一个实施方式中,对人口服给予作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物的混合物时,可以将柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.1~5g/天合计0.2~10g/天、分别以0.1~3g/天合计0.2~6g/天、分别以0.5~3g/天合计1~6g/天给予,优选分别以0.5~1.5g/天合计1~3g/天、分别以1~1.5g/天合计2~3g/天或分别以0.5~1g/天合计1~2g/天进行给予,也可以分为1天1~5次、优选1天3次进行给予。
在一个实施方式中,对人口服给予作为碱化剂的柠檬酸钾一水合物或柠檬酸钠二水合物时,可以以1~10g/天、1~6g/天、2~5.5g/天、1~3g/天、2~3g/天或1~1.5g/天进行给予,也可以分为1天1~5次、优选1天3次进行给予。
在一个实施方式中,对人口服给予作为碱化剂的碳酸氢钠时,可以以1~6g/天、优选1~3g/天或3~5g/天进行给予,也可以分为1天1~5次、优选1天3次进行给予。
在一个实施方式中,碱化剂可以长期给予,例如以1周、2周、3周、6周、8周、10周、12周、24周、40周、60周、80周、100周、120周、1周以上、2周以上、3周以上、6周以上、8周以上、10周以上、12周以上、24周以上、40周以上、60周以上、80周以上、100周以上、120周以上、6周以上且24周以下、12周以上且24周以下、6周以上且30周以下、12周以上且30周以下、6周以上且40周以下、12周以上且40周以下、6周以上且60周以下、12周以上且60周以下、6周以上且80周以下、12周以上且80周以下、6周以上且100周以下、12周以上且100周以下、6周以上且120周以下或12周以上且120周以下进行给予。
在一个实施方式中,本发明所提供的药物组合物通过6周的连续给予、12周的连续给予和/或24周的连续给予,能够检测出对肾病(例如,慢性肾病)的患者有益的效果(例如,尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和/或精氨基琥珀酸)的血中浓度降低效果、尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和/或精氨基琥珀酸)的尿中浓度增加效果(向尿中的排泄促进效果)和/或尿中的β2-微球蛋白浓度的增加抑制效果)。
作为一个实施方式,本发明所提供的药物组合物可对患有肾病的人进行给予。肾病只要没有特别说明,则包括急性肾病和慢性肾病。
急性肾病的例子可举出由药剂(例如,非甾体抗炎药、血管紧张素转换酶抑制剂、血管紧张素ⅱ受体拮抗剂、氨基糖苷系抗生素、新型喹诺酮系抗菌药、碘造影剂、顺铂等铂制剂)引起的急性肾病和由肾缺血引起的急性肾病。
慢性肾病(ckd)是不论原发病如何,包括慢性发展的肾病的概念,是包括由肾小球滤过量(gfr)表示的肾功能降低或者提示发现肾脏损伤的表现慢性地(3个月以上)持续的所有病态的概念。
根据ckd诊疗指南2012(日肾会志2012),慢性肾病的重症度可通过基于原因(cause:c)、肾功能(gfr:g)、蛋白尿(白蛋白尿:a)的分类进行评价。
gfr的区分如下。
g1:gfr为正常或高值(≧90ml/分钟/1.73m2)
g2:gfr为正常或轻度降低(60~89ml/分钟/1.73m2)
g3a:gfr为轻度~中度降低(45~59ml/分钟/1.73m2)
g3b:gfr为中等度~高度降低(30~44ml/分钟/1.73m2)
g4:gfr为高度降低(15~29ml/分钟/1.73m2)
g5:末期肾衰竭(eskd)(<15ml/分钟/1.73m2)
基于蛋白尿(白蛋白尿:a)的分类,在原疾病为糖尿病的情况下,使用尿白蛋白/肌酐(cr)比如下进行分类。
a1:正常(小于30mg/gcr)
a2:微量白蛋白尿(30~299mg/gcr)
a3:显性白蛋白尿(300mg/gcr以上)
另外,基于蛋白尿(白蛋白尿:a)的区分,在原疾病为糖尿病以外的高血压、肾炎、多囊肾病、移植肾、其它的情况下,使用尿蛋白/肌酐(cr)比如下进行分类。
a1:正常(小于0.15g/gcr)
a2:轻度蛋白尿(0.15~0.49g/gcr)
a3:高度蛋白尿(0.50g/gcr以上)
根据ckd诊疗指南2012(日肾会志2012),慢性肾病(ckd)的重症度分类使用上述c、g和a,例如记载为糖尿病g2a3、慢性肾炎g3ba1等。
然而,以往,慢性肾病的重症度考虑仅以由gfr区分的阶段来记载,也可以将慢性肾病的重症度如以往那样以g1、g2、g3a、g3b、g4和g5这样的阶段来记载。
在一个实施方式中,本发明所提供的药物组合物对重症度低的早期的慢性肾病患者进行给予。
在一个实施方式中,本发明所提供的药物组合物对阶段g3b以下、优选阶段g2或其以下的慢性肾病患者进行给予。
在一个实施方式中,本发明所提供的药物组合物对阶段g2以上阶段g3b以下(例如,阶段g2和阶段g3a;或阶段g2、阶段g3a和阶段g3b)的慢性肾病患者进行给予。
在一个实施方式中,本发明所提供的药物组合物对阶段g3b以下且微量白蛋白尿的慢性肾病患者、优选阶段g2且微量白蛋白尿的慢性肾病患者进行给予。
在一个实施方式中,本发明所提供的药物组合物对阶段g2以上且阶段g3b以下(例如,阶段g2和阶段g3a;或阶段g2、阶段g3a和阶段g3b)且微量白蛋白尿的慢性肾病患者进行给予。
在一个实施方式中,本发明所提供的药物组合物对阶段g3b以下且尿中蛋白排泄量小于3.5g/gcr的慢性肾病患者、优选阶段g2且尿中蛋白排泄量小于3.5g/gcr的慢性肾病患者进行给予。
在一个实施方式中,本发明所提供的药物组合物对阶段g2以上且阶段g3b以下(例如,阶段g2和阶段g3a;或阶段g2、阶段g3a和阶段g3b)且尿中蛋白排泄量小于3.5g/gcr的慢性肾病患者进行给予。
在一个实施方式中,本发明所提供的药物组合物对进行性的慢性肾病患者进行给予。
在一个实施方式中,本发明所提供的药物组合物对β2-微球蛋白的尿中(例如,晨尿中)浓度为2000μg/l以下、1000μg/l以下、800μg/l以下、290μg/l以下、200μg/l以下、1~2000μg/l、1~1000μg/l、1~800μg/l、1~290μg/l、1~200μg/l、10~2000μg/l、10~1000μg/l、10~800μg/l、10~290μg/l、10~200μg/l或80~200μg/l的慢性肾病患者进行给予。
在一个实施方式中,本发明所提供的药物组合物对半胱氨酸蛋白酶抑制剂c的血中(例如,血浆中或血清中)浓度为0.1~3.0mg/l、0.1~2.0mg/l、0.1~1.6mg/l、0.1~1.3mg/l、0.5~3.0mg/l、0.5~2.0mg/l、0.5~1.6mg/l、0.5~1.3mg/l或0.9~1.3mg/ml的慢性肾病患者进行给予。
在一个实施方式中,本发明所提供的药物组合物对硫酸吲哚酚的血中浓度为0.001~100μg/ml(例如,0.1~30μg/ml)的慢性肾病患者进行给予。
在一个实施方式中,本发明所提供的药物组合物对硫酸对甲酚的血中浓度为0.003~300μg/ml(例如,0.01~30μg/ml)的慢性肾病患者进行给予。
在一个实施方式中,本发明所提供的药物组合物对马尿酸的血中浓度为0.01~100μg/ml(例如,0.01~10μg/ml)的慢性肾病患者进行给予。
在一个实施方式中,本发明所提供的药物组合物对精氨基琥珀酸的血中浓度为0.01~100μg/ml(例如,0.1~10μg/ml)的慢性肾病患者进行给予。
在一个实施方式中,本发明所提供的药物组合物对苯基乙酰基l谷氨酰胺的血中浓度为0.03~30μg/ml(例如,0.1~10μg/ml)的慢性肾病患者进行给予。
在一个实施方式中,本发明所提供的药物组合物对实施依照ckd诊疗指南的治疗的患者进行给予。例如,对实施依照ckd诊疗指南的血压管理(arb、ace抑制剂等ra系抑制剂、利尿药、ca拮抗剂的给予等)、蛋白尿对策(ra系抑制剂的给予等)、血糖值管理(α葡萄糖苷酶抑制剂的给予等)、脂质管理(他汀、贝特的给予等)、贫血管理(促红细胞生成素的给予等)和/或骨·矿物对策(双膦酸盐的给予等)的患者进行给予。
在一个实施方式中,本发明所提供的药物组合物与降压药(例如,arb、ace抑制剂、利尿药、ca拮抗剂)并用。
在一个实施方式中,本发明所提供的药物组合物与将来自石油系烃的球形微粒多孔碳在高温下进行氧化和还原处理而得到的球形吸附碳(以kremezin(注册商标)在日本销售)并用。
在一个实施方式中,本发明所提供的药物组合物对重症度低的早期的慢性肾病患者(例如,阶段g3b以下、优选阶段g2以上阶段且g3b以下、更优选阶段g2和阶段g3a、进一步更优选阶段g2的慢性肾病患者)进行给予,使该患者的血中的尿毒症物质(例如,硫酸吲哚酚、马尿酸和/或苯基乙酰基l谷氨酰胺)的浓度降低,促进尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、马尿酸、精氨基琥珀酸和/或苯基乙酰基l谷氨酰胺)向体外的(例如,向尿中的)排泄。在该实施方式中,本发明所提供的药物组合物可以为尿毒症症状的改善用药物组合物、尿毒症的治疗或预防用药物组合物、慢性肾病的发展抑制用药物组合物、透析导入的延迟用药物组合物、心肌的纤维化抑制用药物组合物、动脉硬化抑制用药物组合物、动脉硬化改善用药物组合物、血管平滑肌细胞的增殖抑制用药物组合物、血管内皮细胞损伤抑制用药物组合物、动脉壁肥厚抑制用药物组合物、动脉壁肥厚改善用药物组合物、大动脉的钙化抑制用药物组合物或作为并发症的心血管系统疾病(例如,心衰竭、心肌梗塞、中风等)的治疗或预防用药物组合物。
在一个实施方式中,本发明所提供的药物组合物对重症度低的早期的慢性肾病患者(例如,阶段g3b以下、优选阶段g2以上且阶段g3b以下、更优选阶段g2和阶段g3a、进一步更优选阶段g2的慢性肾病患者)进行给予,抑制该患者的尿中的β2-微球蛋白的增加。在该实施方式中,本发明所提供的药物组合物可以为肾小管(例如,近端肾小管)损伤的抑制用组合物、肾小管(例如,近端肾小管)细胞损伤的抑制用组合物、肾小管(例如,近端肾小管)细胞保护用组合物或肾小管(例如,近端肾小管)细胞功能(例如,葡萄糖、氨基酸等的再吸收)维持用药物组合物。
在一个实施方式中,本发明所提供的药物组合物对重症度为中等度以上的慢性肾病患者(例如,阶段g3b以上的慢性肾病患者)进行给予,使该患者的血中的尿毒症物质(例如,硫酸吲哚酚、马尿酸和/或苯基乙酰基l谷氨酰胺)的浓度降低,促进尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、马尿酸、精氨基琥珀酸和/或苯基乙酰基l谷氨酰胺)向体外的(例如,向尿中的)排泄。在该实施方式中,本发明所提供的药物组合物可以为尿毒症症状的改善用药物组合物、尿毒症的治疗或预防用药物组合物、慢性肾病的发展抑制用药物组合物、透析导入的延迟用药物组合物、心肌的纤维化抑制用药物组合物、动脉硬化抑制用药物组合物、动脉硬化改善用药物组合物、血管平滑肌细胞的增殖抑制用药物组合物、血管内皮细胞损伤抑制用药物组合物、动脉壁肥厚抑制用药物组合物、动脉壁肥厚改善用药物组合物、大动脉的钙化抑制用药物组合物、肌肉细胞内的能量产生的降低抑制用药物组合物、肌肉质量和/或肌肉强度的降低抑制用药物组合物或作为并发症的心血管系统疾病(例如,心衰竭、心肌梗塞、中风等)的治疗或预防用药物组合物。
在一个实施方式中,本发明所提供的药物组合物对重症度为中等度以上的慢性肾病患者(例如,阶段g3b以上的慢性肾病患者)进行给予,抑制该患者的尿中的β2-微球蛋白的增加。在该实施方式中,本发明所提供的药物组合物可以为肾小管(例如,近端肾小管)损伤的抑制用组合物、肾小管(例如,近端肾小管)细胞损伤的抑制用组合物、肾小管(例如,近端肾小管)细胞保护用组合物或肾小管(例如,近端肾小管)细胞功能(例如,葡萄糖、氨基酸等的再吸收)维持用药物组合物。
作为本发明的其它实施方式的例子,可举出以下例子。
a)一种使哺乳类对象(例如,人)的尿毒症物质的血中浓度降低的方法,包括对需要使尿毒症物质的血中浓度降低的对象给予有效量的碱化剂;
b)一种促进哺乳类对象(例如,人)的尿毒症物质向尿中排泄的方法,包括对需要促进尿毒症物质向尿中排泄的对象给予有效量的碱化剂;
c)一种哺乳类对象(例如,人)的尿毒症症状的改善方法,包括对需要改善尿毒症症状的对象给予有效量的碱化剂,并且该对象患有肾病;
d)一种哺乳类对象(例如,人)的尿毒症的治疗或预防方法,包括对需要尿毒症的治疗或预防的对象给予有效量的碱化剂,并且该对象患有肾病;
e)一种哺乳类对象(例如,人)的慢性肾病的发展抑制方法,包括对需要抑制慢性肾病的发展的对象给予有效量的碱化剂;
f)一种哺乳类对象(例如,人)的透析导入的延迟方法,包括对需要透析导入的延迟的对象给予有效量的碱化剂,并且该对象患有慢性肾病;
g)一种哺乳类对象(例如,人)的心肌的纤维化抑制方法,包括对需要抑制心肌的纤维化的对象给予有效量的碱化剂,并且该对象患有肾病;
h)一种哺乳类对象(例如,人)的动脉硬化抑制方法,包括对需要抑制动脉硬化的对象给予有效量的碱化剂,并且该对象患有肾病;
i)一种抑制哺乳类对象(例如,人)的血管平滑肌细胞的增殖的方法,包括对需要抑制血管平滑肌细胞的增殖的对象给予有效量的碱化剂,并且该对象患有肾病;
j)一种哺乳类对象(例如,人)的血管内皮细胞损伤抑制方法,包括对需要抑制血管内皮细胞损伤的对象给予有效量的碱化剂,并且该对象患有肾病;
k)一种哺乳类对象(例如,人)的动脉壁的肥厚抑制方法,包括对需要抑制动脉壁的肥厚的对象给予有效量的碱化剂,并且该对象患有肾病;
l)一种哺乳类对象(例如,人)的大动脉的钙化抑制方法,包括对需要抑制大动脉的钙化的对象给予有效量的碱化剂,并且该对象患有肾病;
m)一种哺乳类对象(例如,人)的心血管系统疾病的治疗或预防方法,包括对需要心血管系统疾病的治疗或预防的对象给予有效量的碱化剂,并且该对象患有肾病;
n)一种哺乳类对象(例如,人)的动脉硬化的改善方法,包括对需要动脉硬化的改善的对象给予有效量的碱化剂,并且该对象患有肾病;
o)一种哺乳类对象(例如,人)的动脉壁的肥厚的改善方法,包括对需要改善动脉壁的肥厚的对象给予有效量的碱化剂,并且该对象患有肾病;
p)一种哺乳类对象(例如,人)的急性肾病的治疗方法,包括对需要急性肾病的治疗的对象给予有效量的碱化剂;
q)一种哺乳类对象(例如,人)的从急性肾病向慢性肾病的发展抑制方法,包括对需要抑制从急性肾病向慢性肾病的发展的对象给予有效量的碱化剂;
r)一种哺乳类对象(例如,人)的肾小管损伤的治疗或预防方法,包括对需要治疗或预防肾小管损伤的对象给予有效量的碱化剂;
s)一种哺乳类对象(例如,人)的肾小管损伤的抑制方法,包括对需要抑制肾小管损伤的对象给予有效量的碱化剂;
t)一种哺乳类对象(例如,人)的近端肾小管细胞损伤的抑制方法,包括对需要抑制近端肾小管细胞损伤的对象给予有效量的碱化剂;
u)一种哺乳类对象(例如,人)的近端肾小管细胞保护方法,包括对需要保护近端肾小管细胞的对象给予有效量的碱化剂;
v)一种哺乳类对象(例如,人)的近端肾小管细胞功能维持方法,包括对需要维持近端肾小管细胞的功能的对象给予有效量的碱化剂;
w)一种促进哺乳类对象(例如,人)的尿毒症物质向体外排泄的方法,包括对需要促进尿毒症物质向体外排泄的对象给予有效量的碱化剂;
x)一种依赖于哺乳类对象(例如,人)的尿毒症物质的血中浓度将尿毒症物质向尿中排泄的方法,包括对需要将尿毒症物质向尿中排泄的对象给予有效量的碱化剂;
aa)一种碱化剂,用于降低尿毒症物质的血中浓度;
bb)一种碱化剂,用于促进尿毒症物质向尿中排泄;
cc)一种碱化剂,用于改善肾病患者的尿毒症症状;
dd)一种碱化剂,用于治疗或预防肾病患者的尿毒症;
ee)一种碱化剂,用于抑制慢性肾病的发展;
ff)一种碱化剂,用于慢性肾病患者的透析导入的延迟;
gg)一种碱化剂,用于抑制肾病患者的心肌的纤维化;
hh)一种碱化剂,用于抑制肾病患者的动脉硬化;
ii)一种碱化剂,用于抑制肾病患者的血管平滑肌细胞的增殖;
jj)一种碱化剂,用于抑制肾病患者的血管内皮细胞损伤;
kk)一种碱化剂,是抑制肾病患者的动脉壁的肥厚;
ll)一种碱化剂,用于抑制肾病患者的大动脉的钙化;
mm)一种碱化剂,用于治疗或预防肾病患者的心血管系统疾病;
nn)一种碱化剂,用于改善肾病患者的动脉硬化;
oo)一种碱化剂,用于改善肾病患者的动脉壁的肥厚;
pp)一种碱化剂,用于治疗急性肾病;
qq)一种碱化剂,用于抑制从急性肾病向慢性肾病的发展;
rr)一种碱化剂,用于治疗或预防肾小管损伤;
ss)一种碱化剂,用于抑制肾小管损伤;
tt)一种碱化剂,用于抑制近端肾小管细胞损伤;
uu)一种碱化剂,用于保护近端肾小管细胞;
vv)一种碱化剂,用于维持近端肾小管细胞功能;
ww)一种碱化剂,用于促进尿毒症物质向体外排泄;
xx)一种碱化剂,用于依赖于尿毒症物质的血中浓度而将尿毒症物质向尿中排泄;
aaa)一种包含碱化剂的药物组合物,用于降低尿毒症物质的血中浓度;
bbb)一种包含碱化剂的药物组合物,用于促进尿毒症物质向尿中排泄;
ccc)一种包含碱化剂的药物组合物,用于改善肾病患者的尿毒症症状;
ddd)一种包含碱化剂的药物组合物,用于治疗或预防肾病患者的尿毒症;
eee)一种包含碱化剂的药物组合物,用于抑制慢性肾病的发展;
fff)一种包含碱化剂的药物组合物,用于慢性肾病患者的透析导入的延迟;
ggg)一种包含碱化剂的药物组合物,用于抑制肾病患者的心肌的纤维化;
hhh)一种包含碱化剂的药物组合物,用于抑制肾病患者的动脉硬化;
iii)一种包含碱化剂的药物组合物,用于抑制肾病患者的血管平滑肌细胞的增殖;
jjj)一种包含碱化剂的药物组合物,用于抑制肾病患者的血管内皮细胞损伤;
kkk)一种包含碱化剂的药物组合物,用于抑制肾病患者的动脉壁的肥厚;
lll)一种包含碱化剂的药物组合物,用于抑制肾病患者的大动脉的钙化;
mmm)一种包含碱化剂的药物组合物,用于治疗或预防肾病患者的心血管系统疾病;
nnn)一种包含碱化剂的药物组合物,用于改善肾病患者的动脉硬化;
ooo)一种包含碱化剂的药物组合物,用于改善肾病患者的动脉壁的肥厚;
ppp)一种包含碱化剂的药物组合物,用于治疗急性肾病;
qqq)一种包含碱化剂的药物组合物,用于抑制从急性肾病向慢性肾病的发展;
rrr)一种包含碱化剂的药物组合物,用于治疗或预防肾小管损伤;
sss)一种包含碱化剂的药物组合物,用于抑制肾小管损伤;
ttt)一种包含碱化剂的药物组合物,用于抑制近端肾小管细胞损伤;
uuu)一种包含碱化剂的药物组合物,用于保护近端肾小管细胞;
vvv)一种包含碱化剂的药物组合物,用于维持近端肾小管细胞功能;
www)一种包含碱化剂的药物组合物,用于促进尿毒症物质向体外排泄;
xxx)一种包含碱化剂的药物组合物,用于依赖于尿毒症物质的血中浓度将尿毒症物质向尿中排泄;
aaaa)一种碱化剂的应用,用于制造尿毒症物质的血中浓度降低用药物组合物;
bbbb)一种碱化剂的应用,用于制造尿毒症物质向尿中的排泄促进用药物组合物;
cccc)一种碱化剂的应用,用于制造肾病患者的尿毒症症状的改善用药物组合物;
dddd)一种碱化剂的应用,用于制造肾病患者的尿毒症的治疗或预防用药物组合物;
eeee)一种碱化剂的应用,用于制造慢性肾病的发展抑制用药物组合物;
ffff)一种碱化剂的应用,用于制造慢性肾病患者的透析导入的延迟用药物组合物;
gggg)一种碱化剂的应用,用于制造肾病患者的心肌的纤维化抑制用药物组合物;
hhhh)一种碱化剂的应用,用于制造肾病患者的动脉硬化抑制用药物组合物;
iiii)一种碱化剂的应用,用于制造肾病患者的血管平滑肌细胞的增殖抑制用药物组合物;
jjjj)一种碱化剂的应用,用于制造肾病患者的血管内皮细胞损伤抑制用药物组合物;
kkkk)一种碱化剂的应用,用于制造肾病患者的动脉壁的肥厚抑制用药物组合物;
llll)一种碱化剂的应用,用于制造肾病患者的大动脉的钙化抑制用药物组合物;
mmmm)一种碱化剂的应用,用于制造肾病患者的心血管系统疾病的治疗或预防用药物组合物;
nnnn)一种碱化剂的应用,用于制造肾病患者的动脉硬化的改善用药物组合物;
oooo)一种碱化剂的应用,用于制造肾病患者的动脉壁的肥厚的改善用药物组合物;
pppp)一种碱化剂的应用,用于制造急性肾病的治疗用药物组合物;
qqqq)一种碱化剂的应用,用于制造从急性肾病向慢性肾病的发展抑制用药物组合物;
rrrr)一种碱化剂的应用,用于制造肾小管损伤的治疗或预防用药物组合物;
ssss)一种碱化剂的应用,用于制造肾小管损伤的抑制用药物组合物;
tttt)一种碱化剂的应用,用于制造近端肾小管细胞损伤的抑制用药物组合物;
uuuu)一种碱化剂的应用,用于制造近端肾小管细胞保护用药物组合物;
vvvv)一种碱化剂的应用,用于制造近端肾小管细胞功能维持用药物组合物;
wwww)一种碱化剂的应用,用于制造尿毒症物质向体外的排泄促进用药物组合物;以及
xxxx)一种碱化剂的应用,用于制造依赖于尿毒症物质的血中浓度将尿毒症物质向尿中的排泄用药物组合物。
2.食品组合物
在一个实施方式中,本发明所提供的食品组合物包含碱化剂,发挥尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和/或精氨基琥珀酸,优选硫酸吲哚酚、硫酸对甲酚和苯基乙酰基l谷氨酰胺,更优选硫酸吲哚酚和苯基乙酰基l谷氨酰胺,进一步更优选硫酸吲哚酚)的体外排泄促进效果。
在一个实施方式中,本发明所提供的食品组合物包含碱化剂,发挥尿毒症物质的血中浓度降低效果。
在一个实施方式中,本发明所提供的食品组合物包含碱化剂,发挥尿毒症物质的尿中排泄促进效果。
在一个实施方式中,本发明所提供的食品组合物包含碱化剂,发挥肾功能维持效果。
在一个实施方式中,本发明所提供的食品组合物包含碱化剂,发挥肾小管损伤抑制效果。在此,作为肾小管,例如可举出近端肾小管。
在一个实施方式中,本发明所提供的食品组合物包含碱化剂,发挥近端肾小管细胞损伤抑制效果。
在一个实施方式中,本发明所提供的食品组合物包含碱化剂,发挥近端肾小管细胞保护效果。
在一个实施方式中,本发明所提供的食品组合物包含碱化剂,发挥肾小管功能(例如,水、钠离子、钾离子、钙离子、磷酸离子、碳酸氢根离子、氯离子、葡萄糖、氨基酸、维生素等的再吸收)维持效果。在此,作为肾小管,例如可举出近端肾小管,作为近端肾小管功能,例如可举出葡萄糖、氨基酸、维生素等的再吸收。
在上述实施方式中,本发明所提供的食品组合物发挥抑制伴随慢性肾病的病期发展的尿中(例如,晨尿)的β2-微球蛋白的量(浓度)的增加的效果。
在上述实施方式中,本发明所提供的食品组合物不对慢性肾病患者的肾小球功能造成影响,另一方面,发挥抑制伴随慢性肾病的病期发展的近端肾小管细胞损伤,保护近端肾小管细胞的效果。
对于碱化剂,可以应用上述“1.药物组合物”中记载的碱化剂。作为碱化剂的例子,可举出柠檬酸的可允许作为食品的盐的柠檬酸的医药上可允许的盐(例如,柠檬酸碱金属盐或其水合物或者它们的混合物)、碳酸氢钠,优选为柠檬酸钾的一水合物(c6h5k3o7·h2o)和柠檬酸钠的二水合物(c6h5na3o7·2h2o)的混合物或者柠檬酸钠的二水合物。
对于尿毒症物质,也如上述“1.药物组合物”中所记载。尿毒症物质的例子可举出硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和精氨基琥珀酸。
本发明所提供的食品组合物中的碱化剂的含量可根据食品的种类而适当决定。食品组合物的例子可举出特定保健用食品、营养辅助食品、功能性食品、医院患者用食品、补充剂。作为这些食品组合物的形态,只要包含用于发挥上述效果的有效量的碱化剂且能够口服摄取的形态就没有特别限定,可以为通常的饮食品的形态,也可以作为可应用于上述药物组合物的制剂中适于口服给予的制剂例如片剂、胶囊剂、悬浮剂等制剂提供。对于这些制剂的构成和制造方法,在本说明书中,除能够直接应用上述“1.药物组合物”中记载的药物制剂的构成和制造方法以外,还可以应用药物的制剂技术领域中其本身公知的制剂技术。
例如,在特定保健用食品、营养辅助食品、功能性食品或医院患者用食品的情况下,每1餐的食品可以含有合计1~3g的1/3量的作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物,或者含有1~6g的1/3量的作为碱化剂的碳酸氢钠。特定保健用食品、营养辅助食品、功能性食品、医院患者用食品或补充剂作为片剂提供时,例如,可以在每1片为300mg~600mg的片剂中含有70~80重量%的碱化剂。
本发明所提供的食品组合物不制成制剂而作为通常的饮食品的形态提供时,可根据该食品的种类由本领域技术人员适当制造,例如,可以通过在食品原材料中配合碱化剂(例如,柠檬酸钾和/或柠檬酸钠)而制造。
作为上述饮食品的形态,可举出饮料、酱油、牛奶、酸奶、味噌等液状或乳状或糊状食品;果冻、橡皮糖等半固体状食品;饴糖、口香糖、豆腐、补充剂等固体状食品;或粉末状食品等。
作为饮料,可举出果汁·果实饮料、咖啡饮料、乌龙茶饮料、绿茶饮料、红茶饮料、麦茶饮料、蔬菜饮料、作为软饮料的碳酸饮料、加入果实提取物的饮料、加入蔬菜提取物的果汁、似水饮料、运动饮料、减肥饮料等。
可以在饮料中单独或组合配合抗氧化剂、香料、各种酯类、有机酸类、有机酸盐类、无机酸类、无机酸盐类、无机盐类、色素类、乳化剂、防腐剂、调味剂、甜味剂、酸味剂、果汁提取物类、蔬菜提取物类、花蜜提取物类、ph调节剂、品质稳定剂等添加剂。
本发明所提供的食品组合物除能够与上述“1.药物组合物”中记载的药物组合物的使用方法同样地使用以外,也可以在不以疾病的治疗或预防为目的的范围内使用。即,以本发明的食品组合物中所含的碱化剂为基准时,可以以食品组合物中的碱化剂的使用量与上述药物组合物中所含的碱化剂等量的方式应用于上述药物组合物的应用对象。另外,在一个实施方式中,本发明的“食品组合物”能够应用于不具有“病态的”或“异常的”症状、状态或疾病的对象(例如,人或其它哺乳动物)、即处于“健康的”或“正常的”状态的对象(例如,人或其它哺乳动物),用于维持或增进“健康的”或“正常的”状态。进而,能够应用于“在意肾脏健康的健康人”或“在意肾小管健康的健康人”,用于维持或增进“健康的”或“正常的”状态。此时,上述碱化剂可以为药物组合物的成分,或者也可以为食品组合物的成分,由于上述碱化剂其本身的药理效果基本上相同,因此,上述食品组合物的应用量和应用方法可根据期待的效果,以上述碱化剂为基准而适当调整。
有时将应用于不具有“病态的”或“异常的”症状、状态或疾病的对象(例如,人或其它哺乳动物)即处于“健康的”或“正常的”状态的对象(例如,人或其它哺乳动物)、用于维持或增进“健康的”或“正常的”状态的食品组合物特别称为“功能性食品”。
上述“1.药物组合物”中记载的“给予”这样的术语也能够应用于本发明的“食品组合物”,进而,对于本发明的“食品组合物”,可以将术语“给予”替换为“摄取”。因此,例如,术语“进行给予”、“被给予”等可根据上下文进行词形变化而替换为“使其摄取”、“进行摄取”、“被摄取”等。
因此,作为本发明的食品组合物的实施方式,可举出以下方式。
<1>一种尿毒症物质的血中浓度降低用的食品组合物,包含碱化剂;
<2>一种尿毒症物质的尿中排泄促进用的食品组合物,包含碱化剂;
<3>一种肾功能维持用的食品组合物,包含碱化剂;
<4>一种肾小管损伤抑制用的食品组合物,包含碱化剂;
<5>一种肾小管细胞损伤抑制用、优选近端肾小管细胞损伤抑制用的食品组合物,包含碱化剂;
<6>一种肾小管细胞保护用、优选近端肾小管细胞保护用的食品组合物,包含碱化剂;
<7>一种肾小管功能(例如,水、钠离子、钾离子、钙离子、磷酸离子、碳酸氢根离子、氯离子、葡萄糖、氨基酸、维生素等的再吸收)维持用、优选近端肾小管功能(例如,葡萄糖、氨基酸、维生素等的再吸收)维持用的食品组合物,包含碱化剂;
<11>一种使尿毒症物质的血中浓度降低的方法,包括使需要尿毒症物质的血中浓度降低的对象摄取包含有效量的碱化剂的食品组合物;
<22>一种促进尿毒症物质的尿中排泄的方法,包括使需要促进尿毒症物质的尿中排泄的对象摄取包含有效量的碱化剂的食品组合物;
<33>一种维持肾功能的方法,使需要维持肾功能的对象摄取包含有效量的碱化剂的食品组合物;
<44>一种抑制肾小管损伤的方法,使需要抑制肾小管损伤的对象摄取包含有效量的碱化剂的食品组合物;
<55>一种抑制肾小管细胞、优选近端肾小管细胞损伤的方法,使需要抑制肾小管细胞、优选近端肾小管细胞损伤的对象摄取包含有效量的碱化剂的食品组合物;
<66>一种保护肾小管细胞、优选近端肾小管细胞的方法,使需要保护肾小管细胞、优选近端肾小管细胞的对象摄取包含有效量的碱化剂的食品组合物;
<77>一种维持肾小管功能(例如,水、钠离子、钾离子、钙离子、磷酸离子、碳酸氢根离子、氯离子、葡萄糖、氨基酸、维生素等的再吸收)、优选近端肾小管功能(例如,葡萄糖、氨基酸、维生素等的再吸收)的方法,包括使需要维持肾小管功能、优选近端肾小管功能的对象摄取包含有效量的碱化剂的食品组合物;
<111>一种包含碱化剂的食品组合物,用于降低尿毒症物质的血中浓度;
<222>一种包含碱化剂的食品组合物,用于促进尿毒症物质的尿中排泄;
<333>一种包含碱化剂的食品组合物,用于维持肾功能;
<444>一种包含碱化剂的食品组合物,用于抑制肾小管损伤;
<555>一种包含碱化剂的食品组合物,用于抑制肾小管细胞、优选近端肾小管细胞损伤;
<666>一种包含碱化剂的食品组合物,用于保护肾小管细胞、优选近端肾小管细胞;
<777>一种包含碱化剂的食品组合物,用于维持肾小管功能(例如,水、钠离子、钾离子、钙离子、磷酸离子、碳酸氢根离子、氯离子、葡萄糖、氨基酸、维生素等的再吸收)、优选近端肾小管功能(例如,葡萄糖、氨基酸、维生素等的再吸收);
<1111>一种碱化剂的应用,用于制造尿毒症物质的血中浓度降低用的食品组合物;
<2222>一种碱化剂的应用,用于制造尿毒症物质的尿中排泄促进用的食品组合物;
<3333>一种碱化剂的应用,用于制造肾功能维持用的食品组合物;
<4444>一种碱化剂的应用,用于制造肾小管损伤抑制用的食品组合物;
<5555>一种碱化剂的应用,用于制造肾小管细胞、优选近端肾小管细胞损伤抑制用的食品组合物;
<6666>一种碱化剂的应用,用于制造肾小管细胞、优选近端肾小管细胞保护用的食品组合物;以及
<7777>一种碱化剂的应用,用于制造肾小管功能(例如,水、钠离子、钾离子、钙离子、磷酸离子、碳酸氢根离子、氯离子、葡萄糖、氨基酸、维生素等的再吸收)、优选近端肾小管功能(例如,葡萄糖、氨基酸、维生素等的再吸收)维持用的食品组合物。
本发明的食品组合物优选在其包装、容器或说明书显示尿毒症物质的血中浓度降低、尿毒症物质的尿中排泄促进、肾功能维持、肾小管损伤抑制、肾小管细胞损伤抑制、近端肾小管细胞损伤抑制、肾小管细胞保护、近端肾小管细胞保护、肾小管功能(例如,水、钠离子、钾离子、钙离子、磷酸离子、碳酸氢根离子、氯离子、葡萄糖、氨基酸、维生素等的再吸收)维持、或近端肾小管功能(例如,葡萄糖、氨基酸、维生素等的再吸收)维持等效果。
在一个实施方式中,本发明的“食品组合物”被尿中的β2-微球蛋白浓度为290μg/l以下、优选50~150μg/l的对象(例如,人或其它哺乳动物)摄取。
在一个实施方式中,本发明的“食品组合物”被血中的半胱氨酸蛋白酶抑制剂c浓度为0.5~2.2mg/l、优选1.0~1.3mg/l的对象(例如,人或其它哺乳动物)摄取。
在一个实施方式中,通过本发明的“食品组合物”的摄取,尿中的β2-微球蛋白浓度的增加得到抑制。
在一个实施方式中,通过本发明的“食品组合物”的摄取,在给予12周后,尿中的β2-微球蛋白浓度的增加得到抑制。
在一个实施方式中,通过本发明的“食品组合物”的摄取,与给予开始前相比,尿中的β2-微球蛋白浓度实质上没有降低。
在一个实施方式中,通过本发明的“食品组合物”的摄取,在给予12周后,与给予开始前相比,尿中的β2-微球蛋白浓度实质上没有降低。
在一个实施方式中,通过本发明的“食品组合物”的摄取,与给予开始前相比,血中的半胱氨酸蛋白酶抑制剂c实质上没有增加。
在一个实施方式中,通过本发明的“食品组合物”的摄取,与给予开始前相比,血中的半胱氨酸蛋白酶抑制剂c实质上没有增加。
在一个实施方式中,通过本发明的“食品组合物”的摄取,抑制伴随慢性肾病的病期发展的晨尿中的β2-微球蛋白的量的增加。
在一个实施方式中,通过本发明的“食品组合物”的摄取,不会对慢性肾病患者的肾小球功能造成影响,另一方面,抑制伴随慢性肾病的病期发展的近端肾小管细胞损伤,保护近端肾小管细胞。
3.判定血中的尿毒症物质的浓度降低的方法等
在一个实施方式中,本发明提供一种判定慢性肾病患者的血中的尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和/或精氨基琥珀酸,优选硫酸吲哚酚、马尿酸和/或苯基乙酰基l谷氨酰胺,更优选硫酸吲哚酚和苯基乙酰基l谷氨酰胺,进一步更优选硫酸吲哚酚)的浓度降低的方法,包括测定尿的ph。
另外,在一个实施方式中,本发明提供一种判定慢性肾病患者的尿毒症物质(硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和/或精氨基琥珀酸,优选硫酸吲哚酚、硫酸对甲酚、马尿酸和/或苯基乙酰基l谷氨酰胺,更优选硫酸吲哚酚和苯基乙酰基l谷氨酰胺,进一步更优选硫酸吲哚酚)向尿中的排出促进的方法,包括测定尿的ph。
体液中的尿毒症物质(例如,硫酸吲哚酚)的含量的测定可以通过hplc法、酶法进行测定。然而,这些测定法需要专门且高价的试剂。
如本说明书中记载的那样,通过给予碱化剂,血中的尿毒症物质(例如,硫酸吲哚酚浓度、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和/或精氨基琥珀酸)降低,这些尿毒症物质向尿中的排泄得到促进,因此,通过慢性肾病患者测定自身的尿的ph,能够非常简单且廉价地判定血中的尿毒症物质(例如,硫酸吲哚酚浓度、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和/或精氨基琥珀酸)的降低和/或尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和/或精氨基琥珀酸)向尿中的排泄促进。ph的测定只要使用周知技术即可,例如可以使用ph试纸、ph试验液、简单的ph测定器。
在一个实施方式中,慢性肾病患者从开始服用碱化剂(例如,柠檬酸钾的一水合物和柠檬酸钠的二水合物混合物或者柠檬酸钠的二水合物)时经时测定晨尿(起床后最初的尿)的ph,如果尿的ph变高,则能够简单地判断实现了血中的尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和/或精氨基琥珀酸,优选硫酸吲哚酚、马尿酸和/或苯基乙酰基l谷氨酰胺,更优选硫酸吲哚酚和苯基乙酰基l谷氨酰胺,进一步更优选硫酸吲哚酚)的浓度的降低和/或尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和/或精氨基琥珀酸,优选硫酸吲哚酚、硫酸对甲酚、马尿酸和/或苯基乙酰基l谷氨酰胺,更优选硫酸吲哚酚和苯基乙酰基l谷氨酰胺,进一步更优选硫酸吲哚酚)向尿中的排泄的促进。
另外,在一个实施方式中,慢性肾病患者在服用碱化剂(例如,柠檬酸钾的一水合物和柠檬酸钠的二水合物混合物或者柠檬酸钠的二水合物)后测定晨尿(起床后最初的尿)的ph,如果尿的ph为5.2~6.8的范围(例如,尿的ph为ph5.5~ph6.8、ph5.8~ph6.8、ph5.8~ph6.5、ph5.8~ph6.2、ph5.8以上且小于ph6.2、ph6.0~ph6.5、ph6.0~ph6.4、ph6.0~ph6.3、ph6.0~ph6.2、ph6.0以上且小于ph6.2、ph6.1~ph6.3、ph6.2~6.8、ph6.2~ph6.5或ph6.5~6.8的范围),则能够简单地判断实现了血中的尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和/或精氨基琥珀酸,优选硫酸吲哚酚、马尿酸和/或苯基乙酰基l谷氨酰胺,更优选硫酸吲哚酚和苯基乙酰基l谷氨酰胺,进一步更优选硫酸吲哚酚)的浓度的降低和/或尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和/或精氨基琥珀酸,优选硫酸吲哚酚、硫酸对甲酚、马尿酸和/或苯基乙酰基l谷氨酰胺,更优选硫酸吲哚酚和苯基乙酰基l谷氨酰胺,进一步更优选硫酸吲哚酚)向尿中的排泄的促进。
如此得到的是否实现了血中的尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和/或精氨基琥珀酸)的浓度的降低和/或尿毒症物质(例如,硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和/或精氨基琥珀酸)向尿中的排泄的促进的判断可成为慢性肾病的发展是否得到抑制的诊断的辅助。
因此,在一个实施方式中,本发明提供一种判定慢性肾病的发展抑制的方法,包括测定给予了碱化剂(例如,柠檬酸钾的一水合物和柠檬酸钠的二水合物混合物或者柠檬酸钠的二水合物)的患者的尿(例如,晨尿)的ph。如果确认到经时的尿的ph的上升或者尿的ph为5.8~6.8的范围(例如,尿的ph为6.0~6.2的范围),则可成为慢性肾病的病期发展得到抑制这样的诊断的辅助。
在一个实施方式中,本发明所提供的药物组合物是用于降低尿毒症物质的血中浓度的包含碱化剂的药物组合物,分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物。
在一个实施方式中,本发明所提供的药物组合物是用于降低尿毒症物质的血中浓度的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于促进尿毒症物质向尿中的排泄的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于促进尿毒症物质向尿中的排泄的包含碱化剂的药物组合物。在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于改善肾病患者的尿毒症症状的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于改善肾病患者的尿毒症症状的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于治疗或预防肾病患者的尿毒症的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于治疗或预防肾病患者的尿毒症的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制慢性肾病的发展的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制慢性肾病的发展的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于慢性肾病患者的透析导入的延迟的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于慢性肾病患者的透析导入的延迟的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的心肌的纤维化的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的心肌的纤维化的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的动脉硬化的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的动脉硬化的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的血管平滑肌细胞的增殖的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的血管平滑肌细胞的增殖的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的血管内皮细胞损伤的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的血管内皮细胞损伤的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的动脉壁的肥厚的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的动脉壁的肥厚的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的大动脉的钙化的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的大动脉的钙化的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于预防或治疗肾病患者的心血管系统疾病的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于治疗或预防肾病患者的心血管系统疾病的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于改善肾病患者的动脉硬化的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于改善肾病患者的动脉硬化的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于改善肾病患者的动脉壁的肥厚的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于改善肾病患者的动脉壁的肥厚的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于治疗急性肾病的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于治疗急性肾病的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制从急性肾病向慢性肾病发展的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制从急性肾病向慢性肾病发展的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于治疗或预防肾小管损伤的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于治疗或预防肾小管损伤的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾小管损伤的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾小管损伤的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制近端肾小管细胞损伤的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制近端肾小管细胞损伤的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于保护近端肾小管细胞的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于保护近端肾小管细胞的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于维持近端肾小管细胞功能的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于维持近端肾小管细胞功能的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于促进尿毒症物质向体外排泄的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于促进尿毒症物质向体外排泄的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于依赖于尿毒症物质的血中浓度将尿毒症物质向尿中排泄的包含碱化剂的药物组合物,将作为碱化剂的柠檬酸钾一水合物和柠檬酸钠二水合物分别以0.5~1.5g/天合计1~3g/天、分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于依赖于尿毒症物质的血中浓度将尿毒症物质向尿中排泄的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有柠檬酸钾一水合物231.5mg和柠檬酸钠二水合物195.0mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于降低尿毒症物质的血中浓度的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于降低尿毒症物质的血中浓度的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于促进尿毒症物质向尿中排泄的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于促进尿毒症物质向尿中排泄的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于改善肾病患者的尿毒症症状的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于改善肾病患者的尿毒症症状的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于治疗或预防肾病患者的尿毒症的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于治疗或预防肾病患者的尿毒症的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制慢性肾病的发展的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制慢性肾病的发展的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于慢性肾病患者的透析导入的延迟的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于慢性肾病患者的透析导入的延迟的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的心肌的纤维化的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的心肌的纤维化的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的动脉硬化的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的动脉硬化的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的血管平滑肌细胞的增殖的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的血管平滑肌细胞的增殖的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的血管内皮细胞损伤的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的血管内皮细胞损伤的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的动脉壁的肥厚的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的动脉壁的肥厚的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的大动脉的钙化的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾病患者的大动脉的钙化的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于治疗或预防肾病患者的心血管系统疾病的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是治疗或预防肾病患者的心血管系统疾病的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是改善肾病患者的动脉硬化的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于改善肾病患者的动脉硬化的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是改善肾病患者的动脉壁的肥厚的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于改善肾病患者的动脉壁的肥厚的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于治疗急性肾病的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于治疗急性肾病的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制从急性肾病向慢性肾病发展的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是抑制从急性肾病向慢性肾病发展的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于治疗或预防肾小管损伤的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于治疗或预防肾小管损伤的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾小管损伤的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制肾小管损伤的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制近端肾小管细胞损伤的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于抑制近端肾小管细胞损伤的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于保护近端肾小管细胞的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于保护近端肾小管细胞的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于维持近端肾小管细胞功能的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于维持近端肾小管细胞功能的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于促进尿毒症物质向体外排泄的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于促进尿毒症物质向体外排泄的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于依赖于尿毒症物质的血中浓度将尿毒症物质向尿中排泄的包含碱化剂的药物组合物,将作为碱化剂的碳酸氢钠以1~3g/天分为1天1~5次、优选1天3次进行口服给予。
在一个实施方式中,本发明所提供的药物组合物是用于依赖于尿毒症物质的血中浓度将尿毒症物质向尿中排泄的包含碱化剂的药物组合物,在1给予单位(优选1片的片剂)中含有碳酸氢钠500mg,将每天3给予单位~6给予单位分为1天3次进行口服给予。
以下,通过实施例对本发明进一步进行说明,但本发明并不限定于这些实施例。
实施例
为了研究通过作为口服碱化剂的柠檬酸钾·柠檬酸钠水合物配合制剂和小苏打制剂的口服给予是否促进尿毒症物质的尿中排泄,实施了人临床试验。
1.方法
将阶段g2~g3b的慢性肾病患者(egfr:30~89ml/min/1.73m2)47名随机地分为柠檬酸钾·柠檬酸钠水合物配合制剂给予组(a组:16名)、小苏打(碳酸氢钠)制剂给予组(b组:16名)和对照组(c组:15名)。各组中以年龄、性别、有无糖尿病、egfr没有偏向的方式将患者分类。各组基于“ckd诊疗指南-治疗概要”进行治疗(以下,称为标准治疗)。
对于对照组,不给予碱化剂。对于a组,将含有柠檬酸钾(c6h5k3o7·h2o)231.5mg和柠檬酸钠水合物(c6h5na3o7·2h2o)195.0mg的片剂以1天3片、1天3次(早、午、晚)口服给予24周。应予说明,经时进行晨尿的ph管理,对于晨尿小于ph6.5的病例,可适当地通过医生的判断增量至1天6片、1天3次(早、午、晚)。对于b组,将含有碳酸氢钠500mg的片剂以1天3片、1天3次(早、午、晚)口服给予24周。应予说明,经时进行晨尿的ph管理,对于晨尿小于ph6.5的病例,可适当通过医生的判断增量至1天6片、1天3次(早、午、晚)。
采取给予开始前、给予开始后6周、12周、24周的晨尿和血液,将各检体在-80℃保存。对于尿中和血浆中的硫酸吲哚酚、硫酸对甲酚、苯基乙酰基l谷氨酰胺、马尿酸和精氨基琥珀酸,参照本领域中使用的方法(sato,e.,et.al.,metabolicalterationbyindoxylsulfateinskeletalmuscleinduceuremicsarcopeniainchronickidneydisease.,scirep.2016nov10;6:36618.doi:10.1038/srep36618.等),使用以下的液相色谱三重四级杆质谱仪(lc-ms/ms)进行定量分析。
lc使用nanospacesi-2(资生堂制),分析柱使用capcellpakmgiii。
ms使用tsqquantiva(thermofisherscientific公司制),将5种化合物通过负离子模式进行离子化,使用选择性反应监测法进行检测。使用通过各化合物的标准溶液制作的校准曲线计算定量值。
另外,通过使用lztest‘荣研’β2-m和lz-β2-m标准u‘荣研’(荣研化学,东京,日本)的乳胶凝集免疫法测定尿中的β2-微球蛋白量。进而,通过使用nescoatgc半胱氨酸蛋白酶抑制剂c(nm)(alfresapharma,大阪,日本)的胶体金凝集法测定血清中的半胱氨酸蛋白酶抑制剂c量。
对于统计解析,组间比较使用mann-whitney检验,经时变化的比较使用wilcoxon检验。另外,关于相关性,使用pearson检验。
2.结果
根据使用lc-ms/ms的测定结果,对a组(柠檬酸钾·柠檬酸钠水合物配合制剂给予组)、b组(碳酸氢钠制剂给予组)和c组(对照组)的各患者计算以下项目:
(i)给予开始前的血浆中的各尿毒症物质的浓度
(ii)给予开始前的晨尿中的各尿毒症物质的浓度
(iii)给予开始前的晨尿中的尿毒症物质浓度与血浆中的尿毒症物质浓度之比(尿中的尿毒症物质量/血浆中的尿毒症物质量)
(iv)给予开始后6周、12周、24周的血浆中的各尿毒症物质的浓度
(v)给予开始后6周、12周、24周的晨尿中的各尿毒症物质的浓度
(vi)给予开始后6周、12周、24周的晨尿中的尿毒症物质浓度与血浆中的尿毒症物质浓度之比(尿中的尿毒症物质量/血浆中的尿毒症物质量)
(vii)给予开始后6周、12周、24周的血浆中的各尿毒症物质的浓度的自给予开始前的变化量
(viii)给予开始后6周、12周、24周的晨尿中的各尿毒症物质的浓度的自给予开始前的变化量
(ix)给予开始后6周、12周、24周的晨尿中的尿毒症物质浓度与血浆中的尿毒症物质浓度之比(尿中的尿毒症物质量/血浆中的尿毒症物质量)的自给予开始前的变化量
然后,对上述(i)~(ix)计算各组的平均值和sd。应予说明,对于上述(iv)~(ix),分别以各组的给予开始后6周、12周、24周的全部数据为对象而计算各组的平均值和sd。
将结果示于以下的表。应予说明,表中和图中,将a组:柠檬酸钾·柠檬酸钠水合物配合制剂给予组记载为“柠檬酸盐”,将b组:碳酸氢钠制剂给予组记载为“碳酸氢盐”。另外,表中的括号内的数值表示病例数。
表1-1-1:血浆中的硫酸吲哚酚量(ng/ml)、
表1-1-2:血浆中的硫酸吲哚酚的自给予开始前的变化量(ng/ml)、
表1-2-1:晨尿中的硫酸吲哚酚量(ng/ml)、
表1-2-2:晨尿中的硫酸吲哚酚的自给予开始前的变化量(ng/ml)、
表1-3-1:尿中的硫酸吲哚酚量与血浆中的硫酸吲哚酚量之比、
表1-3-2:尿中的硫酸吲哚酚量与血浆中的硫酸吲哚酚量之比的自给予开始前的变化量、
表2-1-1:血浆中的硫酸对甲酚量(ng/ml)、
表2-1-2:血浆中的硫酸对甲酚的自给予开始前的变化量(ng/ml)、
表2-2-1:晨尿中的硫酸对甲酚量(ng/ml)、
表2-2-2:晨尿中的硫酸对甲酚的自给予开始前的变化量(ng/ml)、
表2-3-1:尿中的硫酸对甲酚量与血浆中的硫酸对甲酚量之比、
表2-3-2:尿中的硫酸对甲酚量与血浆中的硫酸对甲酚量之比的自给予开始前的变化量、
表3-1-1:血浆中的马尿酸量(ng/ml)、
表3-1-2:血浆中的马尿酸的自给予开始前的变化量(ng/ml)、
表3-2-1:晨尿中的马尿酸量(ng/ml)、
表3-2-2:晨尿中的马尿酸的自给予开始前的变化量(ng/ml)、
表3-3-1:尿中的马尿酸量与血浆中的马尿酸量之比、
表3-3-2:尿中的马尿酸量与血浆中的马尿酸量之比的自给予开始前的变化量、
表4-1-1:血浆中的精氨基琥珀酸量(ng/ml)、
表4-1-2:血浆中的精氨基琥珀酸的自给予开始前的变化量(ng/ml)、
表4-2-1:晨尿中的精氨基琥珀酸量(ng/ml)、
表4-2-2:晨尿中的精氨基琥珀酸的自给予开始前的变化量(ng/ml)、
表4-3-1:尿中的精氨基琥珀酸量与血浆中的精氨基琥珀酸量之比、
表4-3-2:尿中的精氨基琥珀酸量与血浆中的精氨基琥珀酸量之比的自给予开始前的变化量、
表5-1-1:血浆中的苯基乙酰基l谷氨酰胺(pag)量(ng/ml)、
表5-1-2:血浆中的苯基乙酰基l谷氨酰胺(pag)的自给予开始前的变化量(ng/ml)、
表5-2-1:晨尿中的苯基乙酰基l谷氨酰胺(pag)量(ng/ml)、
表5-2-2:晨尿中的苯基乙酰基l谷氨酰胺(pag)的自给予开始前的变化量(ng/ml)、
表5-3-1:尿中的苯基乙酰基l谷氨酰胺(pag)量与血浆中的苯基乙酰基l谷氨酰胺(pag)量之比、
表5-3-2:尿中的苯基乙酰基l谷氨酰胺(pag)量与血浆中的苯基乙酰基l谷氨酰胺(pag)量之比的自给予开始前的变化量。
a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)与b组(碳酸氢盐:碳酸氢钠制剂给予组)和c组(对照:对照组)相比,给予6、12和24周后的血浆中的硫酸吲哚酚浓度为低值(参照表1-1-1)。另外,a组与c组相比,给予12和24周后的晨尿中,硫酸吲哚酚(is)浓度为高值(参照表1-2-1)。对于6~24周的血浆硫酸吲哚酚浓度,a组与b组和c组相比,是显著低的值(参照表1-1-1),对于6~24周的晨尿中的硫酸吲哚酚浓度的增加,a组与b组和c组相比,显著大(参照表1-2-2)。
另外,通过将柠檬酸钾·柠檬酸钠水合物配合制剂对慢性肾病患者进行给予,作为尿毒症物质的硫酸吲哚酚的尿中浓度与给予前相比增加,硫酸吲哚酚的血中浓度与给予前相比降低。即使是相同的碱化剂,在碳酸氢钠制剂时没有确认到这样的效果。与碳酸氢钠制剂相比,柠檬酸钾·柠檬酸钠水合物配合制剂发挥更高的血中硫酸吲哚酚浓度降低效果和尿中硫酸吲哚酚浓度增加效果。从给予12周后确认到基于柠檬酸钾·柠檬酸钠水合物配合制剂的血中硫酸吲哚酚浓度降低效果和尿中硫酸吲哚酚浓度增加效果。
根据尿中的硫酸吲哚酚浓度与血浆中的硫酸吲哚酚浓度之比的值,显示通过给予柠檬酸钾·柠檬酸钠水合物配合制剂,硫酸吲哚酚从血中向尿的排泄得到促进,向体外的排泄得到促进。而且,通过给予柠檬酸钾·柠檬酸钠水合物配合制剂确认到硫酸吲哚酚的从血中向尿的排泄效果,另一方面,碳酸氢钠制剂给予没有确认到该效果(参照表1-3-1、1-3-2)。
[表1-1-1]
[表1-1-1]血浆中硫酸吲哚酚
平均值±sd
ap=0.0288,bp=0.0451vs对照以及cp=0.0350vs碳酸氢盐(mann-whltney)
[表1-1-2]
[表1-1-2]血浆中硫酸吲哚酚(从0周起的△实测值变换)
平均值±sd
[表1-2-1]
[表1-2-1]尿中硫酸吲哚酚
平均值±sd
dp=0.0073vs对照以及ap=0.0385vs碳酸氢盐(mann-whltney)
ap=0.0103vs0周(wilcoxon)
[表1-2-2]
[表1-2-2]尿中硫酸吲哚酚(从0周起的△实测值变换)
平均值±sd
ap=0.0141vs对照以及cp=0.0233,dp=0.0438vs碳酸氢盐(mann-whitney)
[表1-3-1]
[表1-3-1]硫酸吲哚酚-尿/血浆比
平均值±sd
ap=0.0482,cp=0.0322以及dp=0.0141vs对照(mann-whltney)
[表1-3-2]
[表1-3-2]硫酸吲哚酚-尿/血浆比(从0周起的△实测值变换)
平均值±sd
bp=0.0239,cp=0.0006vs对照以及dp=0.0457,ep=0.0292vs碳酸氢盐(mann-whltney)
对于硫酸对甲酚(pcs),a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)与c组(对照:对照组)相比,给予12和24周后的晨尿中的硫酸对甲酚浓度为高值,与b组(碳酸氢盐:碳酸氢钠制剂给予组)相比,a组(柠檬酸钾·柠檬酸钠水合物配合制剂给予组)的给予6、12和24周后的晨尿中的硫酸对甲酚浓度也为高值(参照表2-2-1)。仅在a组中确认到6~24周的晨尿中的硫酸对甲酚浓度的增加(参照表2-2-2)。
另外,通过将柠檬酸钾·柠檬酸钠水合物配合制剂对慢性肾病患者进行给予,作为尿毒症物质的硫酸对甲酚的尿中浓度与给予前相比增加(参照表2-2-1、2-2-2)。即使是相同的碱化剂,在碳酸氢钠制剂时没有确认到这样的效果,与碳酸氢钠制剂相比,柠檬酸钾·柠檬酸钠水合物配合制剂发挥强的尿中硫酸对甲酚浓度增加效果。从给予12周后确认到基于柠檬酸钾·柠檬酸钠水合物配合制剂的尿中硫酸对甲酚浓度增加效果。
另一方面,通过给予碳酸氢钠制剂,作为尿毒症物质的硫酸对甲酚的血浆浓度与给予前相比减少(参照表2-1-2)。与a组和c组相比,在b组中较强地确认到这样的硫酸对甲酚的血浆浓度降低效果(参照表2-1-2)。
根据尿中的硫酸对甲酚浓度与血浆中的硫酸对甲酚浓度之比的值,表明通过给予柠檬酸钾·柠檬酸钠水合物配合制剂,硫酸对甲酚的从血中向尿的排泄得到促进,向体外的排泄得到促进。而且,显示柠檬酸钾·柠檬酸钠水合物配合制剂给予与碳酸氢钠制剂给予相比,硫酸对甲酚的从血中向尿的排泄效果强(参照表2-3-1、2-3-2)。
[表2-1-1]
[表2-1-1]血浆中硫酸对甲酚
平均值±sd
[表2-1-2]
[表2-1-2]血浆中硫酸对甲酚(从0周起的△实测值变换)
平均值±sd
cp=0.0377vs碳酸氢盐(mann-whitney)
[表2-2-1]
[表2-2-1]尿中硫酸对甲酚
平均值±sd
[表2-2-2]
[表2-2-2]尿中硫酸对甲酚(从0周起的△实测值变换)
平均值±sd
ap=0.0170,bp=0.0109vs对照以及cp=0.0242vs碳酸氢盐(mann-whltney)
[表2-3-1]
[表2-3-1]硫酸对甲酚-尿/血浆比
平均值±sd
ap=0.0221,bp=0.0094,cp=0.0364以及dp=0.0055vs对照(mann-whitney)
[表2-3-2]
[表2-3-2]硫酸对甲酚-尿/血浆比(从0周起的△实测值变换)
平均值±sd
对于马尿酸(ha),a组(柠檬酸:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)与b组(碳酸氢盐:碳酸氢钠制剂给予组)和c组(对照:对照组)相比,给予24周后的血浆中的马尿酸浓度为低值(参照表3-1-1)。这样的效果在给予碳酸氢钠制剂时没有看到。另外,a组与c组相比,给予12和24周后的晨尿中的马尿酸浓度为高值(参照表3-2-1)。
另外,通过将柠檬酸钾·柠檬酸钠水合物配合制剂对慢性肾病患者进行给予,在给予24周后,作为尿毒症物质的马尿酸的血浆浓度与给予前相比降低(参照表3-1-1、3-2-2),马尿酸的尿中浓度与给予前相比增加(参照表3-2-1、3-2-2)。仅在a组中确认到6~24周的晨尿中的马尿酸浓度的增加(参照表2-2-2)。即使是相同的碱化剂,与碳酸氢钠制剂相比,柠檬酸钾·柠檬酸钠水合物配合制剂发挥更高的尿中马尿酸浓度增加效果。从给予6周后确认到基于柠檬酸钾·柠檬酸钠水合物配合制剂的尿中马尿酸浓度增加效果。
根据尿中的马尿酸浓度与血浆中的马尿酸浓度之比的值,表明通过给予柠檬酸钾·柠檬酸钠水合物配合制剂,马尿酸的从血中向尿的排泄得到促进,向体外的排泄得到促进。而且,显示柠檬酸钾·柠檬酸钠水合物配合制剂给予与碳酸氢钠制剂给予相比,6~24周的马尿酸的从血中向尿的排泄效果强(参照表3-3-1、3-3-2)。
[表3-1-1]
[表3-1-1]血浆中马尿酸
平均值±sd
bp=0.0181以及cp=0.0215vs0周(wilcoxon)
[表3-1-2]
[表3-1-2]血浆中马尿酸(从0周起的△实测值变换)
平均值±sd
ap=0.0430,cp=0.0164,p=0.0008vs对照
以及dp=0.0093vs碳酸氢盐(mann-whitney)
[表3-2-1]
[表3-2-1]尿中马尿酸
平均值±sd
[表3-2-2]
[表3-2-2]尿中马尿酸(从0周起的△实测值变换)
平均值±sd
ap=0.0431vs对照(mann-whltney)
[表3-3-1]
[表3-3-1]马尿酸-尿/血浆比
平均值±sd
bp=0.0239vs对照以及cp=0.0355,
(mann-whltney)
fp=0.0479vs0周(wllcoxon)
[表3-3-2]
[表3-3-2]马尿酸-尿/血浆比(从0周起的△实测值变换)
平均值±sd
ap=0.0451,bp=0.0170vs对照(mann-whltney)
对于精氨基琥珀酸(asa),a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)与c组(对照:对照组)相比,晨尿中的精氨基琥珀酸浓度为高值,另一方面,与b组(碳酸氢盐:碳酸氢钠制剂给予组)相比为低值(参照表4-2-1)。
另外,通过将柠檬酸钾·柠檬酸钠水合物配合制剂对慢性肾病患者进行给予,作为尿毒症物质的精氨基琥珀酸的尿中浓度与给予前相比增加(参照表4-2-1、4-2-2)。从给予12周后确认到基于柠檬酸钾·柠檬酸钠水合物配合制剂的尿中精氨基琥珀酸浓度增加效果。对于6~24周的晨尿中的精氨基琥珀酸浓度的增加,与a组相比,b组更增加(参照表4-2-2)。
根据尿中的精氨基琥珀酸浓度与血浆中的精氨基琥珀酸浓度之比的值,表明通过给予柠檬酸钾·柠檬酸钠水合物配合制剂,精氨基琥珀酸的从血中向尿的排泄得到促进,向体外的排泄得到促进。而且,显示碳酸氢钠制剂给予与柠檬酸钾·柠檬酸钠水合物配合制剂给予相比,6~24周的精氨基琥珀酸的从血中向尿的排泄效果强(参照表4-3-1、4-3-2)。
[表4-1-1]
[表4-1-1]血浆中精氨基琥珀酸
平均值±sd
[表4-1-2]
[表4-1-2]血浆中精氨基琥珀酸(从0周起的△实测值变换)
平均值±sd
[表4-2-1]
[表4-2-1]尿中精氨基琥珀酸
平均值±sd
bp=0.0215vs0周(wllcoxon)
[表4-2-2]
[表4-2-2]尿中精氨基琥珀酸(从0周起的△实测值变换)
平均值±sd
ap=0.0105以及bp=0.0175vs对照(mann-whitney)
[表4-3-1]
[表4-3-1]精氨基琥珀酸-尿/血浆比
平均值±sd
[表4-3-2]
[表4-3-2]精氨基琥珀酸-尿/血浆比(从0周起的△实测值变换)
平均值±sd
ap=0.0403vs对照(mann-whitney)
对于苯基乙酰基l谷氨酰胺(pag),a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)与c组(对照:对照组)相比,血浆中的苯基乙酰基l谷氨酰胺浓度为低值(参照表5-1-1)。a组与c组相比,给予12和24周后的晨尿中,苯基乙酰基l谷氨酰胺浓度为高值(参照表5-2-1)。
另外,通过将柠檬酸钾·柠檬酸钠水合物配合制剂对慢性肾病患者进行给予,给予12和24周后的作为尿毒症物质的苯基乙酰基l谷氨酰胺的尿中浓度与给予前相比增加(参照表5-2-1、5-2-2)。即使是相同的碱化剂,在碳酸氢钠制剂时没有确认到这样的效果。从给予12周后确认到基于柠檬酸钾·柠檬酸钠水合物配合制剂的尿中苯基乙酰基l谷氨酰胺浓度增加效果。通过将柠檬酸钾·柠檬酸钠水合物配合制剂对慢性肾病患者进行给予,作为尿毒症物质的苯基乙酰基l谷氨酰胺的血浆浓度与给予前相比降低(参照表5-1-1、5-2-2)。与柠檬酸钾·柠檬酸钠水合物配合制剂相比,在碳酸氢钠制剂时较强地确认到苯基乙酰基l谷氨酰胺的血浆浓度降低效果(参照表5-1-2)。
根据尿中的苯基乙酰基l谷氨酰胺浓度与血浆中的苯基乙酰基l谷氨酰胺浓度之比的值,显示通过给予柠檬酸钾·柠檬酸钠水合物配合制剂,苯基乙酰基l谷氨酰胺的从血中向尿的排泄得到促进,向体外的排泄得到促进。而且,显示柠檬酸钾·柠檬酸钠水合物配合制剂给予与碳酸氢钠制剂给予相比,苯基乙酰基l谷氨酰胺的从血中向尿的排泄效果强(参照表5-3-1、5-3-2)。
[表5-1-1]
[表5-1-1]血浆中苯基乙酰基l谷氨酰胺(pag)
平均值±sd
ap=0.0326以及cp=0.0065vs对照(mann-whitney)
[表5-1-2]
[表5-1-2]血浆中pag(从0周起的△实测值变换)
平均值±sd
[表5-2-1]
[表5-2-1]尿中苯基乙酰基l谷氨酰胺(pag)
平均值±sd
ap=0.0151,bp=0.0335vs0周(wllcoxon)
[表5-2-2]
[表5-2-2]尿中pag(从0周起的△实测值变换)
平均值±sd
bp=0.0105,cp=0.0062vs对照以及ap=0.0287,dp=0.0282vs碳酸氢盐(mann-whitney)
[表5-3-1]
[表5-3-1]苯基乙酰基l谷氨酰胺-尿/血浆比
平均值±sd
ap=0.0358以及bp=0.0107vs对照(mann-whltney)
op=0.0103vs0周(wilcoxon)
[表5-3-2]
[表5-3-2]pag-尿/血浆比(从0周起的△实测值变换)
平均值±sd
bp=0.0194vs对照(mann-whltney)
对于各尿毒症物质的血浆浓度、晨尿中浓度、晨尿中的浓度与血浆中的浓度之比,如果将将柠檬酸钾·柠檬酸钠水合物配合制剂(柠檬酸盐)和碳酸氢钠制剂(碳酸氢盐)的效果汇总,则如下表所示。下表中,对于对照药,在柠檬酸钾·柠檬酸钠水合物配合制剂(柠檬酸盐)的情况下为碳酸氢钠制剂(碳酸氢盐),在碳酸氢钠制剂(碳酸氢盐)的情况下为柠檬酸钾·柠檬酸钠水合物配合制剂(柠檬酸盐)。与对照组或对照药组相比,效果显著优异时,记载为○,相对于对照组或对照药组,效果显著差时,记载为×,没有显著差异时,记载为-。应予说明,关于晨尿中的硫酸吲哚酚浓度的碳酸氢钠制剂(碳酸氢盐)给予组相对于对照组的效果,在下表中记载为(○)。这是因为碳酸氢钠制剂(碳酸氢盐)给予组与对照组相比,显著使晨尿中的硫酸吲哚酚浓度增加,但与给予开始前相比,碳酸氢钠制剂(碳酸氢盐)给予后的晨尿中硫酸吲哚酚浓度降低,因此,无法判断是否具有硫酸吲哚酚向尿中的排泄的促进效果。
根据下表,在硫酸吲哚酚(is)和苯基乙酰基l谷氨酰胺(pag)时明确地确认到基于碱化剂的血液(血浆)中的尿毒症物质浓度降低效果。其中,在硫酸吲哚酚(is)时,柠檬酸钾·柠檬酸钠水合物配合制剂(柠檬酸盐)的给予比碳酸氢钠制剂(碳酸氢盐)的给予显著降低。
另外,在硫酸吲哚酚(is)、硫酸对甲酚(pcs)、马尿酸(ha)、精氨基琥珀酸(asa)和苯基乙酰基l谷氨酰胺(pag)时明确地确认到基于碱化剂的尿中的尿毒症物质浓度增加效果(向尿中的尿毒素物质排泄效果)。其中,在硫酸吲哚酚(is)、硫酸对甲酚(pcs)和苯基乙酰基l谷氨酰胺(pag)时,柠檬酸钾·柠檬酸钠水合物配合制剂(柠檬酸盐)的给予与碳酸氢钠制剂(碳酸氢盐)的给予相比,尿中的尿毒症物质浓度(向尿中的排泄)显著增加。
在硫酸吲哚酚(is)、硫酸对甲酚(pcs)和苯基乙酰基l谷氨酰胺(pag)时明确地确认到基于碱化剂的从血中向尿中的尿毒症物质排泄效果(体外排泄效果)。其中,在硫酸吲哚酚(is)时,柠檬酸钾·柠檬酸钠水合物配合制剂(柠檬酸盐)的给予与碳酸氢钠制剂(碳酸氢盐)的给予相比,从血中向尿中的尿毒症物质排泄(体外排泄)显著增加。
[表6]
[表6]碱化剂对血浆中和尿中的尿毒症物质浓度的影响-对照、对照药比较-
优选的效果:血浆:尿↑u/p比↑效果优异时:○效果差时:x没有显著差异时:-
根据上述表,大体可以理解柠檬酸钾·柠檬酸钠水合物配合制剂与碳酸氢钠制剂相比,发挥高的尿毒症物质的体外排泄效果。另外,表明通过不仅对阶段g3b而且对阶段g2的慢性肾病患者给予碱化剂,能够抑制慢性肾病的发展,而且,与碳酸氢钠制剂相比,柠檬酸钾·柠檬酸钠水合物配合制剂进一步抑制慢性肾病的发展。
另外,将测定尿中的β2-微球蛋白量和血清中的半胱氨酸蛋白酶抑制剂c量而得的结果示于以下。
[表7-1]
[表7-1]尿中β2-微球蛋白(μg/l)
平均值+/-sd
ap=0.0338.cp=0.0220vs对照以及bp=0.0077,dp=0.0156vs碳酸氢盐(mann-whitney)
ep=0.0110以以及fp=0.0063vs0周(wilcoxon)
(在0周的组间没有显著差异)
[表7-2]
[表7-2]尿中β2-微球蛋白(从0周起的△μg/l变换)
平均值+/-sd
ap=0.009515,dp=0.0415,ep=0.0295vs碳酸氢盐以及bp=0.0002.cp=0.0437vs对照(mann-whitney)
(在0周的组间没有显著差异)
[表8]
[表8]血浆中的半胱氨酸蛋白酶抑制剂c(mg/l)
平均值+/-sd
组间没有显著差异(mann-whitney)
ap=0.0303vs0周(wilcoxon)
(在0周的组间没有显著差异)
血浆中的半胱氨酸蛋白酶抑制剂c的浓度在a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)、b组(碳酸氢盐:碳酸氢钠制剂给予组)和c组(对照:对照组)间没有差异,没有确认到基于柠檬酸钾·柠檬酸钠水合物配合制剂给予或碳酸氢钠制剂给予的对肾小球的功能的影响(表8)。
另一方面,关于尿中的β2-微球蛋白浓度,a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)与c组(对照:对照组)相比,尿中的β2-微球蛋白浓度为低值,与b组(碳酸氢盐:碳酸氢钠制剂给予组)相比,a组(柠檬酸钾·柠檬酸钠水合物配合制剂给予组)的尿中的β2-微球蛋白浓度也为低值。b组(碳酸氢盐:碳酸氢钠制剂给予组)与c组(对照:对照组)相比,尿中的β2-微球蛋白浓度为高值。确认到通过给予柠檬酸钾·柠檬酸钠水合物配合制剂,伴随病期发展的尿中的β2-微球蛋白浓度增加得到抑制,与给予前相比,尿中的β2-微球蛋白浓度没有变化。
根据这些结果,表示通过柠檬酸钾·柠檬酸钠水合物配合制剂给予,伴随病期发展的肾小管损伤(近端肾小管损伤)得到抑制。另外,显示伴随病期发展的肾小管损伤(近端肾小管损伤)没有因给予碳酸氢钠制剂而得到抑制,反而加重。从给予6周后确认到这些效果。
另外,基于柠檬酸钾·柠檬酸钠水合物配合制剂给予的尿中的尿毒症物质浓度增加效果和血中的尿毒症物质浓度降低效果与基于柠檬酸钾·柠檬酸钠水合物配合制剂给予的尿中的β2-微球蛋白浓度增加抑制效果没有确认到相关。表明基于柠檬酸钾·柠檬酸钠水合物配合制剂给予的向尿中的尿毒症物质排泄促进效果不仅是由于抑制肾小球和近端肾小管的损伤。
对于c组(对照:对照组)、a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)、b组(碳酸氢盐:碳酸氢钠制剂给予组)和全部患者(a组、b组和c组的全部患者),分别使用pearson检验解析试验开始6、12和24周后(6w、12w和24w)的晨尿中的硫酸吲哚酚(is)浓度与血浆的硫酸吲哚酚(is)浓度的相关性。将其结果示于图1~图4。
对于硫酸吲哚酚,柠檬酸钾·柠檬酸钠水合物配合制剂给予组与对照组相比,在血浆中浓度与尿中浓度确认到高相关性,与碳酸氢钠制剂给予组相比,也确认到高相关性(参照图1~3的r值)。根据图1~4,表明通过给予柠檬酸钾·柠檬酸钠水合物配合制剂,依赖于血中的硫酸吲哚酚浓度使硫酸吲哚酚向尿中排泄。表明通过依赖于血中的硫酸吲哚酚浓度使硫酸吲哚酚向尿中排泄,硫酸吲哚酚的血中浓度的增加得到抑制,血中硫酸吲哚酚浓度与尿中的硫酸吲哚酚浓度之比成为一定的范围。
对于c组(对照:对照组)、a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)、b组(碳酸氢盐:碳酸氢钠制剂给予组)和全部患者(a组、b组和c组的全部患者),分别使用pearson检验解析试验开始6、12和24周后(6w、12w和24w)的晨尿中的硫酸对甲酚(pcs)浓度与血浆的硫酸对甲酚(pcs)浓度的相关性。将其结果示于图5~图8。
对于硫酸对甲酚,在对照组、柠檬酸钾·柠檬酸钠水合物配合制剂给予组和碳酸氢钠制剂给予组中,在血浆中浓度与尿中浓度确认到相关性,与柠檬酸钾·柠檬酸钠水合物配合制剂给予组相比,在碳酸氢钠制剂给予组中确认到更高的相关性(参照图5~7的r值)。根据图5~8,表明通过给予碳酸氢钠制剂给予或柠檬酸钾·柠檬酸钠水合物配合制剂,依赖于血中的硫酸对甲酚浓度使硫酸对甲酚向尿中排泄。表明通过依赖于血中的硫酸对甲酚浓度使硫酸对甲酚向尿中排泄,硫酸对甲酚的血中浓度的增加得到抑制,血中硫酸对甲酚浓度与尿中的硫酸对甲酚浓度之比成为一定的范围。
对于c组(对照:对照组)、a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)、b组(碳酸氢盐:碳酸氢钠制剂给予组)和全部患者(a组、b组和c组的全部患者),分别使用pearson检验解析试验开始6、12和24周后(6w、12w和24w)的晨尿中的马尿酸(ha)浓度与血浆的马尿酸(ha)浓度的相关性。将其结果示于图9~图12。
对于马尿酸,在对照组、柠檬酸钾·柠檬酸钠水合物配合制剂给予组和碳酸氢钠制剂给予组中,在血浆中浓度与尿中浓度没有确认到高相关性。
对于c组(对照:对照组)、a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)、b组(碳酸氢盐:碳酸氢钠制剂给予组)和全部患者(a组、b组和c组的全部患者),分别使用pearson检验解析试验开始6、12和24周后(6w、12w和24w)的晨尿中的精氨基琥珀酸(asa)浓度与血浆的精氨基琥珀酸(asa)浓度的相关性。将其结果示于图13~图16。
对于精氨基琥珀酸,在对照组、柠檬酸钾·柠檬酸钠水合物配合制剂给予组和碳酸氢钠制剂给予组中,在血浆中浓度与尿中浓度没有确认到高相关性。
对于c组(对照:对照组)、a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)、b组(碳酸氢盐:碳酸氢钠制剂给予组)和全部患者(a组、b组和c组的全部患者),分别使用pearson检验解析试验开始6、12和24周后(6w、12w和24w)的晨尿中的苯基乙酰基l谷氨酰胺(pag)浓度与血浆的苯基乙酰基l谷氨酰胺(pag)浓度的相关性。将其结果示于图17~图20。
对于苯基乙酰基l谷氨酰胺,在对照组、柠檬酸钾·柠檬酸钠水合物配合制剂给予组和碳酸氢钠制剂给予组中,在血浆中浓度与尿中浓度确认到相关性,与柠檬酸钾·柠檬酸钠水合物配合制剂给予组相比,在碳酸氢钠制剂给予组中确认到更高的相关性(参照图17~19的r值)。根据图17~20,表明通过给予碳酸氢钠制剂或给予柠檬酸钾·柠檬酸钠水合物配合制剂,依赖于血中的苯基乙酰基l谷氨酰胺浓度使苯基乙酰基l谷氨酰胺向尿中排泄。表明通过依赖于血中的苯基乙酰基l谷氨酰胺浓度使苯基乙酰基l谷氨酰胺向尿中排泄,苯基乙酰基l谷氨酰胺的血中浓度的增加得到抑制,血中苯基乙酰基l谷氨酰胺浓度与尿中的苯基乙酰基l谷氨酰胺浓度之比成为一定的范围。
对于c组(对照:对照组)、a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)和b组(碳酸氢盐:碳酸氢钠制剂给予组),分别使用pearson检验解析试验开始6、12和24周后(6w、12w和24w)的、硫酸吲哚酚(is)、硫酸对甲酚(pcs)、马尿酸(ha)、精氨基琥珀酸(asa)和苯基乙酰基l谷氨酰胺(pag)的晨尿浓度的相关性。将其结果示于表9。表中“对照”表示对照组,“柠檬酸盐”表示柠檬酸钾·柠檬酸钠水合物配合制剂给予组,“碳酸氢盐”表示碳酸氢钠制剂给予组。
其结果,在柠檬酸钾·柠檬酸钠水合物配合制剂给予组中,在硫酸吲哚酚与苯基乙酰基l谷氨酰胺、硫酸对甲酚与苯基乙酰基l谷氨酰胺、精氨基琥珀酸与苯基乙酰基l谷氨酰胺确认到高相关性。在碳酸氢钠制剂给予组中,在硫酸吲哚酚与精氨基琥珀酸、硫酸吲哚酚与苯基乙酰基l谷氨酰胺、硫酸对甲酚与精氨基琥珀酸、硫酸对甲酚与苯基乙酰基l谷氨酰胺、精氨基琥珀酸与苯基乙酰基l谷氨酰胺确认到高相关性。表明柠檬酸钾·柠檬酸钠水合物配合制剂有可能通过同样的机制提高硫酸吲哚酚、苯基乙酰基l谷氨酰胺、硫酸对甲酚和精氨基琥珀酸的尿中浓度。另外,表明碳酸氢钠制剂有可能通过同样的机制提高硫酸吲哚酚、苯基乙酰基l谷氨酰胺、硫酸对甲酚和精氨基琥珀酸的尿中浓度。
[表9]
[表9]5种尿毒症物质的相对于尿中浓度的彼此的关联性和影响
上段:相关系数(r)、下段:显著水准(p)、pearson。r>0.7时附下划线。3组比较(6-24周、n=45-48)
对于c组(对照:对照组)、a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)和b组(碳酸氢盐:碳酸氢钠制剂给予组),分别使用pearson检验解析试验开始6、12和24周后(6w、12w和24w)的硫酸吲哚酚(is)、硫酸对甲酚(pcs)、马尿酸(ha)、精氨基琥珀酸(asa)和苯基乙酰基l谷氨酰胺(pag)的血浆浓度的相关性。将其结果示于表10。表中“对照”表示对照组,“柠檬酸盐”表示柠檬酸钾·柠檬酸钠水合物配合制剂给予组,“碳酸氢盐”表示碳酸氢钠制剂给予组。
其结果,在柠檬酸钾·柠檬酸钠水合物配合制剂给予组中,在硫酸吲哚酚与硫酸对甲酚、硫酸吲哚酚与苯基乙酰基l谷氨酰胺、硫酸对甲酚与苯基乙酰基l谷氨酰胺确认到高相关性。在碳酸氢钠制剂给予组中,在硫酸吲哚酚与硫酸对甲酚确认到高相关性。表明柠檬酸钾·柠檬酸钠水合物配合制剂有可能通过同样的机制使硫酸吲哚酚、苯基乙酰基l谷氨酰胺和硫酸对甲酚的血中浓度降低。另外,表明碳酸氢钠制剂有可能通过同样的机制使硫酸对甲酚和苯基乙酰基l谷氨酰胺的血中浓度降低。表明柠檬酸钾·柠檬酸钠水合物配合制剂与碳酸氢钠制剂使尿毒症物质的血中浓度降低的机制不同。
[表10]
[表10]5种尿毒症物质的相对于血中浓度的彼此的关联性和影响
上段:相关系数(r)、下段:显著水准(p)、pearson。r>0.7时附下划线。3组比较(6-24周、n=45-48)
对于c组(对照:对照组)、a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)和b组(碳酸氢盐:碳酸氢钠制剂给予组)分别解析试验开始前(0w)以及试验开始6、12和24周后(6w、12w和24w)的晨尿的尿比重。将其结果示于表11-0-1。另外,将从试验开始前起试验开始6、12和24周后的各尿比重的变化量作为相对于试验开始前的尿比重的百分比相对值以及与试验开始前的尿比重的差分分别示于下述表11-0-2和表11-0-3。应予说明,尿比重使用尿比重计(pal-09s,atago株式会社,东京,日本)测定。
[表11-0-1]
[表11-0-1]尿比重
平均值+/-sd
组间没有显著差异(mann-whitney)
ap=0.0464vs0周(wilcoxon)
组间没有显著差异(kruskal-wallis&dunn)
(在0周的组间没有显著差异)
[表11-0-2]
[表11-0-2]尿比重(百分比相对值vs0周)
平均值+/-sd
ap=0.0023,bp=0.0577,cp=0.0734,dp=0.0289以及ep=0.0715vs柠檬酸盐(mann-whitney)
ap=0.0100,bp=0.0652(kruskal-wallis)以及cp=0.0084,dp=0.0941vs柠檬酸盐(dunn)
[表11-0-3]
[表11-0-3]尿比重(△实测值vs0周)
平均值+/-sd
ap=0.0023,bp=0.0592,cp=0.0704,dp=0.0289以及ep=0.0746vs柠檬酸盐(mann-whitney)
ap=0.0102,bp=0.0668(kruskal-wallis)以及cp=0.0085,dp=0.0956vs柠檬酸盐(dunn)
上述的结果,与c组(对照:对照组)相比,a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)和b组(碳酸氢盐:碳酸氢钠制剂给予组)在试验开始6、12和24周后确认到维持尿比重的值或尿比重的值增加的趋势。另外,与b组(碳酸氢盐:碳酸氢钠制剂给予组)相比,a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)确认到进一步维持上述尿比重或尿比重增加的趋势。
尿比重的维持或增加可理解为基于肾功能的维持或改善。因此,根据以上的内容,表明通过不仅对阶段g3b而且对阶段g2的慢性肾病患者给予碱化剂,能够抑制慢性肾病的发展,而且与碳酸氢钠制剂相比,柠檬酸钾·柠檬酸钠水合物配合制剂进一步抑制慢性肾病的发展。
对c组(对照:对照组)、a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)和b组(碳酸氢盐:碳酸氢钠制剂给予组)分别解析将试验开始前(0w)以及试验开始6、12和24周后(6w、12w和24w)的晨尿中的尿毒症物质、即硫酸吲哚酚(is)、硫酸对甲酚(pcs)、苯基乙酰基l谷氨酰胺(pag)、马尿酸(ha)和精氨基琥珀酸(asa)的浓度分别用试验开始前(0w)以及试验开始6、12和24周后(6w、12w和24w)的晨尿的尿比重并通过以下的公式校正而得的值。参照青木哲雄他、医学检查、1995年44卷1号、79~83页。应予说明,将尿比重1.022作为基准值进行换算。
比重校正值(单位/1.022·ug)=实测值×(1.022-1.000)/(比重值-1.000)
将结果示于表11-1-1、表11-2-1、表11-3-1、表11-4-1和表11-5-1。另外,将从试验开始前起试验开始6、12和24周后的晨尿中的上述尿毒症物质的浓度分别用尿比重进行校正,将所得的值的变化量以相对于试验开始前的上述校正值的百分比相对值以及与试验开始前的上述校正值的差分的形式分别示于下述表11-1-2、表11-1-3、表11-2-2、表11-2-3、表11-3-2、表11-3-3、表11-4-2、表11-4-3、表11-5-2和表11-5-3。
[表11-1-1]
[表11-1-1]尿中is(μg·ml-1/1.022·ug)
平均值+/-sd
ap=0.0849,bp=0.0559,cp=0.0065,dp=0.0729,ep=0.0266以及fp=0.0849vs碳酸氢盐(mann-whitney)
ap=0.0052以及bp=0.0730vs0周(wilcoxon)
ap=0.0844,bp=0.0301(kruskal-wallis)以及ep=0.0909,dp=0.0385vs柠檬酸盐(dunn)
(在0周的组间有趋势差异)
[表11-1-2]
[表11-1-2]尿中is(μg·ml-1/1.022·ug,百分比相对值vs0周)
平均值+/-sd
组间没有显著差异(mann-whitney)
组间没有显著差异(kruskal-wallis&dunn)
[表11-1-3]
[表11-1-3]尿中is(μg·ml-1/1.022·ug,△实测值vs0周)
平均值+/-sd
ap=0.0251,bp=0.0135以及cp=0.0651vs碱酸氢盐(mann-whitney)
ap=0.0648,bp=0.0368(kruskal-wallis)以及cp=0.0581,dp=0.0429vs柠檬酸盐(dunn)
[表11-2-1]
[表11-2-1]尿中pcs(μg·ml-1/1.022·ug)
平均值+/-sd
组间没有显著差异(mann-whitney)
ap=0.0507vs0周(wilcoxon)
组间没有显著差异(kruskal-wallis&dunn)
(0周的组间没有显著差异)
[表11-2-2]
[表11-2-2]尿中pcs(μg·ml-1/1.022·ug,百分比相对值vs0周)
平均值+/-sd
ap=0.0095,bp=0.0125,cp=0.0149,dp=0.0240vs柠檬酸盐(mann-whitney)
ap=0.0129,bp=0.0449,cp=0.0869(kruskal-wallis)以及dp=0.0250,ep=0.0439,fp=0.0393,
gp=0.0849vs柠檬酸盐(dunn)
[表11-2-3]
[表11-2-3]尿中pcs(μg·ml-1/1.022·ug,δ实测值vs0周)
平均值+/-sd
ap=0.0226,bp=0.0007,cp=0.0214,dp=0.0287以及ep=0.0465vs柠檬酸盐(mann-whitney)
ap=0.0025,bp=0.0661,cp=0.0795(kruskal-wallis)以及dp=0.0020,ap=0.0736,fp=0.0863,
gp=0.0849vs柠檬酸盐(dunn)
[表11-3-1]
[表11-3-1]尿中pag(μg·ml-1/1.022·ug)
平均值+/-sd
组间没有显著差异(mann-whitney)
ap=0.0302以及bp=0.0110vs0周(wilcoxon)
组间没有显著差异(kruskal-wallis&dunn)
(在0周的组间没有显著差异)
[表11-3-2]
[表11-3-2]尿中pag(μg·ml-1/1.022·ug,百分比相对值vs0周)
平均值+/-sd
ap=0.0828以及bp=0.0799vs碳酸氢盐(mann-whitney)
组间没有显著差异(kruskal-wallis&dunn)
[表11-3-3]
[表11-3-3]尿中pag(μg·ml-1/1.022·ug,△实测值vs0周)
平均值+/-sd
ap=0.0078,cp=0.0385,dp=0.0491vs碳酸氢盐以及bp=0.0712vs对照(mann-whitney)
ap=0.0248,bp=0.0613(kruskal-wallis)以及cp=0.0197vs碳酸氢盐(dunn)
[表11-4-1]
[表11-4-1]尿中ha(μg·ml-1/1.022·ug)
平均值+/-sd
组间没有显著差异(mann-whitney)
没有显著差异vs0周(wilcoxon)
组间没有显著差异(kruskal-wallis&dunn)
(在0周的组间没有显著差异)
[表11-4-2]
[表11-4-2]尿中ha(μg·ml-1/1.022·ug,百分比相对值vs0周)
平均值+/-sd
组间没有显著差异(mann-whitney)
组间没有显著差异(kruskal-wallis&dunn)
[表11-4-3]
[表11-4-3]尿中ha(μg·ml-1/1.022·ug,△实测值vs0周)
平均值+/-sd
组间没有显著差异(mann-whitney)
组间没有显著差异(kruskal-wallis&dunn)
[表11-5-1]
[表11-5-1]尿中asa(μg·ml-1/1.022·ug)
平均值+/-sd
组间没有显著差异(mann-whitney)
ap=0.0413vs0周(wilcoxon)
组间没有显著差异(kruskal-wallis&dunn)
(在0周的组间没有显著差异)
[表11-5-2]
[表11-5-2]尿中asa(μg·ml-1/1.022·ug,百分比相对值vs0周)
平均值+/-sd
组间没有显著差异(mann-whitney)
组间没有显著差异(kruskal-wallis&dunn)
[表11-5-3]
[表11-5-3]尿中asa(μg·ml-1/1.022·ug,△实测值vs0周)
平均值+/-sd
组间没有显著差异(mann-whitney)
组间没有显著差异(kruskal-wallis&dunn)
上述的结果,在硫酸吲哚酚(is)、硫酸对甲酚(pcs)和苯基乙酰基l谷氨酰胺(pag)时,给予了柠檬酸钾·柠檬酸钠水合物配合制剂(柠檬酸盐)的组与对照组和给予了碳酸氢钠制剂(碳酸氢盐)的组相比,尿中的尿毒症物质浓度(向尿中的排泄)显著增加。对于马尿酸(ha)和精氨基琥珀酸(asa),给予了柠檬酸钾·柠檬酸钠水合物配合制剂(柠檬酸盐)的组与对照组和给予了碳酸氢钠制剂(碳酸氢盐)的组相比,尿中的尿毒症物质浓度(向尿中的排泄)也增加。另外,通过给予柠檬酸钾·柠檬酸钠水合物配合制剂(柠檬酸盐),与试验开始前(0w)相比,尿中的硫酸吲哚酚(is)、硫酸对甲酚(pcs)和苯基乙酰基l谷氨酰胺(pag)的浓度(向尿中的排泄)增加。
对c组(对照:对照组)、a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)和b组(碳酸氢盐:碳酸氢钠制剂给予组)分别解析试验开始前(0w)以及试验开始6、12和24周后(6w、12w和24w)的晨尿的渗透压。将其结果示于表12-0-1。另外,将从试验开始前起试验开始6、12和24周后的各晨尿的渗透压的变化量以相对于试验开始前的晨尿的渗透压的百分比相对值以及与试验开始前的晨尿的渗透压的差分的形式分别示于下述表12-0-2和表12-0-3。应予说明,使用冰点下降法测定渗透压。
[表12-0-1]
[表12-0-1]尿渗透压(mosm/kg)
平均值+/-sd
组间没有显著差异(mann-whitney)
ap=0.0616vs0周(wilcoxon)
组间没有显著差异(kruskal-wallis&dunn)
(在0周的组间没有显著差异)
[表12-0-2]
[表12-0-2]尿渗透压(百分比相对值vs0周)
平均值+/-sd
ap=0.0123,bp=0.0997以cp=0.0436vs柠檬酸盐(mann-whitney)
ap=0.0382(kruskal-wallis)以及bp=0.0358vs柠檬酸盐(dunn)
[表12-0-3]
[表12-0-3]尿渗透压(δmosm/kgvs0周)
平均值+/-sd
ap=0.0179以及bp=0.0375vs柠檬酸盐(mann-whitney)
ap=0.0597(kruskal-wallis)以及bp=0.0618vs柠檬酸盐(dunn)
上述的结果,与c组(对照:对照组)相比,在a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)和b组(碳酸氢盐:碳酸氢钠制剂给予组)中,在试验开始6、12和24周后,确认到维持晨尿的渗透压的值或渗透压的值增加的趋势。另外,确认到与b组(碳酸氢盐:碳酸氢钠制剂给予组)相比,a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)进一步维持上述晨尿的渗透压或上述晨尿的渗透压增加的趋势。
晨尿的渗透压的维持或增加可以理解为基于肾功能的维持或改善。因此,根据以上内容,表明通过不仅对阶段g3b而且对阶段g2的慢性肾病患者给予碱化剂,能够抑制慢性肾病的发展,而且,与碳酸氢钠制剂相比,柠檬酸钾·柠檬酸钠水合物配合制剂进一步抑制慢性肾病的发展。
对c组(对照:对照组)、a组(柠檬酸盐:柠檬酸钾·柠檬酸钠水合物配合制剂给予组)和b组(碳酸氢盐:碳酸氢钠制剂给予组)分别解析将试验开始前(0w)以及试验开始6、12和24周后(6w、12w和24w)的晨尿中的尿毒症物质、即硫酸吲哚酚(is)、硫酸对甲酚(pcs)、苯基乙酰基l谷氨酰胺(pag)、马尿酸(ha)和精氨基琥珀酸(asa)的浓度分别用试验开始前(0w)以及试验开始6、12和24周后(6w、12w和24w)的晨尿的渗透压并通过以下的公式校正而得的值。参照青木哲雄他、医学检查、1995年44卷1号、79~83页。应予说明,将尿渗透压770mosm/kg作为基准值进行换算。
渗透压校正值(单位/500mosm·p)=实测值×500/渗透压值
将结果示于表12-1-1、表12-2-1、表12-3-1、表12-4-1和表12-5-1。另外,将从试验开始前起试验开始6、12和24周后的晨尿中的上述尿毒症物质的浓度分别用晨尿的渗透压校正,将所得的值的变化量以相对于试验开始前的上述校正值的百分比相对值以及与试验开始前的上述校正值的差分的形式分别示于下述表12-1-2、表12-1-3、表12-2-2、表12-2-3、表12-3-2、表12-3-3、表12-4-2、表12-4-3、表12-5-2、和表12-5-3。
[表12-1-1]
[表12-1-1]尿中is(μg.ml-1/770mosm·p)
平均值+/-sd
ap=0.0424,bp=0.0060.cp=0.0939,dp=0.0214以及ep=0.0650vs碳酸氢盐(mann-whitney)
ap=0.0092以及bp=0.0413vs0周(wililcoxon)
ap=0.0830,bp=0.0266(kruskal-wallis)以及cp=0.0880,dp=0.0416vs碳酸氢盐(dunn)
(在0周的组间有显著差异)
[表12-1-2]
[表12-1-2]尿中is(μg·ml-1/770mosm·p,百分比相对值vs0周)
平均值+/-sd
组间没有显著差异(mann-whitney)
组间没有显著差异(kruskal-wallis&dunn)
[表12-1-3]
[表12-1-3]尿中is(μg·ml-1/770mosm·p,δ实测值vs0周)
平均值+/-sd
ap=0.0169vs碳酸氢盐(mann·whitney)
ap=0.0492(kruskal-wallis)以及bp=0.0445vs碳酸氢盐(dunn)
[表12-2-1]
[表12-2-1]尿中pcs(μg·ml-1/770mosm·p)
平均值+/-sd
组间没有显著差异(mann-whitney)
ap=0.0637以及bp=0.0507vs0周(wilcoxon)
组间没有显著差异(kruskal-wallis&dunn)
(在0周的组间没有显著差异)
[表12-2-2]
[表12-2-2]尿中pcs(μg·ml-1/770mosm·p,百分比相对值vs0周)
平均值+/-sd
ap=0.0054,bp=0.0127,cp=0.0085,dp=0.0259vs柠檬酸盐以及ep=0.0704vs对照(mann-whitney)
ap=0.0085,bp=0.0266(kruskal-wallis)以及cp=0.0120,dp=0.0524,ep=0.0241vs柠檬酸盐(dunn)
[表12-2-3]
[表12-2-3]尿中pcs(μg·ml-1/770mosm·p,δ实测值vs0周)
平均值+/-sd
ap=0.0117,bp=0.0047,cp=0.0093,dp=0.0465vs柠檬酸盐(mann-whitney)
ap=0.0080,bp=0.0436(kruskal-wallis)以及cp=0.0407,dp=0.0130,ep=0.0370vs柠檬酸盐(dunn)
[表12-3-1]
[表12-3-1]尿中pag(μg·ml-1/770mosm·p)
平均值+/-sd
组间没有显著差异(mann-whitney)
ap=0.0256以及op=0.0092vs0周(wilcoxon)
组间没有显著差异(kruskal-wallis&dunn)
(在0周的组间没有显著差异)
[表12-3-2]
[表12-3-2]尿中pag(μg·ml-1/770mosm·p,百分比相对值vs0周)
平均值+/-sd
ap=0.0764以及bp=0.0912vs碳酸氢盐(mann-whitney)
组间没有显著差异(kruskal-wallis&dunn)
[表12-3-3]
[表12-3-3]尿中pag(μg·ml-1/770mosm·p,△实测值vs0周)
平均值+/-sd
ap=0.0912,bp=0.0386,cp=0.0712,dp=0.0510vs碳酸氢盐以及ep=0.0491vs对照(mann-whitney)
ap=0.0794,bp=0.0727(kruskaal-wallis)以及cp=0.0903vs碳酸氢盐(dunn)
[表12-4-1]
[表12-4-1]尿中ha(μg·ml-1/770mosm·p)
平均值+/-sd
组间没有显著差异(mann-whitney)
没有显著差异vs0周(wilcoxon)
组间没有显著差异(kruskal-wallis&dunn)
(在0周的组间没有显著差异)
[表12-4-2]
[表12-4-2]尿中ha(μg·ml-1/770mosm·p,百分比相对值vs0周)
平均值+/-sd
组间没有显著差异(mann-whitney)
组间没有显著差异(kruskal-wsllis&dunn)
[表12-4-3]
[表12-4-3]尿中ha(μg·ml-1/770mosm·p,△实测值vs0周)
平均值+/-sd
组间没有显著差异(mann-whitney)
组间没有显著差异(kruskal-wallis&dunn)
[表12-5-1]
[表12-5-1]尿中asa(μg·ml-1/770mosm·p)
平均值+/-sd
组间没有显著差异(mann-whitney)
ap=0.0302vs0周(wilcoxon)
组间没有显著差异(kruskal-wallis&dunn)
(在0周的组间没有显著差异)
[表12-5-2]
[表12-5-2]尿中asa(μg·ml-1/770mosm·p,百分比相对值vs0周)
平均值+/-sd
ap=0.0716vs对照(mann-whitney)
组间没有显著差异(kruskal-wallis&dunn)
[表12-5-3]
[表12-5-3]尿中asa(μg·ml-1/770mosm·p,△实测值vs0周)
平均值+/-sd
ap=0.0364vs对照(mann·whitney)
ap=0.0935(kruskal-wallis)以及bp=0.0962vs对照(dunn)
上述的结果,在硫酸对甲酚(pcs)和苯基乙酰基l谷氨酰胺(pag)时,给予了柠檬酸钾·柠檬酸钠水合物配合制剂(柠檬酸盐)的组与对照组和给予了碳酸氢钠制剂(碳酸氢盐)的组相比,尿中的尿毒症物质浓度(向尿中的排泄)显著增加。对于硫酸吲哚酚(is)、马尿酸(ha)和精氨基琥珀酸(asa),给予了柠檬酸钾·柠檬酸钠水合物配合制剂(柠檬酸盐)的组与对照组和给予了碳酸氢钠制剂(碳酸氢盐)的组相比,尿中的尿毒症物质浓度(向尿中的排泄)也增加。另外,通过给予柠檬酸钾·柠檬酸钠水合物配合制剂(柠檬酸盐),与试验开始前(0w)相比,尿中的硫酸吲哚酚(is)、硫酸对甲酚(pcs)和苯基乙酰基l谷氨酰胺(pag)的浓度(向尿中的排泄)增加。
产业上的可利用性
通过本发明所提供的药物组合物等,在哺乳动物中使尿毒症物质排出到体外。通过本发明所提供的方法,能够初步判断尿毒症物质是否被排出到体外和/或是否能够抑制慢性肾病的发展。
- 还没有人留言评论。精彩留言会获得点赞!