以叶酸及小分子多肽修饰的N-琥珀酰壳聚糖为载体包载紫杉醇的纳米粒及其制备方法与流程
本发明涉及一种以叶酸及小分子多肽修饰的n-琥珀酰壳聚糖为载体包载紫杉醇的纳米粒及其制备方法,属于自组装纳米材料技术领域。
背景技术:
肺癌是常见的恶性肿瘤之一,非小细胞肺癌(non-smallcelllungcancer,nsclc)占肺癌的3/4以上,由于早期肺癌缺乏明显的症状,85%以上确诊时已是中晚期从而失去手术治疗的机会。传统化疗由于化疗中使用的抗癌药物对肿瘤细胞缺少有效的选择性,对正常组织的毒副作用以及肿瘤细胞的耐药性限制了抗癌的疗效,使nsclc难以治愈。为了有效的治疗nsclc,包载抗肿瘤药物的纳米肿瘤靶向传递系统的研究已经成为努力实现的热点。
n-琥珀酰壳聚糖(n-succinyl-chitosans,suc)是由壳聚糖和丁二酸酐反应合成的一种羧基酰化的水溶性壳聚糖衍生物。n-琥珀酰壳聚糖是一种两亲聚合物,具有较好的生物相溶性,较低的毒性、较长的体内半期及肿瘤亲和性,能够在水溶液中自发地形成胶束。叶酸受体(folatereceptor,fr)是一个分子量为38kda的糖基磷脂酰肌醇锚式糖蛋白,是癌症治疗中研究最多的靶向因子之一。与正常组织相比,叶酸受体在许多癌细胞上(肺癌、卵巢癌、脑癌、肾癌和乳腺癌)有高度的表达。穿膜肽(cell-penetratingpeptides,cpps)是近年来发现的一类可以携带多种物质如亲水性蛋白质、核酸和颗粒性物质等效应分子穿过细胞膜结构,进入胞浆发挥作用的多肽。这种细胞内的快速传输不受细胞类型的限制,且对细胞膜没有破坏性。hiv-itat蛋白来源于人免疫缺陷病毒(humanimmunodeficiencyvirus,hiv-i)的转录活化因子(trans-activatingtranscriptionalactivator,tat),是目前研究最多的穿膜肽分子。目前尚未见有以叶酸及小分子多肽tat修饰n-琥珀酰壳聚糖所得的tat-suc-fa纳米粒为载体,再包载抗肿瘤天然药物药紫杉醇(paclitaxel)构建紫杉醇/tat-suc-fa自组装纳米传递系统的相关报道。
技术实现要素:
本发明要解决的技术问题是提供一种以叶酸及小分子多肽修饰的n-琥珀酰壳聚糖为载体包载紫杉醇的纳米粒及其制备方法。本发明所述方法制得的紫杉醇/tat-suc-fa纳米粒粒径分布较窄,呈正太分布,药物包封率高,且所得纳米粒能特异性地被靶向细胞识别并结合,快速定位到细胞核,从而提高紫杉醇生物利用度,毒副作用低。
为解决上述技术问题,本发明采用以下技术方案:
以叶酸及小分子多肽修饰的n-琥珀酰壳聚糖为载体包载紫杉醇的纳米粒的制备方法,包括以下步骤:
1)以叶酸及小分子多肽tat修饰n-琥珀酰壳聚糖(suc),得到载体tat-suc-fa纳米粒;
2)取tat-suc-fa纳米粒溶于乙酸-乙酸钠缓冲溶液中,配制得到浓度为3-6mg/ml的纳米聚合物溶液;
3)取紫杉醇溶于水中,配制得到浓度为2-4mg/ml的紫杉醇水溶液;
4)取步骤2)所得纳米聚合物溶液与步骤3)所得紫杉醇水溶液混合,控制所得物料中tat-suc-fa纳米粒和紫杉醇的质量之比为1.5-2.0:1,所得物料于超声和/或搅拌条件下进行自组装反应,过滤,得到紫杉醇/tat-suc-fa纳米粒。
本发明所述技术方案中,所述的小分子多肽tat的氨基酸序列如seqidno:1所示。
上述制备方法的步骤1)中,可采用现有常规方法或参考现有文献以制备得到载体tat-suc-fa纳米粒,优选按以下方法进行制备:
①取1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(edc)和叶酸(folicacid,fa)置于二甲基亚砜(dmso)中,控制体系中叶酸的浓度为30-40mmol/l,所述1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐的量为叶酸物质的量的2.7-3.0倍,待完全溶解,得到溶液a;
②取n-琥珀酰壳聚糖溶于ph=4.5-5.0的乙酸-乙酸钠缓冲溶液中,控制n-琥珀酰壳聚糖在体系中的浓度为1-2%(w/v),得到溶液b;
③向溶液a中加入溶液b,混合均匀后于暗室中在不加热条件下搅拌反应,反应完全后调节体系的ph=8.5-9.0,得到反应物料c;其中,溶液b的加入量为控制所得物料中n-琥珀酰壳聚糖的量为叶酸物质的量的0.15-0.25倍;
④将反应物料c依次用ph=7.4的乙酸-乙酸钠缓冲溶液和去离子水透析,之后采用冻干法分离,得到叶酸修饰的n-琥珀酰壳聚糖;
⑤取1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐和4-二甲氨基吡啶(dmap)溶解于n,n-二甲基甲酰胺(dmf)中,控制1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐在体系中的浓度为12-16mmol/l,4-二甲氨基吡啶在体系中的浓度为1.0-1.2mmol/l,得到溶液d;
⑥在溶液d中加入等摩尔比的小分子多肽tat和步骤④制得的叶酸修饰的n-琥珀酰壳聚糖,在不加热条件下进行反应,所得反应混合物用去离子水透析,得到载体tat-suc-fa纳米粒。
在上述载体tat-suc-fa纳米粒的制备方法中,步骤③中所述反应的时间优选为16-24h,优选用氢氧化钠水溶液调节体系的ph值,所述氢氧化钠水溶液的浓度为1-4%(w/w);步骤④中用ph=7.4的乙酸-乙酸钠缓冲溶液和去离子水透析的目的是为了纯化,用ph=7.4的乙酸-乙酸钠缓冲溶液透析和用去离子水透析的时间均优选为3天甚至更长的时间;步骤⑥中反应的时间优选为大于或等于1h,反应所得反应混合物用去离子水透析的时间优选为2天甚至更长的时间。
上述制备紫杉醇/tat-suc-fa纳米粒方法的步骤2)中,所述乙酸-乙酸钠缓冲溶液的ph=5.0-6.0,优选为ph=5.5。
上述制备紫杉醇/tat-suc-fa纳米粒方法的步骤4)中,所述自组装反应的时间通常≥30min,优选为30-60min;过滤采用微滤膜过滤,所述微滤膜的孔径优选为0.2-0.25μm。
本发明还包括由上述方法制备得到的紫杉醇/tat-suc-fa纳米粒。采用本发明所述方法制得的紫杉醇/tat-suc-fa纳米粒外观呈圆形或类圆形,纳米粒粒径分布较窄,呈正太分布,平均粒径61±18.5nm,聚合物分散系数(pdi)<0.09。所得紫杉醇/tat-suc-fa纳米粒带正电,zeta电位46±0.3mv。药物包封率(%)90.2±5.1,载药量(%)25.2±4.2。
与现有技术相比,本发明所述方法简单易控,制得的紫杉醇/tat-suc-fa纳米粒粒径分布较窄,呈正太分布,药物包封率高,且所得纳米粒能特异性地被靶向细胞识别并结合,快速定位到细胞核,从而提高紫杉醇生物利用度,毒副作用低。
附图说明
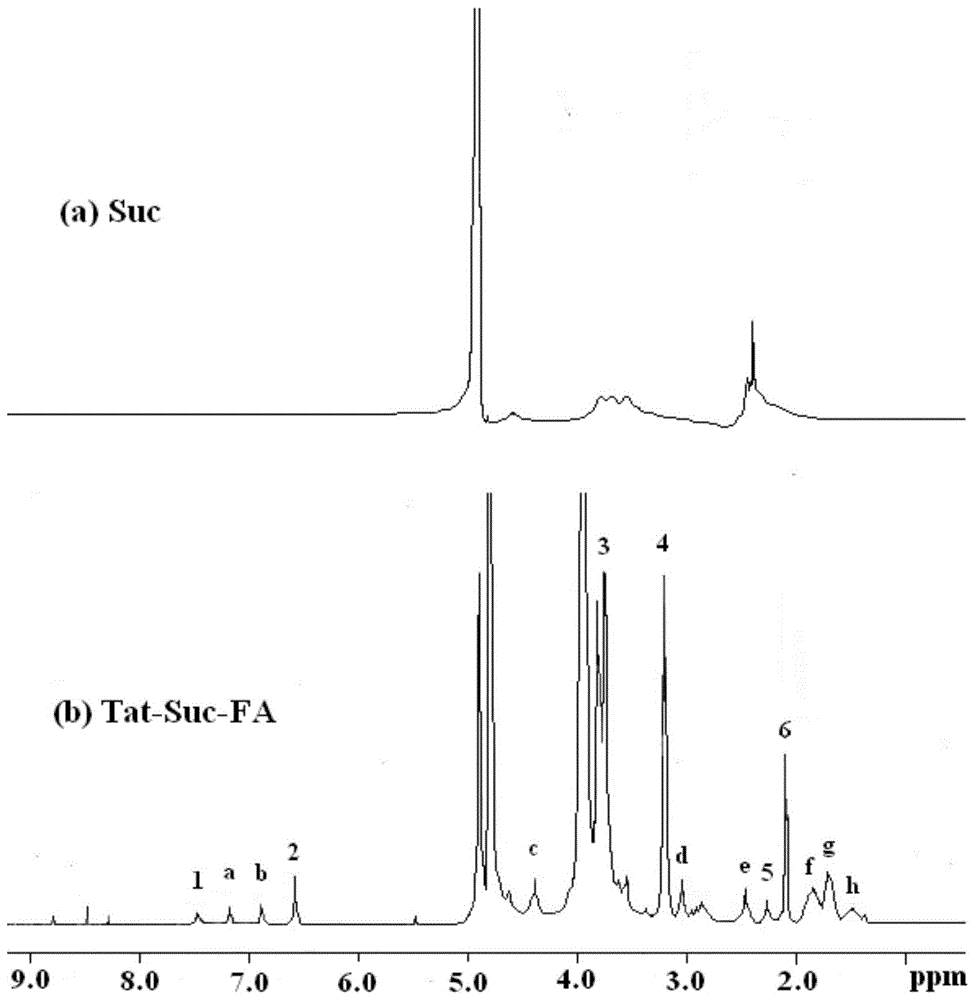
图1为本发明实施例1中采用的原料suc和步骤⑥制得的tat-suc-fa纳米粒的核磁氢谱,其中,(a)为原料suc的核磁氢谱,(b)为tat-suc-fa纳米粒在重水(d2o)中的核磁氢谱;
图2为本发明实施例1中采用的原料suc、步骤④制得的suc-fa和步骤⑥制得的tat-suc-fa纳米粒的红外光谱,其中,(a)为原料suc的红外光谱,(b)为suc-fa的红外光谱,(c)为tat-suc-fa纳米粒的红外光谱;
图3为本发明实施例2制得的紫杉醇/tat-suc-fa纳米粒的透射电镜图。
具体实施方式
下面结合具体实施例对本发明作进一步的详述,以更好地理解本发明的内容,但本发明并不限于以下实施例。
实施例1:载体tat-suc-fa纳米粒的制备
按下述合成路线制备载体tat-suc-fa纳米粒:
具体的制备方法如下:
①取2mmol的edc和0.75mmol的fa置于20mldmso中(体系中fa的浓度为35mmol/l,edc的浓度为100mmol/l),室温条件下搅拌至完全溶解,得到溶液a;
②取suc溶于ph=4.7的乙酸-乙酸钠缓冲溶液中,控制suc在体系中的浓度为1%(w/v),得到溶液b;
③向溶液a中加入溶液b,混合均匀后于暗室中在常温下搅拌反应20h,之后用浓度为4%(w/w)的氢氧化钠水溶液调节体系的ph=9.0,得到反应物料c;其中,溶液b的加入量为控制所得物料中suc的量为叶酸物质的量的0.2倍;
④将反应物料c先用ph=7.4的乙酸-乙酸钠缓冲溶液透析3天,再用去离子水透析3天,之后采用冻干法分离,得到叶酸修饰的n-琥珀酰壳聚糖即suc-fa;
⑤取edc和dmap置于dmf中,控制edc在体系中的浓度为15.5mmol/l,dmap在体系中的浓度为1.2mmol/l,室温条件下搅拌至完全溶解,得到溶液d;
⑥在溶液d中加入等摩尔比的小分子多肽tat(氨基酸序列如seqidno:1所示)和步骤④制得的叶酸修饰的n-琥珀酰壳聚糖,在室温下搅拌反应1h,所得反应混合物用去离子水透析3天,得到载体tat-suc-fa纳米粒。
对本实施例中采用的原料suc和步骤⑥制得的tat-suc-fa纳米粒进行核磁表征,如图1所示。
对本实施例中采用的原料suc、步骤④制得的suc-fa和步骤⑥制得的tat-suc-fa纳米粒进行红外光谱表征,如图2所示。
实施例2:紫杉醇/tat-suc-fa纳米粒的制备
1)按实施例1所述方法制备tat-suc-fa纳米粒;
2)取tat-suc-fa纳米粒溶于ph=5.5的乙酸-乙酸钠缓冲溶液中,配制得到浓度为3mg/ml的纳米聚合物溶液;
3)取紫杉醇溶于去离子水中,配制得到浓度为2mg/ml的紫杉醇水溶液;
4)取步骤2)所得纳米聚合物溶液与步骤3)所得紫杉醇水溶液混合,控制所得物料中tat-suc-fa纳米粒和紫杉醇的质量之比为1.5:1,所得物料于超声条件下进行自组装反应(时间为30min),用孔径为0.22μm的微孔滤膜过滤,收集透过液,冻干法分离,得到紫杉醇/tat-suc-fa纳米粒。
对本实施例中制得的紫杉醇/tat-suc-fa纳米粒进行电镜扫描,其tem图如图3所示。由图3可知,所得紫杉醇/tat-suc-fa纳米粒外观呈圆形或类圆形。由激光粒度仪分析可知,所得紫杉醇/tat-suc-fa纳米粒粒径分布较窄,呈正太分布,平均粒径61±18.5nm,聚合物分散系数(pdi)<0.09。纳米粒带正电,zeta电位46±0.3mv。由高效液相色谱仪分析可知药物包封率(%)90.2±5.1,载药量(%)25.2±4.2。
将按本发明所述方法制得的紫杉醇/tat-suc-fa纳米粒进行动物实验,实验方法及结果如下:建立a549荷瘤小鼠模型,接瘤后第7天尾静脉给药,每隔一天给药一次,持续两周,每次给药前测量肿瘤体积和小鼠体重。动物随机分为四组i,空白对照;ii,tat-suc-fa;iii,紫杉醇/tat-suc-fa;iv,紫杉醇原药。
实验结果表明,与紫杉醇原药相对照,紫杉醇/tat-suc-fa纳米粒能够更有效抑制a549荷瘤小鼠肿瘤生长,且小鼠体重治疗前后没有明显变化。结果表明,紫杉醇/tat-suc-fa有更好的抗肿瘤活性,且毒副作用较低。
实施例3:紫杉醇/tat-suc-fa纳米粒的制备
1)实施例1所述方法制tat-suc-fa纳米粒;
2)取tat-suc-fa纳米粒溶于ph=5.0的乙酸-乙酸钠缓冲溶液中,配制得到浓度为5mg/ml的纳米聚合物溶液;
3)取紫杉醇溶于去离子水中,配制得到浓度为4mg/ml的紫杉醇水溶液;
4)取步骤2)所得纳米聚合物溶液与步骤3)所得紫杉醇水溶液混合,控制所得物料中tat-suc-fa纳米粒和紫杉醇的质量之比为2.0:1,所得物料于超声条件下进行自组装反应(时间为40min),用孔径为0.20μm的微滤膜过滤,收集透过液,冻干法分离,得到紫杉醇/tat-suc-fa纳米粒。
实施例4:紫杉醇/tat-suc-fa纳米粒制备
1)按实施例1所述方法制备tat-suc-fa纳米粒;
2)取tat-suc-fa纳米粒溶于ph=6.0的乙酸-乙酸钠缓冲溶液中,配制得到浓度为6mg/ml的纳米聚合物溶液;
3)取紫杉醇溶于去离子水中,配制得到浓度为3mg/ml的紫杉醇水溶液;
4)取步骤2)所得纳米聚合物溶液与步骤3)所得紫杉醇水溶液混合,控制所得物料中tat-suc-fa纳米粒和紫杉醇的质量之比为1.8:1,所得物料于超声条件下进行自组装反应(时间为60min),用孔径为0.22μm的微滤膜过滤,收集透过液,冻干法分离,得到紫杉醇/tat-suc-fa纳米粒。
序列表
<110>桂林医学院
<120>以叶酸及小分子多肽修饰的n-琥珀酰壳聚糖为载体包载紫杉醇的纳米粒及其制备方法
<141>2019-06-05
<160>1
<170>siposequencelisting1.0
<210>1
<211>12
<212>prt
<213>humanimmunodeficiencyvirus
<400>1
cysglyarglyslysargargglnargargarglys
1510
- 还没有人留言评论。精彩留言会获得点赞!