愈创木酚在制备预防或治疗绝经后骨质疏松症药物中的应用的制作方法
本发明涉及医药技术领域,具体地说,是愈创木酚在制备预防或治疗绝经后骨质疏松症药物中的应用。
背景技术:
当归是一种中药,长期以来一直用于治疗包括骨质疏松症和骨坏死在内的骨病。在中医理论中,当归可以增加骨形成,促进骨折愈合。最近的研究表明,当归可以抑制rankl诱导的破骨细胞生成,抑制骨质疏松症并预防股骨头坏死。然而,其有效成分和机制仍不清楚。我们通过二维细胞膜色谱/整体柱/时间质谱系统,筛选当归中与骨髓单核细胞(bmmcs)细胞膜亲和性高的单体,最终筛选出愈创木酚。
骨质疏松症(osteoporosis,op)是以骨量降低、骨组织显微结构发生改变,以骨脆性增加、骨强度下降、易骨折为特征的一种慢性炎症性疾病。骨吸收与骨形成的失衡是骨质疏松的病理生理学基础,由促骨形成的成骨细胞和促骨吸收的破骨细胞调控(delpuente,esposito,physiopathologyofosteoporosis:fromriskfactorsanalysistotreatment,journal/jbiolregulhomeostagents,2015,29:527-531)。研究表明,在慢性炎症过程中转录因子nf-κb(nuclearfactor-kappab,nf-κb)大量激活,骨质疏松的发生与细胞核因子κb的持续激活关系密切(abu-amer,nf-kappabsignalingandboneresorption,journal/osteoporosint,2013,24:2377-2386)。nf-κb激活能够显著促进破骨细胞的分化、功能与存活。炎症因子激活破骨细胞中的nf-κb转录因子,激活下游信号通路,引起相关基因转录翻译,最终导致破骨细胞分化、成熟与活化,引起骨吸收,造成骨质疏松。研究证实,抑制nf-κb表达和转录活性后能够显著改善骨质疏松情况。同时,在破骨细胞生成过程中mapk通路和akt通路也发挥着重要的作用(yuan,xu,leonurinehydrochlorideinhibitsosteoclastogenesisandpreventsosteoporosisassociatedwithestrogendeficiencybyinhibitingthenf-kappabandpi3k/aktsignalingpathways,journal/bone,2015,75:128-137,zhang,liu,histoneacetyltransferasegcn5regulatesosteogenicdifferentiationofmesenchymalstemcellsbyinhibitingnf-κb,journal/jboneminerres,2016,31:391-402,yang,blair,theproteasomeinhibitorcarfilzomibsuppressesparathyroidhormone-inducedosteoclastogenesisthrougharankl-mediatedsignalingpathway,journal/jbiolchem,2015,290:16918-16928,guan,zhao,epoxyeicosanoidssuppressosteoclastogenesisandpreventovariectomy-inducedboneloss,journal/fasebj,2015,29:1092-1101)。
已有的文献和诊疗指南报道,用于治疗绝经后骨质疏松症的药物主要有:骨吸收抑制剂(包括双膦酸盐、雌激素疗法和选择性雌激素受体调节剂)和骨形成促进剂(甲状旁腺激素)。目前治疗绝经后骨质疏松症的治疗药物之间没有存在相互通用的文献报道和临床实践。
目前尚未有任何文献报道愈创木酚具有抑制破骨细胞生成及治疗绝经后骨质疏松症的作用,也未有任何文献报道其作用机制。
技术实现要素:
本发明的目的在于提供愈创木酚的新用途,特别是在制备预防或治疗绝经后骨质疏松症药物中的应用。
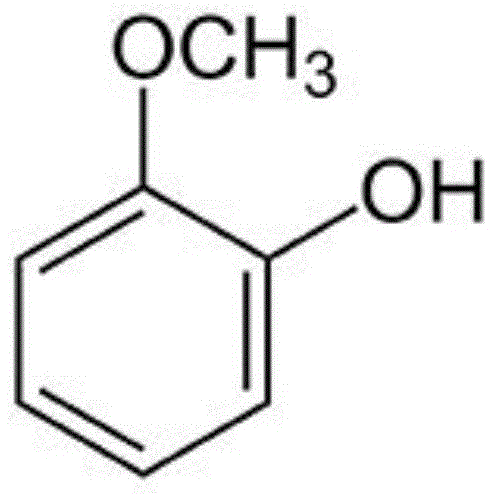
本发明的第一请求,提供愈创木酚、其药学上可接受的盐类在制备预防或治疗绝经后骨质疏松症药物中的应用,所述的愈创木酚的结构如式i所示:
进一步的,所述的药学上可接受的盐类,选自盐酸盐、硫酸盐、硫酸氢盐、氢溴酸盐、草酸盐、柠檬酸盐、甲磺酸盐等。
进一步的,所述的愈创木酚抑制骨量丢失,增加骨小梁数量。
体内动物实验表明愈创木酚对小鼠绝经后骨质疏松症具有显著的保护作用,实验结果显示愈创木酚能够显著抑制去卵巢小鼠的骨量丢失,增加骨小梁数量,可用于制备抗骨质疏松药物。
进一步的,所述的预防或治疗绝经后骨质疏松症药物为注射剂,给药方式包括:静脉、腹腔、局部给药等。
进一步的,所述的预防或治疗绝经后骨质疏松症药物中愈创木酚的给药剂量为125mg/kg/天。
进一步的,所述的预防或治疗绝经后骨质疏松症药物包含治疗有效量的愈创木酚或其药学上可接受的盐类,和常规药用赋形剂、载体或稀释剂。
本发明的第二方面,提供愈创木酚在制备抑制骨量丢失,增加骨小梁数量的药物中的应用。
本发明的第三方面,提供愈创木酚在制备抑制破骨细胞生成和分化,减少骨质流失的药物中的应用。
进一步的,所述的愈创木酚在制备抑制破骨细胞生成和分化,抑制nf-κb,mapk,akt通路活性,抑制胞内p65,p50,iκb,erk,p38,jnk,akt和c-fos的磷酸化的药物中的应用。
进一步的,所述的愈创木酚减轻骨质流失是通过抑制rank与traf6和c-src的结合,抑制了nf-κb,mapk,akt通路,从而抑制破骨细胞生成,同时抑制破骨细胞功能,减轻骨吸收。本发明阐明了愈创木酚治疗绝经后骨质疏松症的机制。
进一步的,所述的愈创木酚通过抑制rank和traf6的结合,从而抑制nf-κb通路和mapk通路激活,还通过抑制rank和c-src的结合,抑制akt通路激活,从而最终抑制骨关键转录因子nfatc1的表达,从而发挥抑制破骨细胞生成,减少骨质流失的作用。
本发明的第四方面,提供一种预防或治疗绝经后骨质疏松症的药物,包括有效量的愈创木酚或其药学上可接受的盐类,和常规药用赋形剂、载体或稀释剂。
本发明优点在于:
本发明为愈创木酚提供了一种新用途,阐明了愈创木酚抑制破骨细胞生成的新机制,也为绝经后骨质疏松症的预防和治疗提供了一种新的思路。
附图说明
图1为愈创木酚的化学结构式。
图2a为cck8实验的结果。图2b和2c为bmmcs细胞和raw264.7细胞培养7天,诱导破骨生成后的trap染色结果(*p<0.05,**p<0.01)。
图3a,图3b和图3c为破骨细胞分化不同时期使用愈创木酚治疗后的trap染色破骨细胞的定量结果。图3d为破骨细胞生成指标进行检测的结果,具体测量指标为trap,cathepsink,mmp-9和ctr。与诱导组比较,高剂量药物处理组,各组蛋白指标均明显降低,数据具有统计学差异(*p<0.05)。
图4a为p65的免疫荧光结果。图4b为nf-κb通路关键因子p65,p50和iκb的磷酸化水平。与对照组相比,愈创木酚处理能够显著抑制nf-κb通路的激活。图4c为mapk通路关键因子erk,jnk,p38,c-fos和akt通路关键因子akt的磷酸化水平。与对照组比较,诱导组细胞内各关键因子磷酸化水平均明显升高,组间差异显著(**p<0.01),愈创木酚能够明显抑制胞内erk,p38,jnk,akt和c-fos的磷酸化,与诱导组比较,数据均有统计学差异(**p<0.01)。
图5a为细胞内的ca2+振荡结果,表明愈创木酚能够抑制rankl诱导破骨分化过程中的ca2+信号。图5b为rank与traf6、c-src的co-ip结果。图5c为nfatc1的免疫荧光结果。表明愈创木酚能够抑制nfatc1的表达和入核。
图6a为6周后小鼠股骨远端micro-ct二维及三维骨结构,统计骨密度(bmd)、骨小梁数量(tb.n)、骨表面积和组织体积之比(bs/tv)和相对骨体积(bv/tv)。图6b为6周后小鼠股骨远端干骺端切片he染色。图6c为6周后小鼠股骨远端干骺端切片trap染色,表明愈创木酚能够抑制体内破骨细胞生成。图6d为血清破骨指标ctx-1和tracp5b的水平。
具体实施方式
下面结合实施例对本发明提供的具体实施方式作详细说明。
实施例1.愈创木酚对c57小鼠去卵巢后骨质丢失具有抑制作用
一、实验材料:
采用生理盐水将愈创木酚稀释成不同浓度的药物溶液。
二、实验方法:
(一)动物实验
1.8周龄雌性c57小鼠,购自北京维通利华公司,饲养于长海医院spf级动物房。分组情况:将30只c57小鼠随机分为3组,每组为10只,分别为假手术组、去卵巢组、药物干预组。
去卵巢组:采用外科手术摘除小鼠双侧卵巢。
假手术组:除不切除小鼠卵巢外其余操作与去卵巢组相同。
药物干预组:切除小鼠双侧卵巢后每日一次腹腔注射给予每只小鼠125mg/kg的愈创木酚。
2.饲养6周后处死小鼠,取小鼠的双侧股骨及血清。
(1)小鼠股骨使用多聚甲醛溶液进行固定、edta脱钙后,石蜡包埋切片(4μm),进行苏木精-伊红(he)染色,显微镜下观察小鼠股骨远端干骺端并拍照。
(2)将固定的小鼠股骨行micro-ct检查,采用skyscan1176微型ct机对小鼠股骨远端行micro-ct扫描,构建小鼠股骨远端干骺端二维及三维图像,并分析股骨骨小梁数量,骨表面积和组织体积之比进行分析,相对骨体积,骨矿物质密度,骨小梁连接数进行分析,获得定量结果。
(3)取得的血清在4℃条件下冷藏1小时后3000转15min进行离心,取得上清液。对血清中ctx-1和tracp5b进行检测。
(二)细胞实验
1.首先进行愈创木酚的细胞毒性试验,采用cck8实验方法。cck8试剂浓度为5mg/ml,将bmmcs细胞以10×104/ml的密度接种于96孔板,每个孔100μl。经过在37℃,5%二氧化碳的条件下24小时的培养之后,加入愈创木酚,浓度梯度分别为100μm、50μm、25μm、12.5μm、6.25μm、4μm、2μm、1μm、0.5μm、0.25μm、0.125μm。经过48小时培养后,加入cck8溶液等待2小时。使用酶标仪检测在490nm光下的吸光度。
2.从c57小鼠骨髓中获得骨髓干细胞(bmscs),进行培养。培养液使用dmem低糖培养基,双抗,胎牛血清混合培养液。使用edta酶进行消化传代。实验分为两组。在进行成骨细胞诱导的同时,一组不做干预,另一组给予1.0μm的愈创木酚,分别在7,14,21天观察矿化结节形成情况,并拍照。
3.实验分为5组。第一组为raw264.7细胞对照组;第二组为raw264.7细胞且使用m-csf和rankl诱导组;第三组为0.25μm愈创木酚处理且使用m-csf和rankl诱导组;第四组为0.5μm愈创木酚处理且使用m-csf和rankl诱导组;第五组为1.0μm愈创木酚处理且使用m-csf和rankl诱导组。7天后,进行trap染色,观察破骨细胞诱导的数量并计数进行统计学分析。相同方法,培养bmmcs细胞进行干预。
4.对3中得到的细胞进行westernblot检测,对trap,cathepsink,mmp9和ctr等破骨细胞生成指标进行分析,统计学分析结果。
5.实验分为3组,分别为bmmcs(对照组),bmmcs+rankl+m-csf(诱导组)和bmmcs+愈创木酚+rankl+m-csf(愈创木酚处理且诱导组),愈创木酚使用1.0μm。在488nm吸光度下使用倒置荧光显微镜检测细胞内ca2+水平每隔2s扫描图像并绘制图像,共持续3min。用基础研究软件分析结果。
6.实验分为3组,分别为raw264.7(对照组),raw264.7+rankl+m-csf(诱导组)和raw264.7+愈创木酚+rankl+m-csf(愈创木酚处理且诱导组),愈创木酚使用1.0μm,处理时间为细胞诱导后第三天,细胞再经4天诱导。细胞完成总计7天的诱导后,收集细胞,提取细胞总蛋白,westernblot分别检测nf-κb通路、mapk通路和akt通路关键因子表达水平,同时,使用免疫荧光对p65入核情况以及破骨关键转录因子nfatc1入核情况进行观察。视野选择随机视野。
三、实验结果
1.通过cck8实验测定了愈创木酚对细胞无毒性的浓度。结果表明当愈创木酚的浓度为1.0μm时,对细胞基本无毒性,所以后续实验最高选择1.0μm为最高干预剂量。使用bmmcs细胞和raw264.7细胞破骨诱导7天,随后行trap染色。结果显示,当使用m-csf和rankl诱导后破骨细胞数量明显增加(**p<0.01),而当使用愈创木酚干预后破骨细胞数量明显减少,并且有剂量依赖性,愈创木酚的浓度为1.0μm时破骨细胞数量最少(**p<0.01)。说明愈创木酚能够显著抑制破骨细胞生成。
2.为破骨细胞分化不同时期给予愈创木酚干预后破骨诱导并trap染色。结果表明。愈创木酚发挥作用在破骨细胞形成早期。随后检测破骨生成相关基因trap,cathepsink,mmp-9和ctr的表达。raw264.7细胞经7天m-csf(30ng/ml)和rankl(50ng/ml)诱导,细胞中trap,cathepsink,mmp-9和ctr各组蛋白表达均明显增强,与对照组比较,差异显著(**p<0.01)。细胞诱导的过程中加入愈创木酚(0.25,0.5和1.0μm),可以明显抑制各组蛋白上升趋势,且药物浓度与蛋白表达的抑制程度呈梯度依赖,与诱导组比较,高剂量药物处理组各组蛋白指标均明显降低,数据具有统计学差异(*p<0.05),这说明愈创木酚可以明显抑制m-csf和rankl诱导的raw264.7细胞破骨分化。
3.当使用m-csf和rankl进行诱导后,nf-κb通路关键因子p65的入核数目明显增多,当同时使用愈创木酚进行干预时,p65入核数目显著减少。说明愈创木酚能够抑制p65的激活。westernblot检测nf-κb通路关键因子p65,p50和iκb的磷酸化水平结果显示,与对照组相比,诱导组细胞内p65,p50和iκb的磷酸化水平均明显升高,组间差异显著(**p<0.01),1.0μm的愈创木酚处能够明显抑制胞内p65,p50和iκb的磷酸化水平,与诱导组相比,数据均有显著统计学差异(**p<0.01)。说明愈创木酚能够显著抑制nf-κb通路的激活。同样地,愈创木酚能抑制mapk通路关键因子erk,jnk,p38,c-fos和akt通路关键因子akt的磷酸化水平。与对照组相比较,诱导组细胞内各关键因子磷酸化水平均明显升高,组间差异显著(**p<0.01),愈创木酚能够明显抑制胞内erk,p38,jnk,c-fos和akt的磷酸化,与诱导组比较,数据均有统计学差异(**p<0.01)。
4.细胞内ca2+振荡结果表明愈创木酚能够抑制rankl诱导破骨分化过程中的ca2+的释放。rank与traf6、c-src的co-ip结果,表明愈创木酚能够抑制rank与traf6、c-src的结合,说明愈创木酚通过抑制rank与traf6、c-src的结合而发挥抑制破骨细胞分化的作用。nfatc1的表达量表明愈创木酚能够抑制nfatc1的表达,且具有剂量依赖性。图5c为nfatc1的免疫荧光结果。综上结果表明,愈创木酚通过抑制rank与traf6、c-src的结合,从而抑制nf-κb通路、mapk通路和akt通路,最终抑制破骨关键转录因子nfatc1的表达,从而发挥抑制破骨细胞生成,减少骨质流失。
5.使用愈创木酚干预去卵巢模型小鼠结果显示,去卵巢组小鼠骨小梁数目较正常组明显减少,给予愈创木酚后小鼠股骨远端干骺端骨小梁数目明显多于卵巢切除组。统计骨密度(bmd)、骨小梁数量(tb.n)、骨表面积和组织体积之比(bs/tv)和相对骨体积或骨体积分数(bv/tv)后发现,愈创木酚组小鼠显著优于去卵巢组小鼠,但不及假手术组,且差异具有统计学意义(*p<0.05)。he染色结果也能得出相同的结论,结果显示去卵巢组小鼠骨小梁数目较正常组明显减少,骨小梁间距增大,表现为骨质疏松;给予愈创木酚后小鼠股骨远端干骺端骨小梁数目明显多于卵巢切除组。骨小梁面积统计结果也显示去卵巢后骨质流失,给予愈创木酚后骨质流失得到缓解。trap染色结果显示愈创木酚能够抑制体内破骨细胞生成。同时愈创木酚抑制了血清ctx-1和tracp5b等破骨指标的水平。表明愈创木酚通过抑制破骨细胞生成减轻去卵巢小鼠骨质流失。
四、结果讨论
女性绝经后骨质疏松症属于原发性骨质疏松症,与雌激素水平降低后破骨细胞分化增多、成骨减少有关。去卵巢组小鼠模型人类绝经,在去卵巢6周后表现出显著的骨质疏松表现,主要表现为骨小梁数量明显减少、骨皮质变薄等。目前研究表明,骨质疏松症的发生与骨骼的慢性炎症有关。慢性炎症使得破骨细胞过度激活,造成骨质显著丢失。
其中traf6与c-src募集激活的nf-κb,mapk,akt通路与破骨细胞的过度激活有密切关联。作为一种nf-κb,mapk,akt通路的抑制剂,愈创木酚显著减少了去卵巢后小鼠骨量的丢失,表现为骨小梁数目、骨表面积和组织体积之比、相对骨体积或骨体积分数和骨小梁连接数的增加。
以上已对本发明创造的较佳实施例进行了具体说明,但本发明创造并不限于所述实施例,熟悉本领域的技术人员在不违背本发明创造精神的前提下还可做出种种的等同的变型或替换,这些等同的变型或替换均包含在本申请权利要求所限定的范围内。
- 还没有人留言评论。精彩留言会获得点赞!