PPARα激活子联合PD-1抗体在制备肿瘤免疫治疗药物中的应用的制作方法
本发明涉及肿瘤免疫治疗领域,具体涉及pparα激活子联合pd-1抗体在制备肿瘤免疫治疗药物中的应用。
背景技术:
大量研究表明人体免疫系统能识别并杀死肿瘤细胞,因此当免疫系统功能降低时会诱发肿瘤发生,而提高机体免疫力则能有效抑制癌症发生。当前肿瘤免疫治疗已成为研究的热点,大量免疫治疗相关药物正在研究开发或已投入临床使用。pd-1(programmeddeath-1)抗体/pd-l1抗体属于免疫检查点阻断药物。pd-1是表达在t细胞表面的另一种重要的免疫印制跨膜蛋白,为cd28超家族成员,其最初是从凋亡的小鼠t细胞杂交瘤2b4.11克隆出来。pd-1有两个配体,pd-l1和pd-l2,pd-l1比pd-l2表达更为广谱,在肿瘤的微环境中,肿瘤细胞能够表达pd-l1或者pd-l2。尽管免疫治疗相对于传统治疗有着较高的疗效,但它仍存在一定的缺陷,如美国食品与药品管理局(fda)批准并作用于免疫检查点(immunecheckpoint)的抗体药物能有效治疗25种类型以上的癌症,但是有将近40%的癌症患者对上述作用于免疫检查点的抗体药物没有响应。
pparα是过氧化酶体增殖物激活受体(peroxisome-proliferator-activatedreceptors,ppars)家族的成员之一,其在调节肿瘤、炎症、代谢方面发挥关键的作用。在大多数组织中,pparα蛋白广泛表达。然而,对于pparα激活子与抗体药物之间是否存在协同关系目前尚不清楚。
技术实现要素:
有鉴于此,本发明提供了pparα激活子联合pd-1抗体在制备肿瘤免疫治疗药物中的应用。本发明对pparα激活子与肿瘤免疫检查点阻断药物进行研究后发现pparα激活子能显著降低pd-l1的蛋白水平,抑制pd-l1的基因表达,pparα激活子联合pd-1抗体能显著增强pd-1抗体的肿瘤免疫治疗能力。
本发明提供了pparα激活子联合pd-1抗体在制备肿瘤免疫治疗药物中的应用。
进一步地,所述的pd-1抗体是抗人pd-1单克隆抗体;所述的pparα激活子是clofibrate或wy-14,643。所述的肿瘤是结肠癌。
本发明还提供了一种治疗肿瘤的药物组合物,所述的药物组合物中包含有效剂量的pparα激活子和pd-1抗体。所述的药物组合物中的pparα激活子是clofibrate或wy-14,643,所述的pd-1抗体是抗人pd-1单克隆抗体。
与现有技术相比较,本发明的有益效果是:
本发明公开了一种pparα激活子联合pd-1抗体在肿瘤免疫治疗药物中的新用途。本发明研究发现细胞过氧化物酶体增殖物激活受体α(pparα)激活子能够降低pd-l1蛋白水平进而增加pd-1抗体的肿瘤免疫治疗,从而抑制肿瘤生长;进而发现pparα激活子能显著增强pd-1抗体的肿瘤免疫治疗效果。与单一pd-1抗体治疗相比,本发明中公开的pparα激活子联合pd-1抗体能显著抑制小鼠中肿瘤的生长水平,明显高于单纯使用常用的抗体。在肿瘤免疫治疗效果方面具有显著的作用。
附图说明
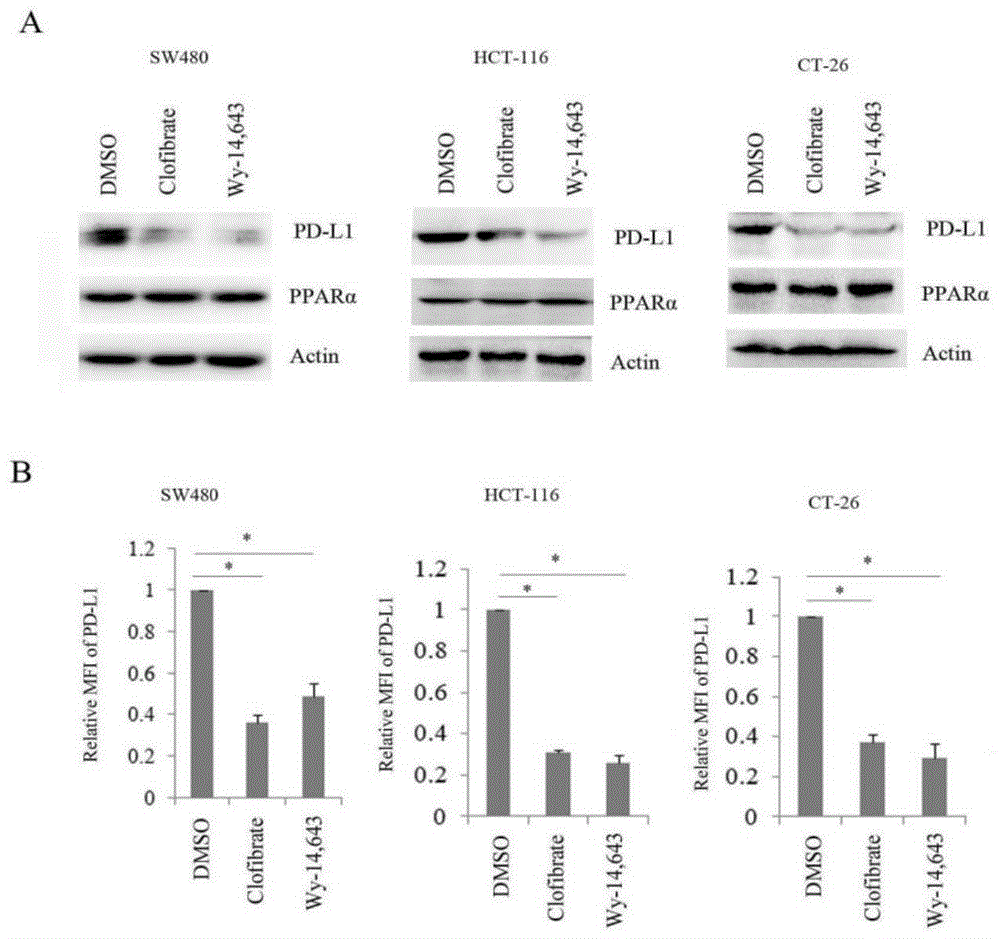
图1是pparα激活子对pd-l1蛋白表达影响分析结果;图中,a是westernblot分析图;b是流式细胞术结果分析图;
图2是pparα激活子对pd-l1的基因表达水平分析结果;图中,a是qpcr分析结果图,b是双荧光报告分析结果图;
图3是pparα激活子联合pd-1抗体对肿瘤生长影响结果;图中,a是肿瘤体积对比图,b是westernblot分析结果图。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
进一步需要说明的是,本发明使用的各种术语和短语具有本领域技术人员公知的一般含义,即便如此,本发明仍然希望在此对这些术语和短语作更详尽的说明和解释,提及的术语和短语如有与公知含义不一致的,以本发明所表述的含义为准。术语“激活子”是指能特异性结合pparα蛋白并调节pparα转录活力的物质。
本发明对试验中所使用到的材料以及试验方法进行一般性和/或具体的描述。虽然为实现本发明目的所使用的许多材料和操作方法是本领域公知的,但是本发明仍然在此作尽可能详细描述。本领域技术人员清楚,在下文中,如果未特别说明,本发明所用材料和操作方法是本领域公知的。
实验试剂:
sw480、hct-116、ct-26小鼠结肠癌细胞购买于美国atcc;actin、pd-l1、pparα抗体购买于上海生物工程有限公司;clofibrate、wy-14,643购买于csnpharm(中国);0.25%胰酶(含edta)购买于gibco公司;胎牛血清(fbs)和dmem完全培养基皆为本领域技术人员常用的药品,配制和使用方法皆为本领域公知常识。总rna提取试剂盒购买于上海生工,qpcr反应试剂盒购买于takara。
本发明中所用pd-l1与actin引物序列如下:
pd-l1-lu的上游引物序列如seqidno:1所示,即:cggggtaccgaagcaaaagtggcaagcaggg,其下游引物序列如seqidno:2所示,即:ccgctcgagacagaagcgcggctggtgcgg;
pd-l1的上游引物序列如seqidno:3所示,即:tggcatttgctgaacgcattt,其下游引物序列如seqidno:4所示,即:tgcagccaggtctaattgtttt;
actin的上游引物序列如seqidno:5所示,即:ggtgggcatgggtcagaaggat,其下游引物序列如seqidno:6所示,即:cacacgcagctcattgtagaaggt。
实施例1:pparα激活子降低pd-l1的蛋白水平
本实施例中以二甲基亚砜(dmso)为对照组,氯贝丁酯(clofibrate)和wy-14,643为实验组来验证pparα激活子对pd-l1的蛋白水平的影响。分别将sw480、hct-116、ct-26细胞以含10%胎牛血清(fbs)的dmem完全培养基常规培养,显微镜下镜检达80%融合度时,用0.25%胰酶消化,细胞接种于12孔板中,并置于37ºc,5%co2培养箱中过夜后,并且密度长至孔的70%-90%时,细胞处理对照组、实验组(5μm)12小时。
(1)细胞裂解、westernblot分析pd-l1蛋白表达,其中pparδ是内源性pparδ蛋白;actin是内参蛋白;
(2)收集细胞离心,细胞利用40μm滤器过滤。2×105细胞孵育荧光标记的pd-l1抗体,对应igg1为对照,室温孵育30分钟,细胞利用pbs洗几次,最后利用流式细胞仪分析pd-l1膜蛋白表达水平,结果用均值±sem表示(n=3),*p<0.05。
图1是pparα激活子对pd-l1蛋白表达影响分析图;图中,a是sw480、hct-116以及ct-26细胞的westernblot分析图;b是流式细胞术分析pd-l1表达水平对比图。由图1可见,pparα激活子clofibrate、wy-14,643均能显著降低sw480、hct-116、ct-26结肠癌细胞系pd-l1蛋白水平;流式细胞术分析结果也表明clofibrate、wy-14,643显著降低sw480、hct-116、ct-26结肠癌细胞系细胞膜pd-l1蛋白水平。
实施例2:pparα激活子抑制pd-l1基因表达
本实施例中以dmso为对照组,clofibrate(5μm)和wy-14,643(5μm)为实验组来验证pparα激活子对pd-l1基因表达的影响。将sw480、hct-116、ct-26细胞以含10%胎牛血清(fbs)的dmem完全培养基常规培养,显微镜下镜检达80%融合度时,用0.25%胰酶消化,细胞接种于12孔板中,并置于37ºc、5%co2培养箱中过夜后,并且密度长至孔的70%-90%时。
(1)细胞处理12小时后细胞裂解,qpcr分析pd-l1基因表达水平;结果用均值±sem表示(n=3),*p<0.05。
(2)sw480,hct-116,ct-26细胞转染pd-l1报告基因质粒,30小时后,双荧光报告分析pd-l1基因转录水平。
图2是pparα激活子对pd-l1的基因表达水平图;图中,a是qpcr分析结果图,b是双荧光报告分析结果图;由图2可见pparα激活子clofibrate、wy-14,643显著降低sw480、hct-116、ct-26结肠癌细胞系pd-l1的mrna水平;此外,双荧光报告分析结果表明clofibrate、wy-14,643显著降低sw480、hct-116、ct-26结肠癌细胞系pd-l1基因转录水平。
实施例3:pparα激活子联合pd-1抗体显著抑制肿瘤生长
本实施例中验证pparα激活子联合pd-1抗体对肿瘤生长的影响。
将ct-26小鼠结肠癌细胞(5×105)接种到裸鼠皮下,接种后的小鼠随机分成四组:igg(对照组)、pd-1、clofibrate以及pd-1+clofibrate组;每三天皮下注射igg/pd-1抗体(200μg/小鼠),每天灌胃clofibrate(20mg/kg/day)。每天每周测量肿瘤体积,共4周,最后断颈法处死小鼠。取肿瘤组织检测,肿瘤体积计算公式=1/2(长×宽2)。结果用均值±sem表示(n=8),*p<0.05。并使用westernblot分析肿瘤组织裂解物中pd-l1蛋白的表达水平,其中actin是内参蛋白。
图3是pparα激活子联合pd-1抗体对肿瘤生长影响图;图中,a是肿瘤体积对照图;b是westernblot分析肿瘤组织中pd-l1蛋白表达水平图。由图3可见,pd-1+clofibrate组小鼠肿瘤体积明显小于pd-1组和clofibrate组,pd-1抗体和pparα激活子clofibrate联合使用增强了pd-1抗体的肿瘤免疫治疗能力。
上述实例只为说明本发明的技术构思及特点,其目的在于让熟悉此项技术的人是能够了解本发明的内容并据以实施,并不能以此限制本发明的保护范围。凡根据本发明精神实质所做的等效变换或修饰,都应涵盖在本发明的保护范围。
序列表
<110>江苏大学
<120>pparα激活子联合pd-1抗体在制备肿瘤免疫治疗药物中的应用
<160>6
<170>siposequencelisting1.0
<210>1
<211>31
<212>dna
<213>人工序列(artificialsequence)
<400>1
cggggtaccgaagcaaaagtggcaagcaggg31
<210>2
<211>30
<212>dna
<213>人工序列(artificialsequence)
<400>2
ccgctcgagacagaagcgcggctggtgcgg30
<210>3
<211>21
<212>dna
<213>人工序列(artificialsequence)
<400>3
tggcatttgctgaacgcattt21
<210>4
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>4
tgcagccaggtctaattgtttt22
<210>5
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>5
ggtgggcatgggtcagaaggat22
<210>6
<211>24
<212>dna
<213>人工序列(artificialsequence)
<400>6
cacacgcagctcattgtagaaggt24
- 还没有人留言评论。精彩留言会获得点赞!